 золото платина осмий
золото платина осмий
 цезий ртуть медь
цезий ртуть медь
 МКОУ «Давыдовская СОШ» Урок-практикум по химии в 11 классе «ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ»
МКОУ «Давыдовская СОШ» Урок-практикум по химии в 11 классе «ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ»
 Цели проверить знания о строении металлов и их физических свойствах; сформировать понятие об общих химических свойствах металлов; научиться использовать приобретённые знания для объяснения явлений окружающей среды; научиться грамотному использованию металлических изделий.
Цели проверить знания о строении металлов и их физических свойствах; сформировать понятие об общих химических свойствах металлов; научиться использовать приобретённые знания для объяснения явлений окружающей среды; научиться грамотному использованию металлических изделий.
 ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ С простыми веществами Na c S Fe c Cl 2 Mg c O 2 Al c I 2
ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ С простыми веществами Na c S Fe c Cl 2 Mg c O 2 Al c I 2
 Со сложными веществами С водой С кислотами С солями
Со сложными веществами С водой С кислотами С солями
 ЛАБОРАТОРНЫЙ ОПЫТ 1. К магнию, цинку и меди прилейте соляную кислоту. Прокомментируйте наблюдения и сделайте вывод. Напишите уравнения реакции. 2. В раствор сульфата меди (II) опустите гранулу цинка, а в раствор сульфата цинка – медную проволоку. Прокомментируйте наблюдения и сделайте вывод. Напишите уравнения реакции.
ЛАБОРАТОРНЫЙ ОПЫТ 1. К магнию, цинку и меди прилейте соляную кислоту. Прокомментируйте наблюдения и сделайте вывод. Напишите уравнения реакции. 2. В раствор сульфата меди (II) опустите гранулу цинка, а в раствор сульфата цинка – медную проволоку. Прокомментируйте наблюдения и сделайте вывод. Напишите уравнения реакции.
 ЗАДАЧА Цинковая пластинка массой 10 г опущена в раствор сульфата меди (II). После реакции масса стала равна 9, 9 г. Определите массу меди, осевшую на пластинке.
ЗАДАЧА Цинковая пластинка массой 10 г опущена в раствор сульфата меди (II). После реакции масса стала равна 9, 9 г. Определите массу меди, осевшую на пластинке.
 Медная пластинка массой 101, 87 г опущена в раствор нитрата серебра. Через некоторое время масса пластинки стала равна 118, 61 г. Определите массу меди, ушедшую в раствор.
Медная пластинка массой 101, 87 г опущена в раствор нитрата серебра. Через некоторое время масса пластинки стала равна 118, 61 г. Определите массу меди, ушедшую в раствор.
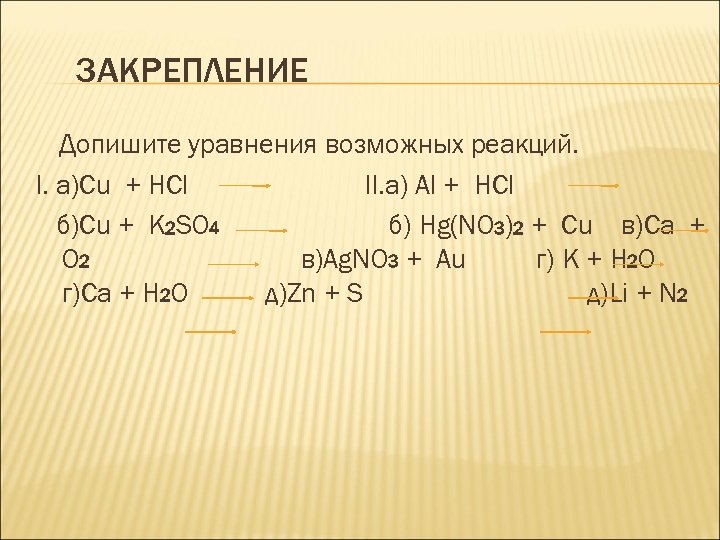 ЗАКРЕПЛЕНИЕ Допишите уравнения возможных реакций. I. а)Cu + HCl II. а) Al + HCl б)Cu + K 2 SO 4 б) Hg(NO 3)2 + Cu в)Ca + O 2 в)Ag. NO 3 + Au г) K + H 2 O г)Ca + H 2 O д)Zn + S д)Li + N 2
ЗАКРЕПЛЕНИЕ Допишите уравнения возможных реакций. I. а)Cu + HCl II. а) Al + HCl б)Cu + K 2 SO 4 б) Hg(NO 3)2 + Cu в)Ca + O 2 в)Ag. NO 3 + Au г) K + H 2 O г)Ca + H 2 O д)Zn + S д)Li + N 2
 Допишите уравнения возможных реакций. I. а)Cu + HCl → не идет II. а) 2 Al + 6 HCl → 2 Al. Cl 3 +3 H 2 б)Cu + K 2 SO 4 →не идет б)Hg(NO 3)2 + Cu → Cu(NO 3)2 + Hg в)2 Ca + O 2 → 2 Ca. O в)Ag. NO 3 + Au → не идет г)2 K +2 H 2 O → 2 KOH +H 2 г)Ca +2 H 2 O →Ca(OH)2 + H 2 д)Zn + S → Zn. S д)6 Li + N 2 → 2 Li 3 N
Допишите уравнения возможных реакций. I. а)Cu + HCl → не идет II. а) 2 Al + 6 HCl → 2 Al. Cl 3 +3 H 2 б)Cu + K 2 SO 4 →не идет б)Hg(NO 3)2 + Cu → Cu(NO 3)2 + Hg в)2 Ca + O 2 → 2 Ca. O в)Ag. NO 3 + Au → не идет г)2 K +2 H 2 O → 2 KOH +H 2 г)Ca +2 H 2 O →Ca(OH)2 + H 2 д)Zn + S → Zn. S д)6 Li + N 2 → 2 Li 3 N
 Задание на дом: 18 (до оксидов металлов) упр. 6, 7. 30
Задание на дом: 18 (до оксидов металлов) упр. 6, 7. 30