молекулярные методы2.ppt
- Количество слайдов: 98
 "Значение и возможности современных молекулярных методов в cистематике и флорогенетике «Молекулярная филогенетика»
"Значение и возможности современных молекулярных методов в cистематике и флорогенетике «Молекулярная филогенетика»
 Молекулярная филогенетика Это область биологической систематики, которая занимается идентификацией и прояснением эволюционных взаимоотношений среди разных видов жизни на Земле, как современных, так и вымерших с помощью молекулярно-генетических методов. Nothing in Biology Makes Sense Except in the Light of Evolution Theodosius Dobzhansky (1900 -1975)
Молекулярная филогенетика Это область биологической систематики, которая занимается идентификацией и прояснением эволюционных взаимоотношений среди разных видов жизни на Земле, как современных, так и вымерших с помощью молекулярно-генетических методов. Nothing in Biology Makes Sense Except in the Light of Evolution Theodosius Dobzhansky (1900 -1975)
 Возможности и ограничения в использовании молекулярных методов в систематике При выполнении определенных условий, с помощью молекулярных методов можно решать практически любые таксономические и биогеографические вопросы! Необходимые условия: 1 - Корректно поставленная проблема 2 - Выбор подходящего метода для каждой конкретной задачи 3 - Правильный подбор образцов для анализа 4 - Использование для анализа только достоверного материала Выполнение этих условий, без знания объекта (в нашем случае растений), невозможно. Нужно всегда помнить, что молекулярные методы не заменяют классических методов систематики, а только дополняют их!
Возможности и ограничения в использовании молекулярных методов в систематике При выполнении определенных условий, с помощью молекулярных методов можно решать практически любые таксономические и биогеографические вопросы! Необходимые условия: 1 - Корректно поставленная проблема 2 - Выбор подходящего метода для каждой конкретной задачи 3 - Правильный подбор образцов для анализа 4 - Использование для анализа только достоверного материала Выполнение этих условий, без знания объекта (в нашем случае растений), невозможно. Нужно всегда помнить, что молекулярные методы не заменяют классических методов систематики, а только дополняют их!
 Эволюция является процессом двух фаз, в котором генетическая изменчивость первоначально накапливается произвольно, после чего морфологические или физиологические изменения часто подвержены давлению окружающей среды или селективному отбору (Mayr, 1969). До недавнего времени систематика растений базировалась в основном на данных второй фазы эволюционного процесса, подверженных давлению со стороны, данные молекулярных методов позволяют реконструировать эволюционный процесс на первичных признаках. За последние 15 - 20 лет разработано большое количество доступных молекулярных методов, позволяющих решать любые таксономические и биогеографические проблемы. Объектом исследования большинства молекулярных методов является макромолекула ДНК. Сама природа ДНК позволяет использовать его как “документ” эволюционной истории.
Эволюция является процессом двух фаз, в котором генетическая изменчивость первоначально накапливается произвольно, после чего морфологические или физиологические изменения часто подвержены давлению окружающей среды или селективному отбору (Mayr, 1969). До недавнего времени систематика растений базировалась в основном на данных второй фазы эволюционного процесса, подверженных давлению со стороны, данные молекулярных методов позволяют реконструировать эволюционный процесс на первичных признаках. За последние 15 - 20 лет разработано большое количество доступных молекулярных методов, позволяющих решать любые таксономические и биогеографические проблемы. Объектом исследования большинства молекулярных методов является макромолекула ДНК. Сама природа ДНК позволяет использовать его как “документ” эволюционной истории.
 ДНК - Дезоксирибонуклеиновая кислота ДНК – макромолекула обеспечивающая хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. Способность ДНК денатурировать, ренатурировать, а также самоудваиваться, является основой практически для всех методов в молекулярной биологии
ДНК - Дезоксирибонуклеиновая кислота ДНК – макромолекула обеспечивающая хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. Способность ДНК денатурировать, ренатурировать, а также самоудваиваться, является основой практически для всех методов в молекулярной биологии
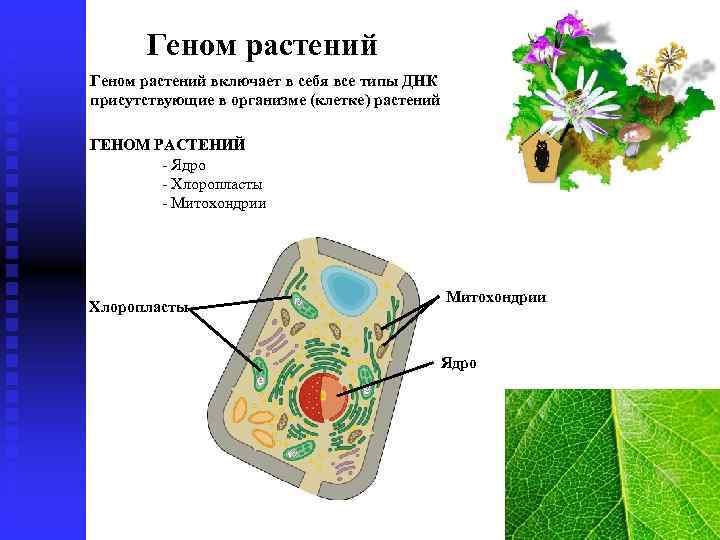 Геном растений включает в себя все типы ДНК присутствующие в организме (клетке) растений ГЕНОМ РАСТЕНИЙ - Ядро - Хлоропласты - Митохондрии Хлоропласты Митохондрии Ядро
Геном растений включает в себя все типы ДНК присутствующие в организме (клетке) растений ГЕНОМ РАСТЕНИЙ - Ядро - Хлоропласты - Митохондрии Хлоропласты Митохондрии Ядро
 Величина генома у различных живых организмах Покрытосеменные Голосеменные Млекопитающиеся Рептилии Птицы Рыбы Членистоногие Кольчатые черви Нематоды Мягкотелые Иглокожие Кищечнополостные Одноклеточные Водоросли Грибы
Величина генома у различных живых организмах Покрытосеменные Голосеменные Млекопитающиеся Рептилии Птицы Рыбы Членистоногие Кольчатые черви Нематоды Мягкотелые Иглокожие Кищечнополостные Одноклеточные Водоросли Грибы
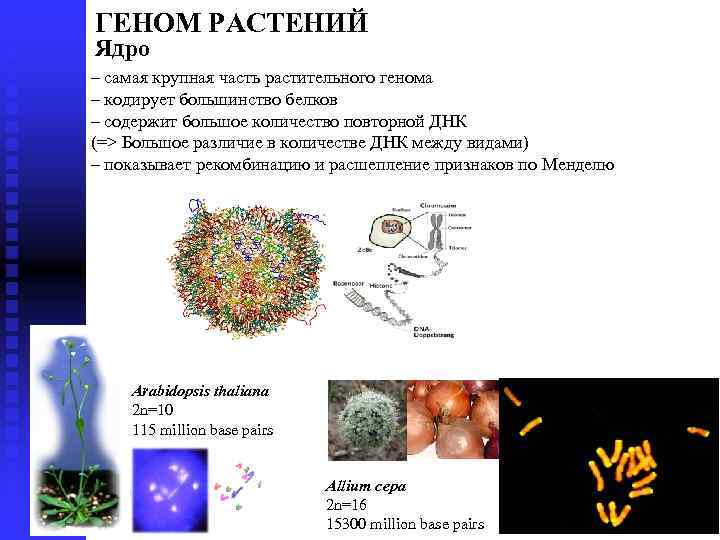 ГЕНОМ РАСТЕНИЙ Ядро – самая крупная часть растительного генома – кодирует большинство белков – содержит большое количество повторной ДНК (=> Большоe различие в количестве ДНК между видами) – показывает рекомбинацию и расшепление признаков по Менделю Arabidopsis thaliana 2 n=10 115 million base pairs Allium cepa 2 n=16 15300 million base pairs
ГЕНОМ РАСТЕНИЙ Ядро – самая крупная часть растительного генома – кодирует большинство белков – содержит большое количество повторной ДНК (=> Большоe различие в количестве ДНК между видами) – показывает рекомбинацию и расшепление признаков по Менделю Arabidopsis thaliana 2 n=10 115 million base pairs Allium cepa 2 n=16 15300 million base pairs
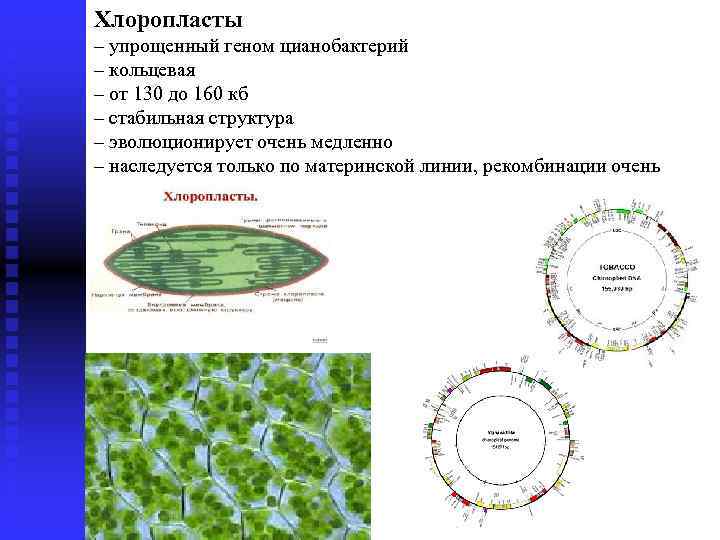 Хлоропласты ГЕНОМ РАСТЕНИЙ – упрощенный геном цианобактерий – кольцевая – от 130 до 160 кб – стабильная структура – эволюционирует очень медленно – наследуется только по материнской линии, рекомбинации очень редки
Хлоропласты ГЕНОМ РАСТЕНИЙ – упрощенный геном цианобактерий – кольцевая – от 130 до 160 кб – стабильная структура – эволюционирует очень медленно – наследуется только по материнской линии, рекомбинации очень редки
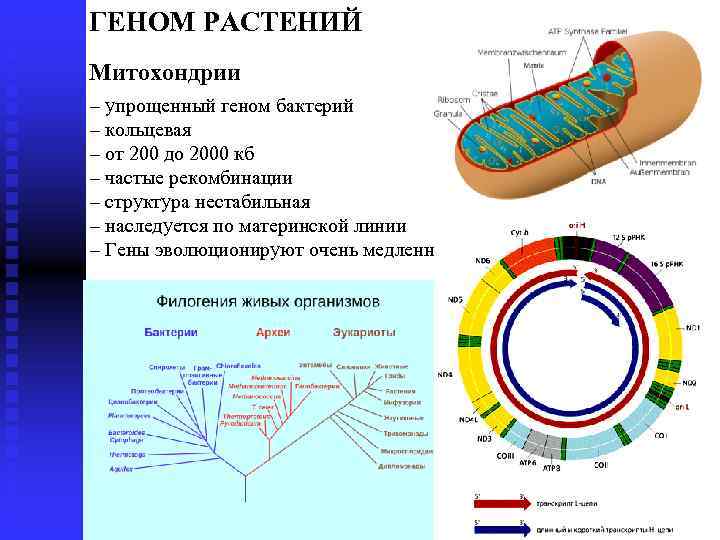 ГЕНОМ РАСТЕНИЙ Митохондрии – упрощенный геном бактерий – кольцевая – от 200 до 2000 кб – частые рекомбинации – структура нестабильная – наследуется по материнской линии – Гены эволюционируют очень медленно
ГЕНОМ РАСТЕНИЙ Митохондрии – упрощенный геном бактерий – кольцевая – от 200 до 2000 кб – частые рекомбинации – структура нестабильная – наследуется по материнской линии – Гены эволюционируют очень медленно
 Выделение ДНК из растений Экстракция чистой недеградированной ДНК из растительных объектов остается определяющим первым этапом в любой сфере использования молекулярно-генетических подходов для изучения растительных организмов. Особенности выделения ДНК из растений! При экстракции ДНК из растительных объектов необходимо не только дезактивировать клеточные ферменты, но и «удалить» запасные вещества, например, полисахариды и вторичные метаболиты, такие как алкалоиды, фенольные соединения, терпены, которые не просто мешают изолированию ДНК, но и отрицательно влияют на ее качество. Процедура выделения ДНК включает обязательные процедуры: - разрушение клеток; - удаление мембранных липидов; - удаление вторичных метаболитов и запасных веществ; - удаление белков; - удаление РНК; - осаждение ДНК. Колонка с силиконовой мембраной Разработано огромное количество протоколов для выделения ДНК. Комерческими компаниями предлагаются множество КИТов для выделения ДНК из растений, основанных на силиконовых мембранах, стоимость выделения одной пробы которыми колеблется от 1 до 6 Евро
Выделение ДНК из растений Экстракция чистой недеградированной ДНК из растительных объектов остается определяющим первым этапом в любой сфере использования молекулярно-генетических подходов для изучения растительных организмов. Особенности выделения ДНК из растений! При экстракции ДНК из растительных объектов необходимо не только дезактивировать клеточные ферменты, но и «удалить» запасные вещества, например, полисахариды и вторичные метаболиты, такие как алкалоиды, фенольные соединения, терпены, которые не просто мешают изолированию ДНК, но и отрицательно влияют на ее качество. Процедура выделения ДНК включает обязательные процедуры: - разрушение клеток; - удаление мембранных липидов; - удаление вторичных метаболитов и запасных веществ; - удаление белков; - удаление РНК; - осаждение ДНК. Колонка с силиконовой мембраной Разработано огромное количество протоколов для выделения ДНК. Комерческими компаниями предлагаются множество КИТов для выделения ДНК из растений, основанных на силиконовых мембранах, стоимость выделения одной пробы которыми колеблется от 1 до 6 Евро
 Из каких частей (органов) растений лучше всего выделять ДНК? Лучше всего выделять ДНК из молодых органов растений (молодые листья, соцветия и т. д. ). В них меньше всего запасных веществ и вторичных метаболитов. Но к сожалению это не всегда доступно! Чаще всего для таксономических работ мы имеем дело со специально собранными образцами или с гербарным материалом. Кроме того растения сильно различаются по компонентному составу вторичных метаболитов. Поэтому для каждой группы растений иногда приходиться модифицировать протоколы выделения ДНК (например: суккулентные растения; хвойные). Сбор материала в поле и т. д. : Наилучший результат при сборе материала получают при высушивании проб в силикагеле. При работе с Гербарным материалом особо важное значение имеет, как был высушен гербарий. Чем естественей цвет растения в гербарии, тем больше вероятность в получении рабочей, мало деградированной ДНК. Ваучер! В таксономических исследованиях к любым публикуемым последовательностям ДНК неоходимо указание на Гербарный образец с которого выделена ДНК (vouchered specimen).
Из каких частей (органов) растений лучше всего выделять ДНК? Лучше всего выделять ДНК из молодых органов растений (молодые листья, соцветия и т. д. ). В них меньше всего запасных веществ и вторичных метаболитов. Но к сожалению это не всегда доступно! Чаще всего для таксономических работ мы имеем дело со специально собранными образцами или с гербарным материалом. Кроме того растения сильно различаются по компонентному составу вторичных метаболитов. Поэтому для каждой группы растений иногда приходиться модифицировать протоколы выделения ДНК (например: суккулентные растения; хвойные). Сбор материала в поле и т. д. : Наилучший результат при сборе материала получают при высушивании проб в силикагеле. При работе с Гербарным материалом особо важное значение имеет, как был высушен гербарий. Чем естественей цвет растения в гербарии, тем больше вероятность в получении рабочей, мало деградированной ДНК. Ваучер! В таксономических исследованиях к любым публикуемым последовательностям ДНК неоходимо указание на Гербарный образец с которого выделена ДНК (vouchered specimen).
 Набор для выделения ДНК из засушенных растений и семян Diamond. DNA Genomic DNA Extraction Kit for Dry Plants & Seeds http: //diamond-dna. ru
Набор для выделения ДНК из засушенных растений и семян Diamond. DNA Genomic DNA Extraction Kit for Dry Plants & Seeds http: //diamond-dna. ru
 Маркерные системы ДНК (Молекулярные маркеры) Молекулярные маркеры представляют собой генетические маркеры, позволяющие анализировать организм на уровне ДНК. К ним применимы термины классической генетики, такие как локус, аллель, доминантный и кодоминантный тип наследования. Аллели маркерных локусов представляют собой различные формы (нуклеотидные последовательности, отличающиеся по длине и/или по нуклеотидным заменам) одного и того же маркера, расположенные в одинаковых участках (локусах) гомологичных хромосом. Если метод анализа маркера позволяет выявлять оба аллеля, говорят о кодоминантном типе наследования данного маркера, если выявляется только один аллель – о доминантном наследовании ДНК маркеры условно можно разделить на три группы: маркеры, основанные на гибридизации, маркеры, основанные на ПЦР и маркеры, основанные на ДНК-чипах.
Маркерные системы ДНК (Молекулярные маркеры) Молекулярные маркеры представляют собой генетические маркеры, позволяющие анализировать организм на уровне ДНК. К ним применимы термины классической генетики, такие как локус, аллель, доминантный и кодоминантный тип наследования. Аллели маркерных локусов представляют собой различные формы (нуклеотидные последовательности, отличающиеся по длине и/или по нуклеотидным заменам) одного и того же маркера, расположенные в одинаковых участках (локусах) гомологичных хромосом. Если метод анализа маркера позволяет выявлять оба аллеля, говорят о кодоминантном типе наследования данного маркера, если выявляется только один аллель – о доминантном наследовании ДНК маркеры условно можно разделить на три группы: маркеры, основанные на гибридизации, маркеры, основанные на ПЦР и маркеры, основанные на ДНК-чипах.
 PCR - polimerase chain reaction Полимеразная цепная реакция - ПЦР очень мощный метод размножения фрагментов ДНК вне организмов (in vitro). С момента его открытия в 1985 году, этот метод используется сейчас практически во всех молекулярно-биологических лабораториях. В 1980 году Каледин с сотрудниками впервые выделили и описали свойства днк-полимеразы из термофильной бактерии Thermus aquaticus. В 1985, технология полимерной цепной реакции (PCR) была введена Миллисом (Mullis) c сотрудниками. Полимеразная цепная реакция - ПЦР „Baby Blue“ Thermocycler, 1986. Денатурация 95°C Отжиг 52°-68° C Элонгация 72° C
PCR - polimerase chain reaction Полимеразная цепная реакция - ПЦР очень мощный метод размножения фрагментов ДНК вне организмов (in vitro). С момента его открытия в 1985 году, этот метод используется сейчас практически во всех молекулярно-биологических лабораториях. В 1980 году Каледин с сотрудниками впервые выделили и описали свойства днк-полимеразы из термофильной бактерии Thermus aquaticus. В 1985, технология полимерной цепной реакции (PCR) была введена Миллисом (Mullis) c сотрудниками. Полимеразная цепная реакция - ПЦР „Baby Blue“ Thermocycler, 1986. Денатурация 95°C Отжиг 52°-68° C Элонгация 72° C
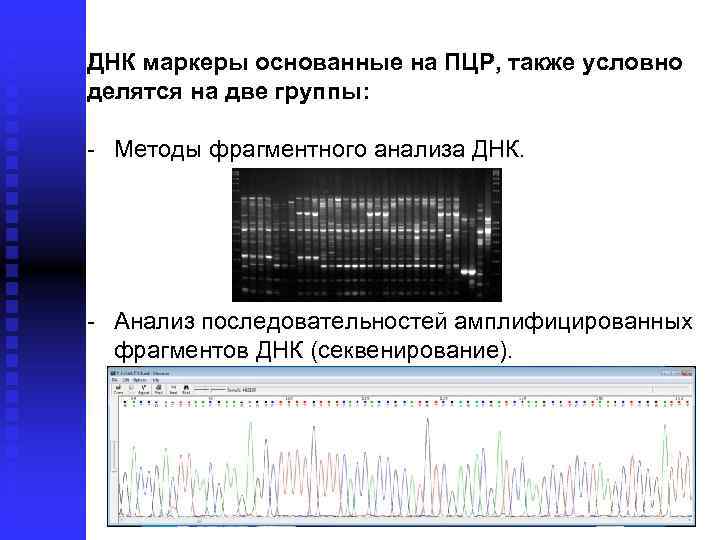 ДНК маркеры основанные на ПЦР, также условно делятся на две группы: Методы фрагментного анализа ДНК. Анализ последовательностей амплифицированных фрагментов ДНК (секвенирование).
ДНК маркеры основанные на ПЦР, также условно делятся на две группы: Методы фрагментного анализа ДНК. Анализ последовательностей амплифицированных фрагментов ДНК (секвенирование).
 Молекулярные методы исследования ДНК растений, базирующиеся на фрагментном (анонимном) полиморфизме ДНК: RFLP, RAPD, AFLP, ISSR, микросателлиты, SCо. T и другие. .
Молекулярные методы исследования ДНК растений, базирующиеся на фрагментном (анонимном) полиморфизме ДНК: RFLP, RAPD, AFLP, ISSR, микросателлиты, SCо. T и другие. .
 Маркеры различных последовательностей ДНК, отношение которых к структурным генам, как правило, неизвестно Молекулярные маркеры представляют собой генетические маркеры, позволяющие анализировать организм на уровне ДНК. К ним применимы термины классической генетики, такие как локус, аллель, доминантный и кодоминантный тип наследования. Аллели маркерных локусов представляют собой различные формы (нуклеотидные после довательности, отличающиеся по длине и/или по нуклеотидным заменам) одного и того же маркера, расположенные в одинаковых участках (локусах) гомологичных хромосом. Если метод анализа маркера позволяет выявлять оба аллеля, говорят о кодоминантном типе наследования данного маркера, если выявляется только один аллель – о доминантном наследовании
Маркеры различных последовательностей ДНК, отношение которых к структурным генам, как правило, неизвестно Молекулярные маркеры представляют собой генетические маркеры, позволяющие анализировать организм на уровне ДНК. К ним применимы термины классической генетики, такие как локус, аллель, доминантный и кодоминантный тип наследования. Аллели маркерных локусов представляют собой различные формы (нуклеотидные после довательности, отличающиеся по длине и/или по нуклеотидным заменам) одного и того же маркера, расположенные в одинаковых участках (локусах) гомологичных хромосом. Если метод анализа маркера позволяет выявлять оба аллеля, говорят о кодоминантном типе наследования данного маркера, если выявляется только один аллель – о доминантном наследовании
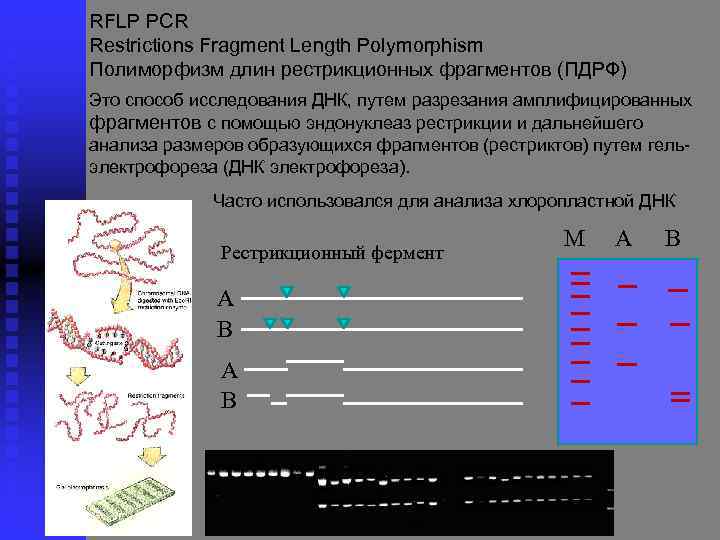 RFLP PCR Restrictions Fragment Length Polymorphism Полиморфизм длин рестрикционных фрагментов (ПДРФ) Это способ исследования ДНК, путем разрезания амплифицированных фрагментов с помощью эндонуклеаз рестрикции и дальнейшего анализа размеров образующихся фрагментов (рестриктов) путем гель электрофореза (ДНК электрофореза). Часто использовался для анализа хлоропластной ДНК Рестрикционный фермент A B М А В
RFLP PCR Restrictions Fragment Length Polymorphism Полиморфизм длин рестрикционных фрагментов (ПДРФ) Это способ исследования ДНК, путем разрезания амплифицированных фрагментов с помощью эндонуклеаз рестрикции и дальнейшего анализа размеров образующихся фрагментов (рестриктов) путем гель электрофореза (ДНК электрофореза). Часто использовался для анализа хлоропластной ДНК Рестрикционный фермент A B М А В
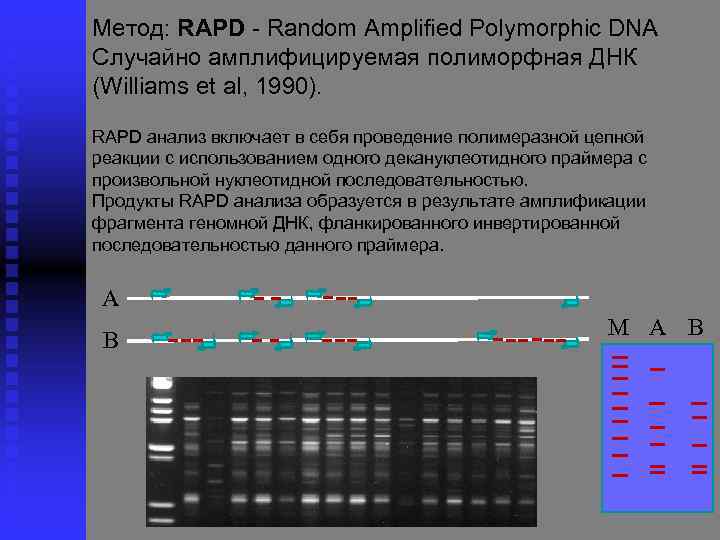 Метод: RAPD Random Amplified Polymorphic DNA Cлучайно амплифицируемая полиморфная ДНК (Williams et al, 1990). RAPD анализ включает в себя проведение полимеразной цепной реакции с использованием одного декануклеотидного праймера с произвольной нуклеотидной последовательностью. Продукты RAPD анализа образуется в результате амплификации фрагмента геномной ДНК, фланкированного инвертированной последовательностью данного праймера. A B М А В
Метод: RAPD Random Amplified Polymorphic DNA Cлучайно амплифицируемая полиморфная ДНК (Williams et al, 1990). RAPD анализ включает в себя проведение полимеразной цепной реакции с использованием одного декануклеотидного праймера с произвольной нуклеотидной последовательностью. Продукты RAPD анализа образуется в результате амплификации фрагмента геномной ДНК, фланкированного инвертированной последовательностью данного праймера. A B М А В
 Плюсы и минусы RAPD Метода: Доминантный маркер + Сравнительно быстрый и дещевый метод - Высокая чувствительность к изменениям условий реакций – сравнивать можно только фрагменты амплификации из одной ПЦР реакции ограниченное количество образцов в каждом анализе Для повышения достоверности необходимо использование большого количества ПЦР реакций с различтыми праймерами RAPD анализ может служить своеобразным экспресс методом выявления генетического полиморфизма, что особенно актуально для малоизученных таксономических групп, Диагностические возможности RAPD технологии успешно проиллюстрированы на многочисленных примерах описания генетического разнообразия микроорганизмов, высших растений, беспозвоночных и позвоночных животных.
Плюсы и минусы RAPD Метода: Доминантный маркер + Сравнительно быстрый и дещевый метод - Высокая чувствительность к изменениям условий реакций – сравнивать можно только фрагменты амплификации из одной ПЦР реакции ограниченное количество образцов в каждом анализе Для повышения достоверности необходимо использование большого количества ПЦР реакций с различтыми праймерами RAPD анализ может служить своеобразным экспресс методом выявления генетического полиморфизма, что особенно актуально для малоизученных таксономических групп, Диагностические возможности RAPD технологии успешно проиллюстрированы на многочисленных примерах описания генетического разнообразия микроорганизмов, высших растений, беспозвоночных и позвоночных животных.
 AFLP - Amplified Fragment Length Polymorphism AFLP маркеры – маркеры полиморфизма длин амплифицированных фрагментов ДНК (Vos et al. , 1995). 1 Геномная ДНК рестрицируется двумя рестриктазами (Eco. RI и Mse. I) с образованием фрагментов с выступающими 3’ – концами. 2 Рестрицированная геномная ДНК легируется с адаптером, содержащим «липкие» концы для данных рестрикционных сайтов. Далее проводятся две последовательные ПЦР: 3 В первой ПЦР используются праймеры полностью комплементарные адаптерам Eco. RI и Mse. I, в результате чего образуется большое количество продуктов амплификации между адаптерами Eco. RI и Mse. I, которые невозможно дифференцировать с помощью электрофореза. Eco. RI 1 4 Во второй ПЦР праймеры с адаптерами Eco. RI и Mse. I 2 содержат на 3’ – конце дополнительные и 4 3 некомплементарные адаптерам основания (от 1 до 3) для селективной амплификации.
AFLP - Amplified Fragment Length Polymorphism AFLP маркеры – маркеры полиморфизма длин амплифицированных фрагментов ДНК (Vos et al. , 1995). 1 Геномная ДНК рестрицируется двумя рестриктазами (Eco. RI и Mse. I) с образованием фрагментов с выступающими 3’ – концами. 2 Рестрицированная геномная ДНК легируется с адаптером, содержащим «липкие» концы для данных рестрикционных сайтов. Далее проводятся две последовательные ПЦР: 3 В первой ПЦР используются праймеры полностью комплементарные адаптерам Eco. RI и Mse. I, в результате чего образуется большое количество продуктов амплификации между адаптерами Eco. RI и Mse. I, которые невозможно дифференцировать с помощью электрофореза. Eco. RI 1 4 Во второй ПЦР праймеры с адаптерами Eco. RI и Mse. I 2 содержат на 3’ – конце дополнительные и 4 3 некомплементарные адаптерам основания (от 1 до 3) для селективной амплификации.
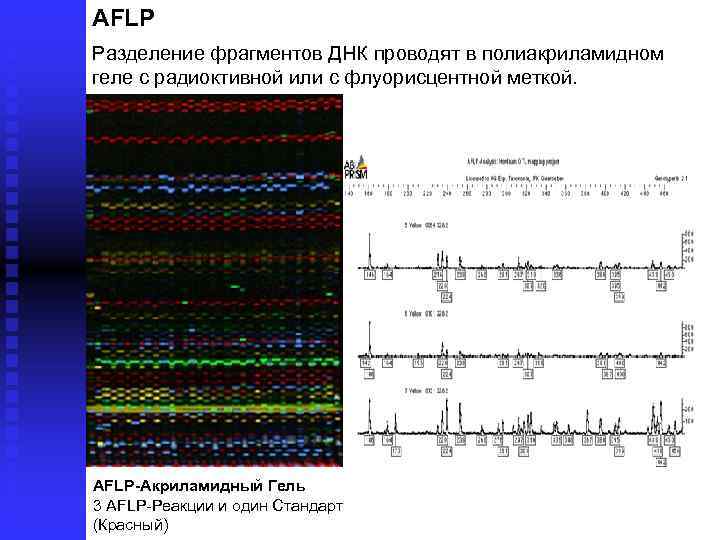 AFLP Разделение фрагментов ДНК проводят в полиакриламидном геле с радиоктивной или с флуорисцентной меткой. AFLP-Акриламидный Гель 3 AFLP Реакции и один Стандарт (Красный)
AFLP Разделение фрагментов ДНК проводят в полиакриламидном геле с радиоктивной или с флуорисцентной меткой. AFLP-Акриламидный Гель 3 AFLP Реакции и один Стандарт (Красный)
 Плюсы и минусы AFLP Метода: Доминантный маркер + Полиморфизм AFLP выше чем у RAPD и ISSR. + неограниченное количество образцов в каждом анализе - Сравнительно дорогое оборудование, програмное обеспечение и также дорогие расходные материалы.
Плюсы и минусы AFLP Метода: Доминантный маркер + Полиморфизм AFLP выше чем у RAPD и ISSR. + неограниченное количество образцов в каждом анализе - Сравнительно дорогое оборудование, програмное обеспечение и также дорогие расходные материалы.
 ISSR — Inter Simple Sequence Repeats (Zietkiewicz et al, 1994). ISSR маркеры – маркеры основанные на межмикросателитных последовательностях При ISSR анализе также как и в RAPD используется один или несколько праймеров длиной 15 24 нуклеотида. Праймеры комплементарны повторяющимся участкам генома, таким как микросателлиты. Микросателлиты характеризуются высокой скоростью изменения последовательностей, обусловленной «проскальзыванием» при репликации ДНК и точечными мутациями. Микросателлитная ДНК – ДНК из коротких тандемных повторов длиной от 1 до 6 пар оснований. Используются как молекулярные маркеры в определении родства, принадлежности к конкретной популяции, для исследования гибридизации. Пример ISSR праймера 5‘ CACACACAG 3‘
ISSR — Inter Simple Sequence Repeats (Zietkiewicz et al, 1994). ISSR маркеры – маркеры основанные на межмикросателитных последовательностях При ISSR анализе также как и в RAPD используется один или несколько праймеров длиной 15 24 нуклеотида. Праймеры комплементарны повторяющимся участкам генома, таким как микросателлиты. Микросателлиты характеризуются высокой скоростью изменения последовательностей, обусловленной «проскальзыванием» при репликации ДНК и точечными мутациями. Микросателлитная ДНК – ДНК из коротких тандемных повторов длиной от 1 до 6 пар оснований. Используются как молекулярные маркеры в определении родства, принадлежности к конкретной популяции, для исследования гибридизации. Пример ISSR праймера 5‘ CACACACAG 3‘
 Плюсы и минусы ISSR Метода: Доминантный маркер + Сравнительно быстрый и дешевый метод Относительно высокая точность и улучшенная воспроизводимость по сравнению с RAPD в связи с большей длиной праймера и более высокой температурой отжига. Однако локализация в геноме продуктов амплификации, так же как и функция, остаются неизвестными
Плюсы и минусы ISSR Метода: Доминантный маркер + Сравнительно быстрый и дешевый метод Относительно высокая точность и улучшенная воспроизводимость по сравнению с RAPD в связи с большей длиной праймера и более высокой температурой отжига. Однако локализация в геноме продуктов амплификации, так же как и функция, остаются неизвестными
 Simple Sequence Repeats (SSRs) Микросателиты ПЦР с флангирующими праймерами к короткому мини или микросателитному повтору позволяет выявлять маркеры с кодоминантным наследованием и, соответственно, удобен для выявления гетерозигот по данному локусу. Однако, одна пара праймеров для флангов в ПЦР позволяет рассматривать полиморфизм только одного локуса. Для многих микросателлитных локусов не удается выявить полиморфизм. Как правило, фланкирующие последовательности для данного микросателлитного локуса оказываются видоспецифичными.
Simple Sequence Repeats (SSRs) Микросателиты ПЦР с флангирующими праймерами к короткому мини или микросателитному повтору позволяет выявлять маркеры с кодоминантным наследованием и, соответственно, удобен для выявления гетерозигот по данному локусу. Однако, одна пара праймеров для флангов в ПЦР позволяет рассматривать полиморфизм только одного локуса. Для многих микросателлитных локусов не удается выявить полиморфизм. Как правило, фланкирующие последовательности для данного микросателлитного локуса оказываются видоспецифичными.
 SSR - Simple Sequence Repeats Кодоминантный маркер универсальность метода в использовании высокая степень полиморфизма возможность делать внутривидовые филогенетические построения, в том числе изучать малые, изолированные и однополые популяции ограничение: участие в рекомбинационном процессе, трудно сравнивать далекие в систематическом отношении организмы
SSR - Simple Sequence Repeats Кодоминантный маркер универсальность метода в использовании высокая степень полиморфизма возможность делать внутривидовые филогенетические построения, в том числе изучать малые, изолированные и однополые популяции ограничение: участие в рекомбинационном процессе, трудно сравнивать далекие в систематическом отношении организмы
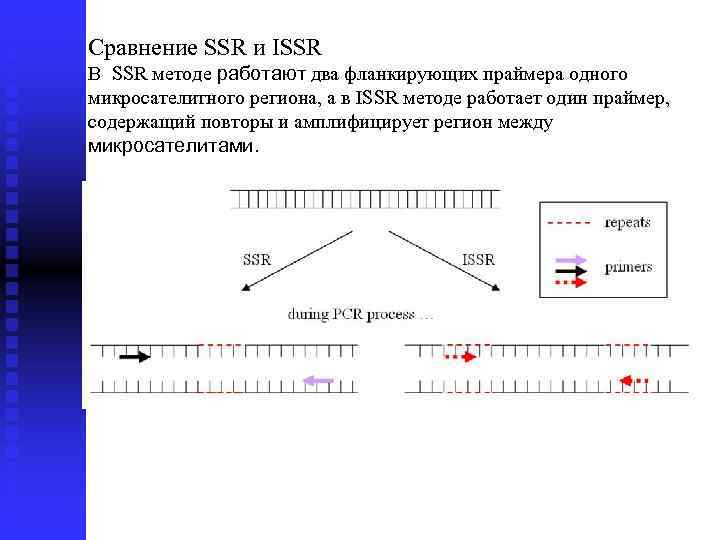 Сравнение SSR и ISSR В SSR методе работают два фланкирующих праймера одного микросателитного региона, а в ISSR методе работает один праймер, содержащий повторы и амплифицирует регион между микросателитами.
Сравнение SSR и ISSR В SSR методе работают два фланкирующих праймера одного микросателитного региона, а в ISSR методе работает один праймер, содержащий повторы и амплифицирует регион между микросателитами.
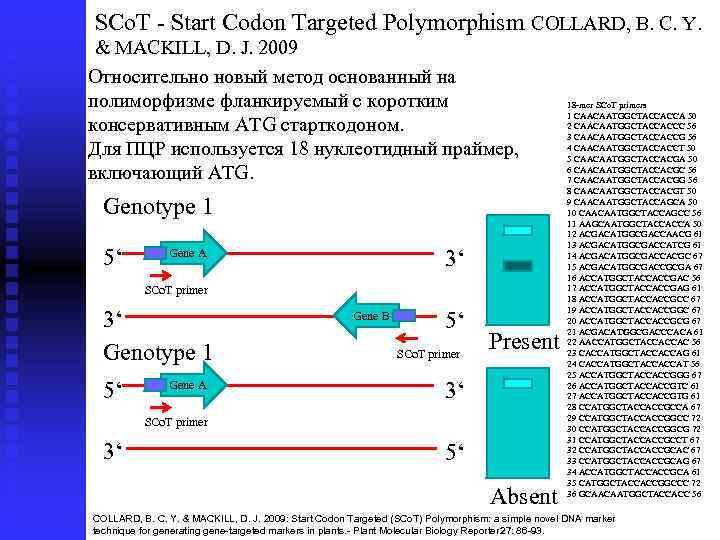 SCo. T - Start Codon Targeted Polymorphism COLLARD, B. C. Y. & MACKILL, D. J. 2009 Относительно новый метод основанный на полиморфизме фланкируемый с коротким консервативным ATG старткодоном. Для ПЦР используется 18 нуклеотидный праймер, включающий ATG. Genotype 1 5‘ 3‘ Gene A SCo. T primer 3‘ Genotype 1 5‘ Gene A Gene B 5‘ SCo. T primer Present 3‘ SCo. T primer 3‘ 5‘ Absent 18 -mer SCo. T primers 1 CAACAATGGCTACCACCA 50 2 CAACAATGGCTACCACCC 56 3 CAACAATGGCTACCACCG 56 4 CAACAATGGCTACCACCT 50 5 CAACAATGGCTACCACGA 50 6 CAACAATGGCTACCACGC 56 7 CAACAATGGCTACCACGG 56 8 CAACAATGGCTACCACGT 50 9 CAACAATGGCTACCAGCA 50 10 CAACAATGGCTACCAGCC 56 11 AAGCAATGGCTACCACCA 50 12 ACGACATGGCGACCAACG 61 13 ACGACATGGCGACCATCG 61 14 ACGACATGGCGACCACGC 67 15 ACGACATGGCGACCGCGA 67 16 ACCATGGCTACCACCGAC 56 17 ACCATGGCTACCACCGAG 61 18 ACCATGGCTACCACCGCC 67 19 ACCATGGCTACCACCGGC 67 20 ACCATGGCTACCACCGCG 67 21 ACGACATGGCGACCCACA 61 22 AACCATGGCTACCACCAC 56 23 CACCATGGCTACCACCAG 61 24 CACCATGGCTACCACCAT 56 25 ACCATGGCTACCACCGGG 67 26 ACCATGGCTACCACCGTC 61 27 ACCATGGCTACCACCGTG 61 28 CCATGGCTACCACCGCCA 67 29 CCATGGCTACCACCGGCC 72 30 CCATGGCTACCACCGGCG 72 31 CCATGGCTACCACCGCCT 67 32 CCATGGCTACCACCGCAC 67 33 CCATGGCTACCACCGCAG 67 34 ACCATGGCTACCACCGCA 61 35 CATGGCTACCACCGGCCC 72 36 GCAACAATGGCTACCACC 56 COLLARD, B. C. Y. & MACKILL, D. J. 2009: Start Codon Targeted (SCo. T) Polymorphism: a simple novel DNA marker technique for generating gene targeted markers in plants. Plant Molecular Biology Reporter 7: 86 93. 2
SCo. T - Start Codon Targeted Polymorphism COLLARD, B. C. Y. & MACKILL, D. J. 2009 Относительно новый метод основанный на полиморфизме фланкируемый с коротким консервативным ATG старткодоном. Для ПЦР используется 18 нуклеотидный праймер, включающий ATG. Genotype 1 5‘ 3‘ Gene A SCo. T primer 3‘ Genotype 1 5‘ Gene A Gene B 5‘ SCo. T primer Present 3‘ SCo. T primer 3‘ 5‘ Absent 18 -mer SCo. T primers 1 CAACAATGGCTACCACCA 50 2 CAACAATGGCTACCACCC 56 3 CAACAATGGCTACCACCG 56 4 CAACAATGGCTACCACCT 50 5 CAACAATGGCTACCACGA 50 6 CAACAATGGCTACCACGC 56 7 CAACAATGGCTACCACGG 56 8 CAACAATGGCTACCACGT 50 9 CAACAATGGCTACCAGCA 50 10 CAACAATGGCTACCAGCC 56 11 AAGCAATGGCTACCACCA 50 12 ACGACATGGCGACCAACG 61 13 ACGACATGGCGACCATCG 61 14 ACGACATGGCGACCACGC 67 15 ACGACATGGCGACCGCGA 67 16 ACCATGGCTACCACCGAC 56 17 ACCATGGCTACCACCGAG 61 18 ACCATGGCTACCACCGCC 67 19 ACCATGGCTACCACCGGC 67 20 ACCATGGCTACCACCGCG 67 21 ACGACATGGCGACCCACA 61 22 AACCATGGCTACCACCAC 56 23 CACCATGGCTACCACCAG 61 24 CACCATGGCTACCACCAT 56 25 ACCATGGCTACCACCGGG 67 26 ACCATGGCTACCACCGTC 61 27 ACCATGGCTACCACCGTG 61 28 CCATGGCTACCACCGCCA 67 29 CCATGGCTACCACCGGCC 72 30 CCATGGCTACCACCGGCG 72 31 CCATGGCTACCACCGCCT 67 32 CCATGGCTACCACCGCAC 67 33 CCATGGCTACCACCGCAG 67 34 ACCATGGCTACCACCGCA 61 35 CATGGCTACCACCGGCCC 72 36 GCAACAATGGCTACCACC 56 COLLARD, B. C. Y. & MACKILL, D. J. 2009: Start Codon Targeted (SCo. T) Polymorphism: a simple novel DNA marker technique for generating gene targeted markers in plants. Plant Molecular Biology Reporter 7: 86 93. 2
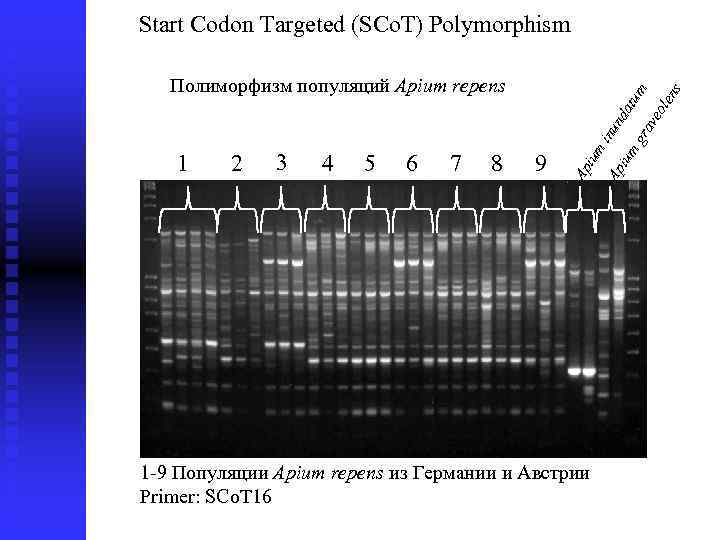 4 5 6 7 8 9 1 -9 Популяции Apium repens из Германии и Австрии Primer: SCo. T 16 gr ium 3 Ap 2 Ap 1 ium inu nd a tum Полиморфизм популяций Apium repens av eo len s Start Codon Targeted (SCo. T) Polymorphism
4 5 6 7 8 9 1 -9 Популяции Apium repens из Германии и Австрии Primer: SCo. T 16 gr ium 3 Ap 2 Ap 1 ium inu nd a tum Полиморфизм популяций Apium repens av eo len s Start Codon Targeted (SCo. T) Polymorphism
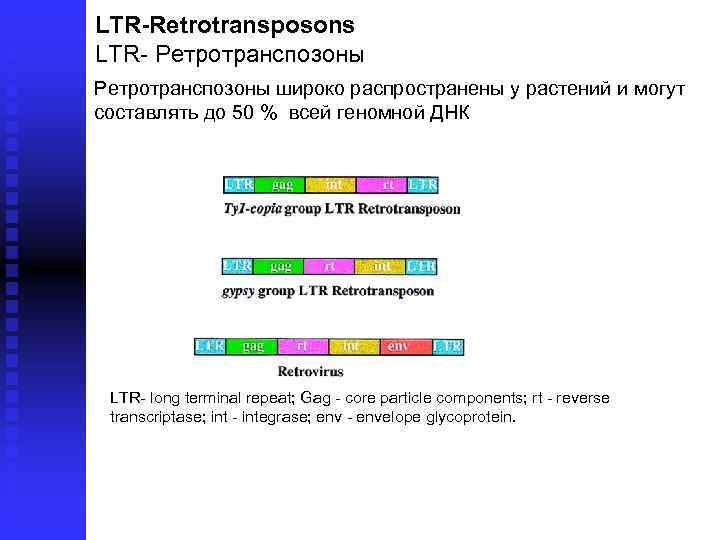 LTR-Retrotransposons LTR Ретротранспозоны широко распространены у растений и могут составлять до 50 % всей геномной ДНК LTR long terminal repeat; Gag core particle components; rt reverse transcriptase; integrase; envelope glycoprotein.
LTR-Retrotransposons LTR Ретротранспозоны широко распространены у растений и могут составлять до 50 % всей геномной ДНК LTR long terminal repeat; Gag core particle components; rt reverse transcriptase; integrase; envelope glycoprotein.
 Обработка и анализ данных фрагментного анализа 1. Перевод наличие или отсутствие одинаковых фрагментов ДНК в бинарную матрицу (есть / нет полосы) a. Анализ геля на наличие полос вручную или при помощи программ Программы : Phoretix 1 D Professional Gene. Mapper Программы бесплатные: Cross. Checker (http: //www. plantbreeding. wur. nl/UK/software_crosschecker. html) В любом случае проверка вручную на адекватность интерпретации !
Обработка и анализ данных фрагментного анализа 1. Перевод наличие или отсутствие одинаковых фрагментов ДНК в бинарную матрицу (есть / нет полосы) a. Анализ геля на наличие полос вручную или при помощи программ Программы : Phoretix 1 D Professional Gene. Mapper Программы бесплатные: Cross. Checker (http: //www. plantbreeding. wur. nl/UK/software_crosschecker. html) В любом случае проверка вручную на адекватность интерпретации !
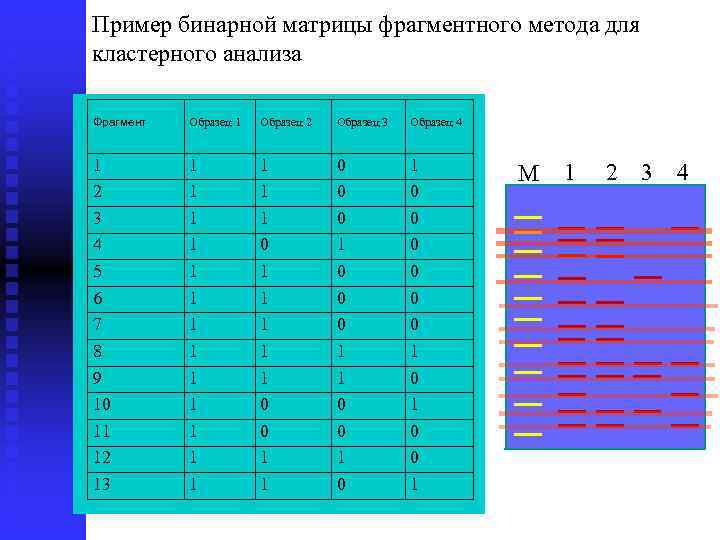 Пример бинарной матрицы фрагментного метода для кластерного анализа Фрагмент Образец 1 Образец 2 Образец 3 Образец 4 1 2 3 4 5 6 7 8 9 10 11 12 13 1 1 1 1 0 1 1 1 0 0 0 1 1 0 0 0 1 0 0 1 М 1 2 3 4
Пример бинарной матрицы фрагментного метода для кластерного анализа Фрагмент Образец 1 Образец 2 Образец 3 Образец 4 1 2 3 4 5 6 7 8 9 10 11 12 13 1 1 1 1 0 1 1 1 0 0 0 1 1 0 0 0 1 0 0 1 М 1 2 3 4
 Обработка данных фрагментного анализа 2. Анализ сходства и построение деревьев а. Создать матрицу попарных расстояний б. Провести кластеризацию одним из имеющихся многочисленных методов ( UPGMA, NJ и т. п. ) Расстояния: коэффициенты по парного сходства ( S ) между фингерпринтами отдельно по каждому праймеру по формуле: S=2 Fab( Fa+Fb ), где Fab - число полос, общих для двух особей, Fa и Fb –общее число полос для каждой особи.
Обработка данных фрагментного анализа 2. Анализ сходства и построение деревьев а. Создать матрицу попарных расстояний б. Провести кластеризацию одним из имеющихся многочисленных методов ( UPGMA, NJ и т. п. ) Расстояния: коэффициенты по парного сходства ( S ) между фингерпринтами отдельно по каждому праймеру по формуле: S=2 Fab( Fa+Fb ), где Fab - число полос, общих для двух особей, Fa и Fb –общее число полос для каждой особи.
 Обработка микросателлитных последовательностей Перевод в частоты аллелей Проверки на соответствие распределение Харди Вайнберга Подсчет многочисленными программами для популяционной генетики (Bio. Sys, Arlequine, Gene. Pop и многие другие )
Обработка микросателлитных последовательностей Перевод в частоты аллелей Проверки на соответствие распределение Харди Вайнберга Подсчет многочисленными программами для популяционной генетики (Bio. Sys, Arlequine, Gene. Pop и многие другие )
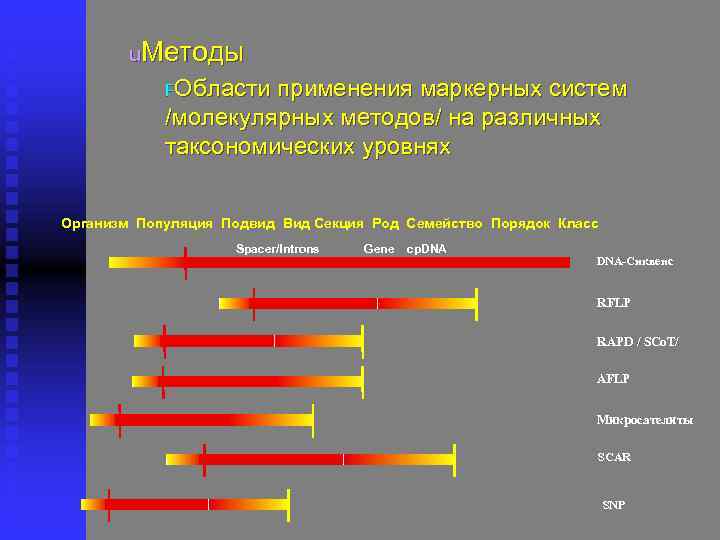 u. Методы FОбласти применения маркерных систем /молекулярных методов/ на различных таксономических уровнях Организм Популяция Подвид Вид Секция Род Семейство Порядок Класс Spacer/Introns Gene cp. DNA-Сиквенс RFLP RAPD / SCo. T/ AFLP Микросателиты SCAR SNP
u. Методы FОбласти применения маркерных систем /молекулярных методов/ на различных таксономических уровнях Организм Популяция Подвид Вид Секция Род Семейство Порядок Класс Spacer/Introns Gene cp. DNA-Сиквенс RFLP RAPD / SCo. T/ AFLP Микросателиты SCAR SNP
 "RAPD-Analyse у Allium ramosum и A. tuberosum 1 8 L 18 0 0582 0 0 0 1 1 0 1 0 0 0 1 2499 0 1 1 0 0 0 1 2014 0 1 1 0 0 0 0 1 0 2755 0 1 0 0 1 0 0 0 0 2371 0 1 0 0 1 0 0 1695 1 1 0 0 0 0 2339 0 0 0 0 1 0 0 0 0 0 3643 0 0 0 0 1 1 0 0
"RAPD-Analyse у Allium ramosum и A. tuberosum 1 8 L 18 0 0582 0 0 0 1 1 0 1 0 0 0 1 2499 0 1 1 0 0 0 1 2014 0 1 1 0 0 0 0 1 0 2755 0 1 0 0 1 0 0 0 0 2371 0 1 0 0 1 0 0 1695 1 1 0 0 0 0 2339 0 0 0 0 1 0 0 0 0 0 3643 0 0 0 0 1 1 0 0
 ДНК Таксономия и современные методы изучения последовательностей ДНК (секвенирование).
ДНК Таксономия и современные методы изучения последовательностей ДНК (секвенирование).
 ДНА секвенировани для нужд филогеники • Амплификация определенного фрагмента днк у сравнимых таксонов. • Проведение реакции секвенирования всех амплифицированных фрагментов. • Прочтение амплифицированных фрагментов на секвенаторе. • Составление алаймента. • Анализ последовательностей и построение филогенетических деревьев
ДНА секвенировани для нужд филогеники • Амплификация определенного фрагмента днк у сравнимых таксонов. • Проведение реакции секвенирования всех амплифицированных фрагментов. • Прочтение амплифицированных фрагментов на секвенаторе. • Составление алаймента. • Анализ последовательностей и построение филогенетических деревьев
 u. Методы FОбласти применения маркерных систем /молекулярных методов/ на различных таксономических уровнях Организм Популяция Подвид Вид Секция Род Семейство Порядок Класс SNP-Retrotransposons Spacer/Introns Gene cp. DNA-mn. DNA-Сиквенс RFLP RAPD / SCo. T/ AFLP Микросателиты SCAR SNP
u. Методы FОбласти применения маркерных систем /молекулярных методов/ на различных таксономических уровнях Организм Популяция Подвид Вид Секция Род Семейство Порядок Класс SNP-Retrotransposons Spacer/Introns Gene cp. DNA-mn. DNA-Сиквенс RFLP RAPD / SCo. T/ AFLP Микросателиты SCAR SNP
 Найболее популярные фрагменты ДНК используемые в филогенетике растений • ITS – internal transribed spacer of ribosomale DNA – внутригенный спейсор рибосомальной ДНК • Гены, интроны и межгенные спейсоры хлоропластной ДНК
Найболее популярные фрагменты ДНК используемые в филогенетике растений • ITS – internal transribed spacer of ribosomale DNA – внутригенный спейсор рибосомальной ДНК • Гены, интроны и межгенные спейсоры хлоропластной ДНК
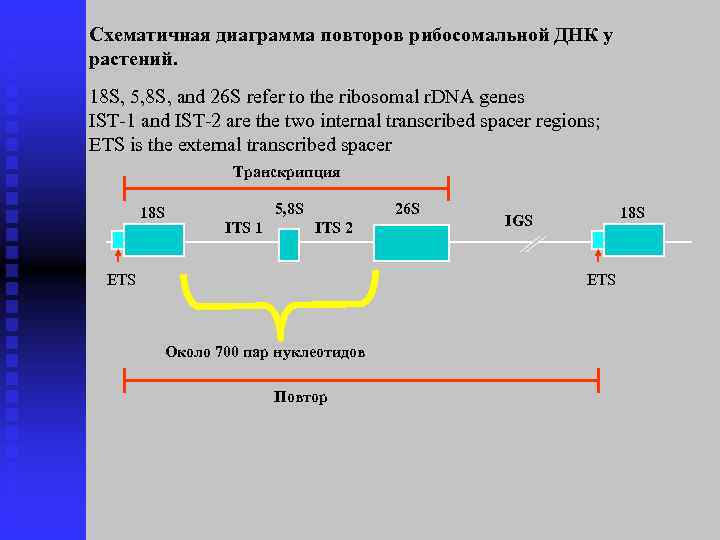 Схематичная диаграмма повторов рибосомальной ДНК у растений. 18 S, 5, 8 S, and 26 S refer to the ribosomal r. DNA genes IST-1 and IST-2 are the two internal transcribed spacer regions; ETS is the external transcribed spacer Транскрипция 18 S 5, 8 S ITS 1 26 S ITS 2 ETS 18 S IGS ETS Около 700 пар нуклеотидов Повтор
Схематичная диаграмма повторов рибосомальной ДНК у растений. 18 S, 5, 8 S, and 26 S refer to the ribosomal r. DNA genes IST-1 and IST-2 are the two internal transcribed spacer regions; ETS is the external transcribed spacer Транскрипция 18 S 5, 8 S ITS 1 26 S ITS 2 ETS 18 S IGS ETS Около 700 пар нуклеотидов Повтор
 >Am 261_nigrum AATCGTCTAGATGTAGATTCTAGAATCCGATTTAGAATGGATGAATAAAGGTTCTTTTAAACTCTTTTGTTTAAACTAAAGTATTCTTTGAATTTTTAATAACACTTAGAAAGATATTTTTATAAAATATAAATTAAATAGGATTTTATACATATCAAAATGTAATTACTAAATTTAATAAATGAAATTAGAAATTTAAAGACTCTTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTAAATGTACTTAGTGTAATTTTATTATTCTAAGTTATATAGAAAATATATAATTAATTAAGTTATAATTAAGTATATATATATACTCTTTGTTGTTATGTATATAATTTAAATATAGGATAATATTTAGTAAACAAAACCAATTTGATCTTGAGATATACATATAAT AAAACAGTTTGAATATTCATCATAATTGCATTTTATTTCTTTTCCTAATGGAAAAGAAATAATACTTAGAACCAAACTAGCAGATAAGTTAGTATTCGACATAAAATAGCAGCGAGTTCTAATCTTGAGGAG GTCAATACATAAGGTAATAAAAATTTTCCATATTCTAAATATAGAAAAGTTCTTTAAATCCCGGAATTCMAATTATTCCAAGGTTTTCTTATTTGGCGCACAAAAAAACTTTTAGAATTTCCCCGTAGAAAACTGGCTTTGGTAAAG AAAAGGCTTTTATTGCAACTAAATTTCCCTTTTTCTTCC >Am 262_victorialis AATCGTCTAGATGTAGATTCTAGAATCCGATATAGTTATACTTTAGGAAACATTAGAATGGATGAATAAAGGTTCTTTTAAACTCGTTTAAACTAAAGTATTCTTTGAATTTTTAATAACACTTAGAAAACTTAGAACGATATTTTTT TTTATCAAAAATATAAATAAATAGGATTTTATACATATCAAAATGTAATTACTAAATTTAATAAATTAGAAATTAAAAGACTCTTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGTACTTAGTATAATTTTAT TAATTATTCTAATTATATAGAAAATATATAATTAATTATATATATATACTCTTTGTTGTTATGTACATAATTTAAATATAGGATAATATTTAGAAAACCAATTTGATCTTGAGATATACATATAA TAAAACAGTTTTAATATTCATCATAATTGCATTTTATTTCTTTTCCTAATGGAAAATTTTCTACTGAGAAATAAAATAATACTTAGAACCAAACTAGCAGATAAGTTAGTATTCGACATAAAATAGCAGCGA GTTCTAACAAATCTTGAGGAGGTCAATACATAAGTTAATGAAAATTTTTCATATTCTAAATATAGAAAAATTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTCTTATTTGCTGCACAAAAAAACTTTTTGAATTTCCTGTAG AAACTGACTTTGCTAAAGAAAAGGCTTTTATTGCAACTAAATTTCCCTTTTTCTTCC >Am 264_wallichii AATCGTCTAGATGTAGATTCTAGAATCCGATCTAGTTATACTTTAGTAAACATTAGAATAGATTAATAAGGGTTCCTTTCAACTCTTTTGTTTAAACTAAAGTATTCTTTAAATTGTTAATAACACTTATAAAACTTAGAAAAATAT TTTTATTAAAATATAAATTCGATAAATAGGATTTTATACATATCAAAATGAAATTAAAGGACTCTTTTTCGAAAAATCTTGTTTTTAGTCTACTTTTTTTAATGTACTTAATGTAATTTCATTATTCGAATTCT ATAAATATAGAAAATATAATGTTAATTATATAAAAAATATATTTTTTTTATATACTCTTTGTTGTTATGTACATAATTTTAATATAGGATAATATTTAGTAAAGGGAACCAATTTGATCTTC AGATAGACATATAATAAAACAAAATAGTTTTAATATTCATCATAATTTCATTTTATTTCTTTTCCTAATGGAAAAAAATATTTTTCTACTGGGAAAAGAAATAATACTTAGAACCAAACTAGTA GACAGATAAGTTAGTATTCGACATAAAATAGCAGCGAGTTCTAATCTTGAGGAGGTCAATACATAAGTTAATGCAAATTTTTCATATTCTAAATATAGAAAAGTTCTTTAAATCACAGAATTCAAATTATTCCAAGATTTTCTTATT TGTTTGCCGCACAAAAAAACTTTTTGAATTTCCCGTAGAAACGGACTTTGCTAAAGAAAAGGCTTTTATTGCAACTAAATTTCCCCTTTTCTTCC >Am 263_insubricum GATCGCAGATGGGATTCAGAATCCGTATAGTTATACTTAGGAAACATTAGAATAGATGAATAAGGGTTCCTTTCAACTCTTTTGGTTAATTTAAACTAAAGTATTCTTTAAATTGTTAATAACACTTATAAAACTTAGAAAGATATTTCTT TAAATTCAAAGAAATATAAATTCAATAGGATTTTATACCCNATCAAAATGTAATTACTAAATTTCATAARTGAAATTCGAAATTAAAGGACTCTTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGTACTTAATGTAATTTCA TGAATTATTATTTCATTATTCTAATTATATAAATATAGAAAATATAATGTTAATTATATAAAATATATTCTTTGTTTATATACTCTTTGTTGTTATGTACATAATTTAAATATAGGATAATATTTAGTAAACG AAACCCATTTTATTTGATCTTCAGATAGACATATAATAAAACAAAATAGTTTTAATATTCATCATAATTACATTTTCTTTTCCTAATAGAAAAAAATATTTTTCTACTGGGAAAAGRAAAAAAATTAATACTTAGAACCAAACTAGT AGACAGATAAGTTAGTATTCGACATAAAATAGCAACTTAGTTCTAATCTTGAGGAGGTCAATACATAAGTTAATGCAAATTTTTCATATTCTAAATATAGAAAAGTTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTATTA TTTGCCGCACAAAAAAACTTTTTGAATTTCCCGTAGAAACTGACTTGCAAAGAAAAGGCTTTTATG >Am 277_oreoprason AATCGTCTAGATGTAGATTCTAGAATCCGATATAGTTATACTTTAGGAAACATTAGAATGGATGAATAAGGGTTCTTTTAAACTCTTTTGTTTAAAATAAAGTATTCTTTGCATTTTTAATAACAATTAGAAAACTTAGAAAGATCTTTTTT ATCAAAAATATATTTATCAAAAATATAAATAAATAGGATTTTTTACATATAAAAATGTAATTACTAAATTTAATAAATTAGAAATTCAAAGACTCTTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGT ACTTAGTGTAATTAATTATTCTAATTATATAGAAAATATACTTTTTGTTGTTATGTACATAATTTAAATATAGGATAATATTTAGTAAACAAAACCAATTTTATTTGATCTTGAGATAGACATATAATAAAACA GTTTTAATATTCATCATAATTGCATTTTATTTCTTTTCCTAATGGAAAAAAATTTTTCTACTGGGAAAAGAAATAATACTTAGACCCAAACTAGCAAACAGATAAGTTAGTATTCGACATAAAATAGTAGCTTGTTCTAATC TTGAAGAGGTCAATACATAAGTTAATGAAAATTTTTCATATTCTATAGAAAAGTTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTCTTATTTGCCGCACAAAAAAACTTTTTGAATTTCCCGTAGAA ACTGACTTTGCTAAGGAAAAGGCTTTTATTGCAACTAAATTTCCCTTTTTCTTCC >Am 270_tuvinicum AATCGTCTAGATGTAGATTCTAGAATCCGATATAGTTATCCTTTAGGAAATGGATGAATAAGGGTTCTTTTAAACTCTTTTGTTTAAACTAAAGTATTCTTTTTAATAACACTTAGAAAGATCTTTTTTATCAAAAAGAAATATAAATAAATAGGATGATTTTATACATATCAAAATATAATTACTAATTTTAATAAATTAGAAATAAAAAGACTCGTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGTATTTAGTGTAATTT AATTATTCTAATTATATAGTGATTATATAGAAAATATATATATAATAATTATATTAATATTTGTTGTTATGTACATAATTTAAATATAGAATNATAATTAGTAANCAAAACAAATTTCATTTGATCTTGAGATAGA CATATAATAAAACAGTTTTAATATTCATTATAATTACATTTTATTTCTTTTCCTAATGGAAAAAAATTTCTACTGGGAAAAGAAATAATACTTAGAACCAAACTAGCAGATAAGTTAATATTCGACATAAAATAGCTGCTA GTTCTAATCTTGAGGAGGTAAATACAAAAGTTAATGAAAAATTTTCCTATTCTATATATGGAAAAGTTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTCTTATTTGCCGAACAAAAAAACTTTTTGAATTTCTC GTAGAAACTGACTTTGCTAAAGAAAAGGCTTTTATTGCAACCAAATTTCCTTTTTTCTTCC >Am 278_eduardii AATCGTCTAGATGTAGATTCTAGAATCCGATATAGTTATCCTTTAGGAAATGGATGAATAAGGGTTCTTTTAAACTCTTTTGTTTAAACTAAAGTATTCTTTTTAATAACACTTAGAAAGATCTTTTTTATCAAAAAGAAATATAANTTAAATAGGANGATTTTATACATATCAAAATATAATTACTAAATTTAATAAATTANAAATTAAAAGACTCGTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGTATTTAGTGT AATTTAATTATTCTAATTATATAGTGATTATATAGAAAATATATAATAATTATATTAATATTTGTTGTTATGTACATAATTTAAATATAGAATAATAATTAGTAAACAAATTTCATTTGATCTTGAGATAGAC ATATAATAAAACAGTTTTAATATTCATTATAATTACATTTTATTTCTTTTCCTAATGGAAAAAAATTTCTACTGGGAAAAGAAATAATACTTAGAACCAAACTAGCAGATAAGTTAATATTCGACATAAAATAGCTGCTAG TTCTAATCTTGAGGAGGTAAATACATAAGTTAATGAAAAATTTTCATATTCTATAGAAAAGTTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTCTTATTTGTCGAACAAAAAAACTTTTTGAATTTCTCG TAGAAACTGACTTTGCTAAAGAAAAGGCTTTTATTGCAACTAAATTTCCCTTTTTCTTCC
>Am 261_nigrum AATCGTCTAGATGTAGATTCTAGAATCCGATTTAGAATGGATGAATAAAGGTTCTTTTAAACTCTTTTGTTTAAACTAAAGTATTCTTTGAATTTTTAATAACACTTAGAAAGATATTTTTATAAAATATAAATTAAATAGGATTTTATACATATCAAAATGTAATTACTAAATTTAATAAATGAAATTAGAAATTTAAAGACTCTTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTAAATGTACTTAGTGTAATTTTATTATTCTAAGTTATATAGAAAATATATAATTAATTAAGTTATAATTAAGTATATATATATACTCTTTGTTGTTATGTATATAATTTAAATATAGGATAATATTTAGTAAACAAAACCAATTTGATCTTGAGATATACATATAAT AAAACAGTTTGAATATTCATCATAATTGCATTTTATTTCTTTTCCTAATGGAAAAGAAATAATACTTAGAACCAAACTAGCAGATAAGTTAGTATTCGACATAAAATAGCAGCGAGTTCTAATCTTGAGGAG GTCAATACATAAGGTAATAAAAATTTTCCATATTCTAAATATAGAAAAGTTCTTTAAATCCCGGAATTCMAATTATTCCAAGGTTTTCTTATTTGGCGCACAAAAAAACTTTTAGAATTTCCCCGTAGAAAACTGGCTTTGGTAAAG AAAAGGCTTTTATTGCAACTAAATTTCCCTTTTTCTTCC >Am 262_victorialis AATCGTCTAGATGTAGATTCTAGAATCCGATATAGTTATACTTTAGGAAACATTAGAATGGATGAATAAAGGTTCTTTTAAACTCGTTTAAACTAAAGTATTCTTTGAATTTTTAATAACACTTAGAAAACTTAGAACGATATTTTTT TTTATCAAAAATATAAATAAATAGGATTTTATACATATCAAAATGTAATTACTAAATTTAATAAATTAGAAATTAAAAGACTCTTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGTACTTAGTATAATTTTAT TAATTATTCTAATTATATAGAAAATATATAATTAATTATATATATATACTCTTTGTTGTTATGTACATAATTTAAATATAGGATAATATTTAGAAAACCAATTTGATCTTGAGATATACATATAA TAAAACAGTTTTAATATTCATCATAATTGCATTTTATTTCTTTTCCTAATGGAAAATTTTCTACTGAGAAATAAAATAATACTTAGAACCAAACTAGCAGATAAGTTAGTATTCGACATAAAATAGCAGCGA GTTCTAACAAATCTTGAGGAGGTCAATACATAAGTTAATGAAAATTTTTCATATTCTAAATATAGAAAAATTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTCTTATTTGCTGCACAAAAAAACTTTTTGAATTTCCTGTAG AAACTGACTTTGCTAAAGAAAAGGCTTTTATTGCAACTAAATTTCCCTTTTTCTTCC >Am 264_wallichii AATCGTCTAGATGTAGATTCTAGAATCCGATCTAGTTATACTTTAGTAAACATTAGAATAGATTAATAAGGGTTCCTTTCAACTCTTTTGTTTAAACTAAAGTATTCTTTAAATTGTTAATAACACTTATAAAACTTAGAAAAATAT TTTTATTAAAATATAAATTCGATAAATAGGATTTTATACATATCAAAATGAAATTAAAGGACTCTTTTTCGAAAAATCTTGTTTTTAGTCTACTTTTTTTAATGTACTTAATGTAATTTCATTATTCGAATTCT ATAAATATAGAAAATATAATGTTAATTATATAAAAAATATATTTTTTTTATATACTCTTTGTTGTTATGTACATAATTTTAATATAGGATAATATTTAGTAAAGGGAACCAATTTGATCTTC AGATAGACATATAATAAAACAAAATAGTTTTAATATTCATCATAATTTCATTTTATTTCTTTTCCTAATGGAAAAAAATATTTTTCTACTGGGAAAAGAAATAATACTTAGAACCAAACTAGTA GACAGATAAGTTAGTATTCGACATAAAATAGCAGCGAGTTCTAATCTTGAGGAGGTCAATACATAAGTTAATGCAAATTTTTCATATTCTAAATATAGAAAAGTTCTTTAAATCACAGAATTCAAATTATTCCAAGATTTTCTTATT TGTTTGCCGCACAAAAAAACTTTTTGAATTTCCCGTAGAAACGGACTTTGCTAAAGAAAAGGCTTTTATTGCAACTAAATTTCCCCTTTTCTTCC >Am 263_insubricum GATCGCAGATGGGATTCAGAATCCGTATAGTTATACTTAGGAAACATTAGAATAGATGAATAAGGGTTCCTTTCAACTCTTTTGGTTAATTTAAACTAAAGTATTCTTTAAATTGTTAATAACACTTATAAAACTTAGAAAGATATTTCTT TAAATTCAAAGAAATATAAATTCAATAGGATTTTATACCCNATCAAAATGTAATTACTAAATTTCATAARTGAAATTCGAAATTAAAGGACTCTTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGTACTTAATGTAATTTCA TGAATTATTATTTCATTATTCTAATTATATAAATATAGAAAATATAATGTTAATTATATAAAATATATTCTTTGTTTATATACTCTTTGTTGTTATGTACATAATTTAAATATAGGATAATATTTAGTAAACG AAACCCATTTTATTTGATCTTCAGATAGACATATAATAAAACAAAATAGTTTTAATATTCATCATAATTACATTTTCTTTTCCTAATAGAAAAAAATATTTTTCTACTGGGAAAAGRAAAAAAATTAATACTTAGAACCAAACTAGT AGACAGATAAGTTAGTATTCGACATAAAATAGCAACTTAGTTCTAATCTTGAGGAGGTCAATACATAAGTTAATGCAAATTTTTCATATTCTAAATATAGAAAAGTTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTATTA TTTGCCGCACAAAAAAACTTTTTGAATTTCCCGTAGAAACTGACTTGCAAAGAAAAGGCTTTTATG >Am 277_oreoprason AATCGTCTAGATGTAGATTCTAGAATCCGATATAGTTATACTTTAGGAAACATTAGAATGGATGAATAAGGGTTCTTTTAAACTCTTTTGTTTAAAATAAAGTATTCTTTGCATTTTTAATAACAATTAGAAAACTTAGAAAGATCTTTTTT ATCAAAAATATATTTATCAAAAATATAAATAAATAGGATTTTTTACATATAAAAATGTAATTACTAAATTTAATAAATTAGAAATTCAAAGACTCTTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGT ACTTAGTGTAATTAATTATTCTAATTATATAGAAAATATACTTTTTGTTGTTATGTACATAATTTAAATATAGGATAATATTTAGTAAACAAAACCAATTTTATTTGATCTTGAGATAGACATATAATAAAACA GTTTTAATATTCATCATAATTGCATTTTATTTCTTTTCCTAATGGAAAAAAATTTTTCTACTGGGAAAAGAAATAATACTTAGACCCAAACTAGCAAACAGATAAGTTAGTATTCGACATAAAATAGTAGCTTGTTCTAATC TTGAAGAGGTCAATACATAAGTTAATGAAAATTTTTCATATTCTATAGAAAAGTTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTCTTATTTGCCGCACAAAAAAACTTTTTGAATTTCCCGTAGAA ACTGACTTTGCTAAGGAAAAGGCTTTTATTGCAACTAAATTTCCCTTTTTCTTCC >Am 270_tuvinicum AATCGTCTAGATGTAGATTCTAGAATCCGATATAGTTATCCTTTAGGAAATGGATGAATAAGGGTTCTTTTAAACTCTTTTGTTTAAACTAAAGTATTCTTTTTAATAACACTTAGAAAGATCTTTTTTATCAAAAAGAAATATAAATAAATAGGATGATTTTATACATATCAAAATATAATTACTAATTTTAATAAATTAGAAATAAAAAGACTCGTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGTATTTAGTGTAATTT AATTATTCTAATTATATAGTGATTATATAGAAAATATATATATAATAATTATATTAATATTTGTTGTTATGTACATAATTTAAATATAGAATNATAATTAGTAANCAAAACAAATTTCATTTGATCTTGAGATAGA CATATAATAAAACAGTTTTAATATTCATTATAATTACATTTTATTTCTTTTCCTAATGGAAAAAAATTTCTACTGGGAAAAGAAATAATACTTAGAACCAAACTAGCAGATAAGTTAATATTCGACATAAAATAGCTGCTA GTTCTAATCTTGAGGAGGTAAATACAAAAGTTAATGAAAAATTTTCCTATTCTATATATGGAAAAGTTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTCTTATTTGCCGAACAAAAAAACTTTTTGAATTTCTC GTAGAAACTGACTTTGCTAAAGAAAAGGCTTTTATTGCAACCAAATTTCCTTTTTTCTTCC >Am 278_eduardii AATCGTCTAGATGTAGATTCTAGAATCCGATATAGTTATCCTTTAGGAAATGGATGAATAAGGGTTCTTTTAAACTCTTTTGTTTAAACTAAAGTATTCTTTTTAATAACACTTAGAAAGATCTTTTTTATCAAAAAGAAATATAANTTAAATAGGANGATTTTATACATATCAAAATATAATTACTAAATTTAATAAATTANAAATTAAAAGACTCGTTTTCTAAAAATCTTGTTTTTAGTCTACTTTTTAATGTATTTAGTGT AATTTAATTATTCTAATTATATAGTGATTATATAGAAAATATATAATAATTATATTAATATTTGTTGTTATGTACATAATTTAAATATAGAATAATAATTAGTAAACAAATTTCATTTGATCTTGAGATAGAC ATATAATAAAACAGTTTTAATATTCATTATAATTACATTTTATTTCTTTTCCTAATGGAAAAAAATTTCTACTGGGAAAAGAAATAATACTTAGAACCAAACTAGCAGATAAGTTAATATTCGACATAAAATAGCTGCTAG TTCTAATCTTGAGGAGGTAAATACATAAGTTAATGAAAAATTTTCATATTCTATAGAAAAGTTCTTTAAATCACGGAATTCAAATTATTCCAAGATTTTCTTATTTGTCGAACAAAAAAACTTTTTGAATTTCTCG TAGAAACTGACTTTGCTAAAGAAAAGGCTTTTATTGCAACTAAATTTCCCTTTTTCTTCC
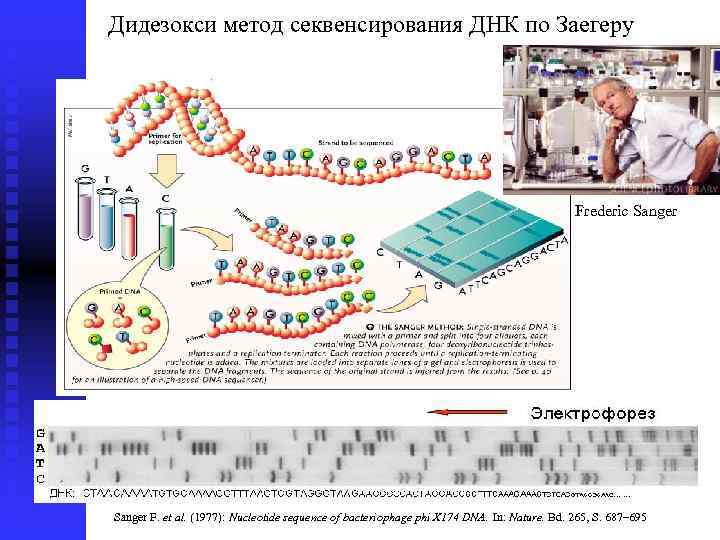 Дидезокси метод секвенсирования ДНК по Заeгеру Frederic Sanger F. et al. (1977): Nucleotide sequence of bacteriophage phi X 174 DNA. In: Nature. Bd. 265, S. 687– 695
Дидезокси метод секвенсирования ДНК по Заeгеру Frederic Sanger F. et al. (1977): Nucleotide sequence of bacteriophage phi X 174 DNA. In: Nature. Bd. 265, S. 687– 695
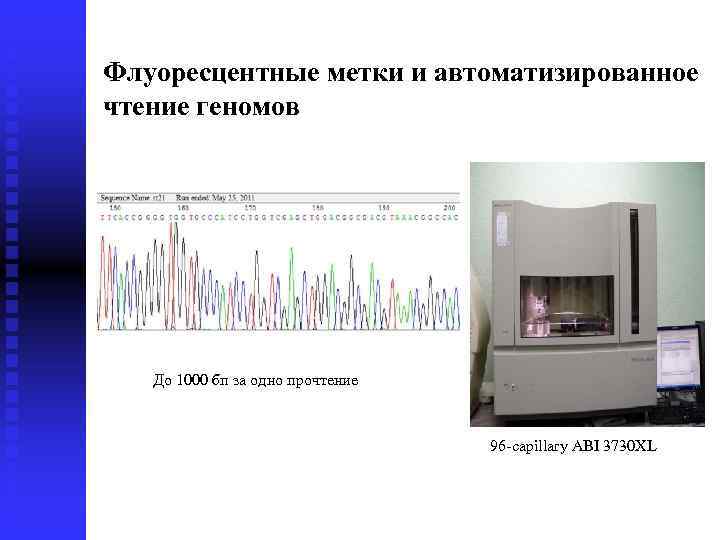 Флуоресцентные метки и автоматизированное чтение геномов До 1000 бп за одно прочтение 96 -capillary ABI 3730 XL
Флуоресцентные метки и автоматизированное чтение геномов До 1000 бп за одно прочтение 96 -capillary ABI 3730 XL
 Современные методы секвенирования второго и третьего поколения Next-generation DNA sequencing NGS the Roche/454 FLX Pyrosequencer (http: //www. 454. com/enabling- technology/the-system. asp) the Illumina/Solexa Genome Analyzer (7) (http: //www. llumina. com/pages. ilmn? ID=203) Applied Biosystems SOLi. D TM System (http: //marketing. appliedbiosystems. com/images/Product / Solid. Knowledge / flash /102207/solid. html). Анонсирова ны Helicos Heliscope TM (www. helicosbio. com) Pacific Biosciences SMRT (www. pacificbiosciences. com) instruments. И многие другие. . . .
Современные методы секвенирования второго и третьего поколения Next-generation DNA sequencing NGS the Roche/454 FLX Pyrosequencer (http: //www. 454. com/enabling- technology/the-system. asp) the Illumina/Solexa Genome Analyzer (7) (http: //www. llumina. com/pages. ilmn? ID=203) Applied Biosystems SOLi. D TM System (http: //marketing. appliedbiosystems. com/images/Product / Solid. Knowledge / flash /102207/solid. html). Анонсирова ны Helicos Heliscope TM (www. helicosbio. com) Pacific Biosciences SMRT (www. pacificbiosciences. com) instruments. И многие другие. . . .
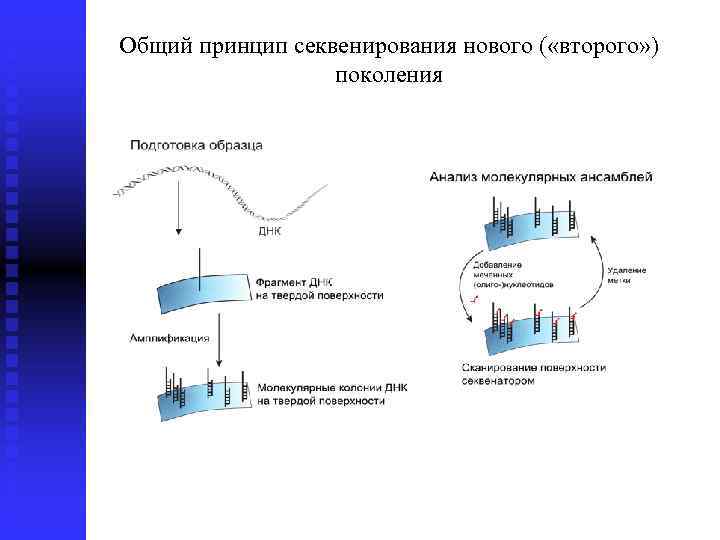 Общий принцип секвенирования нового ( «второго» ) поколения
Общий принцип секвенирования нового ( «второго» ) поколения
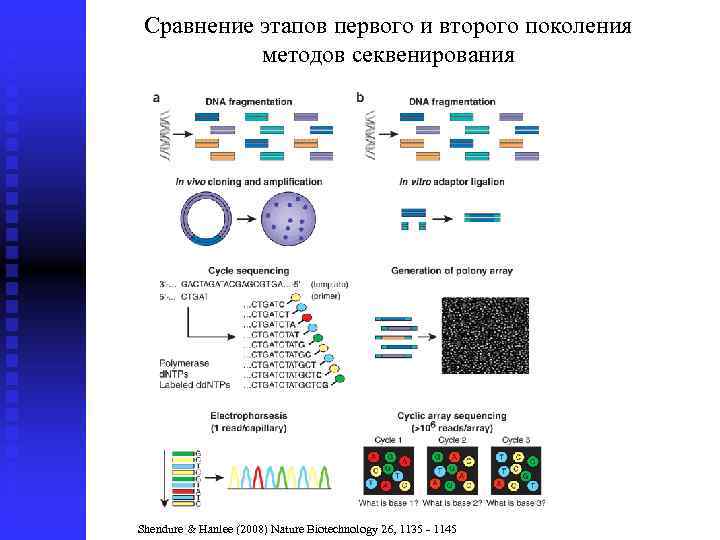 Сравнение этапов первого и второго поколения методов секвенирования Shendure 1& Hanlee (2008) Nature Biotechnology 26, 1135 - 1145
Сравнение этапов первого и второго поколения методов секвенирования Shendure 1& Hanlee (2008) Nature Biotechnology 26, 1135 - 1145
 Секвенаторы «нового поколения» — высокопроизводительные секвенаторы ДНК, не использующие метод терминации цепи Сэнгера и капиллярный электрофорез. Принципы работы приборов различаются от производителя к производителю. Производительность таких секвенаторов на несколько порядков превосходит производительность самых мощных капиллярных приборов и достигает сотен млрд. пар оснований за запуск
Секвенаторы «нового поколения» — высокопроизводительные секвенаторы ДНК, не использующие метод терминации цепи Сэнгера и капиллярный электрофорез. Принципы работы приборов различаются от производителя к производителю. Производительность таких секвенаторов на несколько порядков превосходит производительность самых мощных капиллярных приборов и достигает сотен млрд. пар оснований за запуск
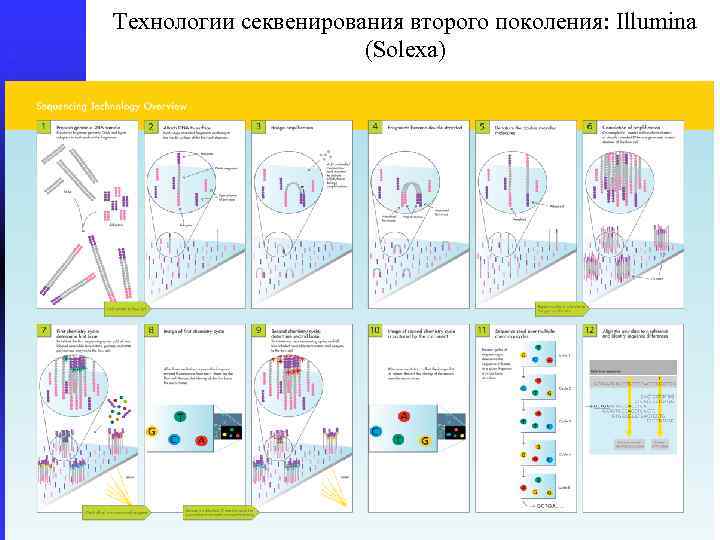 Технологии секвенирования второго поколения: Illumina (Solexa)
Технологии секвенирования второго поколения: Illumina (Solexa)
 Технологии секвенирования второго поколения: Applied Biosystems SOLi. D
Технологии секвенирования второго поколения: Applied Biosystems SOLi. D
 Сравнение производительности секвенаторов второго поколения 454 -FLX Titanium Illumina Hi. Seq Длина прочтения 240– 400 одного 700 фрагмента 2 x 100 Количество прочтенных фрагментов за одну реакцию 2 миллиарда 500 тысяч SOLi. D 5500 2 x 50 2 миллиарда
Сравнение производительности секвенаторов второго поколения 454 -FLX Titanium Illumina Hi. Seq Длина прочтения 240– 400 одного 700 фрагмента 2 x 100 Количество прочтенных фрагментов за одну реакцию 2 миллиарда 500 тысяч SOLi. D 5500 2 x 50 2 миллиарда
 Новые горизонты и ограничения в применении секвенирования второго и третьего поколения в систематике и филогенетике Чтобы «собрать» геномную последовательность из нескольких миллиардов коротких отсеквенированных фрагментов, необходимы очень мощные компьютеры и также наличие реферативного (уже) отсеквенированного ранее близкородственного генома. Для дикорастущих видов растений с большим геномом это практически еще проблематично. • Секвенирование хлоропластного Генома любых видов (наличие реферативной последовательности ) • Снип метод • Довольно быстрое определения Микросателитных примеров • И многое другое. . . .
Новые горизонты и ограничения в применении секвенирования второго и третьего поколения в систематике и филогенетике Чтобы «собрать» геномную последовательность из нескольких миллиардов коротких отсеквенированных фрагментов, необходимы очень мощные компьютеры и также наличие реферативного (уже) отсеквенированного ранее близкородственного генома. Для дикорастущих видов растений с большим геномом это практически еще проблематично. • Секвенирование хлоропластного Генома любых видов (наличие реферативной последовательности ) • Снип метод • Довольно быстрое определения Микросателитных примеров • И многое другое. . . .
 Single nucleotide polymorphism, SNP Однонуклеотидный полиморфизм (ОНП или снип) Отличия последовательности ДНК размером в один нуклеотид (A, T, G или C) в геноме (или в другой сравниваемой последовательности) представителей одного вида или между гомологичными участками гомологичных хромосом. Если две последовательности ДНК — AAGCCTA и AAGCTTA — отличаются на один нуклеотид, в таком случае говорят о существовании двух аллелей: C и T. SNP возникают в результате точечных мутаций.
Single nucleotide polymorphism, SNP Однонуклеотидный полиморфизм (ОНП или снип) Отличия последовательности ДНК размером в один нуклеотид (A, T, G или C) в геноме (или в другой сравниваемой последовательности) представителей одного вида или между гомологичными участками гомологичных хромосом. Если две последовательности ДНК — AAGCCTA и AAGCTTA — отличаются на один нуклеотид, в таком случае говорят о существовании двух аллелей: C и T. SNP возникают в результате точечных мутаций.
 DNA Тaxonomy and Barcoding
DNA Тaxonomy and Barcoding
 Три важнейших задачи Таксономии 1. Опредление и описание новых видов. Названия видов – это основа для любых флористических списков 2. Классификация Выяснение таксономического статуса и номенклатуры 3. Создание алгоритмов (пособий) для определение видов (Определители и Флоры; Ключи для видов, родов и т. д. . . . • Определение видов это достаточно трудоемкий и сложный процесс, который часто требует высокой квалификации. • К этому еще дополняется проблемма перепроверки – без сравнительного материала (т. Н. „Vouchers“), любое название растения, независимо от того, где оно опубликовано, в лучщем случае является предположением. Очень важную роль здесь играют Гербарии.
Три важнейших задачи Таксономии 1. Опредление и описание новых видов. Названия видов – это основа для любых флористических списков 2. Классификация Выяснение таксономического статуса и номенклатуры 3. Создание алгоритмов (пособий) для определение видов (Определители и Флоры; Ключи для видов, родов и т. д. . . . • Определение видов это достаточно трудоемкий и сложный процесс, который часто требует высокой квалификации. • К этому еще дополняется проблемма перепроверки – без сравнительного материала (т. Н. „Vouchers“), любое название растения, независимо от того, где оно опубликовано, в лучщем случае является предположением. Очень важную роль здесь играют Гербарии.
 Barcoding Возможность определения любого таксона с помощью прочтения одного или двух фрагментов ДНК. Для этого необходимо создание Базы данных с сиквенсами этих фрагментов.
Barcoding Возможность определения любого таксона с помощью прочтения одного или двух фрагментов ДНК. Для этого необходимо создание Базы данных с сиквенсами этих фрагментов.
 ДНК штрих-код (Barcodes) First International Conference for the Barcoding of Life Februar 2005
ДНК штрих-код (Barcodes) First International Conference for the Barcoding of Life Februar 2005
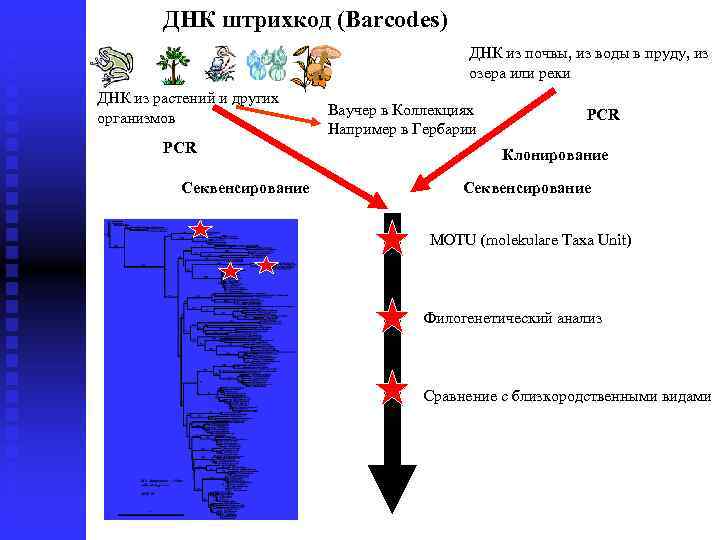 ДНК штрихкод (Barcodes) ДНК из почвы, из воды в пруду, из озера или реки ДНК из растений и других организмов PCR Секвенсирование Ваучер в Коллекциях Например в Гербарии PCR Клонирование Секвенсирование MOTU (molekulare Taxa Unit) Филогенетический анализ Сравнение с близкородственными видами
ДНК штрихкод (Barcodes) ДНК из почвы, из воды в пруду, из озера или реки ДНК из растений и других организмов PCR Секвенсирование Ваучер в Коллекциях Например в Гербарии PCR Клонирование Секвенсирование MOTU (molekulare Taxa Unit) Филогенетический анализ Сравнение с близкородственными видами
 Примеры из практики Ботанического сада Университета Оснабрюк В коллекции Ботатического сада находится целый ряд растений без названия
Примеры из практики Ботанического сада Университета Оснабрюк В коллекции Ботатического сада находится целый ряд растений без названия
 Пример 1 86 -09 -0064 -10 Boraginaceae 1985 из Мексики
Пример 1 86 -09 -0064 -10 Boraginaceae 1985 из Мексики
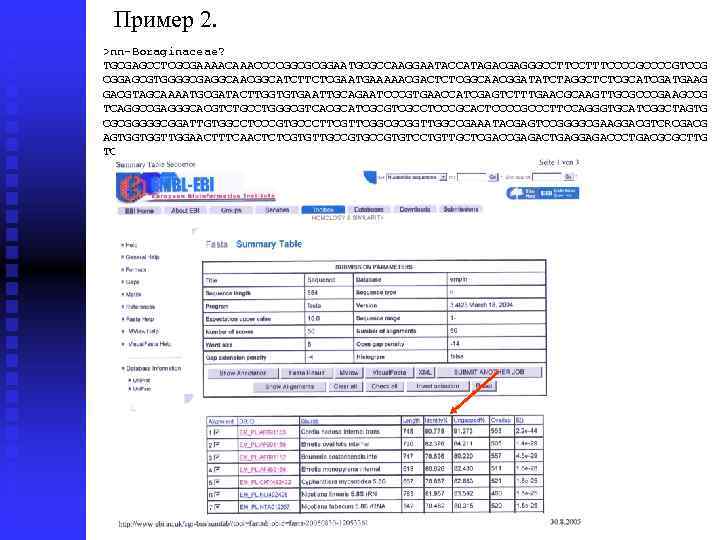 Пример 2. >nn-Boraginaceae? TGCGAGCCTCGCGAAAACCCCGGCGCGGAATGCGCCAAGGAATACCATAGACGAGGGCCTTTCCCCGTCCG CGGAGCGTGGGGCGAGGCAACGGCATCTTCTCGAATGAAAAACGACTCTCGGCAACGGATATCTAGGCTCTCGCATCGATGAAG GACGTAGCAAAATGCGATACTTGGTGTGAATTGCAGAATCCCGTGAACCATCGAGTCTTTGAACGCAAGTTGCGCCCGAAGCCG TCAGGCCGAGGGCACGTCTGCCTGGGCGTCACGCATCGCGTCGCCTCCCGCACTCCCCGCCCTTCCAGGGTGCATCGGCTAGTG CGCGGGGGCGGATTGTGGCCTCCCGTGCCCTTCGGCGCGGTTGGCCGAAATACGAGTCCGGGGCGAAGGACGTCRCGACG AGTGGTGGTTGGAACTTTCAACTCTCGTGTTGCCGTGTCCTGTTGCTCGACCGAGACTGAGGAGACCCTGACGCGCTTG TCTCGTTCCGACGGGAGGAGCCACGCGCTACGACCGCGACCCCAGGTCAG
Пример 2. >nn-Boraginaceae? TGCGAGCCTCGCGAAAACCCCGGCGCGGAATGCGCCAAGGAATACCATAGACGAGGGCCTTTCCCCGTCCG CGGAGCGTGGGGCGAGGCAACGGCATCTTCTCGAATGAAAAACGACTCTCGGCAACGGATATCTAGGCTCTCGCATCGATGAAG GACGTAGCAAAATGCGATACTTGGTGTGAATTGCAGAATCCCGTGAACCATCGAGTCTTTGAACGCAAGTTGCGCCCGAAGCCG TCAGGCCGAGGGCACGTCTGCCTGGGCGTCACGCATCGCGTCGCCTCCCGCACTCCCCGCCCTTCCAGGGTGCATCGGCTAGTG CGCGGGGGCGGATTGTGGCCTCCCGTGCCCTTCGGCGCGGTTGGCCGAAATACGAGTCCGGGGCGAAGGACGTCRCGACG AGTGGTGGTTGGAACTTTCAACTCTCGTGTTGCCGTGTCCTGTTGCTCGACCGAGACTGAGGAGACCCTGACGCGCTTG TCTCGTTCCGACGGGAGGAGCCACGCGCTACGACCGCGACCCCAGGTCAG
 Cordia sonorae Rose Boraginaceae из 86 -09 -0064 -10
Cordia sonorae Rose Boraginaceae из 86 -09 -0064 -10
 Пример 2 Растение под номером 84 -00 -0313 -80 с 1984 года находилось в коллекции Ботатического сада без названия. ITS 1
Пример 2 Растение под номером 84 -00 -0313 -80 с 1984 года находилось в коллекции Ботатического сада без названия. ITS 1
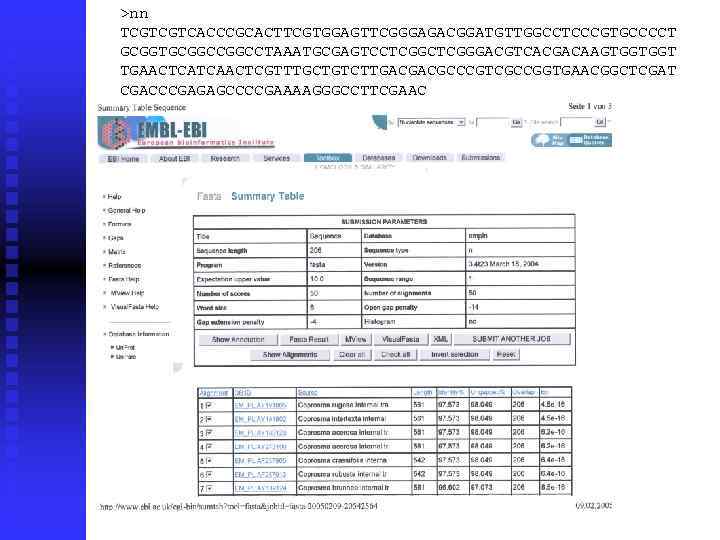 >nn TCGTCGTCACCCGCACTTCGTGGAGTTCGGGAGACGGATGTTGGCCTCCCGTGCCCCT GCGGTGCGGCCTAAATGCGAGTCCTCGGGACGTCACGACAAGTGGTGGT TGAACTCATCAACTCGTTTGCTGTCTTGACGACGCCCGTCGCCGGTGAACGGCTCGAT CGACCCGAGAGCCCCGAAAAGGGCCTTCGAAC
>nn TCGTCGTCACCCGCACTTCGTGGAGTTCGGGAGACGGATGTTGGCCTCCCGTGCCCCT GCGGTGCGGCCTAAATGCGAGTCCTCGGGACGTCACGACAAGTGGTGGT TGAACTCATCAACTCGTTTGCTGTCTTGACGACGCCCGTCGCCGGTGAACGGCTCGAT CGACCCGAGAGCCCCGAAAAGGGCCTTCGAAC
 Coprosma montanum Hillebr. Rubiaceae
Coprosma montanum Hillebr. Rubiaceae
 ДНК Таксономия в ближайшем (и не совсем ) будующем.
ДНК Таксономия в ближайшем (и не совсем ) будующем.
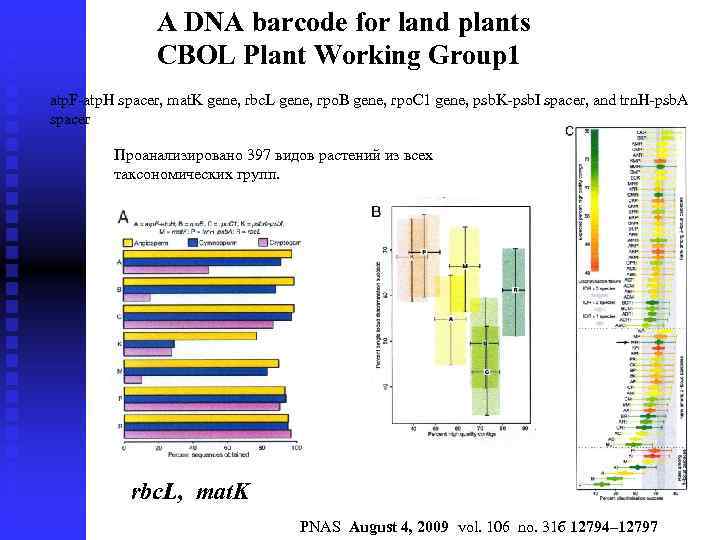 A DNA barcode for land plants CBOL Plant Working Group 1 atp. F-atp. H spacer, mat. K gene, rbc. L gene, rpo. B gene, rpo. C 1 gene, psb. K-psb. I spacer, and trn. H-psb. A spacer Проанализировано 397 видов растений из всех таксономических групп. rbc. L, mat. K PNAS August 4, 2009 vol. 106 no. 31 б 12794– 12797
A DNA barcode for land plants CBOL Plant Working Group 1 atp. F-atp. H spacer, mat. K gene, rbc. L gene, rpo. B gene, rpo. C 1 gene, psb. K-psb. I spacer, and trn. H-psb. A spacer Проанализировано 397 видов растений из всех таксономических групп. rbc. L, mat. K PNAS August 4, 2009 vol. 106 no. 31 б 12794– 12797
 Методы филогенетического анализа: процедура выравнивания, филогенетические деревья и методы их построения
Методы филогенетического анализа: процедура выравнивания, филогенетические деревья и методы их построения
 Задача молекулярной филогенетики состоит в преобразовании информации содержащейся в семантидах (ДНК ) в эволюционное дерево. . Для преобразовании информации содержащейся в ДНК, необходимо подготовить полученные сиквенсы (или данные RAPD, AFLP и др. ) для анализа - Матрица или Alingnment
Задача молекулярной филогенетики состоит в преобразовании информации содержащейся в семантидах (ДНК ) в эволюционное дерево. . Для преобразовании информации содержащейся в ДНК, необходимо подготовить полученные сиквенсы (или данные RAPD, AFLP и др. ) для анализа - Матрица или Alingnment
 Alignment Процедура выравнивания Alignment - это гипотеза о Гомологии между нуклеотидами - Гомология: Сходство это результат Наследства от одного общего предка - установление и сравнение гомологичных признаков это центральный принцип филогенетического анализа
Alignment Процедура выравнивания Alignment - это гипотеза о Гомологии между нуклеотидами - Гомология: Сходство это результат Наследства от одного общего предка - установление и сравнение гомологичных признаков это центральный принцип филогенетического анализа
 Процесс выравнивания (alignment) подразумевает выстраивание последовательностей наиболее близких к исследуемому объекту видов друг под другом с таким расчетом, чтобы они совпадали как можно более полно, тогда одни консервативные участки будут располагаться под другими.
Процесс выравнивания (alignment) подразумевает выстраивание последовательностей наиболее близких к исследуемому объекту видов друг под другом с таким расчетом, чтобы они совпадали как можно более полно, тогда одни консервативные участки будут располагаться под другими.
 ДНК Алфавит Все ДНК молекулы состоят из нуклеотидов, которые содержат сахар, фосфатную группу и одну из четырех нуклеидных кислот: Adenin, Cytosin, Guanin и Thymin. Из их начальных букв и состоит алфавит ДНК (A, C, G; T) Однобуквенные сокращения для ДНК алфавита A C T G W S R Y K M Adenine Cytosine Thymine Guanine Weack bonds (A, T) Strong bonds (C, G) Purines (A, G) Pyramidines (C, T) Keto (T, G) Amino (A, C) B D H V N C, G or T A, C or G A, C, T or G
ДНК Алфавит Все ДНК молекулы состоят из нуклеотидов, которые содержат сахар, фосфатную группу и одну из четырех нуклеидных кислот: Adenin, Cytosin, Guanin и Thymin. Из их начальных букв и состоит алфавит ДНК (A, C, G; T) Однобуквенные сокращения для ДНК алфавита A C T G W S R Y K M Adenine Cytosine Thymine Guanine Weack bonds (A, T) Strong bonds (C, G) Purines (A, G) Pyramidines (C, T) Keto (T, G) Amino (A, C) B D H V N C, G or T A, C or G A, C, T or G
 Мутации 1) Характеризуемые по длине сиквенса a) Точечная мутация (только один нуклеотид) b) длинная мутация (затрагивает 2 или многих соседних нуклеотидов 2) Характеризуемые по способу замены нуклеотидов a) Substitution (замена одного нуклеотида на другой) b) Inversion (переворот 2 или нескольких нуклеотидов одной части ДНК на 180° ) c) Insertion (вставка одного или нескольких нуклеотидов) d) Deletion (потеря одного или нескольких нуклеотидов) Insertion AATTGCATG AAT-GCATG gap Deletion совпадение (match) несовпадение (mismatch) AATGCATGAAGATCGG AATGCCTCGATT In. Dels
Мутации 1) Характеризуемые по длине сиквенса a) Точечная мутация (только один нуклеотид) b) длинная мутация (затрагивает 2 или многих соседних нуклеотидов 2) Характеризуемые по способу замены нуклеотидов a) Substitution (замена одного нуклеотида на другой) b) Inversion (переворот 2 или нескольких нуклеотидов одной части ДНК на 180° ) c) Insertion (вставка одного или нескольких нуклеотидов) d) Deletion (потеря одного или нескольких нуклеотидов) Insertion AATTGCATG AAT-GCATG gap Deletion совпадение (match) несовпадение (mismatch) AATGCATGAAGATCGG AATGCCTCGATT In. Dels
 Выравнивание может быть простым или сложным Простое Сложное изза вставок или делеций (indels)
Выравнивание может быть простым или сложным Простое Сложное изза вставок или делеций (indels)
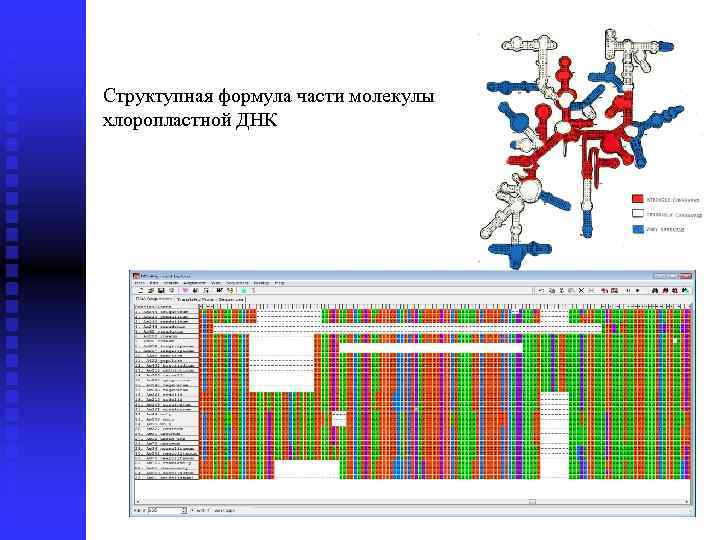 Структупная формула части молекулы хлоропластной ДНК
Структупная формула части молекулы хлоропластной ДНК
 Алгоритмы выравнивания Искоммый алгоритм должен выбрать выравнивание с наименьшей дистанцией (наибольшим сходством) из всех возможных вариантов. Учитывая, что два сравнительно коротких сиквенса в 300 бп дает 1088 различных вариантов, то анализ всех этих вариантов является не самым экономным путем.
Алгоритмы выравнивания Искоммый алгоритм должен выбрать выравнивание с наименьшей дистанцией (наибольшим сходством) из всех возможных вариантов. Учитывая, что два сравнительно коротких сиквенса в 300 бп дает 1088 различных вариантов, то анализ всех этих вариантов является не самым экономным путем.
 Методы выравнивания сиквенсов 3 главных метода: • Ручной (Manual) • Компьютерный • Комбинированный
Методы выравнивания сиквенсов 3 главных метода: • Ручной (Manual) • Компьютерный • Комбинированный
 Ручное выравнивание Почему? • Может применяться: – Выравнивание простое. – Имеется дополнительная информация о структуре ДНК – Компьютерное выравнивание имеет локальные проблеммы – Компьютерное выравнивание можно проверить и откоректировать
Ручное выравнивание Почему? • Может применяться: – Выравнивание простое. – Имеется дополнительная информация о структуре ДНК – Компьютерное выравнивание имеет локальные проблеммы – Компьютерное выравнивание можно проверить и откоректировать
 Clustal. W ПРИНЦИП 1. Каждые две ДНК последовательности выравниваются при помощи Needleman Wunsch коэфициента сходства 2. Отсюда получают генетические дистанции. 3. На основе генетических дистанций расчитывается NJ дерево 4. На основе этого модельного дерева составляется множественное выравнивание (multiples Alignment) ДНК последовательностей. Последовательно составляются вначале из соседних последовательностей в NJ дереве блоки последовательностей и затем из блоков конструируется полное выравнивание всех последовательностей.
Clustal. W ПРИНЦИП 1. Каждые две ДНК последовательности выравниваются при помощи Needleman Wunsch коэфициента сходства 2. Отсюда получают генетические дистанции. 3. На основе генетических дистанций расчитывается NJ дерево 4. На основе этого модельного дерева составляется множественное выравнивание (multiples Alignment) ДНК последовательностей. Последовательно составляются вначале из соседних последовательностей в NJ дереве блоки последовательностей и затем из блоков конструируется полное выравнивание всех последовательностей.
 Филогенетические Деревья – способ графического выражения эволюционных взаимоотношений
Филогенетические Деревья – способ графического выражения эволюционных взаимоотношений
 Элементы филогенетического дерева. Филогенетическое дерево представляет собой математическую структуру, используемую для моделирования эволюционой истории группы последовательностей или организмов. Филогения или эволюционное дерево графически отражают состояние исторических связей Филогенетическое дерево - это практически всегда Гипотеза
Элементы филогенетического дерева. Филогенетическое дерево представляет собой математическую структуру, используемую для моделирования эволюционой истории группы последовательностей или организмов. Филогения или эволюционное дерево графически отражают состояние исторических связей Филогенетическое дерево - это практически всегда Гипотеза
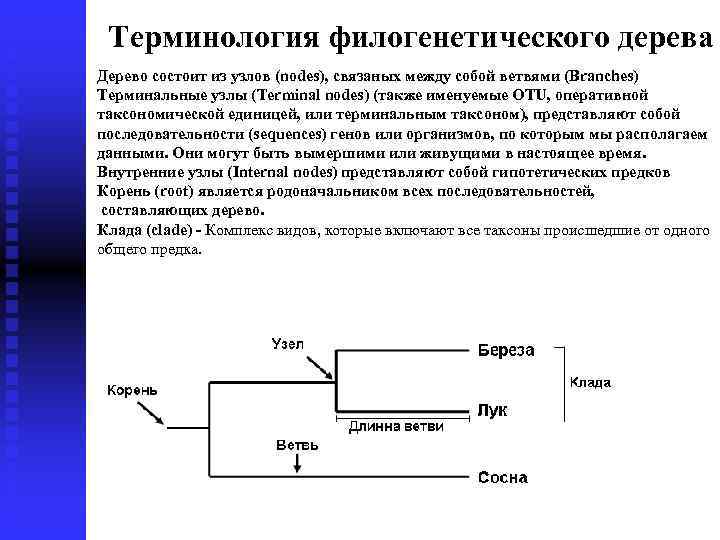 Терминология филогенетического дерева Дерево состоит из узлов (nodes), связаных между собой ветвями (Branches) Терминальные узлы (Terminal nodes) (также именуемые OTU, оперативной таксономической единицей, или терминальным таксоном), представляют собой последовательности (sequences) генов или организмов, по которым мы располагаем данными. Они могут быть вымершими или живущими в настоящее время. Внутренние узлы (Internal nodes) представляют собой гипотетических предков Корень (root) является родоначальником всех последовательностей, составляющих дерево. Клада (clade) - Комплекс видов, которые включают все таксоны происшедшие от одного общего предка.
Терминология филогенетического дерева Дерево состоит из узлов (nodes), связаных между собой ветвями (Branches) Терминальные узлы (Terminal nodes) (также именуемые OTU, оперативной таксономической единицей, или терминальным таксоном), представляют собой последовательности (sequences) генов или организмов, по которым мы располагаем данными. Они могут быть вымершими или живущими в настоящее время. Внутренние узлы (Internal nodes) представляют собой гипотетических предков Корень (root) является родоначальником всех последовательностей, составляющих дерево. Клада (clade) - Комплекс видов, которые включают все таксоны происшедшие от одного общего предка.
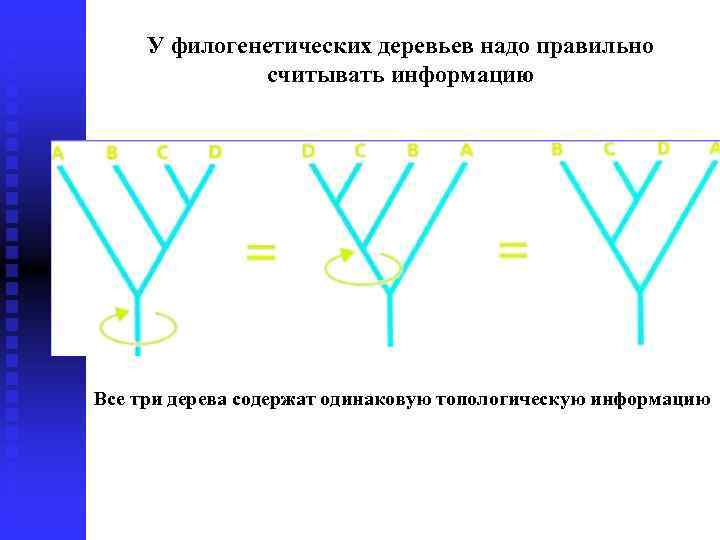 У филогенетических деревьев надо правильно считывать информацию Все три дерева содержат одинаковую топологическую информацию
У филогенетических деревьев надо правильно считывать информацию Все три дерева содержат одинаковую топологическую информацию
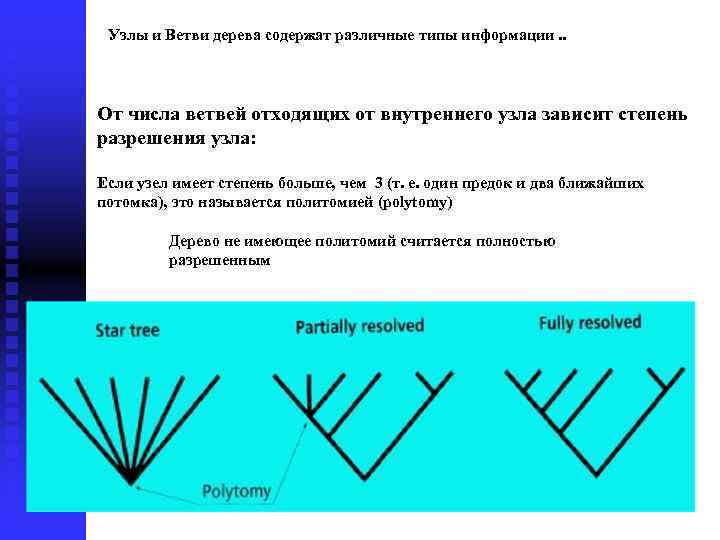 Узлы и Ветви дерева содержат различные типы информации. . От числа ветвей отходящих от внутреннего узла зависит степень разрешения узла: Если узел имеет степень больше, чем 3 (т. е. один предок и два ближайших потомка), это называется политомией (polytomy) Дерево не имеющее политомий считается полностью разрешенным
Узлы и Ветви дерева содержат различные типы информации. . От числа ветвей отходящих от внутреннего узла зависит степень разрешения узла: Если узел имеет степень больше, чем 3 (т. е. один предок и два ближайших потомка), это называется политомией (polytomy) Дерево не имеющее политомий считается полностью разрешенным
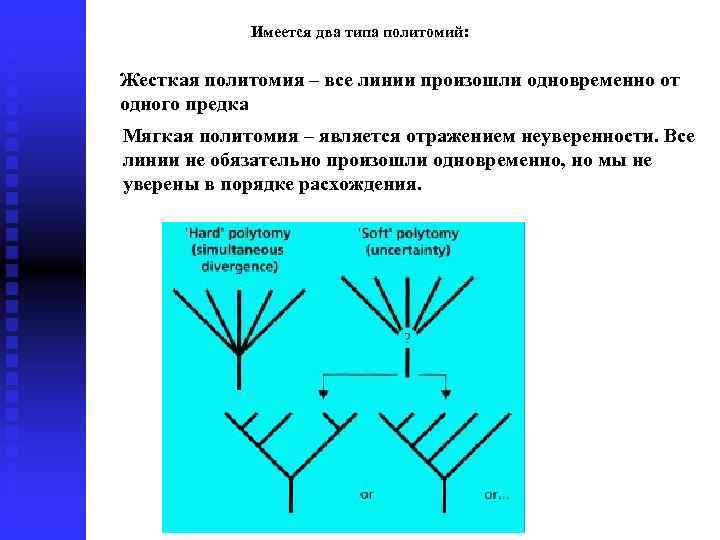 Имеется два типа политомий: Жесткая политомия – все линии произошли одновременно от одного предка Мягкая политомия – является отражением неуверенности. Все линии не обязательно произошли одновременно, но мы не уверены в порядке расхождения.
Имеется два типа политомий: Жесткая политомия – все линии произошли одновременно от одного предка Мягкая политомия – является отражением неуверенности. Все линии не обязательно произошли одновременно, но мы не уверены в порядке расхождения.
 Понятия моно- поли- и парафилии - ключевые термины в таксономи и филогенетике. Монофилия (др. греч. μόνος — один и φυλή — семейный клан) — происхождение таксона от одного общего предка Полифилия (др. греч. πολύς — многочисленный и φυλή — семейный клан) — происхождение таксона от разных предков Парафилия - Парафилетическая группа включает ближайшего общего предка, но в отличие от монофилетической, не всех потомков Парафилетическую группу невозможно охарактеризовать уникальными cинапоморфиями. Все общие свойства, которые можно указать для её представителей относятся к симплезиоморфиям (унаследованы от более отдаленных предков, чем ближайший общий предок представителей группы) или гомоплазиям (возникли у разных представителей исследуемой группы независимо).
Понятия моно- поли- и парафилии - ключевые термины в таксономи и филогенетике. Монофилия (др. греч. μόνος — один и φυλή — семейный клан) — происхождение таксона от одного общего предка Полифилия (др. греч. πολύς — многочисленный и φυλή — семейный клан) — происхождение таксона от разных предков Парафилия - Парафилетическая группа включает ближайшего общего предка, но в отличие от монофилетической, не всех потомков Парафилетическую группу невозможно охарактеризовать уникальными cинапоморфиями. Все общие свойства, которые можно указать для её представителей относятся к симплезиоморфиям (унаследованы от более отдаленных предков, чем ближайший общий предок представителей группы) или гомоплазиям (возникли у разных представителей исследуемой группы независимо).
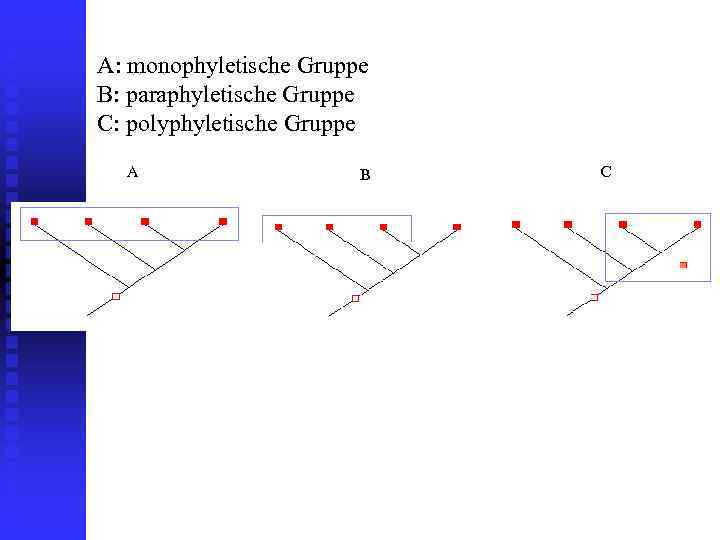 A: monophyletische Gruppe B: paraphyletische Gruppe C: polyphyletische Gruppe A B C
A: monophyletische Gruppe B: paraphyletische Gruppe C: polyphyletische Gruppe A B C
 Три возможных типа гомологии признаков (Гомоплазии - Homoplasy). (независимая эволюция одинаковых изменений) Паралельная эволюция Конвергентная эволюция Повторная потеря независимая эволюция Возврат к одинаковых изменений предковым при наличии общего предка при наличии разных предков признпкам
Три возможных типа гомологии признаков (Гомоплазии - Homoplasy). (независимая эволюция одинаковых изменений) Паралельная эволюция Конвергентная эволюция Повторная потеря независимая эволюция Возврат к одинаковых изменений предковым при наличии общего предка при наличии разных предков признпкам
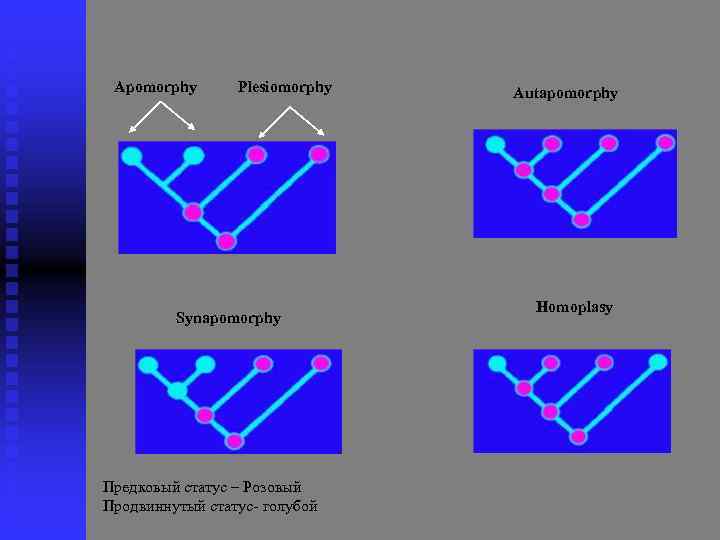 Apomorphy Plesiomorphy Synapomorphy Предковый статус – Розовый Продвиннутый статус- голубой Autapomorphy Homoplasy
Apomorphy Plesiomorphy Synapomorphy Предковый статус – Розовый Продвиннутый статус- голубой Autapomorphy Homoplasy
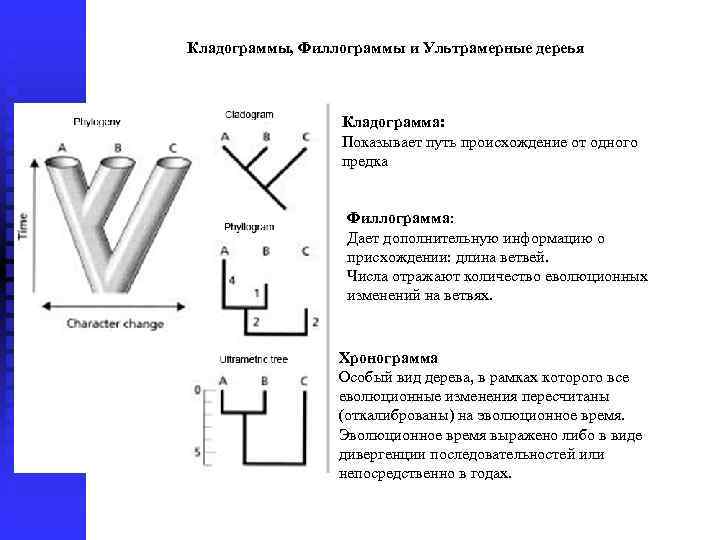 Кладограммы, Филлограммы и Ультрамерные дереья Кладограмма: Показывает путь происхождение от одного предка Филлограмма: Дает дополнительную информацию о присхождении: длина ветвей. Числа отражают количество еволюционных изменений на ветвях. Хронограмма Особый вид дерева, в рамках которого все еволюционные изменения пересчитаны (откалиброваны) на эволюционное время. Эволюционное время выражено либо в виде дивергенции последовательностей или непосредственно в годах.
Кладограммы, Филлограммы и Ультрамерные дереья Кладограмма: Показывает путь происхождение от одного предка Филлограмма: Дает дополнительную информацию о присхождении: длина ветвей. Числа отражают количество еволюционных изменений на ветвях. Хронограмма Особый вид дерева, в рамках которого все еволюционные изменения пересчитаны (откалиброваны) на эволюционное время. Эволюционное время выражено либо в виде дивергенции последовательностей или непосредственно в годах.
 Что отражают горизонтальные и вертикальные оси у различных типов деревьев? Только последовательность дивергенции Число эволюционных изменений на ветвях хорошо коррелирует с временем
Что отражают горизонтальные и вертикальные оси у различных типов деревьев? Только последовательность дивергенции Число эволюционных изменений на ветвях хорошо коррелирует с временем
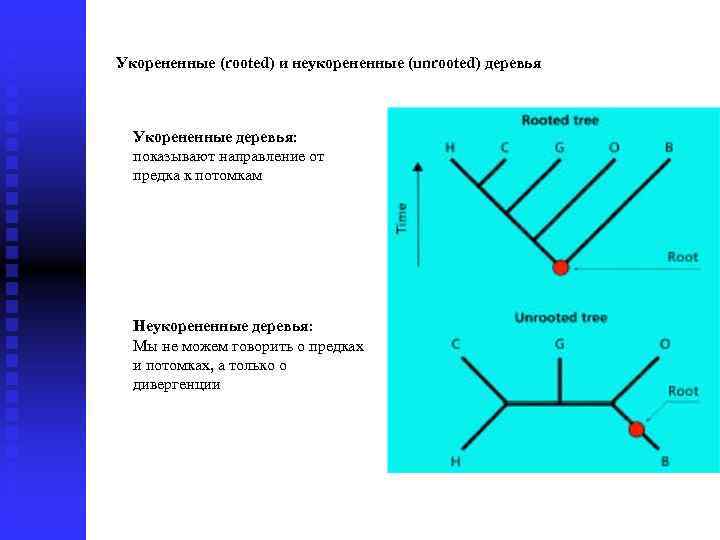 Укорененные (rooted) и неукорененные (unrooted) деревья Укорененные деревья: показывают направление от предка к потомкам Неукорененные деревья: Мы не можем говорить о предках и потомках, а только о дивергенции
Укорененные (rooted) и неукорененные (unrooted) деревья Укорененные деревья: показывают направление от предка к потомкам Неукорененные деревья: Мы не можем говорить о предках и потомках, а только о дивергенции
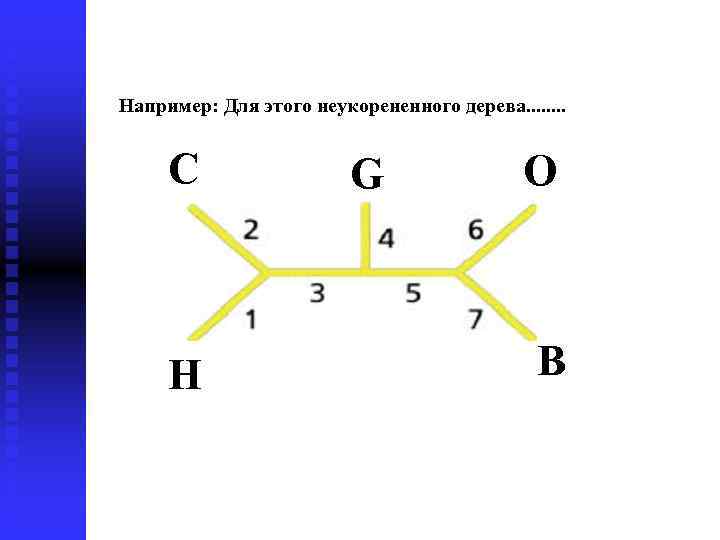 Например: Для этого неукорененного дерева. . . . С H G O B
Например: Для этого неукорененного дерева. . . . С H G O B
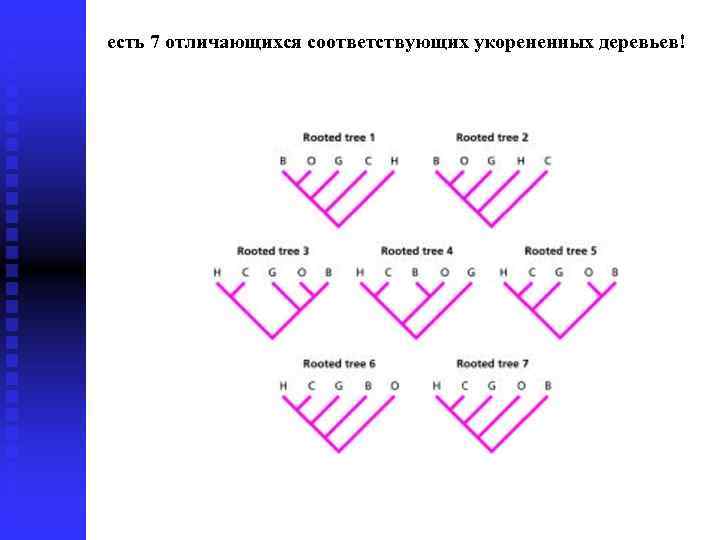 есть 7 отличающихся соответствующих укорененных деревьев!
есть 7 отличающихся соответствующих укорененных деревьев!
 Очень важно различать укорененные и неукорененные деревья Поскольку многие филогенетические методы реконструкции генерируют неукорененные деревья и не могут самостоятельно выявить различие между этими семью укорененных деревьев. Количество возможных неукорененных деревьев Un для n сиквенсов Un = (2 n-5) (2 n-7). . . (etc) Количество возможных укорененных деревьев Rn для n сиквенсов Rn = (2 n-3) (2 n-5). . . (etc)
Очень важно различать укорененные и неукорененные деревья Поскольку многие филогенетические методы реконструкции генерируют неукорененные деревья и не могут самостоятельно выявить различие между этими семью укорененных деревьев. Количество возможных неукорененных деревьев Un для n сиквенсов Un = (2 n-5) (2 n-7). . . (etc) Количество возможных укорененных деревьев Rn для n сиквенсов Rn = (2 n-3) (2 n-5). . . (etc)
 Количество возможных деревьев возрастает в геометрической прогрессии при возрастании количества сиквенсов Количество Сиквенсов 2 3 4 5 6 7 8 9 10 Количество неукорененных деревьев 1 1 3 15 105 945 10395 135135 2027025 Количество укорененных деревьев 1 3 15 105 945 10395 135135 2027025 344594425
Количество возможных деревьев возрастает в геометрической прогрессии при возрастании количества сиквенсов Количество Сиквенсов 2 3 4 5 6 7 8 9 10 Количество неукорененных деревьев 1 1 3 15 105 945 10395 135135 2027025 Количество укорененных деревьев 1 3 15 105 945 10395 135135 2027025 344594425


