ЗВЕРЕВ В.В. анапа.ppt
- Количество слайдов: 43


ЗНАЧЕНИЕ ФУНДАМЕНТЕЛЬНЫХ ИССЛЕДОВАНИЙ В ОБЛАСТИ МЕДИЦИНСКОЙ БИОТЕХНОЛОГИИ ДЛЯ РЕАЛИЗАЦИИ НАЦИОНАЛЬНОГО ПРОЕКТА «ЗДОРОВЬЕ» ЗВЕРЕВ В. В.

ОСНОВНЫЕ НАПРАВЛЕНИЯ æ Повышение качества медицинского обслуживания населения, разработка стандартов и критериев оценки качества медицинской помощи; æ Борьба с инфекционными заболеваниями, обеспечение биологической безопасности страны; æ Охрана материнства и детства; æ Обеспечение лечебных учреждений современной медицинской техникой, диагностическими и лекарственными препаратами.

РОЛЬ НАУКИ æ Участие в разработке и научном сопровождении программ здравоохранения; æ Независимая научная экспертиза программ и проектов; æ Подготовка медицинских кадров для выполнения программы; æ Участие в экспертизе при закупке медицинского оборудования и препаратов для диагностики, лечения и профилактики заболеваний; æ Создание новейших технологий оказания медицинской помощи.

МЕДИЦИНСКИЕ ТЕХНОЛОГИИ æ Создание новых технологий производства вакцин и других иммунологических препаратов для диагностики, лечения и специфической профилактики инфекционных заболеваний; æ Создание новых молекулярно-генетических методов диагностики и лечения врожденных патологий и наследственных заболеваний; æ Разработка новых методов диагностики и лечения онкологических заболеваний. æ Новые методологические подходы к лечению, диагностике и профилактике «соматических» заболеваний.

Неизвестные микроорганизмы, с которыми столкнулось человечество в 1972 – 2006 г. г.
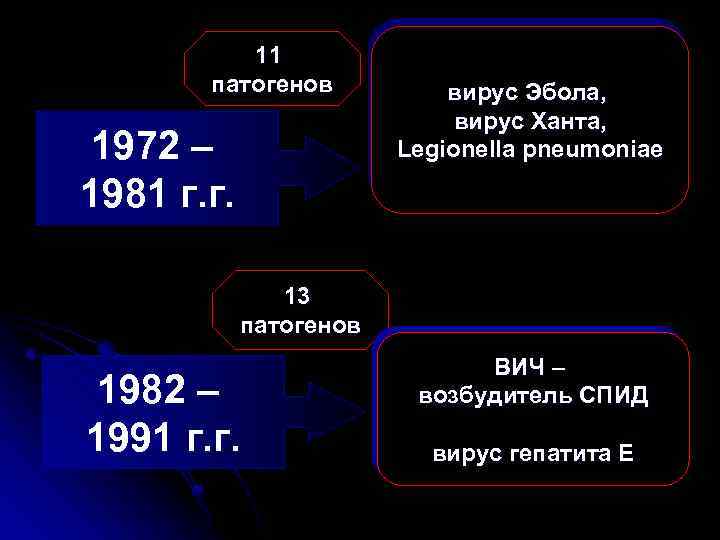
11 патогенов 1972 – 1981 г. г. вирус Эбола, вирус Ханта, Legionella pneumoniae 13 патогенов 1982 – 1991 г. г. ВИЧ – возбудитель СПИД вирус гепатита Е
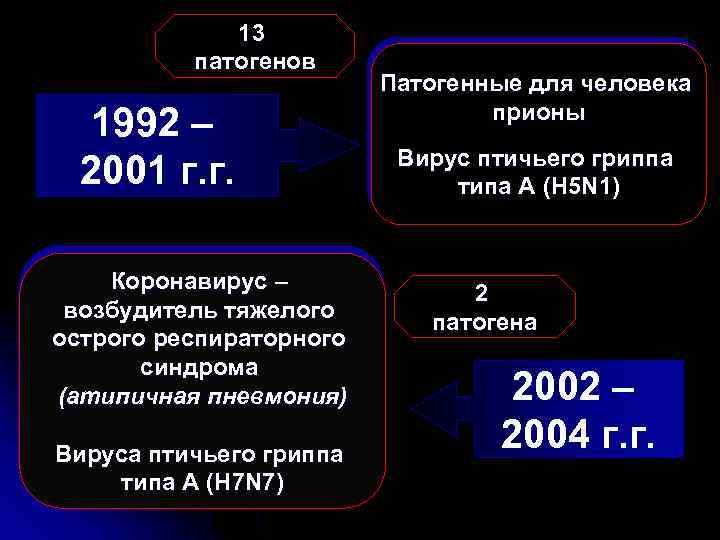
13 патогенов 1992 – 2001 г. г. Коронавирус – возбудитель тяжелого острого респираторного синдрома (атипичная пневмония) Вируса птичьего гриппа типа А (H 7 N 7) Патогенные для человека прионы Вирус птичьего гриппа типа А (H 5 N 1) 2 патогена 2002 – 2004 г. г.

Всего за период 1972 - 2006 г. г. (32 года) выделено и идентифицировано 39 новых патогенов

иммунологические методы для борьбы с эпидемиями методы патоген известный неизвестный вакцинация да нет иммунотерапия активация врожденного иммунитета да в конце эпидемии обсуждается разрабатывается

VACCINAL MONSTER LONDON,

1. Сохранение и расширение прививок в рамках национальных календарей. 2. Создание вакцин для предупреждения новых и возвращающихся инфекций, а также для защиты от биотеррористических актов. 3. Разработки препаратов для иммунопрофилактики и иммунотерапии онкологических заболеваний. 4. Создание средств для иммунологической защиты и лечения наркозависимости и курения. 5. Вакцины, предупреждающие и нормализующие болезни иммунной системы (аллергия, аутоиммунные процессы). 6. Терапевтические вакцины для лечения хронических болезней. 7. Применение вакцин для профилактики соматических заболеваний.

ТЕХНОЛОГИИ РЕКОМБИНАНТНОЙ ДНК СУБЪЕДИНИЧНЫЕ ВАКЦИНЫ: ВАКЦИНА ПРОТИВ ГЕПАТИТА В ВАКЦИНА ПРОТИВ B. Pertussis

За последние 10 лет в вакцинологии сформировалось новое направление, основанное на другом принципе, когда в организм вводится не белок, а нуклеиновая кислота (ДНК или РНК). Это направление называют «генетической иммунизацией» , «вакцинацией нуклеиновыми кислотами» , «ДНКвакцинацией» и связывают с этим направлением революционные изменения в вакцинологии ближайшего будущего.

Вакцины Инактивиров. ДНК, живые. Антиген/мишень внеклеточное АРС процессинг интрацел. везикулы протеосомы Представление МНС II MHC I Регуляция Th 2 -тип Th 1 -тип Специфические цитокины IL- 4, 5, 10, 13 IL-2, IFN-γ, IFN-β Доминантные Ig. G 1 Ig. G 2 a Эффекторные механизмы нейтрализация, лизис цитотоксические Ткомплемента, АТ-зави клетки (CTL) сим. цитотоксичность цитозоль/клетка

Преимущества 1. 2. 3. Простота и доступность. Относительная дешевизна Возможность унифицировать методические подходы. 4. Нет работы с патогенами. 5. Отпадает сложная и дорогая процедура очистки антигенов. 6. Не требуется специальных методов доставки. 7. Стабильность при хранении.

НЕДОСТАТКИ 1. Эффективность на людях ниже чем на мышиных моделях. 2. Потенциальная опасность введенной ДНК (встраивание в геном, бесконтрольная экспрессия антигенов. 3. Индукция аутоиммунных заболеваний.

БИОИНФОРМАТИКА ГЕНОМИКА ПРОТЕОМИКА «REVERSE» ВАКЦИНОЛОГИЯ
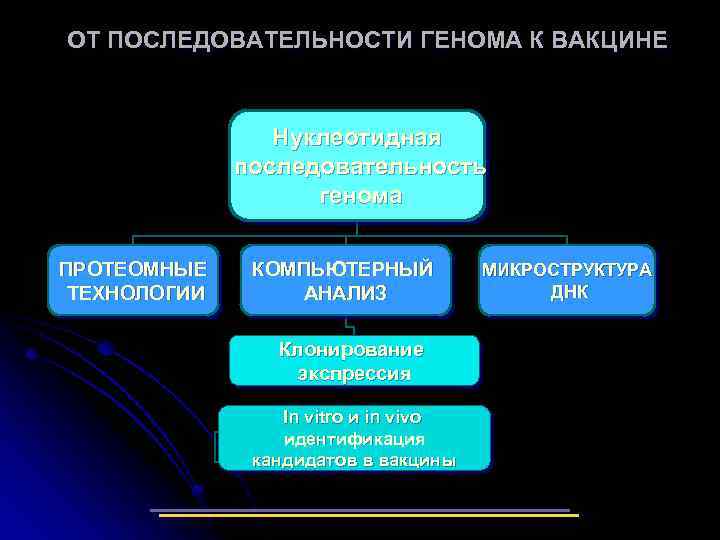
ОТ ПОСЛЕДОВАТЕЛЬНОСТИ ГЕНОМА К ВАКЦИНЕ Нуклеотидная последовательность генома ПРОТЕОМНЫЕ ТЕХНОЛОГИИ КОМПЬЮТЕРНЫЙ АНАЛИЗ Клонирование экспрессия In vitro и in vivo идентификация кандидатов в вакцины МИКРОСТРУКТУРА ДНК
![1. ИДЕНТИФИКАЦИЯ ЭКСПРЕССИРУЮЩИХСЯ ГЕНОВ [ 50 -60% ГЕНОМА (1000 ГЕНОВ)] 2. УДАЛЕНИЕ НЕ МЕМБРАННЫХ 1. ИДЕНТИФИКАЦИЯ ЭКСПРЕССИРУЮЩИХСЯ ГЕНОВ [ 50 -60% ГЕНОМА (1000 ГЕНОВ)] 2. УДАЛЕНИЕ НЕ МЕМБРАННЫХ](https://present5.com/presentation/30710124_161392377/image-20.jpg)
1. ИДЕНТИФИКАЦИЯ ЭКСПРЕССИРУЮЩИХСЯ ГЕНОВ [ 50 -60% ГЕНОМА (1000 ГЕНОВ)] 2. УДАЛЕНИЕ НЕ МЕМБРАННЫХ БЕЛКОВ (КОМП. АНАЛИЗ) [20 -30% ГЕНОМА (400 ГЕНОВ)] 3. ДОБАВЛЕНИЕ МЕМБРАННЫХ БЕЛКОВ (ПРОТЕОМИКА) [25 -35% ГЕНОМА (500 ГЕНОВ)] 4. ДОБАВЛЕНИЕ ГЕНОВ ПО IN VIVO ЭКСПЕРИМЕНТАМ (30 -35% ГЕНОМА)

ВАКЦИНА ПРОТИВ МЕНИНГОКОККОВ ГРУППЫ В (Men. B) Геномный анализ – 600 поверхностных антигенов 350 - экспрессия в E. coli, очистка и проверка на моделях на сполобность индуцировать антитела. Только несколько из них обладали протективным эффектом и вошли в состав вакцины.

Streptococcus agalactiae (2002) Staphilococcus aureus (2002) S. Pneumoniae (2001) Porphyromonas gingivalis (2001) Chlamidia pneumoniae (2002) Plasmodium falciparum (2000)

МУКОЗАЛЬНЫЕ ВАКЦИНЫ СЛИЗИСТЫЕ ПОВЕРХНОСТИ – 400 КВ. М СОДЕРЖАТ ЛИМФОИДНЫЕ ЭЛЕМЕНТЫ (тлимфоциты, В-клетки, плазматические клетки др. участвующие в иммунном ответе). СПЕЦИАЛЬНЫЕ АДЪЮВАНТЫ (термолабильный токсин E. coli, холерный токсин)

Разрабатывается концепция экстренной защиты от патогенов (часы) основана на предположении, что стимуляция созревания дендритных клеток с помощью носителей PAMPs (иммуномодуляторов бактериального происхождения) приведет к активации эффекторных механизмов врожденного иммунитета (24 часа) и формированию протективного иммунитета против конкретного патогена (7 -14 дней)
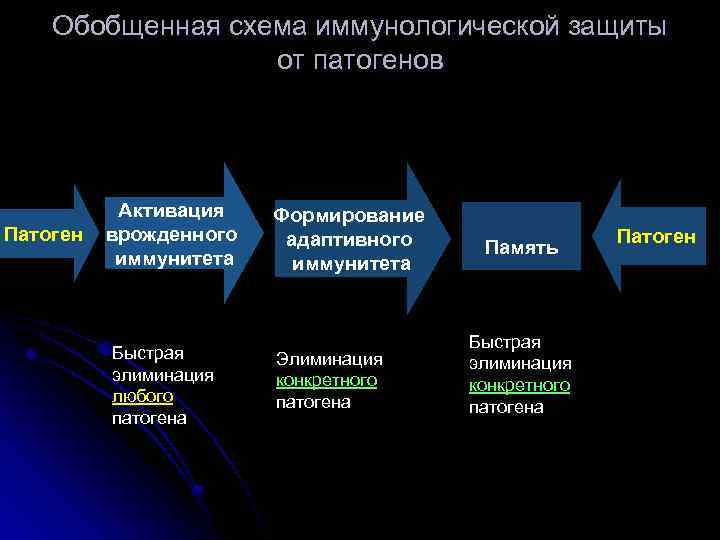
Обобщенная схема иммунологической защиты от патогенов Патоген Активация врожденного иммунитета Быстрая элиминация любого патогена Формирование адаптивного иммунитета Элиминация конкретного патогена Память Быстрая элиминация конкретного патогена Патоген

Рецепторы врожденного иммунитета, распознающие патоген ассоциированные структуры микроорганизмов Рецепторы Toll-подобные NOD Маннозные Мусорщики Активация NK Экспрессированы На мембранах МФ, ДК, моноцитов, тучных клеток, нейтрофилов и т. д. В цитоплазме На мембранах МФ, ДК, соматических клеток и. т. д На мембранах, МФ, ДК и т. д. На мембранах NK, МФ
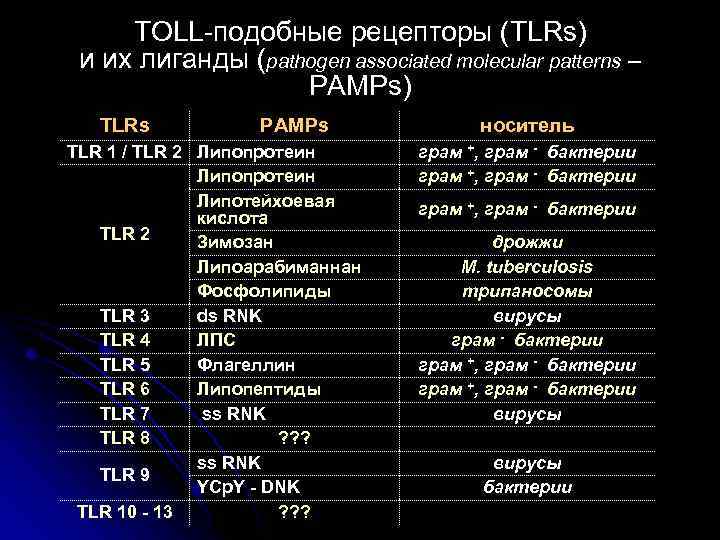
ТОLL-подобные рецепторы (TLRs) и их лиганды (pathogen associated molecular patterns – PAMPs) TLRs PAMPs TLR 1 / TLR 2 Липопротеин Липотейхоевая кислота TLR 2 Зимозан Липоарабиманнан Фосфолипиды TLR 3 ds RNK TLR 4 ЛПС TLR 5 Флагеллин TLR 6 Липопептиды TLR 7 ss RNK TLR 8 ? ? ? ss RNK TLR 9 YCp. Y - DNK TLR 10 - 13 ? ? ? носитель грам +, грам - бактерии дрожжи M. tuberculosis трипаносомы вирусы грам - бактерии грам +, грам - бактерии вирусы бактерии

Дендритные клетки (ДК) – ключевой элемент врожденного иммунитета Распознают патоген ассоциированные молекулярные структуры (ПАМС) микроорганизмов 2. После распознавания ПАМС начинается экспрессия - костимулирующих молекул (CD 40, CD 86) - молекул антигенного представления (MHCI, MHCII) секреция цитокинов 3. Передают сигнал активации наивным Т-лимфоцитам (формирование приобретенного иммунитета 4. Определяют развитие иммунного ответа по Th 1 и Th 2 типу. 1.

Иммунологическая защита от инфекций, возбудителями которых являются неизвестные атогены или патогены, против которых не созданы вакц ОРЗ > 100 Риновирусы Аденовирусы 32 Реовирусы 3 комбинации Коронавирусы 3 бактерий Парагрипп 4 и РС-вирусов H. Influenza Mycoplasma pneumoniae Staphylococcus sp Streptococcus sp
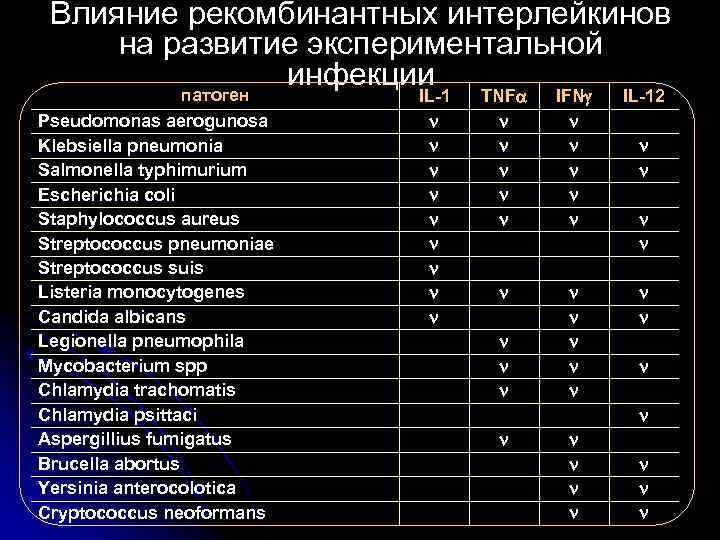
Влияние рекомбинантных интерлейкинов на развитие экспериментальной инфекции патоген Pseudomonas aerogunosa Klebsiella pneumonia Salmonella typhimurium Escherichia coli Staphylococcus aureus Streptococcus pneumoniae Streptococcus suis Listeria monocytogenes Candida albicans Legionella pneumophila Mycobacterium spp Chlamydia trachomatis Chlamydia psittaci Aspergillius fumigatus Brucella abortus Yersinia anterocolotica Cryptococcus neoformans IL-1 TNF IFN IL-12
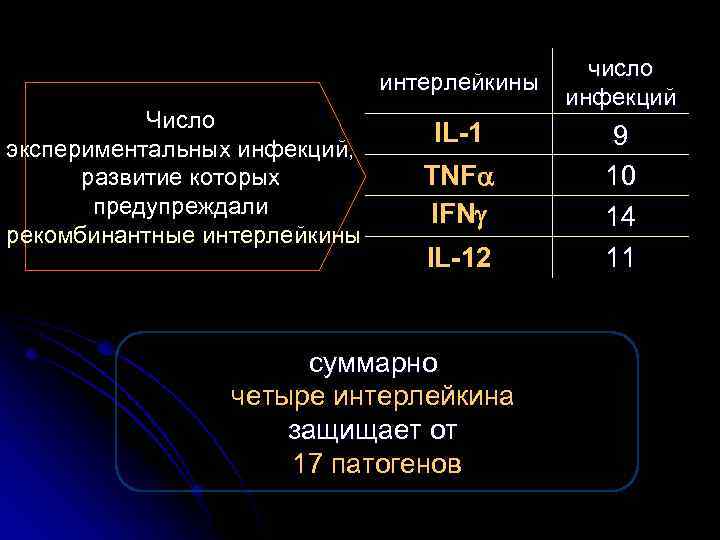
интерлейкины Число экспериментальных инфекций, развитие которых предупреждали рекомбинантные интерлейкины IL-1 TNF IFN IL-12 суммарно четыре интерлейкина защищает от 17 патогенов число инфекций 9 10 14 11

МЕДИЦИНСКИЕ ТЕХНОЛОГИИ æ Создание новых технологий производства вакцин и других иммунологических препаратов для диагностики, лечения и специфической профилактики инфекционных заболеваний; æ Создание новых молекулярно-генетических методов диагностики и лечения врожденных патологий и наследственных заболеваний; æ Разработка новых методов диагностики и лечения онкологических заболеваний. æ Новые методологические подходы к лечению, диагностике и профилактике «соматических» заболеваний.

Новообразования, ассоциированные с микроорганизмами Локализация Патоген Желудок аденокарцином Helicobacter pylori а, лимфома и т. д. Половые органы Вирус папилломы человека (типы 16, 18, 31, 45) Печень Вирус гепатита В гепатокарцинома *) Опухолей, ассоциированных с патогенами Вирус гепатита С **) В развитых странах ***) В развивающихся странах *) Доля (%) 55 65 **) 87 ***) 73 27

Подходы к вакцинопрофилактике и вакцинотерапии рака Введение в организм (опухоль) ДНК, кодирующих раковые антигены. 1. Активация антиген-представляющих клеток. 2. Введение в раковые клетки генов цитокинов и иммуномодуляторов. 3. Комбинированные подходы.

ТРУДНОСТИ ВАКЦИНОТЕРАПИИ РАКА 1. Опухолевые клетки ускользают от узнавания ЦТЛ 2. Неэффективность АПК 3. Продукция раковыми клетками иммуносупрессивных факторов 4. Опухоль-индуцированные изменения в сигналах для Т-клеток 5. Опухоль-индуцированный сдвиг Th 1 -Th 2 6. Большинство опухолевых антигенов вызывает толерантность 7. Цитокиновый состав опухолей негативно действует на Т-клетки.

Вакцинотерапия различных опухолей при помощи различных рекомбинантных ДНК представляется одним из самых перспективных направлений в борьбе с раком.

МЕДИЦИНСКИЕ ТЕХНОЛОГИИ æ Создание новых технологий производства вакцин и других иммунологических препаратов для диагностики, лечения и специфической профилактики инфекционных заболеваний; æ Создание новых молекулярно-генетических методов диагностики и лечения врожденных патологий и наследственных заболеваний; æ Разработка новых методов диагностики и лечения онкологических заболеваний. æ Новые методологические подходы к лечению, диагностике и профилактике «соматических» заболеваний.

Области применения или предполагаемого применения вакцин Профилактика - инфекций - аллергии - некоторых болезней Иммунотерапия - хронических инфекций - некоторых онкологических болезней неинфекционных - аллергии онкологических - наркомании * - курения * * I и II фаза клинических испытаний Принцип – индукция антител, которые блокируют действие патогена или вредного вещества (кокаина, никотина)

"Соматическая" патология, ассоциированная с вирусными патогенами ВИРУСЫ ПАТОЛОГИЯ Эпид. пароти т Просто го герпеса Цитомегал о- Энтеро - Аден о- + + + + Кор и Крас нухи + МИОКАРДИТ + КАРДИОМИОПАТИИ + ФИБРОЭЛАСТОЗ + ХР. ПАНКРЕАТИТ + + ХР. НЕФРИТ + Варицелл а-Зостер + + ДИАБЕТ + + ГЛАУКОМА ПОРАЖ. ЗРИТ. НЕРВА + + АУТОИММУННЫЕ ЗАБ. + + + + + ПОЛИРАДИКУЛОНЕВР. + + АРТРИТЫ + + ЭНЦЕФАЛОМИЕЛИТ Ы + ХР. ОТИТЫ БОЛЕЗНЬ КРОНА БОЛЕЗНЬ МИНЬЕРА + + + + +

Хронические соматические болезни, связанные с микроорганизмами Патология Патогены Сердечно-сосудистая Атеросклероз Chlamydia pneumonia вирусы Коксаки, паротита Миокардит вирус гепатита С Инфаркт вирус гриппа Инсульт вирус гриппа Желудочно-кишечная Язва желудка и 12 Helicobacter pylori перстной кишки, гастриты Обмена Ювенильный диабет вирус краснухи

Вакцины с доказанным или предполагаемым профилактическим эффектом при различной патологии Вакцина Против гриппа Патология инсульт инфаркт Эффект *) I 19% 1623% II 48 -50% гепатита В гепатокарцинома изучается краснухи ювенильный предполагается диабет паротита мужское предполагается *) Уменьшение госпитализации (I), летальности (II) бесплодие **) Проходит клинические испытания

ВАКЦИНОТЕРАПИЯ Лечение вирусных, бактериальных и паразитарных инфекций Лечение соматических заболеваний различной этиологии (рассеянный склероз, диабет, наркомания и др. ) Лечение онкологических (раковых) заболеваний

РОЛЬ НАУКИ æ Участие в разработке и научном сопровождении программ здравоохранения; æ Независимая научная экспертиза программ и проектов; æ Подготовка медицинских кадров для выполнения программы; æ Участие в экспертизе при закупке медицинского оборудования и препаратов для диагностики, лечения и профилактики заболеваний; æ Создание новейших технологий оказания медицинской помощи.
ЗВЕРЕВ В.В. анапа.ppt