Лекция Обмен белков.ppt
- Количество слайдов: 93


ЗНАЧЕНИЕ БЕЛКОВОГО ОБМЕНА Белковый обмен – стержневой процесс среди многообразных превращений веществ, свойственных живой материи. Белки определяют: микро- и макроструктуру отдельных субклеточных образований, специфику клеток, органов и целостного организма, динамическое состояние между организмом и ОС. Белковый обмен весьма строго специфичен, обеспечивая специфичен непрерывность воспроизводства и обновления белковых тел организма. Все другие виды обмена – обслуживают обмен белков, специфический биосинтез белка. Белки выполняют и энергетическую функцию. При «сгорании» 1 г белков освобождается 16, 8 к. Дж энергии. Уникальна каталитическая функция белков.


АЗОТИСТЫЙ БАЛАНС Азотистый баланс – количественная разница между введением N с пищей и выведением его в виде конечных продуктов азотистого обмена, выраженных в одинаковых единицах (в г/сут. ). Положительный азотистый баланс: (вывод. N) < (ввод. N) (синтез преобладает над распадом белков органов и тканей – в молодом, растущем организме и в период беременности и лактации). Отрицательный азотистый баланс: (вывод. N) > (ввод. N) (при голодании, белковой недостаточности, тяжелых заболеваниях и часто – у пожилых людей). Азотистое равновесие: (вывод. N) = (ввод. N) (у здорового взрослого человека, соблюдающего полноценную диету).

НОРМЫ БЕЛКА В ПИТАНИИ Первые эксперименты по этому вопросу были выполнены в 70– 80 -х годах XIX в. Фойт на основании статистических данных рассчитал суточное потребление питательных веществ одним человеком. Для взрослого человека со средней массой и ростом: белков – 118 г углеводов – 500 г жиров – 56 г

КОЭФФИЦИЕНТ ИЗНАШИВАНИЯ Дальнейшие эксперименты были посвящены: определению минимального количество белка в диете, полноценной в отношении энергетических потребностей, при котором достигалось азотистое равновесие, установлению суточного выделения азотистых веществ у людей, находящихся в течение 8– 10 дней на безбелковой, но полностью обеспечивающей энергетические потребности организма, диете. В последнем случае взрослый человек выделяет довольно постоянное количество N – 53 мг/сут. на 1 кг массы тела На основании этого можно рассчитать количество белка, постоянно расщепляющееся в организме человека при безбелковой диете – коэффициент изнашивания (Рубнер): 0, 053 · 70 · 6, 25 = 23, 2 (г), где 70 кг – средняя масса тела; 6, 25 – коэффициент, учитывающий 16%-ное содержание азота в белках – 100: 16 = 6, 25)

ФИЗИОЛОГИЧЕСКИЙ МИНИМУМ БЕЛКА Однако прием лишь 23 г белка приводит к развитию резко отрицательного баланса. Тогда стали повышать количество белка в суточной диете. В зависимости от источника белка оно колеблется в широких пределах: яичный белок – 19, 9 г, говядина – 26, 0 г, молоко – 27, 6 г, картофель – 30, 0 г, хлеб из пшеничной муки – 67, 0 г). Однако в среднем азотистое равновесие у человека устанавливается уже приеме в сутки 30– 45 г белка. Это минимальное количество белка, позволяющее поддерживать азотистое равновесие при диете, полностью покрывающей энергетические потребности организма человека, – физиологический минимум белка.

СОВРЕМЕННЫЕ НОРМЫ БЕЛКА В ПИТАНИИ Прием 50 г белка не предотвращает частичного истощения. Принятые в настоящее время нормы учитывают: климатические условия, условия труда, профессию, возраст и другие факторы. Так, взрослый человек, занимающийся умственным трудом и подвергающийся средней физической нагрузке, должен получать 100– 120 г белка в сутки


ИСТОЧНИКИ БЕЛКА Главными источниками белков для человека являются пищевые продукты животного и растительного происхождения. Главным образом животные продукты (мясо, рыба, сыр) и только некоторые растительные продукты (горох, соя) богаты белками. Наиболее распространенные растительные пищевые продукты (хлеб, рис, макароны, гречневая крупа, пшено, орехи, картофель, капуста, морковь, свекла, яблоки, вишня и др. ) содержат мало белка.

Белки пищи, за весьма редким исключением, не усваиваются организмом, если они не будут расщеплены в процессе переваривания пищи до свободных аминокислот, из которых затем в клетках организма строятся свойственные данному виду специфические белки. Весь сложный процесс гидролиза пищевых белков, начиная от желудка и кончая тонким кишечником, «настроен» таким образом, чтобы путем последовательного действия протеолитических ферментов лишить белки пищи видовой специфичности и придать продуктам гидролиза способность всасываться в кровь через стенки кишечника (примерно 95 – 97% белков пищи всасываются в виде свободных аминокислот).
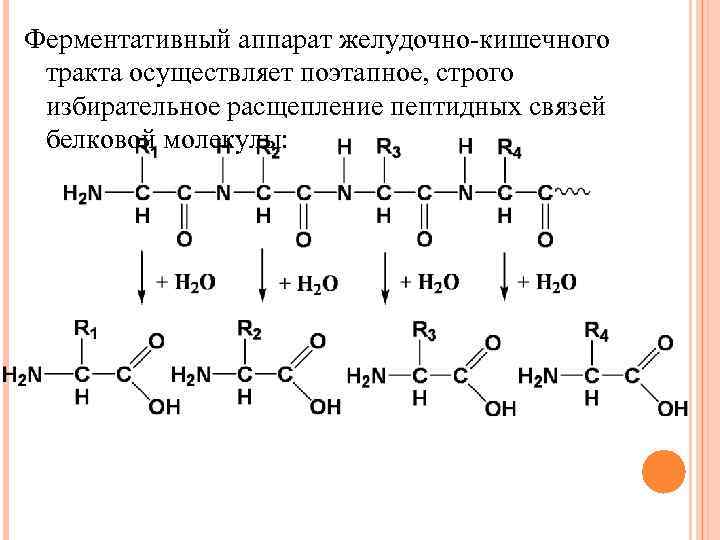
Ферментативный аппарат желудочно-кишечного тракта осуществляет поэтапное, строго избирательное расщепление пептидных связей белковой молекулы:

Термодинамические условия способствуют подобному расщеплению, т. к. G < 0, поэтому одного фермента, специфичного в отношении пептидной связи, теоретически должно быть достаточно для переваривания пищевых белков. Однако в действительности положение более сложное, т. к. протеолитические ферменты более специфичны и могут быть чувствительны к размеру полипептида, локализации места приложения гидролиза и к природе радикалов аминокислот

ГЛАВНЫЕ ПРОТЕОЛИТИЧЕСКИЕ ФЕРМЕНТЫ Протеолитические ферменты относятся: к классу гидролаз, подклассу пептидаз. Различают группы: экзопептидазы (катализирующие разрыв концевой пептидной связи с освобождением одной какойлибо концевой аминокислоты) эндопептидазы (преимущественно гидролизующие пептидные связи внутри полипептидной цепи)

Эндопептидазы желудка: Пепсин Гастриксин Реннин Эндопептидазы поджелудочной железы: Трипсин Химотрипсин Эластаза Все три эндопептидазы поджелудочной железы являются сериновыми протеиназами, поэтому имеют сходные структуру и механизм действия Экзопептидазы: Карбоксипептидазы Аминопептидазы Дипептидазы

ПЕРЕВАРИВАНИЕ БЕЛКОВ В ЖЕЛУДКЕ В желудке имеются все условия для переваривания белков: Активный пепсин гидролизует преимущественно пептидные связи, образованные аминогруппами ароматических аминокислот (фен, тир). Он расщепляет практически все природные белки. Соляная кислота переводит неактивный пепсиноген в активный пепсин, создает оптимальную среду для действия пепсина (р. Н чистого желудочного сока 0, 9– 1, 6, а оптимум р. Н пепсина 1, 5– 2, 5). в присутствии соляной кислоты происходят набухание белков (увеличение поверхности соприкосновения фермента с субстратом), частичная денатурация и, возможно, гидролиз пищевых белков. В зависимости от природы белка, р. Н и скорости опорожнения желудка белки пищи в желудке подвергаются гидролизу пепсином с образованием полипептидов меньшего размера (альбумоз и пептонов) или коротких пептидов и, возможно, небольшого числа свободных аминокислот.

ПЕРЕВАРИВАНИЕ БЕЛКОВ В КИШЕЧНИКЕ В тонком кишечнике на белки действуют ферменты панкреатического и кишечного соков. В поджелудочной железе вырабатываются ферменты: Трипсин разрывает пептидные связи, образованные карбоксильными группами лиз и арг Химотрипсин – карбоксильными группами ароматических аминокислот (фен, тир, три). Оптимум р. Н трипсина и химотрипсина 7, 2– 7, 8 В результате образуются различной длины пептиды и некоторое количество свободных аминокислот. Дальнейший гидролиз осуществляется под действием панкреатических ферментов: Аминопептидаза гидролизует пептидные связи с N-конца пептидов. Карбоксипептидаза разрывает пептидные связи с С-конца пептида. В конечном счете остаются дипептиды, на которые действуют специфические дипептидазы, гидролизующие их до свободных аминокислот. Аминокислоты подвергаются всасыванию клетками кишечника. Этот процесс требует затрат энергии (АТФ или электрохимического потенциала, возникающего за счет движения ионов Nа+ и К+ через мембрану).


ПРОЦЕССЫ ГНИЕНИЯ БЕЛКОВ В КИШЕЧНИКЕ Микроорганизмы кишечника для своего роста нуждаются в доставке с пищей определенных аминокислот. Кроме того, микрофлора кишечника располагает набором ферментных систем, отличных от соответствующих ферментов животных тканей и катализирующих разнообразные превращения пищевых аминокислот (окисление, восстановление, дезаминирование, декарбоксилирование, распад). Благодаря этому в кишечнике создаются оптимальные условия для образования ядовитых продуктов распада аминокислот (фенола, индола, крезола, скатола, сероводорода, метилмеркаптана), а также нетоксичных – спиртов, аминов, жирных кислот, кетокислот, оксикислот и др.

В процессе постепенного и глубокого распада серосодержащих аминокислот (цис, цистина, мет) образуются H 2 S и CH 3 SH. Диаминокислоты декарбоксилируют с образованием протеиногенных аминов (птоаминов, или трупных ядов): Оба амина легко всасываются в кровь и выделяются с мочой, но открываются в ней редко (при патологиях), т. к. обезвреживаются уже в клетках слизистой оболочки.
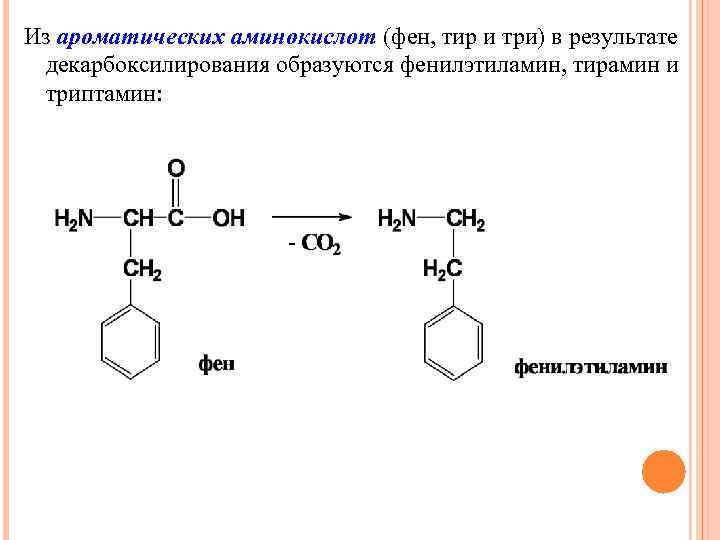
Из ароматических аминокислот (фен, тир и три) в результате декарбоксилирования образуются фенилэтиламин, тирамин и триптамин:
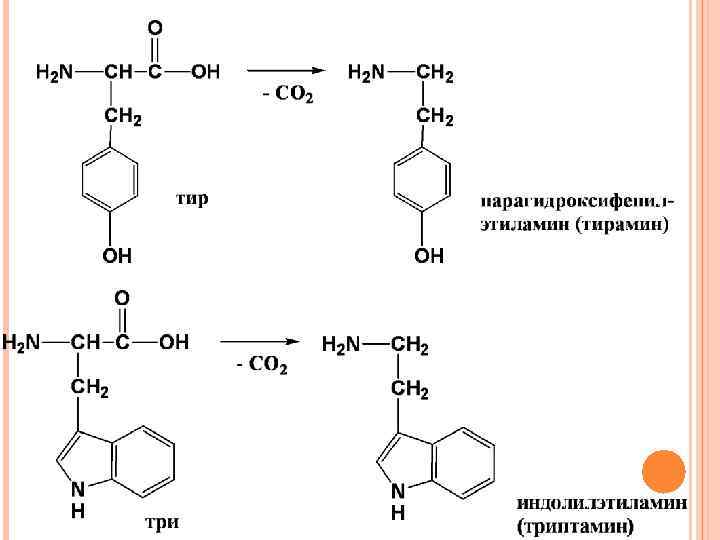
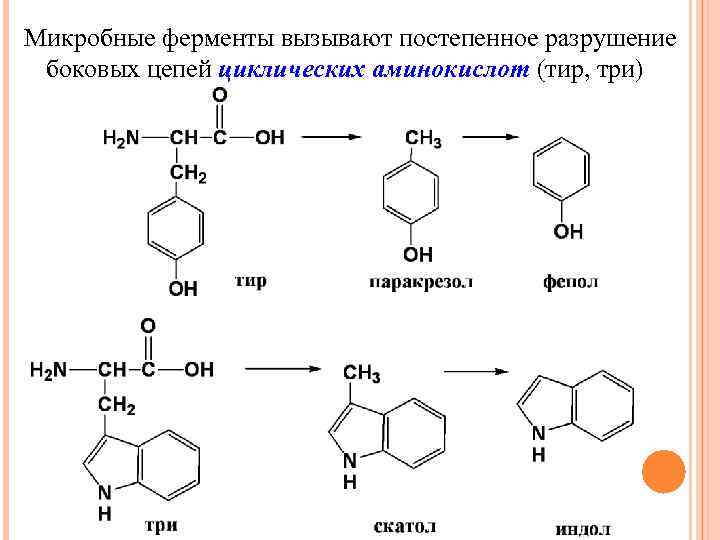
Микробные ферменты вызывают постепенное разрушение боковых цепей циклических аминокислот (тир, три)
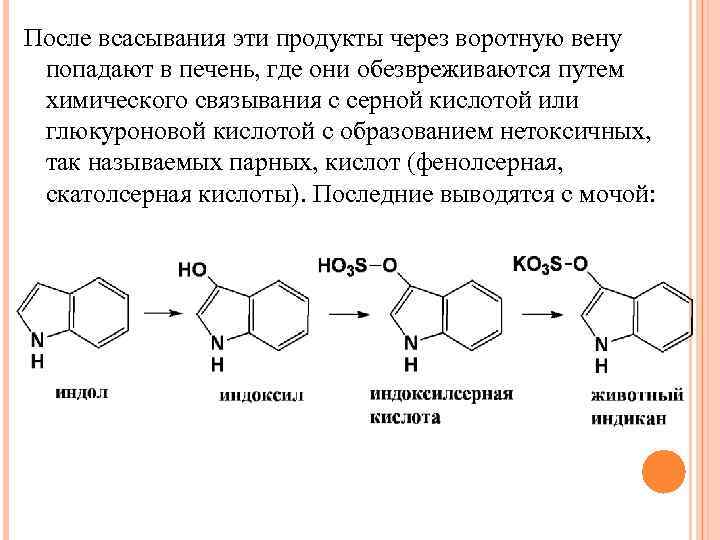
После всасывания эти продукты через воротную вену попадают в печень, где они обезвреживаются путем химического связывания с серной кислотой или глюкуроновой кислотой с образованием нетоксичных, так называемых парных, кислот (фенолсерная, скатолсерная кислоты). Последние выводятся с мочой:

СУДЬБА ВСОСАВШИХСЯ АМИНОКИСЛОТ Всосавшиеся в кровь аминокислоты по воротной вене попадают в печень, где подвергаются ряду превращений, или разносятся кровью по всему организму и используются для физиологических целей. Аминокислоты в первую очередь используются в качестве строительного материала для синтеза тканевых белков, ферментов, гормонов и других БАВ. Некоторое количество аминокислот подвергается распаду до СО 2, Н 2 О и NН 3 с освобождением энергии (около 1200 к. Дж в сутки за счет окисления примерно 70 г аминокислот – около 10% суточной потребности в энергии).

ОБЩИЕ ПУТИ ОБМЕНА АМИНОКИСЛОТ Почти все аминокислоты в организме подвергаются реакциям: дезаминирования трансаминирования (переаминирования) декарбоксилирования
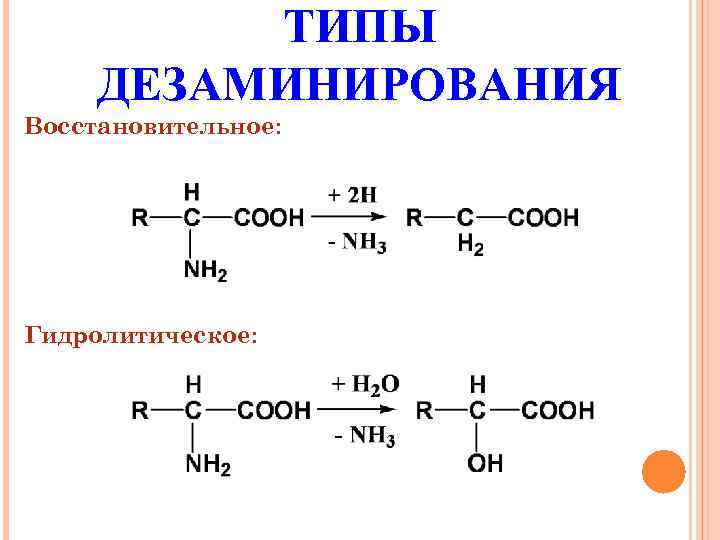
ТИПЫ ДЕЗАМИНИРОВАНИЯ Восстановительное: Гидролитическое:
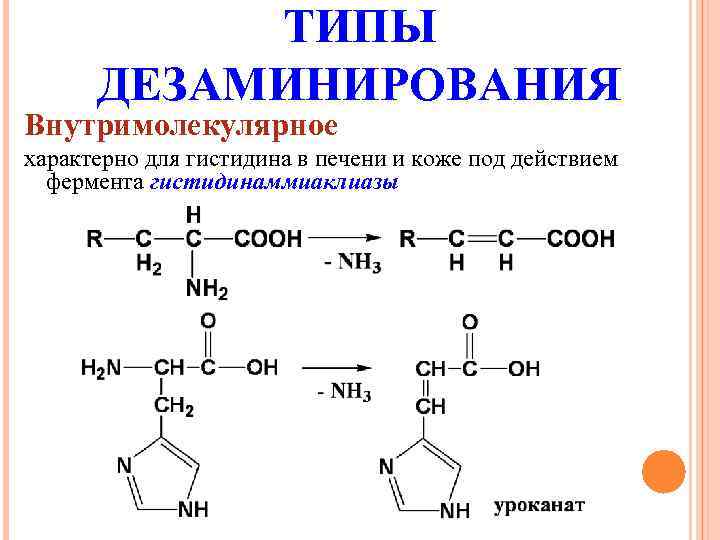
ТИПЫ ДЕЗАМИНИРОВАНИЯ Внутримолекулярное характерно для гистидина в печени и коже под действием фермента гистидинаммиаклиазы

ТИПЫ ДЕЗАМИНИРОВАНИЯ Окислительное n Реакция протекает в две стадии – Первая стадия – ферментативная, ферменты – оксидазы аминокислот (дегидрогеназы), коферменты – ФМН, ФАД, НАД или НАДФ – Вторая стадия идет спонтанно в присутствии воды
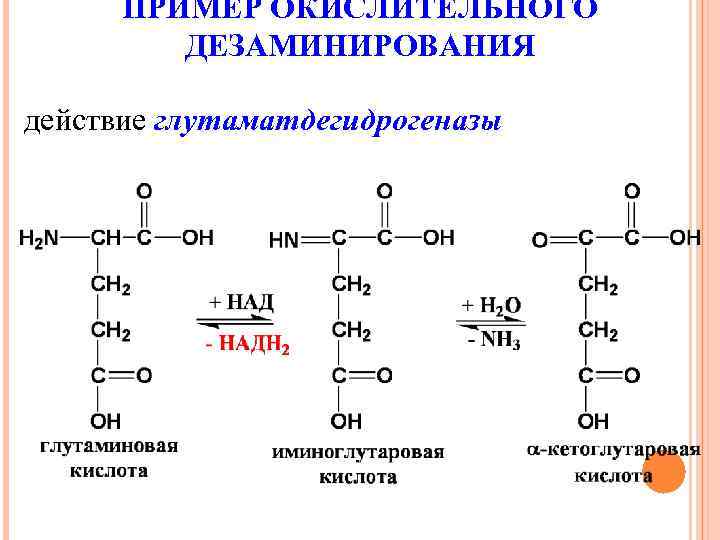
ПРИМЕР ОКИСЛИТЕЛЬНОГО ДЕЗАМИНИРОВАНИЯ действие глутаматдегидрогеназы

ПЕРЕАМИНИРОВАНИЕ АМИНОКИСЛОТ Реакции межмолекулярного переноса аминогруппы от аминокислоты на -кетокислоту без промежуточного образования аммиака Процессы переаминирования универсальны для всех живых организмов. Реакции обратимы и протекают при участии ферментов аминотрансфераз, кофермент – пиридоксальфосфат (витамин В 6)
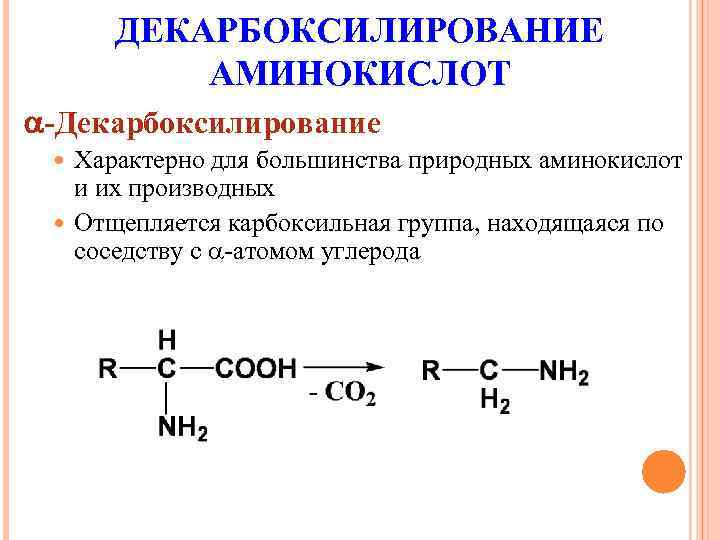
ДЕКАРБОКСИЛИРОВАНИЕ АМИНОКИСЛОТ -Декарбоксилирование Характерно для большинства природных аминокислот и их производных Отщепляется карбоксильная группа, находящаяся по соседству с -атомом углерода
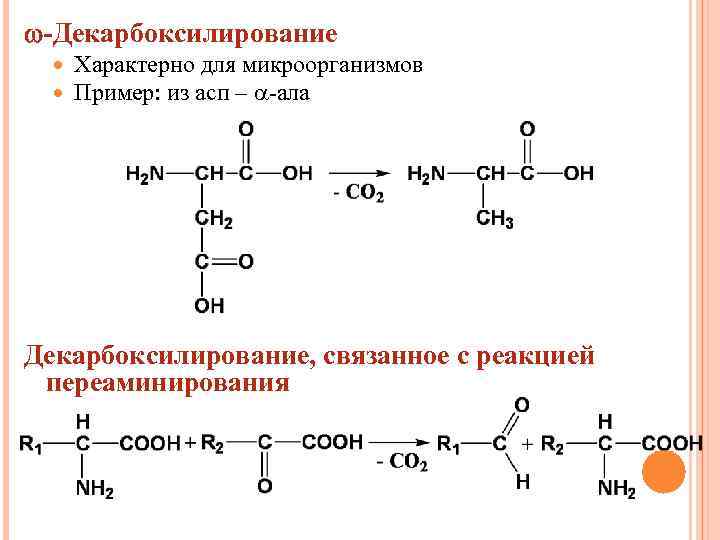
-Декарбоксилирование Характерно для микроорганизмов Пример: из асп – -ала Декарбоксилирование, связанное с реакцией переаминирования
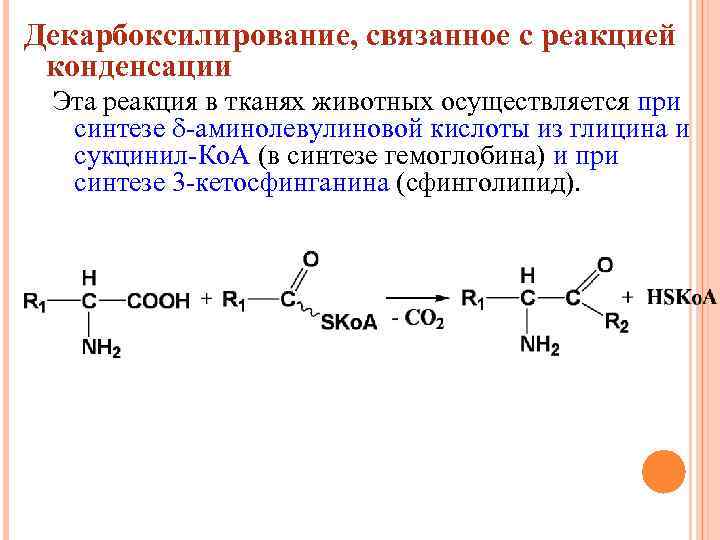
Декарбоксилирование, связанное с реакцией конденсации Эта реакция в тканях животных осуществляется при синтезе -аминолевулиновой кислоты из глицина и сукцинил-Ко. А (в синтезе гемоглобина) и при синтезе 3 -кетосфинганина (сфинголипид).

Реакции декарбоксилирования необратимы и осуществляются специфическими ферментами декарбоксилазами аминокислот, коферментом которых является пиридоксальфосфат (витамин В 6)
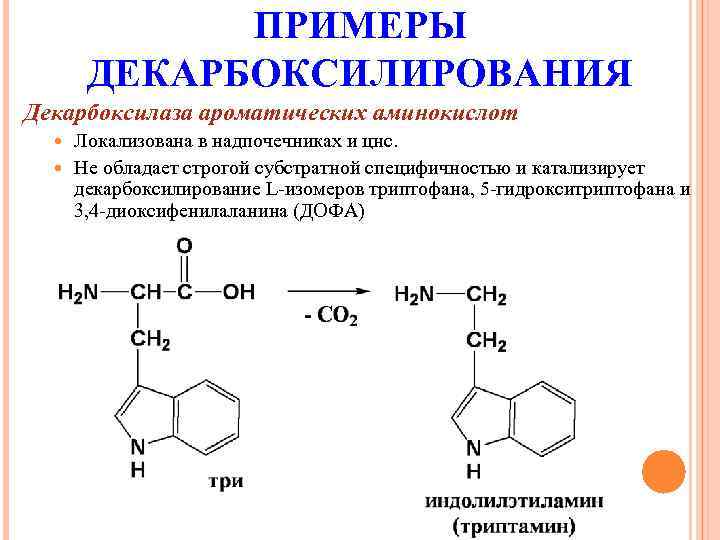
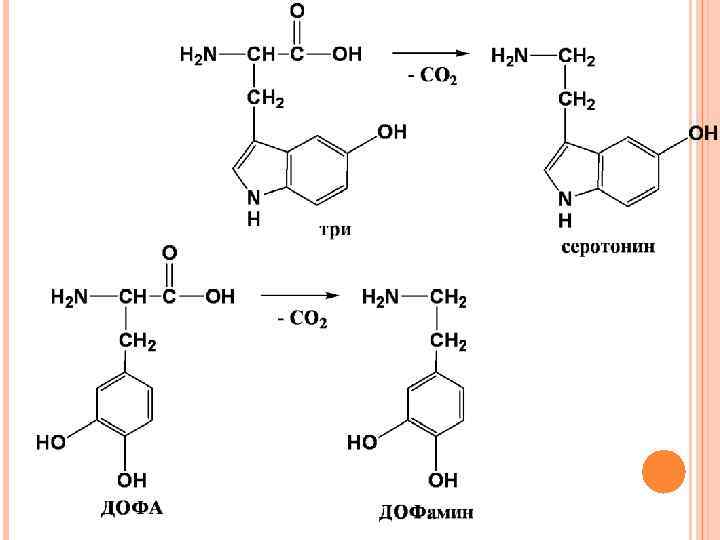
ПРИМЕРЫ ДЕКАРБОКСИЛИРОВАНИЯ Декарбоксилаза ароматических аминокислот Локализована в надпочечниках и цнс. Не обладает строгой субстратной специфичностью и катализирует декарбоксилирование L-изомеров триптофана, 5 -гидрокситриптофана и 3, 4 -диоксифенилаланина (ДОФА)
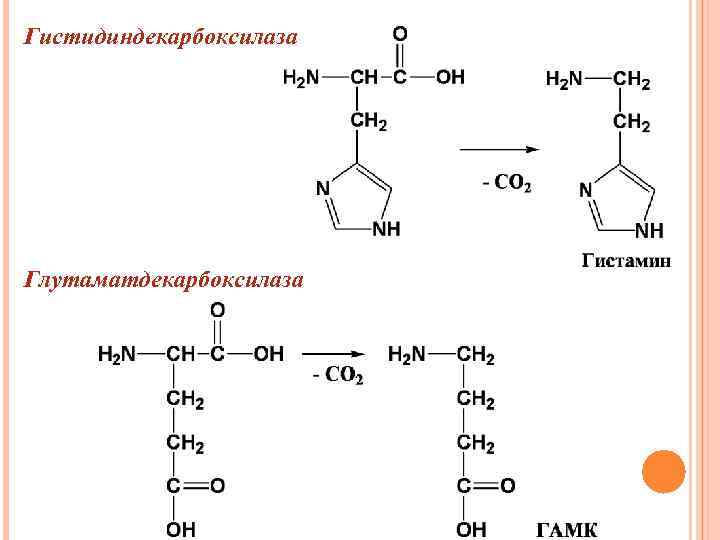
Гистидиндекарбоксилаза Глутаматдекарбоксилаза

Превращение орнитина в путресцин и лизина в кадаверин Накопление биогенных аминов может отрицательно сказаться на физиологическом статусе и вызывать ряд серьезных нарушений в организме. Однако органы и ткани (и организм в целом) располагают специальными механизмами обезвреживания биогенных аминов, которые в общем виде сводятся к их окислительному дезаминированию Ферменты: моноамин- и диаминоксидазы (кофермент ФАД)
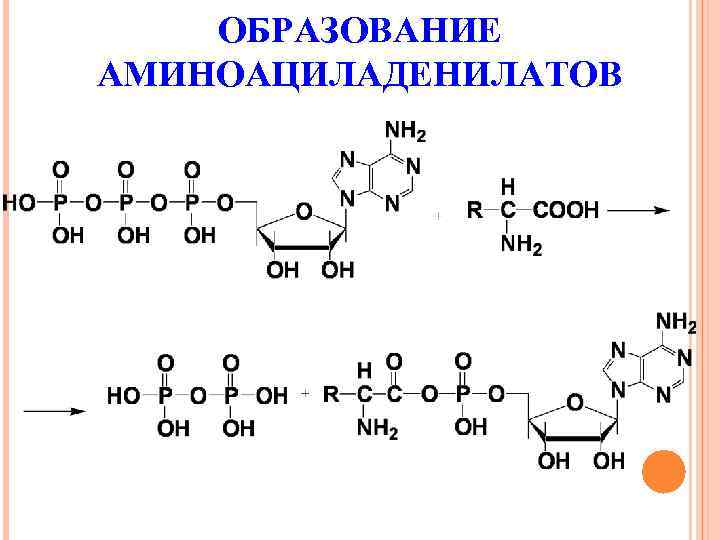
ОБРАЗОВАНИЕ АМИНОАЦИЛАДЕНИЛАТОВ


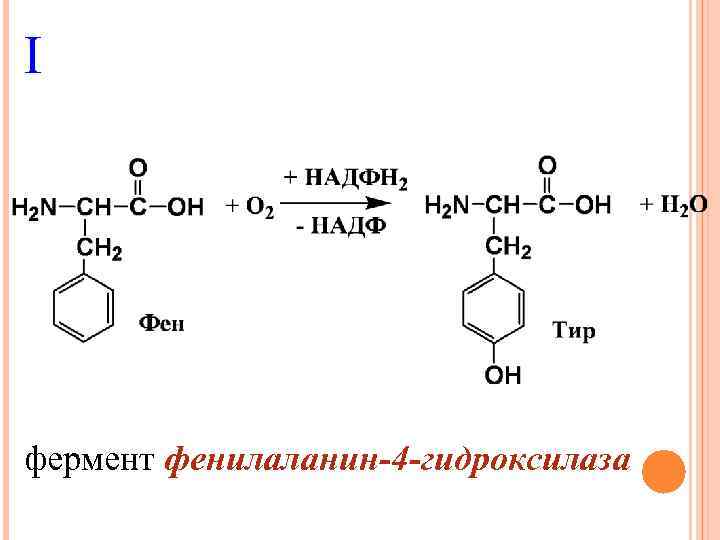
I фермент фенилаланин-4 -гидроксилаза
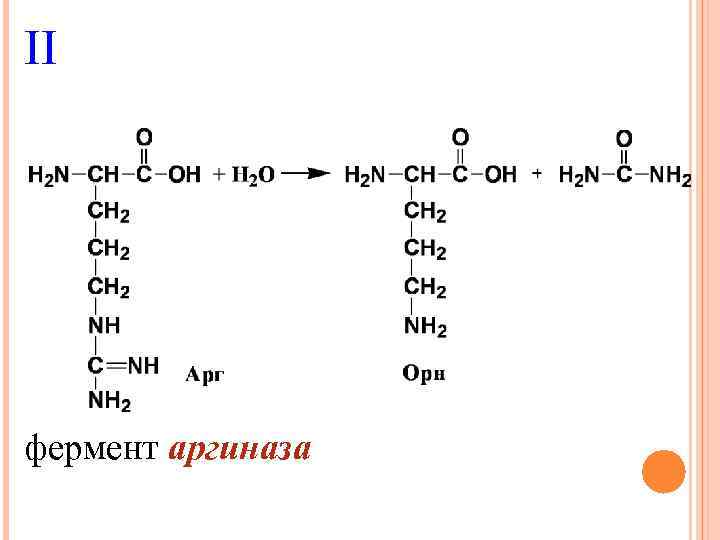
II фермент аргиназа
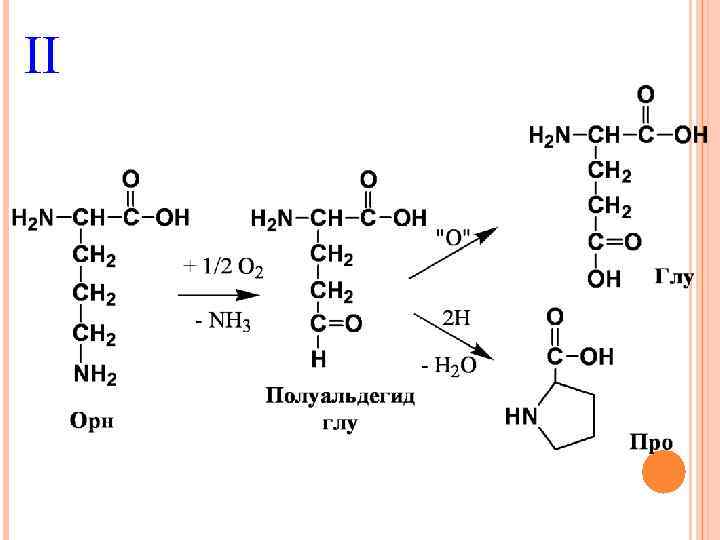
II
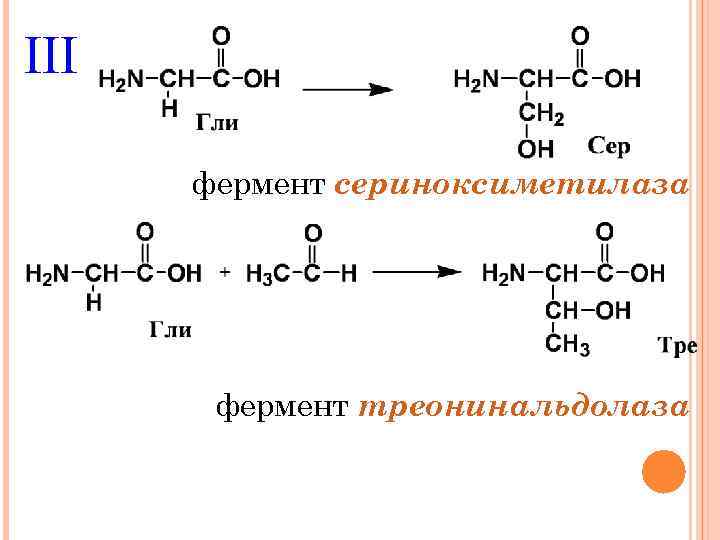
III фермент сериноксиметилаза фермент треонинальдолаза

IV Три → Ала; Глн → Три; Глн → Асн; Глн → Гис и др.

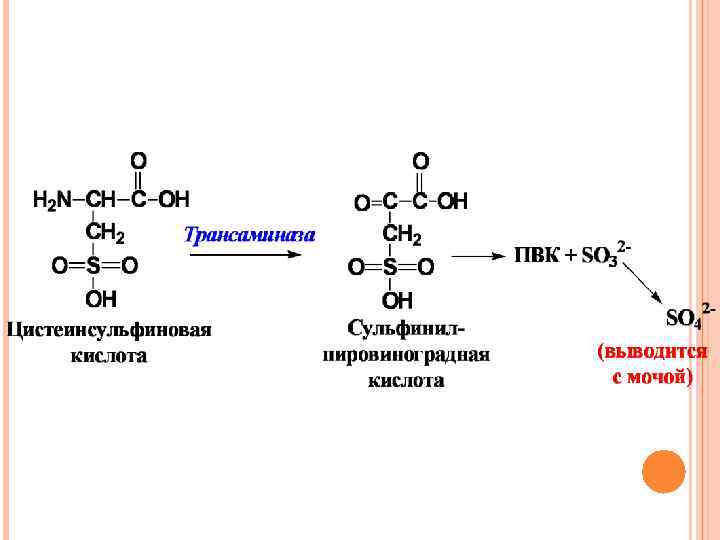
Окислительновосстановительные реакции по серосодержащим радикалам цистеина и цистина
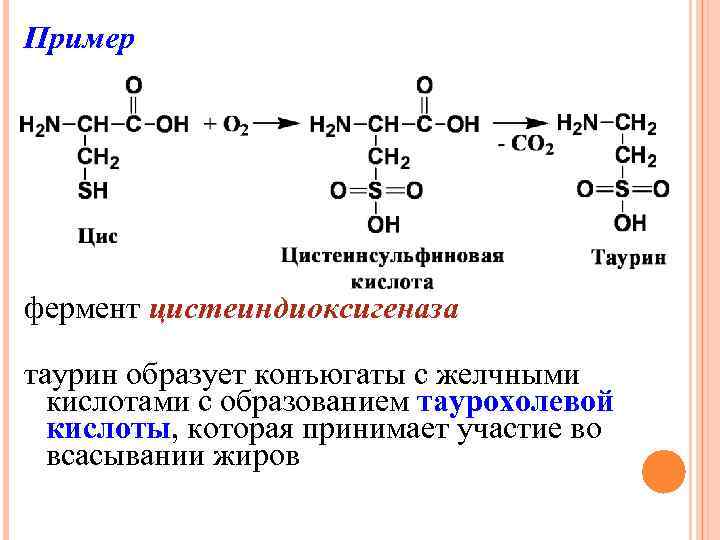
Пример фермент цистеиндиоксигеназа таурин образует конъюгаты с желчными кислотами с образованием таурохолевой кислоты, которая принимает участие во всасывании жиров

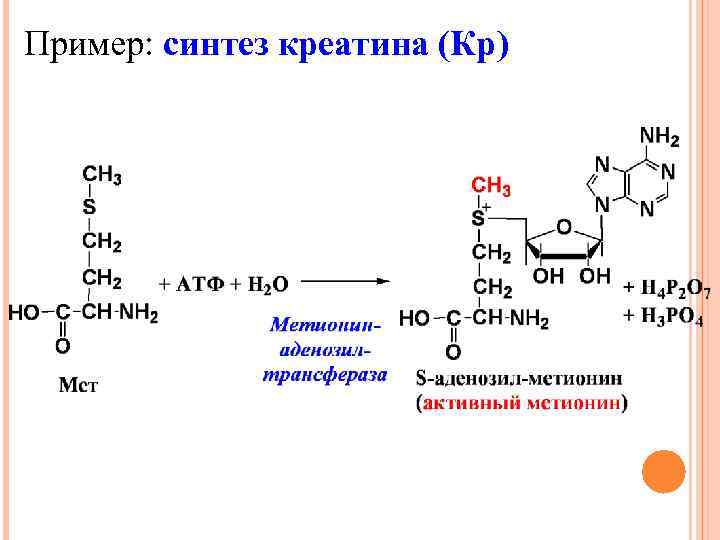
Пример: синтез креатина (Кр)
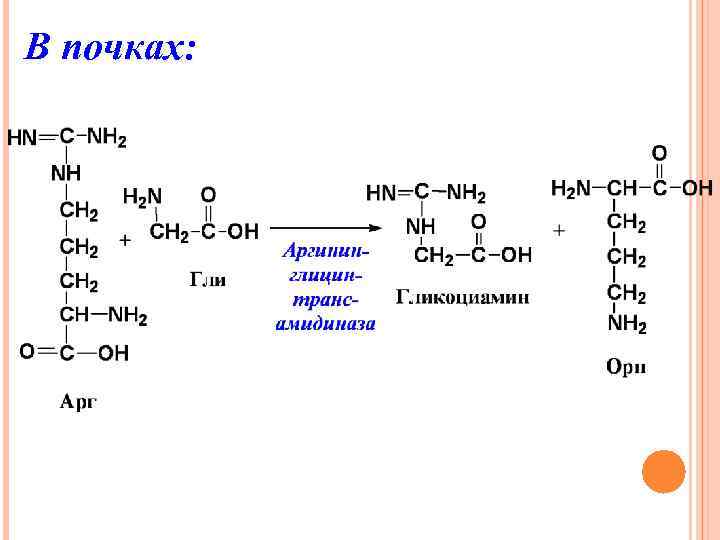
В почках:
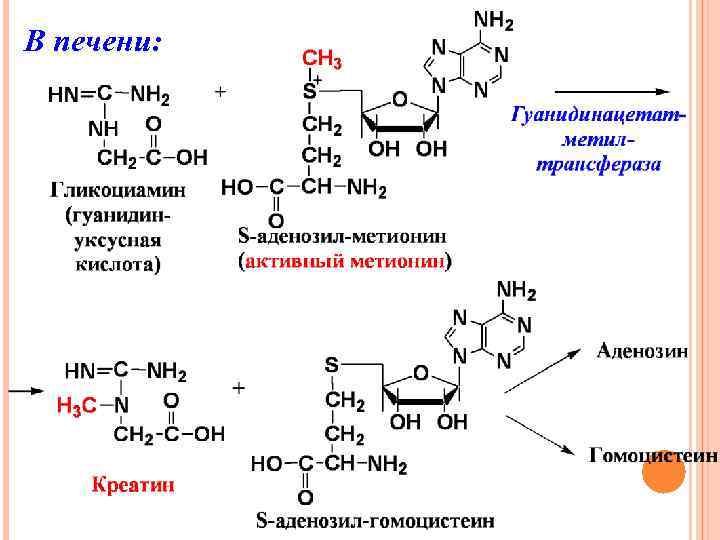
В печени:
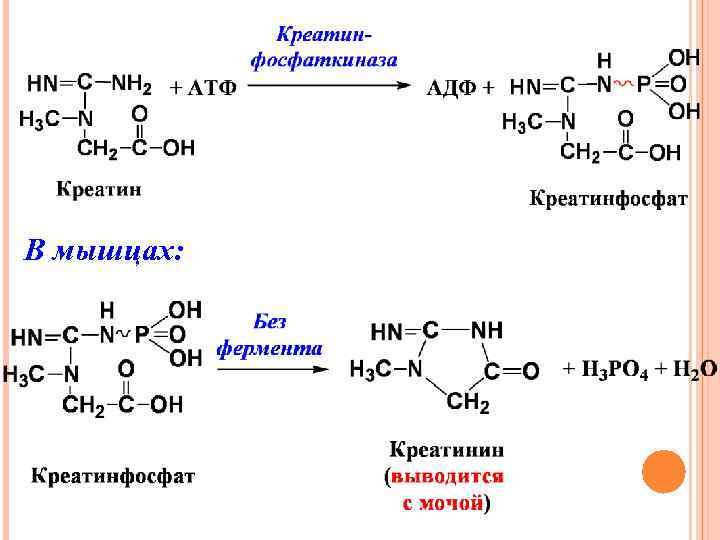
В мышцах:

Креатинфосфат (Кр. Ф) – макроэргическое соединение, обеспечивающее ресинтез АТФ в работающей мышце (фермент креатинкиназа): Кр. Ф + АДФ ⇄ Кр + АТФ. Креатинкиназный путь ресинтеза АТФ чрезвычайно быстрый и максимально эффективный (за счет каждой молекулы Кр. Ф синтезируется 1 молекула АТФ). Запасы креатинфосфата в мышце невелики, а доступность его энергии имеет ценность для работающей мышцы только в том случае, если расход его постоянно возмещается синтезом АТФ в процессах метаболизма. Поэтому основными источниками энергии являются тканевое дыхание и гликолиз. Креатинфосфат играет роль транспортной формы макроэргических связей, образующихся в процессе тканевого дыхания и окислительного фосфорилирования.

Схема перехода энергии из митохондрии в цитоплазму клетки миокарда
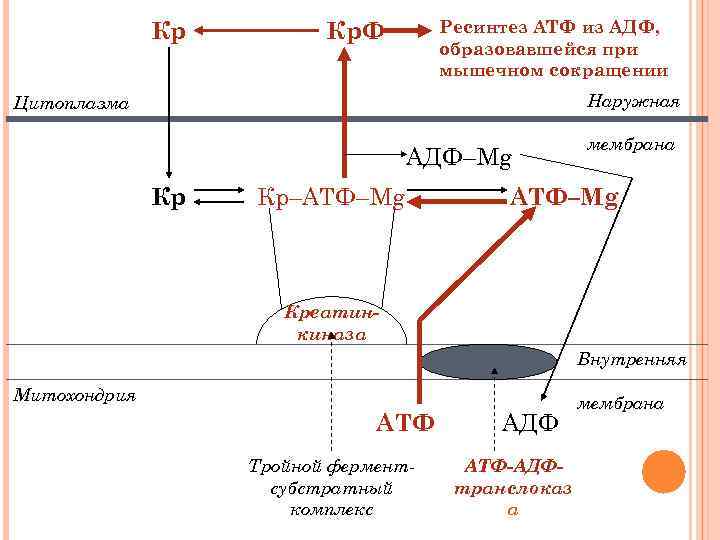
Кр Ресинтез АТФ из АДФ, образовавшейся при мышечном сокращении Кр. Ф Наружная Цитоплазма АДФ–Mg Кр Кр–АТФ–Mg мембрана АТФ–Mg Креатинкиназа Внутренняя Митохондрия АТФ Тройной ферментсубстратный комплекс АДФ АТФ-АДФтранслоказ а мембрана


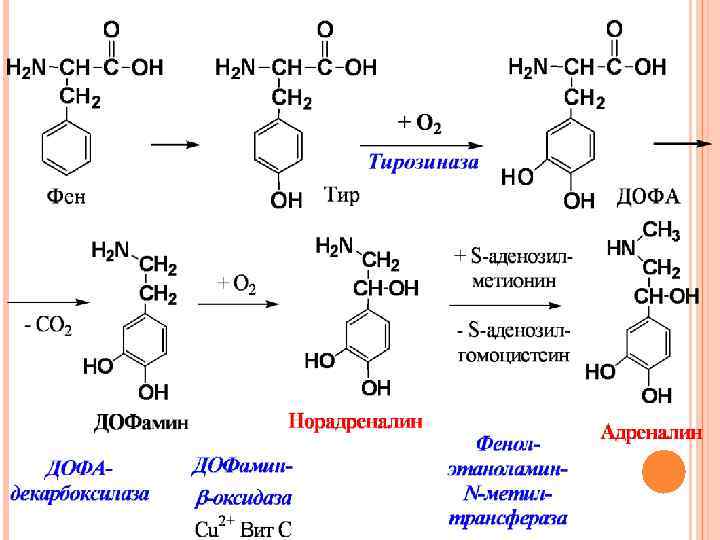
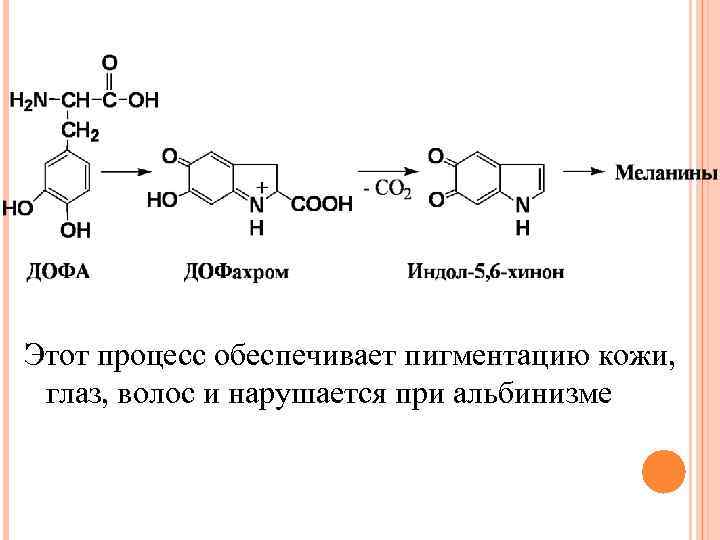
Этот процесс обеспечивает пигментацию кожи, глаз, волос и нарушается при альбинизме

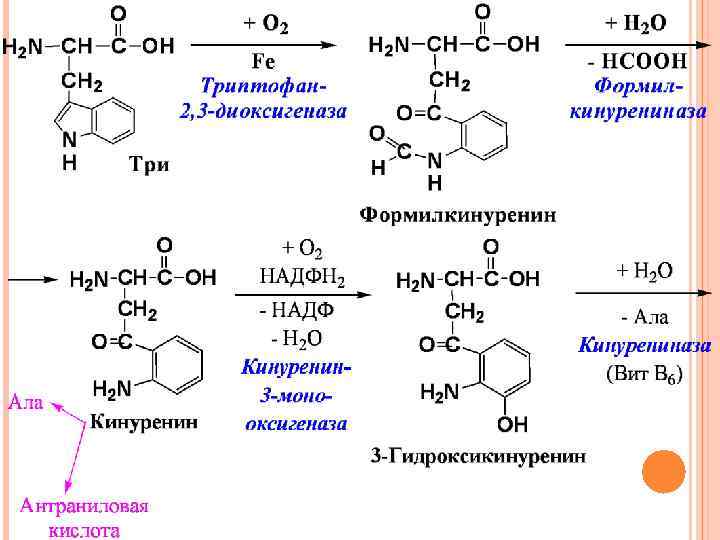
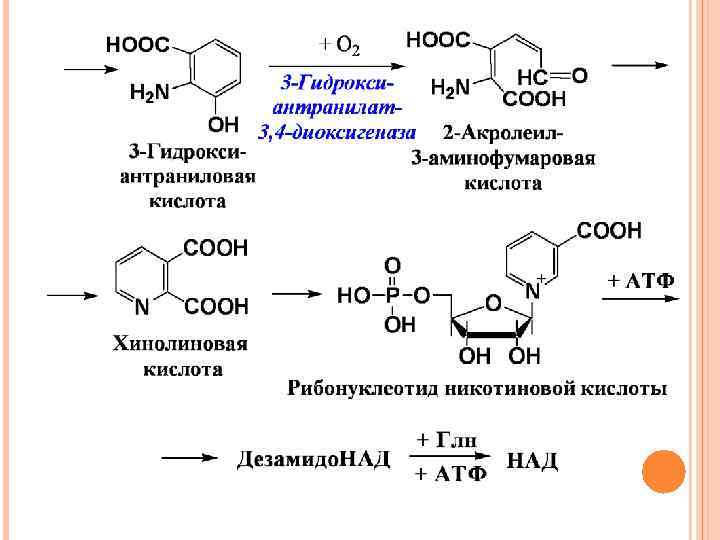

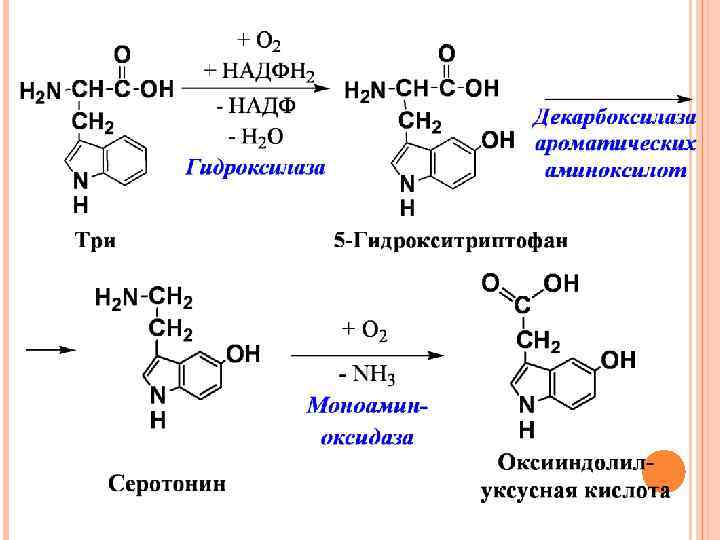

Индолилуксусная кислота – ростовое вещество растений В норме не более 1% три превращается в серотонин Содержание индолилуксусной кислоты в моче резко повышается при поражении злокачественными карциномами, тогда около 60% три превращается в серотонин.


Ала, цис, гли, сер, тре → ПВК Иле, лей, три → ацетил-Ко. А Асн, асп → ЩУК Арг, глн, про, гис → глу → -кетоглутаровая кислота Иле, мет, вал → сукцинил-Ко. А Тир, фен → фумаровая кислота


В результате распада аминокислот возникают СО 2, NН 3, амины, кетокислоты и другие сложные органические вещества. Все они (кроме СО 2 и NH 3) подвергаются дальнейшей деструкции. Амины путем окислительного дезаминирования превращаются в карбоновые кислоты: R–CH 2–NH 2 + H 2 O + CO 2 → R–CHO + NH 3 + H 2 O 2 (фермент моноаминооксидаза) R–CHO + H 2 O + НАД → R–СООН + НАДН 2 (фермент альдегидрогеназа) Аналогично идет реакция окислительного дезаминирования диаминов при посредстве диаминоксидаз. Кетокислоты и карбоновые кислоты постепенно окисляются до СО 2 и Н 2 О.

Таким образом, конечными продуктами распада аминокислот являются Н 2 О, СО 2 и NН 3. Вода поступает в общий метаболический фонд, углекислый газ выводится из организма. Аммиак является высокотоксичным соединением, поэтому концентрация его в организме должна сохраняться на низком уровне (1– 2 мг/л в крови; концентрация 50 мг/л является летальной). Поэтому аммиак должен подвергаться связыванию в тканях с образованием нетоксичных соединений, легко выделяемых с мочой


1. ОБРАЗОВАНИЕ АММОНИЙНЫХ СОЛЕЙ 2 NH 3 + H 2 O + CO 2 → (NH 4)2 CO 3 у некоторых обитателей гидросферы – пиявок, крабов, раков и др.

2. БИОСИНТЕЗ ГЛУТАМИНА (И АСПАРАГИНА) В мозге, сетчатке, почках, печени и мышцах. Амиды выполняют транспортную функцию. Синтез амидов требует энергии АТФ и присутствия глу или асп, свободного аммиака Катализируется глутамин- и аспарагинсинтетазами:
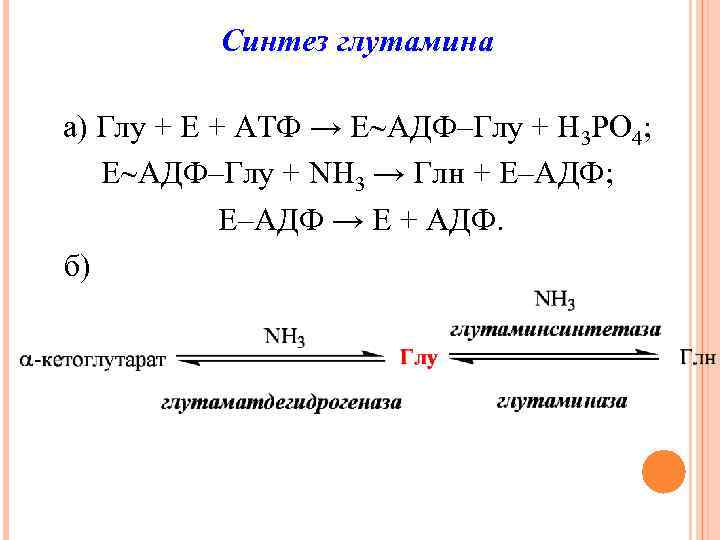
Синтез глутамина а) Глу + Е + АТФ → Е АДФ–Глу + Н 3 РО 4; Е АДФ–Глу + NH 3 → Глн + Е–АДФ; Е–АДФ → Е + АДФ. б)

Синтез аспарагина Асп + Е + АТФ → Е–аспартил АМФ + Н 4 Р 2 О 7; а) аммиак-зависимая аспарагинсинтетаза (у микроорганизмов и в животных тканях): Е–аспартил АМФ + NН 3 → Асн + Е + АМФ; б) глутамин-зависимая аспарагинсинтетаза (у животных): Е–аспартил АМФ + Глн → Асн + Е + АМФ + Глу.

3. БИОСИНТЕЗ МОЧЕВИНЫ Основной механизм обезвреживания аммиака в организме. Образующаяся мочевина выводится с мочой, на долю ее приходится до 80– 85% всего азота мочи. Синтез мочевины локализован в печени. Механизм синтеза мочевины описал Х. А. Кребс в 1932 г.


Сначала происходит синтез макроэргического соединения карбамилфосфорной кислоты (карбамилфосфата) из СО 2 и NH 3 (или глн): Карбамоилфосфатсинтаза содержит биотин (витамин Н) и сначала реагирует с 1 молекулой АТФ, образуя комплекс (СО 2)*–Е, который затем реагирует с молекулой аммиака (или амидной группой глн) и со второй молекулой АТФ (в качестве донора Н 3 РО 4). Специфическим активатором реакции является N-ацетилглутамат. Образовавшийся карбамилфосфат включается в специфический цикл, в котором в качестве регенерируемого компонента ( «катализатора» ) принимает участие аминокислота орнитин, которая легко возникает при гидролизе аргинина.

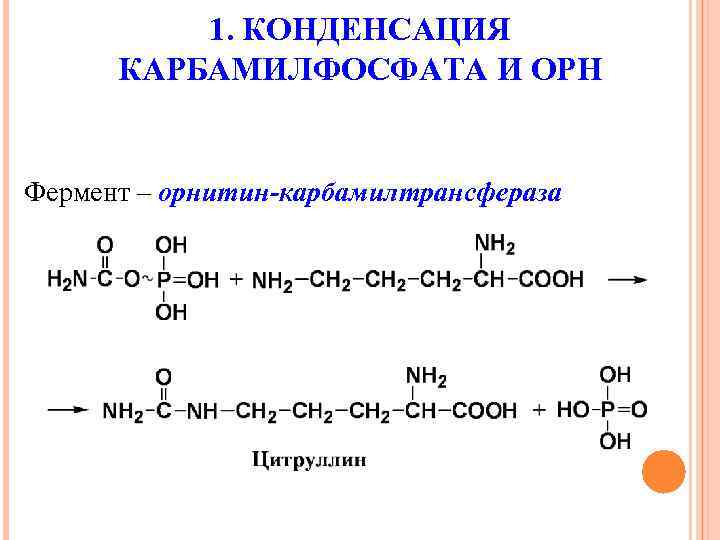
1. КОНДЕНСАЦИЯ КАРБАМИЛФОСФАТА И ОРН Фермент – орнитин-карбамилтрансфераза
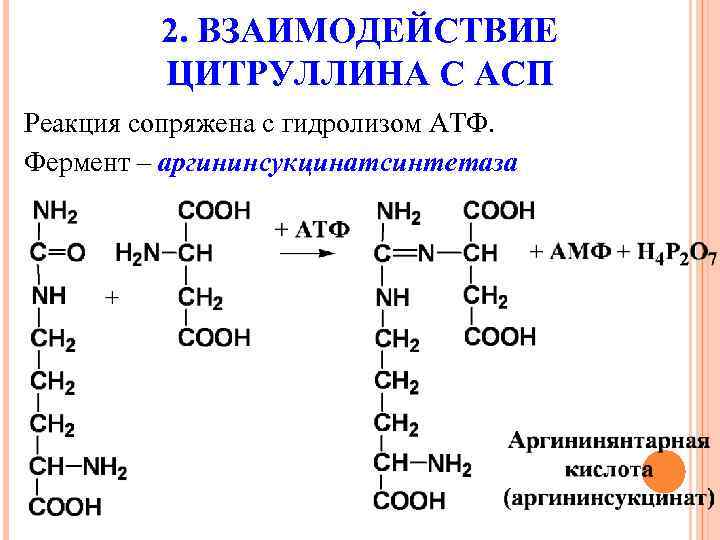
2. ВЗАИМОДЕЙСТВИЕ ЦИТРУЛЛИНА С АСП Реакция сопряжена с гидролизом АТФ. Фермент – аргининсукцинатсинтетаза
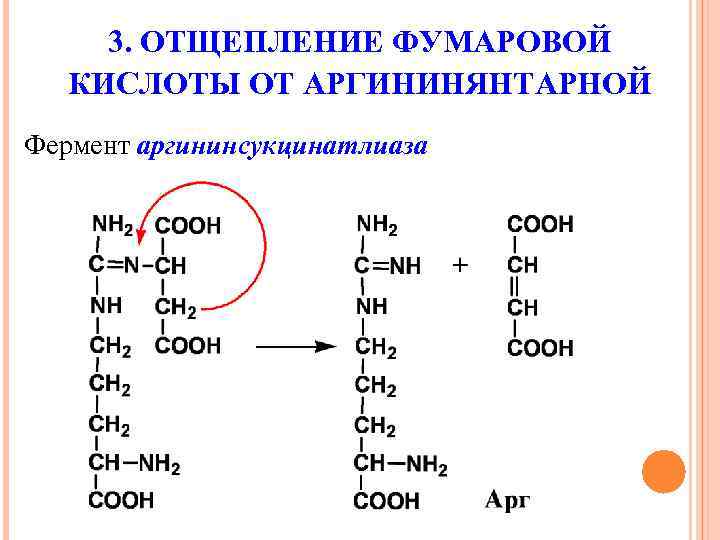
3. ОТЩЕПЛЕНИЕ ФУМАРОВОЙ КИСЛОТЫ ОТ АРГИНИНЯНТАРНОЙ Фермент аргининсукцинатлиаза
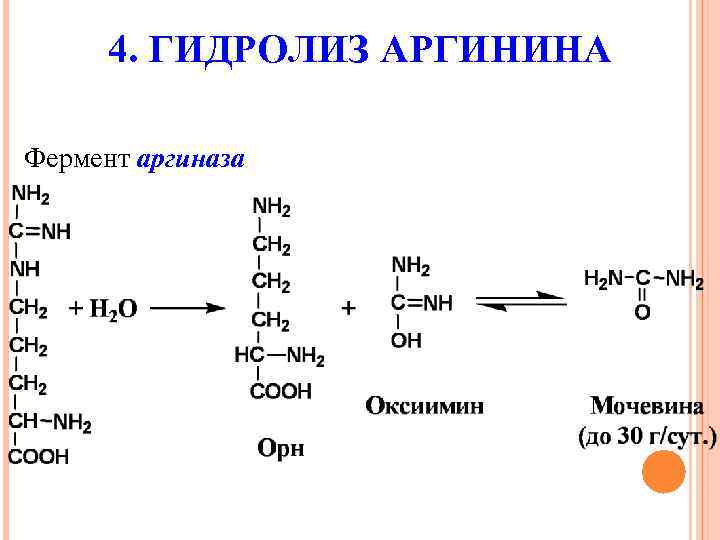
4. ГИДРОЛИЗ АРГИНИНА Фермент аргиназа

СУММАРНОЕ УРАВНЕНИЕ СИНТЕЗА МОЧЕВИНЫ СО 2 + NH 3 + 3 АТФ + 2 Н 2 О + асп → → Н 2 N–CO–NH 2 + 2 АДФ + АМФ + фумарат + 2 Н 3 РО 4 + Н 4 Р 2 О 7


ПЕРВИЧНЫЙ СИНТЕЗ Прямое аминирование непредельных кислот редкая реакция, происходит в основном у бактерий и растений фермент – аспартат-аммиаклиаза 1.

ПЕРВИЧНЫЙ СИНТЕЗ Восстановительное аминирование кетокислот главный путь – обращение окислительного дезаминирования аминокислот фермент глутаматдегидрогеназа – см. выше фермент аланиндегидрогеназа: 2.

ВТОРИЧНЫЙ СИНТЕЗ Переаминирование с кетокислотами Остальные аминокислоты образуются, в основном, путем переаминирования глу и ала с кетокислотами или путем превращения одних аминокислот в другие. Поэтому ала, асп и глу – первичные аминокислоты, а все остальные – вторичные.

ЗАМЕНИМЫЕ И НЕЗАМЕНИМЫЕ АМИНОКИСЛОТЫ В растениях осуществляется непрерывный синтез разнообразных аминокислот (постоянно встречающихся в белках и «экзотических» ). В отличие от этого животные синтезируют далеко не все аминокислоты. Синтезируемые аминокислоты называются заменимыми, а не синтезируемые – незаменимыми Незаменимые аминокислоты: вал, лей, иле, тре, мет, лиз, аминокислоты фен, три; есть видовые различия. Незаменимые аминокислоты должны быть в достаточном количестве в корме животных и пище человека, поэтому их получают в промышленности путем микробиологического синтеза.

БИОСИНТЕЗ БЕЛКОВ И НЕЗАМЕНИМЫХ АМИНОКИСЛОТ ДЛЯ ПРАКТИЧЕСКИХ ЦЕЛЕЙ Индустриальное производство белков Производство кормовых дрожжей Приготовление белкововитаминных концентратов (БВК) Выделение белков из непищевого сырья растительного происхождения Индустриальное производство пищи
Лекция Обмен белков.ppt