lecture_5_2013.ppt
- Количество слайдов: 48
 Zn-органические соединения Методы синтеза 1
Zn-органические соединения Методы синтеза 1
![Методы синтеза R 2 Zn – [1 а], [2], [4] [1 а] C 2 Методы синтеза R 2 Zn – [1 а], [2], [4] [1 а] C 2](https://present5.com/presentation/5652994_177566283/image-2.jpg) Методы синтеза R 2 Zn – [1 а], [2], [4] [1 а] C 2 H 5 I + Zn(Cu) “C 2 H 5 Zn. I” + (C 2 H 5)2 Zn + Zn. I 2 [2] Zn + R 2 Hg R 2 Zn + Hg [4] Zn. Cl 2 + 2 RLi R 2 Zn + 2 Li. Cl Zn. Cl 2 + 2 RMg. X R 2 Zn + 2 Mg. XCl 3 Zn(OAc)2 + 2 R 3 Al 3 R 2 Zn + 2 Al(OAc)3 2
Методы синтеза R 2 Zn – [1 а], [2], [4] [1 а] C 2 H 5 I + Zn(Cu) “C 2 H 5 Zn. I” + (C 2 H 5)2 Zn + Zn. I 2 [2] Zn + R 2 Hg R 2 Zn + Hg [4] Zn. Cl 2 + 2 RLi R 2 Zn + 2 Li. Cl Zn. Cl 2 + 2 RMg. X R 2 Zn + 2 Mg. XCl 3 Zn(OAc)2 + 2 R 3 Al 3 R 2 Zn + 2 Al(OAc)3 2
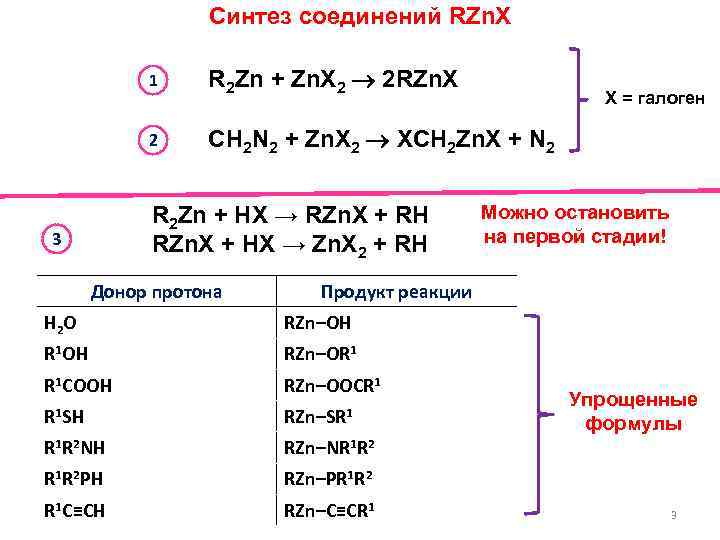 Синтез соединений RZn. X 1 R 2 Zn + Zn. X 2 2 RZn. X 2 CH 2 N 2 + Zn. X 2 XCH 2 Zn. X + N 2 R 2 Zn + HX → RZn. X + RH RZn. X + HX → Zn. X 2 + RH 3 Донор протона X = галоген Можно остановить на первой стадии! Продукт реакции H 2 O RZn–OH R 1 OH RZn–OR 1 R 1 COOH RZn–OOCR 1 R 1 SH RZn–SR 1 R 1 R 2 NH RZn–NR 1 R 2 PH RZn–PR 1 R 2 R 1 C≡CH RZn–C≡CR 1 Упрощенные формулы 3
Синтез соединений RZn. X 1 R 2 Zn + Zn. X 2 2 RZn. X 2 CH 2 N 2 + Zn. X 2 XCH 2 Zn. X + N 2 R 2 Zn + HX → RZn. X + RH RZn. X + HX → Zn. X 2 + RH 3 Донор протона X = галоген Можно остановить на первой стадии! Продукт реакции H 2 O RZn–OH R 1 OH RZn–OR 1 R 1 COOH RZn–OOCR 1 R 1 SH RZn–SR 1 R 1 R 2 NH RZn–NR 1 R 2 PH RZn–PR 1 R 2 R 1 C≡CH RZn–C≡CR 1 Упрощенные формулы 3
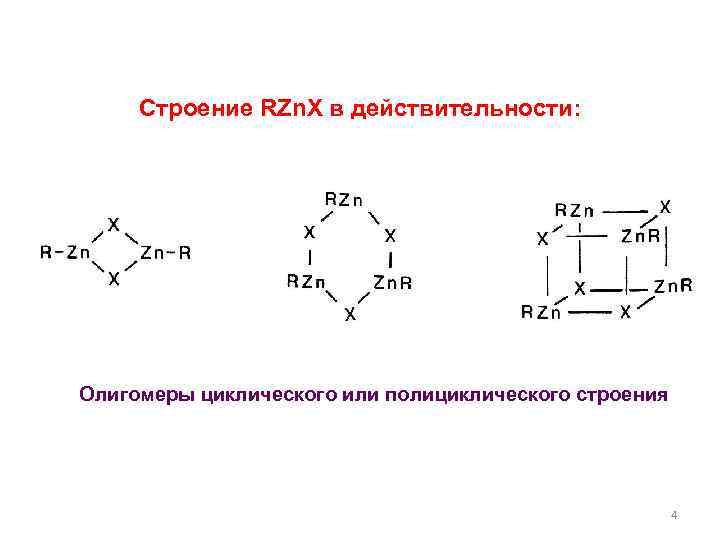 Строение RZn. X в действительности: Олигомеры циклического или полициклического строения 4
Строение RZn. X в действительности: Олигомеры циклического или полициклического строения 4
 Zn-органические соединения Строение 5
Zn-органические соединения Строение 5
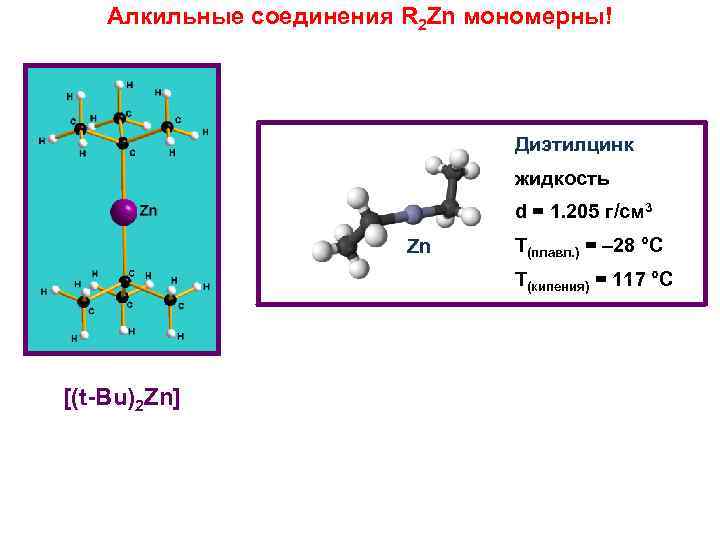 Алкильные соединения R 2 Zn мономерны! Диэтилцинк жидкость d = 1. 205 г/см 3 Zn Т(плавл. ) = – 28 °C Т(кипения) = 117 °C [(t-Bu)2 Zn]
Алкильные соединения R 2 Zn мономерны! Диэтилцинк жидкость d = 1. 205 г/см 3 Zn Т(плавл. ) = – 28 °C Т(кипения) = 117 °C [(t-Bu)2 Zn]
![Комплексы [R 2 Zn(L)n] [Et 2 Zn(TMEDA)] 7 Комплексы [R 2 Zn(L)n] [Et 2 Zn(TMEDA)] 7](https://present5.com/presentation/5652994_177566283/image-7.jpg) Комплексы [R 2 Zn(L)n] [Et 2 Zn(TMEDA)] 7
Комплексы [R 2 Zn(L)n] [Et 2 Zn(TMEDA)] 7
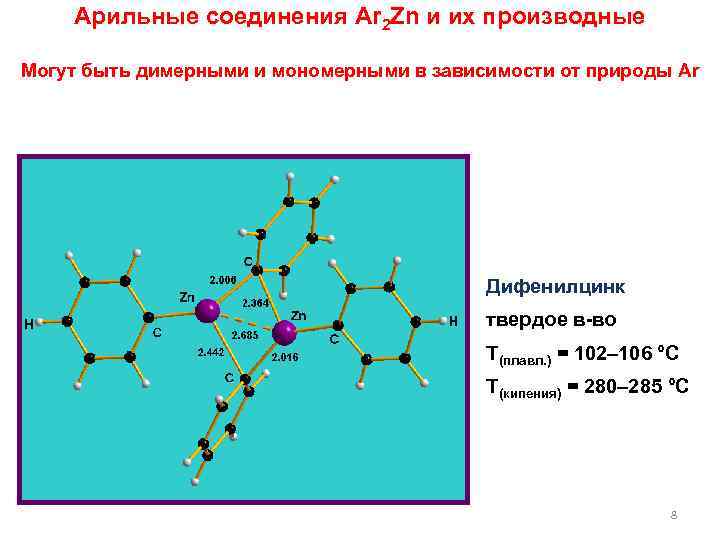 Арильные соединения Ar 2 Zn и их производные Могут быть димерными и мономерными в зависимости от природы Ar Дифенилцинк твердое в-во Т(плавл. ) = 102– 106 °C Т(кипения) = 280– 285 °C 8
Арильные соединения Ar 2 Zn и их производные Могут быть димерными и мономерными в зависимости от природы Ar Дифенилцинк твердое в-во Т(плавл. ) = 102– 106 °C Т(кипения) = 280– 285 °C 8
![Арильные соединения Ar 2 Zn и их производные [Ph 2 Zn(Py)2] [Ph 2 Zn(18 Арильные соединения Ar 2 Zn и их производные [Ph 2 Zn(Py)2] [Ph 2 Zn(18](https://present5.com/presentation/5652994_177566283/image-9.jpg) Арильные соединения Ar 2 Zn и их производные [Ph 2 Zn(Py)2] [Ph 2 Zn(18 -crown-6)] 9
Арильные соединения Ar 2 Zn и их производные [Ph 2 Zn(Py)2] [Ph 2 Zn(18 -crown-6)] 9
![Сэндвичевые соединения 1 -Cp 5 -Cp [Cp 2 Be] = [( 5 -Cp)( 1 Сэндвичевые соединения 1 -Cp 5 -Cp [Cp 2 Be] = [( 5 -Cp)( 1](https://present5.com/presentation/5652994_177566283/image-10.jpg) Сэндвичевые соединения 1 -Cp 5 -Cp [Cp 2 Be] = [( 5 -Cp)( 1 -Cp)Be] Число валентных электронов: 5 e(Cp) + 1 e(Cp) + 2 e(Be) = 8 e 10
Сэндвичевые соединения 1 -Cp 5 -Cp [Cp 2 Be] = [( 5 -Cp)( 1 -Cp)Be] Число валентных электронов: 5 e(Cp) + 1 e(Cp) + 2 e(Be) = 8 e 10
![Сэндвичевые соединения 2. 09 Å 1. 93 Å [Cp*2 Zn] = [( 5 -Cp*)( Сэндвичевые соединения 2. 09 Å 1. 93 Å [Cp*2 Zn] = [( 5 -Cp*)(](https://present5.com/presentation/5652994_177566283/image-11.jpg) Сэндвичевые соединения 2. 09 Å 1. 93 Å [Cp*2 Zn] = [( 5 -Cp*)( 1 -Cp*)Zn] Число валентных электронов: 5 e(Cp*) + 12 e(Zn) = 18 e 11
Сэндвичевые соединения 2. 09 Å 1. 93 Å [Cp*2 Zn] = [( 5 -Cp*)( 1 -Cp*)Zn] Число валентных электронов: 5 e(Cp*) + 12 e(Zn) = 18 e 11
![Полусэндвичевые соединения [Cp. Be. Me]: 1. 71 Å 1. 50 Å Аналогично для цинка, Полусэндвичевые соединения [Cp. Be. Me]: 1. 71 Å 1. 50 Å Аналогично для цинка,](https://present5.com/presentation/5652994_177566283/image-12.jpg) Полусэндвичевые соединения [Cp. Be. Me]: 1. 71 Å 1. 50 Å Аналогично для цинка, [Cp*Zn. Me]: 1. 90 Å 1. 93 Å 12
Полусэндвичевые соединения [Cp. Be. Me]: 1. 71 Å 1. 50 Å Аналогично для цинка, [Cp*Zn. Me]: 1. 90 Å 1. 93 Å 12
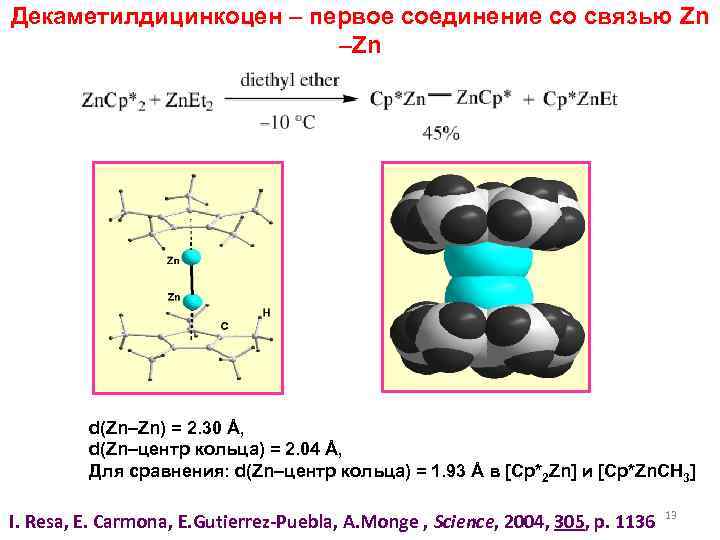 Декаметилдицинкоцен – первое соединение со связью Zn –Zn d(Zn–Zn) = 2. 30 Å, d(Zn–центр кольца) = 2. 04 Å, Для сравнения: d(Zn–центр кольца) = 1. 93 Å в [Cp*2 Zn] и [Cp*Zn. CH 3] I. Resa, E. Carmona, E. Gutierrez-Puebla, A. Monge , Science, 2004, 305, p. 1136 13
Декаметилдицинкоцен – первое соединение со связью Zn –Zn d(Zn–Zn) = 2. 30 Å, d(Zn–центр кольца) = 2. 04 Å, Для сравнения: d(Zn–центр кольца) = 1. 93 Å в [Cp*2 Zn] и [Cp*Zn. CH 3] I. Resa, E. Carmona, E. Gutierrez-Puebla, A. Monge , Science, 2004, 305, p. 1136 13
 Zn-органические соединения Реакции соединений Zn(II) 14
Zn-органические соединения Реакции соединений Zn(II) 14
 «Мягкое» замещение галогенов В отличие от литий- и магнийорганики реакция протекает «чисто» , не приводит к смеси продуктов разной степени замещения галогенов 16
«Мягкое» замещение галогенов В отличие от литий- и магнийорганики реакция протекает «чисто» , не приводит к смеси продуктов разной степени замещения галогенов 16
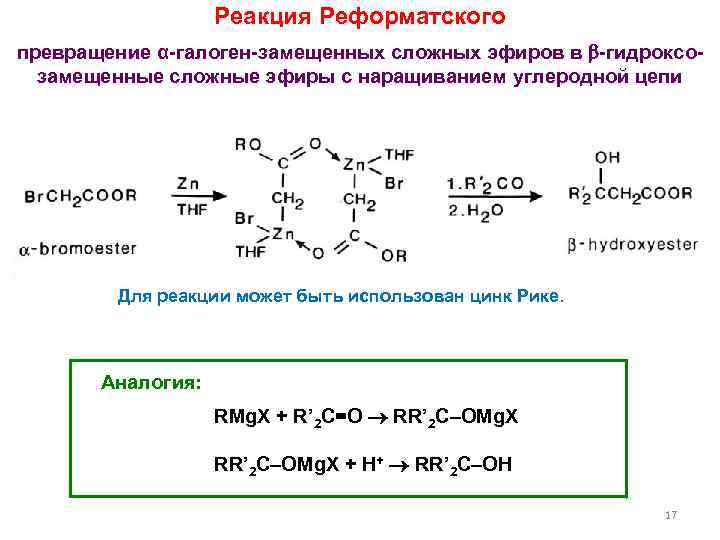 Реакция Реформатского превращение α-галоген-замещенных сложных эфиров в -гидроксозамещенные сложные эфиры с наращиванием углеродной цепи Для реакции может быть использован цинк Рике. Аналогия: RMg. X + R’ 2 C=O RR’ 2 C–OMg. X + H+ RR’ 2 C–OH 17
Реакция Реформатского превращение α-галоген-замещенных сложных эфиров в -гидроксозамещенные сложные эфиры с наращиванием углеродной цепи Для реакции может быть использован цинк Рике. Аналогия: RMg. X + R’ 2 C=O RR’ 2 C–OMg. X + H+ RR’ 2 C–OH 17
 Наращивание сложного углеродного скелета для ряда функционализованных органических соединений Метод Кнохеля (Knochel ) Преимущества цинкорганических соединений: могут быть получены с очень большим набором функциональных групп! Соль [Cu. CN 2 Li. X] может быть использована в каталитических кол-вах. [Cu. CN 2 Li. X], в отличие от Cu. CN, прилично растворяется в ТГФ. Строение FGR–Cu(CN)Zn. X 2 Li. X не установлено, но методика работает. 18
Наращивание сложного углеродного скелета для ряда функционализованных органических соединений Метод Кнохеля (Knochel ) Преимущества цинкорганических соединений: могут быть получены с очень большим набором функциональных групп! Соль [Cu. CN 2 Li. X] может быть использована в каталитических кол-вах. [Cu. CN 2 Li. X], в отличие от Cu. CN, прилично растворяется в ТГФ. Строение FGR–Cu(CN)Zn. X 2 Li. X не установлено, но методика работает. 18
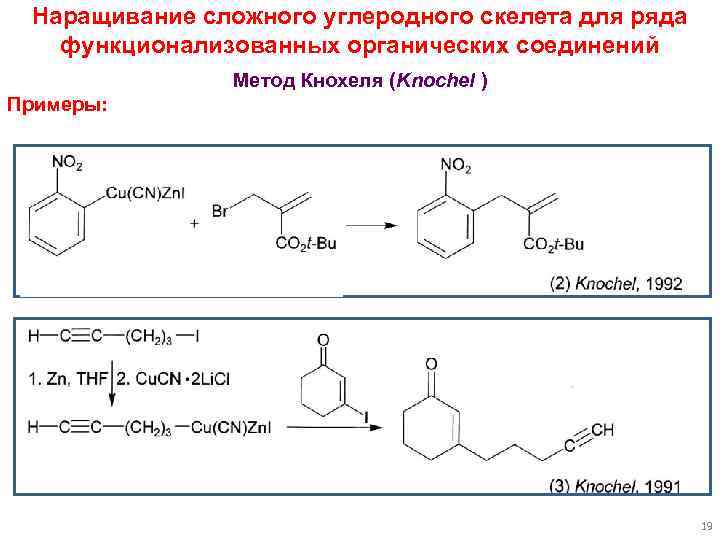 Наращивание сложного углеродного скелета для ряда функционализованных органических соединений Метод Кнохеля (Knochel ) Примеры: 19
Наращивание сложного углеродного скелета для ряда функционализованных органических соединений Метод Кнохеля (Knochel ) Примеры: 19
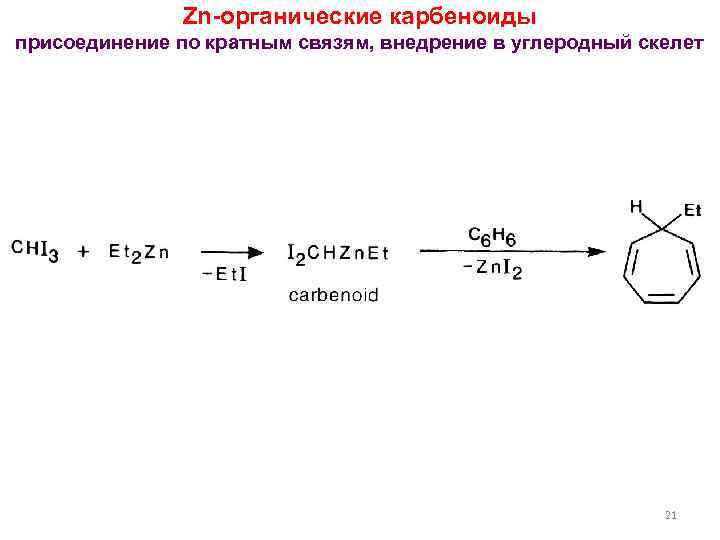 Zn-органические карбеноиды присоединение по кратным связям, внедрение в углеродный скелет 21
Zn-органические карбеноиды присоединение по кратным связям, внедрение в углеродный скелет 21
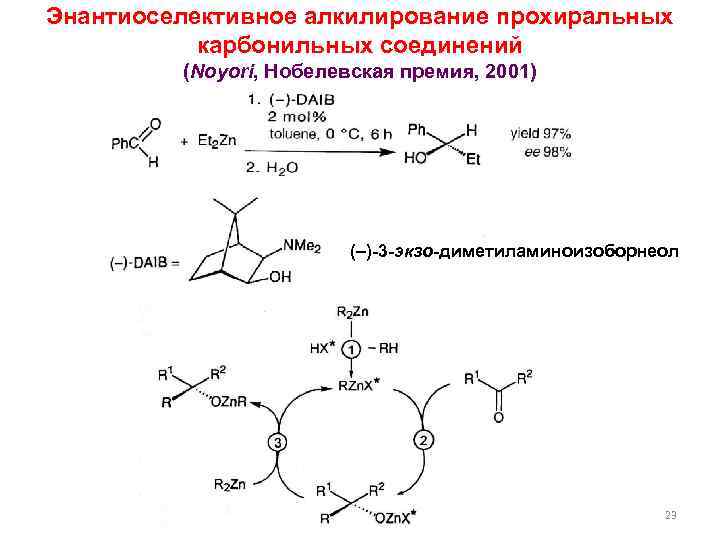 Энантиоселективное алкилирование прохиральных карбонильных соединений (Noyori, Нобелевская премия, 2001) ( )-3 -экзо-диметиламиноизоборнеол 23
Энантиоселективное алкилирование прохиральных карбонильных соединений (Noyori, Нобелевская премия, 2001) ( )-3 -экзо-диметиламиноизоборнеол 23
 Zn-органические соединения Реакции соединений Zn(I) 24
Zn-органические соединения Реакции соединений Zn(I) 24
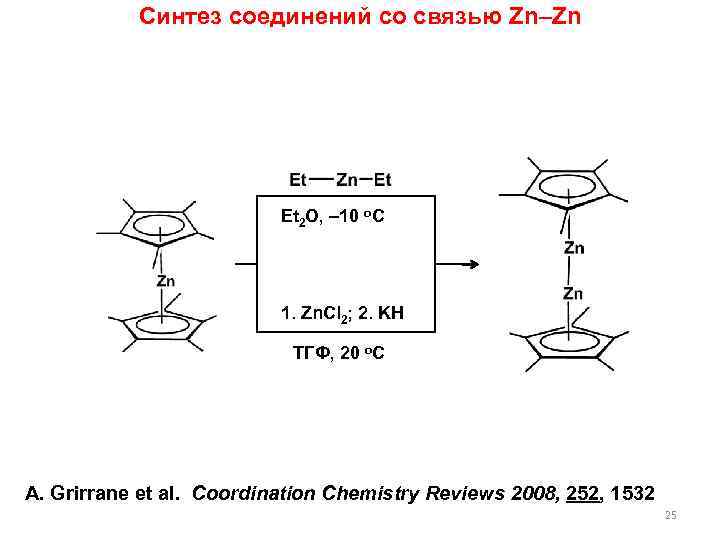 Синтез соединений со связью Zn–Zn Et 2 O, 10 o. C 1. Zn. Cl 2; 2. KH ТГФ, 20 o. C A. Grirrane et al. Coordination Chemistry Reviews 2008, 252, 1532 25
Синтез соединений со связью Zn–Zn Et 2 O, 10 o. C 1. Zn. Cl 2; 2. KH ТГФ, 20 o. C A. Grirrane et al. Coordination Chemistry Reviews 2008, 252, 1532 25
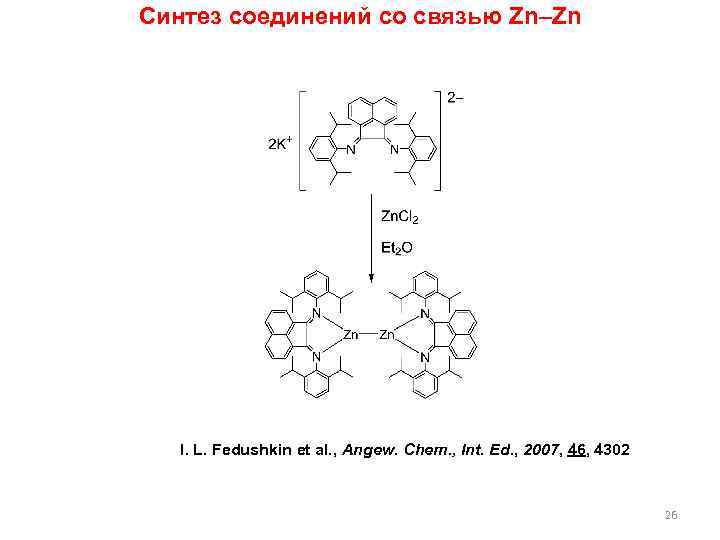 Синтез соединений со связью Zn–Zn I. L. Fedushkin et al. , Angew. Chem. , Int. Ed. , 2007, 46, 4302 26
Синтез соединений со связью Zn–Zn I. L. Fedushkin et al. , Angew. Chem. , Int. Ed. , 2007, 46, 4302 26
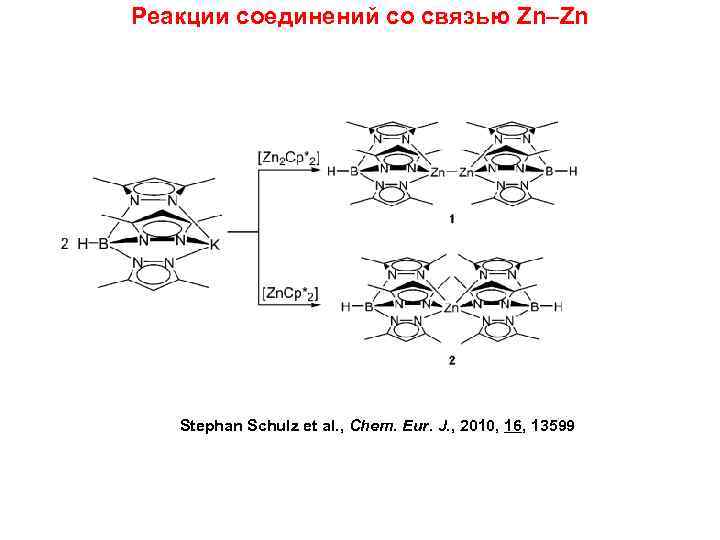 Реакции соединений со связью Zn–Zn Stephan Schulz et al. , Chem. Eur. J. , 2010, 16, 13599
Реакции соединений со связью Zn–Zn Stephan Schulz et al. , Chem. Eur. J. , 2010, 16, 13599
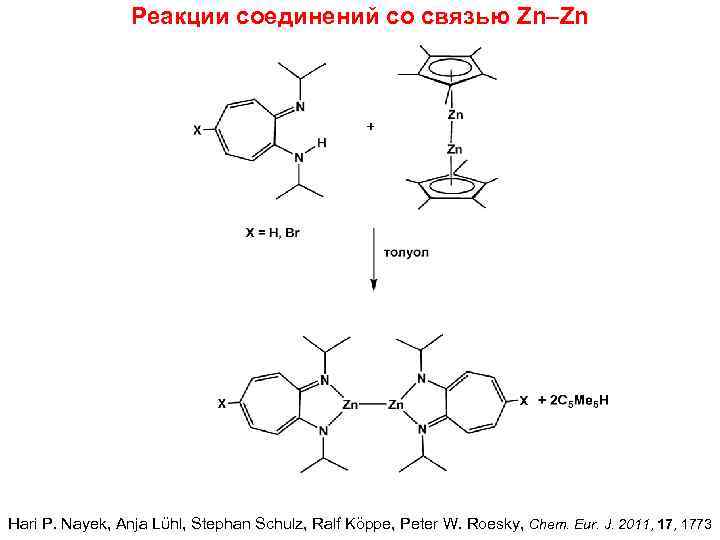 Реакции соединений со связью Zn–Zn Hari P. Nayek, Anja Lϋhl, Stephan Schulz, Ralf Köppe, Peter W. Roesky, Chem. Eur. J. 2011, 1773
Реакции соединений со связью Zn–Zn Hari P. Nayek, Anja Lϋhl, Stephan Schulz, Ralf Köppe, Peter W. Roesky, Chem. Eur. J. 2011, 1773
![The Rich Chemistry of [Zn 2 Cp*2]: Trapping Three Different Types of Zinc Ligands The Rich Chemistry of [Zn 2 Cp*2]: Trapping Three Different Types of Zinc Ligands](https://present5.com/presentation/5652994_177566283/image-26.jpg) The Rich Chemistry of [Zn 2 Cp*2]: Trapping Three Different Types of Zinc Ligands in the Pd. Zn 7 Complex [Pd(Zn. Cp*)4(Zn. Me)2{Zn(tmeda)}] Gernot Frenking and Roland A. Fischer et al. , Inorg. chem. 2011, 50, 10486 (2)
The Rich Chemistry of [Zn 2 Cp*2]: Trapping Three Different Types of Zinc Ligands in the Pd. Zn 7 Complex [Pd(Zn. Cp*)4(Zn. Me)2{Zn(tmeda)}] Gernot Frenking and Roland A. Fischer et al. , Inorg. chem. 2011, 50, 10486 (2)
![The Reactivity of [Zn 2 Cp*2]: Trapping Monovalent {∙Zn. Cp*} in the Metal-Rich Compounds The Reactivity of [Zn 2 Cp*2]: Trapping Monovalent {∙Zn. Cp*} in the Metal-Rich Compounds](https://present5.com/presentation/5652994_177566283/image-27.jpg) The Reactivity of [Zn 2 Cp*2]: Trapping Monovalent {∙Zn. Cp*} in the Metal-Rich Compounds [(Pd, Pt)(Ga. Cp*)a(Zn. Cp*)4 -a(Zn. Cp*)4 -a] (a=0, 2) Gernot Frenking and Roland A. Fischer at al. , Angew. Chem. Int. Ed. 2011, 50, 772 (1)
The Reactivity of [Zn 2 Cp*2]: Trapping Monovalent {∙Zn. Cp*} in the Metal-Rich Compounds [(Pd, Pt)(Ga. Cp*)a(Zn. Cp*)4 -a(Zn. Cp*)4 -a] (a=0, 2) Gernot Frenking and Roland A. Fischer at al. , Angew. Chem. Int. Ed. 2011, 50, 772 (1)
 Hg-органические соединения Синтез, строение и свойства 31
Hg-органические соединения Синтез, строение и свойства 31
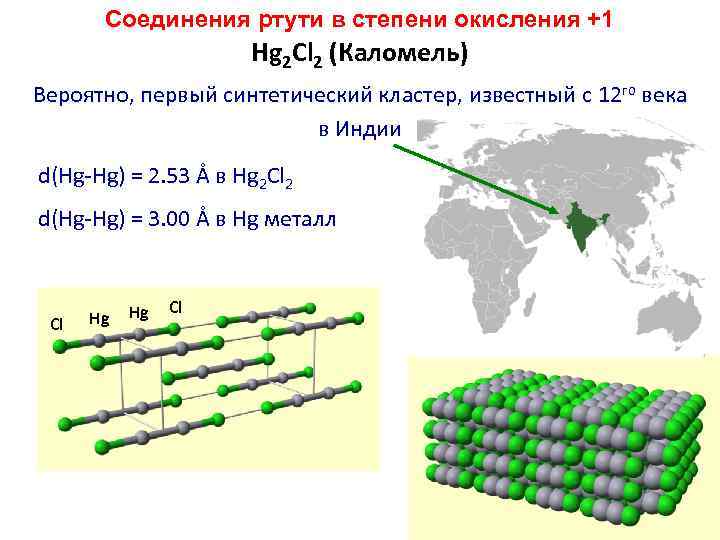 Соединения ртути в степени окисления +1 Hg 2 Cl 2 (Каломель) Вероятно, первый синтетический кластер, известный с 12 го века в Индии d(Hg-Hg) = 2. 53 Å в Hg 2 Cl 2 d(Hg-Hg) = 3. 00 Å в Hg металл Cl Hg Hg Cl
Соединения ртути в степени окисления +1 Hg 2 Cl 2 (Каломель) Вероятно, первый синтетический кластер, известный с 12 го века в Индии d(Hg-Hg) = 2. 53 Å в Hg 2 Cl 2 d(Hg-Hg) = 3. 00 Å в Hg металл Cl Hg Hg Cl
 Металлоорганические соединения ртути в степени окисления +1 По сути, отсутстствуют! Соединение типа R–Hg–Hg–R надежно охарактеризовано только одно: R = Si(Si. Me 2 Si. Me 3)3 (Apeloig, 1999) 33
Металлоорганические соединения ртути в степени окисления +1 По сути, отсутстствуют! Соединение типа R–Hg–Hg–R надежно охарактеризовано только одно: R = Si(Si. Me 2 Si. Me 3)3 (Apeloig, 1999) 33
![Металлоорганические соединения ртути в степени окисления +2 [1 а] солнечный свет (история) [1 б] Металлоорганические соединения ртути в степени окисления +2 [1 а] солнечный свет (история) [1 б]](https://present5.com/presentation/5652994_177566283/image-31.jpg) Металлоорганические соединения ртути в степени окисления +2 [1 а] солнечный свет (история) [1 б] 2 Na + Hg + 2 CH 3 Br (CH 3)2 Hg + 2 Na. Br [12] [4] 34
Металлоорганические соединения ртути в степени окисления +2 [1 а] солнечный свет (история) [1 б] 2 Na + Hg + 2 CH 3 Br (CH 3)2 Hg + 2 Na. Br [12] [4] 34
![Металлоорганические соединения ртути в степени окисления +2 [7] [10] [11] [электроалкилирование] 35 Металлоорганические соединения ртути в степени окисления +2 [7] [10] [11] [электроалкилирование] 35](https://present5.com/presentation/5652994_177566283/image-32.jpg) Металлоорганические соединения ртути в степени окисления +2 [7] [10] [11] [электроалкилирование] 35
Металлоорганические соединения ртути в степени окисления +2 [7] [10] [11] [электроалкилирование] 35
 Свойства связи Hg–C, общие свойства R 2 Hg и RHg. X Связь Hg–C практически неполярна. Соединения R 2 Hg и RHg. X абсолютно устойчивы к воде и кислороду воздуха. Легкость восстановления Hg(II) до Hg(0) обеспечивает легкость трансметаллирования. 36
Свойства связи Hg–C, общие свойства R 2 Hg и RHg. X Связь Hg–C практически неполярна. Соединения R 2 Hg и RHg. X абсолютно устойчивы к воде и кислороду воздуха. Легкость восстановления Hg(II) до Hg(0) обеспечивает легкость трансметаллирования. 36
 Металлоорганические соединения ртути в степени окисления +2 (CH 3)2 Hg CH 3 Hg + CH 3 (CH 3)Hg Hg + CH 3 D 1(Hg – C) = 214 к. Дж/моль D 2(Hg – C) = 29 к. Дж/моль Применение: генерация свободных углеводородных радикалов 37
Металлоорганические соединения ртути в степени окисления +2 (CH 3)2 Hg CH 3 Hg + CH 3 (CH 3)Hg Hg + CH 3 D 1(Hg – C) = 214 к. Дж/моль D 2(Hg – C) = 29 к. Дж/моль Применение: генерация свободных углеводородных радикалов 37
 Свойства связи Hg–C, общие свойства R 2 Hg и RHg. X В R 2 Hg у ртути практически отсутствуют свойства кислоты Льюиса: известны комплексы с дополнительными лигандами только для R = сильный акцептор (CF 3, например) [(CF 3)2 Hg(dppe)] (dppe = Ph 2 PCH 2 PPh 2) Координация лигандов к атому ртути в RHg. X приводит к «диспропорционированию» : 38
Свойства связи Hg–C, общие свойства R 2 Hg и RHg. X В R 2 Hg у ртути практически отсутствуют свойства кислоты Льюиса: известны комплексы с дополнительными лигандами только для R = сильный акцептор (CF 3, например) [(CF 3)2 Hg(dppe)] (dppe = Ph 2 PCH 2 PPh 2) Координация лигандов к атому ртути в RHg. X приводит к «диспропорционированию» : 38
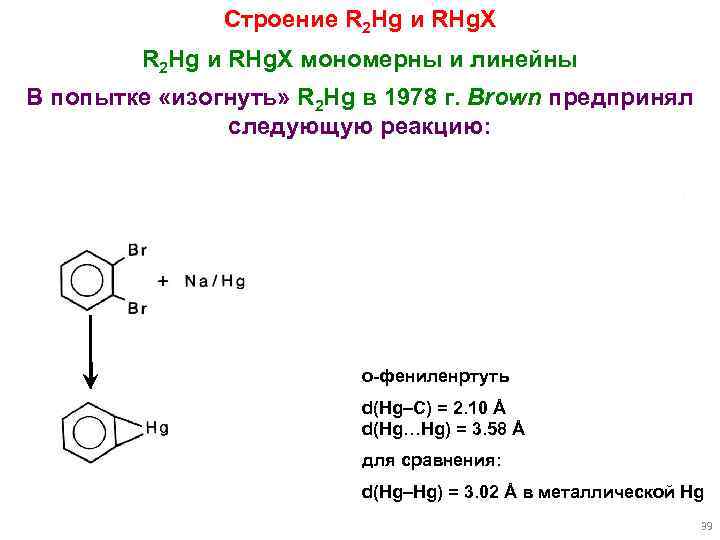 Строение R 2 Hg и RHg. X мономерны и линейны В попытке «изогнуть» R 2 Hg в 1978 г. Brown предпринял следующую реакцию: о-фениленртуть d(Hg–C) = 2. 10 Å d(Hg…Hg) = 3. 58 Å для сравнения: d(Hg–Hg) = 3. 02 Å в металлической Hg 39
Строение R 2 Hg и RHg. X мономерны и линейны В попытке «изогнуть» R 2 Hg в 1978 г. Brown предпринял следующую реакцию: о-фениленртуть d(Hg–C) = 2. 10 Å d(Hg…Hg) = 3. 58 Å для сравнения: d(Hg–Hg) = 3. 02 Å в металлической Hg 39
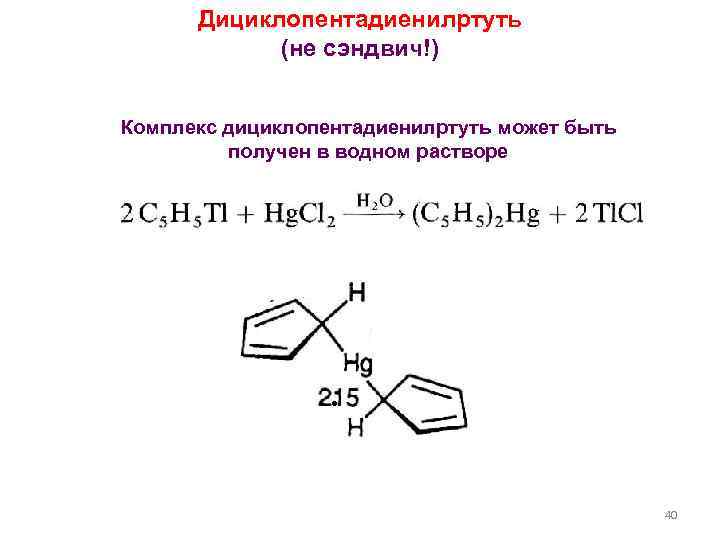 Дициклопентадиенилртуть (не сэндвич!) Комплекс дициклопентадиенилртуть может быть получен в водном растворе . 40
Дициклопентадиенилртуть (не сэндвич!) Комплекс дициклопентадиенилртуть может быть получен в водном растворе . 40
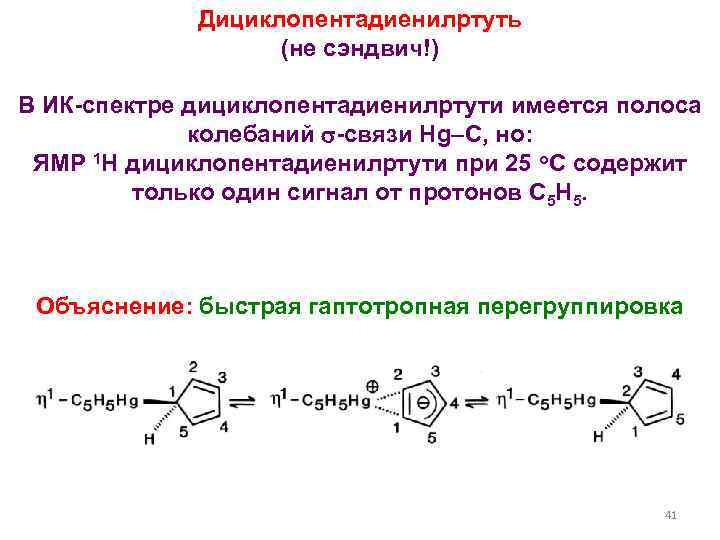 Дициклопентадиенилртуть (не сэндвич!) В ИК-спектре дициклопентадиенилртути имеется полоса колебаний -связи Hg–C, но: ЯМР 1 H дициклопентадиенилртути при 25 о. С содержит только один сигнал от протонов C 5 H 5. Объяснение: быстрая гаптотропная перегруппировка 41
Дициклопентадиенилртуть (не сэндвич!) В ИК-спектре дициклопентадиенилртути имеется полоса колебаний -связи Hg–C, но: ЯМР 1 H дициклопентадиенилртути при 25 о. С содержит только один сигнал от протонов C 5 H 5. Объяснение: быстрая гаптотропная перегруппировка 41
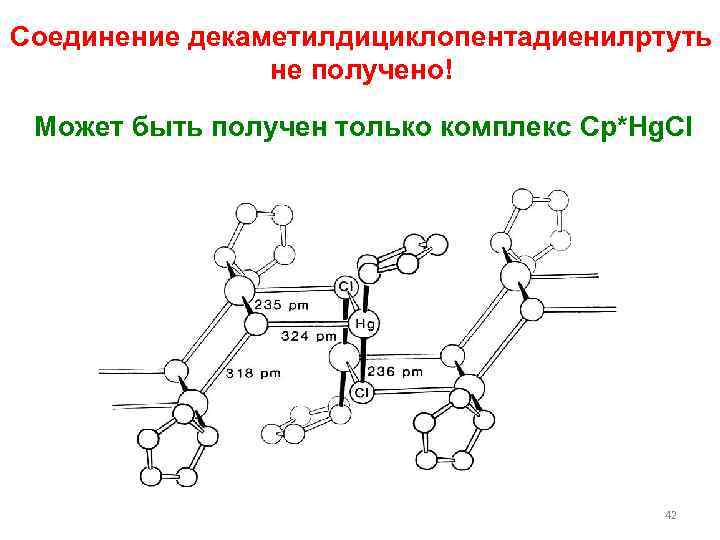 Соединение декаметилдициклопентадиенилртуть не получено! Может быть получен только комплекс Cp*Hg. Cl 42
Соединение декаметилдициклопентадиенилртуть не получено! Может быть получен только комплекс Cp*Hg. Cl 42
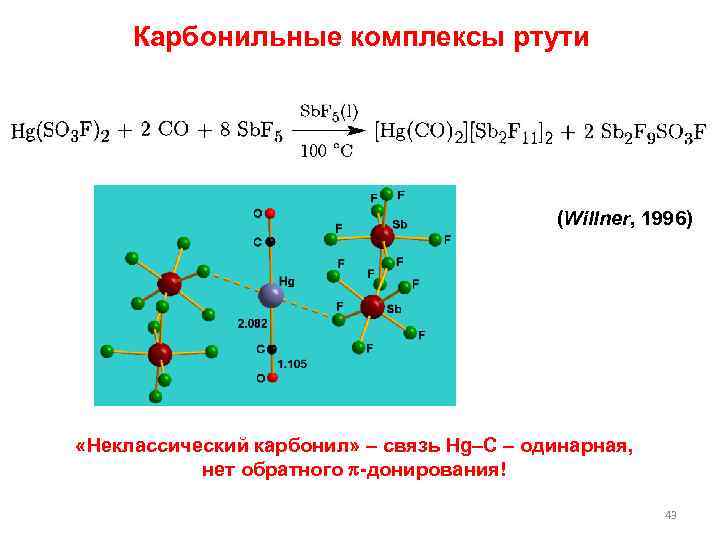 Карбонильные комплексы ртути (Willner, 1996) «Неклассический карбонил» – связь Hg–C – одинарная, нет обратного -донирования! 43
Карбонильные комплексы ртути (Willner, 1996) «Неклассический карбонил» – связь Hg–C – одинарная, нет обратного -донирования! 43
![Немного подробнее о меркурировании Электрофильное замещение H+ на [Hg(OAc)]+ кроме аренов могут реагировать алкины, Немного подробнее о меркурировании Электрофильное замещение H+ на [Hg(OAc)]+ кроме аренов могут реагировать алкины,](https://present5.com/presentation/5652994_177566283/image-41.jpg) Немного подробнее о меркурировании Электрофильное замещение H+ на [Hg(OAc)]+ кроме аренов могут реагировать алкины, нитроалканы, 1, 3 -дикетоны т. е. соединения с достаточной C–H кислотностью Катализ хлорной кислотой: 44
Немного подробнее о меркурировании Электрофильное замещение H+ на [Hg(OAc)]+ кроме аренов могут реагировать алкины, нитроалканы, 1, 3 -дикетоны т. е. соединения с достаточной C–H кислотностью Катализ хлорной кислотой: 44
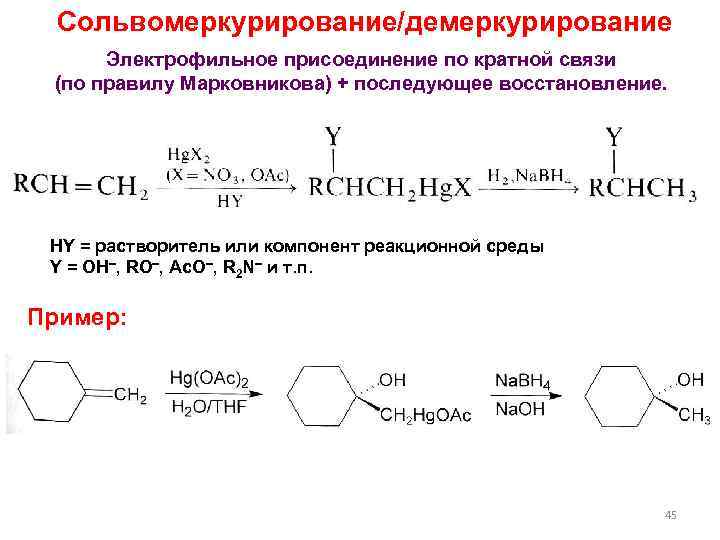 Сольвомеркурирование/демеркурирование Электрофильное присоединение по кратной связи (по правилу Марковникова) + последующее восстановление. HY = растворитель или компонент реакционной среды Y = OH , RO , Ac. O , R 2 N и т. п. Пример: 45
Сольвомеркурирование/демеркурирование Электрофильное присоединение по кратной связи (по правилу Марковникова) + последующее восстановление. HY = растворитель или компонент реакционной среды Y = OH , RO , Ac. O , R 2 N и т. п. Пример: 45
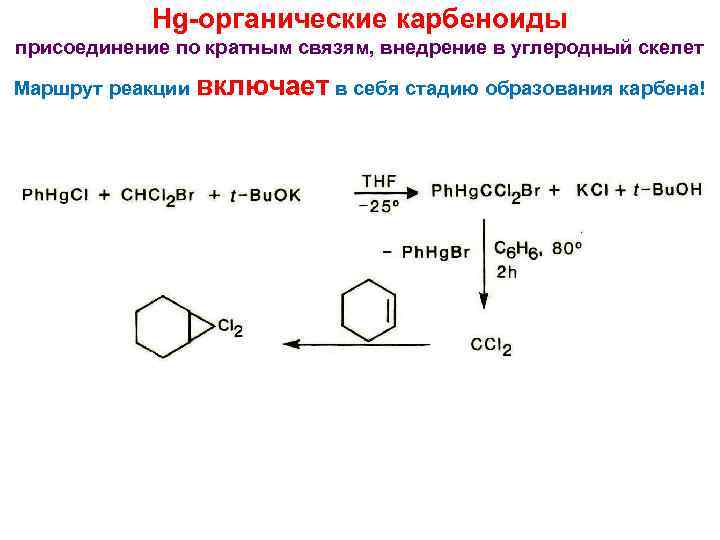 Hg-органические карбеноиды присоединение по кратным связям, внедрение в углеродный скелет Маршрут реакции включает в себя стадию образования карбена!
Hg-органические карбеноиды присоединение по кратным связям, внедрение в углеродный скелет Маршрут реакции включает в себя стадию образования карбена!
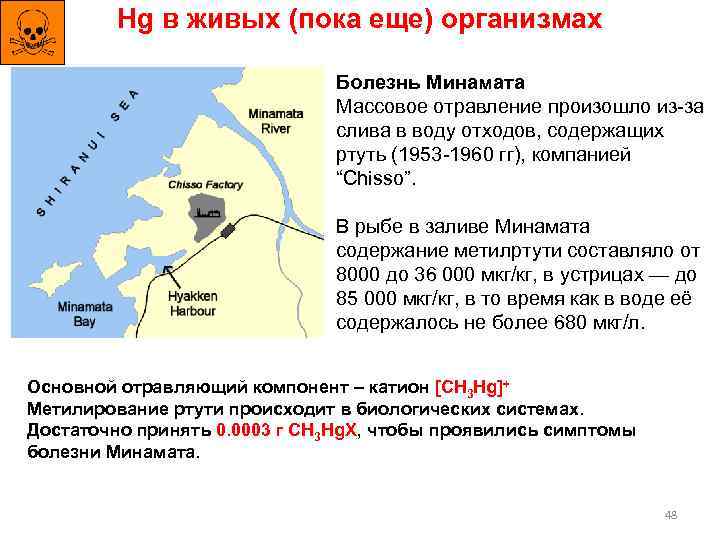 Hg в живых (пока еще) организмах Болезнь Минамата Массовое отравление произошло из-за слива в воду отходов, содержащих ртуть (1953 -1960 гг), компанией “Chisso”. В рыбе в заливе Минамата содержание метилртути составляло от 8000 до 36 000 мкг/кг, в устрицах — до 85 000 мкг/кг, в то время как в воде её содержалось не более 680 мкг/л. Основной отравляющий компонент – катион [CH 3 Hg]+ Метилирование ртути происходит в биологических системах. Достаточно принять 0. 0003 г CH 3 Hg. X, чтобы проявились симптомы болезни Минамата. 48
Hg в живых (пока еще) организмах Болезнь Минамата Массовое отравление произошло из-за слива в воду отходов, содержащих ртуть (1953 -1960 гг), компанией “Chisso”. В рыбе в заливе Минамата содержание метилртути составляло от 8000 до 36 000 мкг/кг, в устрицах — до 85 000 мкг/кг, в то время как в воде её содержалось не более 680 мкг/л. Основной отравляющий компонент – катион [CH 3 Hg]+ Метилирование ртути происходит в биологических системах. Достаточно принять 0. 0003 г CH 3 Hg. X, чтобы проявились симптомы болезни Минамата. 48
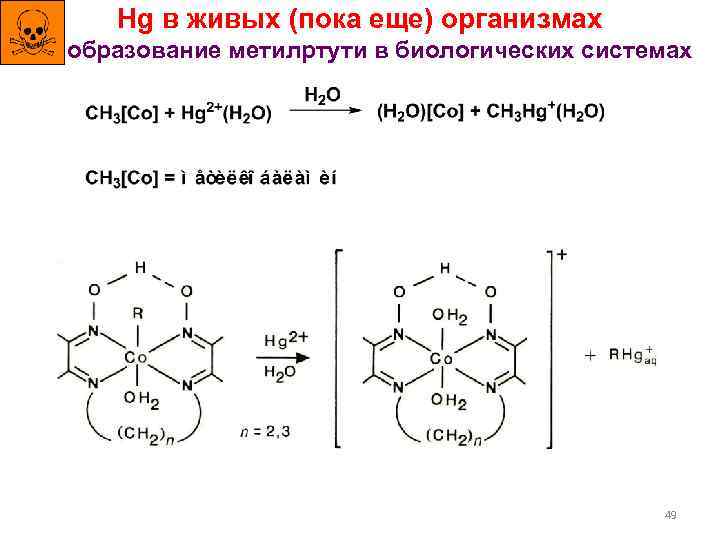 Hg в живых (пока еще) организмах образование метилртути в биологических системах 49
Hg в живых (пока еще) организмах образование метилртути в биологических системах 49
 Hg в живых (пока еще) организмах проникновение ртути в биологическую систему 50
Hg в живых (пока еще) организмах проникновение ртути в биологическую систему 50
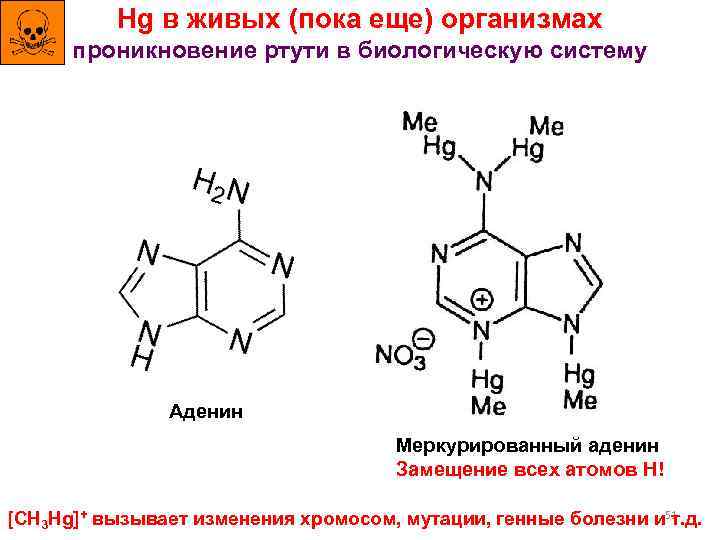 Hg в живых (пока еще) организмах проникновение ртути в биологическую систему Аденин Меркурированный аденин Замещение всех атомов H! [CH 3 Hg]+ вызывает изменения хромосом, мутации, генные болезни и 51 т. д.
Hg в живых (пока еще) организмах проникновение ртути в биологическую систему Аденин Меркурированный аденин Замещение всех атомов H! [CH 3 Hg]+ вызывает изменения хромосом, мутации, генные болезни и 51 т. д.
 Hg в живых (пока еще) организмах Диметилртуть Hg(CH 3)2 В 1997 году зафиксирован случай, когда после попадания нескольких капель Me 2 Hg на руки исследователя, он внезапно умер через 10 месяцев! Me 2 Hg проникает сквозь латексные перчатки! При попадании Me 2 Hg на перчатки, до кожи она добирается в течение нескольких секунд! Если кто-то по соседству начнет заниматься ртутьорганикой, сообщите заранее, чтоб успеть уехать подальше! 52
Hg в живых (пока еще) организмах Диметилртуть Hg(CH 3)2 В 1997 году зафиксирован случай, когда после попадания нескольких капель Me 2 Hg на руки исследователя, он внезапно умер через 10 месяцев! Me 2 Hg проникает сквозь латексные перчатки! При попадании Me 2 Hg на перчатки, до кожи она добирается в течение нескольких секунд! Если кто-то по соседству начнет заниматься ртутьорганикой, сообщите заранее, чтоб успеть уехать подальше! 52


