9-Цинк (51).ppt
- Количество слайдов: 54
 Zn
Zn
 Гидролазы Катализируют расщепление связей путем гидролиза Металлосодержащие гидролазы
Гидролазы Катализируют расщепление связей путем гидролиза Металлосодержащие гидролазы
 Кофакторы некоторых гидролитических ферментов Zn 2+, Ca 2+, Ni 2+, Mg 2+, Na+, K+
Кофакторы некоторых гидролитических ферментов Zn 2+, Ca 2+, Ni 2+, Mg 2+, Na+, K+
 Примеры металлоферментов, которые катализируют реакции гидролиза и другие аналогичные реакции
Примеры металлоферментов, которые катализируют реакции гидролиза и другие аналогичные реакции
 Zn Карбоангидраза Карбоксипептидаза Щелочная фосфатаза
Zn Карбоангидраза Карбоксипептидаза Щелочная фосфатаза
 Металлосодержащие гидролазы : В чем заключается роль металла ? • Связывает и активирует субстрат(ы) • Способствует генерированию нуклеофила Metal Ion Log K None 14. 0 Ca 2+ 13. 4 Mn 2+ 11. 1 Cu 2+ 10. 7 Zn 2+ 10. 0 Кислотность молекулы воды может изменяться при изменении лигандного окружения металла. Большинство моноядерных гидролаз содержат Zn
Металлосодержащие гидролазы : В чем заключается роль металла ? • Связывает и активирует субстрат(ы) • Способствует генерированию нуклеофила Metal Ion Log K None 14. 0 Ca 2+ 13. 4 Mn 2+ 11. 1 Cu 2+ 10. 7 Zn 2+ 10. 0 Кислотность молекулы воды может изменяться при изменении лигандного окружения металла. Большинство моноядерных гидролаз содержат Zn
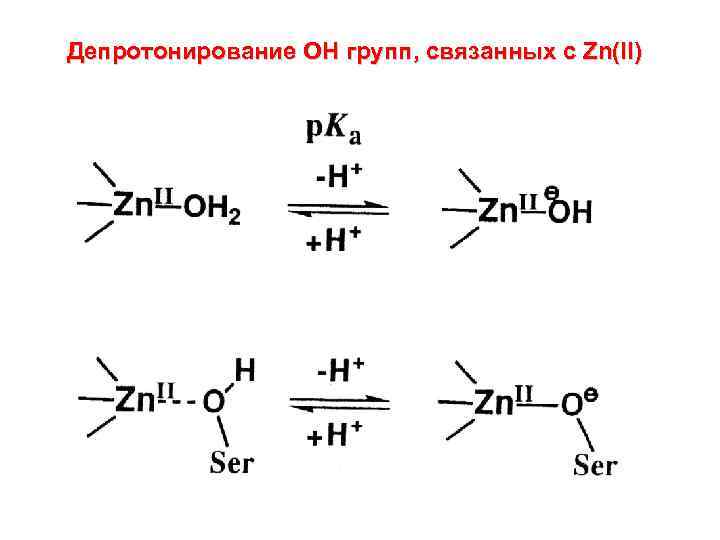 Депротонирование ОН групп, связанных с Zn(II)
Депротонирование ОН групп, связанных с Zn(II)
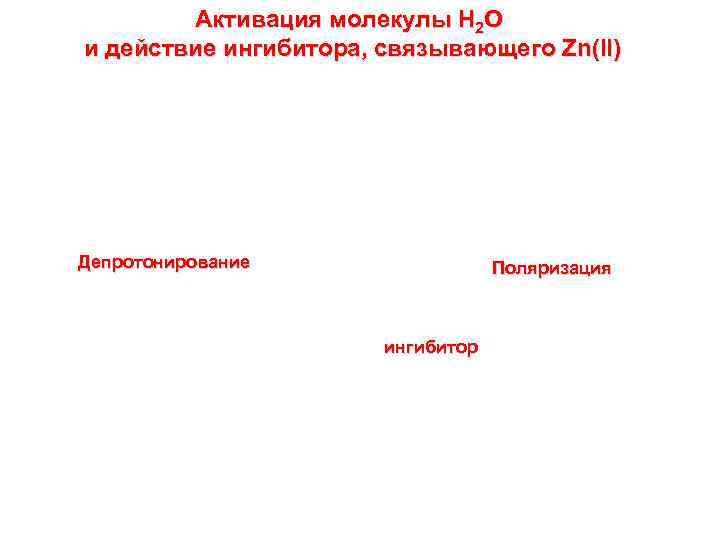 Активация молекулы Н 2 О и действие ингибитора, связывающего Zn(II) Депротонирование Поляризация ингибитор
Активация молекулы Н 2 О и действие ингибитора, связывающего Zn(II) Депротонирование Поляризация ингибитор
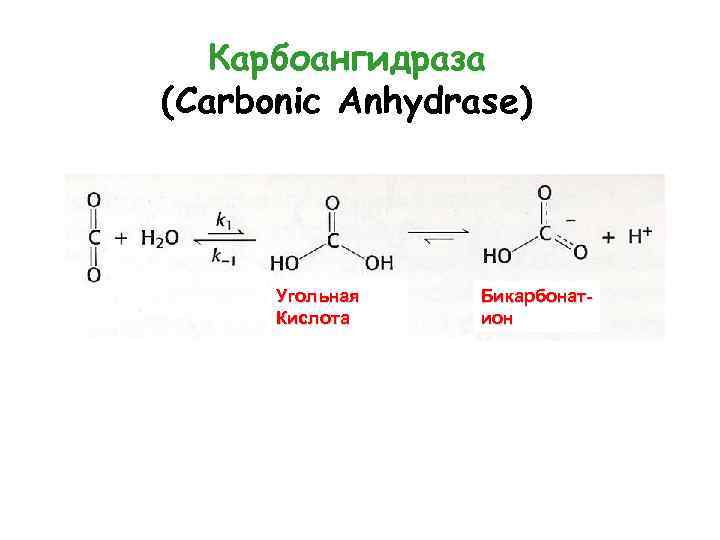 Карбоангидраза (Carbonic Anhydrase) Угольная Кислота Бикарбонатион
Карбоангидраза (Carbonic Anhydrase) Угольная Кислота Бикарбонатион
 Реакции, катализируемые карбоангидразой Константы равновесия Константы скорости Некатализируемой реакции Основание Льюиса Кислота Льюиса
Реакции, катализируемые карбоангидразой Константы равновесия Константы скорости Некатализируемой реакции Основание Льюиса Кислота Льюиса
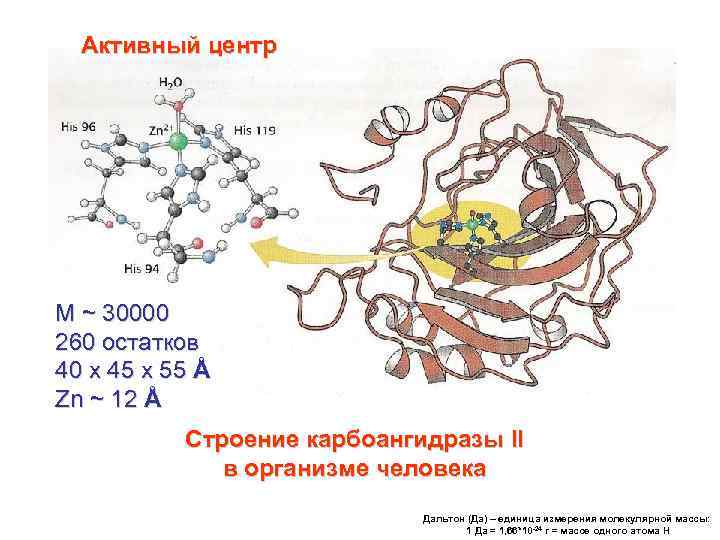 Активный центр M ~ 30000 260 остатков 40 x 45 x 55 Å Zn ~ 12 Å Строение карбоангидразы II в организме человека Дальтон (Да) – единица измерения молекулярной массы: 1 Да = 1, 66*10 -24 г = массе одного атома Н
Активный центр M ~ 30000 260 остатков 40 x 45 x 55 Å Zn ~ 12 Å Строение карбоангидразы II в организме человека Дальтон (Да) – единица измерения молекулярной массы: 1 Да = 1, 66*10 -24 г = массе одного атома Н
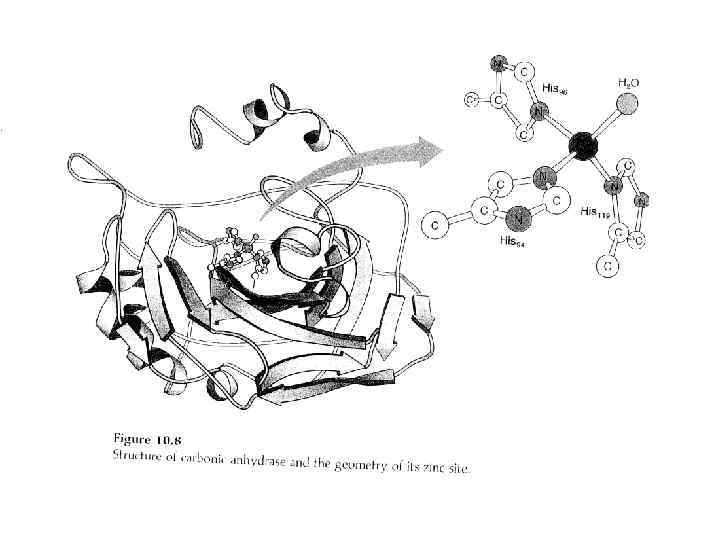
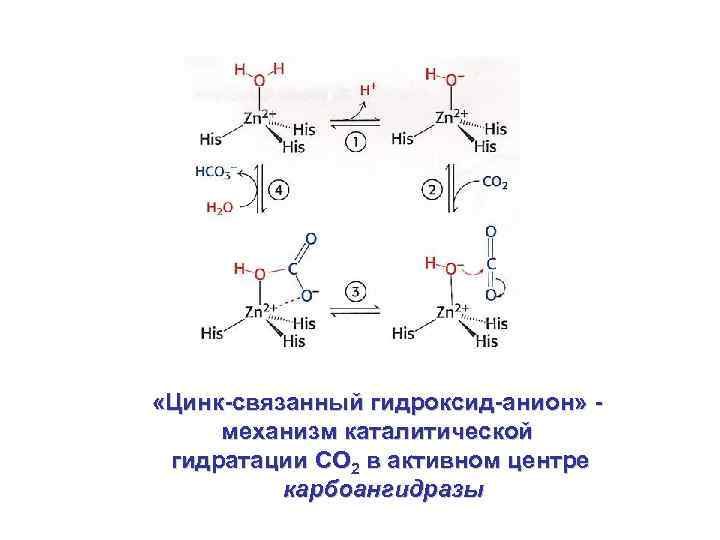 «Цинк-связанный гидроксид-анион» механизм каталитической гидратации CO 2 в активном центре карбоангидразы
«Цинк-связанный гидроксид-анион» механизм каталитической гидратации CO 2 в активном центре карбоангидразы
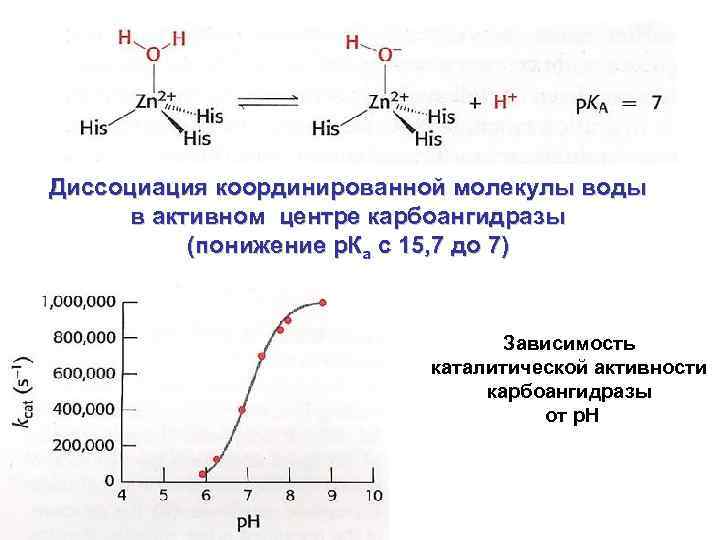 Диссоциация координированной молекулы воды в активном центре карбоангидразы (понижение р. Ка с 15, 7 до 7) Зависимость каталитической активности карбоангидразы от р. Н
Диссоциация координированной молекулы воды в активном центре карбоангидразы (понижение р. Ка с 15, 7 до 7) Зависимость каталитической активности карбоангидразы от р. Н
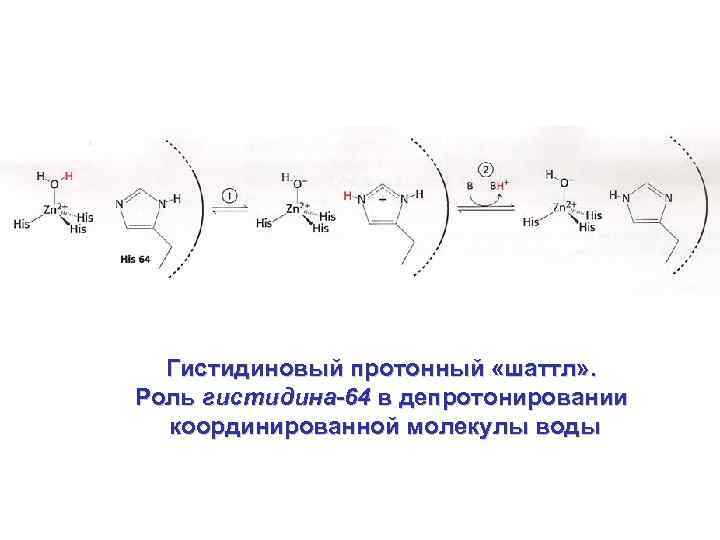 Гистидиновый протонный «шаттл» . Роль гистидина-64 в депротонировании координированной молекулы воды
Гистидиновый протонный «шаттл» . Роль гистидина-64 в депротонировании координированной молекулы воды
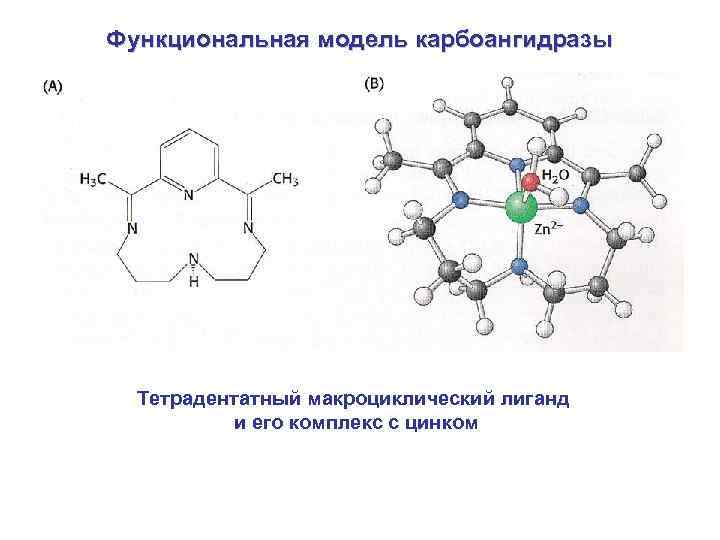 Функциональная модель карбоангидразы Тетрадентатный макроциклический лиганд и его комплекс с цинком
Функциональная модель карбоангидразы Тетрадентатный макроциклический лиганд и его комплекс с цинком
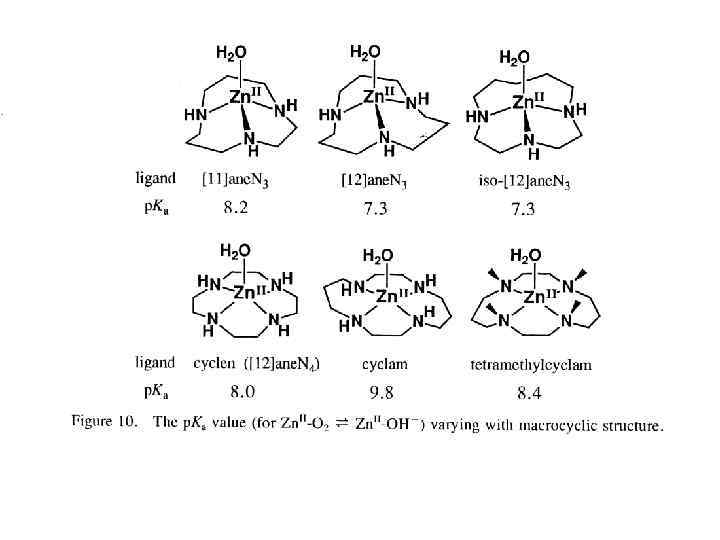
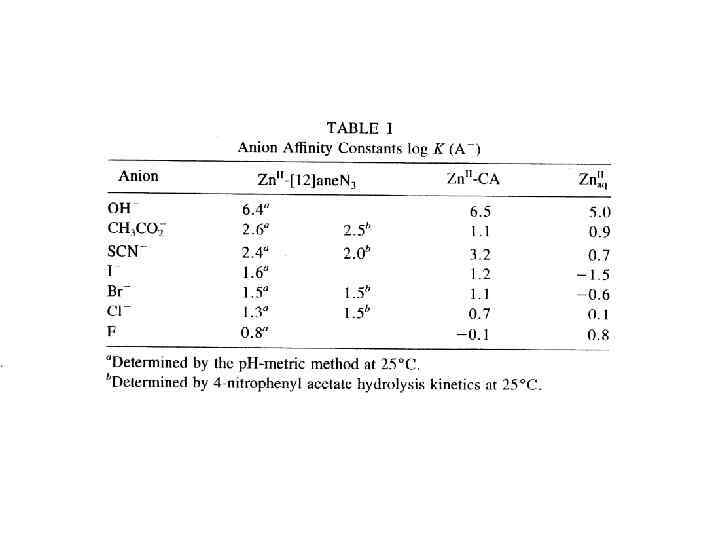
 Константы скорости реакций второго порядка (M-1 s-1) для гидролиза 4 -нитрофенилацетата и значения p. Ka для M-OH 2
Константы скорости реакций второго порядка (M-1 s-1) для гидролиза 4 -нитрофенилацетата и значения p. Ka для M-OH 2
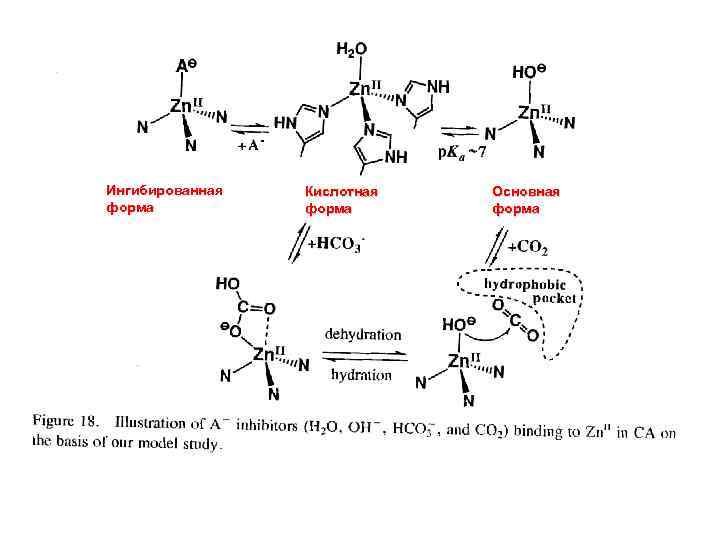 Ингибированная форма Кислотная форма Основная форма
Ингибированная форма Кислотная форма Основная форма
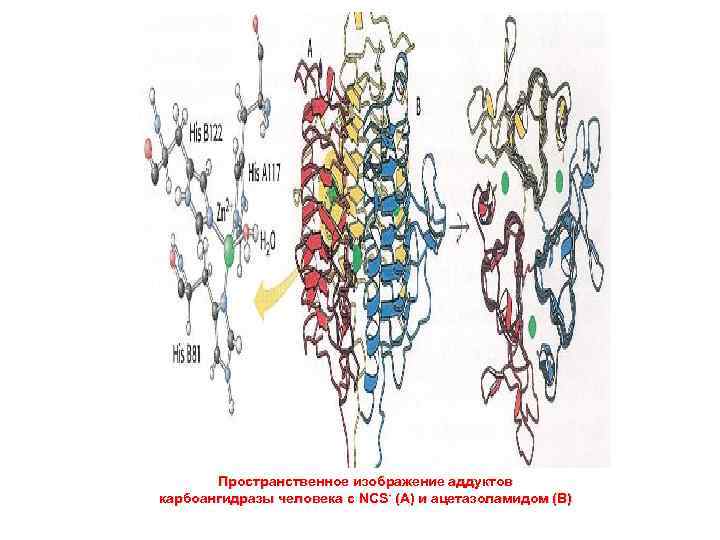 Пространственное изображение аддуктов карбоангидразы человека с NCS- (А) и ацетазоламидом (В)
Пространственное изображение аддуктов карбоангидразы человека с NCS- (А) и ацетазоламидом (В)
 ПЕРЕВАРИВАНИЕ В ТОНКОМ КИШЕЧНИКЕ
ПЕРЕВАРИВАНИЕ В ТОНКОМ КИШЕЧНИКЕ
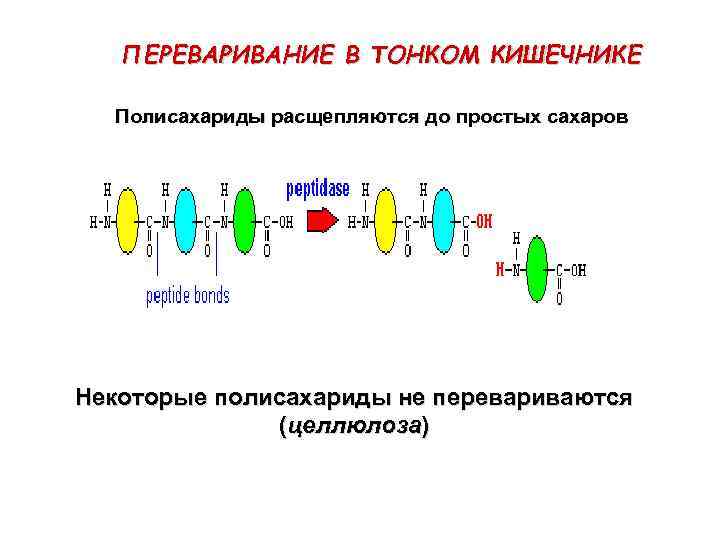 ПЕРЕВАРИВАНИЕ В ТОНКОМ КИШЕЧНИКЕ Полисахариды расщепляются до простых сахаров Некоторые полисахариды не перевариваются (целлюлоза)
ПЕРЕВАРИВАНИЕ В ТОНКОМ КИШЕЧНИКЕ Полисахариды расщепляются до простых сахаров Некоторые полисахариды не перевариваются (целлюлоза)
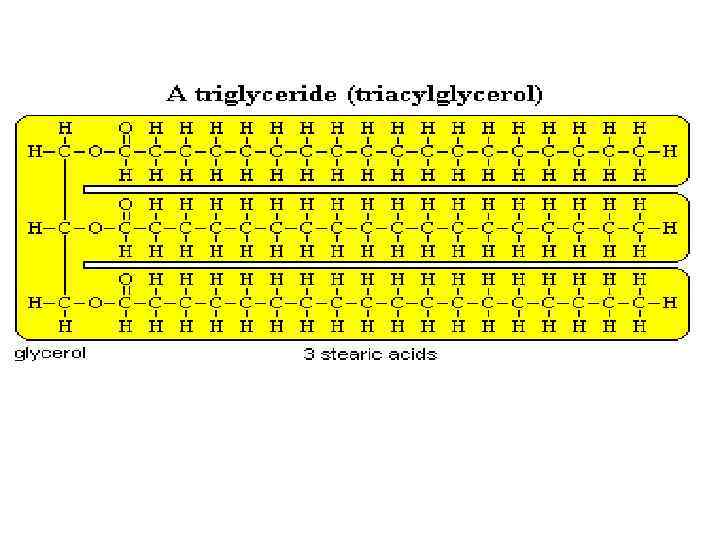
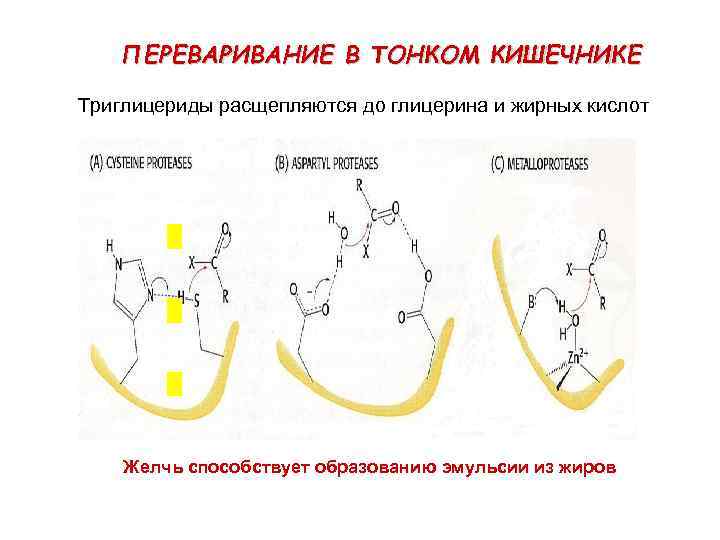 ПЕРЕВАРИВАНИЕ В ТОНКОМ КИШЕЧНИКЕ Tриглицериды расщепляются до глицерина и жирных кислот Желчь способствует образованию эмульсии из жиров
ПЕРЕВАРИВАНИЕ В ТОНКОМ КИШЕЧНИКЕ Tриглицериды расщепляются до глицерина и жирных кислот Желчь способствует образованию эмульсии из жиров
 ПЕРЕВАРИВАНИЕ В ТОНКОМ КИШЕЧНИКЕ Белки расщепляются до пептидов и аминокислот
ПЕРЕВАРИВАНИЕ В ТОНКОМ КИШЕЧНИКЕ Белки расщепляются до пептидов и аминокислот
 Три типа протеаз (протеиназ) Катализируют расщепление белков до свободных аминокислот
Три типа протеаз (протеиназ) Катализируют расщепление белков до свободных аминокислот
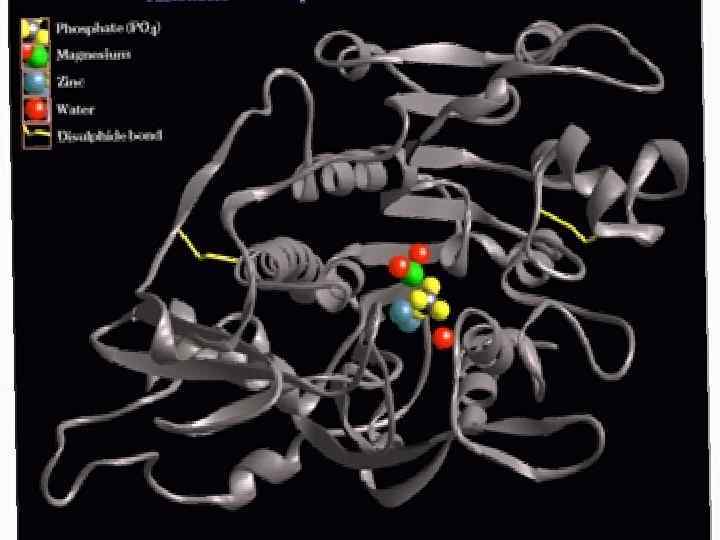
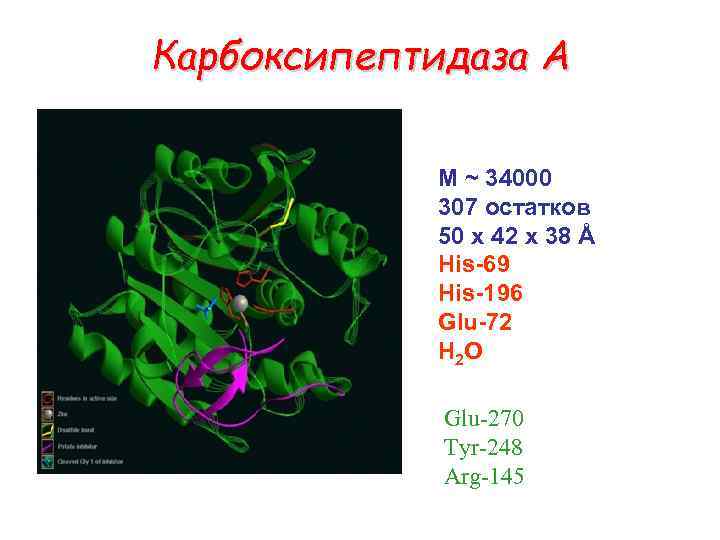 Карбоксипептидаза А M ~ 34000 307 остатков 50 x 42 x 38 Å His-69 His-196 Glu-72 H 2 O Glu-270 Tyr-248 Arg-145
Карбоксипептидаза А M ~ 34000 307 остатков 50 x 42 x 38 Å His-69 His-196 Glu-72 H 2 O Glu-270 Tyr-248 Arg-145
 Карбоксипептидаза А Zn
Карбоксипептидаза А Zn
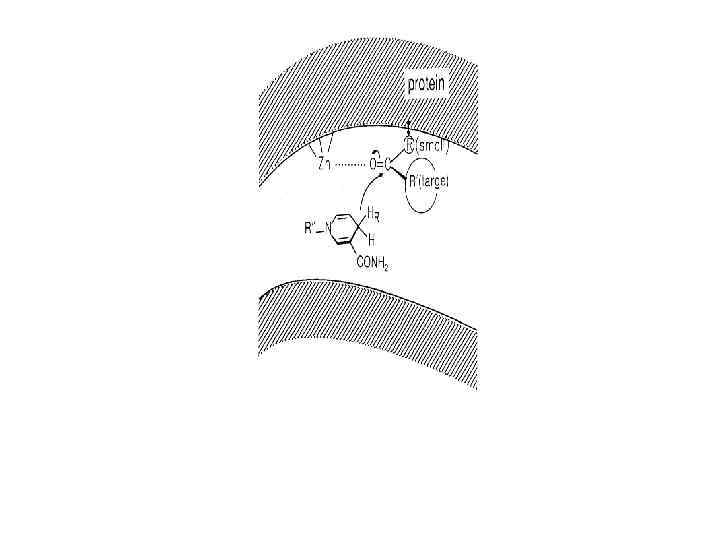
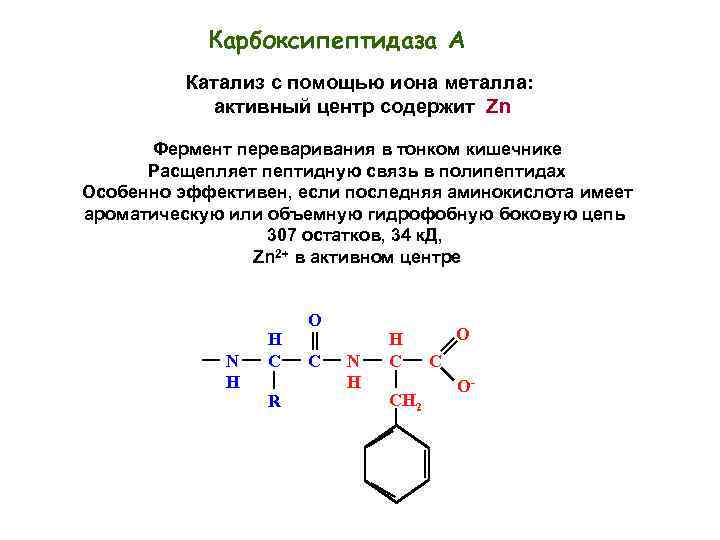 Карбоксипептидаза А Катализ с помощью иона металла: активный центр содержит Zn Фермент переваривания в тонком кишечнике Расщепляет пептидную связь в полипептидах Особенно эффективен, если последняя аминокислота имеет ароматическую или объемную гидрофобную боковую цепь 307 остатков, 34 к. Д, Zn 2+ в активном центре N H H C R O C N H H C CH 2 O C O-
Карбоксипептидаза А Катализ с помощью иона металла: активный центр содержит Zn Фермент переваривания в тонком кишечнике Расщепляет пептидную связь в полипептидах Особенно эффективен, если последняя аминокислота имеет ароматическую или объемную гидрофобную боковую цепь 307 остатков, 34 к. Д, Zn 2+ в активном центре N H H C R O C N H H C CH 2 O C O-

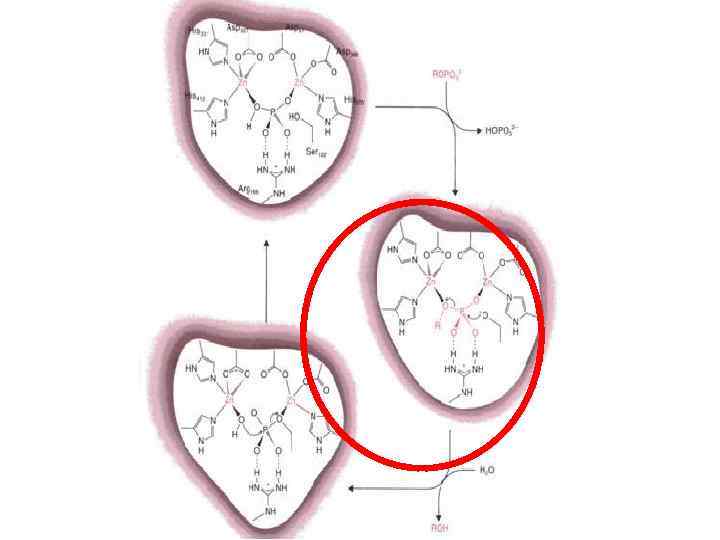
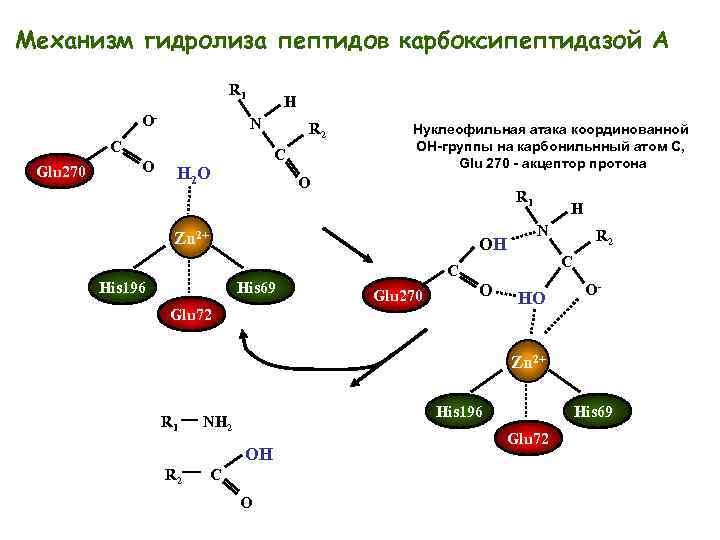 Механизм гидролиза пептидов карбоксипептидазой A R 1 O- H N C Glu 270 O R 2 C H 2 O Нуклеофильная атака координованной OH-группы на карбонильнный атом С, Glu 270 - акцептор протона O R 1 Zn 2+ OH His 196 His 69 H N C C Glu 270 O Glu 72 R 2 HO O- Zn 2+ R 1 His 196 NH 2 OH R 2 C O His 69 Glu 72
Механизм гидролиза пептидов карбоксипептидазой A R 1 O- H N C Glu 270 O R 2 C H 2 O Нуклеофильная атака координованной OH-группы на карбонильнный атом С, Glu 270 - акцептор протона O R 1 Zn 2+ OH His 196 His 69 H N C C Glu 270 O Glu 72 R 2 HO O- Zn 2+ R 1 His 196 NH 2 OH R 2 C O His 69 Glu 72
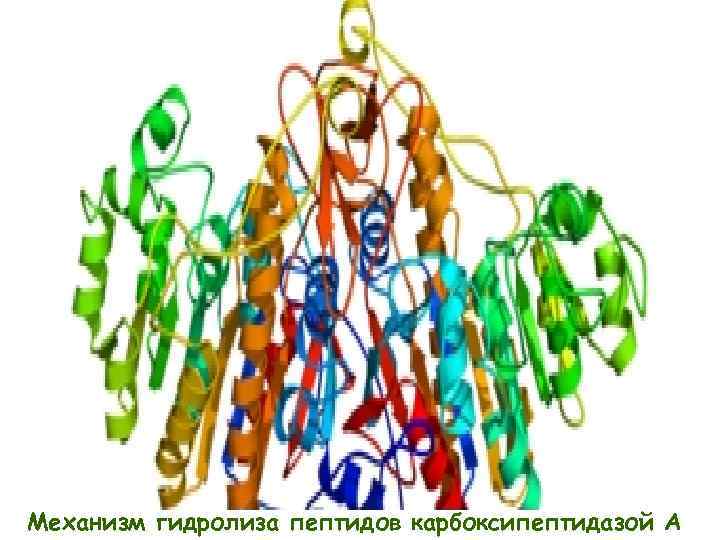 Механизм гидролиза пептидов карбоксипептидазой A
Механизм гидролиза пептидов карбоксипептидазой A
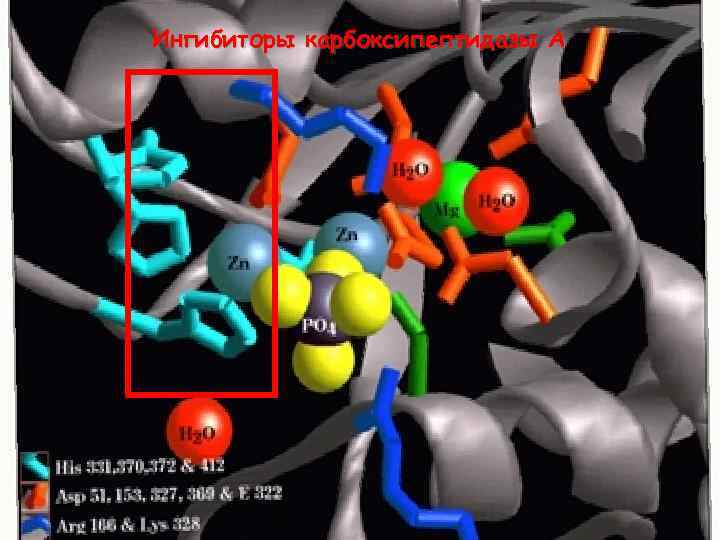 Ингибиторы карбоксипептидазы A
Ингибиторы карбоксипептидазы A
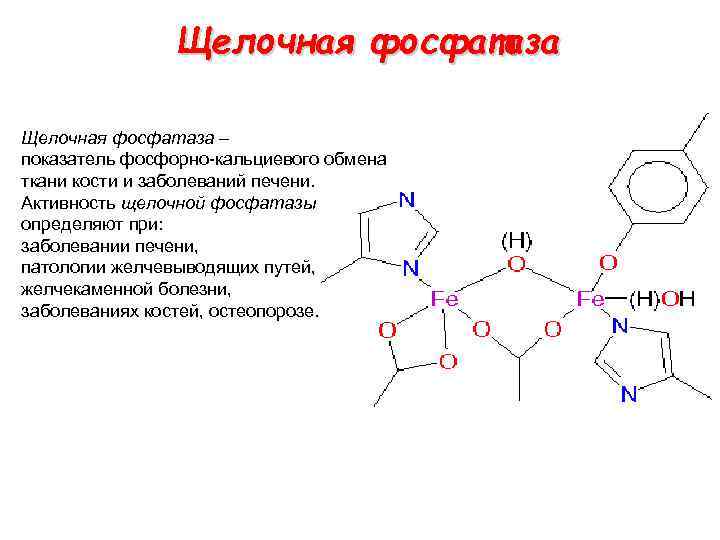 Щелочная фосфатаза – показатель фосфорно-кальциевого обмена ткани кости и заболеваний печени. Активность щелочной фосфатазы определяют при: заболевании печени, патологии желчевыводящих путей, желчекаменной болезни, заболеваниях костей, остеопорозе.
Щелочная фосфатаза – показатель фосфорно-кальциевого обмена ткани кости и заболеваний печени. Активность щелочной фосфатазы определяют при: заболевании печени, патологии желчевыводящих путей, желчекаменной болезни, заболеваниях костей, остеопорозе.
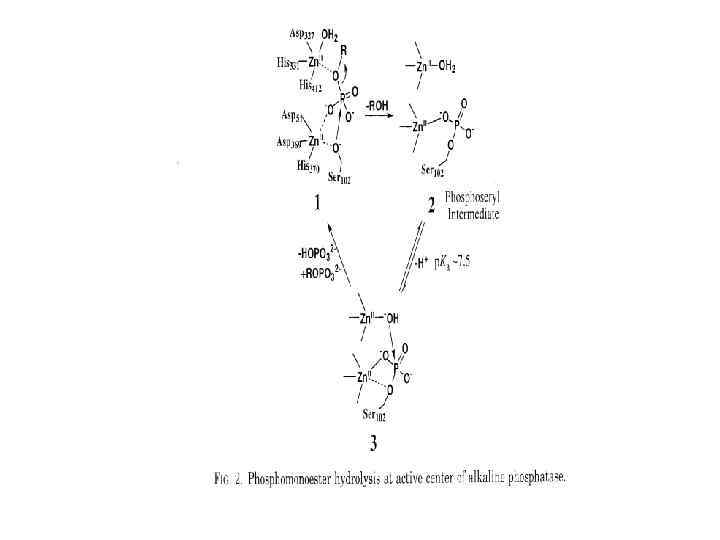
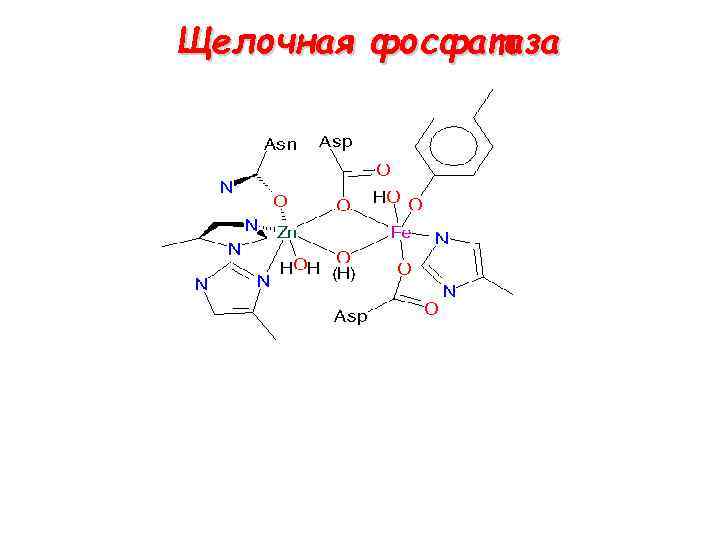 Щелочная фосфатаза
Щелочная фосфатаза
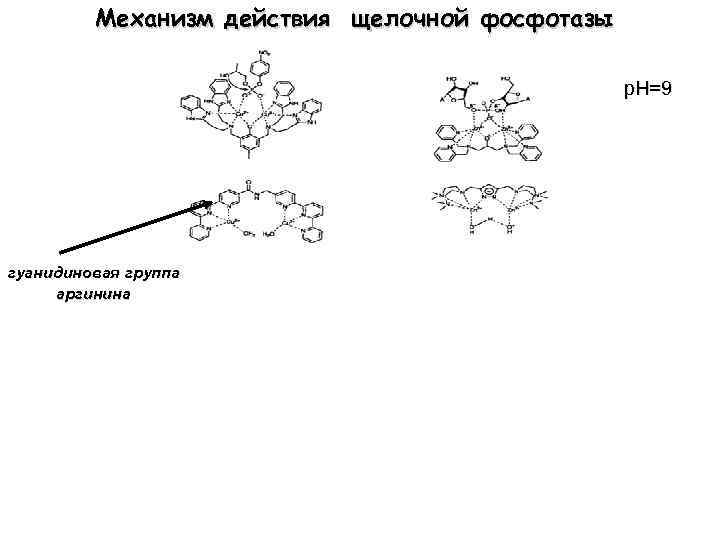 Механизм действия щелочной фосфотазы р. Н=9 гуанидиновая группа аргинина
Механизм действия щелочной фосфотазы р. Н=9 гуанидиновая группа аргинина
 Purple Acid Phosphatases Plant Catalytically active form: Fe(III)Fe(II) is labile, can be easily replaces with other +2 transition metal cations (such as Zn 2+). Oxidized form: Fe(III) Catalytically Inactive Mammalian Optimal p. H: 4. 9 – 6. 0 Fe. III – OH- is the predominant species Note higher acidity of water coordinated to Fe(III) compared to Zn(II)–coordinated water Intense purple color is due to Tyr Fe(III) charge transfer
Purple Acid Phosphatases Plant Catalytically active form: Fe(III)Fe(II) is labile, can be easily replaces with other +2 transition metal cations (such as Zn 2+). Oxidized form: Fe(III) Catalytically Inactive Mammalian Optimal p. H: 4. 9 – 6. 0 Fe. III – OH- is the predominant species Note higher acidity of water coordinated to Fe(III) compared to Zn(II)–coordinated water Intense purple color is due to Tyr Fe(III) charge transfer
 Thermolysin
Thermolysin
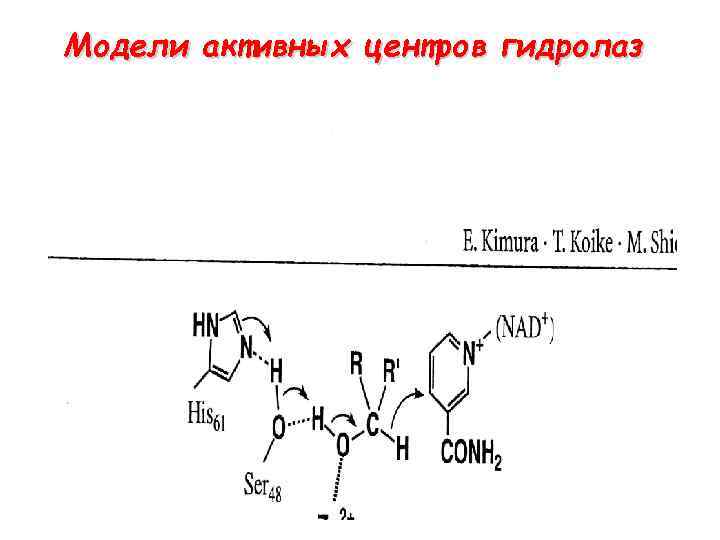 Модели активных центров гидролаз
Модели активных центров гидролаз

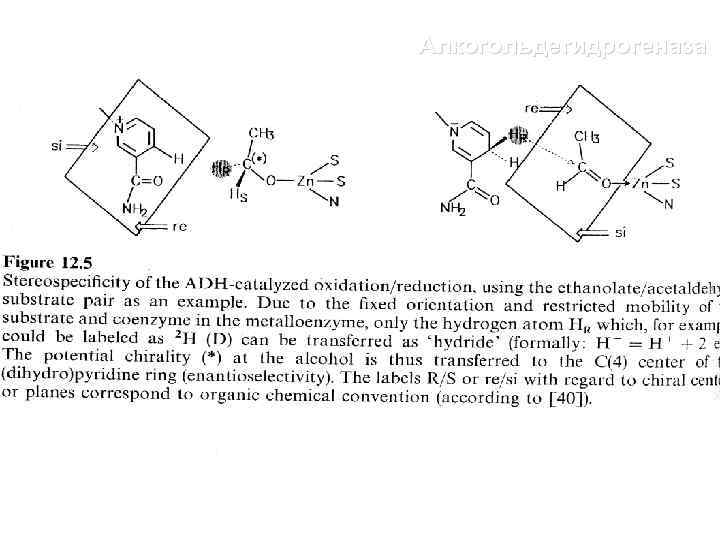 Алкогольдегидрогеназа ацетальдегид этанол
Алкогольдегидрогеназа ацетальдегид этанол