Жёсткость воды, Петров Д.ppt
- Количество слайдов: 10
 Жёсткость воды Петров Дмитрий, ученик 11 «В» класса
Жёсткость воды Петров Дмитрий, ученик 11 «В» класса
 Определение Жесткостью - свойство воды, обусловленное наличием в ней растворимых солей кальция и магния.
Определение Жесткостью - свойство воды, обусловленное наличием в ней растворимых солей кальция и магния.
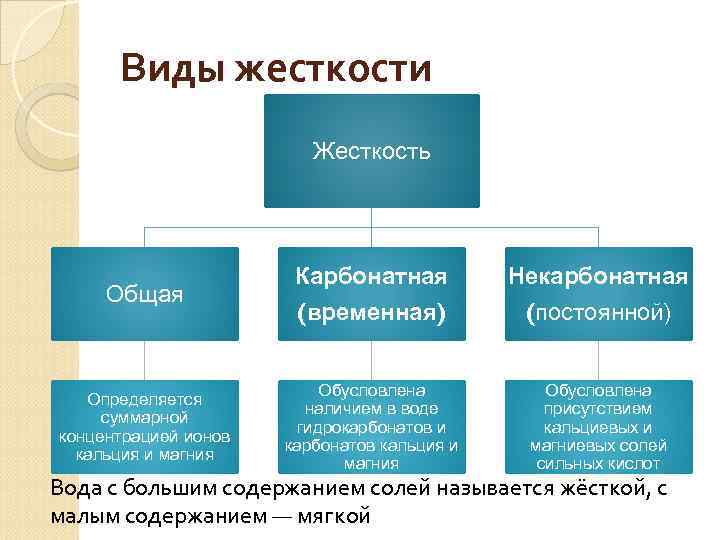 Виды жесткости Жесткость Общая Определяется суммарной концентрацией ионов кальция и магния Карбонатная Некарбонатная (временная) (постоянной) Обусловлена наличием в воде гидрокарбонатов и карбонатов кальция и магния Обусловлена присутствием кальциевых и магниевых солей сильных кислот Вода с большим содержанием солей называется жёсткой, с малым содержанием — мягкой
Виды жесткости Жесткость Общая Определяется суммарной концентрацией ионов кальция и магния Карбонатная Некарбонатная (временная) (постоянной) Обусловлена наличием в воде гидрокарбонатов и карбонатов кальция и магния Обусловлена присутствием кальциевых и магниевых солей сильных кислот Вода с большим содержанием солей называется жёсткой, с малым содержанием — мягкой
 Единицы измерения Рекомендованная единица СИ для измерения концентрации — моль на кубический метр(моль/м³) В России Госстандартом в качестве единицы жесткости воды установлен моль на кубический метр (моль/м 3). В зарубежных странах широко используются такие единицы жесткости, как немецкий градус (do, d. H), французский градус (fo), американский градус, ppm Ca. CO 3.
Единицы измерения Рекомендованная единица СИ для измерения концентрации — моль на кубический метр(моль/м³) В России Госстандартом в качестве единицы жесткости воды установлен моль на кубический метр (моль/м 3). В зарубежных странах широко используются такие единицы жесткости, как немецкий градус (do, d. H), французский градус (fo), американский градус, ppm Ca. CO 3.
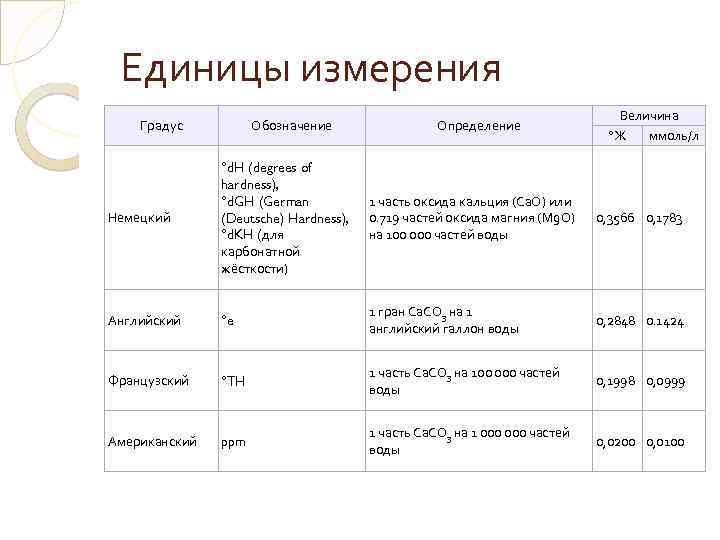 Единицы измерения Градус Обозначение Определение Величина °Ж ммоль/л Немецкий °d. H (degrees of hardness), °d. GH (German (Deutsche) Hardness), °d. KH (для карбонатной жёсткости) 1 часть оксида кальция (Са. О) или 0. 719 частей оксида магния (Mg. O) на 100 000 частей воды 0, 3566 0, 1783 Английский °e 1 гран Ca. CO 3 на 1 английский галлон воды 0, 2848 0. 1424 Французский °TH 1 часть Ca. CO 3 на 100 000 частей воды 0, 1998 0, 0999 Американский ppm 1 часть Ca. CO 3 на 1 000 частей воды 0, 0200 0, 0100
Единицы измерения Градус Обозначение Определение Величина °Ж ммоль/л Немецкий °d. H (degrees of hardness), °d. GH (German (Deutsche) Hardness), °d. KH (для карбонатной жёсткости) 1 часть оксида кальция (Са. О) или 0. 719 частей оксида магния (Mg. O) на 100 000 частей воды 0, 3566 0, 1783 Английский °e 1 гран Ca. CO 3 на 1 английский галлон воды 0, 2848 0. 1424 Французский °TH 1 часть Ca. CO 3 на 100 000 частей воды 0, 1998 0, 0999 Американский ppm 1 часть Ca. CO 3 на 1 000 частей воды 0, 0200 0, 0100
 Влияние на жизнь человека Жесткая вода образует налет на сантехнических приборах и арматуре, образует накипь в водонагревательных системах и приборах. В системах водоснабжения - жесткая вода приводит к быстрому износу водонагревательной технике. Соли жесткости, отлагаясь на внутренних стенках труб, и образуя накипные отложения в водонагревательных и охлаждающих системах, приводят к занижению проходного сечения, уменьшают теплоотдачу.
Влияние на жизнь человека Жесткая вода образует налет на сантехнических приборах и арматуре, образует накипь в водонагревательных системах и приборах. В системах водоснабжения - жесткая вода приводит к быстрому износу водонагревательной технике. Соли жесткости, отлагаясь на внутренних стенках труб, и образуя накипные отложения в водонагревательных и охлаждающих системах, приводят к занижению проходного сечения, уменьшают теплоотдачу.
 Влияние на жизнь человека При хозяйственно-бытовом использовании жесткой воды увеличивается расход моющих средств и мыла вследствие образования осадка кальциевых и магниевых солей жирных кислот, замедляется процесс приготовления пищи. Постоянное употребление внутрь воды с повышенной жесткостью приводит к снижению моторики желудка, к накоплению солей в организме, и к заболеванию суставов и образованию камней в почках и желчных путях. Очень мягкая вода не менее опасная, чем излишне жесткая. Мягкая вода способна вымывать из костей кальций. У человека может развиться рахит, у взрослого человека становятся ломкие кости. Она, проходя через пищеварительный тракт, не только вымывает минеральные вещества, но и полезные органические вещества, в том числе и полезные бактерии.
Влияние на жизнь человека При хозяйственно-бытовом использовании жесткой воды увеличивается расход моющих средств и мыла вследствие образования осадка кальциевых и магниевых солей жирных кислот, замедляется процесс приготовления пищи. Постоянное употребление внутрь воды с повышенной жесткостью приводит к снижению моторики желудка, к накоплению солей в организме, и к заболеванию суставов и образованию камней в почках и желчных путях. Очень мягкая вода не менее опасная, чем излишне жесткая. Мягкая вода способна вымывать из костей кальций. У человека может развиться рахит, у взрослого человека становятся ломкие кости. Она, проходя через пищеварительный тракт, не только вымывает минеральные вещества, но и полезные органические вещества, в том числе и полезные бактерии.
 Методы устранения Термоумягчение. Основан на кипячении воды, в результате термически нестойкие гидрокарбонаты кальция и магния разлагаются с образованием накипи: Ca(HCO 3)2 → Ca. CO 3↓ + CO 2 + H 2 O. Mg(HCO 3)2→Mg. CO 3↓+H 2 O+CO 2 Кипячение устраняет только временную (карбонатную) жёсткость. Находит применение в быту. Реагентное умягчение. Метод основан на добавлении в воду соды или гашеной извести. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Например, добавление гашёной извести приводит к переводу солей кальция в нерастворимый карбонат: Ca(HCO 3)2 + Ca(OH)2 → 2 Ca. CO 3↓ + 2 H 2 O Этот метод оправдан при относительно больших расходах воды, поскольку связан с решением ряда специфических проблем: фильтрации осадка, точной дозировки реагента.
Методы устранения Термоумягчение. Основан на кипячении воды, в результате термически нестойкие гидрокарбонаты кальция и магния разлагаются с образованием накипи: Ca(HCO 3)2 → Ca. CO 3↓ + CO 2 + H 2 O. Mg(HCO 3)2→Mg. CO 3↓+H 2 O+CO 2 Кипячение устраняет только временную (карбонатную) жёсткость. Находит применение в быту. Реагентное умягчение. Метод основан на добавлении в воду соды или гашеной извести. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Например, добавление гашёной извести приводит к переводу солей кальция в нерастворимый карбонат: Ca(HCO 3)2 + Ca(OH)2 → 2 Ca. CO 3↓ + 2 H 2 O Этот метод оправдан при относительно больших расходах воды, поскольку связан с решением ряда специфических проблем: фильтрации осадка, точной дозировки реагента.
 Методы устранения Катионирование. Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости. Взамен, в зависимости от ионной формы, отдавая ионы натрия или водорода. Эти методы соответственно называются Naкатионирование и Н-катионирование. При правильно подобранной ионообменной загрузке жёсткость воды снижается при одноступенчатом натрий-катионировании до 0, 05 -0, 1 мг-экв/л, при двухступенчатом — до 0, 01 мг-экв/л. Лучшим реагентом для устранения общей жесткости воды является ортофосфат натрия Na 3 PO 4: 3 Ca(HCO 3)2 + 2 Na 3 PO 4 → Ca 3(PO 4)2↓+ 6 Na. HCO 3 3 Mg. SO 4 + 2 Na 3 PO 4 → Mg 3(PO 4)2↓ + 3 Na 2 SO 4 Ортофосфаты кальция и магния очень плохо растворимы в воде, поэтому достигается лучшее умягчение воды. В промышленности с помощью ионообменных фильтров заменяют ионы кальция и магния на ионы натрия и калия, получая мягкую воду.
Методы устранения Катионирование. Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости. Взамен, в зависимости от ионной формы, отдавая ионы натрия или водорода. Эти методы соответственно называются Naкатионирование и Н-катионирование. При правильно подобранной ионообменной загрузке жёсткость воды снижается при одноступенчатом натрий-катионировании до 0, 05 -0, 1 мг-экв/л, при двухступенчатом — до 0, 01 мг-экв/л. Лучшим реагентом для устранения общей жесткости воды является ортофосфат натрия Na 3 PO 4: 3 Ca(HCO 3)2 + 2 Na 3 PO 4 → Ca 3(PO 4)2↓+ 6 Na. HCO 3 3 Mg. SO 4 + 2 Na 3 PO 4 → Mg 3(PO 4)2↓ + 3 Na 2 SO 4 Ортофосфаты кальция и магния очень плохо растворимы в воде, поэтому достигается лучшее умягчение воды. В промышленности с помощью ионообменных фильтров заменяют ионы кальция и магния на ионы натрия и калия, получая мягкую воду.
 Методы устранения Обратный осмос. Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99, 9 %. Этот метод нашёл наибольшее применение в бытовых системах подготовки питьевой воды. В качестве недостатков данного метода следует отметить: - необходимость предварительной подготовки воды, подаваемой на обратноосмотическую мембрану; - относительно высокая стоимость 1 л получаемой воды; - низкую минерализацию получаемой воды Электродиализ. Основан на удалении из воды солей под действием электрического поля. Удаление ионов растворенных веществ происходит за счёт специальных мембран. Так же как и при использовании технологии обратного осмоса, происходит удаление и других солей, помимо ионов жёсткости. Полностью очистить воду от солей жёсткости можно дистилляцией.
Методы устранения Обратный осмос. Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99, 9 %. Этот метод нашёл наибольшее применение в бытовых системах подготовки питьевой воды. В качестве недостатков данного метода следует отметить: - необходимость предварительной подготовки воды, подаваемой на обратноосмотическую мембрану; - относительно высокая стоимость 1 л получаемой воды; - низкую минерализацию получаемой воды Электродиализ. Основан на удалении из воды солей под действием электрического поля. Удаление ионов растворенных веществ происходит за счёт специальных мембран. Так же как и при использовании технологии обратного осмоса, происходит удаление и других солей, помимо ионов жёсткости. Полностью очистить воду от солей жёсткости можно дистилляцией.


