 Жозеф Луі Гей-Люссак (Франція)
Жозеф Луі Гей-Люссак (Франція)
 Перший закон Закон теплового розширення газів: при сталому тискові залежність об'єму Vt даної маси газу від температури описується формулою: V = V 0(1+at), a=1 / 273, 15 0 C p p 0 -273, 15 0 a - температурный коэффициент. 0 t, C
Перший закон Закон теплового розширення газів: при сталому тискові залежність об'єму Vt даної маси газу від температури описується формулою: V = V 0(1+at), a=1 / 273, 15 0 C p p 0 -273, 15 0 a - температурный коэффициент. 0 t, C
 Другий закон Закон об'ємних відношень, за яким при постійних температурі і тиску об'єми газів, які вступають у реакцію, відносяться між собою і до об'ємів газоподібних продуктів реакції, як невеликі прості числа. Наприклад, при взаємодії одного об'єму водню з одним об'ємом хлору утворюється два об'єми хлористого водню.
Другий закон Закон об'ємних відношень, за яким при постійних температурі і тиску об'єми газів, які вступають у реакцію, відносяться між собою і до об'ємів газоподібних продуктів реакції, як невеликі прості числа. Наприклад, при взаємодії одного об'єму водню з одним об'ємом хлору утворюється два об'єми хлористого водню.
 Зако н Ша рля Закон теплового розширення газів: при сталому об'ємі залежність тиску Р даної маси газу від температури описується формулою:
Зако н Ша рля Закон теплового розширення газів: при сталому об'ємі залежність тиску Р даної маси газу від температури описується формулою:
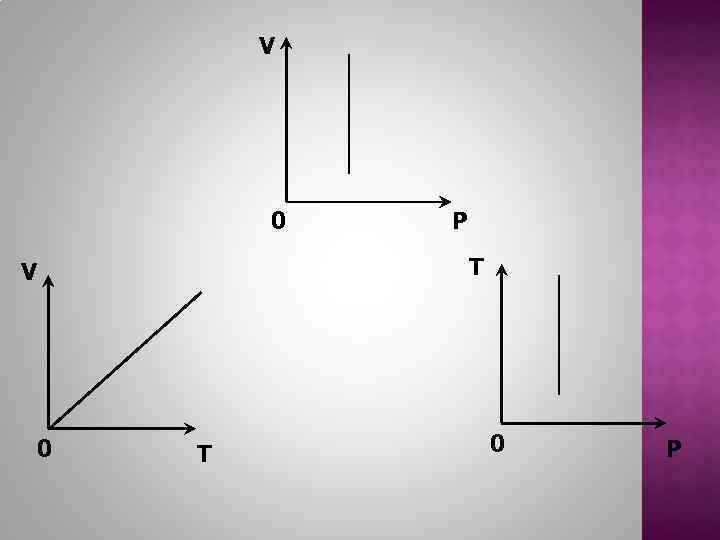 V 0 T V 0 P T 0 P
V 0 T V 0 P T 0 P