 ЖИРЫ И ЭФИРЫ
ЖИРЫ И ЭФИРЫ
 Определение Сложные эфиры — производные оксокислот (как карбоновых, так и минеральных) Rk. E(=O)l(OH)m, (l ≠ 0), формально являющиеся продуктами замещения атомов водорода гидроксилов —OH кислотной функции на углеводородный остаток (алифатический, алкенильный, ароматический или гетероароматический); рассматриваются также как ацилпроизводные спиртов. Жиры , или триглицериды — природные органические соединения, полные сложные эфиры глицерина и одноосновных жирных кислот; входят в класс липидов.
Определение Сложные эфиры — производные оксокислот (как карбоновых, так и минеральных) Rk. E(=O)l(OH)m, (l ≠ 0), формально являющиеся продуктами замещения атомов водорода гидроксилов —OH кислотной функции на углеводородный остаток (алифатический, алкенильный, ароматический или гетероароматический); рассматриваются также как ацилпроизводные спиртов. Жиры , или триглицериды — природные органические соединения, полные сложные эфиры глицерина и одноосновных жирных кислот; входят в класс липидов.
 Введение Вы не однократно встречались с производными спиртов и карбоновых кислот– сложными эфирами. Приятный аромат цветов, плодов и ягод в значительной степени обусловлен присутствием в них тех или иных сложных эфиров. Синтетические сложные эфиры в виде фруктовых эссенций используются в производстве фруктовых вод, при изготовлении духов. Некоторые сложные эфиры служат растворителями. Важнейшими представителями сложных эфиров являются жиры. Среди сложных эфиров особое место занимают природные эфиры — жиры и масла, которые образованы трехатомным спиртом глицерином и высшими жирными кислотами, содержащими четное число углеродных атомов. Жиры входят в состав растительных и животных организмов и служат одним из источников энергии живых организмов, которая выделяется при окислении жиров.
Введение Вы не однократно встречались с производными спиртов и карбоновых кислот– сложными эфирами. Приятный аромат цветов, плодов и ягод в значительной степени обусловлен присутствием в них тех или иных сложных эфиров. Синтетические сложные эфиры в виде фруктовых эссенций используются в производстве фруктовых вод, при изготовлении духов. Некоторые сложные эфиры служат растворителями. Важнейшими представителями сложных эфиров являются жиры. Среди сложных эфиров особое место занимают природные эфиры — жиры и масла, которые образованы трехатомным спиртом глицерином и высшими жирными кислотами, содержащими четное число углеродных атомов. Жиры входят в состав растительных и животных организмов и служат одним из источников энергии живых организмов, которая выделяется при окислении жиров.
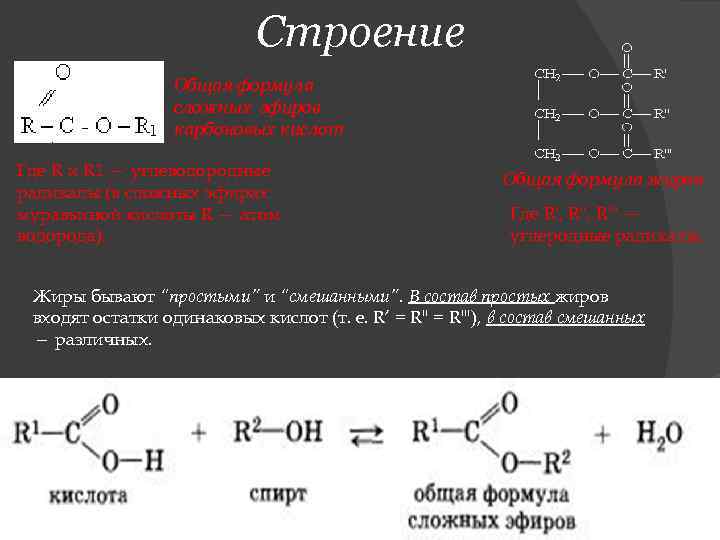 Строение Общая формула сложных эфиров карбоновых кислот Где R и R 1 — углеводородные радикалы (в сложных эфирах муравьиной кислоты R — атом водорода). Общая формула жиров Где R', R"' — углеродные радикалы. Жиры бывают “простыми” и “смешанными”. В состав простых жиров входят остатки одинаковых кислот (т. е. R’ = R" = R'"), в состав смешанных — различных.
Строение Общая формула сложных эфиров карбоновых кислот Где R и R 1 — углеводородные радикалы (в сложных эфирах муравьиной кислоты R — атом водорода). Общая формула жиров Где R', R"' — углеродные радикалы. Жиры бывают “простыми” и “смешанными”. В состав простых жиров входят остатки одинаковых кислот (т. е. R’ = R" = R'"), в состав смешанных — различных.
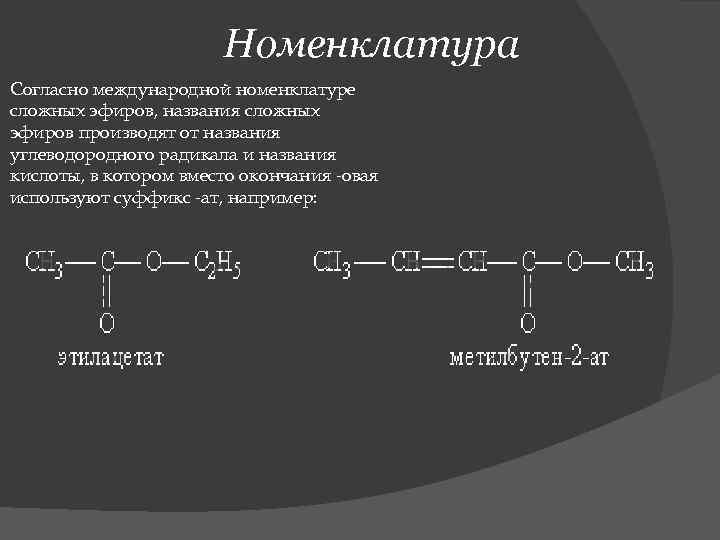 Номенклатура Согласно международной номенклатуре сложных эфиров, названия сложных эфиров производят от названия углеводородного радикала и названия кислоты, в котором вместо окончания -овая используют суффикс -ат, например:
Номенклатура Согласно международной номенклатуре сложных эфиров, названия сложных эфиров производят от названия углеводородного радикала и названия кислоты, в котором вместо окончания -овая используют суффикс -ат, например:
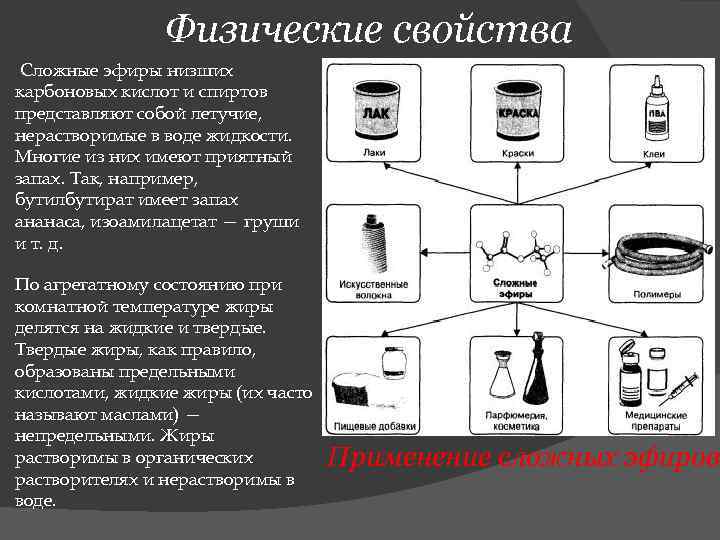 Физические свойства Сложные эфиры низших карбоновых кислот и спиртов представляют собой летучие, нерастворимые в воде жидкости. Многие из них имеют приятный запах. Так, например, бутилбутират имеет запах ананаса, изоамилацетат — груши и т. д. По агрегатному состоянию при комнатной температуре жиры делятся на жидкие и твердые. Твердые жиры, как правило, образованы предельными кислотами, жидкие жиры (их часто называют маслами) — непредельными. Жиры растворимы в органических растворителях и нерастворимы в воде. Применение сложных эфиров
Физические свойства Сложные эфиры низших карбоновых кислот и спиртов представляют собой летучие, нерастворимые в воде жидкости. Многие из них имеют приятный запах. Так, например, бутилбутират имеет запах ананаса, изоамилацетат — груши и т. д. По агрегатному состоянию при комнатной температуре жиры делятся на жидкие и твердые. Твердые жиры, как правило, образованы предельными кислотами, жидкие жиры (их часто называют маслами) — непредельными. Жиры растворимы в органических растворителях и нерастворимы в воде. Применение сложных эфиров
 Химические свойства 1. Реакция гидролиза, или омыления. Так, как реакция этерификации является обратимой, поэтому в присутствии кислот протекает обратная реакция гидролиза: 2. Реакция присоединения. Сложные эфиры, имеющие в своем составе непредельную кислоту или спирт, способны к реакциям присоединения. 3. Реакция восстановления. Восстановление сложных эфиров водородом приводит к образованию двух спиртов: 4. Реакция образования амидов. Под действием аммиака сложные эфиры превращаются в амиды кислот и спирты:
Химические свойства 1. Реакция гидролиза, или омыления. Так, как реакция этерификации является обратимой, поэтому в присутствии кислот протекает обратная реакция гидролиза: 2. Реакция присоединения. Сложные эфиры, имеющие в своем составе непредельную кислоту или спирт, способны к реакциям присоединения. 3. Реакция восстановления. Восстановление сложных эфиров водородом приводит к образованию двух спиртов: 4. Реакция образования амидов. Под действием аммиака сложные эфиры превращаются в амиды кислот и спирты:
 Применение Метилацетат СН 3 СООСН 3. Метилацетат также образуется в виде побочного продукта при производстве поливинилового спирта. По растворяющей способности метилацетат аналогичен ацетону и применяется в ряде случаев как его заменитель. Однако он обладает большей токсичностью, чем ацетон. Этилацетат С 2 Н 5 СООСН 3. Получают методом этерификации на лесохимических предприятиях при переработке синтетической и лесохимической уксусной кислоты, гидролизного и синтетического этилового спирта или конденсацией ацетальдегида. Этилацетат подобно ацетону растворяет большинство полимеров. По сравнению с ацетоном его преимущество в более высокой температуре кипения (меньшей летучести). Добавка 15 -20 % этилового спирта повышает растворяющую способность этилацетата в отношении эфиров целлюлозы, особенно ацетилцеллюлозы. Амилацетат CH 3 COOCH 2 CH 2 CH 3, т. кип. 148° С, иногда называют «банановым маслом» (которое он напоминает по запаху). Он образуется в реакции между амиловым спиртом и уксусной кислотой в присутствии катализатора. Амилацетат широко применяется как растворитель для лаков, поскольку он испаряется медленнее, чем этилацетат. Винилацетат CH 2=CHOOCCH 3, образуется при взаимодействии уксусной кислоты с ацетиленом в присутствии катализатора. Это важный мономер для приготовления поливинилацетатных смол, клеев и красок. Мыла — соли высших карбоновых кислот. Обычные мыла состоят главным образом из смеси солей пальмитиновой, стеариновой и олеиновой кислот. Натриевые соли образуют твердые мыла, калиевые соли — жидкие мыла.
Применение Метилацетат СН 3 СООСН 3. Метилацетат также образуется в виде побочного продукта при производстве поливинилового спирта. По растворяющей способности метилацетат аналогичен ацетону и применяется в ряде случаев как его заменитель. Однако он обладает большей токсичностью, чем ацетон. Этилацетат С 2 Н 5 СООСН 3. Получают методом этерификации на лесохимических предприятиях при переработке синтетической и лесохимической уксусной кислоты, гидролизного и синтетического этилового спирта или конденсацией ацетальдегида. Этилацетат подобно ацетону растворяет большинство полимеров. По сравнению с ацетоном его преимущество в более высокой температуре кипения (меньшей летучести). Добавка 15 -20 % этилового спирта повышает растворяющую способность этилацетата в отношении эфиров целлюлозы, особенно ацетилцеллюлозы. Амилацетат CH 3 COOCH 2 CH 2 CH 3, т. кип. 148° С, иногда называют «банановым маслом» (которое он напоминает по запаху). Он образуется в реакции между амиловым спиртом и уксусной кислотой в присутствии катализатора. Амилацетат широко применяется как растворитель для лаков, поскольку он испаряется медленнее, чем этилацетат. Винилацетат CH 2=CHOOCCH 3, образуется при взаимодействии уксусной кислоты с ацетиленом в присутствии катализатора. Это важный мономер для приготовления поливинилацетатных смол, клеев и красок. Мыла — соли высших карбоновых кислот. Обычные мыла состоят главным образом из смеси солей пальмитиновой, стеариновой и олеиновой кислот. Натриевые соли образуют твердые мыла, калиевые соли — жидкие мыла.
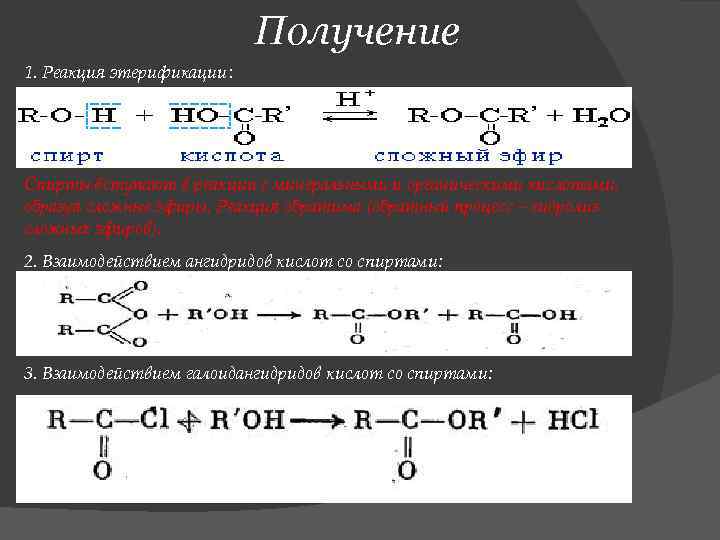 Получение 1. Реакция этерификации: Спирты вступают в реакции с минеральными и органическими кислотами, образуя сложные эфиры. Реакция обратима (обратный процесс – гидролиз сложных эфиров). 2. Взаимодействием ангидридов кислот со спиртами: 3. Взаимодействием галоидангидридов кислот со спиртами:
Получение 1. Реакция этерификации: Спирты вступают в реакции с минеральными и органическими кислотами, образуя сложные эфиры. Реакция обратима (обратный процесс – гидролиз сложных эфиров). 2. Взаимодействием ангидридов кислот со спиртами: 3. Взаимодействием галоидангидридов кислот со спиртами:
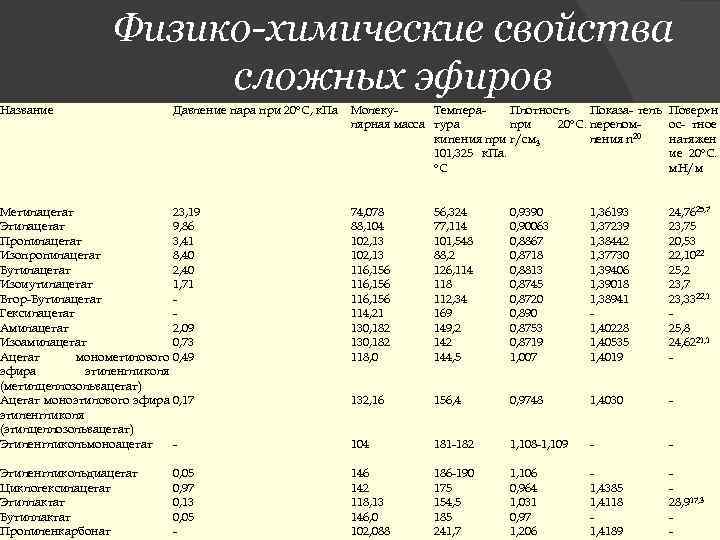 Физико-химические свойства сложных эфиров Название Давление пара при 20°С, к. Па Молеку. Темпера. Плотность Показа- тель лярная масса тура при 20°С. переломкипения при г/см 3 ления n 20 101, 325 к. Па. °С Поверхн ос- тное натяжен ие 20°С. м. Н/м Метилацетат 23, 19 Этилацетат 9, 86 Пропилацетат 3, 41 Изопропилацетат 8, 40 Бутилацетат 2, 40 Изоиутилацетат 1, 71 Втор-Бутилацетат Гексилацетат Амилацетат 2, 09 Изоамилацетат 0, 73 Ацетат монометилового 0, 49 эфира этиленгликоля (метилцеллозольвацетат) Ацетат моноэтилового эфира 0, 17 этиленгликоля (этилцеллозольвацетат) Этиленгликольмоноацетат - 74, 078 88, 104 102, 13 116, 156 114, 21 130, 182 118, 0 56, 324 77, 114 101, 548 88, 2 126, 114 118 112, 34 169 149, 2 144, 5 0, 9390 0, 90063 0, 8867 0, 8718 0, 8813 0, 8745 0, 8720 0, 890 0, 8753 0, 8719 1, 007 1, 36193 1, 37239 1, 38442 1, 37730 1, 39406 1, 39018 1, 38941 1, 40228 1, 40535 1, 4019 24, 7625, 7 23, 75 20, 53 22, 1022 25, 2 23, 7 23, 3322, 1 25, 8 24, 6221, 1 - 132, 16 156, 4 0, 9748 1, 4030 - 104 181 -182 1, 108 -1, 109 - - Этиленгликольдиацетат Циклогексилацетат Этиллактат Бутиллактат Пропиленкарбонат 146 142 118, 13 146, 0 102, 088 186 -190 175 154, 5 185 241, 7 1, 106 0, 964 1, 031 0, 97 1, 206 1, 4385 1, 4118 1, 4189 28, 917, 3 - 0, 05 0, 97 0, 13 0, 05 -
Физико-химические свойства сложных эфиров Название Давление пара при 20°С, к. Па Молеку. Темпера. Плотность Показа- тель лярная масса тура при 20°С. переломкипения при г/см 3 ления n 20 101, 325 к. Па. °С Поверхн ос- тное натяжен ие 20°С. м. Н/м Метилацетат 23, 19 Этилацетат 9, 86 Пропилацетат 3, 41 Изопропилацетат 8, 40 Бутилацетат 2, 40 Изоиутилацетат 1, 71 Втор-Бутилацетат Гексилацетат Амилацетат 2, 09 Изоамилацетат 0, 73 Ацетат монометилового 0, 49 эфира этиленгликоля (метилцеллозольвацетат) Ацетат моноэтилового эфира 0, 17 этиленгликоля (этилцеллозольвацетат) Этиленгликольмоноацетат - 74, 078 88, 104 102, 13 116, 156 114, 21 130, 182 118, 0 56, 324 77, 114 101, 548 88, 2 126, 114 118 112, 34 169 149, 2 144, 5 0, 9390 0, 90063 0, 8867 0, 8718 0, 8813 0, 8745 0, 8720 0, 890 0, 8753 0, 8719 1, 007 1, 36193 1, 37239 1, 38442 1, 37730 1, 39406 1, 39018 1, 38941 1, 40228 1, 40535 1, 4019 24, 7625, 7 23, 75 20, 53 22, 1022 25, 2 23, 7 23, 3322, 1 25, 8 24, 6221, 1 - 132, 16 156, 4 0, 9748 1, 4030 - 104 181 -182 1, 108 -1, 109 - - Этиленгликольдиацетат Циклогексилацетат Этиллактат Бутиллактат Пропиленкарбонат 146 142 118, 13 146, 0 102, 088 186 -190 175 154, 5 185 241, 7 1, 106 0, 964 1, 031 0, 97 1, 206 1, 4385 1, 4118 1, 4189 28, 917, 3 - 0, 05 0, 97 0, 13 0, 05 -
 Вывод Исходя из вышесказанного, можно сделать вывод, что сложные эфиры находят широкое применение, как в быту, так и в промышленности. Некоторые из сложных эфиров готовятся искусственно и под названием «фруктовых эссенций» широко применяются в кондитерском деле, в производстве прохладительных напитков, в парфюмерии и во многих других отраслях. Жиры используют для многих технических целей. Однако особенно велико их значение как важнейшей составной части рациона человека и животных, наряду с углеводами и белками. Прекращение использования пищевых жиров в технике и замена их непищевыми материалами – одна из важнейших задач народного хозяйства. Эта задача может быть разрешена только при достаточно основательных знаниях о сложных эфирах и дальнейшем изучении этого класса органических соединений.
Вывод Исходя из вышесказанного, можно сделать вывод, что сложные эфиры находят широкое применение, как в быту, так и в промышленности. Некоторые из сложных эфиров готовятся искусственно и под названием «фруктовых эссенций» широко применяются в кондитерском деле, в производстве прохладительных напитков, в парфюмерии и во многих других отраслях. Жиры используют для многих технических целей. Однако особенно велико их значение как важнейшей составной части рациона человека и животных, наряду с углеводами и белками. Прекращение использования пищевых жиров в технике и замена их непищевыми материалами – одна из важнейших задач народного хозяйства. Эта задача может быть разрешена только при достаточно основательных знаниях о сложных эфирах и дальнейшем изучении этого класса органических соединений.
 Презентацию подготовили курсанты К-111 группы: Воевода А. Леоненко К. Фесенко А. В. Литература 1. Цветков Л. А. Органическая химия: Учебник для 10 -11 классов общеобразовательных учебных заведений. 2. Несмеянов А. Н. , Несмеянов Н. А. , Начала органической химии, кн. 1 -2. 3. Глинка Н. Л. Общая химия: Учебное пособие для вузов. 1983
Презентацию подготовили курсанты К-111 группы: Воевода А. Леоненко К. Фесенко А. В. Литература 1. Цветков Л. А. Органическая химия: Учебник для 10 -11 классов общеобразовательных учебных заведений. 2. Несмеянов А. Н. , Несмеянов Н. А. , Начала органической химии, кн. 1 -2. 3. Глинка Н. Л. Общая химия: Учебное пособие для вузов. 1983


