Дыхательная цепь.ppt
- Количество слайдов: 47
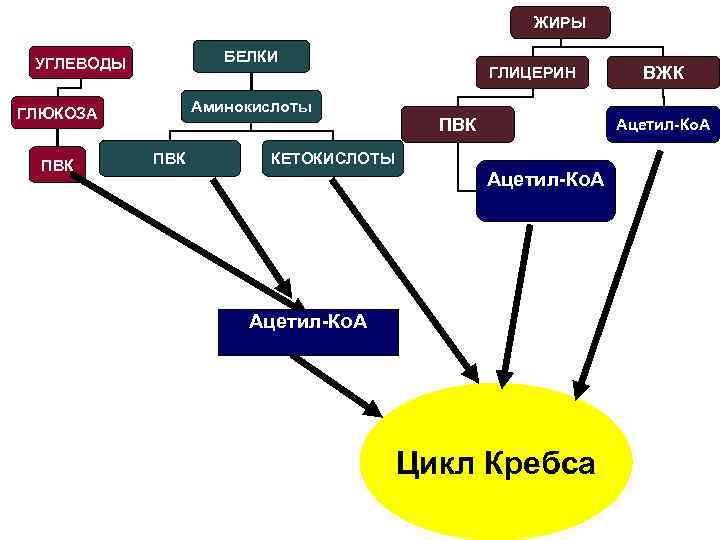
ЖИРЫ БЕЛКИ УГЛЕВОДЫ Аминокислоты ГЛЮКОЗА ПВК ГЛИЦЕРИН ПВК ВЖК Ацетил-Ко. А КЕТОКИСЛОТЫ Ацетил-Ко. А Цикл Кребса

Биологическим окислением или тканевым дыханием называется процесс потребления кислорода Окислительное фосфорилирование – синтез АТФ, который использует энергию электрохимического потенциала переноса электронов мембраны митохондрий. Для этого пути синтеза АТФ необходим кислород. Общая реакция синтеза АТФ: АДФ+НАДН Н+О 2 +Н 3 РО 4 АТФ + НАД+ +Н 2 О

Дыхательная цепь это комплекс специфических белков, встроенных в мембрану митохондрий, способных транспортировать электроны от восстановленных эквивалентов на кислород. Электроны, поступающие в эту цепь переносчиков, богаты энергией, по мере продвижения их по цепи, от одного переносчика к другому, они теряют свободную энергию. Значительная часть этой энергии запасается в виде АТФ.
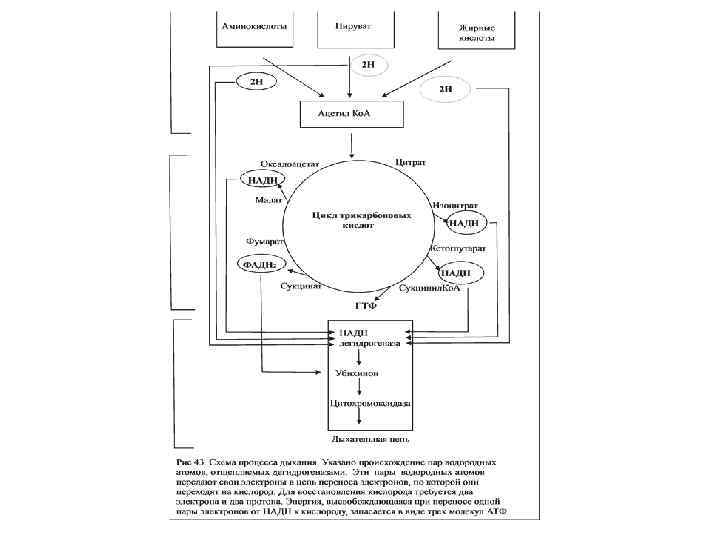

Дыхательная цепь состоит из: 1. Пиридинзависимых дегидрогеназ, которые в качестве коферментов содержат НАД либо НАДФ 2. Флавинзависимых дегидрогеназ, у которых роль простетической группы выполнят ФАД или ФМН. 3. Убихинона коэнзим Q 4. Цитохромов – белков содержащих гем.
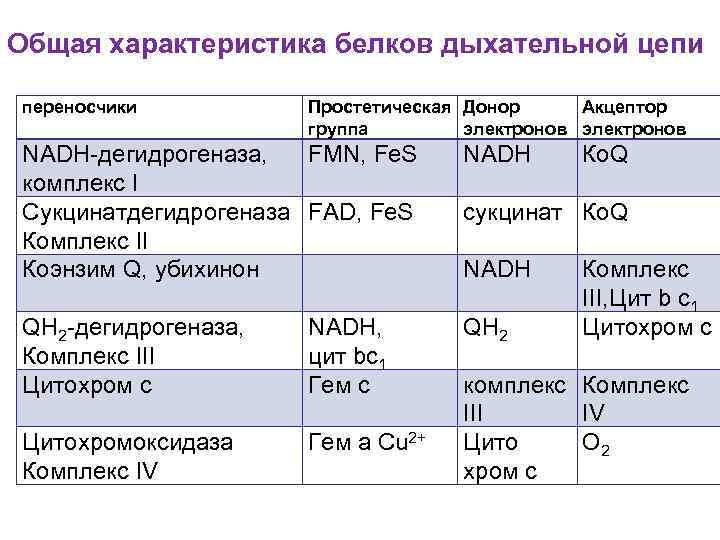
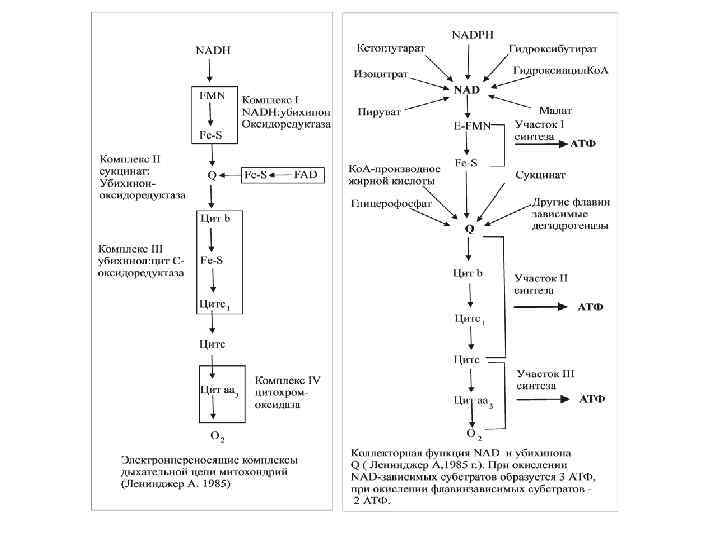
Общая характеристика белков дыхательной цепи переносчики Простетическая Донор Акцептор группа электронов NADH дегидрогеназа, FMN, Fe. S комплекс I Сукцинатдегидрогеназа FAD, Fe. S Комплекс II Коэнзим Q, убихинон NADH QH 2 дегидрогеназа, Комплекс III Цитохром с NADH, цит bс1 Гем с QH 2 Цитохромоксидаза Комплекс IV Гем а Cu 2+ Ко. Q сукцинат Ко. Q NADH Комплекс III, Цит b c 1 Цитохром с комплекс Комплекс III IV Цито O 2 хром с
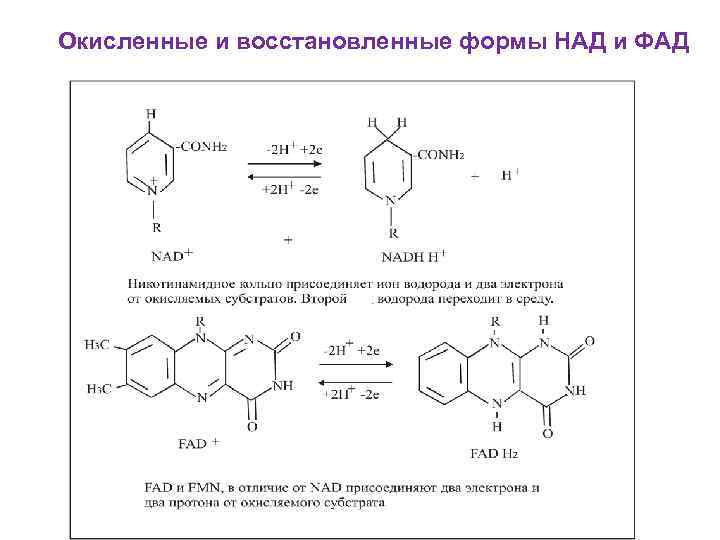
Окисленные и восстановленные формы НАД и ФАД

Убихинон Q является производным бензохинона с длинной боковой цепью, которая в большинстве тканей млекопитающих состоит из 10 изопреновых единиц. Восстановленная форма флавиновых ферментов в цепи дыхательных катализаторов передает атомы водорода Ко. Q. Как всякий хинон Ко. Q может существовать в окисленной и восстановленной формах Окисленная и восстановленная форма убихинона

Цитохромы Дальнейший перенос электронов от Ко. Q на кислород осуществляет система цитохромов. Цитохромы это гемопротеины 5 типов b, c, c 1, a, a 3, Внутри комплекса III электроны передаются от цитохромов b на железосерные центры, потом на цитохром с1, а затем на цитохром с. Цитохромы а и а 3 (цитохромоксидаза) образуют IV комплекс переносчиков электронов. Особенность химического строения цитохромоксидазы заключается в наличии ионов меди, меняющих свою валентность. Цитохромоксидаза непосредственно реагирует с молекулярным кислородом.
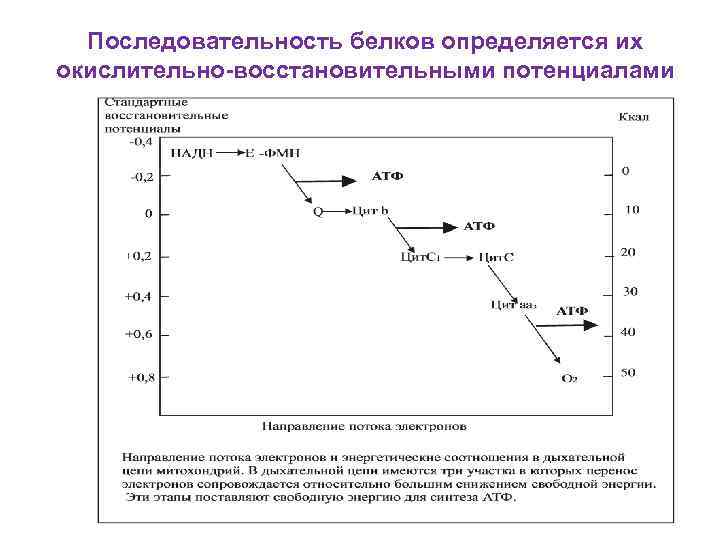
Последовательность белков определяется их окислительно-восстановительными потенциалами

• В каждом из 3 пунктов: • 1 -й пункт - это НАДН-дегидрогеназный комплекс; • 2 -й пункт - QН 2 -цитохром -с-редуктазный комплекс; • 3 -й пункт - цитохром-с-оксидазный комплекс • при переносе пары электронов от НАДН 2 одновременно на наружную поверхность внутренней мембраны Мх, т. е. в межмембранное пространство выносится по паре протонов.

Теории сопряжения окисления (переноса электронов) и фосфорилирования (синтеза АТФ) Каким же образом энергия электронов запасается в виде АТФ? Самыми первыми гипотезами сопряжения окисления и фосфорилирования были химическая и механохимическая гипотезы, предполагавшие наличие некого промежуточного, высокоэнергетического вещества преобразующего энергию электронов в энергию АТФ. В настоящее время эти гипотезы представляют исторический интерес. Современной теорией сопряжения является хемиосмотическая теория английского биохимика Питера Митчелла (1961 г. ). Суть этой теории заключается в том, что при прохождении электронов по дыхательной цепи высвобождается энергия, которая используется для перемещения протонов из матрикса в межмембранное пространство. Особое значение в транспорте водорода в межмембранное пространство отводится Ко. Q, который является липофильным веществом и может легко перемещаться по мембране
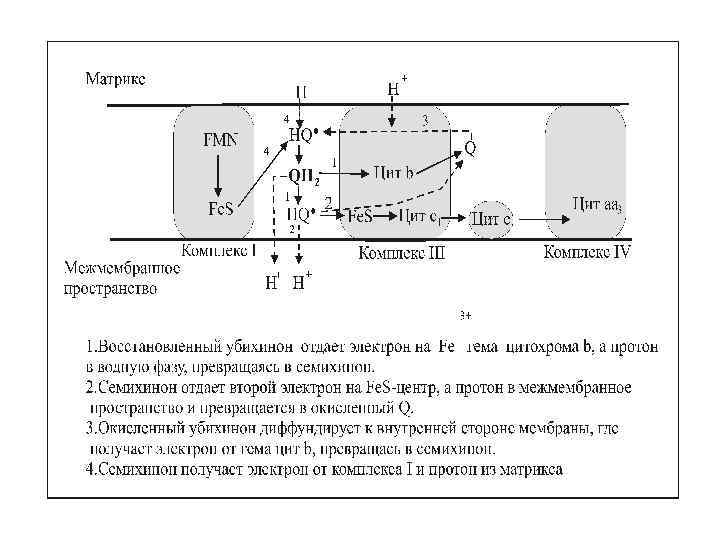

В результате между двумя сторонами внутренней мембраны создается электрохимический протонный градиент: н = + z р Н, - мембранный потенциал (разница зарядов наружной и внутренней, отрицательной поверхности мембраны) z р Н – градиент р. Н ( формируется за счет более кислой среды межмембранного пространства)
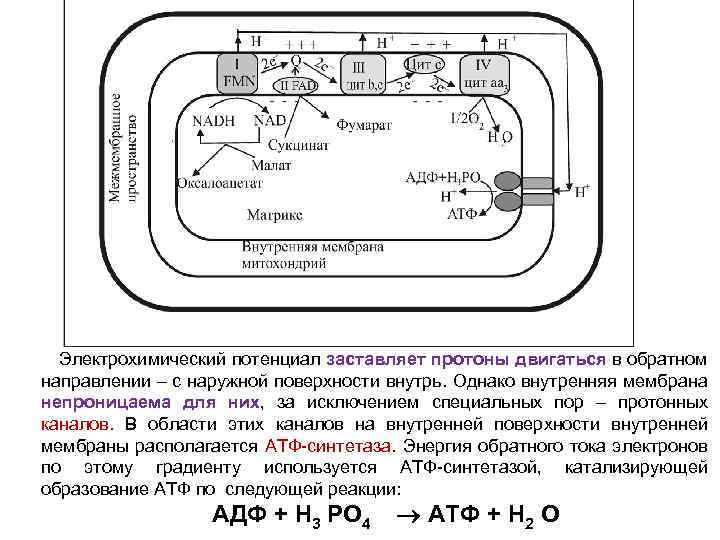
Электрохимический потенциал заставляет протоны двигаться в обратном направлении – с наружной поверхности внутрь. Однако внутренняя мембрана непроницаема для них, за исключением специальных пор – протонных каналов. В области этих каналов на внутренней поверхности внутренней мембраны располагается АТФ синтетаза. Энергия обратного тока электронов по этому градиенту используется АТФ синтетазой, катализирующей образование АТФ по следующей реакции: АДФ + Н 3 РО 4 АТФ + Н 2 О

АТФ синтетаза – интегральный белок внутренней мембраны митохондрий. Он расположен в непосредственной близости к дыхательной цепи. АТФ синтетаза состоит из 2 белковых комплексов, обозначаемых как F 0 и F 1. Гидрофобный комплекс F 0 погружен в мембрану. Он служит основанием, которое фиксирует АТФ синтетазу в мембране. Комплекс F 0 состоит из нескольких субъединиц, образующих канал, по которому протоны переносятся в матрикс.

Комплекс F 1 выступает в митохондриальный матрикс. Он состоит из 9 субъединиц, которые образуют сферический вырост. Повышение концентрации протонов в межмембранном пространстве активирует АТФ синтетазу. Электрохимический потенциал заставляет протоны двигаться по каналу АТФ синтетазы в матрикс. Параллельно под действием электрохимического потенциала происходит конформационное изменение субъединиц F 1 комплекса, в результате чего из АДФ и неорганического фосфата образуется АТФ. Образующаяся АТФ, при участии фермента адениннуклеотидтранслоказы с абсолютной специфичностью, транспортируется из матрикс на наружную сторону мембраны и попадает в цитозоль. АДФ транспортируется за счет антипорта АТФ. Фосфат транспортируется по типу симпорта с ионами водорода при участии фермента фосфаттранслоказы.

ИНГИБИТОРЫ ДЫХАТЕЛЬНОЙ ЦЕПИ И ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ Ингибиторы можно разделить на 3 группы: 1) Ингибиторы собственно дыхательной цепи; 2)Ингибиторы окислительного фосфорилирования; 3)Разобщители окислительного фосфорилирования.

1) Ингибиторы, блокирующие дыхательную цепь, могут действовать в 3 местах, соответствующих трем комплексам дыхательной цепи: В первом комплексе дыхательная цепь ингибируется барбитуратами (например, амобарбиталом), а также ротеноном (высокотоксичное в-во, добываемое из растений, которое использовалось американскими индейцами в качестве яда при ловле рыб). Эти ингибиторы препятствуют НАД-зависимому окислению субстратов.

• Второй участок, где может блокироваться дыхательная цепь это участок между цитохромом b и цитохромом с, т. е. во втором комплексе. Таким ингибитором является антибиотик антимицин А. • Третий участок это цитохромоксидаза. Он ингибируется классическими ядами - сернистым водородом, окисью углерода и цианидом.

• 2) К ингибиторам, подавляющим стадию фосфорилирования относится антибиотик олигомицин. Он полностью блокирует окисление и фосфорилирование в интактных митохондриях за счет того, что не пропускает протоны через канал F 0. • Атрактилозид также ингибирует окислительное фосфорилирование. Он ингибирует фермент - транслоказу, который производит поступление АДФ в митохондрию и выход АТФ из митохондрий.

Разобщители отличаются тем, что они нарушают систему сопряжения процессов окисления в дыхательной цепи и фосфорилирования. В этих условиях процесс дыхания происходит неконтролируемым образом. Т. е. концентрации АДФ и Рi в этом случае не являются лимитирующими. • Различают разные типы разобщения

Механизм разобщения: Снижение электрохимического градиента н. Устранение мембранного потенциала и/или протонного градиента. Динитрофенол - градиент протонов Валиномицин – перенос ионов калия Грамицидин – перенос ионов калия, натрия

Разобщители, как правило легко растворимы в липидном слое мембран, этим и объясняется их действие как разобщителей. • Среди разобщителей надо назвать некоторые лекарственные вещества: строфантин, папаверин, салицилаты. • Разобщителями могут быть и собственные соединения организма, его естественные метаболиты, например, жирные кислоты. Это имеет большое значение для организма на

Снижение температуры возбуждает терморецепторы, это ведет к повышению выделения норадреналина. Затем увеличивается липолиз, повышается содержание ВЖК, увеличивается концентрация ацетил-Ко. А. Это ведет к повышению активности цикла Кребса, повышению содержания НАДН и ФАДН 2. Увеличивается активность тканевого дыхания, возрастает электрохимический потенциал.

• ВЖК снижают электрохимический потенциал, синтез АТФ снижается, но н будет расходоваться на согревание. При этом на холоде человек дрожит. Рефлекторно возникает возбуждение терморецепторов, снижается содержание АТФ, увеличивается АДФ. Активируется ЦТК. Увеличивается концентрация НАДН, повышается электрохимический потенциал - человек согревается.

Гормоны это химические соединения, синтезируемые специализированными (эндокринными) железами в очень малых концентрациях (нмоль/л, пмоль/л), оказывающие действие вдали от места синтеза (дистантность), обладающие высокой биологической активностью (эффект усиления).
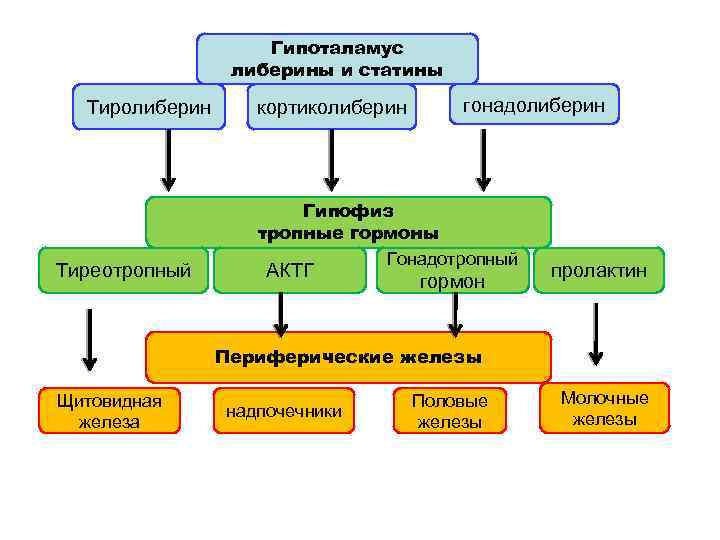
Гипоталамус либерины и статины Тиролиберин Тиреотропный кортиколиберин гонадолиберин Гипофиз тропные гормоны Гонадотропный АКТГ гормон пролактин Периферические железы Щитовидная железа надпочечники Половые железы Молочные железы

Классификация и механизм действия гормонов Существует несколько видов классификации гормонов: 1. По железам внутренней секреции разделяют: гормоны гипоталамуса, гипофиза, щитовидной, паращитовидной, поджелудочной желез и т. д. 2. По биологическому действию можно выделить гормоны, влияющие на углеводный, белковый, липидный обмен, минеральный, водно солевой обмены.

3. По химической природе гормоны делят на: а) Белки и пептиды– к ним относятся, например, гормоны гипоталамуса, гипофиза, инсулин, глюкагон б) Гликопротеины – тиреотропный гормон, ФСГ, ЛГ в) Производные аминокислот – адреналин, тироксин, трийодтиронин г) Стероидные: гормоны коры надпочечников, половые гормоны

По механизму действия гормоны подразделяют на: 1. мембранный механизм действия – для гормонов, влияющих на структуру и проницаемость мембраны клеток, например белковые гормоны, адреналин, инсулин. 2. внутриклеточный механизм действия для гидрофобных гормонов, которые могут приникать внутрь клетки (стероиды и гормоны щитовидной железы)

Классификация является условной, т. к. практически очень трудно выявить механизм действия гормонов. В последнее время в молекулярной биологии используется классификация гормонов по физико-химическим свойствам (полярности). Все гормоны подразделяются на две неравные группы: I. полярные, или гидрофильные гормоны — белки, пептиды и производные аминокислот (кроме тиреоидных гормонов). II. неполярные, или гидрофобные гормоны — стероиды (половые гормоны и гормоны коры надпочечников. ) и тиреоидные гормоны.

Механизм действия гормонов Подразделение гормонов на гидрофильные и гидрофобные имеет принципиальное значение, т. к. связано с механизмом действия. а) Гидрофильные гормоны не способны проникать через плазмолемму. Должен существовать специальный механизм для восприятия сигнала и передачи его на эффекторные структуры. б) Гидрофобные же гормоны проходят через мембраны клетки и действуют внутриклеточно (в «сопровождении» специального рецепторного белка, достигают определенных областей хромосом).

Общая схема действия гидрофильных гормонов Для каждого гидрофильного (полярного) гормона на по верхности клеток мишеней имеются белки-рецепторы. Возбуждение рецептора гормоном ведет к изменению концентрации в клетке определенного внутриклеточного медиатора. Такими медиаторами (вторичным посредником) могут быть ц. АМФ, ц. ГМФ, Инозитолтрифосфат оксид азота (N 0), эйкозаноиды, и т. д.

ц. АМФ Гормоны, взаимодействие которых с рецепторами клетки мишени приводит к образованию ц. АМФ, действуют через трехкомпонентную систему. Эта система (еще ее называют аденилатциклазной) включает белок рецептор, G белок и фермент аденилатциклазу. G белок состоит из 3 субъединиц , , . В отсутствии гормонального сигнала эти субъединицы связаны между собой, а субъединица еще связана с ГМФ. Субъединица бывает двух типов стимулирующего ( s) и ингибирующего ( I). G белок контактирует с рецептором, воспринимающим внешний сигнал.

Связывание гормона с рецептором приводит к изменению структуры G белка: 1. вначале субъединица теряет сродство к ГМФ и заменяет его на ГТФ 2. В связанном с ГТФ состоянии субъединица высвобождается из комплекса, диффундирует по внутренней поверхности и активирует (если это s) или ингибирует ( если I) аденилатциклазу 3. через некоторое время ГТФ гидролизуется до ГМФ, в результате чего субъединица отделяется от АЦ и связывается с другими субъединицами G белка (т. е. возвращается в исходное состояние) 4. Аденилатциклаза синтезирует из АТФ циклический аденозинмонофосфат (ц. АМФ) 5. ц. АМФ активирует протеинкиназу

Протеинкиназы (ПК) — специальные регуляторные ферменты, способные фосфорилировать (за счет фосфатных групп АТФ) строго определенные белки, причем по строго определенным аминокислотным остаткам серина, треонина или тирозина (все эти аминокислоты содержат в радикале гидроксильную группу). Фосфорилирование (и обратное ему дефосфорилирование под действием протеинфосфатаз) — один из наиболее универсальных способов регуляции активности белков — как структурных, так и ферментов (см. регуляцию активности ферментов). Такая химическая модификация белка меняет его конфигурацию. В итоге в одних случаях активность белка в результате фосфорилирования повышается, в других — напротив, снижается. ц. АМФ гидролизуется фосфодиэстеразой. Ингибиторы фосфодиэстеразы (кофеин, например), увеличивая внутриклеточный уровень ц. АМФ, усиливают действие гормонов.

Инозитолтрифосфат является вторичным посредником для гормонов, связывающихся с рецептором подобному 2 адренорецептору, который активирует G белок, последний, в свою очередь, стимулирует фосфолипазу С. Основным субстратом этого фермента является мембранный липид – фосфатидилинозитолдифосфат (см химию липидов). При действии гормона в мембране клеток мишеней увеличивается активность фосфолипазы С, которая расщепляет фосфатидилинозитол 4 5 дифосфат на инозитол-1, 4, 5 трифосфат (ИТФ) и диацилглицерол (ДАГ). ИТФ как полярное вещество легко диффундирует внутри клетки, связываясь с кальцевыми каналами плазмолеммы и эндоплазматического ретикулума. В результате чего повышается концентрация кальция. Кальций активирует белки ферменты, кальмодулин. Кальций зависимыми ферментами являются, например, киназа фосфорилазы, пируваткарбоксилаза, дегидрогеназы, киназа гликогенсинтетазы.

Диацилглицерол неполярное гидрофобное вещество, которое способно лишь к латеральной диффузии в составе плазмолеммы. Он активирует еще один мембраносвязанный регуляторный фермент – протеинкиназу С (ПК С). У ПК С множество белков мишеней, что и определяет физиологический ответ.

В регуляторной цепочке нередко имеется не одна ПК (протеинкиназа), а каскад из двух или даже более протеинкиназ. Первая из них (которая непосредственно активируется вторичным посредником фосфорилирует другую ПК, а эта вторая ПК действует уже на непосредственные объекты регуляции. В качестве последних могут быть ключевые ферменты метаболизма, структурные белки, факторы транскрипции или трансляции. Фосфорилирование или дефосфорилирование каких то из этих белков и вызывает тот конечный эффект, который «требовал» от клетки действующий на нее гормональный сигнал: • изменяется активность соответствующих ферментов или структурных белков, • изменяется активность соответствующих генов и скорость синтеза ферментов или структурных белков.

Общая схема действия гидрофобных гормонов Для гидрофобных (неполярных) гормонов мембранные рецепторы не требуются: как уже отмечалось, эти гормоны диффундируют через плазмолемму клетки мишени. Правда, отсюда следует, что они могут проникать и в любые другие клетки. Но в цитоплазме (или в ядрах) клеток мишеней содержатся специфические рецепторные белки, связывающие соответствующие гормоны. Благодаря этому, диффузия гормона в клетку мишень оказывается значительно более интенсивной, чем в прочие клетки.

Комплекс рецептор гормон (если он образуется в цитоплазме) проникает в клеточное ядро, достигая тех или иных генов, причем активность одних генов может возрастать, а других (в той же клетке) — уменьшаться.

Комплекс рецептор гормон влияет на сродство определенных транскрипционных факторах (ТЕ) к соответствующим участкам ДНК (энхансерам). В каких то случаях это сродство повышается и тогда РНК полимераза с большей скоростью связывается с промотором регулируемого гена, начинает считывать информацию, т. е. стимулируется транскрипция, а с ней и синтез определенного белка. В других случаях, напротив, сродство ТР к энхансеру снижается и синтез белка тормозится. Не исключено также, что комплекс рецептор гормон и сам может выступать в роли транскрипционного фактора.
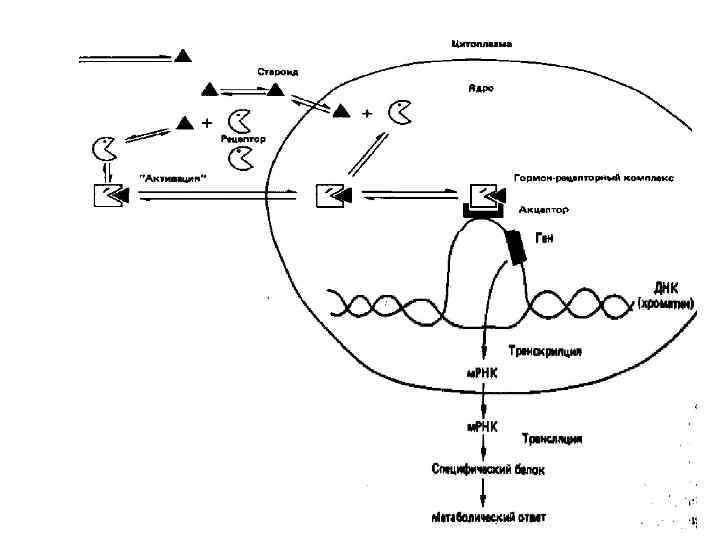
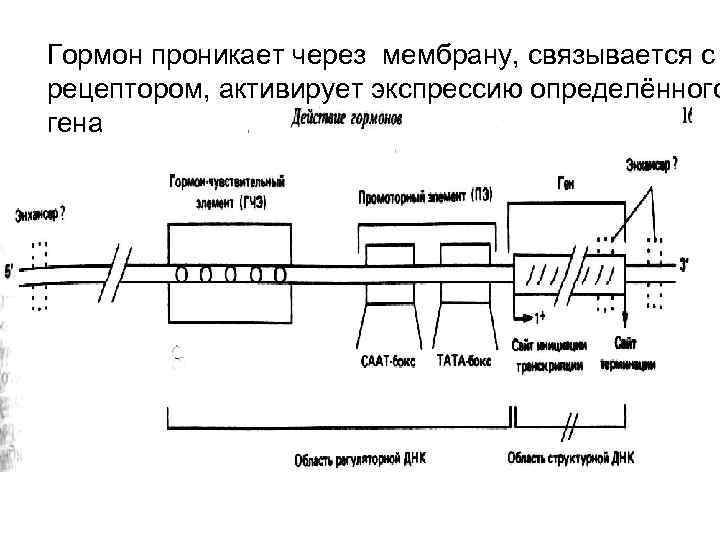
Гормон проникает через мембрану, связывается с рецептором, активирует экспрессию определённого гена

Итак, если гидрофильные гормоны могут влиять как на активность ферментов (белков), так и на их синтез, то гидрофобные гормоны лишь на синтез белков, реализуемое на генном уровне.
Дыхательная цепь.ppt