ЖИДКОЕ СОСТОЯНИЕ ВЕЩЕСТВА.pptx
- Количество слайдов: 12
 ЖИДКОЕ СОСТОЯНИЕ ВЕЩЕСТВА презентация по химии Выполнил Ученик 11 Б класса Анцыгин Даниил
ЖИДКОЕ СОСТОЯНИЕ ВЕЩЕСТВА презентация по химии Выполнил Ученик 11 Б класса Анцыгин Даниил
 План презентации Особенности жидкостей Физические св-ва воды Вода в природе Жесткость воды
План презентации Особенности жидкостей Физические св-ва воды Вода в природе Жесткость воды
 Особенности жидкого состояния вещества Текучи, т. е. не имеют формы , а принимают форму сосуда, в котором находятся В состоянии невесомости принимают форму шара или круглой капли Молекулы находятся непосредственно друг возле друга, поэтому жидкости – мало сжимаемы, в отличие от газов
Особенности жидкого состояния вещества Текучи, т. е. не имеют формы , а принимают форму сосуда, в котором находятся В состоянии невесомости принимают форму шара или круглой капли Молекулы находятся непосредственно друг возле друга, поэтому жидкости – мало сжимаемы, в отличие от газов
 Вода в природе Важнейшим жидким веществом является вода, которая покрывает 2/3 поверхности Земли. 97, 2% общего запаса приходится на воды Мирового океана. Запас пресной воды на Земле всего 2, 8%, но из них пригодна к использованию лишь 0, 3% водных ресурсов. Животные, растения и человек на 70 -80 % состоят из воды, потеря 15 -20 % массы тела в результате обезвоживания приводит к гибели организма. Благодаря круговороту воды в природе её запасы практически неисчерпаемы. Круговорот воды состоит из 2 процессов: испарения и конденсации.
Вода в природе Важнейшим жидким веществом является вода, которая покрывает 2/3 поверхности Земли. 97, 2% общего запаса приходится на воды Мирового океана. Запас пресной воды на Земле всего 2, 8%, но из них пригодна к использованию лишь 0, 3% водных ресурсов. Животные, растения и человек на 70 -80 % состоят из воды, потеря 15 -20 % массы тела в результате обезвоживания приводит к гибели организма. Благодаря круговороту воды в природе её запасы практически неисчерпаемы. Круговорот воды состоит из 2 процессов: испарения и конденсации.
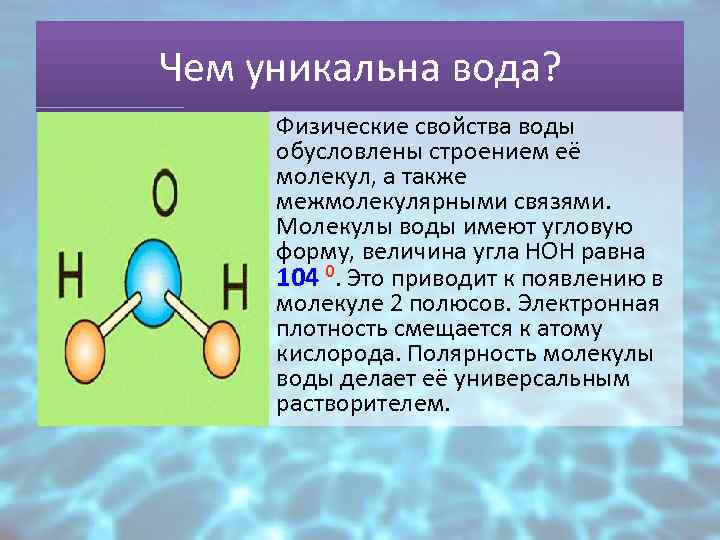 Чем уникальна вода? Физические свойства воды обусловлены строением её молекул, а также межмолекулярными связями. Молекулы воды имеют угловую форму, величина угла НОН равна 104 0. Это приводит к появлению в молекуле 2 полюсов. Электронная плотность смещается к атому кислорода. Полярность молекулы воды делает её универсальным растворителем.
Чем уникальна вода? Физические свойства воды обусловлены строением её молекул, а также межмолекулярными связями. Молекулы воды имеют угловую форму, величина угла НОН равна 104 0. Это приводит к появлению в молекуле 2 полюсов. Электронная плотность смещается к атому кислорода. Полярность молекулы воды делает её универсальным растворителем.
 Вода имеет аномально высокую температуру плавления и кипения Н 2 О – М(Н 2 О) = 18 г/ моль +100 0 Жидкость! Н 2 S – M(H 2 S) = 34 г/ моль -50 0 Газ Н 2 Se – M (H 2 Se)= 81 г/ моль - 420 Газ Н 2 Те – М(Н 2 Те) = 130 г/ моль 00 Газ В группах с увеличением молекулярной массы соединений увеличиваются температуры кипения и плавления веществ. ПРИЧИНА ВЫВОД Сравнение молекулярных масс воды и других гибридов элементов 6 А группы с их температурами кипения Аномально высокой температуры кипения воды наличие межмолекулярных водородных связей.
Вода имеет аномально высокую температуру плавления и кипения Н 2 О – М(Н 2 О) = 18 г/ моль +100 0 Жидкость! Н 2 S – M(H 2 S) = 34 г/ моль -50 0 Газ Н 2 Se – M (H 2 Se)= 81 г/ моль - 420 Газ Н 2 Те – М(Н 2 Те) = 130 г/ моль 00 Газ В группах с увеличением молекулярной массы соединений увеличиваются температуры кипения и плавления веществ. ПРИЧИНА ВЫВОД Сравнение молекулярных масс воды и других гибридов элементов 6 А группы с их температурами кипения Аномально высокой температуры кипения воды наличие межмолекулярных водородных связей.
 Еще одна аномалия воды Лёд благодаря водо- родным связям имеет ячеистое строение и поэтому легче воды. Плотность его 0, 92 г/ см 3
Еще одна аномалия воды Лёд благодаря водо- родным связям имеет ячеистое строение и поэтому легче воды. Плотность его 0, 92 г/ см 3
 Бывает ли вода «жесткой» ? n Природная вода, содержащая в растворе большое количество солей кальция и магния называется водой. Жесткость природных вод может меняться в зависимости от года: она понижается зимой, а летом – повышается. Содержание солей кальция и магния в воде зависит и от состава почвы в водоносных слоях. жесткой n n
Бывает ли вода «жесткой» ? n Природная вода, содержащая в растворе большое количество солей кальция и магния называется водой. Жесткость природных вод может меняться в зависимости от года: она понижается зимой, а летом – повышается. Содержание солей кальция и магния в воде зависит и от состава почвы в водоносных слоях. жесткой n n
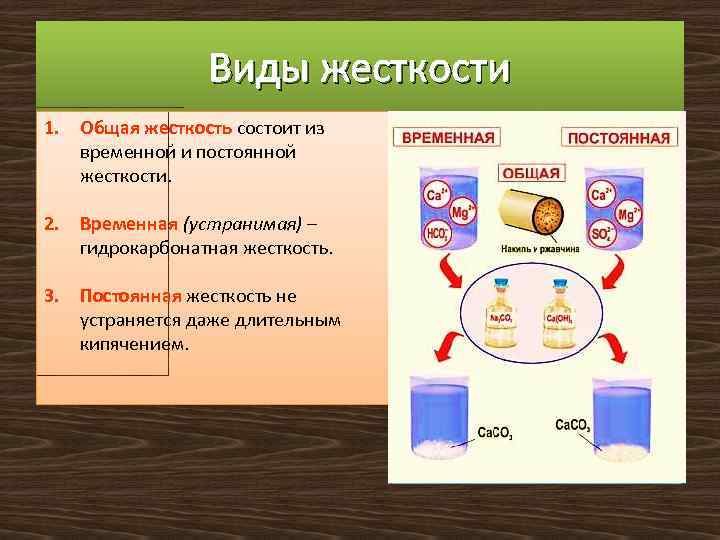 Виды жесткости 1. Общая жесткость состоит из временной и постоянной жесткости. 2. Временная (устранимая) – гидрокарбонатная жесткость. 3. Постоянная жесткость не устраняется даже длительным кипячением.
Виды жесткости 1. Общая жесткость состоит из временной и постоянной жесткости. 2. Временная (устранимая) – гидрокарбонатная жесткость. 3. Постоянная жесткость не устраняется даже длительным кипячением.
 Виды жесткости ГИДРОКАРБОНАТНАЯ жесткость зависит от содержания в воде гидрокарбонатов кальция и магния Са(НСО 3)2, Mg(HCO 3)2 КИСЛЫЕ СОЛИ НЕКАРБОНАТНАЯ жесткость вызвана присутствием в воде других солей, например сульфатов кальция и магния Са. SO 4, Mg. SO 4 продукт неполного замещения атомов водорода в кислоте
Виды жесткости ГИДРОКАРБОНАТНАЯ жесткость зависит от содержания в воде гидрокарбонатов кальция и магния Са(НСО 3)2, Mg(HCO 3)2 КИСЛЫЕ СОЛИ НЕКАРБОНАТНАЯ жесткость вызвана присутствием в воде других солей, например сульфатов кальция и магния Са. SO 4, Mg. SO 4 продукт неполного замещения атомов водорода в кислоте
 1. Жесткая вода – это накипь на деталях бытовой техники, стенках котлов и радиаторов. 2. В жесткой воде плохо разваривается мясо. 3. В жесткой воде не мылится мыло.
1. Жесткая вода – это накипь на деталях бытовой техники, стенках котлов и радиаторов. 2. В жесткой воде плохо разваривается мясо. 3. В жесткой воде не мылится мыло.
 Устранение жесткости Кипячение переводит растворимые гидрокарбонаты в нерастворимые карбонаты. Са(НСО 3)2 =Са. СО 3+Н 2 О+СО 2 Метод осаждения и ионного обмена переводит ионы Са 2+ и Мg 2+ в нерастворимые соединения. При помощи изв. воды удаляется временная жесткость Сa(HCO 3)2+Ca(OH)2=2 Ca. CO 3+2 H 2 O+2 CO 2↑ При помощи кальцинированной соды удаляется постоянная жесткость Ca. Cl 2+Na 2 CO 3=Ca. CO 3↓+2 Na. Cl
Устранение жесткости Кипячение переводит растворимые гидрокарбонаты в нерастворимые карбонаты. Са(НСО 3)2 =Са. СО 3+Н 2 О+СО 2 Метод осаждения и ионного обмена переводит ионы Са 2+ и Мg 2+ в нерастворимые соединения. При помощи изв. воды удаляется временная жесткость Сa(HCO 3)2+Ca(OH)2=2 Ca. CO 3+2 H 2 O+2 CO 2↑ При помощи кальцинированной соды удаляется постоянная жесткость Ca. Cl 2+Na 2 CO 3=Ca. CO 3↓+2 Na. Cl


