Жидкие и твёрдые вещества








![Методы определения жёсткости воды • Карбонатная жёсткость (временная) [Жв. ] – метод кислотно-основного Методы определения жёсткости воды • Карбонатная жёсткость (временная) [Жв. ] – метод кислотно-основного](https://present5.com/presentation/3/179770264_341228179.pdf-img/179770264_341228179.pdf-9.jpg)










 Жидкие и твёрдые вещества
Жидкие и твёрдые вещества
 Жидкость — одно из агрегатных состояний вещества.
Жидкость — одно из агрегатных состояний вещества.
 Жидкие вещества Свойства жидких веществ: • Молекулы находятся друг возле друга, поэтому при попытке изменить объем жидкости начинается деформация самих молекул, то есть жидкости малосжимаемы. • Они текучи, то есть не имеют своей формы и принимают форму сосуда. • Если жидкость поместить в условия невесомости, то она примет форму шара или капли.
Жидкие вещества Свойства жидких веществ: • Молекулы находятся друг возле друга, поэтому при попытке изменить объем жидкости начинается деформация самих молекул, то есть жидкости малосжимаемы. • Они текучи, то есть не имеют своей формы и принимают форму сосуда. • Если жидкость поместить в условия невесомости, то она примет форму шара или капли.
 Вода – самое уникальное вещество на планете. • Самое уникальное вещество на нашей планете – это вода. • Животные, растения, человек на 70 -80% состоят из воды. • Все реакции обмена веществ в организме человека – это реакции гидролиза. • Без воды невозможно существование биосферы, потому что круговорот веществ и энергии возможен с участием воды.
Вода – самое уникальное вещество на планете. • Самое уникальное вещество на нашей планете – это вода. • Животные, растения, человек на 70 -80% состоят из воды. • Все реакции обмена веществ в организме человека – это реакции гидролиза. • Без воды невозможно существование биосферы, потому что круговорот веществ и энергии возможен с участием воды.
 Переход жидкостей из одного состояния в другое • Испарение — постепенный переход вещества из жидкости в газообразную фазу (пар). • Конденсация – это обратный процесс, переход вещества из газообразного состояния в жидкое. При этом в жидкость переходит из пара больше молекул, чем в пар из жидкости. • Кипение – это процесс парообразования внутри жидкости. • Смачивание — поверхностное явление, возникающее при контакте жидкости с твёрдой поверхностью в присутствии пара, то есть на границах раздела трёх фаз. • Смешиваемость— способность жидкостей растворяться друг в друге. Пример смешиваемых жидкостей: вода и этиловый спирт, пример несмешиваемых: вода и жидкое масло.
Переход жидкостей из одного состояния в другое • Испарение — постепенный переход вещества из жидкости в газообразную фазу (пар). • Конденсация – это обратный процесс, переход вещества из газообразного состояния в жидкое. При этом в жидкость переходит из пара больше молекул, чем в пар из жидкости. • Кипение – это процесс парообразования внутри жидкости. • Смачивание — поверхностное явление, возникающее при контакте жидкости с твёрдой поверхностью в присутствии пара, то есть на границах раздела трёх фаз. • Смешиваемость— способность жидкостей растворяться друг в друге. Пример смешиваемых жидкостей: вода и этиловый спирт, пример несмешиваемых: вода и жидкое масло.
 Жесткость воды Жёсткость воды – это совокупность химических и физических свойств воды, связанных с содержанием в ней растворённых солей щёлочноземельных металлов, главным образом, кальция и магния.
Жесткость воды Жёсткость воды – это совокупность химических и физических свойств воды, связанных с содержанием в ней растворённых солей щёлочноземельных металлов, главным образом, кальция и магния.
 Пресная природная вода Жесткая Мягкая
Пресная природная вода Жесткая Мягкая
 Жёсткая вода непригодна: • Для питания паровых котлов • Для применения в химической технологии • В производстве керамике, бетонных смесей • Приводит к нарушению работ теплосетей В жёсткой воде: • Мыло не образует пену; • Плохо развариваются овощи; • Не заваривается чай.
Жёсткая вода непригодна: • Для питания паровых котлов • Для применения в химической технологии • В производстве керамике, бетонных смесей • Приводит к нарушению работ теплосетей В жёсткой воде: • Мыло не образует пену; • Плохо развариваются овощи; • Не заваривается чай.
![>Методы определения жёсткости воды • Карбонатная жёсткость (временная) [Жв. ] – метод кислотно-основного >Методы определения жёсткости воды • Карбонатная жёсткость (временная) [Жв. ] – метод кислотно-основного](https://present5.com/presentation/3/179770264_341228179.pdf-img/179770264_341228179.pdf-9.jpg) Методы определения жёсткости воды • Карбонатная жёсткость (временная) [Жв. ] – метод кислотно-основного титрования. • Общая жёсткость [Жо. ] – метод комплексонометрии • Некарбонатная (постоянная) [Жп. ] – определяют по разности между Ж общая - Ж временная • Жв. (постоянная) = Ж общая - Ж временная
Методы определения жёсткости воды • Карбонатная жёсткость (временная) [Жв. ] – метод кислотно-основного титрования. • Общая жёсткость [Жо. ] – метод комплексонометрии • Некарбонатная (постоянная) [Жп. ] – определяют по разности между Ж общая - Ж временная • Жв. (постоянная) = Ж общая - Ж временная
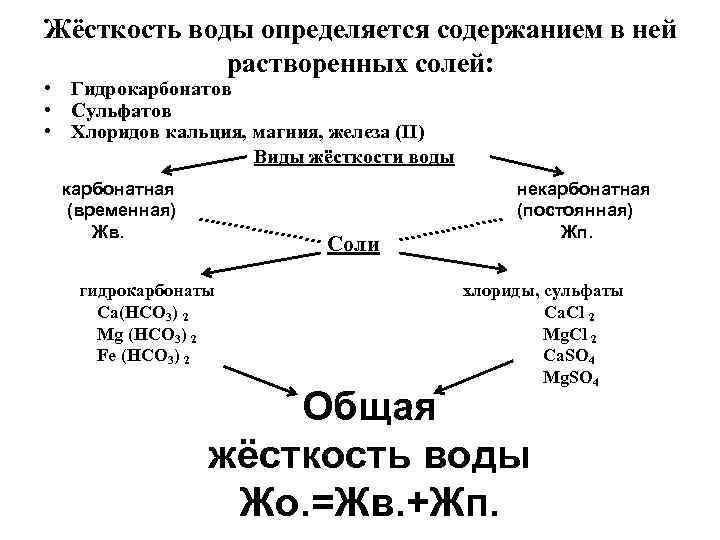
 Жёсткость воды определяется содержанием в ней растворенных солей: • Гидрокарбонатов • Сульфатов • Хлоридов кальция, магния, железа (II) Виды жёсткости воды карбонатная некарбонатная (временная) (постоянная) Жв. Жп. Соли гидрокарбонаты хлориды, сульфаты Ca(HCO 3) 2 Ca. Cl 2 Mg (HCO 3) 2 Mg. Cl 2 Fe (HCO 3) 2 Ca. SO 4 Mg. SO 4 Общая жёсткость воды Жо. =Жв. +Жп.
Жёсткость воды определяется содержанием в ней растворенных солей: • Гидрокарбонатов • Сульфатов • Хлоридов кальция, магния, железа (II) Виды жёсткости воды карбонатная некарбонатная (временная) (постоянная) Жв. Жп. Соли гидрокарбонаты хлориды, сульфаты Ca(HCO 3) 2 Ca. Cl 2 Mg (HCO 3) 2 Mg. Cl 2 Fe (HCO 3) 2 Ca. SO 4 Mg. SO 4 Общая жёсткость воды Жо. =Жв. +Жп.
 Способы устранения жесткости Различают общую жесткость, которая складывается из временной и постоянной: • Временная жесткость (устранимая или карбонатная) обусловлена присутствием в воде гидрокарбонатов Са(НСО 3)2 и Mg(НСО 3)2. Карбонатную жесткость легко устранить кипячением воды, при котором Са 2+ и Mg 2+ удаляются образуя нерастворимые осадки: • Са(НСО 3)2 → Cа. СО 3↓ + СО 2↑ + Н 2 О
Способы устранения жесткости Различают общую жесткость, которая складывается из временной и постоянной: • Временная жесткость (устранимая или карбонатная) обусловлена присутствием в воде гидрокарбонатов Са(НСО 3)2 и Mg(НСО 3)2. Карбонатную жесткость легко устранить кипячением воды, при котором Са 2+ и Mg 2+ удаляются образуя нерастворимые осадки: • Са(НСО 3)2 → Cа. СО 3↓ + СО 2↑ + Н 2 О
 Способы устранения временной жесткости • Для уменьшения карбонатной жесткости применяется метод известкования, при котором в обрабатываемую воду вводят известь Са(ОН)2. Реакции, протекающие при введении извести, можно записать в молекулярной форме: • Са(НСО 3)2 + Са(ОН)2 → 2 Са. СО 3↓ + Н 2 О • Mg(НСО 3)2 + Са(ОН)2 → Mg(ОН)2↓ + 2 Са. СО 3 + Н 2 О
Способы устранения временной жесткости • Для уменьшения карбонатной жесткости применяется метод известкования, при котором в обрабатываемую воду вводят известь Са(ОН)2. Реакции, протекающие при введении извести, можно записать в молекулярной форме: • Са(НСО 3)2 + Са(ОН)2 → 2 Са. СО 3↓ + Н 2 О • Mg(НСО 3)2 + Са(ОН)2 → Mg(ОН)2↓ + 2 Са. СО 3 + Н 2 О
 Способы устранения постоянной жесткости • Постоянная жесткость (неустранимая или некарбонатная) сохраняется при кипячении воды, поскольку постоянная жесткость обусловлена присутствием в воде сульфатов, хлоридов и других солей Са и Mg. Для снижения карбонатной жесткости обычно используют кальцинированную соду (Na 2 CO 3): • Mg. SO 4 + Na 2 CO 3 → Mg. CO 3↓ + Na 2 SO 4
Способы устранения постоянной жесткости • Постоянная жесткость (неустранимая или некарбонатная) сохраняется при кипячении воды, поскольку постоянная жесткость обусловлена присутствием в воде сульфатов, хлоридов и других солей Са и Mg. Для снижения карбонатной жесткости обычно используют кальцинированную соду (Na 2 CO 3): • Mg. SO 4 + Na 2 CO 3 → Mg. CO 3↓ + Na 2 SO 4
 Способы устранения жесткости • Лучшим реагентом для устранения общей жесткости воды является ортофосфат натрия Na 3 PO 4, входящий в состав большинства препаратов бытового и промышленного назначения: • 3 Ca(HCO 3)2 + 2 Na 3 PO 4 → Ca 3(PO 4)2↓ + 6 Na. HCO 3 • 3 Mg. SO 4 + 2 Na 3 PO 4 → Mg 3(PO 4)2↓ + 3 Na 2 SO 4
Способы устранения жесткости • Лучшим реагентом для устранения общей жесткости воды является ортофосфат натрия Na 3 PO 4, входящий в состав большинства препаратов бытового и промышленного назначения: • 3 Ca(HCO 3)2 + 2 Na 3 PO 4 → Ca 3(PO 4)2↓ + 6 Na. HCO 3 • 3 Mg. SO 4 + 2 Na 3 PO 4 → Mg 3(PO 4)2↓ + 3 Na 2 SO 4
 Твёрдые тела Твёрдое тело — это одно из четырёх агрегатных состояний вещества, отличающееся от других агрегатных состояний (жидкости, газов, плазмы) стабильностью формы и характером теплового движения атомов, совершающих малые колебания около положений равновесия.
Твёрдые тела Твёрдое тело — это одно из четырёх агрегатных состояний вещества, отличающееся от других агрегатных состояний (жидкости, газов, плазмы) стабильностью формы и характером теплового движения атомов, совершающих малые колебания около положений равновесия.
 Твердые вещества Кристаллические Аморфные Na. Cl, K 2 SO 4, Ca. CO 3
Твердые вещества Кристаллические Аморфные Na. Cl, K 2 SO 4, Ca. CO 3
 Аморфное вещество • Аморфные вещества – это твердые вещества, которые не имеют кристаллической решетки, сохраняющие свою форму достаточно долго, но через длительное время форма тел изменяется под действие температуры. • Примеры аморфных тел: Восковая свеча, шоколад, жевательная резинка, смола.
Аморфное вещество • Аморфные вещества – это твердые вещества, которые не имеют кристаллической решетки, сохраняющие свою форму достаточно долго, но через длительное время форма тел изменяется под действие температуры. • Примеры аморфных тел: Восковая свеча, шоколад, жевательная резинка, смола.
 • Аморфные вещества неустойчивые и рано или поздно переходят в кристаллические. • Например: А) аморфное стекло под влиянием ударных нагрузок образуются мелкие кристаллы, которые мутнеют. Б) Твердый мед, так же засахаривается с течением и при длительном хранении образуется стекловидная карамель. В) Пластическая сера S 8 представляет собой аморфное вещество и через некоторое время превращается в кристаллическую ромбическую серу с молекулярной решеткой.
• Аморфные вещества неустойчивые и рано или поздно переходят в кристаллические. • Например: А) аморфное стекло под влиянием ударных нагрузок образуются мелкие кристаллы, которые мутнеют. Б) Твердый мед, так же засахаривается с течением и при длительном хранении образуется стекловидная карамель. В) Пластическая сера S 8 представляет собой аморфное вещество и через некоторое время превращается в кристаллическую ромбическую серу с молекулярной решеткой.
 Задание 1 1) Na. Cl → Na. OH → Na 2 O 2) KOH → KO 3 → O 2 → K 2 O 4 → KOH 3) Na 2 O 2→ Na. OH → Na. HCO 3 → Na 2 CO 3→ Na. OH 4) Ca. CO 3→ Ca. O→ Ca. C 2 → Ca(OH)2 → Ca(HCO 3)
Задание 1 1) Na. Cl → Na. OH → Na 2 O 2) KOH → KO 3 → O 2 → K 2 O 4 → KOH 3) Na 2 O 2→ Na. OH → Na. HCO 3 → Na 2 CO 3→ Na. OH 4) Ca. CO 3→ Ca. O→ Ca. C 2 → Ca(OH)2 → Ca(HCO 3)
 Решение задания № 1 1) Цепочка: Na. Cl + H 2 O (e. t. ) = Na. OH + Cl 2 + H 2 Na. OH (e. t. ) = Na + H 2 O + O 2 Na + O 2 = Na 2 O 2 + Na = Na 2 O 2) Цепочка KOH + O 3 = KO 3 + O 2 + H 2 O KO 3 (t) = KO 2 + K = K 2 O 4 + H 2 O = KOH + O 2
Решение задания № 1 1) Цепочка: Na. Cl + H 2 O (e. t. ) = Na. OH + Cl 2 + H 2 Na. OH (e. t. ) = Na + H 2 O + O 2 Na + O 2 = Na 2 O 2 + Na = Na 2 O 2) Цепочка KOH + O 3 = KO 3 + O 2 + H 2 O KO 3 (t) = KO 2 + K = K 2 O 4 + H 2 O = KOH + O 2
 Решение задания № 1 3) Цепочка: Na 2 O 2 + H 2 O = Na. OH + O 2 Na. OH + CO 2 = Na. HCO 3 (t) = Na 2 CO 3 + H 2 O + CO 2 Na 2 CO 3 + Ba(OH)2 = Na. OH + Ba. CO 3 4) Цепочка: Ca. CO 3 (t) = Ca. O + CO 2 Ca. O + C (t) = Ca. C 2 + CO Ca. C 2 + H 2 O = Ca(OH)2 + C 2 H 2 Ca(OH)2 + CO 2 = Ca(HCO 3)2
Решение задания № 1 3) Цепочка: Na 2 O 2 + H 2 O = Na. OH + O 2 Na. OH + CO 2 = Na. HCO 3 (t) = Na 2 CO 3 + H 2 O + CO 2 Na 2 CO 3 + Ba(OH)2 = Na. OH + Ba. CO 3 4) Цепочка: Ca. CO 3 (t) = Ca. O + CO 2 Ca. O + C (t) = Ca. C 2 + CO Ca. C 2 + H 2 O = Ca(OH)2 + C 2 H 2 Ca(OH)2 + CO 2 = Ca(HCO 3)2

