 Жесткость воды
Жесткость воды
 Введение: Вода широко используется в нашей жизни. Среди множества экологических проблем, проблема чистой питьевой воды занимает не последнее место. Мыло в жесткой воде не мылится, овощи плохо развариваются, а при использовании такой воды в паровых котлах образуется накипь, которая снижает эффективность их работы и может привести к взрыву. Актуальность данной работы заключается в том, что водопроводная вода в нашем городе отличается повышенной жесткостью и признана непригодной для питья.
Введение: Вода широко используется в нашей жизни. Среди множества экологических проблем, проблема чистой питьевой воды занимает не последнее место. Мыло в жесткой воде не мылится, овощи плохо развариваются, а при использовании такой воды в паровых котлах образуется накипь, которая снижает эффективность их работы и может привести к взрыву. Актуальность данной работы заключается в том, что водопроводная вода в нашем городе отличается повышенной жесткостью и признана непригодной для питья.
 Цель: выявление жесткости воды в зависимости от источников и от времени года.
Цель: выявление жесткости воды в зависимости от источников и от времени года.
 Задачи: Анализ водопроводной воды осадочных воды р. Томь вод г. Кемерово
Задачи: Анализ водопроводной воды осадочных воды р. Томь вод г. Кемерово
 1. Жесткость воды В природе чистая вода не встречается. Существенное влияние на свойства воды оказывают растворенные в ней примеси. Наличие солей кальция и магния в воде обусловливает ее жесткость. Наличие в воде сульфатов и хлоридов кальция и магния обуславливает постоянную жесткость воды.
1. Жесткость воды В природе чистая вода не встречается. Существенное влияние на свойства воды оказывают растворенные в ней примеси. Наличие солей кальция и магния в воде обусловливает ее жесткость. Наличие в воде сульфатов и хлоридов кальция и магния обуславливает постоянную жесткость воды.
 Характеристика воды Жесткость, ммоль/дм 3 Мягкая Менее 4 Средней жесткости 4 -8 Жесткая 8 -12 Очень жесткая Более 12
Характеристика воды Жесткость, ммоль/дм 3 Мягкая Менее 4 Средней жесткости 4 -8 Жесткая 8 -12 Очень жесткая Более 12
 Взаимодействия Известь взаимодействует с солями магния и осаждает их в виде гидроокиси: Сода взаимодействует с солями кальция, образуя труднорастворимый карбонат кальция:
Взаимодействия Известь взаимодействует с солями магния и осаждает их в виде гидроокиси: Сода взаимодействует с солями кальция, образуя труднорастворимый карбонат кальция:
 Взаимодействия Для устранения постоянной жесткости используют содовый и фосфатный методы:
Взаимодействия Для устранения постоянной жесткости используют содовый и фосфатный методы:
 Взаимодействия Для устранения временной жесткости методом осаждения используют известковый, натронный и содовый методы:
Взаимодействия Для устранения временной жесткости методом осаждения используют известковый, натронный и содовый методы:
 Часть дождевых вод превращается в грунтовые воды. Однако для жизнедеятельности человеческого организма кальций и магний необходимы.
Часть дождевых вод превращается в грунтовые воды. Однако для жизнедеятельности человеческого организма кальций и магний необходимы.
 2. Методы и проведения исследования Метод основан на осаждении ионов Ca 2+ и Mg 2+ избытком раствора ортофосфата натрия Na 3 Po 4 споследующим определением остатка осадителя:
2. Методы и проведения исследования Метод основан на осаждении ионов Ca 2+ и Mg 2+ избытком раствора ортофосфата натрия Na 3 Po 4 споследующим определением остатка осадителя:
 Расчеты 1. Рассчитываем временную жесткость воды (ммоль/л) по формуле: Где. V’(HCl) – объем соляной кислоты, пошедшей на титрование, л; сэ(HCl)– молярная концентрация эквивалентна соляной кислоты, моль/л; V(H 2 O) – объем анализируемой воды, л; Vколбы– объем мерной колбы, л; Vпр – объем воды, взятой при титрования, л.
Расчеты 1. Рассчитываем временную жесткость воды (ммоль/л) по формуле: Где. V’(HCl) – объем соляной кислоты, пошедшей на титрование, л; сэ(HCl)– молярная концентрация эквивалентна соляной кислоты, моль/л; V(H 2 O) – объем анализируемой воды, л; Vколбы– объем мерной колбы, л; Vпр – объем воды, взятой при титрования, л.
 Расчеты 2. Рассчитываем общую жесткость (ммоль/л) по формуле: Где cэ(Na 3 PO 4)–молярная концентрация эквивалента Na 3 PO 4 , моль/л; V(Na 3 PO 4) – объем раствора Na 3 PO 4, добавленного к анализируемому объему воды, л; V(HCl) – объем соляной кислоты, израсходованной на определение остатка Na 3 PO 4, л; V’(HCl)- объем соляной кислоты, израсходованной на определение временной жесткости, л.
Расчеты 2. Рассчитываем общую жесткость (ммоль/л) по формуле: Где cэ(Na 3 PO 4)–молярная концентрация эквивалента Na 3 PO 4 , моль/л; V(Na 3 PO 4) – объем раствора Na 3 PO 4, добавленного к анализируемому объему воды, л; V(HCl) – объем соляной кислоты, израсходованной на определение остатка Na 3 PO 4, л; V’(HCl)- объем соляной кислоты, израсходованной на определение временной жесткости, л.
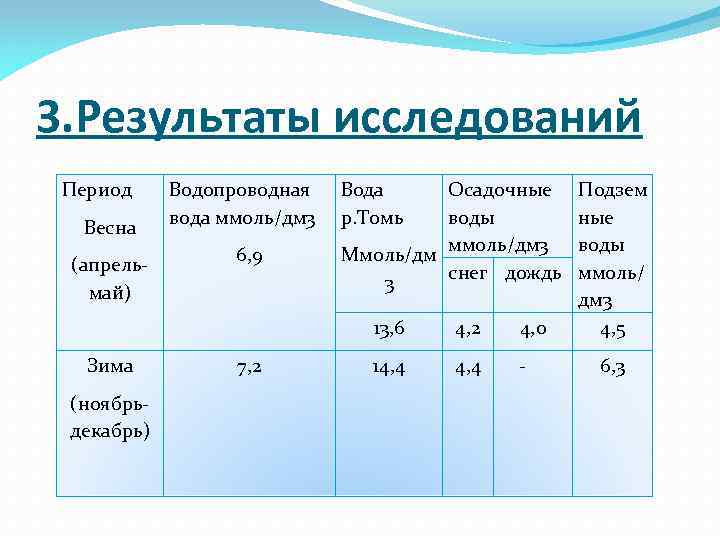 3. Результаты исследований Период Весна (апрельмай) Водопроводная вода ммоль/дм 3 6, 9 Вода р. Томь Осадочные воды Ммоль/дм ммоль/дм 3 снег дождь 3 13, 6 Зима (ноябрьдекабрь) 7, 2 4, 0 14, 4 - Подзем ные воды ммоль/ дм 3 4, 5 6, 3
3. Результаты исследований Период Весна (апрельмай) Водопроводная вода ммоль/дм 3 6, 9 Вода р. Томь Осадочные воды Ммоль/дм ммоль/дм 3 снег дождь 3 13, 6 Зима (ноябрьдекабрь) 7, 2 4, 0 14, 4 - Подзем ные воды ммоль/ дм 3 4, 5 6, 3
 Выводы: Водопроводная вода в зимнее время имеет повышенную жесткость, поэтому ее необходимо смягчать. Осадочные воды близки к мягким, их хорошо использовать для полива растений. Прежде чем использовать водопроводную воду в приготовлении пищи, ее нужно профильтровать.
Выводы: Водопроводная вода в зимнее время имеет повышенную жесткость, поэтому ее необходимо смягчать. Осадочные воды близки к мягким, их хорошо использовать для полива растений. Прежде чем использовать водопроводную воду в приготовлении пищи, ее нужно профильтровать.