ЖДА наш.ppt
- Количество слайдов: 72
 Железодефицитные анемии.
Железодефицитные анемии.
 Классификация анемий (Идельсон, 1979 г) 1. Анемии, связанные с кровопотерей. – Острая постгеморрагическая анемия. – Хроническая постгеморрагическая анемия 2. Анемии, связанные с нарушенным кровообразованием. – Анемии, связанные с нарушением образования гемоглобина. – Анемии, связанные с нарушением синтеза ДНК и РНК (мегалобластные анемии). – Анемии, связанные с нарушением процесса деления эритроцитов.
Классификация анемий (Идельсон, 1979 г) 1. Анемии, связанные с кровопотерей. – Острая постгеморрагическая анемия. – Хроническая постгеморрагическая анемия 2. Анемии, связанные с нарушенным кровообразованием. – Анемии, связанные с нарушением образования гемоглобина. – Анемии, связанные с нарушением синтеза ДНК и РНК (мегалобластные анемии). – Анемии, связанные с нарушением процесса деления эритроцитов.
 - Анемии, связанные с угнетением пролиферации клеток костного мозга. - Анемии, связанные с замещением кроветворного костного мозга опухолевым процессом. - Анемии, связанные с нарушением выработки эритропоэтина или появлением ингибиторов эритропоэтина. 3. Анемии, связанные с повышенным кроворазрушением. - Наследственные гемолитические анемии. - Приобретенные гемолитические анемии.
- Анемии, связанные с угнетением пролиферации клеток костного мозга. - Анемии, связанные с замещением кроветворного костного мозга опухолевым процессом. - Анемии, связанные с нарушением выработки эритропоэтина или появлением ингибиторов эритропоэтина. 3. Анемии, связанные с повышенным кроворазрушением. - Наследственные гемолитические анемии. - Приобретенные гемолитические анемии.
 Определение. n Анемия - уменьшение общего количества гемоглобина, чаще всего проявляющееся уменьшением его концентрации в единице объема крови. В большинстве случаев, за исключением железодефицитных состояний и талассемии, анемия сопровождается и снижением содержания эритроцитов в единице объема крови.
Определение. n Анемия - уменьшение общего количества гемоглобина, чаще всего проявляющееся уменьшением его концентрации в единице объема крови. В большинстве случаев, за исключением железодефицитных состояний и талассемии, анемия сопровождается и снижением содержания эритроцитов в единице объема крови.
 Гипохромные анемии, характеризующиеся снижением содержания гемоглобина в эритроците. Понятие "гипохромная анемия" является чисто лабораторным. Основным лабораторным признаком гипохромной анемии является низкий цветовой показатель (в норме 0, 85– 1, 05), отражающий, как известно, содержание гемоглобина в эритроците.
Гипохромные анемии, характеризующиеся снижением содержания гемоглобина в эритроците. Понятие "гипохромная анемия" является чисто лабораторным. Основным лабораторным признаком гипохромной анемии является низкий цветовой показатель (в норме 0, 85– 1, 05), отражающий, как известно, содержание гемоглобина в эритроците.
 Физиология железа. n Железо — один из основных микроэлементов в организме человека. В норме в организме взрослого человека содержится 3– 5 г железа в связанной форме. 70% общего количества железа входит в состав гемопротеинов. Железо в этих соединениях связано с порфирином. Основной представитель этой группы — гемоглобин (58% железа); также железо содержится в миоглобине (8%), цитохромах, пероксидазах, каталазах — до 4%.
Физиология железа. n Железо — один из основных микроэлементов в организме человека. В норме в организме взрослого человека содержится 3– 5 г железа в связанной форме. 70% общего количества железа входит в состав гемопротеинов. Железо в этих соединениях связано с порфирином. Основной представитель этой группы — гемоглобин (58% железа); также железо содержится в миоглобине (8%), цитохромах, пероксидазах, каталазах — до 4%.
 Железо входит и в состав негемовых ферментов (ксантиноксидаза, никотинамидадениндинуклеотид (НАДН)-дегидрогеназа, аконитаза, локализующиеся в митохондриях); транспортной формы железа (трансферрин, лактоферрин). Запасы железа в организме существуют в двух формах: в виде ферритина (до 70%) и гемосидерина (до 30%). Особенность распределения железа у детей младшего возраста заключается в том, что у них выше содержание железа в эритроидных клетках и меньше железа приходится на мышечную ткань.
Железо входит и в состав негемовых ферментов (ксантиноксидаза, никотинамидадениндинуклеотид (НАДН)-дегидрогеназа, аконитаза, локализующиеся в митохондриях); транспортной формы железа (трансферрин, лактоферрин). Запасы железа в организме существуют в двух формах: в виде ферритина (до 70%) и гемосидерина (до 30%). Особенность распределения железа у детей младшего возраста заключается в том, что у них выше содержание железа в эритроидных клетках и меньше железа приходится на мышечную ткань.
 Всасывание солей железа n n в кишечнике происходит, когда микроэлемент находится в двухвалентной форме, которая проходить через клеточную мембрану слизистой оболочки кишечника. Попадая в желудочнокишечный тракт, трехвалентное железо в просвете кишечника переводится в двухвалентную форму (закисное) и в таком виде достигает мембраны кишечных микроворсинок, где вновь переводится в окисное железо, которое и подвергается метаболизму. Дальнейшая судьба железа, находящегося в микроворсинках щеточной каймы слизистой кишечника, зависит от содержания железа в организме.
Всасывание солей железа n n в кишечнике происходит, когда микроэлемент находится в двухвалентной форме, которая проходить через клеточную мембрану слизистой оболочки кишечника. Попадая в желудочнокишечный тракт, трехвалентное железо в просвете кишечника переводится в двухвалентную форму (закисное) и в таком виде достигает мембраны кишечных микроворсинок, где вновь переводится в окисное железо, которое и подвергается метаболизму. Дальнейшая судьба железа, находящегося в микроворсинках щеточной каймы слизистой кишечника, зависит от содержания железа в организме.
 n n Если запасы железа избыточны, то железо задерживается в эпителиальных клетках слизистой оболочки тонкой кишки в соединении с ферритином, а затем вместе со слущивающимся эпителием кишечника удаляется из организма. При наличии сидеропении увеличиваются абсорбционная поверхность кишечника и скорость всасывания железа. При этом большая часть железа поступает в кровоток и соединяется там с трансферрином. Следует отметить, что у детей раннего возраста с железодефицитным состоянием усвоение железа не возрастает, так как не происходит компенсаторного увеличения абсорбционной поверхности кишечника.
n n Если запасы железа избыточны, то железо задерживается в эпителиальных клетках слизистой оболочки тонкой кишки в соединении с ферритином, а затем вместе со слущивающимся эпителием кишечника удаляется из организма. При наличии сидеропении увеличиваются абсорбционная поверхность кишечника и скорость всасывания железа. При этом большая часть железа поступает в кровоток и соединяется там с трансферрином. Следует отметить, что у детей раннего возраста с железодефицитным состоянием усвоение железа не возрастает, так как не происходит компенсаторного увеличения абсорбционной поверхности кишечника.
 Всасывание железа n происходит преимущественно в двенадцатиперстной кишке и проксимальных отделах тощей кишки. В суточном рационе обычно содержится около 5– 20 мг железа, а усваивается только около 1– 2 мг в сутки. Степень абсорбции железа зависит как от его количества в потребляемой пище и биодоступности, так и от состояния желудочно-кишечного тракта (ЖКТ).
Всасывание железа n происходит преимущественно в двенадцатиперстной кишке и проксимальных отделах тощей кишки. В суточном рационе обычно содержится около 5– 20 мг железа, а усваивается только около 1– 2 мг в сутки. Степень абсорбции железа зависит как от его количества в потребляемой пище и биодоступности, так и от состояния желудочно-кишечного тракта (ЖКТ).
 Биодоступность железа. Биодоступность (всасывание) гемового железа в пищевых продуктах (мясные) более высокая, чем негемовых соединений, и составляет 25– 30% [1, 6, 7]. Большая часть поступающего с пищей железа представлена негемовой его формой. Факторы снижающие биодоступность: n - вещества (танины, фетины, фосфаты), которые образуют с Fe (II) нерастворимые соединения и выводятся с калом; n - пищевые волокна, которыми богаты крупы, свежие овощи, фрукты, в кишечнике пищевые волокна практически не перевариваются, железо фиксируется на их поверхности и выводится с калом. n
Биодоступность железа. Биодоступность (всасывание) гемового железа в пищевых продуктах (мясные) более высокая, чем негемовых соединений, и составляет 25– 30% [1, 6, 7]. Большая часть поступающего с пищей железа представлена негемовой его формой. Факторы снижающие биодоступность: n - вещества (танины, фетины, фосфаты), которые образуют с Fe (II) нерастворимые соединения и выводятся с калом; n - пищевые волокна, которыми богаты крупы, свежие овощи, фрукты, в кишечнике пищевые волокна практически не перевариваются, железо фиксируется на их поверхности и выводится с калом. n
 Факторы повышающие биодоступность: n - аскорбиновая кислота; n - животный белок (мясо, рыба), который увеличивает абсорбцию микроэлемента.
Факторы повышающие биодоступность: n - аскорбиновая кислота; n - животный белок (мясо, рыба), который увеличивает абсорбцию микроэлемента.
 Биодоступность железа грудного молока. n Особенно активно всасывание железа происходит из грудного молока, хотя его содержание в нем невелико — всего 1, 5 мг в литре; биодоступность железа грудного молока составляет до 60%. Этому способствует особая форма, в которой оно представлено, — в виде железосодержащего белка лактоферрина. n Лактоферрин в грудном молоке содержится в виде насыщенной и ненасыщенной форм.
Биодоступность железа грудного молока. n Особенно активно всасывание железа происходит из грудного молока, хотя его содержание в нем невелико — всего 1, 5 мг в литре; биодоступность железа грудного молока составляет до 60%. Этому способствует особая форма, в которой оно представлено, — в виде железосодержащего белка лактоферрина. n Лактоферрин в грудном молоке содержится в виде насыщенной и ненасыщенной форм.
 n Соотношение форм лактоферрина меняется в зависимости от периода лактации. В течение первых 1– 3 мес жизни превалирует насыщенная железотранспортная форма лактоферрина. n Кроме того, лактоферрин, связывая лишнее, не всосавшееся в кишечнике железо, лишает условно-патогенную микрофлору необходимого для ее жизнедеятельности микроэлемента и запускает неспецифические бактерицидные механизмы. Установлено, что бактерицидная функци иммуноглобулина A реализуется только в присутствии лактоферрина.
n Соотношение форм лактоферрина меняется в зависимости от периода лактации. В течение первых 1– 3 мес жизни превалирует насыщенная железотранспортная форма лактоферрина. n Кроме того, лактоферрин, связывая лишнее, не всосавшееся в кишечнике железо, лишает условно-патогенную микрофлору необходимого для ее жизнедеятельности микроэлемента и запускает неспецифические бактерицидные механизмы. Установлено, что бактерицидная функци иммуноглобулина A реализуется только в присутствии лактоферрина.
 Механизмы регуляции процесса всасывания железа в организме. n Наиболее важным звеном в поддержании гомеостаза железа является состояние эпителия слизистой оболочки двенадцатиперстной кишки, в частности его крипт.
Механизмы регуляции процесса всасывания железа в организме. n Наиболее важным звеном в поддержании гомеостаза железа является состояние эпителия слизистой оболочки двенадцатиперстной кишки, в частности его крипт.
 Первый механизм всасывания железа. n Всасывание железа в организме осуществляется через две поверхности кишечного эпителия: апикальную и базолатеральную. Апикальная мембрана дифференцированного энтероцита обращена в просвет кишечника и "специализируется" на транспорте гема и Fe 2+ в клетку.
Первый механизм всасывания железа. n Всасывание железа в организме осуществляется через две поверхности кишечного эпителия: апикальную и базолатеральную. Апикальная мембрана дифференцированного энтероцита обращена в просвет кишечника и "специализируется" на транспорте гема и Fe 2+ в клетку.
 В настоящее время изучено три механизма транспорта железа n 1. Наиболее распространенный механизм с участием белка DMT 1 (divalent metal transporter) [12, 13]. Белок DMT 1 осуществляет транспорт Fe 2+ и других двухвалентных микроэлементов через кишечную пластинку энтероцита. Располагаясь на апикальной мембране энтероцитов, DMT 1 способствует "захвату" и переносу Fe 2+ из двенадцатиперстной кишки в энтероцит. Транспорт железа из энтероцита осуществляется через базолатеральную мембрану с помощью базолатерального транспортного белка – ферропортина (MTP 1 или Ireg 1) [14, 15]. 2. Всасывания железа в виде соединения гем-железо, однако механизмы транспорта данного соединения через эпителий слизистой оболочки кишечника в настоящее время мало изучены [10]. 3. Транспорт железа осуществляется через апикальную мембрану кишечного энтероцита (проникновение железа в клетку с помощью транспортного белка – мобилферрина) [10, 11, 13, 15].
В настоящее время изучено три механизма транспорта железа n 1. Наиболее распространенный механизм с участием белка DMT 1 (divalent metal transporter) [12, 13]. Белок DMT 1 осуществляет транспорт Fe 2+ и других двухвалентных микроэлементов через кишечную пластинку энтероцита. Располагаясь на апикальной мембране энтероцитов, DMT 1 способствует "захвату" и переносу Fe 2+ из двенадцатиперстной кишки в энтероцит. Транспорт железа из энтероцита осуществляется через базолатеральную мембрану с помощью базолатерального транспортного белка – ферропортина (MTP 1 или Ireg 1) [14, 15]. 2. Всасывания железа в виде соединения гем-железо, однако механизмы транспорта данного соединения через эпителий слизистой оболочки кишечника в настоящее время мало изучены [10]. 3. Транспорт железа осуществляется через апикальную мембрану кишечного энтероцита (проникновение железа в клетку с помощью транспортного белка – мобилферрина) [10, 11, 13, 15].
 n n n Таким образом, регуляция обмена железа в организме осуществляется энтероцитами слизистой оболочки двенадцатиперстной кишки, которые "получают информацию" от различных тканей (печень, мышцы, эритроциты) организма о состоянии запасов железа в них. При истощении запасов железа в тканях включаются механизмы, усиливающие процесс абсорбции Fe. В случае же избытка железа в организме всасывание железа через кишечный эпителий уменьшается (механизм обратной связи).
n n n Таким образом, регуляция обмена железа в организме осуществляется энтероцитами слизистой оболочки двенадцатиперстной кишки, которые "получают информацию" от различных тканей (печень, мышцы, эритроциты) организма о состоянии запасов железа в них. При истощении запасов железа в тканях включаются механизмы, усиливающие процесс абсорбции Fe. В случае же избытка железа в организме всасывание железа через кишечный эпителий уменьшается (механизм обратной связи).
 Второй механизм регуляции процесса всасывания железа в организме осуществляется посредством сигнальной системы: n n костный мозг (эритроидный росток) энтероциты двенадцатиперстной кишки Данная связь осуществляется с помощью белковрегуляторов эритропоэза, находящихся в плазме крови. Сигналы в эритроидный росток костного мозга поступают от тканей, находящихся в условиях гипоксии, или непосредственно от самих эритроцитов, в результате чего абсорбция железа в кишечнике усиливается.
Второй механизм регуляции процесса всасывания железа в организме осуществляется посредством сигнальной системы: n n костный мозг (эритроидный росток) энтероциты двенадцатиперстной кишки Данная связь осуществляется с помощью белковрегуляторов эритропоэза, находящихся в плазме крови. Сигналы в эритроидный росток костного мозга поступают от тканей, находящихся в условиях гипоксии, или непосредственно от самих эритроцитов, в результате чего абсорбция железа в кишечнике усиливается.
 n Роль молекулярного посредника между клетками-потребителями О 2 и клетками костного мозга - продуцентами гемоглобинсодержащих клеток эритрона, играет эритропоэтин (ЭПО), вырабатывающийся в почках [17]. Регуляторные механизмы, поддерживающие гомеостаз железа, находятся в каждой клетке. Нарушения гомеостаза железа проявляются в преобладающем большинстве случаев в форме дефицита железа.
n Роль молекулярного посредника между клетками-потребителями О 2 и клетками костного мозга - продуцентами гемоглобинсодержащих клеток эритрона, играет эритропоэтин (ЭПО), вырабатывающийся в почках [17]. Регуляторные механизмы, поддерживающие гомеостаз железа, находятся в каждой клетке. Нарушения гомеостаза железа проявляются в преобладающем большинстве случаев в форме дефицита железа.
 Обмен железа n У взрослого мужчины весом 70 кг содержится 4 г железа: в геме гемоглобина эритроцитов содержится 2500 мг, в запасах (ткани и паренхиматозные органы) - 1000 мг (у женщин около 300 мг), в миоглобине и дыхательных ферментах - 300 мг, в плазму поступают из разрушающихся стареющих эритроцитов и уходят для формирования эритрона 20 мг ежедневно, всасываются в кишечнике и теряются ежедневно 1 -2 мг.
Обмен железа n У взрослого мужчины весом 70 кг содержится 4 г железа: в геме гемоглобина эритроцитов содержится 2500 мг, в запасах (ткани и паренхиматозные органы) - 1000 мг (у женщин около 300 мг), в миоглобине и дыхательных ферментах - 300 мг, в плазму поступают из разрушающихся стареющих эритроцитов и уходят для формирования эритрона 20 мг ежедневно, всасываются в кишечнике и теряются ежедневно 1 -2 мг.
 n Основная масса железа пищи представлена как его закись (трехвалентное железо). В сильно кислой среде закись железа растворима, при ощелачивании желудочного содержимого (р. Н более 2) она превращается в нерастворимые полигидроксиды. В двенадцатиперстной и тощей кишке происходит максимальное всасывание закиси (трехвалентного) железа в виде хелатов - они удерживают его в растворимой форме - аскорбат, цитрат и другие органические кислоты и аминокислоты. Оно связывается с муцином и остается в растворимой форме при ощелачивании среды. Окись железа всасывается лучше закиси.
n Основная масса железа пищи представлена как его закись (трехвалентное железо). В сильно кислой среде закись железа растворима, при ощелачивании желудочного содержимого (р. Н более 2) она превращается в нерастворимые полигидроксиды. В двенадцатиперстной и тощей кишке происходит максимальное всасывание закиси (трехвалентного) железа в виде хелатов - они удерживают его в растворимой форме - аскорбат, цитрат и другие органические кислоты и аминокислоты. Оно связывается с муцином и остается в растворимой форме при ощелачивании среды. Окись железа всасывается лучше закиси.
 n n n Белки, связывающие железо, выявлены на мембране ворсинок тонкой кишки. Они представлены полипептидами интегрина. Другой белок - мобилферрин - образует комплексы с интегрином, которые "складируют" железо в цитоплазме энтероцита для последующего транспорта в кровоток. Двухвалентное железо лучше, чем трехвалентное, всасывается из просвета кишки, так как при существующем р. Н оно остается растворимым. У позвоночных транспорт железа от места всасывания, хранения и утилизации обеспечивается гликопротеином плазмы - трансферрином. Он связывает железо прочно, но обратимо.
n n n Белки, связывающие железо, выявлены на мембране ворсинок тонкой кишки. Они представлены полипептидами интегрина. Другой белок - мобилферрин - образует комплексы с интегрином, которые "складируют" железо в цитоплазме энтероцита для последующего транспорта в кровоток. Двухвалентное железо лучше, чем трехвалентное, всасывается из просвета кишки, так как при существующем р. Н оно остается растворимым. У позвоночных транспорт железа от места всасывания, хранения и утилизации обеспечивается гликопротеином плазмы - трансферрином. Он связывает железо прочно, но обратимо.
 n Трансферрин связывается с клетками через собственные рецепторы на их мембране. Железо в клетках хранится в виде ферритина. У мужчин содержание железа равно 55 мг/кг веса, у женщин - 45 мг/кг веса. Трансферрин связывается с клетками при помощи рецепторов к нему, расположенных на мембранах всех клеток, кроме зрелых эритроцитов.
n Трансферрин связывается с клетками через собственные рецепторы на их мембране. Железо в клетках хранится в виде ферритина. У мужчин содержание железа равно 55 мг/кг веса, у женщин - 45 мг/кг веса. Трансферрин связывается с клетками при помощи рецепторов к нему, расположенных на мембранах всех клеток, кроме зрелых эритроцитов.
 железосвязывающая способность плазмы. n Для клинических целей уровень трансферрина в плазме выражается в количестве железа, которое он может связать - это так называемая общая железосвязывающая способность плазмы. Уровень железа в плазме около 18 мкмоль/литр, а общая железосвязывающая способность 56 мкм/л, то есть трансферрин насыщен железом на 30%. При полном насыщении трансферрина в плазме начинает определяться низкомолекулярное железо; оно откладывается в печени и поджелудочной железе, вызывая их повреждение. Эритроциты циркулируют 120 дней, постепенно разрушаясь и возвращая железо гема в запасы и трансферрин.
железосвязывающая способность плазмы. n Для клинических целей уровень трансферрина в плазме выражается в количестве железа, которое он может связать - это так называемая общая железосвязывающая способность плазмы. Уровень железа в плазме около 18 мкмоль/литр, а общая железосвязывающая способность 56 мкм/л, то есть трансферрин насыщен железом на 30%. При полном насыщении трансферрина в плазме начинает определяться низкомолекулярное железо; оно откладывается в печени и поджелудочной железе, вызывая их повреждение. Эритроциты циркулируют 120 дней, постепенно разрушаясь и возвращая железо гема в запасы и трансферрин.
 Физиологические потери железа n n через желудочно-кишечный тракт (не более 2 мл крови - не более 2 мг железа за сутки по определению с радиоактивным хромом), на менструации у женщин (около 2 -3 мг в сутки), на одну беременность, роды и лактацию - 800 мг, у детей 0. 1 -0. 3 мг в сутки, возрастая до 0. 5 -1. 0 мг в сутки у подростков.
Физиологические потери железа n n через желудочно-кишечный тракт (не более 2 мл крови - не более 2 мг железа за сутки по определению с радиоактивным хромом), на менструации у женщин (около 2 -3 мг в сутки), на одну беременность, роды и лактацию - 800 мг, у детей 0. 1 -0. 3 мг в сутки, возрастая до 0. 5 -1. 0 мг в сутки у подростков.
 Потребности в железе. n n Ежедневная потребность детского организма в железе составляет 0, 5– 1, 2 мг в сутки. У детей раннего возраста в связи с быстрыми темпами роста и развития наблюдается повышенная потребность в железе. В этот период жизни запасы железа быстро истощаются из-за усиленного его потребления из депо: у недоношенных детей к 3 -му месяцу, у доношенных — к 5– 6 -му мес жизни. Для обеспечения нормального развития ребенка в суточном рационе новорожденного должно содержаться 1, 5 мг железа, а у ребенка 1– 3 лет — не менее 10 мг.
Потребности в железе. n n Ежедневная потребность детского организма в железе составляет 0, 5– 1, 2 мг в сутки. У детей раннего возраста в связи с быстрыми темпами роста и развития наблюдается повышенная потребность в железе. В этот период жизни запасы железа быстро истощаются из-за усиленного его потребления из депо: у недоношенных детей к 3 -му месяцу, у доношенных — к 5– 6 -му мес жизни. Для обеспечения нормального развития ребенка в суточном рационе новорожденного должно содержаться 1, 5 мг железа, а у ребенка 1– 3 лет — не менее 10 мг.
 Дефицит железа у детей приводит: n к росту инфекционной заболеваемости органов дыхания и ЖКТ, n нарушению нервно-психического развития ребенка.
Дефицит железа у детей приводит: n к росту инфекционной заболеваемости органов дыхания и ЖКТ, n нарушению нервно-психического развития ребенка.
 Лабораторные критерии анемии (Н. П. Шабалов, 2003). 0– 1 сутки жизни — < 145 г/л; n 1– 14 дней жизни — < 130 г/л; n 14– 28 дней жизни — < 120 г/л; n 1 мес — 6 лет — < 110 г/л. Из всех анемий самой распространенной является железодефицитная (ЖДА), которая составляет примерно 80% от всех анемий. По данным Всемирной организации здравоохранения (ВОЗ), в мире более 500 тыс. человек страдает ЖДА. Распространенность ЖДА у детей в России и развитых европейских странах составляет: около 50% — у детей младшего возраста; более 20% — у детей старшего возраста. n
Лабораторные критерии анемии (Н. П. Шабалов, 2003). 0– 1 сутки жизни — < 145 г/л; n 1– 14 дней жизни — < 130 г/л; n 14– 28 дней жизни — < 120 г/л; n 1 мес — 6 лет — < 110 г/л. Из всех анемий самой распространенной является железодефицитная (ЖДА), которая составляет примерно 80% от всех анемий. По данным Всемирной организации здравоохранения (ВОЗ), в мире более 500 тыс. человек страдает ЖДА. Распространенность ЖДА у детей в России и развитых европейских странах составляет: около 50% — у детей младшего возраста; более 20% — у детей старшего возраста. n
 Определение n ЖДА — это клиникогематологический синдром, характеризующийся нарушением синтеза гемоглобина в результате дефицита железа, развивающегося на фоне различных патологических (физиологических) процессов, и проявляющийся признаками анемии и сидеропении.
Определение n ЖДА — это клиникогематологический синдром, характеризующийся нарушением синтеза гемоглобина в результате дефицита железа, развивающегося на фоне различных патологических (физиологических) процессов, и проявляющийся признаками анемии и сидеропении.
 Причины железодефицитных состояний. 1. Основной причиной ЖДА у новорожденных: n наличие ЖДА или скрытого дефицита железа у матери во время беременности, n осложненное течение беременности, n нарушение маточно-плацентарного кровообращения, n фетоматеринские и фетоплацентарные кровотечения, n синдром фетальной трансфузии при многоплодной беременности.
Причины железодефицитных состояний. 1. Основной причиной ЖДА у новорожденных: n наличие ЖДА или скрытого дефицита железа у матери во время беременности, n осложненное течение беременности, n нарушение маточно-плацентарного кровообращения, n фетоматеринские и фетоплацентарные кровотечения, n синдром фетальной трансфузии при многоплодной беременности.
 2. Интранатальные причины: n преждевременная или поздняя перевязка пуповины, n интранатальные кровотечения из-за травматических акушерских пособий или аномалий развития плаценты или пуповины. 3. Постнатальные причины: n недостаточное поступление железа с пищей, n повышенная потребность организма в железе, n потери железа, превышающие физиологические,
2. Интранатальные причины: n преждевременная или поздняя перевязка пуповины, n интранатальные кровотечения из-за травматических акушерских пособий или аномалий развития плаценты или пуповины. 3. Постнатальные причины: n недостаточное поступление железа с пищей, n повышенная потребность организма в железе, n потери железа, превышающие физиологические,
 n n n заболевания ЖКТ, синдром нарушенного кишечного всасывания; дефицит запасов железа при рождении; анатомические врожденные аномалии (дивертикул Меккеля, полипозы кишечника); употребление продуктов, тормозящих абсорбцию железа, приём некоторых медикаментов (НПВС, салицилаты, глюкокортикостероиды)
n n n заболевания ЖКТ, синдром нарушенного кишечного всасывания; дефицит запасов железа при рождении; анатомические врожденные аномалии (дивертикул Меккеля, полипозы кишечника); употребление продуктов, тормозящих абсорбцию железа, приём некоторых медикаментов (НПВС, салицилаты, глюкокортикостероиды)
 Группы риска. 1. Недоношенные дети. 2. Дети, родившиеся с очень большой массой тела. 3. Дети с лимфатикогипопластическим типом конституции.
Группы риска. 1. Недоношенные дети. 2. Дети, родившиеся с очень большой массой тела. 3. Дети с лимфатикогипопластическим типом конституции.
 Диагностика ЖДА. Диагноз ЖДА ставится на основании: n клинической картины, n лабораторных признаков анемии и дефицита железа в организме: гипохромная (цветовой показатель < 0, 85) анемия различной степени тяжести, гипохромия эритроцитов, снижение средней концентрации гемоглобина в эритроците (менее 24 пг), микроцитоз и пойкилоцитоз эритроцитов (в мазке периферической крови); n уменьшение количества сидеробластов в пунктате костного мозга;
Диагностика ЖДА. Диагноз ЖДА ставится на основании: n клинической картины, n лабораторных признаков анемии и дефицита железа в организме: гипохромная (цветовой показатель < 0, 85) анемия различной степени тяжести, гипохромия эритроцитов, снижение средней концентрации гемоглобина в эритроците (менее 24 пг), микроцитоз и пойкилоцитоз эритроцитов (в мазке периферической крови); n уменьшение количества сидеробластов в пунктате костного мозга;
 уменьшение содержания железа в сыворотке крови (< 12, 5 мкмоль/л); n повышение общей железосвязывающей способности сыворотки (ОЖСС) более 85 мкмоль/л (показатель «голодания» ); n повышение уровня трансферрина в сыворотке крови, при снижении его насыщения железом (менее 15%); снижение уровня ферритина в сыворотке (< 15 мкг/л). n
уменьшение содержания железа в сыворотке крови (< 12, 5 мкмоль/л); n повышение общей железосвязывающей способности сыворотки (ОЖСС) более 85 мкмоль/л (показатель «голодания» ); n повышение уровня трансферрина в сыворотке крови, при снижении его насыщения железом (менее 15%); снижение уровня ферритина в сыворотке (< 15 мкг/л). n
 Основными критериями ЖДА являются следующие: низкий цветовой показатель; n гипохромия эритроцитов, микроцитоз; n снижение уровня сывороточного железа; n повышение общей железосвязывающей способности сыворотки; n
Основными критериями ЖДА являются следующие: низкий цветовой показатель; n гипохромия эритроцитов, микроцитоз; n снижение уровня сывороточного железа; n повышение общей железосвязывающей способности сыворотки; n
 Цветовой показатель. Отражает содержание гемоглобина в эритроците. Норма 0. 85 -1. 05. Поскольку при ЖДА нарушен главным образом синтез гемоглобина при незначительном снижении количества эритроцитов, рассчитываемый цветовой показатель всегда оказывается ниже 0, 85, составляя часто 0, 7 и ниже, т. е. все ЖДА являются гипохромными.
Цветовой показатель. Отражает содержание гемоглобина в эритроците. Норма 0. 85 -1. 05. Поскольку при ЖДА нарушен главным образом синтез гемоглобина при незначительном снижении количества эритроцитов, рассчитываемый цветовой показатель всегда оказывается ниже 0, 85, составляя часто 0, 7 и ниже, т. е. все ЖДА являются гипохромными.
 МСН n непосредственное определение содержания гемоглобина в эритроците, выражающегося в пикограммах (в норме 27 – 35 пг).
МСН n непосредственное определение содержания гемоглобина в эритроците, выражающегося в пикограммах (в норме 27 – 35 пг).
 Таблица. Основные дифференциально -диагностические признаки гипохромных анемий Железоперераспределитель ные Железодефици тные Сидероахрестич еские Сывороточное железо Снижено Повышено Норма или повышено Общая железосвязывающая способность сыворотки Повышена Снижена Норма или снижена Содержание ферритина в крови Снижено Повышено Количество ретикулоцитов Норма или повышено Мишеневидность эритроцитов Может быть Базофильная пунктация эритроцитов Отсутствует Имеется Отсутствует Количество сидеробластов и сидероцитов Снижено Повышено Непрямой билирубин Норма Проба с десфералом Отрицательная Положительная Признаки гипосидероза Имеются Отсутствуют Эффект от препаратов железа Имеется Отсутствует Основные признаки
Таблица. Основные дифференциально -диагностические признаки гипохромных анемий Железоперераспределитель ные Железодефици тные Сидероахрестич еские Сывороточное железо Снижено Повышено Норма или повышено Общая железосвязывающая способность сыворотки Повышена Снижена Норма или снижена Содержание ферритина в крови Снижено Повышено Количество ретикулоцитов Норма или повышено Мишеневидность эритроцитов Может быть Базофильная пунктация эритроцитов Отсутствует Имеется Отсутствует Количество сидеробластов и сидероцитов Снижено Повышено Непрямой билирубин Норма Проба с десфералом Отрицательная Положительная Признаки гипосидероза Имеются Отсутствуют Эффект от препаратов железа Имеется Отсутствует Основные признаки
 Железосвязывающая способность сыворотки. n отражает степень «голодания» сыворотки и насыщения белка трансферрина железом. Общая железосвязывающая способность сыворотки при ЖДА всегда повышена в отличие от других гипохромных анемий.
Железосвязывающая способность сыворотки. n отражает степень «голодания» сыворотки и насыщения белка трансферрина железом. Общая железосвязывающая способность сыворотки при ЖДА всегда повышена в отличие от других гипохромных анемий.
 Ферритин. n n Ферритин характеризует величину запасов железа в организме. уровень ферритина является одним из специфических признаков железодефицитного характера гипохромных анемий. Следует, однако, иметь в виду, что наличие сопутствующего активного воспалительного процесса у больных ЖДА может маскировать гипоферритинемию.
Ферритин. n n Ферритин характеризует величину запасов железа в организме. уровень ферритина является одним из специфических признаков железодефицитного характера гипохромных анемий. Следует, однако, иметь в виду, что наличие сопутствующего активного воспалительного процесса у больных ЖДА может маскировать гипоферритинемию.
 n Дополнительными методами определения запасов железа в организме могут быть подсчет числа эритроидных клеток костного мозга, содержащих гранулы железа (сидеробластов) и количество железа в моче после введения препаратов, связывающих железо (десфериоксиамин). Количество сидеробластов при ЖДА значительно снижено вплоть до полного их отсутствия, а содержание железа в моче после введения десферриоксиамина не увеличивается
n Дополнительными методами определения запасов железа в организме могут быть подсчет числа эритроидных клеток костного мозга, содержащих гранулы железа (сидеробластов) и количество железа в моче после введения препаратов, связывающих железо (десфериоксиамин). Количество сидеробластов при ЖДА значительно снижено вплоть до полного их отсутствия, а содержание железа в моче после введения десферриоксиамина не увеличивается
 Основными наиболее частыми причинами развития ЖДА являются 1. Хронические кровопотери различной локализации. 2. Нарушение всасывания железа: энтериты различного генеза; синдром недостаточности всасывания; резекции тонкой кишки; резекция желудка с выключением двенадцатиперстной кишки. 3. Повышенная потребность в железе: беременность, лактация; интенсивный рост в пубертатный период; В 12 -дефицитная анемия, леченная витамином В 12. 4. Нарушение транспорта железа (гипопротеинемии различного генеза). 5. Алиментарная недостаточность.
Основными наиболее частыми причинами развития ЖДА являются 1. Хронические кровопотери различной локализации. 2. Нарушение всасывания железа: энтериты различного генеза; синдром недостаточности всасывания; резекции тонкой кишки; резекция желудка с выключением двенадцатиперстной кишки. 3. Повышенная потребность в железе: беременность, лактация; интенсивный рост в пубертатный период; В 12 -дефицитная анемия, леченная витамином В 12. 4. Нарушение транспорта железа (гипопротеинемии различного генеза). 5. Алиментарная недостаточность.
 Сидероахрестические анемии n Это группа гипохромных анемий, при которых содержание железа в организме и его запасы в депо находятся в пределах нормы или даже повышены, однако в связи с нарушением включения его в молекулу гемоглобина (в силу различных причин) железо не используется для синтеза гемма, (ахрезия – неиспользование).
Сидероахрестические анемии n Это группа гипохромных анемий, при которых содержание железа в организме и его запасы в депо находятся в пределах нормы или даже повышены, однако в связи с нарушением включения его в молекулу гемоглобина (в силу различных причин) железо не используется для синтеза гемма, (ахрезия – неиспользование).
 Критерии сидероахрестических анемий: n n n низкий цветовой показатель; гипохромия эритроцитов; повышенное (реже нормальное) содержание железа в сыворотке; нормальная или сниженная железосвязывающая способность сыворотки; нормальное или повышенное содержание ферритина в сыворотке; повышенное количество сидеробластов в костном мозге.
Критерии сидероахрестических анемий: n n n низкий цветовой показатель; гипохромия эритроцитов; повышенное (реже нормальное) содержание железа в сыворотке; нормальная или сниженная железосвязывающая способность сыворотки; нормальное или повышенное содержание ферритина в сыворотке; повышенное количество сидеробластов в костном мозге.
 Варианты сидероахрестических анемий: 1. наследственные формы (аутосомные и рецессивные, чувствительные и рефрактерные к применению пиридоксина); n связанные с дефицитом фермента гемсинтетазы (обеспечивающей включение железа в молекулу гема); n - связанные с нарушением синтеза гемоглобина из-за патологии его глобиновой части (талассемия 2. приобретенные формы (алкогольная интоксикация, хроническая свинцовая интоксикация, воздействие некоторых медикаментов, миелопролиферативные заболевания, кожная порфирия, идиопатические формы).
Варианты сидероахрестических анемий: 1. наследственные формы (аутосомные и рецессивные, чувствительные и рефрактерные к применению пиридоксина); n связанные с дефицитом фермента гемсинтетазы (обеспечивающей включение железа в молекулу гема); n - связанные с нарушением синтеза гемоглобина из-за патологии его глобиновой части (талассемия 2. приобретенные формы (алкогольная интоксикация, хроническая свинцовая интоксикация, воздействие некоторых медикаментов, миелопролиферативные заболевания, кожная порфирия, идиопатические формы).
 Железоперераспределительные анемии n n анемии при различных воспалительных заболеваниях как инфекционного, так и неинфекционного происхождения. Возникающие в подобных ситуациях анемии принято условно обозначать как анемии при хронических заболеваниях (АХЗ), хотя такое обозначение условно, поскольку анемия может развиваться и при острых воспалениях, в частности при нагноительных процессах (апостематозный нефрит, абсцесс легкого и др. )
Железоперераспределительные анемии n n анемии при различных воспалительных заболеваниях как инфекционного, так и неинфекционного происхождения. Возникающие в подобных ситуациях анемии принято условно обозначать как анемии при хронических заболеваниях (АХЗ), хотя такое обозначение условно, поскольку анемия может развиваться и при острых воспалениях, в частности при нагноительных процессах (апостематозный нефрит, абсцесс легкого и др. )
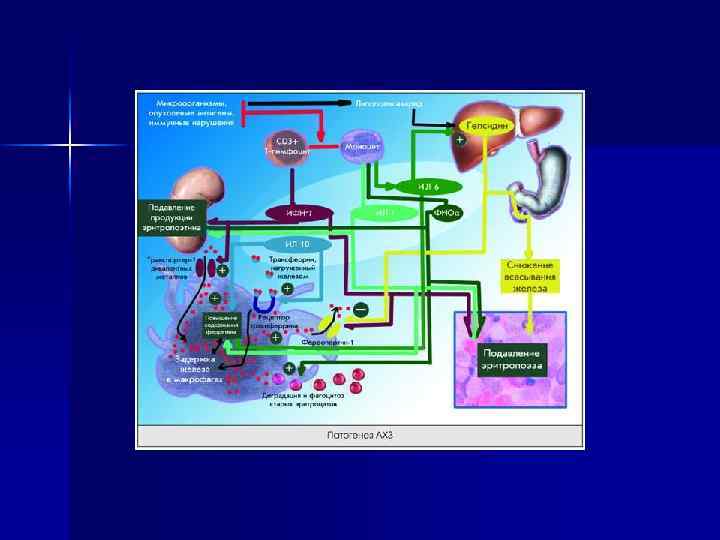
 патогенетический механизм при АХЗ Основной патогенетический механизм при АХЗ считается перераспределение железа в клетки макрофагальной системы, активирующейся при различных воспалительных (инфекционных и неинфекционных) или опухолевых процессах. Поступающее в организм и высвобождающееся из разрушающихся эритроцитов железо переходит главным образом в депо, где и накапливается в макрофагальных клетках в виде железосодержащего белка ферритина. Включение железа в эритроидные клетки костного мозга при этом снижено. Поскольку истинного дефицита железа при этих АХЗ не наблюдается, более оправданно говорить не о железодефицитных, а о железоперераспределительных анемиях.
патогенетический механизм при АХЗ Основной патогенетический механизм при АХЗ считается перераспределение железа в клетки макрофагальной системы, активирующейся при различных воспалительных (инфекционных и неинфекционных) или опухолевых процессах. Поступающее в организм и высвобождающееся из разрушающихся эритроцитов железо переходит главным образом в депо, где и накапливается в макрофагальных клетках в виде железосодержащего белка ферритина. Включение железа в эритроидные клетки костного мозга при этом снижено. Поскольку истинного дефицита железа при этих АХЗ не наблюдается, более оправданно говорить не о железодефицитных, а о железоперераспределительных анемиях.
 Критерии железоперераспределительных анемий. n n n нормохромный или умеренно гипохромный характер анемии; нормальное или умеренное сниженное содержание сывороточного железа; нормальная или сниженная железосвязывающая способность сыворотки; повышение содержания ферритина в сыворотке; повышение количества сидеробластов в костном мозге; клинико-лабораторные признаки активного процесса (воспалительного, опухолевого).
Критерии железоперераспределительных анемий. n n n нормохромный или умеренно гипохромный характер анемии; нормальное или умеренное сниженное содержание сывороточного железа; нормальная или сниженная железосвязывающая способность сыворотки; повышение содержания ферритина в сыворотке; повышение количества сидеробластов в костном мозге; клинико-лабораторные признаки активного процесса (воспалительного, опухолевого).
 Клинические рекомендации лечения ПЖ для приема внутрь: n n n назначение ПЖ в виде солей внутрь с достаточным содержанием двухвалентного железа; назначение ПЖ, содержащих вещества, усиливающие всасывание железа; нежелательность одновременного приема пищевых веществ и лекарственных препаратов, уменьшающих всасывание железа;
Клинические рекомендации лечения ПЖ для приема внутрь: n n n назначение ПЖ в виде солей внутрь с достаточным содержанием двухвалентного железа; назначение ПЖ, содержащих вещества, усиливающие всасывание железа; нежелательность одновременного приема пищевых веществ и лекарственных препаратов, уменьшающих всасывание железа;
 Клинические рекомендации лечения ПЖ для приема внутрь ( продолжение) n n целесообразность назначения препаратов железа, содержащих фолиевую кислоту, цианокобаламин при наличии смешанного характера анемии; назначение препаратов железа парентерально при нарушении кишечного всасывания; достаточная продолжительность насыщающего курса терапии (не менее 1– 1, 5 мес); необходимость проведения поддерживающей терапии ПЖ в соответствующих ситуациях.
Клинические рекомендации лечения ПЖ для приема внутрь ( продолжение) n n целесообразность назначения препаратов железа, содержащих фолиевую кислоту, цианокобаламин при наличии смешанного характера анемии; назначение препаратов железа парентерально при нарушении кишечного всасывания; достаточная продолжительность насыщающего курса терапии (не менее 1– 1, 5 мес); необходимость проведения поддерживающей терапии ПЖ в соответствующих ситуациях.
 n При выборе лекарственного ПЖ следует ориентироваться на содержание в нем двухвалентного железа, которое только и всасывается в кишечнике. Входящие в состав многих лекарственных форм ПЖ аскорбиновая кислота, цистеин, фруктоза усиливают всасывание железа. Назначение препаратов железа в высоких дозах (300 мг в сутки) не приводит к увеличению всасывания ионов железа, однако вызывает значительное увеличение числа побочных эффект
n При выборе лекарственного ПЖ следует ориентироваться на содержание в нем двухвалентного железа, которое только и всасывается в кишечнике. Входящие в состав многих лекарственных форм ПЖ аскорбиновая кислота, цистеин, фруктоза усиливают всасывание железа. Назначение препаратов железа в высоких дозах (300 мг в сутки) не приводит к увеличению всасывания ионов железа, однако вызывает значительное увеличение числа побочных эффект
 Препараты железа, используемые в педиатрии Препарат Количество железа в препарате Ранний возраст (до 3 лет) Феррум лек, сироп в 1 мл сиропа – 10 мг Мальтофер, капли в 1 капле – 2, 5 мг Гемофер, капли в 1 капле – 1, 6 мг Актиферрин, капли в 1 капле – 0, 53 мг Дошкольный возраст (с 3 до 6 лет) Феррум лек, сироп в 1 мл – 10 мг Мальтофер, сироп в 1 мл – 10 мг Актиферрин, сироп в 1 мл – 6, 8 мг Тотема, раствор для приема внутрь в 1 мл – 5 мг
Препараты железа, используемые в педиатрии Препарат Количество железа в препарате Ранний возраст (до 3 лет) Феррум лек, сироп в 1 мл сиропа – 10 мг Мальтофер, капли в 1 капле – 2, 5 мг Гемофер, капли в 1 капле – 1, 6 мг Актиферрин, капли в 1 капле – 0, 53 мг Дошкольный возраст (с 3 до 6 лет) Феррум лек, сироп в 1 мл – 10 мг Мальтофер, сироп в 1 мл – 10 мг Актиферрин, сироп в 1 мл – 6, 8 мг Тотема, раствор для приема внутрь в 1 мл – 5 мг
 Препараты железа, используемые в педиатрии (продолжение) Ферроплекс 1 драже – 10 мг Препубертатный возраст (от 7 до 12 лет), подростки Феррум лек, жевательные таблетки в 1 таблетке – 100 мг Мальтофер, жевательные таблетки в 1 таблетке – 100 мг Актиферрин в 1 капсуле – 34, 5 мг Гемофер пролонгатум в 1 таблетке – 105 мг Тардиферон в 1 таблетке – 80 мг Тотема, раствор для приема внутрь в 1 мл – 5 мг Ферроплекс 1 драже – 10 мг
Препараты железа, используемые в педиатрии (продолжение) Ферроплекс 1 драже – 10 мг Препубертатный возраст (от 7 до 12 лет), подростки Феррум лек, жевательные таблетки в 1 таблетке – 100 мг Мальтофер, жевательные таблетки в 1 таблетке – 100 мг Актиферрин в 1 капсуле – 34, 5 мг Гемофер пролонгатум в 1 таблетке – 105 мг Тардиферон в 1 таблетке – 80 мг Тотема, раствор для приема внутрь в 1 мл – 5 мг Ферроплекс 1 драже – 10 мг
 Степень всасывания солей железа. Хорошая Сульфат n Глюконат n Хлорид n Фумарат n Сорбитол n Глицин сульфат n Никотинамид Плохая
Степень всасывания солей железа. Хорошая Сульфат n Глюконат n Хлорид n Фумарат n Сорбитол n Глицин сульфат n Никотинамид Плохая
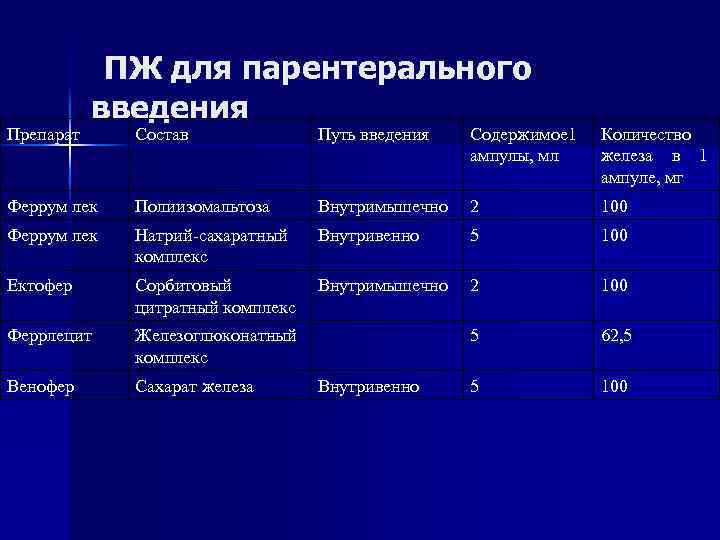 Препарат ПЖ для парентерального введения Состав Путь введения Содержимое 1 ампулы, мл Количество железа в 1 ампуле, мг Феррум лек Полиизомальтоза Внутримышечно 2 100 Феррум лек Натрий-сахаратный комплекс Внутривенно 5 100 Ектофер Сорбитовый цитратный комплекс Внутримышечно 2 100 Феррлецит Железоглюконатный комплекс 5 62, 5 Венофер Сахарат железа 5 100 Внутривенно
Препарат ПЖ для парентерального введения Состав Путь введения Содержимое 1 ампулы, мл Количество железа в 1 ампуле, мг Феррум лек Полиизомальтоза Внутримышечно 2 100 Феррум лек Натрий-сахаратный комплекс Внутривенно 5 100 Ектофер Сорбитовый цитратный комплекс Внутримышечно 2 100 Феррлецит Железоглюконатный комплекс 5 62, 5 Венофер Сахарат железа 5 100 Внутривенно
 Препараты железа разделяют на две группы: ионные железосодержащие препараты (солевые, полисахаридные соединения железа) n неионные соединения, к которым относятся препараты, представленные гидроксидполимальтозным комплексом (ГПК) трехвалентного железа [2, 30] (табл. 1). Всасывание железа из ионных соединений происходит преимущественно в двухвалентной форме. Вследствие этого наиболее часто используются двухвалентные солевые препараты железа, обладающие хорошей растворимостью. n
Препараты железа разделяют на две группы: ионные железосодержащие препараты (солевые, полисахаридные соединения железа) n неионные соединения, к которым относятся препараты, представленные гидроксидполимальтозным комплексом (ГПК) трехвалентного железа [2, 30] (табл. 1). Всасывание железа из ионных соединений происходит преимущественно в двухвалентной форме. Вследствие этого наиболее часто используются двухвалентные солевые препараты железа, обладающие хорошей растворимостью. n
 n n Попадая в ЖКТ, соединения двухвалентного железа проникают в мукозные клетки слизистой кишечника (проходят "слизистый барьер"), а затем в кровяное русло посредством механизма пассивной диффузии. В кровяном русле происходит процесс восстановления двухвалентного железа в трехвалентную форму с участием ферроксидазы – I и соединения с трансферрином и ферритином. Образуется пул депонированного железа, которое используется в синтезе гемоглобина, миоглобина, других железосодержащих соединений.
n n Попадая в ЖКТ, соединения двухвалентного железа проникают в мукозные клетки слизистой кишечника (проходят "слизистый барьер"), а затем в кровяное русло посредством механизма пассивной диффузии. В кровяном русле происходит процесс восстановления двухвалентного железа в трехвалентную форму с участием ферроксидазы – I и соединения с трансферрином и ферритином. Образуется пул депонированного железа, которое используется в синтезе гемоглобина, миоглобина, других железосодержащих соединений.
 Побочные эффекты приёме солевых препаратов железа. Частота побочных эффектов зависит от дозы препарата. n Со стороны ЖКТ: - диарея или запор; - дисфункция верхних отделов ЖКТ (тошнота, дискомфорт в эптгастрии, боль в животе, рвота); - металлический привкус во рту; - потемнение зубной эмали и дёсен
Побочные эффекты приёме солевых препаратов железа. Частота побочных эффектов зависит от дозы препарата. n Со стороны ЖКТ: - диарея или запор; - дисфункция верхних отделов ЖКТ (тошнота, дискомфорт в эптгастрии, боль в животе, рвота); - металлический привкус во рту; - потемнение зубной эмали и дёсен
 n n Лечение солевым препаратом железа необходимо начинать с 1/4 от рассчитанной терапевтической дозы с последующим постепенным достижением полной дозы в течение 7 дней – "трапециевидная методика" Важным аспектом ферротерапии, особенно в педиатрической практике, является терапевтическая безопасность используемых препаратов железа. Таким образом, заместительная терапия дефицита железа с помощью солевых препаратов железа является достаточно эффективной. Однако высокий риск развития тяжелых побочных эффектов в дозе 6– 8 мг на 1 кг массы тела в сутки снижает приверженность к лечению. По нашим данным, снижение дозы солевых препаратов железа до 3 мг на 1 кг массы тела в сутки уменьшает частоту побочных явлений.
n n Лечение солевым препаратом железа необходимо начинать с 1/4 от рассчитанной терапевтической дозы с последующим постепенным достижением полной дозы в течение 7 дней – "трапециевидная методика" Важным аспектом ферротерапии, особенно в педиатрической практике, является терапевтическая безопасность используемых препаратов железа. Таким образом, заместительная терапия дефицита железа с помощью солевых препаратов железа является достаточно эффективной. Однако высокий риск развития тяжелых побочных эффектов в дозе 6– 8 мг на 1 кг массы тела в сутки снижает приверженность к лечению. По нашим данным, снижение дозы солевых препаратов железа до 3 мг на 1 кг массы тела в сутки уменьшает частоту побочных явлений.
 n К новым эффективным и безопасным лекарственным средствам для коррекции ЖДС относятся препараты, представляющие собой неионные соединения железа. Химическая структура комплекса максимально приближена к структуре естественных соединений железа с ферритином. Абсорбция железа в виде ГПК обеспечивается поступлением Fe (III) из кишечника в кровь путем активного всасывания. При этом железо переносится через щеточную каемку мембраны на белке-переносчике и высвобождается для связывания с трансферрином и ферритином, в блоке с которыми депонируется и используется организмом по мере необходимости. Физиологические процессы саморегуляции полностью исключают возможность передозировки и отравления.
n К новым эффективным и безопасным лекарственным средствам для коррекции ЖДС относятся препараты, представляющие собой неионные соединения железа. Химическая структура комплекса максимально приближена к структуре естественных соединений железа с ферритином. Абсорбция железа в виде ГПК обеспечивается поступлением Fe (III) из кишечника в кровь путем активного всасывания. При этом железо переносится через щеточную каемку мембраны на белке-переносчике и высвобождается для связывания с трансферрином и ферритином, в блоке с которыми депонируется и используется организмом по мере необходимости. Физиологические процессы саморегуляции полностью исключают возможность передозировки и отравления.
 Преимущества неионных препаратов железа. – Низкая частота побочных эффектов (редко чувство переполнения желудка, давления в эпигастрии, тошнота, диарея или запор). – Лучшая переносимость препаратов (мальтофер, феррум лек). – Возможность использовать эти препараты во время еды.
Преимущества неионных препаратов железа. – Низкая частота побочных эффектов (редко чувство переполнения желудка, давления в эпигастрии, тошнота, диарея или запор). – Лучшая переносимость препаратов (мальтофер, феррум лек). – Возможность использовать эти препараты во время еды.
 Терапевтический эффект при пероральном приеме n n n Терапевтический эффект при пероральном приеме железа появляется постепенно. Первым положительным клиническим признаком, появляющимся при лечении препаратами железа, является исчезновение или уменьшение мышечной слабости. На 10– 12 -й дни от начала лечения повышается содержание ретикулоцитов в периферической крови. Чаще всего начало подъема уровня гемоглобина происходит на 3– 4 -й неделе от начала терапии. Как показали многочисленные исследования, исчезновение клинических проявлений заболевания отмечается к 1– 2 мес терапии, а преодоление тканевой сидеропении – от 3 до 6 мес лечения.
Терапевтический эффект при пероральном приеме n n n Терапевтический эффект при пероральном приеме железа появляется постепенно. Первым положительным клиническим признаком, появляющимся при лечении препаратами железа, является исчезновение или уменьшение мышечной слабости. На 10– 12 -й дни от начала лечения повышается содержание ретикулоцитов в периферической крови. Чаще всего начало подъема уровня гемоглобина происходит на 3– 4 -й неделе от начала терапии. Как показали многочисленные исследования, исчезновение клинических проявлений заболевания отмечается к 1– 2 мес терапии, а преодоление тканевой сидеропении – от 3 до 6 мес лечения.
 n n Суточная доза элементарного железа после нормализации уровня гемоглобина должна соответствовать 1/2 терапевтической доз. По нашим данным, восстановление уровня гемоглобина при легкой и средней степени ЖДА достигается к 4 -й неделе терапии препаратом "Феррум Лек", а восстановление нормального уровня ферритина сыворотки крови – к 8– 10 -й неделе терапии. Прием препарата у детей с латентным дефицитом железа в дозе 2, 5 мг/кг/сут составляет 4– 8 нед.
n n Суточная доза элементарного железа после нормализации уровня гемоглобина должна соответствовать 1/2 терапевтической доз. По нашим данным, восстановление уровня гемоглобина при легкой и средней степени ЖДА достигается к 4 -й неделе терапии препаратом "Феррум Лек", а восстановление нормального уровня ферритина сыворотки крови – к 8– 10 -й неделе терапии. Прием препарата у детей с латентным дефицитом железа в дозе 2, 5 мг/кг/сут составляет 4– 8 нед.
 Назначение эритропоэтина. n При развитии тяжелых анемий, сопровождаемых угнетением эритропоэза и снижением продукции эритропоэтина, показано назначение препаратов рекомбинантного человеческого эритропоэтина (рч. ЭПО). Особое значение имеет применение рч. ЭПО при развитии ранней анемии недоношенных, которая развивается на втором месяце жизни и встречается, по данным различных авторов, в 20– 90% случаев. Назначение препаратов рч. ЭПО (рекормон, эпрекс, эпокрин) приводит к резкой активизации эритропоэза и, как следствие, к значительному возрастанию потребностей в железе.
Назначение эритропоэтина. n При развитии тяжелых анемий, сопровождаемых угнетением эритропоэза и снижением продукции эритропоэтина, показано назначение препаратов рекомбинантного человеческого эритропоэтина (рч. ЭПО). Особое значение имеет применение рч. ЭПО при развитии ранней анемии недоношенных, которая развивается на втором месяце жизни и встречается, по данным различных авторов, в 20– 90% случаев. Назначение препаратов рч. ЭПО (рекормон, эпрекс, эпокрин) приводит к резкой активизации эритропоэза и, как следствие, к значительному возрастанию потребностей в железе.
 Профилактика ЖДА. 1. Антенатальная (правильный режим и питание беременной, своевременное выявление и лечение анемии беременной, превентивное назначение препаратов железа женщинам из групп риска по развитию ЖДА); 2. Постнатальную (соблюдение гигиенических условий жизни ребенка, длительное грудное вскармливание и своевременное введение прикормов, адекватный выбор смеси для детей, находящихся на смешанном и искусственном вскармливании, профилактика развития у ребенка рахита, гипотрофии и ОРВИ).
Профилактика ЖДА. 1. Антенатальная (правильный режим и питание беременной, своевременное выявление и лечение анемии беременной, превентивное назначение препаратов железа женщинам из групп риска по развитию ЖДА); 2. Постнатальную (соблюдение гигиенических условий жизни ребенка, длительное грудное вскармливание и своевременное введение прикормов, адекватный выбор смеси для детей, находящихся на смешанном и искусственном вскармливании, профилактика развития у ребенка рахита, гипотрофии и ОРВИ).
 В профилактическом назначении препаратов железа нуждаются: женщины репродуктивного возраста, страдающие обильными и длительными менструальными кровотечениями; n постоянные доноры; n беременные, особенно повторные беременности, следующие с коротким интервалом; n женщины с дефицитом железа в период лактации. n
В профилактическом назначении препаратов железа нуждаются: женщины репродуктивного возраста, страдающие обильными и длительными менструальными кровотечениями; n постоянные доноры; n беременные, особенно повторные беременности, следующие с коротким интервалом; n женщины с дефицитом железа в период лактации. n
 Профилактическое назначение препаратов железа показано детям из групп риска по развитию ЖДА: недоношенные дети (с 2 -месячного возраста); n дети от многоплодной беременности, осложненных беременностей и родов; n крупные дети с высокими темпами прибавки массы и роста; n дети с аномалиями конституции; n
Профилактическое назначение препаратов железа показано детям из групп риска по развитию ЖДА: недоношенные дети (с 2 -месячного возраста); n дети от многоплодной беременности, осложненных беременностей и родов; n крупные дети с высокими темпами прибавки массы и роста; n дети с аномалиями конституции; n
 Профилактическое назначение препаратов железа показано детям из групп риска по развитию ЖДА: n n n страдающие атопическими заболеваниями; находящиеся на искусственном вскармливании неадаптированными смесями; с хроническими заболеваниями; после кровопотерь и хирургических вмешательств; с синдромом мальабсорбции.
Профилактическое назначение препаратов железа показано детям из групп риска по развитию ЖДА: n n n страдающие атопическими заболеваниями; находящиеся на искусственном вскармливании неадаптированными смесями; с хроническими заболеваниями; после кровопотерь и хирургических вмешательств; с синдромом мальабсорбции.
 Доза железа, назначаемого с профилактической целью, зависит от степени недоношенности ребенка: n n n для детей с массой тела при рождении менее 1000 г — 4 мг Fe /кг/день; для детей с массой тела при рождении от 1000 до 1500 г — 3 мг Fe/кг/день; для детей с массой тела при рождении от 1500 до 3000 г — 2 мг Fe/кг/день.
Доза железа, назначаемого с профилактической целью, зависит от степени недоношенности ребенка: n n n для детей с массой тела при рождении менее 1000 г — 4 мг Fe /кг/день; для детей с массой тела при рождении от 1000 до 1500 г — 3 мг Fe/кг/день; для детей с массой тела при рождении от 1500 до 3000 г — 2 мг Fe/кг/день.


