 Железо
Железо
 Характеристика элемента Fe (железо) Порядковый номер: 26 Период: IV Группа: VIII Подгруппа: побочная Электронное строение атома: 3 d 64 S 2 l 26 электронов, 26 протонов, относительная атомная масса 56, 30 нейтронов. l 4 электронных слоя, 1 s 22 s 2 p 63 s 2 p 6 d 64 s 2 l Степень окисления 0, +2, +3 , +4 и иногда + 6; является восстановителем
Характеристика элемента Fe (железо) Порядковый номер: 26 Период: IV Группа: VIII Подгруппа: побочная Электронное строение атома: 3 d 64 S 2 l 26 электронов, 26 протонов, относительная атомная масса 56, 30 нейтронов. l 4 электронных слоя, 1 s 22 s 2 p 63 s 2 p 6 d 64 s 2 l Степень окисления 0, +2, +3 , +4 и иногда + 6; является восстановителем
 Физические свойства железа Серебристо-серый, мягкий металл, обладает хорошей пластичностью, ковкостью и способностью к намагничиванию. l Плотность 7, 864 г/см 3, температура плавления 1539 * С l
Физические свойства железа Серебристо-серый, мягкий металл, обладает хорошей пластичностью, ковкостью и способностью к намагничиванию. l Плотность 7, 864 г/см 3, температура плавления 1539 * С l
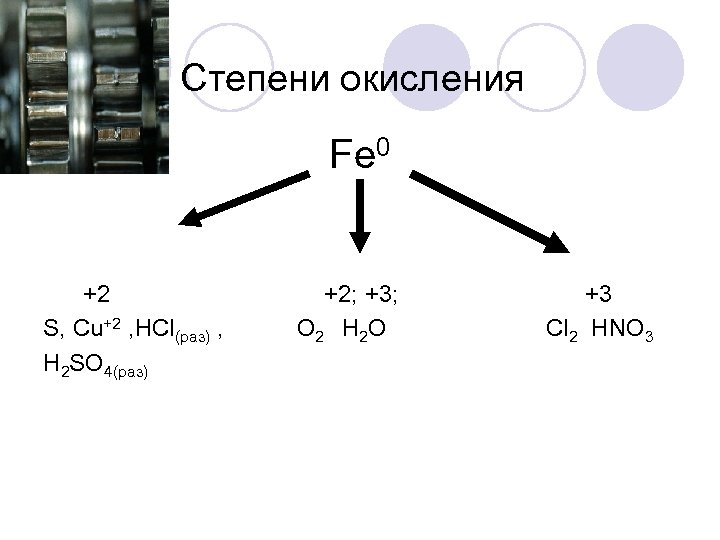 Степени окисления Fe 0 +2 S, Cu+2 , HCl(раз) , H 2 SO 4(раз) +2; +3; O 2 H 2 O +3 Cl 2 HNO 3
Степени окисления Fe 0 +2 S, Cu+2 , HCl(раз) , H 2 SO 4(раз) +2; +3; O 2 H 2 O +3 Cl 2 HNO 3
 Химические свойства При нагревании 2 Fe + 3 Cl 2 =2 Fe. Cl 3 3 Fe +2 O 2= Fe 3 O 4 (Fe. O Fe 2 O 3) Fe +S =Fe. S l При очень высокой температуре l 4 Fe + 3 C =Fe 4 C 3 l 4 Fe + 3 Si =Fe 4 Si 3 l 3 Fe + 2 P = Fe 3 P 2 l
Химические свойства При нагревании 2 Fe + 3 Cl 2 =2 Fe. Cl 3 3 Fe +2 O 2= Fe 3 O 4 (Fe. O Fe 2 O 3) Fe +S =Fe. S l При очень высокой температуре l 4 Fe + 3 C =Fe 4 C 3 l 4 Fe + 3 Si =Fe 4 Si 3 l 3 Fe + 2 P = Fe 3 P 2 l
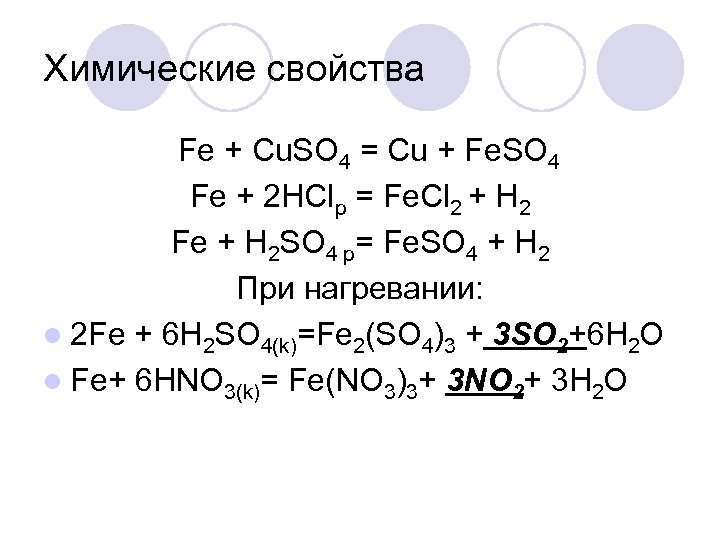 Химические свойства Fe + Cu. SO 4 = Cu + Fe. SO 4 Fe + 2 HClр = Fe. Cl 2 + H 2 Fe + H 2 SO 4 p= Fe. SO 4 + H 2 При нагревании: l 2 Fe + 6 H 2 SO 4(k)=Fe 2(SO 4)3 + 3 SO 2+6 H 2 O l Fe+ 6 HNO 3(k)= Fe(NO 3)3+ 3 NO 2+ 3 H 2 O
Химические свойства Fe + Cu. SO 4 = Cu + Fe. SO 4 Fe + 2 HClр = Fe. Cl 2 + H 2 Fe + H 2 SO 4 p= Fe. SO 4 + H 2 При нагревании: l 2 Fe + 6 H 2 SO 4(k)=Fe 2(SO 4)3 + 3 SO 2+6 H 2 O l Fe+ 6 HNO 3(k)= Fe(NO 3)3+ 3 NO 2+ 3 H 2 O
 Химические свойства Fe 0 + HNO 3 (p) = Fe +2(NO 3 )2 + N 20 + H 2 O Fe 0 + HNO 3(р) = Fe+3 (NO 3)3 + N+2 O + H 20 Fe 0 + HNO 3(р) = Fe+2(NO 3)2 + N-3 H 4 N+5 O 3+ H 2 O
Химические свойства Fe 0 + HNO 3 (p) = Fe +2(NO 3 )2 + N 20 + H 2 O Fe 0 + HNO 3(р) = Fe+3 (NO 3)3 + N+2 O + H 20 Fe 0 + HNO 3(р) = Fe+2(NO 3)2 + N-3 H 4 N+5 O 3+ H 2 O
 Минералы железа Fe 3 O 4 магнитный железняк или магнетит Fe 2 O 3 красный железняк или гематит 2 Fe 2 O 3. 3 H 2 O бурый железняк или лимонит Fe. S 2 железный или серный колчедан Fe. SO 4. 7 H 2 O железный купорос
Минералы железа Fe 3 O 4 магнитный железняк или магнетит Fe 2 O 3 красный железняк или гематит 2 Fe 2 O 3. 3 H 2 O бурый железняк или лимонит Fe. S 2 железный или серный колчедан Fe. SO 4. 7 H 2 O железный купорос
 Применение l l l l Магнитный, красный, бурый железняки –для производства черной металлургии (чугуна и стали) Железный колчедан – для производства серной кислоты Железный купорос– для борьбы с вредителями растений, для приготовления минеральных красок, для обработки древесины Соединение железа издавна применяют для лечения малокровия, при истощении, упадке сил. Чугун и сталь в технике и в быту. Хлорид железа(lll)– при очистке воды, в качестве протравы при крашении тканей. Сульфат железа(lll) при очистке воды, в качестве растворителя в гидрометаллургии.
Применение l l l l Магнитный, красный, бурый железняки –для производства черной металлургии (чугуна и стали) Железный колчедан – для производства серной кислоты Железный купорос– для борьбы с вредителями растений, для приготовления минеральных красок, для обработки древесины Соединение железа издавна применяют для лечения малокровия, при истощении, упадке сил. Чугун и сталь в технике и в быту. Хлорид железа(lll)– при очистке воды, в качестве протравы при крашении тканей. Сульфат железа(lll) при очистке воды, в качестве растворителя в гидрометаллургии.
 Источники железа Шпинат Салат Ка пуста Черная черешня Говядина Телятина
Источники железа Шпинат Салат Ка пуста Черная черешня Говядина Телятина
![Качественная реакция на катионы железа K 3[Fe(CN)6]—красная кровяная соль K 4[Fe(CN)6]– желтая кровяная соль Качественная реакция на катионы железа K 3[Fe(CN)6]—красная кровяная соль K 4[Fe(CN)6]– желтая кровяная соль](https://present5.com/presentation/ba852f0aa04f488e22ff74a0ec841881/image-11.jpg) Качественная реакция на катионы железа K 3[Fe(CN)6]—красная кровяная соль K 4[Fe(CN)6]– желтая кровяная соль Fe. Cl 2+ K 3[Fe(CN)6 = KFe[Fe(CN)6] турнбуллева синь Fe. Cl 3 + K 4[Fe(CN)6] = KFe[Fe(CN)6] берлинская лазурь KFe+2 [Fe+3 (CN)6] = KFe+3 [Fe+2 (CN)6] Турнбуллева синь берлинская лазурь
Качественная реакция на катионы железа K 3[Fe(CN)6]—красная кровяная соль K 4[Fe(CN)6]– желтая кровяная соль Fe. Cl 2+ K 3[Fe(CN)6 = KFe[Fe(CN)6] турнбуллева синь Fe. Cl 3 + K 4[Fe(CN)6] = KFe[Fe(CN)6] берлинская лазурь KFe+2 [Fe+3 (CN)6] = KFe+3 [Fe+2 (CN)6] Турнбуллева синь берлинская лазурь
 l Железо играет важную роль в жизнедеятельности живых организмов. l Входит в состав гемоглобина крови, соединения железа применяют l Используют для лечения малокровия, истощении, упадке сил.
l Железо играет важную роль в жизнедеятельности живых организмов. l Входит в состав гемоглобина крови, соединения железа применяют l Используют для лечения малокровия, истощении, упадке сил.