Железо и его соединения Триада железа Элементы







































![Качественные реакции на железо (II) и (III): 2 К 3[Fe(CN)6 ] +3 Fe Качественные реакции на железо (II) и (III): 2 К 3[Fe(CN)6 ] +3 Fe](https://present5.com/presentation/3/162870528_141599894.pdf-img/162870528_141599894.pdf-46.jpg)




Железо.ppt
- Количество слайдов: 45
 Железо и его соединения
Железо и его соединения
 Триада железа Элементы d-семейства Кристаллическая решетка железа
Триада железа Элементы d-семейства Кристаллическая решетка железа
 Fe 0 – 2 e → Fe 2+ Fe 0 – 3 e → Fe 3+ Fe 0 – 6 e → Fe 6+ Степени окисления 0, +2, +3, +6. Валентности II, III, VI
Fe 0 – 2 e → Fe 2+ Fe 0 – 3 e → Fe 3+ Fe 0 – 6 e → Fe 6+ Степени окисления 0, +2, +3, +6. Валентности II, III, VI
 Физические свойства
Физические свойства
 Ø Серебристо-серый металл, Ø ковкий, пластичный, Ø имеет относительно низкую тепло- и электропроводность (в 6 раз меньше Cu).
Ø Серебристо-серый металл, Ø ковкий, пластичный, Ø имеет относительно низкую тепло- и электропроводность (в 6 раз меньше Cu).
 Обладает сильными магнитными свойствами
Обладает сильными магнитными свойствами
 Нахождение в природе
Нахождение в природе
 v Второй по распространенности в земной коре металл после алюминия v Известно около 300 минералов
v Второй по распространенности в земной коре металл после алюминия v Известно около 300 минералов
 Железо в свободном состоянии встречается в метеоритах
Железо в свободном состоянии встречается в метеоритах
 Пирит (железный колчедан) (Fe. S 2)
Пирит (железный колчедан) (Fe. S 2)
 Халькопирит (Cu. Fe. S 2)
Халькопирит (Cu. Fe. S 2)
 Лимонит (бурый железняк) Fe 2 O 3· 3 H 2 O
Лимонит (бурый железняк) Fe 2 O 3· 3 H 2 O
 Гематит (красный железняк) (Fe 2 O 3)
Гематит (красный железняк) (Fe 2 O 3)
 Гематит (красный железняк) (Fe 2 O 3)
Гематит (красный железняк) (Fe 2 O 3)
 Магнетит (магнитный железняк) (Fe 3 O 4)
Магнетит (магнитный железняк) (Fe 3 O 4)
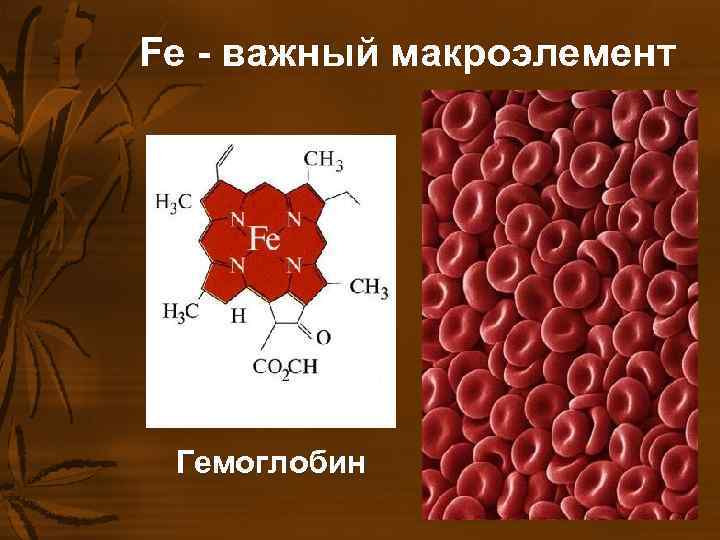
 Fe - важный макроэлемент Гемоглобин
Fe - важный макроэлемент Гемоглобин
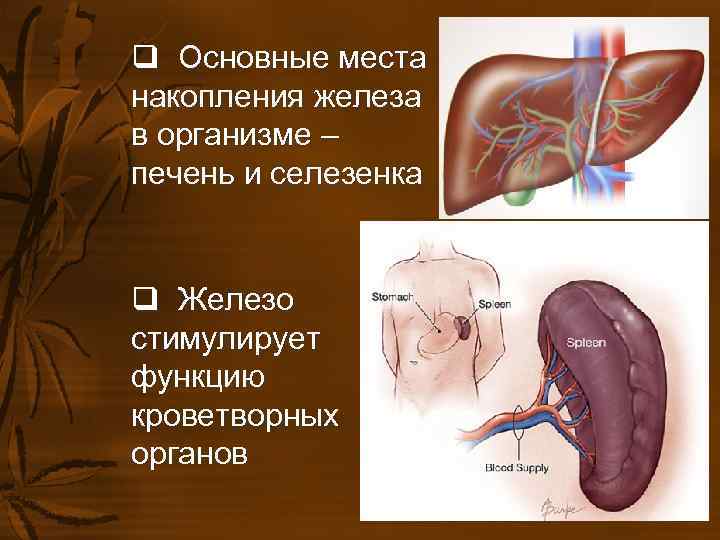
 q Основные места накопления железа в организме – печень и селезенка q Железо стимулирует функцию кроветворных органов
q Основные места накопления железа в организме – печень и селезенка q Железо стимулирует функцию кроветворных органов
 Хлороз листьев
Хлороз листьев
 Способы получения: 4 Fe. S 2 + 11 O 2 → 2 Fe 2 O 3 + 8 SO 2 Далее проводят восстановление Fe из оксида коксом (С) или СО в доменных печах: 3 Fe 2 O 3 + CO → 2 Fe 3 O 4 + CO 2 Fe 3 O 4 + CO → 3 Fe. O + CO 2 Fe. O + CO → Fe + CO 2
Способы получения: 4 Fe. S 2 + 11 O 2 → 2 Fe 2 O 3 + 8 SO 2 Далее проводят восстановление Fe из оксида коксом (С) или СО в доменных печах: 3 Fe 2 O 3 + CO → 2 Fe 3 O 4 + CO 2 Fe 3 O 4 + CO → 3 Fe. O + CO 2 Fe. O + CO → Fe + CO 2
 Схема устройства доменной печи
Схема устройства доменной печи
 Химические свойства
Химические свойства
 Взаимодействие с простыми веществами: С более активными неметаллами (F, Cl, Br) до Fe 3+ 2 Fe + 3 Cl 2 → 2 Fe. Cl 3 С кислородом: 3 Fe + 2 O 2 → Fe 3 O 4 железная окалина Fe. O·Fe 2 O 3
Взаимодействие с простыми веществами: С более активными неметаллами (F, Cl, Br) до Fe 3+ 2 Fe + 3 Cl 2 → 2 Fe. Cl 3 С кислородом: 3 Fe + 2 O 2 → Fe 3 O 4 железная окалина Fe. O·Fe 2 O 3
 С менее активными неметаллами (S, I) до Fe 2+ Fe + S → Fe. S Fe + I 2 → Fe. I 2 С P, С и Si реагирует только при очень высокой tº 3 Fe + 2 P → Fe 3 P 2 фосфид железа (II) 3 Fe + С → Fe 3 C карбид железа 3 Fe + Si → Fe 3 Si силицид железа
С менее активными неметаллами (S, I) до Fe 2+ Fe + S → Fe. S Fe + I 2 → Fe. I 2 С P, С и Si реагирует только при очень высокой tº 3 Fe + 2 P → Fe 3 P 2 фосфид железа (II) 3 Fe + С → Fe 3 C карбид железа 3 Fe + Si → Fe 3 Si силицид железа
 Взаимодействие со сложными веществами: С водой без доступа кислорода реагирует только при высокой температуре: 3 Fe + 4 H 2 O = Fe 3 O 4 + 4 H 2↑ На влажном воздухе или в воде корродирует: 4 Fe + 3 O 2 + 6 H 2 O = 4 Fe(OH)3 = Fe. O(OH) + H 2 O 2 Fe. O(OH) = Fe 2 O 3 + H 2 O
Взаимодействие со сложными веществами: С водой без доступа кислорода реагирует только при высокой температуре: 3 Fe + 4 H 2 O = Fe 3 O 4 + 4 H 2↑ На влажном воздухе или в воде корродирует: 4 Fe + 3 O 2 + 6 H 2 O = 4 Fe(OH)3 = Fe. O(OH) + H 2 O 2 Fe. O(OH) = Fe 2 O 3 + H 2 O
 Взаимодействие со сложными веществами: Со всеми кислотами, кроме азотной и серной концентрированной до Fe 2+ Fe + 2 HCl → Fe. Cl 2 + H 2 O Fe + H 2 SO 4(разб. ) → Fe. SO 4 + H 2 O С азотной и серной концентрированной до Fe 3+ При комнатной температуре концентрированной серной и азотной кислотой пассивируется
Взаимодействие со сложными веществами: Со всеми кислотами, кроме азотной и серной концентрированной до Fe 2+ Fe + 2 HCl → Fe. Cl 2 + H 2 O Fe + H 2 SO 4(разб. ) → Fe. SO 4 + H 2 O С азотной и серной концентрированной до Fe 3+ При комнатной температуре концентрированной серной и азотной кислотой пассивируется
 Взаимодействие со сложными веществами: 2 Fe + 6 H 2 SO 4(конц. ) → Fe 2(SO 4)3 + 3 SO 2↑ + 6 H 2 O Fe + 4 HNO 3(разб. ) → Fe(NO 3)3 + NO↑ + 2 H 2 O Fe + 6 HNO 3(конц. ) → Fe(NO 3)3 + 3 NO 2↑ + 3 H 2 O
Взаимодействие со сложными веществами: 2 Fe + 6 H 2 SO 4(конц. ) → Fe 2(SO 4)3 + 3 SO 2↑ + 6 H 2 O Fe + 4 HNO 3(разб. ) → Fe(NO 3)3 + NO↑ + 2 H 2 O Fe + 6 HNO 3(конц. ) → Fe(NO 3)3 + 3 NO 2↑ + 3 H 2 O
 Взаимодействие железа с концентрированной азотной кислотой:
Взаимодействие железа с концентрированной азотной кислотой:
 Взаимодействие с солями: Медь Cu Fe + Cu. SO 4 = Fe. SO 4 + Cu↓
Взаимодействие с солями: Медь Cu Fe + Cu. SO 4 = Fe. SO 4 + Cu↓
 Взаимодействие с солями: Ферратный вулкан Fe + 2 KNO 3 = K 2 Fe. O 4 + 2 NO
Взаимодействие с солями: Ферратный вулкан Fe + 2 KNO 3 = K 2 Fe. O 4 + 2 NO
 Соединения железа
Соединения железа
 +2 – основные свойства +3 - амфотерные свойства Fe. O – порошок черного цвета Fe 2 O 3 - вещества Fe(OН)2 – осадок белого Fe(OН)3 бурого или слегка зеленого цвета цвета Соли Fe 2+– бледно- Соли Fe 3+ – желто-бурого зеленого цвета +6 – кислотные свойства H 2 Fe. O 4 – железная кислота не выделена в свободном виде Ферраты (например, К 2 Fe. O 4 ) – пурпурно-красного цвета
+2 – основные свойства +3 - амфотерные свойства Fe. O – порошок черного цвета Fe 2 O 3 - вещества Fe(OН)2 – осадок белого Fe(OН)3 бурого или слегка зеленого цвета цвета Соли Fe 2+– бледно- Соли Fe 3+ – желто-бурого зеленого цвета +6 – кислотные свойства H 2 Fe. O 4 – железная кислота не выделена в свободном виде Ферраты (например, К 2 Fe. O 4 ) – пурпурно-красного цвета
 Оксид железа (II) (Fe. O)
Оксид железа (II) (Fe. O)
 Хлорид железа (II) (Fe. Cl 2)
Хлорид железа (II) (Fe. Cl 2)
 Железный купорос Fe. SO 4· 7 H 2 O)
Железный купорос Fe. SO 4· 7 H 2 O)
 Оксид железа (III) (Fe 2 O 3)
Оксид железа (III) (Fe 2 O 3)
 Гидроксид железа (III) (Fe(OH)3)
Гидроксид железа (III) (Fe(OH)3)
 Хлорид железа (III) (Fe. Cl 3)
Хлорид железа (III) (Fe. Cl 3)
 Железная окалина (Fe 3 O 4)
Железная окалина (Fe 3 O 4)
 Феррат калия (K 2 Fe. O 4)
Феррат калия (K 2 Fe. O 4)
 Оксид цинка Zn. O – порошок белого цвета
Оксид цинка Zn. O – порошок белого цвета
![> Качественные реакции на железо (II) и (III): 2 К 3[Fe(CN)6 ] +3 Fe > Качественные реакции на железо (II) и (III): 2 К 3[Fe(CN)6 ] +3 Fe](https://present5.com/presentation/3/162870528_141599894.pdf-img/162870528_141599894.pdf-46.jpg) Качественные реакции на железо (II) и (III): 2 К 3[Fe(CN)6 ] +3 Fe SO 4 = KFe[Fe(CN)6])↓ + 3 K 2 SO 4 3 К 4[Fe(CN)6 ] +4 Fe. Cl 3 = KFe[Fe(CN)6])↓ + 12 KCl Fe. Cl 3 + 3 КCNS = Fe(CNS)3 + 3 KCl
Качественные реакции на железо (II) и (III): 2 К 3[Fe(CN)6 ] +3 Fe SO 4 = KFe[Fe(CN)6])↓ + 3 K 2 SO 4 3 К 4[Fe(CN)6 ] +4 Fe. Cl 3 = KFe[Fe(CN)6])↓ + 12 KCl Fe. Cl 3 + 3 КCNS = Fe(CNS)3 + 3 KCl
 Кристаллы красной кровяной соли
Кристаллы красной кровяной соли
 Чугун
Чугун
 Сталь
Сталь
 Препараты железа необходимо применять при железодефицитных состояниях, связанных с длительными кровотечениями, недостаточной всасываемостью железа из желудочно-кишечного тракта, повышении потребности в ионах железа при беременности. • Мальтофер® • Актиферрин • Тирозол® • Диован® • Ферретаб® комп.
Препараты железа необходимо применять при железодефицитных состояниях, связанных с длительными кровотечениями, недостаточной всасываемостью железа из желудочно-кишечного тракта, повышении потребности в ионах железа при беременности. • Мальтофер® • Актиферрин • Тирозол® • Диован® • Ферретаб® комп.

