Эк_хим_Fe.ppt
- Количество слайдов: 13
 ЖЕЛЕЗО Формы нахождения в природе (по Ковде, 1985). Железо, по геохимической классификации, является типичным сидерофильным элементом (типичным металлом). К числу таких элементов также относятся и спутники железа в природе: кобальт, никель, молибден и др. Эти элементы имеют химическое сродство: • к углероду (образуют карбонаты), • к фосфору (многочисленные фосфаты), • а также к сере и кремнию (сульфаты, сульфиды, силикаты). Это вместе с тем элементы, образующие рудные жилы и месторождения. • Основные и ультраосновные (более тяжелые и более глубоко лежащие) магматические породы – базальты, перидотиты, диабазы – содержат от 5. 8 -9. 8 до 12 -16 % Fe. • Кислые изверженные породы – гнейсы, граниты – бедны Fe, его содержание в них 2. 7 -3. 0%. • Остальные породы в среднем содержат также немного Fe – 3 -4. 5%, но в рудных месторождениях содержание железа достигает 20 -40% и выше. Почва в среднем содержит 3 -4% Fe. Однако ожелезненные почвы и почвенные горизонты или конкреции содержат 15 -20% и даже 40 -60% Fe. В то же время известны песчаные почвы, которые имеют всего 0. 8 -1. 5%железа, и известняки – около 0. 5% Fe. В железосодержащих минералах изверженных и метаморфических пород (силикаты, сидерит, пирит) оно находится в восстановленной двухвалентной форме. В продуктах выветривания, в осадочных породах и в почвах Fe чаще присутствует в трехвалентной форме. Общая эволюция растительности и образования кислородной атмосферы на Земле способствовали господству окислительных процессов и преобладанию окисленных форм железа. Но и в осадочных породах, в почвах и водоемах формирование восстановленных форм железа (и марганца) – весьма распространенное явление и, пожалуй, главный механизм мобилизации его геохимически подвижных форм.
ЖЕЛЕЗО Формы нахождения в природе (по Ковде, 1985). Железо, по геохимической классификации, является типичным сидерофильным элементом (типичным металлом). К числу таких элементов также относятся и спутники железа в природе: кобальт, никель, молибден и др. Эти элементы имеют химическое сродство: • к углероду (образуют карбонаты), • к фосфору (многочисленные фосфаты), • а также к сере и кремнию (сульфаты, сульфиды, силикаты). Это вместе с тем элементы, образующие рудные жилы и месторождения. • Основные и ультраосновные (более тяжелые и более глубоко лежащие) магматические породы – базальты, перидотиты, диабазы – содержат от 5. 8 -9. 8 до 12 -16 % Fe. • Кислые изверженные породы – гнейсы, граниты – бедны Fe, его содержание в них 2. 7 -3. 0%. • Остальные породы в среднем содержат также немного Fe – 3 -4. 5%, но в рудных месторождениях содержание железа достигает 20 -40% и выше. Почва в среднем содержит 3 -4% Fe. Однако ожелезненные почвы и почвенные горизонты или конкреции содержат 15 -20% и даже 40 -60% Fe. В то же время известны песчаные почвы, которые имеют всего 0. 8 -1. 5%железа, и известняки – около 0. 5% Fe. В железосодержащих минералах изверженных и метаморфических пород (силикаты, сидерит, пирит) оно находится в восстановленной двухвалентной форме. В продуктах выветривания, в осадочных породах и в почвах Fe чаще присутствует в трехвалентной форме. Общая эволюция растительности и образования кислородной атмосферы на Земле способствовали господству окислительных процессов и преобладанию окисленных форм железа. Но и в осадочных породах, в почвах и водоемах формирование восстановленных форм железа (и марганца) – весьма распространенное явление и, пожалуй, главный механизм мобилизации его геохимически подвижных форм.
 Природные и антропогенные источники железа. При окислительном выветривании и почвообразовании образуются и накапливаются в остаточных типах коры выветривания и в автоморфных почвах преимущественно окисные и гидроокисные минералы трехвалентного железа. Они слаборастворимы и геихимически инертны. В первичных изверженных породах минералы железа представлены: силикатами, сидеритом (Fe. CO 3), оливином (Mg. Fe. Si. O 4), биотитом [H 4 K 2(Mg. Fe)6 Al 2 Si 6 O 24], титанатами (Fe 2 Ti. O 5, Fe. Ti. O 3), пирротином (Fe. S), пиритом (Fe. S 2). В основном железо здесь – в двухвалентной форме. В осадочных породах и почвах минералы железа унаследованы от исходных изверженных пород. Но в почвах и осадочных породах всегда присутствуют, а в мелкоземе преобладают, - вторичные минералы железа двухвалентной и трехвалентной форм. Таковы окислы гематит (Fe 2 O 3), магнетит (Fe. O·Fe 2 O 3), меггематит (Fe 2 O 3), гидроокислы (гетит - Fe. O·OH, лимонит – 2 Fe 2 O 3· 3 Н 2 О), сульфиды железа, кислые железистые минералы феронатрит [Na 3 Fe(SO 4)3· 3 H 2 O], ромерит и др. , многочисленные фосфаты и силикаты железа, арсенаты железа. Существуют также органожелезистые соединения (комплексы, хелаты), аморфные осадки гидроокислов, железо, поглощенное коллоидами. Из этого перечня видно, что соединения железа чрезвычайно многообразны и многочисленны. Именно различные минералы и соединения железа и марганца обусловливают яркие окраски различных почв: красную, желтоватую, оранжевую, темно-фиолетовую тропических; зеленоватую, синеватую, сизую глеевых; черную и черно-синюю лечебных сероводородных грязей и солончаков.
Природные и антропогенные источники железа. При окислительном выветривании и почвообразовании образуются и накапливаются в остаточных типах коры выветривания и в автоморфных почвах преимущественно окисные и гидроокисные минералы трехвалентного железа. Они слаборастворимы и геихимически инертны. В первичных изверженных породах минералы железа представлены: силикатами, сидеритом (Fe. CO 3), оливином (Mg. Fe. Si. O 4), биотитом [H 4 K 2(Mg. Fe)6 Al 2 Si 6 O 24], титанатами (Fe 2 Ti. O 5, Fe. Ti. O 3), пирротином (Fe. S), пиритом (Fe. S 2). В основном железо здесь – в двухвалентной форме. В осадочных породах и почвах минералы железа унаследованы от исходных изверженных пород. Но в почвах и осадочных породах всегда присутствуют, а в мелкоземе преобладают, - вторичные минералы железа двухвалентной и трехвалентной форм. Таковы окислы гематит (Fe 2 O 3), магнетит (Fe. O·Fe 2 O 3), меггематит (Fe 2 O 3), гидроокислы (гетит - Fe. O·OH, лимонит – 2 Fe 2 O 3· 3 Н 2 О), сульфиды железа, кислые железистые минералы феронатрит [Na 3 Fe(SO 4)3· 3 H 2 O], ромерит и др. , многочисленные фосфаты и силикаты железа, арсенаты железа. Существуют также органожелезистые соединения (комплексы, хелаты), аморфные осадки гидроокислов, железо, поглощенное коллоидами. Из этого перечня видно, что соединения железа чрезвычайно многообразны и многочисленны. Именно различные минералы и соединения железа и марганца обусловливают яркие окраски различных почв: красную, желтоватую, оранжевую, темно-фиолетовую тропических; зеленоватую, синеватую, сизую глеевых; черную и черно-синюю лечебных сероводородных грязей и солончаков.
 Благодаря своим свойствам Fe в различных формах широко вовлекается в индустриальнохозяйственную деятельность человека и отличается высокой технофильностью. Сейчас можно говорить о процессах современного «ожелезнения» окружающей человека среды и почв. В природную среду в процессе хозяйственной деятельности внесено > 10 млрд. т железо, из которых > 60% было рассеяно в пространстве. По этим же данным (Сысуев В. В. Железо. В кн. : Круговорот вещества в природе. М. : Изд-во МГУ, 1980, С. 118 -131), ежегодно в окружающую среду поступает в различной форме около 0. 25 млрд. т железа. Химические свойства Fe (по Глинке, 1978). Из элементов восьмой группы периодической системы элементов нас интересуют - железо, кобальт и никель (есть еще - рутений, родий, палладий, осмий, иридий и платина). Большинство элементов рассматриваемой группы имеют два электрона в наружном электронном слое атома; все эти элементы представляют собой металлы. Кроме наружных электронов, в образовании химических связей принимают участие также электроны из Предыдущего недостроенного слоя. Для этих элементов характерны степени окисления 2, 3, 4. Более высокие степени окисления проявляются реже. Сравнение химических и физических свойств элементов восьмой группы показывает, что Fe, Co, Ni очень сходны между собой и в то же время сильно отличаются от других элементов группы. Поэтому их обычно выделяют в семейство железа (остальные шесть элементов выделяются в группу платиновых металлов). Чистое железо получают различными методами. Чаще всего используют метод разложения пентакарбонила железа - Fe(CO)5. Во влажном воздухе железо быстро ржавеет, т. е. покрывается бурым налетом гидратированного оксида железа, который вследствие своей рыхлости не защищает железо от дальнейшего окисления.
Благодаря своим свойствам Fe в различных формах широко вовлекается в индустриальнохозяйственную деятельность человека и отличается высокой технофильностью. Сейчас можно говорить о процессах современного «ожелезнения» окружающей человека среды и почв. В природную среду в процессе хозяйственной деятельности внесено > 10 млрд. т железо, из которых > 60% было рассеяно в пространстве. По этим же данным (Сысуев В. В. Железо. В кн. : Круговорот вещества в природе. М. : Изд-во МГУ, 1980, С. 118 -131), ежегодно в окружающую среду поступает в различной форме около 0. 25 млрд. т железа. Химические свойства Fe (по Глинке, 1978). Из элементов восьмой группы периодической системы элементов нас интересуют - железо, кобальт и никель (есть еще - рутений, родий, палладий, осмий, иридий и платина). Большинство элементов рассматриваемой группы имеют два электрона в наружном электронном слое атома; все эти элементы представляют собой металлы. Кроме наружных электронов, в образовании химических связей принимают участие также электроны из Предыдущего недостроенного слоя. Для этих элементов характерны степени окисления 2, 3, 4. Более высокие степени окисления проявляются реже. Сравнение химических и физических свойств элементов восьмой группы показывает, что Fe, Co, Ni очень сходны между собой и в то же время сильно отличаются от других элементов группы. Поэтому их обычно выделяют в семейство железа (остальные шесть элементов выделяются в группу платиновых металлов). Чистое железо получают различными методами. Чаще всего используют метод разложения пентакарбонила железа - Fe(CO)5. Во влажном воздухе железо быстро ржавеет, т. е. покрывается бурым налетом гидратированного оксида железа, который вследствие своей рыхлости не защищает железо от дальнейшего окисления.
 В воде железо интенсивно корродирует; при обильном доступе кислорода образуются гидратные формы оксида железа (III): • 2 Fe + 3/2 O 2 + n. H 2 O = Fe 2 O 3 n. H 2 O При недостатке кислорода или при его затрудненном доступе образуется смешанный оксид Fe 3 O 4 (или - Fe. O Fe 2 O 3): • 3 Fe + 2 O 2 + n. H 2 O = Fe 3 O 4 n. H 2 O Железо растворяется в соляной кислоте любой концентрации: • Fe + 2 HCl = Fe. Cl 2 + H 2 Аналогично происходит растворение в разбавленной серной кислоте: • Fe + H 2 SO 4 = Fe. SO 4 + H 2 В концентрированных растворах серной кислоты железо окисляется до Fe(III): • 2 Fe + 6 H 2 SO 4 = Fe 2(SO 4)3 + 3 SO 2 + 6 H 2 O В разбавленных и умеренно концентрированных растворах азотной кислоты железо раств-ся: • Fe + 4 HNO 3 = Fe(NO 3)3 + NO + 2 H 2 O • • Для железа характерны два ряда соединений: соединения железа (II) и соединения железа (III). Первые отвечают оксиду железа (II), или закиси железа Fe. O; вторые - оксиду железа (III), или окиси железа, Fe 2 O 3. Кроме того, известны соли железной кислоты H 2 Fe. O 4, в которой степень окисления железа равна +6.
В воде железо интенсивно корродирует; при обильном доступе кислорода образуются гидратные формы оксида железа (III): • 2 Fe + 3/2 O 2 + n. H 2 O = Fe 2 O 3 n. H 2 O При недостатке кислорода или при его затрудненном доступе образуется смешанный оксид Fe 3 O 4 (или - Fe. O Fe 2 O 3): • 3 Fe + 2 O 2 + n. H 2 O = Fe 3 O 4 n. H 2 O Железо растворяется в соляной кислоте любой концентрации: • Fe + 2 HCl = Fe. Cl 2 + H 2 Аналогично происходит растворение в разбавленной серной кислоте: • Fe + H 2 SO 4 = Fe. SO 4 + H 2 В концентрированных растворах серной кислоты железо окисляется до Fe(III): • 2 Fe + 6 H 2 SO 4 = Fe 2(SO 4)3 + 3 SO 2 + 6 H 2 O В разбавленных и умеренно концентрированных растворах азотной кислоты железо раств-ся: • Fe + 4 HNO 3 = Fe(NO 3)3 + NO + 2 H 2 O • • Для железа характерны два ряда соединений: соединения железа (II) и соединения железа (III). Первые отвечают оксиду железа (II), или закиси железа Fe. O; вторые - оксиду железа (III), или окиси железа, Fe 2 O 3. Кроме того, известны соли железной кислоты H 2 Fe. O 4, в которой степень окисления железа равна +6.
 Соединения железа (II). Соли железа (II) образуются при растворении железа в разбавленных кислотах, кроме азотной. Важнейшая из них - сульфат железа, или железный купорос Fe. SO 4 7 Н 2 О, образующий светлозеленые кристаллы, хорошо растворимые в воде. На воздухе железный купорос постепенно выветривается и одновременно окисляется с поверхности, переходя в желто-бурую основную соль железа (III). Fe. SO 4 применяется для борьбы с вредителями растений, в производстве чернил и минеральных красок, при крашении тканей. При нагревании железного купороса выделяется вода и получается белая масса безводной соли Fe. SO 4. При взаимодействии раствора соли железа (II) со щелочью выпадает белый осадок гидроксида железа (II) Fe(OH)2, который на воздухе вследствие окисления быстро принимает зеленоватую, а затем бурую окраску, переходя в гидроксид железа (III) Fe(OH)3: • 4 Fe(OH)2 + O 2 + H 2 O = 4 Fe(OH)3 Карбонаты щелочных металлов осаждают из растворов солей железа (II) белый карбонат железа (II) Fe. CO 3. При действии воды, содержащей СО 2, карбонат железа, подобно карбонату кальция, частично переходит в более растворимую кислую соль Fe(HCO)3. В виде этой соли (гидрокарбоната железа) железо содержится в природных железистых водах. Соли железа (II) легко могут быть переведены в соли железа (III) действием различных окислителей: азотной кислоты, перманганата калия, хлора, например: • 6 Fe. SO 4 + 2 HNO 3 + 3 H 2 SO 4 = 3 Fe 2(SO 4)3 + 2 NO +4 H 2 O • 10 Fe. SO 4 + 2 KMn. O 4 + 8 H 2 SO 4 = 5 Fe 2(SO 4)3 + K 2 SO 4 + 2 Mn. SO 4 + 8 H 2 O Ввиду способности легко окисляться, соли железа (II) часто применяются как восстановители.
Соединения железа (II). Соли железа (II) образуются при растворении железа в разбавленных кислотах, кроме азотной. Важнейшая из них - сульфат железа, или железный купорос Fe. SO 4 7 Н 2 О, образующий светлозеленые кристаллы, хорошо растворимые в воде. На воздухе железный купорос постепенно выветривается и одновременно окисляется с поверхности, переходя в желто-бурую основную соль железа (III). Fe. SO 4 применяется для борьбы с вредителями растений, в производстве чернил и минеральных красок, при крашении тканей. При нагревании железного купороса выделяется вода и получается белая масса безводной соли Fe. SO 4. При взаимодействии раствора соли железа (II) со щелочью выпадает белый осадок гидроксида железа (II) Fe(OH)2, который на воздухе вследствие окисления быстро принимает зеленоватую, а затем бурую окраску, переходя в гидроксид железа (III) Fe(OH)3: • 4 Fe(OH)2 + O 2 + H 2 O = 4 Fe(OH)3 Карбонаты щелочных металлов осаждают из растворов солей железа (II) белый карбонат железа (II) Fe. CO 3. При действии воды, содержащей СО 2, карбонат железа, подобно карбонату кальция, частично переходит в более растворимую кислую соль Fe(HCO)3. В виде этой соли (гидрокарбоната железа) железо содержится в природных железистых водах. Соли железа (II) легко могут быть переведены в соли железа (III) действием различных окислителей: азотной кислоты, перманганата калия, хлора, например: • 6 Fe. SO 4 + 2 HNO 3 + 3 H 2 SO 4 = 3 Fe 2(SO 4)3 + 2 NO +4 H 2 O • 10 Fe. SO 4 + 2 KMn. O 4 + 8 H 2 SO 4 = 5 Fe 2(SO 4)3 + K 2 SO 4 + 2 Mn. SO 4 + 8 H 2 O Ввиду способности легко окисляться, соли железа (II) часто применяются как восстановители.
 Соединения железа (III). Хлорид железа (III) Fe. Cl 3 представляет собой темно-коричневые с зеленоватым отливом кристаллы. Это вещество сильно гигроскопично; поглощая влагу из воздуха, оно превращается в кристаллогидраты, содержащие различное количество воды и расплывающееся на воздухе. В разбавленном растворе Fe. Cl 3 гидролизуется до основных солей (например, Fe(OH)2 Cl). Сульфат железа (III) Fe 2(SO 4)3 - очень гигроскопичные, расплывающиеся на воздухе белые кристаллы. В водных растворах сульфат железа (III) сильно гидролизован. С сульфатами щелочных металлов и аммония он образует двойные соли - квасцы, например, железоаммонийные квасцы (NH 4)Fe(SO 4)2 12 H 2 O - хорошо растворимые в воде. Раствор Fe 2(SO 4)3 способен растворять Cu 2 S и Cu. S с образованием сульфата меди; это используется при гидрометаллургическом производстве меди. При действии щелочей на растворы солей железа (III) выпадает красно-бурый гидроксид железа Fe(OH)3, нерастворимый в избытке щелочи. Гидролизом объясняется цвет растворов солей железа (III): несмотря на то, что ион Fe 3+ почти бесцветен, содержащие его растворы окрашены в желто-бурый цвет, что объясняется присутствием гидроксионов железа или молекул Fe(OH)3, которые образуются благодаря гидролизу: • Fe 3+ + H 2 O Fe. OH 2+ + H+ • Fe. OH 2+ + H 2 O Fe(OH)2+ + H+ • Fe(OH)2+ + H 2 O Fe(OH)3 + H+ При прокаливании гидроксид железа (III), теряя воду, переходит в оксид железа (III), или окись железа, Fe 2 O 3. Оксид железа (III) встречается в природе в виде красного железняка и применяется как коричневая краска - железный сурик, или мумия.
Соединения железа (III). Хлорид железа (III) Fe. Cl 3 представляет собой темно-коричневые с зеленоватым отливом кристаллы. Это вещество сильно гигроскопично; поглощая влагу из воздуха, оно превращается в кристаллогидраты, содержащие различное количество воды и расплывающееся на воздухе. В разбавленном растворе Fe. Cl 3 гидролизуется до основных солей (например, Fe(OH)2 Cl). Сульфат железа (III) Fe 2(SO 4)3 - очень гигроскопичные, расплывающиеся на воздухе белые кристаллы. В водных растворах сульфат железа (III) сильно гидролизован. С сульфатами щелочных металлов и аммония он образует двойные соли - квасцы, например, железоаммонийные квасцы (NH 4)Fe(SO 4)2 12 H 2 O - хорошо растворимые в воде. Раствор Fe 2(SO 4)3 способен растворять Cu 2 S и Cu. S с образованием сульфата меди; это используется при гидрометаллургическом производстве меди. При действии щелочей на растворы солей железа (III) выпадает красно-бурый гидроксид железа Fe(OH)3, нерастворимый в избытке щелочи. Гидролизом объясняется цвет растворов солей железа (III): несмотря на то, что ион Fe 3+ почти бесцветен, содержащие его растворы окрашены в желто-бурый цвет, что объясняется присутствием гидроксионов железа или молекул Fe(OH)3, которые образуются благодаря гидролизу: • Fe 3+ + H 2 O Fe. OH 2+ + H+ • Fe. OH 2+ + H 2 O Fe(OH)2+ + H+ • Fe(OH)2+ + H 2 O Fe(OH)3 + H+ При прокаливании гидроксид железа (III), теряя воду, переходит в оксид железа (III), или окись железа, Fe 2 O 3. Оксид железа (III) встречается в природе в виде красного железняка и применяется как коричневая краска - железный сурик, или мумия.
 Соединения железа в почвах и природных водах(по Ковде, 1985). Педохимическая судьба соединений железа (а также марганца и алюминия) в значительной степени зависит от: • условий увлажнения, • реакции среды, • аэрированности почвы и величины Eh, • условий разложения органического вещества и • деятельности микроорганизмов. Восстановление железа (и марганца) наступает при Eh от +400 до +100 м. В. При отрицательных величинах Eh происходит восстановление сульфатов, нитратов и образование сульфидов, метана, водорода (табл. 1).
Соединения железа в почвах и природных водах(по Ковде, 1985). Педохимическая судьба соединений железа (а также марганца и алюминия) в значительной степени зависит от: • условий увлажнения, • реакции среды, • аэрированности почвы и величины Eh, • условий разложения органического вещества и • деятельности микроорганизмов. Восстановление железа (и марганца) наступает при Eh от +400 до +100 м. В. При отрицательных величинах Eh происходит восстановление сульфатов, нитратов и образование сульфидов, метана, водорода (табл. 1).
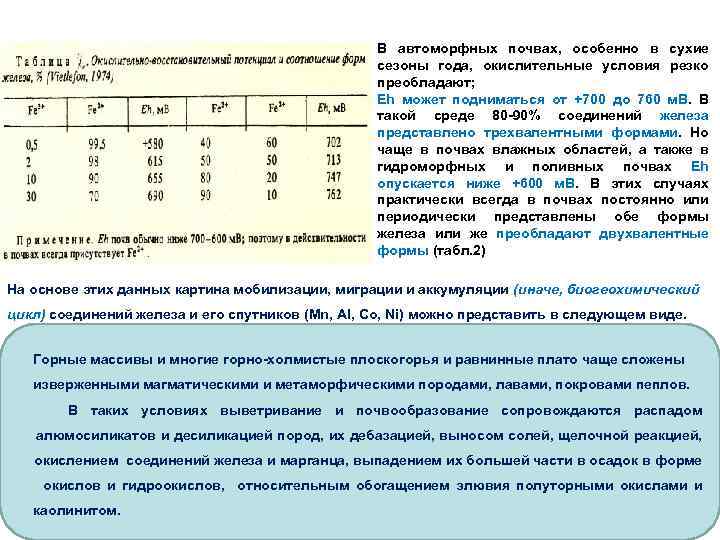 В автоморфных почвах, особенно в сухие сезоны года, окислительные условия резко преобладают; Eh может подниматься от +700 до 760 м. В. В такой среде 80 -90% соединений железа представлено трехвалентными формами. Но чаще в почвах влажных областей, а также в гидроморфных и поливных почвах Eh опускается ниже +600 м. В. В этих случаях практически всегда в почвах постоянно или периодически представлены обе формы железа или же преобладают двухвалентные формы (табл. 2) На основе этих данных картина мобилизации, миграции и аккумуляции (иначе, биогеохимический цикл) соединений железа и его спутников (Mn, Al, Co, Ni) можно представить в следующем виде. Горные массивы и многие горно-холмистые плоскогорья и равнинные плато чаще сложены изверженными магматическими и метаморфическими породами, лавами, покровами пеплов. В таких условиях выветривание и почвообразование сопровождаются распадом алюмосиликатов и десиликацией пород, их дебазацией, выносом солей, щелочной реакцией, окислением соединений железа и марганца, выпадением их большей части в осадок в форме окислов и гидроокислов, относительным обогащением элювия полуторными окислами и каолинитом.
В автоморфных почвах, особенно в сухие сезоны года, окислительные условия резко преобладают; Eh может подниматься от +700 до 760 м. В. В такой среде 80 -90% соединений железа представлено трехвалентными формами. Но чаще в почвах влажных областей, а также в гидроморфных и поливных почвах Eh опускается ниже +600 м. В. В этих случаях практически всегда в почвах постоянно или периодически представлены обе формы железа или же преобладают двухвалентные формы (табл. 2) На основе этих данных картина мобилизации, миграции и аккумуляции (иначе, биогеохимический цикл) соединений железа и его спутников (Mn, Al, Co, Ni) можно представить в следующем виде. Горные массивы и многие горно-холмистые плоскогорья и равнинные плато чаще сложены изверженными магматическими и метаморфическими породами, лавами, покровами пеплов. В таких условиях выветривание и почвообразование сопровождаются распадом алюмосиликатов и десиликацией пород, их дебазацией, выносом солей, щелочной реакцией, окислением соединений железа и марганца, выпадением их большей части в осадок в форме окислов и гидроокислов, относительным обогащением элювия полуторными окислами и каолинитом.
 Во влажных субтропиках и тропиках дебазация и десиликация горных пород и почв приводит к образованию кислых остаточных фералитных и аллитных кор выветривания и почв (красноземы, бокситы), которые обогащены остаточными формами окисленных соединений железа, марганца, титана, алюминия. В холодных лесных областях их аналогом являются кислые бурые почвы. Эрозия и переотложение смытого ферсиаллитного (содержащего Fe, Si, Al), аллитного и фераллитного мелкоземного материала приводят к образованию склонового делювия, пролювия, аллювия речных террас, также обогащенных окислами и гидроокислами Fe, Mn, Al и закрытых покровом фералитных и аллитных почв (бурых лесных, красноземов, бокситов) с возможными признаками литологической слоистости. Но этот сравнительно простой процесс осложнен крайней неустойчивостью окислов железа, марганца, алюминия, обусловленной растущей кислотностью среды, присутствием в почвах органических веществ, повышенной влажностью, анаэробностью и деятельностью микроорганизмов. Известно, что в этих условиях, особенно в теплый сезон, периодически или постоянно возникают резко восстановительные условия среды; при этом железо (и марганец) переходит в двухвалентные формы, возникают активные геохимические миграции в виде хелатных соединений, бикарбонатов (НСО 3+) и, возможно даже сульфидов и сульфатов. С водными потоками делювиальных, внутрипочвенных грунтовых вод геохимически активные соединения железа (а также Mn и Al) мигрируют в нисходящем и горизонтально-боковом направлении по склонам, в низменности, поймы, дельты и устья рек, в озера, моря, океан. Смены теплового и окислительно-восстановительного режимов, доступ кислорода, транспирация и испарение влаги, минерализация органики, деятельность железобактерий неизбежно ведут к осаждению значительной части подвижных соединений Fe, Mn, Al в транзитных и особенно в аккумулятивных ландшафтах.
Во влажных субтропиках и тропиках дебазация и десиликация горных пород и почв приводит к образованию кислых остаточных фералитных и аллитных кор выветривания и почв (красноземы, бокситы), которые обогащены остаточными формами окисленных соединений железа, марганца, титана, алюминия. В холодных лесных областях их аналогом являются кислые бурые почвы. Эрозия и переотложение смытого ферсиаллитного (содержащего Fe, Si, Al), аллитного и фераллитного мелкоземного материала приводят к образованию склонового делювия, пролювия, аллювия речных террас, также обогащенных окислами и гидроокислами Fe, Mn, Al и закрытых покровом фералитных и аллитных почв (бурых лесных, красноземов, бокситов) с возможными признаками литологической слоистости. Но этот сравнительно простой процесс осложнен крайней неустойчивостью окислов железа, марганца, алюминия, обусловленной растущей кислотностью среды, присутствием в почвах органических веществ, повышенной влажностью, анаэробностью и деятельностью микроорганизмов. Известно, что в этих условиях, особенно в теплый сезон, периодически или постоянно возникают резко восстановительные условия среды; при этом железо (и марганец) переходит в двухвалентные формы, возникают активные геохимические миграции в виде хелатных соединений, бикарбонатов (НСО 3+) и, возможно даже сульфидов и сульфатов. С водными потоками делювиальных, внутрипочвенных грунтовых вод геохимически активные соединения железа (а также Mn и Al) мигрируют в нисходящем и горизонтально-боковом направлении по склонам, в низменности, поймы, дельты и устья рек, в озера, моря, океан. Смены теплового и окислительно-восстановительного режимов, доступ кислорода, транспирация и испарение влаги, минерализация органики, деятельность железобактерий неизбежно ведут к осаждению значительной части подвижных соединений Fe, Mn, Al в транзитных и особенно в аккумулятивных ландшафтах.
 • Этим путем образуются ожелезненные иллювиальные горизонты почв, ортзанды, горизонты конкреций полуторных окислов, ортштейны, железисто-гумусовые прослои и хардпены, железистые погребенные древние горизонты в толще склоновых почв, латеритные горизонты в низменностях, пойменных и надпойменных отложениях. Этим же путем образуются болотные луговые железистые руды в депрессиях, низменностях, торфяниках. • Существенная часть геохимических мигрантов уносится подземными водами в океан. Таким образом, общая биогеохимическая направленность истории и миграции железа (и марганца) на поверхности земной коры включает: генерирование подвижных соединений, их транспорт и накопление в транзитных и аккумулятивных ландшафтах. • Многими исследованиями показано, что решающая роль в мобилизации и миграции соединений железа принадлежит фульвокислотам. Fe, Mn, Al образуют с фульвокислотами подвижные, активно мигрирующие в пространстве комплексные соединения. Так, фульвокислоты на 1 г углерода могут связывать несколько сот мг железа в виде хелатных соединений, мигрирующих на значительные расстояния (Лукашев К. И. Краткий очерк состояния четвертичных (антропогеновых) отложений Белоруссии. Минск: Изд-во АН БССР, 1969). Например, сезонное или постоянное заболачивание в почвах средней тайги сопровождается образованием комплексных Fe-органических соединений (с дубильными веществами и низкомолекулярными кислотами), которые могут свободно передвигаться как в нисходящем, так и в боковом горизонтальном и восходящем направлениях.
• Этим путем образуются ожелезненные иллювиальные горизонты почв, ортзанды, горизонты конкреций полуторных окислов, ортштейны, железисто-гумусовые прослои и хардпены, железистые погребенные древние горизонты в толще склоновых почв, латеритные горизонты в низменностях, пойменных и надпойменных отложениях. Этим же путем образуются болотные луговые железистые руды в депрессиях, низменностях, торфяниках. • Существенная часть геохимических мигрантов уносится подземными водами в океан. Таким образом, общая биогеохимическая направленность истории и миграции железа (и марганца) на поверхности земной коры включает: генерирование подвижных соединений, их транспорт и накопление в транзитных и аккумулятивных ландшафтах. • Многими исследованиями показано, что решающая роль в мобилизации и миграции соединений железа принадлежит фульвокислотам. Fe, Mn, Al образуют с фульвокислотами подвижные, активно мигрирующие в пространстве комплексные соединения. Так, фульвокислоты на 1 г углерода могут связывать несколько сот мг железа в виде хелатных соединений, мигрирующих на значительные расстояния (Лукашев К. И. Краткий очерк состояния четвертичных (антропогеновых) отложений Белоруссии. Минск: Изд-во АН БССР, 1969). Например, сезонное или постоянное заболачивание в почвах средней тайги сопровождается образованием комплексных Fe-органических соединений (с дубильными веществами и низкомолекулярными кислотами), которые могут свободно передвигаться как в нисходящем, так и в боковом горизонтальном и восходящем направлениях.
 Восстановительные процессы в почвах и образование в них двухвалентных подвижных органоминеральных соединений железа протекают тем интенсивнее в анаэробных условиях, чем больше содержат эти почвы гумуса • Почти все железо-марганцевые новообразования в почвах - ортштейнов, железистые хардпены и болотные руды - всегда содержат несколько процентов гумуса. Наиболее интенсивно осаждение и аккумуляция соединений железа в верхних горизонтах болотных почв происходят при р. Н 6. 3 -7. 4. При кислой реакции (р. Н ниже 5. 5) накопление железа в почвенных приповерхностных горизонтах не наблюдается. При высушивании болотных почв замечено повышение кислотности за счет окисления сульфидов. • Осаждение окислов железа является функцией окислительно-восстановительного потенциала среды. Так, упомянутые выше "маслянистые" пленки болот имели Eh на 50 -100 м. В выше, чем болота, на которых не наблюдается выпадение соединений железа в осадок. • В ландшафтах транзитного или аккумулятивного типа в зоне влажных лесов севера соединения железа (и алюминия) накапливаются в почвах тем в большем количестве, чем сильнее последние оглеены, т. е. чем хуже общие условия дренированности местности. При этом аккумулируются и соединения кремния.
Восстановительные процессы в почвах и образование в них двухвалентных подвижных органоминеральных соединений железа протекают тем интенсивнее в анаэробных условиях, чем больше содержат эти почвы гумуса • Почти все железо-марганцевые новообразования в почвах - ортштейнов, железистые хардпены и болотные руды - всегда содержат несколько процентов гумуса. Наиболее интенсивно осаждение и аккумуляция соединений железа в верхних горизонтах болотных почв происходят при р. Н 6. 3 -7. 4. При кислой реакции (р. Н ниже 5. 5) накопление железа в почвенных приповерхностных горизонтах не наблюдается. При высушивании болотных почв замечено повышение кислотности за счет окисления сульфидов. • Осаждение окислов железа является функцией окислительно-восстановительного потенциала среды. Так, упомянутые выше "маслянистые" пленки болот имели Eh на 50 -100 м. В выше, чем болота, на которых не наблюдается выпадение соединений железа в осадок. • В ландшафтах транзитного или аккумулятивного типа в зоне влажных лесов севера соединения железа (и алюминия) накапливаются в почвах тем в большем количестве, чем сильнее последние оглеены, т. е. чем хуже общие условия дренированности местности. При этом аккумулируются и соединения кремния.
 • При низкой дренированности территории и близких грунтовых водах (1 -1. 5 м) соединения железа доходят с капиллярной каймой до верхних горизонтов ( 0 -10, 0 -30 см), где накапливаются не только Fe и Mn, но и кремнезем (Si). Образуется белесый мучнистый горизонт А 1 и А 2 с обильной мучнистой массой кремнезема и многочисленными конкрециями полуторных окислов. • Аккумуляция соединений железа в поймах и дельтах выражена особенно сильно. • Перемежаемость окислительно-восстановительных условий и обилие органических веществ в поймах и дельтах создают благоприятные условия для образования и миграции двууглекислых ( НСО 3+) и органоминеральных комплексных соединений восстановленных форм железа, марганца и их спутников - никеля и кобальта. В грунтовых водах и почвенных растворах пойм и дельт всегда присутствуют подвижные соединения железа и марганца (особенно, если реакция среды слабокислая - тайга, субтропики и тропики), которые аккумулируются близ поверхности почв, в горизонтах скопления корешков травянистой и древесной растительности. В итоге происходит интенсивное новообразование вторичных соединений (конкреций, трубок, прослоев) железа и марганца во всей толще почвы над грунтовой водой. Максимум скопления вторичных соединений Fe и Mn обычно отмечается в верхних 20 -30 см почвы, пронизанных и скрепленных корнями (рис. 2, табл. 3).
• При низкой дренированности территории и близких грунтовых водах (1 -1. 5 м) соединения железа доходят с капиллярной каймой до верхних горизонтов ( 0 -10, 0 -30 см), где накапливаются не только Fe и Mn, но и кремнезем (Si). Образуется белесый мучнистый горизонт А 1 и А 2 с обильной мучнистой массой кремнезема и многочисленными конкрециями полуторных окислов. • Аккумуляция соединений железа в поймах и дельтах выражена особенно сильно. • Перемежаемость окислительно-восстановительных условий и обилие органических веществ в поймах и дельтах создают благоприятные условия для образования и миграции двууглекислых ( НСО 3+) и органоминеральных комплексных соединений восстановленных форм железа, марганца и их спутников - никеля и кобальта. В грунтовых водах и почвенных растворах пойм и дельт всегда присутствуют подвижные соединения железа и марганца (особенно, если реакция среды слабокислая - тайга, субтропики и тропики), которые аккумулируются близ поверхности почв, в горизонтах скопления корешков травянистой и древесной растительности. В итоге происходит интенсивное новообразование вторичных соединений (конкреций, трубок, прослоев) железа и марганца во всей толще почвы над грунтовой водой. Максимум скопления вторичных соединений Fe и Mn обычно отмечается в верхних 20 -30 см почвы, пронизанных и скрепленных корнями (рис. 2, табл. 3).
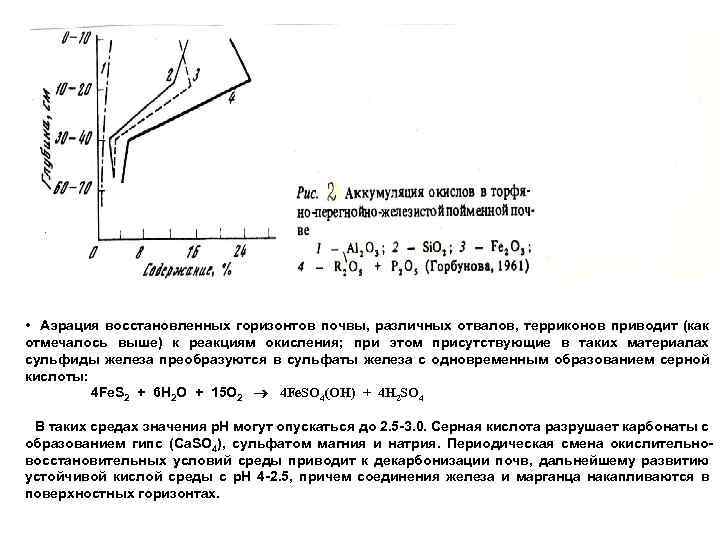 • Аэрация восстановленных горизонтов почвы, различных отвалов, терриконов приводит (как отмечалось выше) к реакциям окисления; при этом присутствующие в таких материалах сульфиды железа преобразуются в сульфаты железа с одновременным образованием серной кислоты: 4 Fe. S 2 + 6 H 2 O + 15 O 2 4 Fe. SO 4(OH) + 4 H 2 SO 4 В таких средах значения р. Н могут опускаться до 2. 5 -3. 0. Серная кислота разрушает карбонаты с образованием гипс (Ca. SO 4), сульфатом магния и натрия. Периодическая смена окислительновосстановительных условий среды приводит к декарбонизации почв, дальнейшему развитию устойчивой кислой среды с р. Н 4 -2. 5, причем соединения железа и марганца накапливаются в поверхностных горизонтах.
• Аэрация восстановленных горизонтов почвы, различных отвалов, терриконов приводит (как отмечалось выше) к реакциям окисления; при этом присутствующие в таких материалах сульфиды железа преобразуются в сульфаты железа с одновременным образованием серной кислоты: 4 Fe. S 2 + 6 H 2 O + 15 O 2 4 Fe. SO 4(OH) + 4 H 2 SO 4 В таких средах значения р. Н могут опускаться до 2. 5 -3. 0. Серная кислота разрушает карбонаты с образованием гипс (Ca. SO 4), сульфатом магния и натрия. Периодическая смена окислительновосстановительных условий среды приводит к декарбонизации почв, дальнейшему развитию устойчивой кислой среды с р. Н 4 -2. 5, причем соединения железа и марганца накапливаются в поверхностных горизонтах.


