 Желе зо (Fe) Желе зо — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 26. Один из самых распространённых в земной коре металлов.
Желе зо (Fe) Желе зо — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 26. Один из самых распространённых в земной коре металлов.
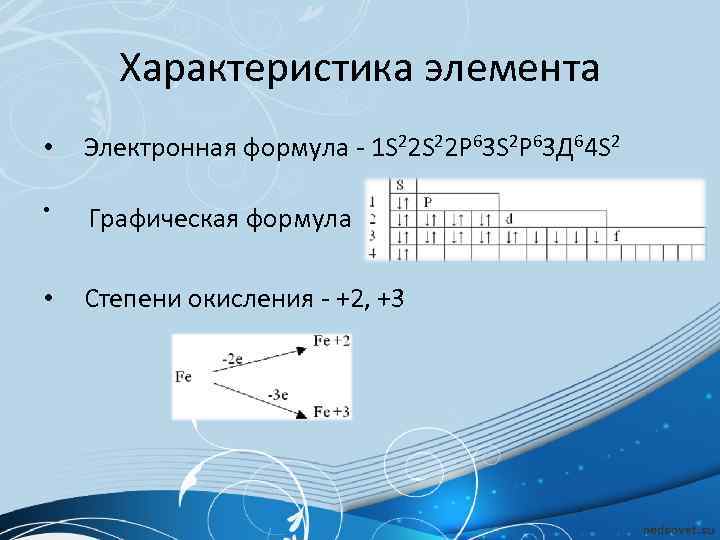 Характеристика элемента • Электронная формула - 1 S 22 P 63 S 2 Р 63 Д 64 S 2 • Графическая формула • Степени окисления - +2, +3
Характеристика элемента • Электронная формула - 1 S 22 P 63 S 2 Р 63 Д 64 S 2 • Графическая формула • Степени окисления - +2, +3
 Кристаллическая решетка • Кристаллическая решетка железа при комнатной температуре – кубическая объемноцентрированная.
Кристаллическая решетка • Кристаллическая решетка железа при комнатной температуре – кубическая объемноцентрированная.
 Физические свойства • Чистое железо — серебристо-белый активный металл, быстро тускнеющий (ржавеющий) на влажном воздухе или в воде, содержащей кислород. Железо пластично, легко подвергается ковке и прокатке, температура плавления 1539°С. Обладает сильными магнитными свойствами (ферромагнетик), хорошей тепло- и электропроводностью.
Физические свойства • Чистое железо — серебристо-белый активный металл, быстро тускнеющий (ржавеющий) на влажном воздухе или в воде, содержащей кислород. Железо пластично, легко подвергается ковке и прокатке, температура плавления 1539°С. Обладает сильными магнитными свойствами (ферромагнетик), хорошей тепло- и электропроводностью.
 Химические свойства • Железо — активный металл. 1. На воздухе образуется защитная оксидная пленка, препятствующая ржавению металла. 3 Fe + 2 O 2 = Fe 2 O 3 • Fe. O (Феррит железа) 2. Во влажном воздухе железо окисляется и покрывается ржавчиной, которая частично состоит из гидратированного оксида железа (III). 4 Fe + 3 О 2 + 6 Н 2 О = 4 Fe(ОН)3 3. Взаимодействует с хлором, углеродом и другими неметаллами при нагревании: 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 4. Железо вытесняет из растворов солей металлы, находящиеся в электрохимическом ряду напряжений правее железа: Fe + Cu. SO 4 = Fe. SO 4 + Cu 5. Растворяется в разбавленных серной и соляной кислотах c выделением водорода: Fe + 2 Cl = Fe. Cl 2 + H 2
Химические свойства • Железо — активный металл. 1. На воздухе образуется защитная оксидная пленка, препятствующая ржавению металла. 3 Fe + 2 O 2 = Fe 2 O 3 • Fe. O (Феррит железа) 2. Во влажном воздухе железо окисляется и покрывается ржавчиной, которая частично состоит из гидратированного оксида железа (III). 4 Fe + 3 О 2 + 6 Н 2 О = 4 Fe(ОН)3 3. Взаимодействует с хлором, углеродом и другими неметаллами при нагревании: 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 4. Железо вытесняет из растворов солей металлы, находящиеся в электрохимическом ряду напряжений правее железа: Fe + Cu. SO 4 = Fe. SO 4 + Cu 5. Растворяется в разбавленных серной и соляной кислотах c выделением водорода: Fe + 2 Cl = Fe. Cl 2 + H 2
 Оксиды и гидроксиды • Оксиды: • Гидроксиды:
Оксиды и гидроксиды • Оксиды: • Гидроксиды:
 Применение Железо — один из самых используемых металлов, на него приходится до 95 % мирового металлургического производства. Чистое железо имеет довольно ограниченное применение. Его используют при изготовлении сердечников электромагнитов, как катализатор химических процессов, для некоторых других целей. Но сплавы железа — чугун и сталь — составляют основу современной техники. Находят широкое применение и многие соединения железа. Так, сульфат железа (III) используют при водоподготовке, оксиды и цианид железа служат пигментами при изготовлении красителей
Применение Железо — один из самых используемых металлов, на него приходится до 95 % мирового металлургического производства. Чистое железо имеет довольно ограниченное применение. Его используют при изготовлении сердечников электромагнитов, как катализатор химических процессов, для некоторых других целей. Но сплавы железа — чугун и сталь — составляют основу современной техники. Находят широкое применение и многие соединения железа. Так, сульфат железа (III) используют при водоподготовке, оксиды и цианид железа служат пигментами при изготовлении красителей
 • Авторы: • Макаров Михаил • Асадченко Михаил
• Авторы: • Макаров Михаил • Асадченко Михаил
