«Зеленый» химический синтез. Общие принципы. доц. Матюшенков


«Зеленый» химический синтез. Общие принципы. доц. Матюшенков Е. А.

План лекции: Меры эффективности химических реакций Стратегия и тактика органического синтеза Общие рекомендации

Химический синтез — в узком смысле это процесс создания или построения сложных молекул из более простых. В широком смысле — получение химических соединений химическими и физическими методами. В зависимости от природы продукта синтез может быть органическим или неорганическим. Следует отметить, что в органическом синтезе продукт химической реакции может являться и более простым веществом, чем одно из исходных соединений. Впервые термин «синтез» в химии был употреблен приблизительно в 121 году н. э. знаменитым римским алхимиком Галадиеном. Понятие синтеза в современном смысле этого слова ввёл немецкий химик Герман Кольбе.
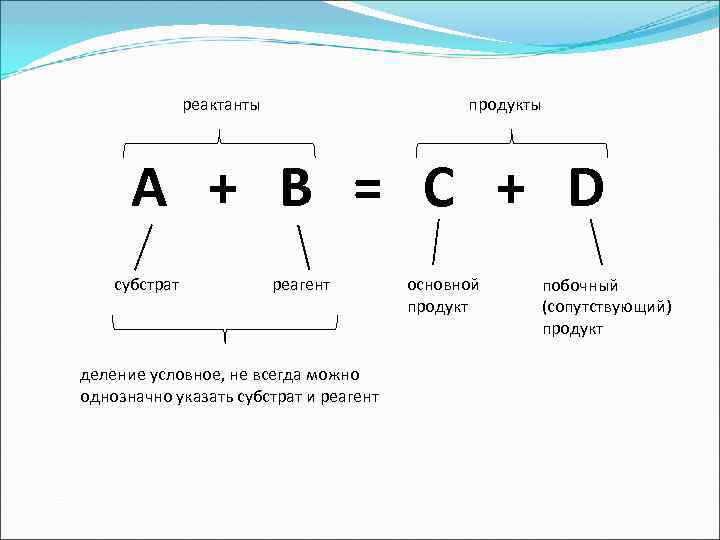
реактанты продукты А + B = C + D субстрат реагент основной побочный продукт (сопутствующий) продукт деление условное, не всегда можно однозначно указать субстрат и реагент

Меры эффективности химических реакций Например: Если из 78. 11 г бензола получили 81. 56 г малеинового ангидрида, то выход равен (81. 56 / 98. 06) х 100 % = 83. 17 %

Меры эффективности химических реакций Например: Если 1 моль толуола полностью прореагировал и из него получили 0. 37 моль желаемого пара-нитротолуола, то селективность равна (0. 37 / 1. 00) х 100 % = 37 %

Меры эффективности химических реакций При расчете необходимо учитывать коэффициенты в уравнении реакции! Например: % экономии атомов = 98 / (78 + 4. 5 х 32) х 100 % = 44. 14 %

Меры эффективности химических реакций Другой пример: % экономии атомов = 98 / (56 + 3 х 32) х 100 % = 64. 47 % Селективность получения малеинового ангидрида из бензола – 65%, а из бутена – 55%, однако за счет более высокой экономии атомов второй метод предпочтительнее.
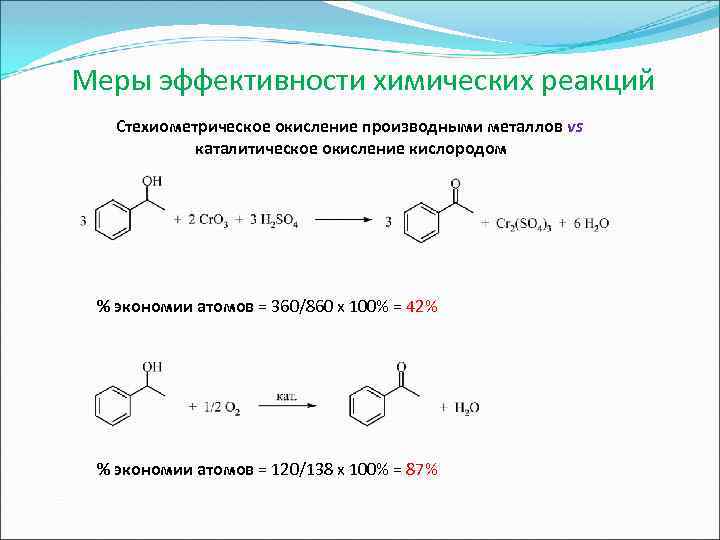
Меры эффективности химических реакций Стехиометрическое окисление производными металлов vs каталитическое окисление кислородом % экономии атомов = 360/860 х 100% = 42% % экономии атомов = 120/138 х 100% = 87%

Меры эффективности химических реакций Некоторые «экономные» и «неэкономные» реакции с точки зрения принципа экономии атомов «Экономные» реакции «Неэкономные» реакции Перегруппировки Реакции замещения Реакции Реакции отщепления присоединения (элиминирования) Реакция Дильса- Реакции окисления Альдера Другие согласованные Реакции с реакции металлоорганическими реагентами
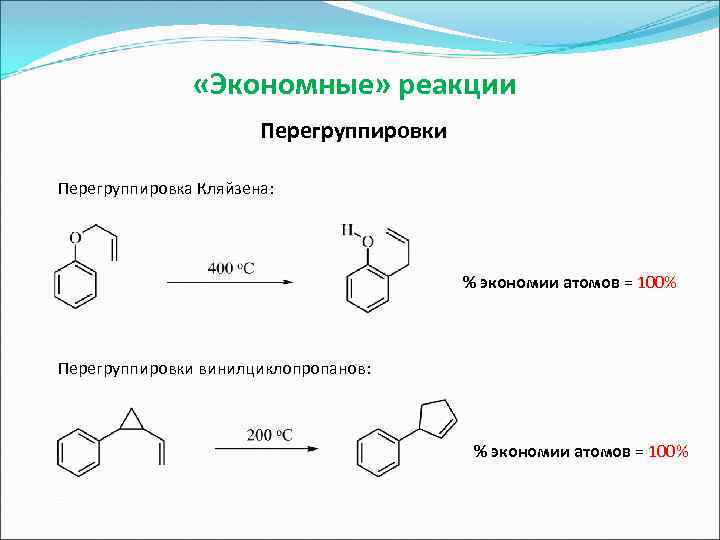
«Экономные» реакции Перегруппировки Перегруппировка Кляйзена: % экономии атомов = 100% Перегруппировки винилциклопропанов: % экономии атомов = 100%
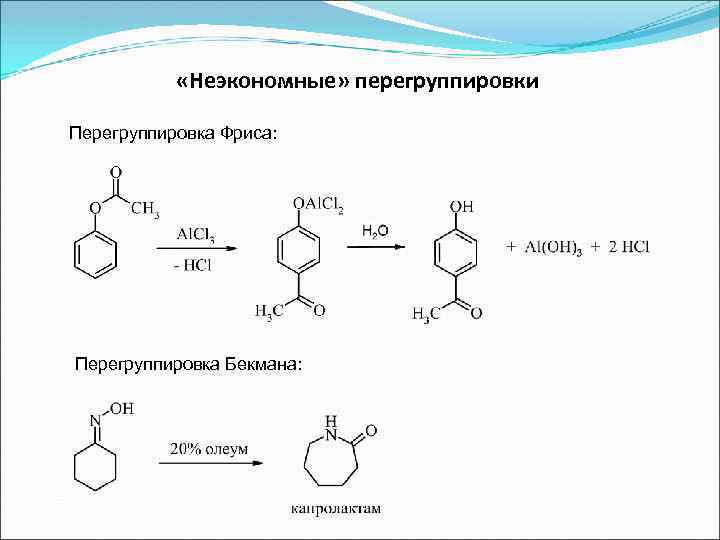
«Неэкономные» перегруппировки Перегруппировка Фриса: Перегруппировка Бекмана:
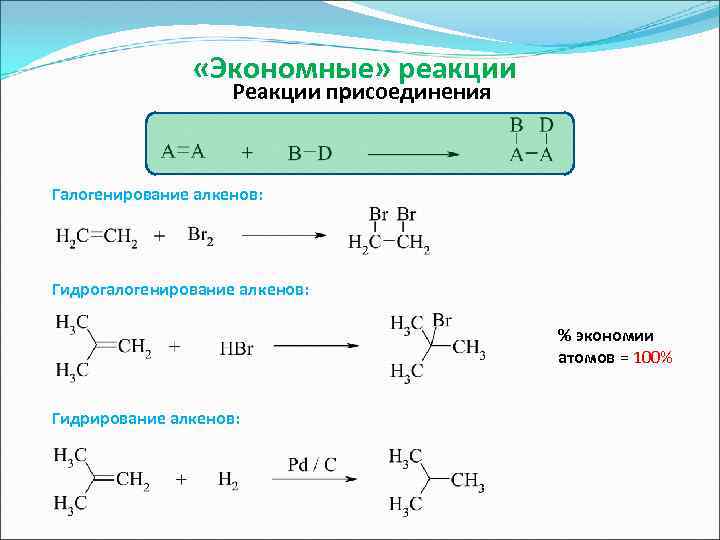
«Экономные» реакции Реакции присоединения Галогенирование алкенов: Гидрогалогенирование алкенов: % экономии атомов = 100% Гидрирование алкенов:
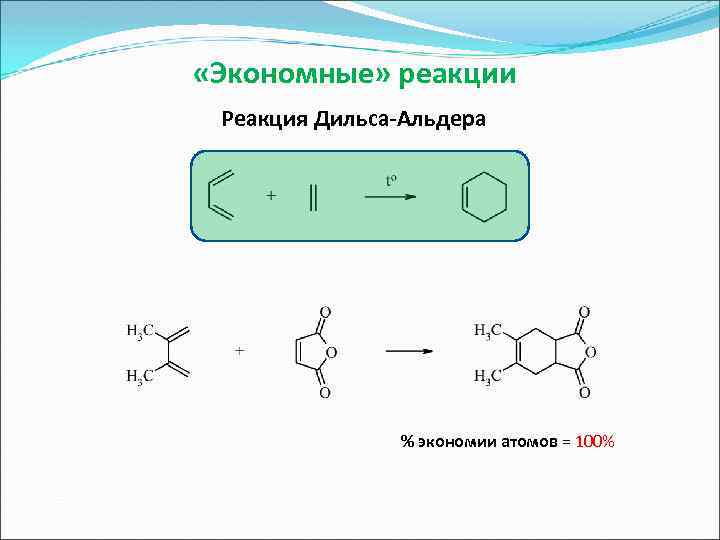
«Экономные» реакции Реакция Дильса-Альдера % экономии атомов = 100%

«Неэкономные» реакции Реакции замещения % экономии атомов = 92. 5/(74 + 36. 5) х 100% = 83. 7% % экономии атомов = 120. 5/(102 + 119) х 100% = 54. 5%

«Неэкономные» реакции Реакции отщепления % экономии атомов = 42/(122 + 112) х 100% = 17. 9%

Меры эффективности химических реакций Например: Е-фактор равен (2 х 44 + 2 х 18)/98 = 1. 26 ( «идеальный» Е-фактор)

Меры эффективности химических реакций При расчете Е-фактора необходимо учитывать: 1) побочные продукты и отходы на всех стадиях многостадийных процессов, 2) потери растворителей, 3) потери вспомогательных веществ, 4) отходы от очистки веществ, 5) отходы от нейтрализации отходов, 6) выходы на всех стадиях, 7) селективность реакций Е-фактор не учитывает токсичность отходов и их влияние на окружающую среду.
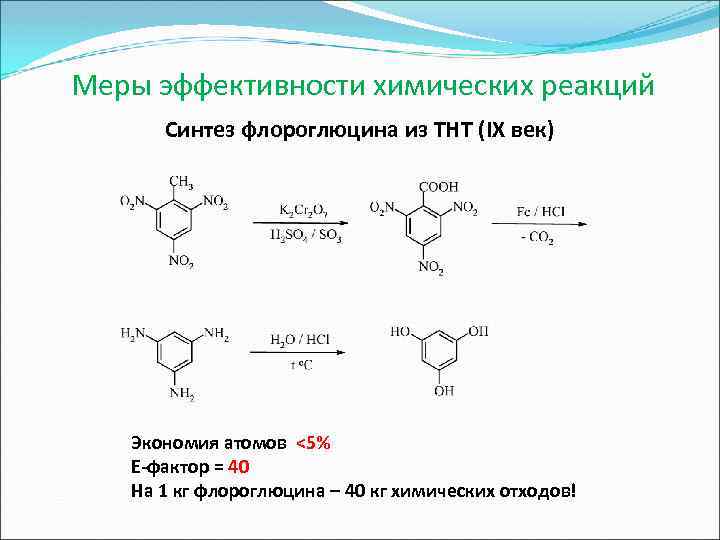
Меры эффективности химических реакций Синтез флороглюцина из ТНТ (IX век) Экономия атомов <5% E-фактор = 40 На 1 кг флороглюцина – 40 кг химических отходов!
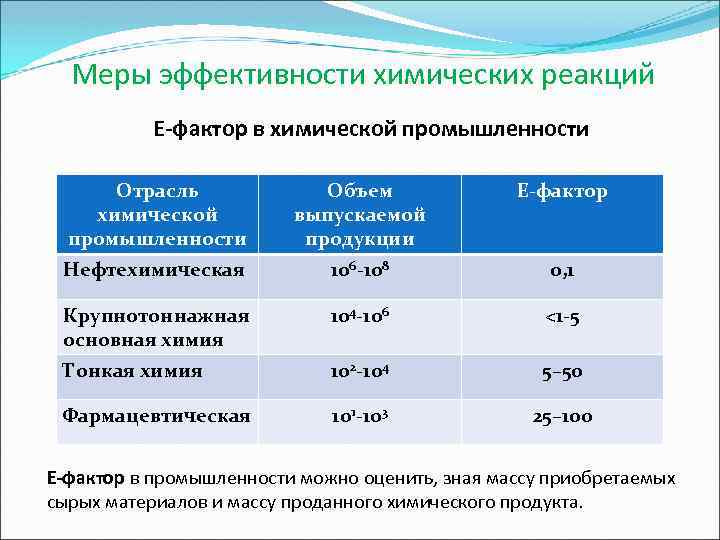
Меры эффективности химических реакций Е-фактор в химической промышленности Отрасль Объем Е-фактор химической выпускаемой промышленности продукции Нефтехимическая 106 -108 0, 1 Крупнотоннажная 104 -106 <1 -5 основная химия Тонкая химия 102 -104 5– 50 Фармацевтическая 101 -103 25– 100 Е-фактор в промышленности можно оценить, зная массу приобретаемых сырых материалов и массу проданного химического продукта.
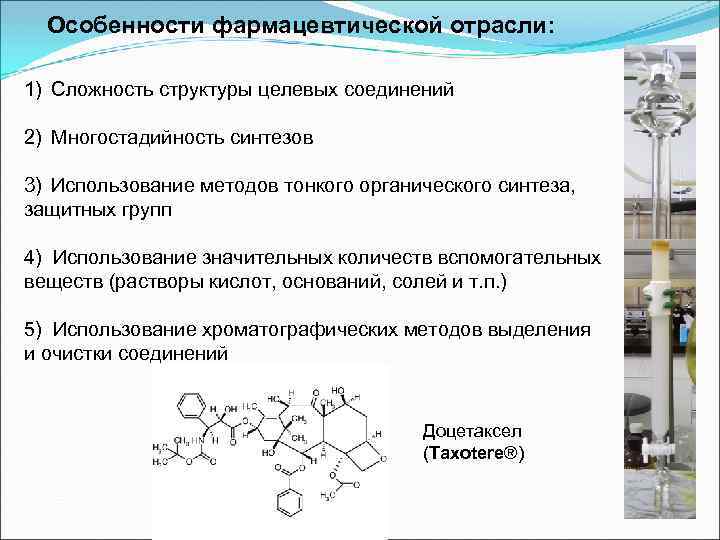
Особенности фармацевтической отрасли: 1) Сложность структуры целевых соединений 2) Многостадийность синтезов 3) Использование методов тонкого органического синтеза, защитных групп 4) Использование значительных количеств вспомогательных веществ (растворы кислот, оснований, солей и т. п. ) 5) Использование хроматографических методов выделения и очистки соединений Доцетаксел (Taxotere®)
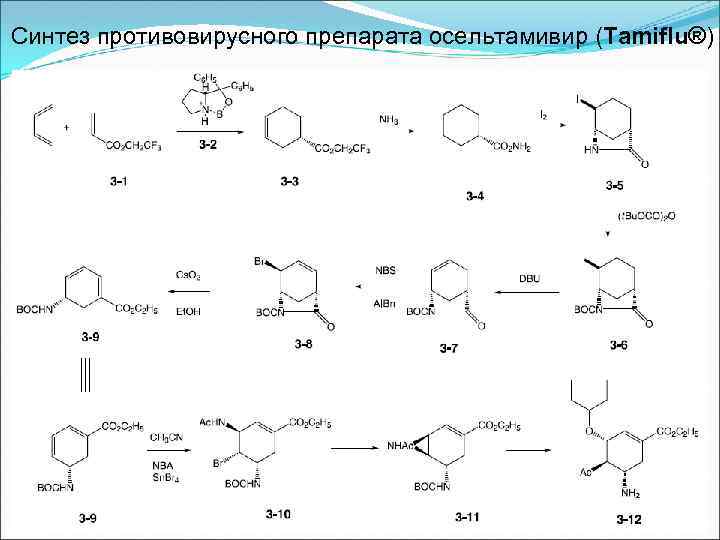
Синтез противовирусного препарата осельтамивир (Tamiflu®)
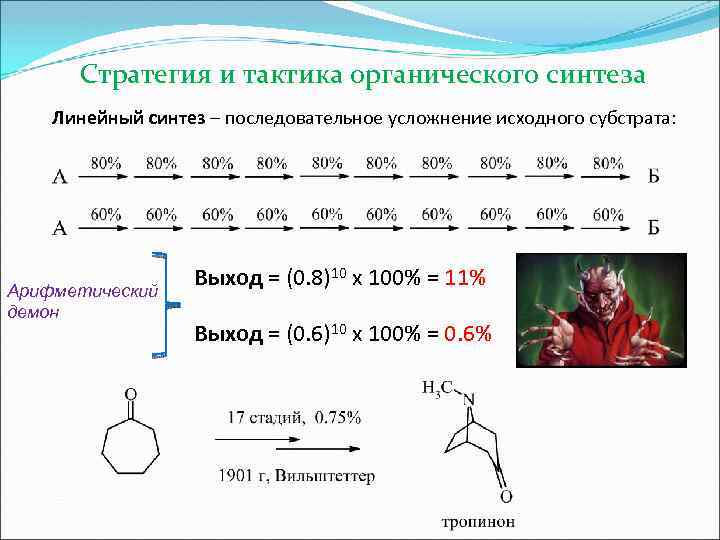
Стратегия и тактика органического синтеза Линейный синтез – последовательное усложнение исходного субстрата: Арифметический Выход = (0. 8)10 х 100% = 11% демон Выход = (0. 6)10 х 100% = 0. 6%
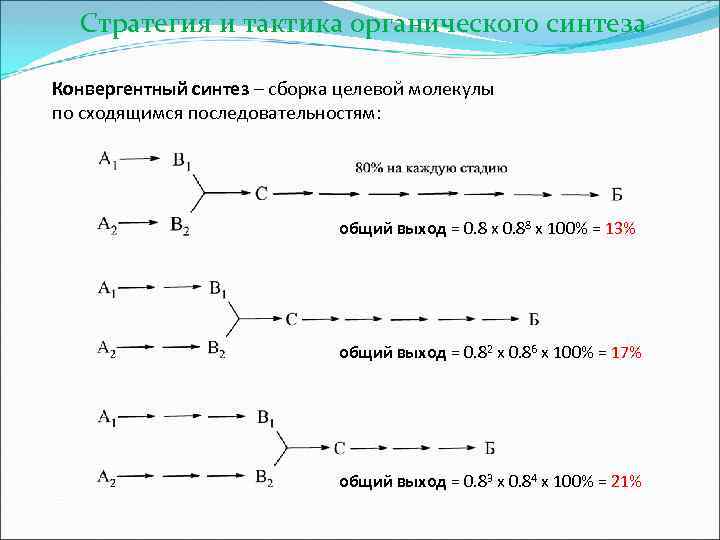
Стратегия и тактика органического синтеза Конвергентный синтез – сборка целевой молекулы по сходящимся последовательностям: общий выход = 0. 8 х 0. 88 х 100% = 13% общий выход = 0. 82 х 0. 86 х 100% = 17% общий выход = 0. 83 х 0. 84 х 100% = 21%
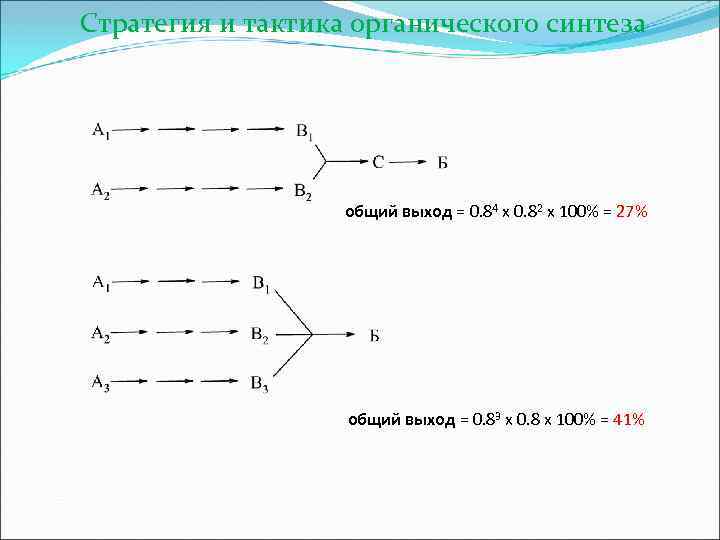
Стратегия и тактика органического синтеза общий выход = 0. 84 х 0. 82 х 100% = 27% общий выход = 0. 83 х 0. 8 х 100% = 41%
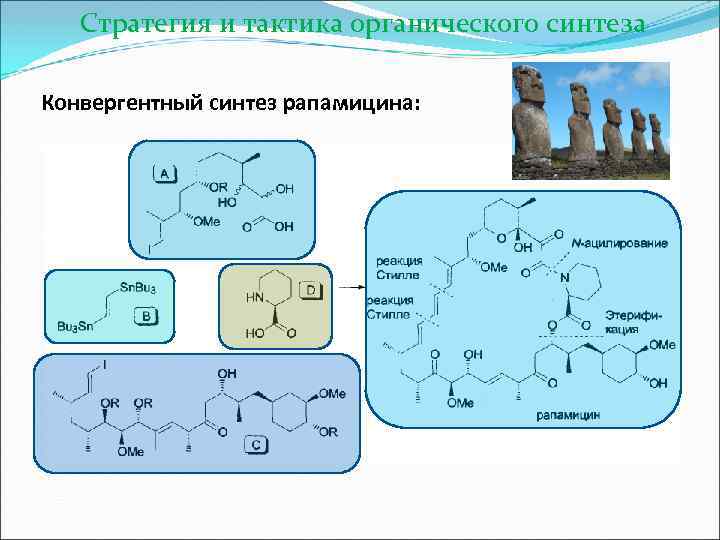
Стратегия и тактика органического синтеза Конвергентный синтез рапамицина:

Стратегия и тактика органического синтеза Выводы: 1) Наиболее эффективна синтетическая последовательность, в которой стадия конвергенции реализуется на поздних этапах синтетической схемы 2) Эффективность схемы синтеза возрастает при ее разветвлении 3) Эффективность схемы возрастает при увеличении выхода на каждой стадии 4) Основная стратегическая линия – увеличение молекулярной сложности

Общие рекомендации Выбор исходных материалов 1) Использование коммерчески доступных исходных материалов (быстрота, экономия, качество, уменьшение отходов) 2) Исходные соединения должны быть как можно ближе по структуре к продукту, чтобы число стадий модификации молекулы было минимальным 3) Исходные материалы должны быть как можно менее токсичными и как можно более устойчивыми при хранении 4) Исходные материалы должны быть представлены как можно большим количеством поставщиков

Общие рекомендации Выбор реагентов 1) Использование как можно более дешевых и коммерчески доступных реагентов 2) Использование как можно более низких избытков реагентов 3) Использование селективных реагентов 4) Рекомендуется использование «зеленых» реагентов (H 2, O 3, H 2 O 2 и др. )

Общие рекомендации Выбор растворителей 1) Минимизация использования растворителей, в идеале – процессы без растворителей 2) Использование дешевых, малотоксичных, немутагенных и неканцерогенных растворителей 3) Растворитель должен быть инертен по отношению к реактантам и продуктам, легко отделяться и регенерироваться 4) Следует избегать применения нескольких растворителей или смесей растворителей 5) Следует учитывать температуру кипения и плавления растворителей, плотность, летучесть, горючесть, смешиваемость с водой 4) Рекомендуется использование «зеленых» растворителей (H 2 O, сверхкритический CO 2)

Общие рекомендации Выбор температуры 1) Предпочтительна температура окружающей среды для проведения реакций – минимизируются затраты энергии 2) Повышение температуры увеличивает скорость реакции, но ведет к росту энергозатрат и иногда к увеличению количества побочных продуктов 3) Использование криогенных температур нежелательно, при этом очень сильно возрастают энергозатраты и расход растворителей

Спасибо за внимание!
Зеленый химический синтез.ppt
- Количество слайдов: 32

