a3403d874edbd951703aca6e61a89ffe.ppt
- Количество слайдов: 77

Zdravotnictví - terapie • chorobně se dělící buňky se častěji dělí a měly by proto být na záření citlivější než buňky zdravé - nemusí to být ale zcela pravda (není v nich obecně tolik kyslíku) • pravděpodobnost buněčné inaktivace vzrůstá s energií předávanou jednotlivým buňkám - pro různé druhy buněk může být tato pravděpodobnost značně rozdílná lze použít: • elektromagnetické záření (g, RTG) radioterapie • těžké nabité částice hadronová terapie • elektrony - nepoužívá se • (radioaktivní lázně - zvýšená přirozená aktivita pomáhá léčit zejména nemoci pohybového ústrojí - Jáchymov, . . . )
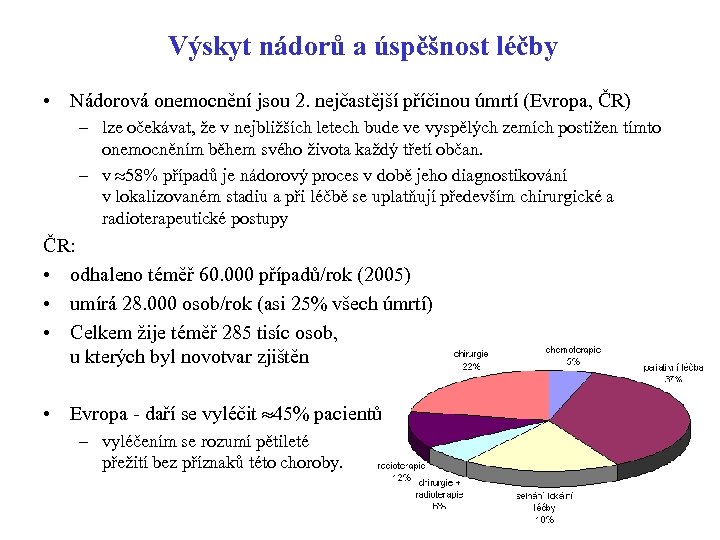
Výskyt nádorů a úspěšnost léčby • Nádorová onemocnění jsou 2. nejčastější příčinou úmrtí (Evropa, ČR) – lze očekávat, že v nejbližších letech bude ve vyspělých zemích postižen tímto onemocněním během svého života každý třetí občan. – v 58% případů je nádorový proces v době jeho diagnostikování v lokalizovaném stadiu a při léčbě se uplatňují především chirurgické a radioterapeutické postupy ČR: • odhaleno téměř 60. 000 případů/rok (2005) • umírá 28. 000 osob/rok (asi 25% všech úmrtí) • Celkem žije téměř 285 tisíc osob, u kterých byl novotvar zjištěn • Evropa - daří se vyléčit 45% pacientů – vyléčením se rozumí pětileté přežití bez příznaků této choroby.

Česká republika a rakovina v číslech (2010) • • • Každý třetí obyvatel ČR v průběhu svého života onemocní rakovinou a každý čtvrtý na ni zemře Každoročně onemocní v ČR rakovinou více než 77 000 lidí (2010) Každý rok zemře v ČR na rakovinu přes 27 000 lidí – ženy: plicní nádory (18 %), nádory prsu (18 %), nádory tlustého střeva (15 %) – muži: plicní nádory (35 %), nádory tlustého střeva (12 %), nádory prostaty (10 %) • • • V roce 2008 celkem žilo 418 887 osob, u kterých bylo v daném roce nebo dříve diagnostikováno onkologické onemocnění. Nejčastějším zhoubným onemocněním u mužů je karcinom plic; výrazně přibylo i karcinomů tl. střeva, konečníku a prostaty. Snižuje se výskyt karcinomu žaludku. Nejčastějším zhoubným onemocněním u žen je karcinom prsu; zarážející je výrazný nárůst nových případů karcinomu plic, pokles výskytu karcinomu žaludku a nezvyšující se nálezy karcinomu děložního čípku (důvodem jsou především zdokonalené preventivní prohlídky) U všech hlavních diagnóz, tedy zhoubných nádorů tlustého střeva a konečníku, prsu, plic a ledvin setrvale narůstá meziroční incidence o 2 – 4 % V posledním desetiletí nejrychleji roste počet nádorů plic (u žen), a nádorů tl. střeva a konečníku. Zvyšuje se i výskyt nádorů prsu, kůže, ledvin, močového měchýře a štítné žlázy. U mužů je vyšší výskyt nádorů jater, prostaty, varlat a mnohočetného myelomu.
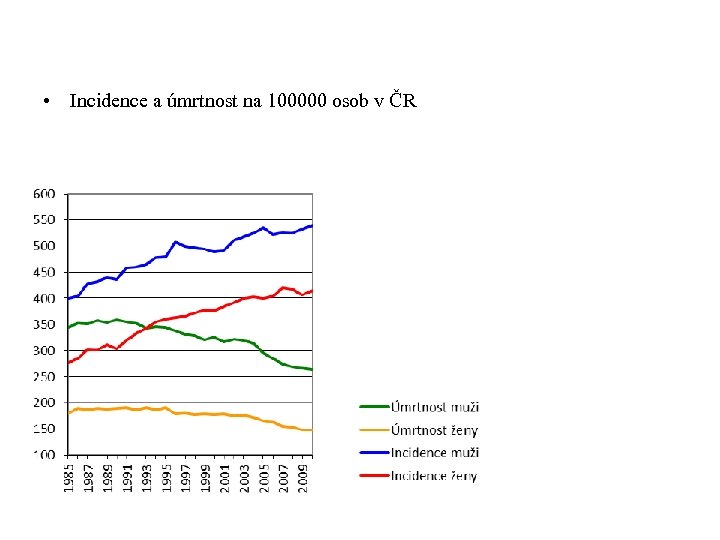
• Incidence a úmrtnost na 100000 osob v ČR
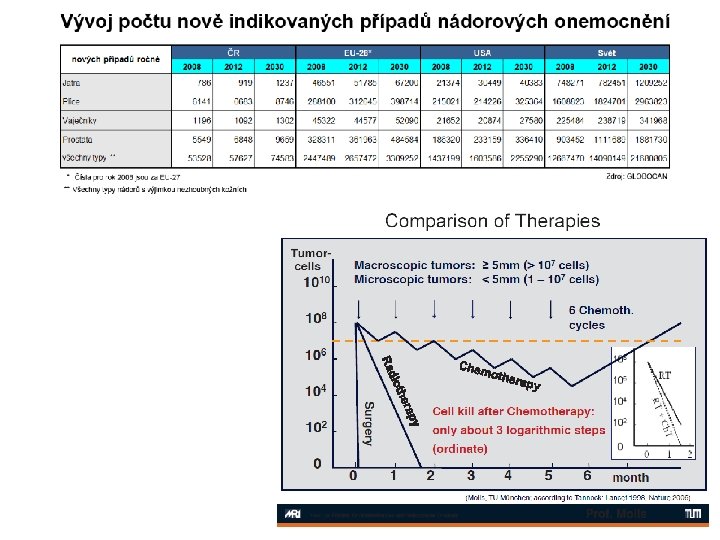

Radioterapie nádorových onemocnění • používá se při kurativní léčbě (vede k úplnému vyléčení pacienta) nádorových onemocnění v lokalizovaném stadiu – u pokročilejších stadií se využívá (někdy v kombinaci s chemoterapií) jako paliativní prostředek (jen léčba následků) • Podíl na léčbě (dnes 40% vyléčených případů) se možná zvýší – nové radioterapeutické metody – při zavádění nových diagnostických procedur a screeningových metod bude více nádorových onemocnění odhaleno již v iniciálním stadiu (radioterapie velmi účinná) • Cílem je likvidace nádorového ložiska při co nejmenším současném poškození okolních zdravých tkání - nesmí se překročit toleranční dávka zdravých tkání • Poškození zdravých tkání lze významně snížit – ozařováním z více směrů. – frakcionované ozařování, - celková dávka se rozdělí do většího počtu frakčních dávek, které se aplikují přibližně v denních intervalech zpravidla po dobu tří až pěti týdnů - využívá příznivého poměru tzv. kumulativního biologického účinku na nádorovou tkáň a na tkáň zdravou, která má větší regenerační schopnost

Radioterapie, Externí svazek • využívá se ozařování pomocí g (60 Co) nebo RTG (brzdné) záření (z LINACu) • místa ležící před cílovou oblastí jsou jednotlivými svazky ozářena zpravidla více než vlastní ložisko. • Pro mnohé nádory ležící v těsné blízkosti kritických orgánů vede radioterapie konvenčními svazky k vysokému riziku nepřípustného poškození těchto struktur • Evropa: 20 000 pacientů na 10 000 obyvatel ročně ozařováno radioterapií Typy ozáření: • • zdroj záření mimo tělo (externí svazek, g nůž, IMRT) zdroj záření uvnitř těla (brachyterapie) Externí svazek • radioizotopy - aplikují se tam, kde je vhodné použít jejich přesně danou energii záření – přirozená spolehlivost a malé nároky na údržbu • Lineární urychlovač - zdroj RTG záření Stav v roce 2002 u nás a v EU – správná činnost se musí kontrolovat denně – paprsek lze přesněji zaměřit a měnit jeho energii EU – přístroj mimo dobu používání nezáří ČR linac obyv/linac 60 Co linac/Co 1460 254 000 448 3, 26 24 425 000 25 0, 9
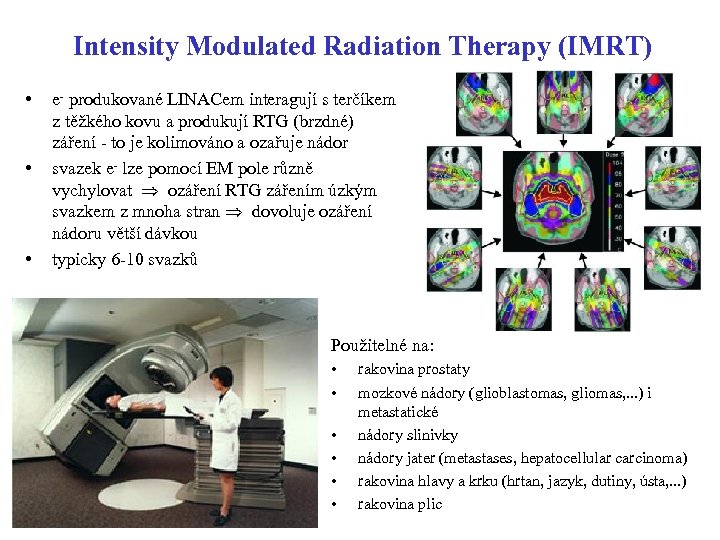
Intensity Modulated Radiation Therapy (IMRT) • • • e- produkované LINACem interagují s terčíkem z těžkého kovu a produkují RTG (brzdné) záření - to je kolimováno a ozařuje nádor svazek e- lze pomocí EM pole různě vychylovat ozáření RTG zářením úzkým svazkem z mnoha stran dovoluje ozáření nádoru větší dávkou typicky 6 -10 svazků Použitelné na: • • • rakovina prostaty mozkové nádory (glioblastomas, gliomas, . . . ) i metastatické nádory slinivky nádory jater (metastases, hepatocellular carcinoma) rakovina hlavy a krku (hrtan, jazyk, dutiny, ústa, . . . ) rakovina plic
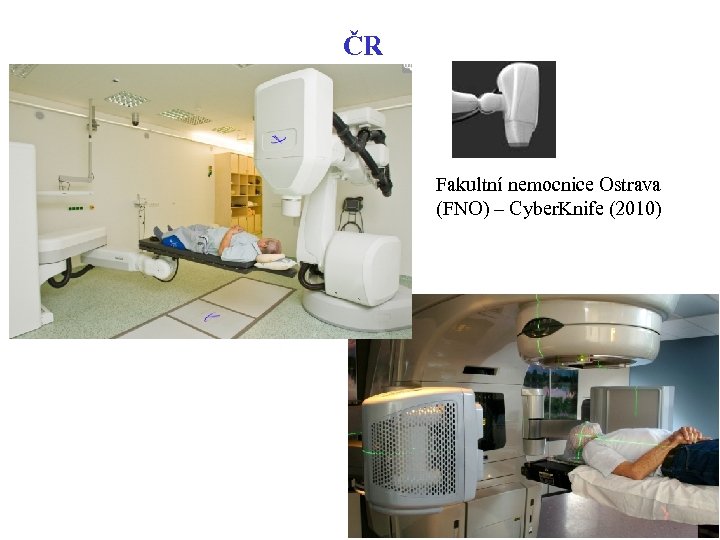
ČR Fakultní nemocnice Ostrava (FNO) – Cyber. Knife (2010)
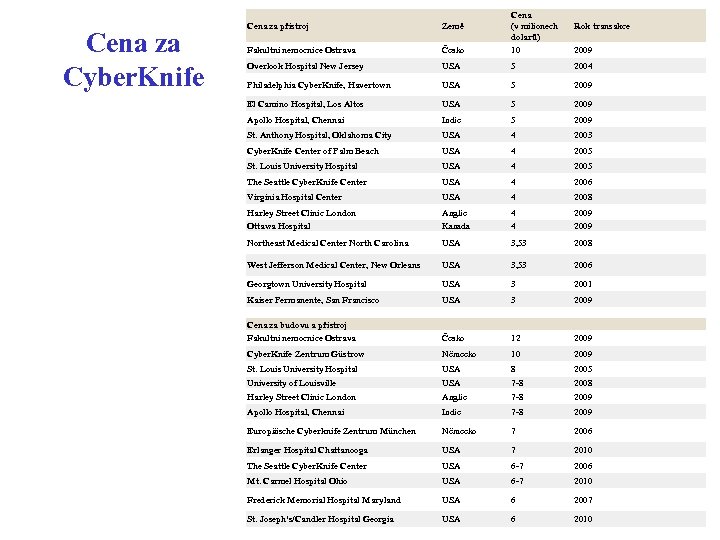
Cena za Cyber. Knife Cena za přístroj Země Cena (v milionech dolarů) Rok transakce Fakultní nemocnice Ostrava Česko 10 2009 Overlook Hospital New Jersey USA 5 2004 Philadelphia Cyber. Knife, Havertown USA 5 2009 El Camino Hospital, Los Altos USA 5 2009 Apollo Hospital, Chennai Indie 5 2009 St. Anthony Hospital, Oklahoma City USA 4 2003 Cyber. Knife Center of Palm Beach USA 4 2005 St. Louis University Hospital USA 4 2005 The Seattle Cyber. Knife Center USA 4 2006 Virginia Hospital Center USA 4 2008 Harley Street Clinic London Anglie 4 2009 Ottawa Hospital Kanada 4 2009 Northeast Medical Center North Carolina USA 3, 53 2008 West Jefferson Medical Center, New Orleans USA 3, 53 2006 Georgtown University Hospital USA 3 2001 Kaiser Permanente, San Francisco USA 3 2009 Fakultní nemocnice Ostrava Česko 12 2009 Cyber. Knife Zentrum Güstrow Německo 10 2009 St. Louis University Hospital USA 8 2005 University of Louisville USA 7 -8 2008 Harley Street Clinic London Anglie 7 -8 2009 Apollo Hospital, Chennai Indie 7 -8 2009 Europäische Cyberknife Zentrum München Německo 7 2006 Erlanger Hospital Chattanooga USA 7 2010 The Seattle Cyber. Knife Center USA 6 -7 2006 Mt. Carmel Hospital Ohio USA 6 -7 2010 Frederick Memorial Hospital Maryland USA 6 2007 St. Joseph's/Candler Hospital Georgia USA 6 2010 Cena za budovu a přístroj

Leksellův gama nůž • 1. v roce 1967 ve Stockholmu (idea od Larse Leksella - stereotactic radiosurgery) • používá se k léčení mozkových nádorů • skládá se z pohyblivého operačního stolu a z velké ocelové ozařovací hlavice, která obsahuje 201 zářičů 60 Co ve formě proutků • systém clon zajistí kolimaci záření do jednoho místa s přesností 0. 1 mm • dávka záření g zničí v krátkém okamžiku přesně vymezený a ostře ohraničený kousek tkáně • terapie trvá 5 až 30 minut (celá procedura včetně předchozího zobrazení tkání a cév v mozku a radiofyzikálních výpočtů asi 3 až 5 hodin) – díky peněžní sbírce má ČR v nemocnici Na Homolce – použití pro zhoubné i nezhoubné nádory Omezení: • není vhodný pro velké terčíky (3 -4 cm) • ztrácí schopnost šetřit okolní tkáň pro velké množství terčíků • není používán mimo hlavu (symetrie)

Leksellův gamma-nůž v ČR • pracoviště Leksellova gama nože v Nemocnici Na Homolce funguje od r. 1992 • Na světě je asi 260 (v 70 nemocnicích? ) na světě – většinou v USA a v Japonsku. V Evropě jich je zatím méně než deset. • v roce 2002 a poté i 2006 prošel nůž kompletní modernizací za 20 mil. Kč a 50 mil. Kč • v letech 1992 – 2012 zde bylo provedeno přes 13 300 ozařovacích výkonů • v posledních letech kolem 800 zákroků ročně • úspěšnost léčby je kolem 90% • léčebný zákrok g nožem je v ČR hrazen zdravotním pojištěním - platba činí zhruba 44 000 Kč za výkon (? ) • Od r. 2010 nahrazen zcela novým nožem (cena 150 mil. Kč)

Brachyradioterapie (ozařování zblízka) • • brachy = řecky „malá vzdálenost“ je to typ radioterapie je používáno u relativně malých a dobře přístupných nádorových ložisek zdroj záření se zavádí do bezprostřední blízkosti nádoru – např. do pochvy při ozařování nádorů děložního hrdla nebo do průdušek při nádorech, které zužují průdušku a znesnadňují dýchání) nebo ve formě jehel či drátů přímo do nádorového ložiska – např. do nádoru prsu nebo konečníku • zdokonalení představuje tzv. afterloading: do cílové oblasti či tělesné dutiny se nejprve zavede hadička, která se přesně nastaví; do ní se pak na stanovenou dobu zavádí vlastní zářič • používají se zářiče: 60 Co, 137 Cs, 192 Ir (dříve i 226 Ra - nevýhoda - vzniká Rn) • zářiče mají tvar jehel, nebo tub • u nás více nemocnic (Masarykův onkol. ústav v Brně, …)

RBE a OER Důležitými veličinami pro popis účinků zážení na tkáň jsou i Relative Biological Effectiveness (RBE) • podíl dávky referenčního typu záření (obvykle 250 ke. V g) vůči dávce záření, jež nás zajímá, při stejném biologickém účinku – pro stejné použité záření je RBE funkcí vyšetřovaného biologického systému a referenčního záření – RBE pro g i p velice podobné Oxygen enhancement ratio (OER) • poměr dávek v tkáni bez O 2 vůči tkáni s O 2 vedoucí ke stejnému biologickém účinku – asi 10% nádorů je hipoxidních relativně vůči fotonům
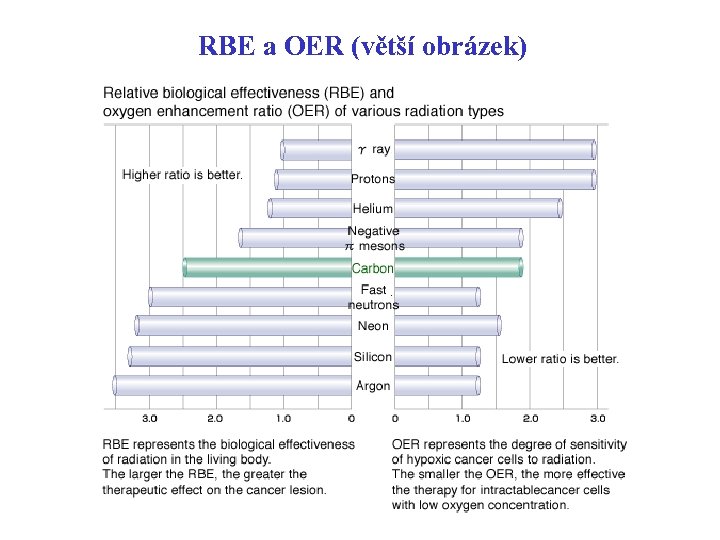
RBE a OER (větší obrázek)
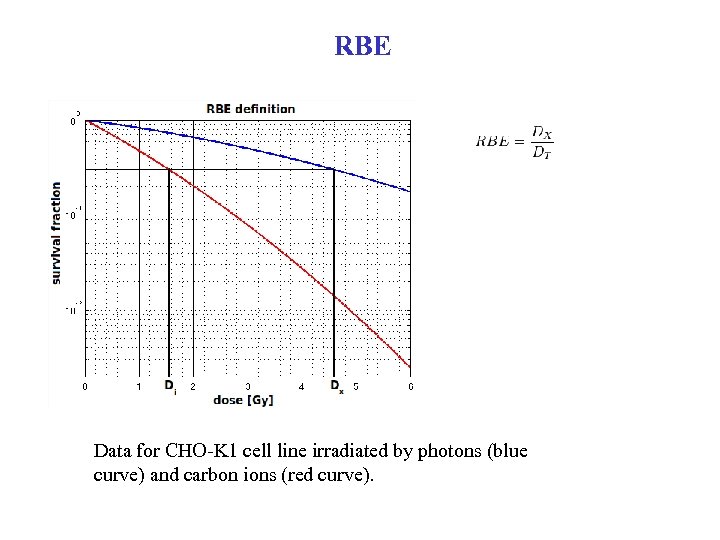
RBE Data for CHO-K 1 cell line irradiated by photons (blue curve) and carbon ions (red curve).
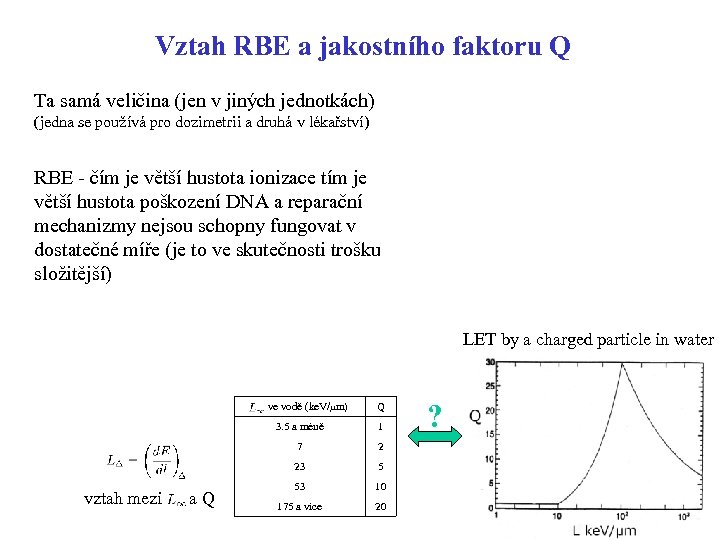
Vztah RBE a jakostního faktoru Q Ta samá veličina (jen v jiných jednotkách) (jedna se používá pro dozimetrii a druhá v lékařství) RBE - čím je větší hustota ionizace tím je větší hustota poškození DNA a reparační mechanizmy nejsou schopny fungovat v dostatečné míře (je to ve skutečnosti trošku složitější) LET by a charged particle in water ve vodě (ke. V/mm) 3. 5 a méně 1 7 2 23 vztah mezi a Q Q 5 53 10 175 a více 20 ?

OER Přítomnost molekulárního kyslíku silně ovlivňuje biologický efekt některých typů záření • kyslík musí být přítomen během expozice, nebo nejméně během života volných radikálů (10 -5 s) • kyslík fixuje (vytváří trvalé) poškození způsobené radikály - při absenci kyslíku mohou být tato poškození opravena (nemá vliv na přímé účinky záření) • už malé množství kyslíku má velký vliv - 0. 5% kyslíku způsobuje poloviční citlivost mezi hypoxickou oblastí a plně okysličenou tkání • v nádorech jsou místa s nedostatkem kyslíku - je to dáno nedostatečně prokrvenou tkání • OER (RTG) 3 při velkých dávkách a zřejmě méně ( 2) při dávce 0. 5 to 2 Gy OER klesá s rostoucími ionizačními ztrátami (LET) - roste vliv přímé interakce záření s DNA OER se přibližuje k jedničce (žádný efekt) pro LET 160 ke. V/mm OER pro n je 1. 6 • • •

Hadronová terapie • Most patients are treated by X-rays. World-wide there are 10, 000 linacs and 4 million patients a year treated. • Hadron therapy (Bragg peak) suggested by Bob Wilson in Radiology 47, 487 (1946) • Pioneered in Berkeley and Harvard.
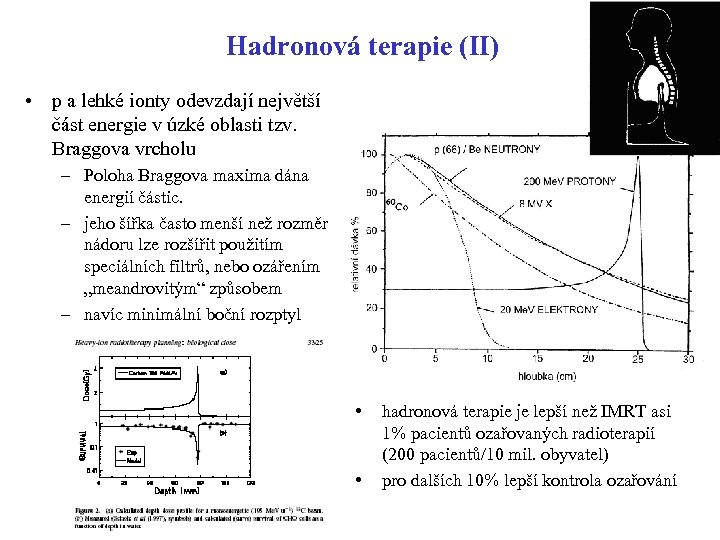
Hadronová terapie (II) • p a lehké ionty odevzdají největší část energie v úzké oblasti tzv. Braggova vrcholu – Poloha Braggova maxima dána energií částic. – jeho šířka často menší než rozměr nádoru lze rozšířit použitím speciálních filtrů, nebo ozářením „meandrovitým“ způsobem – navíc minimální boční rozptyl • • hadronová terapie je lepší než IMRT asi 1% pacientů ozařovaných radioterapií (200 pacientů/10 mil. obyvatel) pro dalších 10% lepší kontrola ozařování

Hadronová terapie (III) • pro doběh 25 cm: Ep = 200 Me. V, E 12 C = 4500 Me. V • největší výhoda lze použít v blízkosti citlivých orgánů • p a g interagují s DNA spíše nepřímo pomocí radikálů x pro 12 C už je důležitá i přímá interakce s DNA (větší LET) – C zanechá 23 x více energie než p se stejným doběhem • přímá interakce s DNA je významná pro LET > 20 ke. V/mm – C má tuto ionizaci na posledních 5 cm dráhy (He na posledním 1 mm) • čím větší ionizační ztráty, tím horší reparace DNA • lze sledovat ozáření pomocí PET (dopadající kladné ionty dávají vzniknout + radioaktivním jádrům)
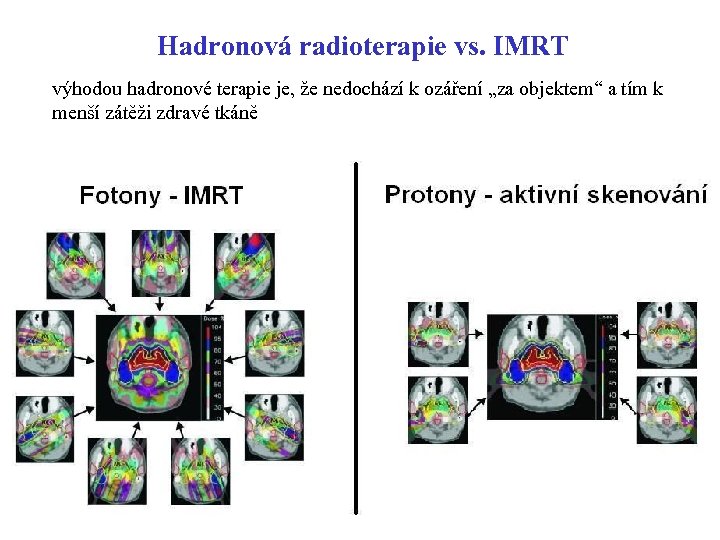
Hadronová radioterapie vs. IMRT výhodou hadronové terapie je, že nedochází k ozáření „za objektem“ a tím k menší zátěži zdravé tkáně

Hadronová terapie Svět • As of August 2013, there were 43 particle therapy facilities in the world, representing a total of 121 treatment rooms available to patients on a regular basis. • They are located in Canada, China, Czech Republic, France, Germany, Italy, Japan, South Korea, Poland, Russia, South Africa, Sweden, Switzerland, the UK and the US. • 28% of the proton therapy facilities are located in the US and 23% are located in Japan and more than 96, 537 patients had been treated ČR • Protonové centrum Na Bulovce (www. ptc. cz) je vybaveno špičkovou technologií belgické společnosti IBA (Ion Beam Application) • Pracoviště má k dispozici cyklotron (230 Me. V protony) a 5 ozařoven, tři z nich pracují s pohyblivým svazkem (tzv. gantry), jedna se svazkem pevným a jedna místnost je určena pro ozařování nádorů oka. • K dispozici je CT, NMR, PET/CT

Protonové centrum Praha (PTC) Protonové centrum Praha (www. ptc. cz) • • • Vlastníkem centra je společnost IMMORENT PTC, s. r. o. ze skupiny Erste Group Immorent Projekt za 4, 2 miliardy Kč financovala Erste Group Immorent, která do něj vstoupila poté, co se bratrům Laštovkovým v roce 2006 podařilo získat smlouvu o smlouvě budoucí s nuceným správcem VZP V dubnu 2006 uzavřel tehdejší nucený správce VZP Antonín Pečenka za pojišťovnu smlouvu o smlouvě budoucí, která VZP zavazuje po dobu 15 let hradit Protonovému centru léčbu 1650 jejích klientů ročně při ceně 26 tisíc Kč za jedno ozáření. Uvážíme-li, že každý pacient potřebuje průměrně 22– 25 ozáření, jedná se o kontrakt v celkové výši až 16 miliard Kč. Nucenou správu, která trvala od listopadu 2005 do května 2006, na VZP uvalil tehdejší ministr zdravotnictví David Rath a do funkce nuceného správce dosadil svého náměstka Pečenku, který měl prověřit a zlepšit hospodaření pojišťovny. Pečenka později v Protonovém centru několik let působil. Nakonec se však s majiteli centra rozešel a v roce 2012 založil konkurenční firmu Proton centrum Praha s. r. o. , jejímž cílem by mohlo být centrum převzít, když se k tomu naskytne příležitost. Ozařování protonem je (možná) šetrnější a působí méně následných komplikací než klasická radioterapie. Výrazně dražší „proton“ je však přínosný jen pro některé typy nádorů, část expertů varuje také před jeho nižší účinností. PTC nemá stále podepsánu smlouvu s VZP, s některými ostatními pojišťovnami ano … cena za ozařování (1 frakce je asi 25 -60 tis. Kč)

Použití 12 C • výhody použití 12 C – lepší kyslíkový poměr než u p – při ozařování lze snížit počet frakcí, do kterých je celková aplikovaná dávka rozdělena (20 -30 sezení pro g, pro 12 C stačí méně než 10) snižují se ekonomické náklady zvyšuje kapacita příslušného centra snižuje se celková léčebná náročnost z pohledu pacienta (menší celková aplikovaná dávka) • to give 12 Gy in a single stage (three entry points) and so treat a patient in simply one visit (as is done at HIMAC). This should be contrasted with X-rays where the dose delivered in one location, and in one visit, is only 1/3 Gy. • nevýhody 12 C – větší magnetická rigidita – vyšší cena
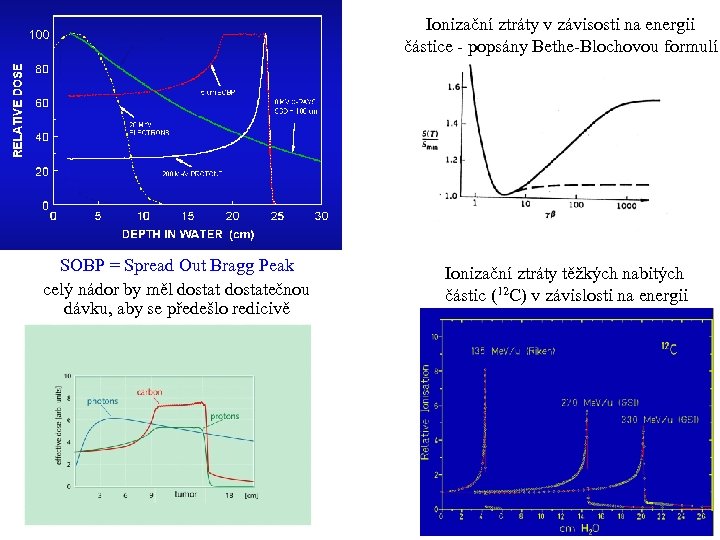
Ionizační ztráty v závisosti na energii částice - popsány Bethe-Blochovou formulí SOBP = Spread Out Bragg Peak celý nádor by měl dostatečnou dávku, aby se předešlo redicivě Ionizační ztráty těžkých nabitých částic (12 C) v závislosti na energii

Zařízení na hadronovou terapii - foto zařízení pro léčbu očních nádorů (Villigen - project OPTIS) více než 3000 pacientů
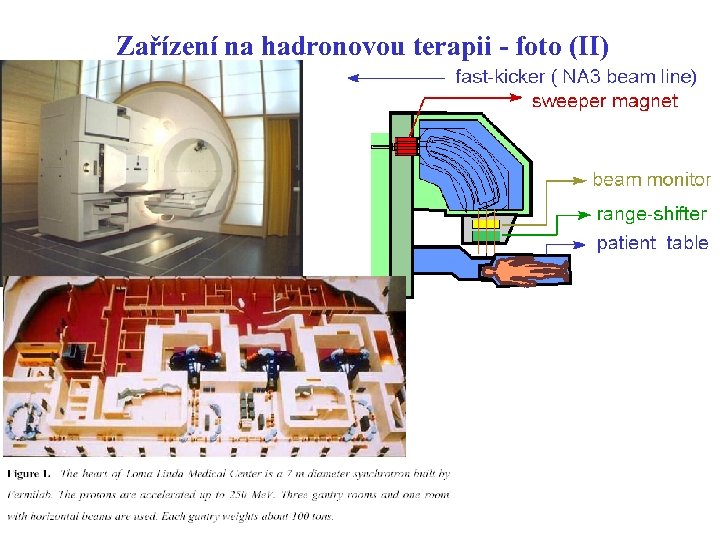
Zařízení na hadronovou terapii - foto (II) schéma gantry
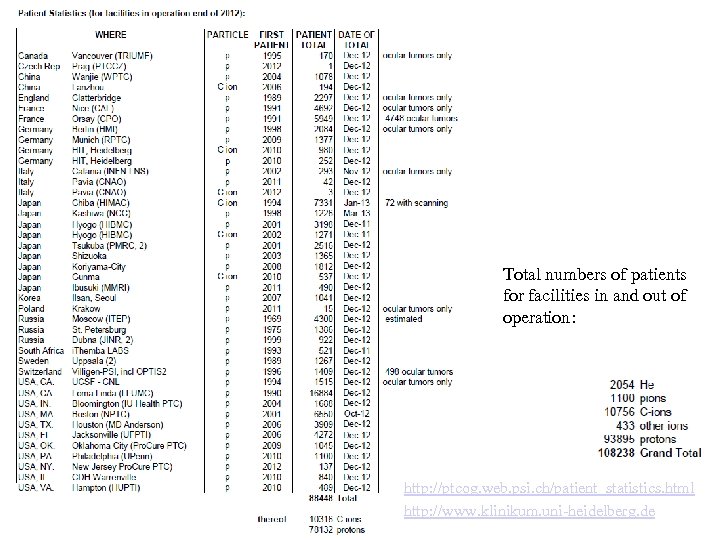
Total numbers of patients for facilities in and out of operation: http: //ptcog. web. psi. ch/patient_statistics. html http: //www. klinikum. uni-heidelberg. de
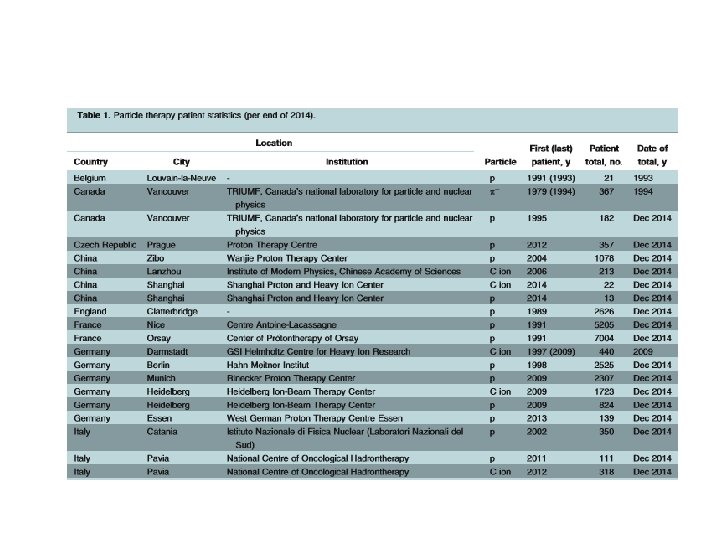

Radioterapie mezony p p- mají výrazné Braggovo maximum • • kromě obvyklého mechanismu jsou p--mezony na konci dráhy zachyceny v jádrech atomů (v tkáni např. v 12 C, 16 O, 14 N) při záchytu p- jádrem dojde k reakci s p (p- + p+ ® n + 140 Me. V) a uvolní se energie 140 Me. V (vyšší než BN) excitované jádro se rozštěpí zpravidla na a-částice, d, n a p (u těžších jader se mezi fragmenty vyskytují i 6 Li nebo 12 C) – např. u C dochází k reakci p- + 12 C ® 2 a + 3 n + p, přičemž částice a odnášejí kinetickou energii cca 30 Me. V a neutrony cca 70 Me. V (zbylých 40 Me. V se spotřebuje na překonání vazbové energie jádra). • • • zabrzděním těchto fragmentů se v daném místě předá značná ionizační energie p- vznikají při ostřelování jader terčíku (např. C, Be) p urychlenými na energie větší než asi 500 Me. V dosah p- o energiích 50 -100 Me. V v tkáni činí cca 10 -25 cm. • • zařízení v Los Alamos, Vancouveru, Villigenu - celkem asi 1200 pacientů nedosáhlo se lepších výsledků než u „konvenční terapie“ zastaveno

Cena Leksellův gamma nůž • pořizovací cena 3 -7 x 106 USD • cena vyšetření 7 500 - 9 500 USD (na jednoho pacienta) IMRT • pořizovací cena 3 -10 x 106 USD za Cyber. Knife (USA, Anglie, Indie) • cena vyšetření 10 000 -30 000 USD (na jednoho pacienta) Hadronová terapie • pořizovací cena 3 - 5 mld Kč (protony) – viz dříve • roční provoz 200 mil Kč jeden pacient je asi 500 000 Kč • u nás předpoklad 1200 pacientů/rok – realita asi o dost jiná • HIMAC (12 C) - pořizovací cena 350 mil. USD (10 mld. Kč) • A p facility costs $100 M to $200 M to construct, and costs of treatment range up to $100, 000 per patient, twice as much as contemporary radiation therapy, and up to four times as much as surgery, brachytherapy, and other options. (wikipedia) – comparison probably depends on the type of tumor

Cena • Na zdravotnictví ročně padne přes 200 miliard korun. • Právě o posouzení nákladů přitom především jde. Výdaje na zdravotnictví narostly od roku 1990 o 190 miliard korun, příjmy přitom budou v souvislosti se stárnutím populace spíše klesat. Podle propočtů Komerční banky má v roce 2025 na účtech zdravotních pojišťoven oproti nynějšku chybět 56 miliard korun. Nadstandard, který to měl řešit, se přitom nerozjel. • Stát musí stanovit, jakou cenu je za lidský život možné platit. Podobně to ostatně udělala už řada jiných států, a Světová zdravotnická organizace k tomu dokonce vydává i návod: medicínská technologie by výměnou za rok kvalitního života neměla stát více než trojnásobek HDP na hlavu příslušné země. To je v kontextu české ekonomiky něco přes milion korun.
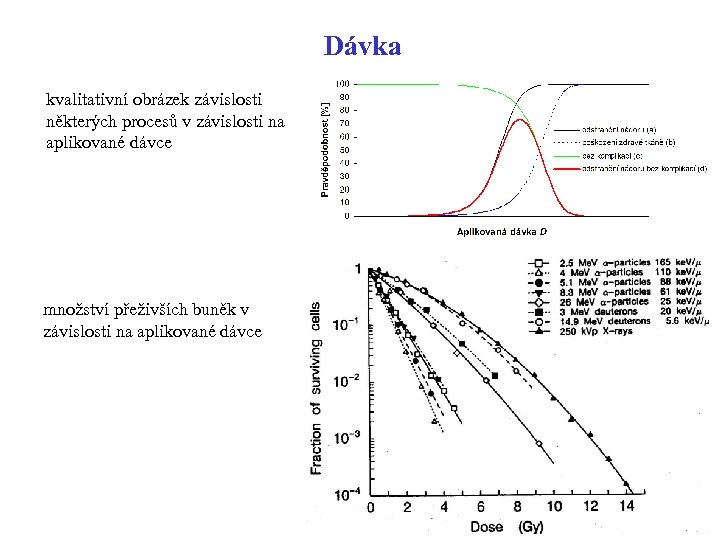
Dávka kvalitativní obrázek závislosti některých procesů v závislosti na aplikované dávce množství přeživších buněk v závislosti na aplikované dávce

Aplikace - dávka Celková dávka • For curative (radical) cases, the typical dose for a solid epithelial tumor ranges from 60 to 80 Gy, while lymphoma tumors are treated with 20 to 40 Gy. Preventative (adjuvant) doses are typically around 45 - 60 Gy in 1. 8 - 2 Gy fractions (for Breast, Head and Neck cancers respectively. ) Rozdělování dávky • • The total dose is fractionated (spread out over time) in order to give normal cells time to recover. In the USA and Europe, the typical fractionation schedule for adults is 1. 8 to 2 Gy per day, five days a week. (In the northern United Kingdom, fractions are more commonly 2. 67 to 2. 75 Gy per day, which eases the burden on thinly spread resources. ) For children, a typical fraction is 1. 5 to 1. 7 Gy per day, reducing the chance and severity of late-onset side effects.
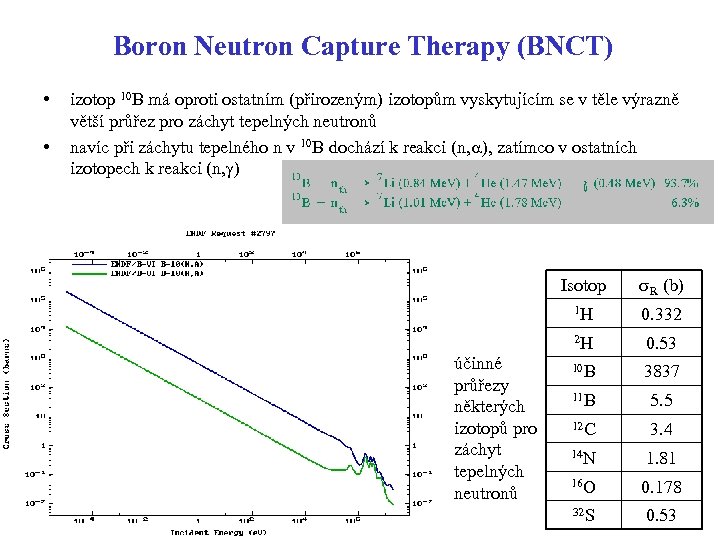
Boron Neutron Capture Therapy (BNCT) • • izotop 10 B má oproti ostatním (přirozeným) izotopům vyskytujícím se v těle výrazně větší průřez pro záchyt tepelných neutronů navíc při záchytu tepelného n v 10 B dochází k reakci (n, a), zatímco v ostatních izotopech k reakci (n, g) Isotop 1 H 0. 332 2 H účinné průřezy některých izotopů pro záchyt tepelných neutronů s. R (b) 0. 53 10 B 3837 11 B 5. 5 12 C 3. 4 14 N 1. 81 16 O 0. 178 32 S 0. 53
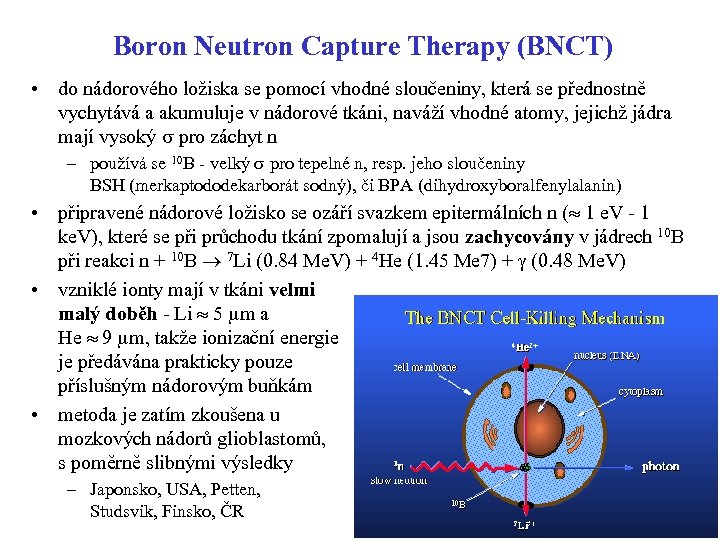
Boron Neutron Capture Therapy (BNCT) • do nádorového ložiska se pomocí vhodné sloučeniny, která se přednostně vychytává a akumuluje v nádorové tkáni, naváží vhodné atomy, jejichž jádra mají vysoký s pro záchyt n – používá se 10 B - velký s pro tepelné n, resp. jeho sloučeniny BSH (merkaptododekarborát sodný), či BPA (dihydroxyboralfenylalanin) • připravené nádorové ložisko se ozáří svazkem epitermálních n ( 1 e. V - 1 ke. V), které se při průchodu tkání zpomalují a jsou zachycovány v jádrech 10 B při reakci n + 10 B ® 7 Li (0. 84 Me. V) + 4 He (1. 45 Me 7) + g (0. 48 Me. V) • vzniklé ionty mají v tkáni velmi malý doběh - Li 5 mm a He 9 mm, takže ionizační energie je předávána prakticky pouze příslušným nádorovým buňkám • metoda je zatím zkoušena u mozkových nádorů glioblastomů, s poměrně slibnými výsledky – Japonsko, USA, Petten, Studsvik, Finsko, ČR
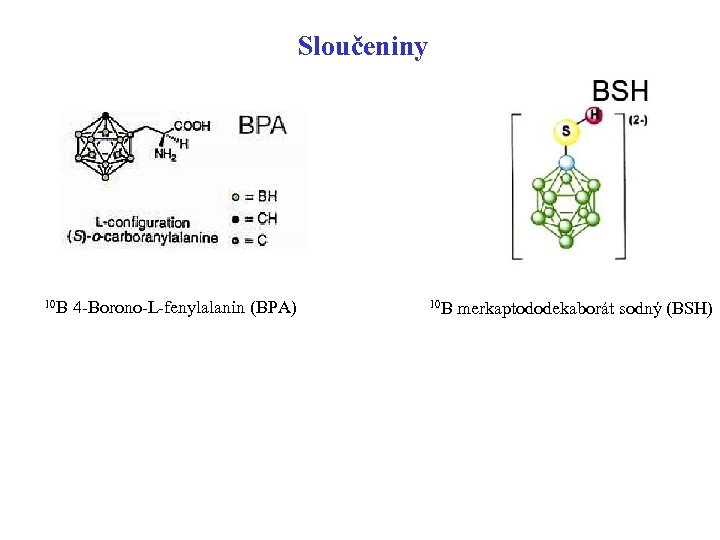
Sloučeniny 10 B 4 -Borono-L-fenylalanin (BPA) 10 B merkaptododekaborát sodný (BSH)
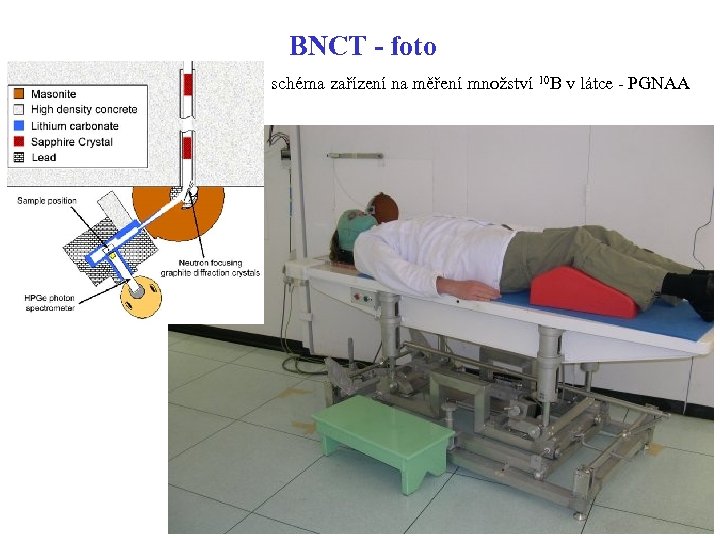
BNCT - foto schéma zařízení na měření množství 10 B v látce - PGNAA

Stav metody BNCT ve světě • zatím (s výjimkou Japonska) ve fázi klinických testů (Švédsko a Finsko - jsou po formální (legislativní) stránce dále) • Společný projekt EU (Petten) : asi 30 pacientů a Finsko: asi 50 pacientů – jediná pracoviště v provozu • Japonsko: asi 100 pacientů (pracoviště zavřena) • USA: asi 80 pacientů – byla 2 pracoviste MIT a BNL (obě uzavřena) • ČR - Řež ozařováno 5 pacientů (+ na 5 studována farmakokinetika) – všechno nádory na mozku (gliblastoma multiforme - nejmalignejší nádorové onemocnění s malou dobou prežití), u kterých nelze použít jiné metody • ve světě se zkoušela i pro nádory kůže – z fyzikalního hlediska jsou vhodnější pro tuto metodu než mozkové nádory – ale zde existují víceméně úspěšné alternativní možnosti • potřeba nových sloučenin • • Kromě B se uvažovalo i Gd – ozařování díky konverzním e. K dispozici jsou zřejmě „lepší“ sloučeniny než pro B; obrovský s pro záchyt
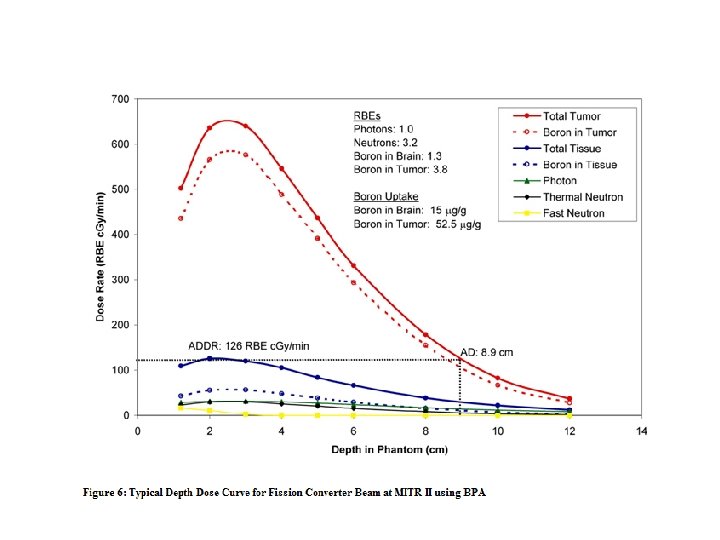

NCT s rychlými n • rychlé n s energií 20 -50 Me. V mohou být kolimovány přesně na terčík - dva možné způsoby využití – během zpomalování je 5 - 10 % rychlých n zpomaleno natolik, že mohou být zachyceny 10 B – pomocí „gantry“ lze provádět ozařování z různých stran a dosáhnou největší dávky v nádoru i bez „přidání“ B • vliv na zdravou tkáň? • • • rakovina prostaty a plic University of Washington Medical Center Karmanos Cancer Center/Wayne State University (KCC/WSU) in Detroit

Radioizotopová terapie • aplikujeme-li do organismu RA látku, vstoupí do metabolického procesu způsobem, který je dán chemickou formou látky - její farmakokinetikou; podaří-li se označit vhodným radionuklidem látku, která se selektivně vychytává a akumuluje v nádorové tkáni, můžeme dostat velmi efektivní způsob radiační likvidace tumoru "zevnitř". • pro většinu nádorových procesů bohužel takovou vhodnou látku zatím nemáme • významnou výjimkou je karcinom štítné žlázy - thyroidální nádorové buňky si zpravidla zachovávají schopnost vychytávat a akumulovat jód – aplikujeme-li tedy radioaktivní jód 131 I (perorálně ve formě jodidu sodného), vychytává se tento radionuklid v nádorových buňkách štítné žlázy (stejně jako neaktivní jód), a to i ve vzdálených metastázách. – záření beta 131 I (t 1/2 = 8 d), má v tkáni dolet 3 -4 mm, a likviduje nádorovou tkáň "zevnitř", a tedy selektivně, při minimální radiační zátěži okolních zdravých tkání – pro terapii karcinomu štítné žlázy se aplikuje aktivita cca 7 GBq radiojódu

Radioisotope therapy (RIT) • Not used very often nowadays but very progressive … future will show • Radioisotopes are given by mouth as a drink or capsules, or injected into a vein (intravenous injection). • Targeting can be due to the chemical properties of the isotope such as radioiodine which is specifically absorbed by the thyroid gland a thousandfold better than other bodily organs. Targeting can also be achieved by attaching the radioisotope to another molecule or antibody to guide it to the target tissue. • Examples are the infusion of metaiodobenzylguanidine (MIBG) to treat neuroblastoma, of oral 131 I to treat thyroid cancer or thyrotoxicosis, and of hormone-bound 177 Lu and 90 Y to treat neuroendocrine tumors (peptide receptor radionuclide therapy).

Radioisotope therapy (RIT) • Another example is the injection of 90 Y radioactive glass or resin microspheres into the hepatic artery to radioembolize liver tumors or liver metastases. These microspheres are used for the treatment approach known as selective internal radiation therapy. The microspheres are approximately 30 µm in diameter (about one-third of a human hair) and are delivered directly into the artery supplying blood to the tumors. These treatments begin by guiding a catheter up through the femoral artery in the leg, navigating to the desired target site and administering treatment. The blood feeding the tumor will carry the microspheres directly to the tumor enabling a more selective approach than traditional systemic chemotherapy. There are currently two different kinds of microspheres: SIRSpheres and Thera. Sphere.

177 Lu production: • • (1) leads to carrier added (c. a. ) 177 Lu and consequently to a lower product quality. In addition, the unwanted long-lived radionuclide 177 m. Lu is produced (T = 160. 1 d) with up to 0. 1% of ½ 177 Lu activity - this contaminant has to been the overall seen very critically. Due to the long half-life of the nuclide a continuing risk of its release into the environment exists. Furthermore, the user in the hospital faces the problem of safe-handling and radioactive waste management of the remaining quantities of 177 m. Lu. • More reasonable alternative seen from a medical and commercial approach is the production of 177 Lu via the indirect nuclear reaction (2). By irradiating highly enriched 176 Yb (> 99%) the short-lived radioisotope 177 Yb (T½ = 1. 9 h) is produced and decays to 177 Lu. In this case, Lu can be chemically isolated from Yb in its non carrier added form. • No 177 m. Lu is generated through the decay of 177 Yb. A drawback of this strategy is the mandatory radiochemical procedure to separate macro quantities of Yb from micro quantities of 177 Lu. As the desired radionuclide and the target nuclide represent two adjacent elements of the lanthanide series the separation poses a great challenge because of their high chemical similarity.

Lázně Jáchymov : -) • • Lázně Jáchymov jsou první radonové lázně na světě. I dnes mezi ostatními vynikají svým vysokým obsahem radonu ve vodě. Podle oficiálních údajů lázní je tato koncentrace dokonce největší na světe. Tím pádem je na veškeré ozdravné procedury pohybového ústrojí potřeba mnohem menší množství vody a kratší čas. Radonová voda blahodárně působí především na nemoci pohybového ústrojí, revmatické bolesti, Bechtěrevovu chorobu (tuhnutí páteře) a poúrazové stavy. Radon je ve zdejší vodě ve vysokém množství, skvěle proniká kůží a ozařuje klouby a všechna problematická místa, čímž startuje léčebné procesy. pramen výkon teplota vody obsah radonu akademika Běhounka 294 l /min 36, 8 °C 9 k. Bq /l C 1 30 l /min 30 °C 10 k. Bq /l Currie 30 l /min 28 °C 5 k. Bq /l Agricola 8 l /min 28 °C 20 k. Bq /l

Trocha historie radiační terapie • The concept of therapeutic radiation was invented by Wilhelm Conrad Rontgen when he discovered that the x-ray (discovered 1895) was a powerful and effective tool with which to treat cancer. • The field of radiation therapy began to grow in the early 1900 s largely due to the work of Marie Curie, who discovered the radioactive elements Po and Ra. This began a new era in medical treatment and research. Ra was used in various forms until the mid-1900 s when Co and Cs units came into use. • Medical linear accelerators have been developed since the late 1940 s. • With Godfrey Hounsfield’s discovery of computed tomography (CT), three-dimensional planning became a possibility and created a shift from 2 -D to 3 -D radiation delivery; CTbased planning allowed physicians to directly measure the dose delivered to the patient's anatomy based on axial tomographical images. • In the last few decades, the advent of new imaging technologies, e. g. , magnetic resonance imaging (MRI) in the 1970 s and PET in the 1980 s, as well as new radiation delivery and visualization products has moved radiation therapy from 3 -D conformal to IMRT and eventually to IGRT (4 -D) - Image-guided radiation therapy = the process of frequent imaging, during a course of radiation treatment - in the near future. These advances have resulted in better treatment outcomes and less side effects.

THE END

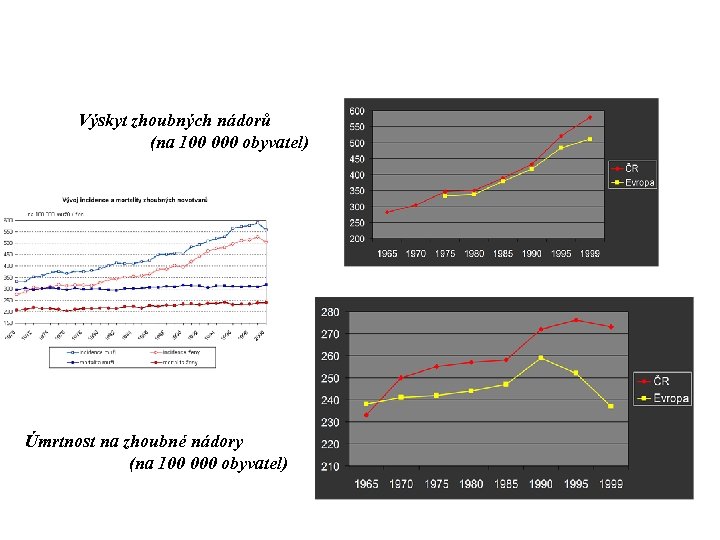
Výskyt zhoubných nádorů (na 100 000 obyvatel) Úmrtnost na zhoubné nádory (na 100 000 obyvatel)

• • Prices for Conventional, Natural, Alternative or Holistic Tumour / Tumor / Cancer Therapy / Treatment in Germany The following prices are presented to give you a clear and (almost) definite idea of the costs you would be facing if you decide to have an operation or other medical treatment done in Germany. They are based on the assumption that there will be no serious complications and that there are no serious risk factors involved (e. g. extreme obesity, underlying other diseases, very old age etc. ) that might create additional potentially costly challenges for the German doctors and hospitals. Prices do include our organisational fees, but they do not cover travel expenses, costs for hotels, costs for hiring translators etc. Please note that not all of our German partners will be able to offer these prices, which is why all price quotations should be regarded as "starting from". If you decide to go to one particular hospital, we will have to confirm for you if that prticulr hospital is able to perform the required procedure at the quoted price or if it might charge a slightly higher price. This price list is currently under preparation. Quotes will be available shortly. BRAIN TUMOUR SURGERY • Gamma Knife Surgery: 11500 EUR or USD (? 7360)

• Cost studies have shown that when compared to conventional neurosurgery, the Gamma Knife is much less expensive. It eliminates lengthy post-surgical hospital stays and expensive medication. In addition, there are virtually no post-surgical disability and convalescent costs with this procedure. • At present, IMRT is applied primarily to prostate, head and neck, breast, and esophageal cancers and to those brain tumors close to sensitive structures such as the eye. Its availability is expanding rapidly: whereas in 1998, only 4% of radiation oncology facilities provided IMRT, in 2003, 38% did. 15 Also, considerable work is being devoted to make IMRT usable in other cancers such as those in the lung and abdomen, where motion is a problem.
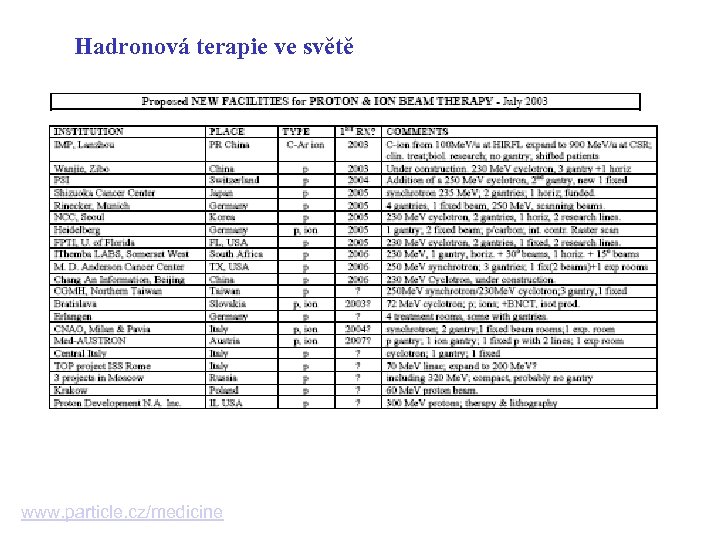
Hadronová terapie ve světě www. particle. cz/medicine
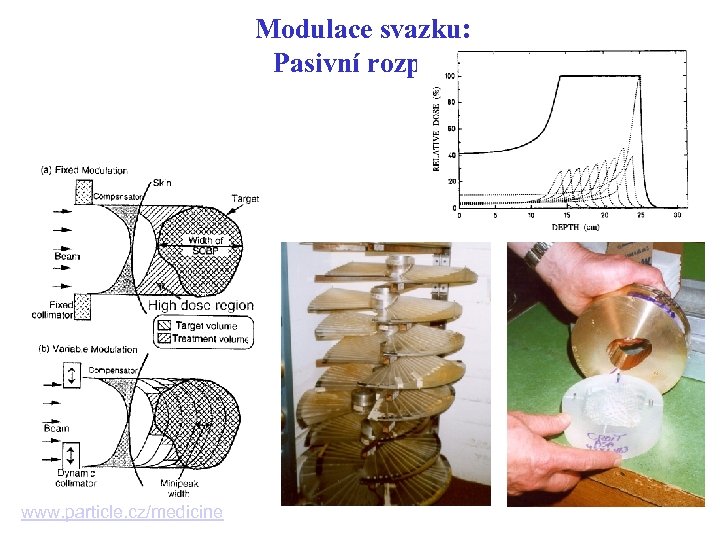
Modulace svazku: Pasivní rozptyl www. particle. cz/medicine
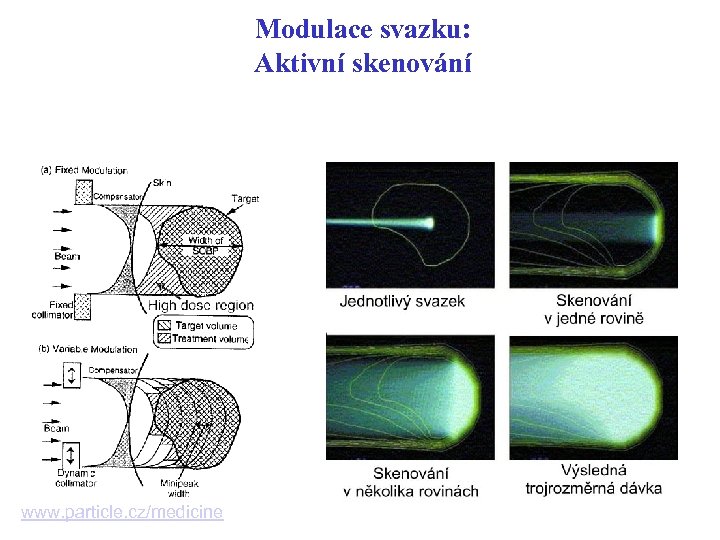
Modulace svazku: Aktivní skenování www. particle. cz/medicine

Technické požadavky • dosah ve tkáni – – – • • protony ionty 220 -250 Me. V až 400 Me. V/u posun Braggova maxima (1 -3 mm) → kroky změny energie (0, 5 -1 Me. V) velikost ozařovacího pole dávková rychlost → tok částic urychlovače – – • • 2 -3, 5 cm 2 -10 cm 2 -25 cm potřebná maximální energie – – • nádory očí oblast hlavy a krku uvnitř těla cyklotron (IBA, Accel) synchrotron (PIMMS, PRAMES, Optivus) gantry aktivní skenování www. particle. cz/medicine
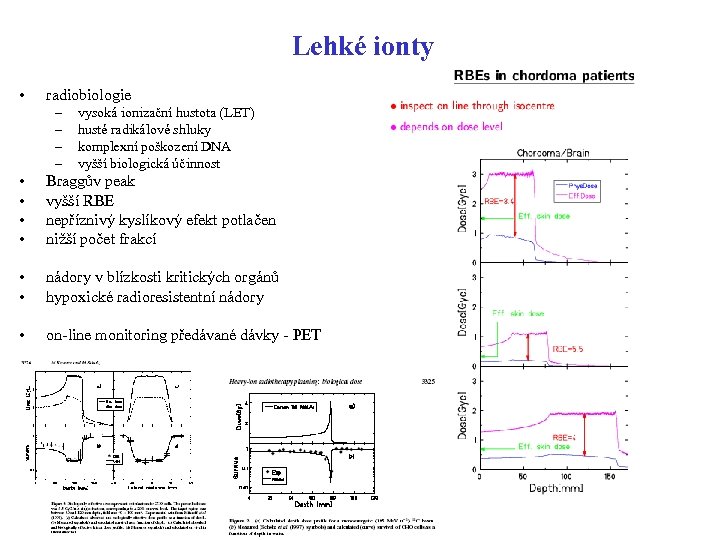
Lehké ionty • radiobiologie – – vysoká ionizační hustota (LET) husté radikálové shluky komplexní poškození DNA vyšší biologická účinnost • • Braggův peak vyšší RBE nepříznivý kyslíkový efekt potlačen nižší počet frakcí • • nádory v blízkosti kritických orgánů hypoxické radioresistentní nádory • on-line monitoring předávané dávky - PET

Aktivity v rámci ČR • interdisciplinární pracovní skupina „Využití ionizujících částic v lékařství a biologii“ – • neutronová záchytová terapie (BNCT) – • 1. LF UK, FZÚ, ÚJF AVČR, ÚJV klinické testy - ÚJV Řež , ÚJF AV ČR, Nemocnice Na Homolce, Onkologická klinika 1. LF UK a VFN hadronová radioterapie – – – výzkumné zprávy, studie PRAMES (1996 -2000) Onkologie 2000 – PIMMS (gantry) studie „Onkologické centrum s hadronovou radioterapií“, FZÚ AVČR, květen 2002 http: //weber. fzu. cz/projekty/medicine/studie. pdf od r. 2002 ENLIGHT

ENLIGHT http: //www. estro. be/estro/Index. html • • European Network for LIGht Ion Hadron Therapy (grant EC, 2002 -2005) využití iontových svazků v radioterapii – fyzikálně technické aspekty, indikace, výběr pacientů, ekonomické otázky – – – – European Society for Therapeutic Radiology and Oncology (ESTRO) European Organization for Nuclear Research (CERN) European Organisation for Research and Treatment of Cancer (EORTC) Gesellschaft für Schwerionenforschung Gmb. H, Darmstadt (GSI) German Cancer Research Center (DKFZ Heidelberg), German Heavy Ion Project (GHIP) Fondazione per Adroterapia Oncologica (TERA) Karolinska Institutet ETOILE Project, Université Claude Bernard Lyon 1 Med-Austron, Wien FZR - Project Forschungszentrum Rossendorf Linköping University Hospital Virgen de la Macarena Charles University Praha

Radiofarmaka UJV Řež produkuje Léčivý přípravek indikace 131 I Natrium Iodhipuricum diagnostika funkce ledvin 131 I jodid sodný roztok diagnostické aplikace štítné žlázy Chlorid thalný 201 Tl diagnostika poruch prokrvení srdce Gallium citricum 67 Ga lokalizace nádorů měkkých tkání (včetně Hodgkinovy choroby, zhoubných nádorů vaječníků, nádorů jater), 111 In chlorid inditý značení komplexotvorných látek, protilátek a buněčných složek krve 153 Sm paliativní léčba bolestivých kostních metastáz při nádorových onemocněních, především karcinomu prostaty, prsu, plic a jiných

Radioterapie (II) • • • Radioterapie je založena na schopnosti ionizujících částic inaktivovat (usmrtit) jednotlivé buňky. Buňkám (jejich jádrům) je při ozáření předána určitá energie, která vede k jejich poškození. Mnohá takto vzniklá poškození je buňka schopna opravit, některá však vedou k jejímu zničení. Pravděpodobnost buněčné inaktivace vzrůstá s energií předávanou jednotlivým buňkám. Pro různé druhy buněk může být tato pravděpodobnost značně rozdílná. Biologický účinek na buňku daného typu závisí kromě předané dávky ještě na dalších faktorech, z nichž za nejdůležitější lze označit tzv. lineární přenos energie (linear energy transfer - LET): inaktivační účinek na jednotlivé buňky je tím větší, čím více energie předávají částice ozařovacího svazku tkáni na jednotku délky své dráhy. Dalším důležitým faktorem je tzv. kyslíkový poměr: inaktivační účinek je nižší, pokud buňka obsahuje menší množství molekulárního kyslíku. Tento rozdíl se však postupně zmenšuje pro záření s vyšším lineárním přenosem energie. Aby bylo možné plně využít možností radioterapie a rozhodnout o její optimální aplikaci, je nutné znát všechny zákonitosti, které se při radiobiologickém mechanismu uplatňují. Týká se to jak účinku na jednotlivá buněčná jádra, tak i celkového účinku na příslušnou ozařovanou tkáň či organismus.

PSI The displacement of the spot position in the body is always performed with the beam switched off. For the fastest varying spot motion we use a deflecting magnet (the sweeper magnet ). The motion along the second axis of scanning is realized with a range shifter system , which scans the dose spot in depth. The third direction is covered by the motion of the patient table itself, which is the slowest and the least frequently used motion. The beam is a parallel beam with about 7 mm FWHM (full width at half maximum) and is scanned in an orthogonal matrix in steps of 4 or 5 mm. For a one litre target volume typically 10'000 spots are deposited in less than 5 minutes. Proton radiotherapy of ocular tumors The OPTIS project The first proton therapy facility in Western Europe Over 3000 patients treated
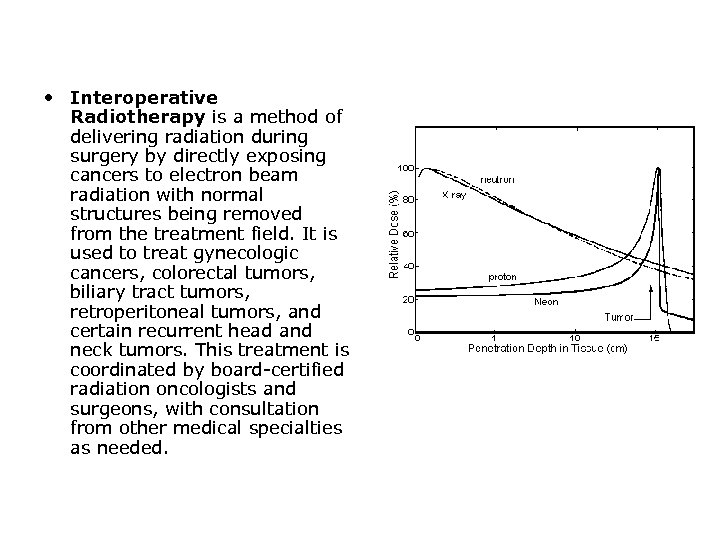
• Interoperative Radiotherapy is a method of delivering radiation during surgery by directly exposing cancers to electron beam radiation with normal structures being removed from the treatment field. It is used to treat gynecologic cancers, colorectal tumors, biliary tract tumors, retroperitoneal tumors, and certain recurrent head and neck tumors. This treatment is coordinated by board-certified radiation oncologists and surgeons, with consultation from other medical specialties as needed.

Protecting the Embryo/Fetus • The only way to protect the embryo/fetus from excess radiation is to protect the mother • “Belly” badge for the baby is issued • Bioassay for radioactive material intake is initiated and repeated monthly • Dose to baby is measured/ estimated and reported • Historically, pregnant women were not allowed to work with radiation • Loss of position and Loss of pay • To protect her baby, a mother must voluntarily, in writing, declare herself pregnant • Present to Principal User/Supervisor and to the Radiation Control Office • Additional information is available through the Radiation Control Office • Confidential discussions with RSO about radiation risks to embryo/fetus • Even if just planning to get pregnant • Arrangements may be made to discuss with female radiation health professional
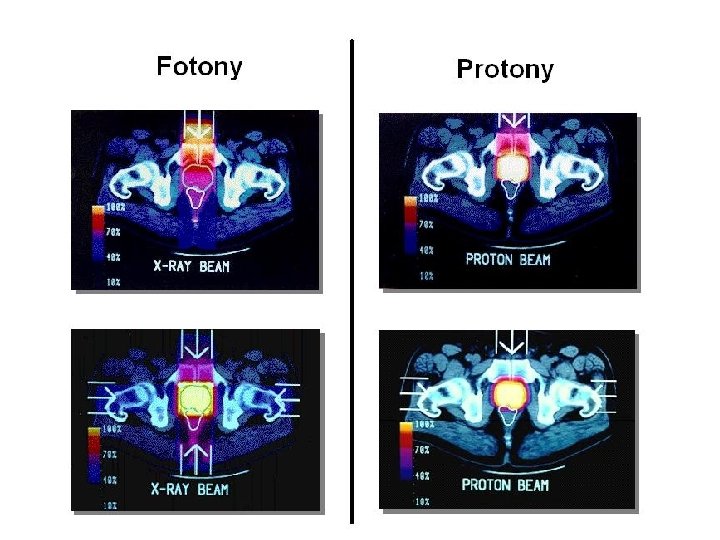

Relative Biological Effectiveness (RBE) ) ( Biological effect of radiation Y at dose X Biological effect of 250 k. Vp x-rays at dose X Both produce the same biological effect. Quality factor (Q) radiation photon, proton, neutron alpha Q 1 10 20
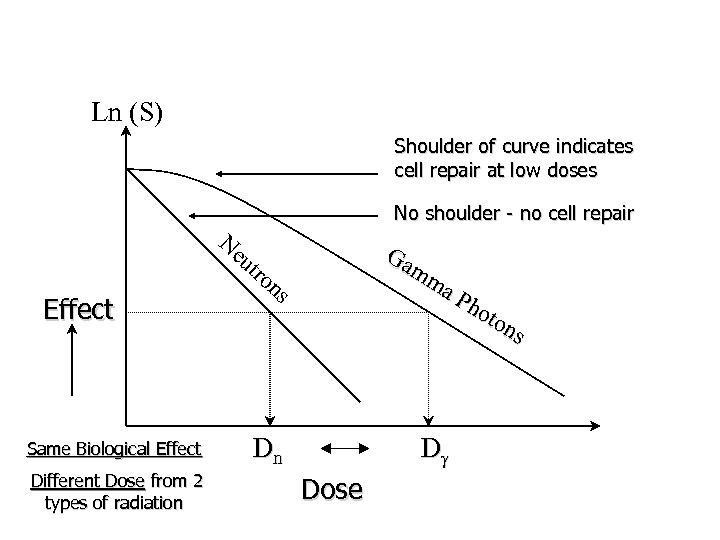
Ln (S) Shoulder of curve indicates cell repair at low doses Ne No shoulder - no cell repair ut Effect Same Biological Effect Different Dose from 2 types of radiation Ga mm a P ho ton s ro ns Dn Dg Dose
Occupational Dose to the Lens of the Eye Dose must not exceed 15 rem/ yr
Occupational Dose Limit for Declared Pregnant Mothers and Occupational Minors Dose must not exceed 0. 5 rem or 500 mrem during the gestation period for declared pregnant mothers. Occupational minors must not exceed this dose in a year long period
Radiation Effects for Embryo Declaration of Pregnancy for Occupational Mothers • Rapidly dividing and non-specialized cells are more sensitive to radiation • Birth defects have been observed • Dose limit to embryo / fetus is 500 mrem for the gestation period
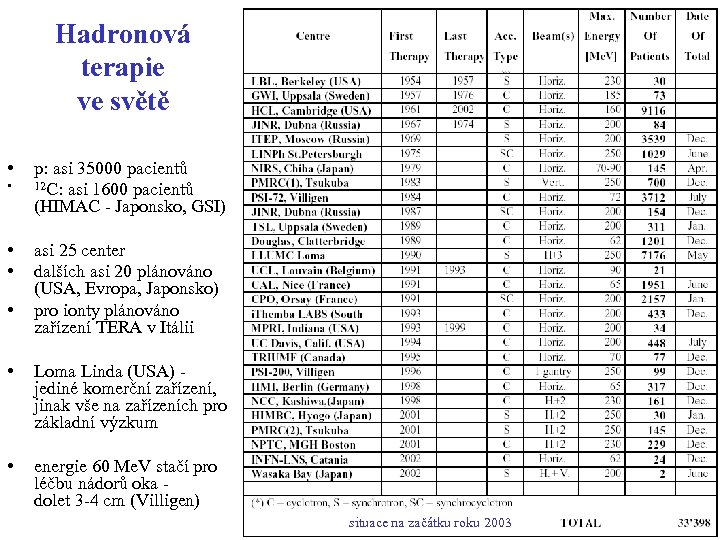
Hadronová terapie ve světě • • • p: asi 35000 pacientů 12 C: asi 1600 pacientů (HIMAC - Japonsko, GSI) asi 25 center dalších asi 20 plánováno (USA, Evropa, Japonsko) pro ionty plánováno zařízení TERA v Itálii • Loma Linda (USA) - jediné komerční zařízení, jinak vše na zařízeních pro základní výzkum • energie 60 Me. V stačí pro léčbu nádorů oka - dolet 3 -4 cm (Villigen) situace na začátku roku 2003

Fungující zařízení • Na počátku roku 2008 fungovalo asi 30 zařízení • As of June 2012, there were a total of 41 proton therapy centers in Canada, China, England, France, Germany, Italy, Japan, Korea, Poland, Russia, South Africa, Sweden, Switzerland, and USA and more than 83, 667 patients had been treated. [

Loma Linda
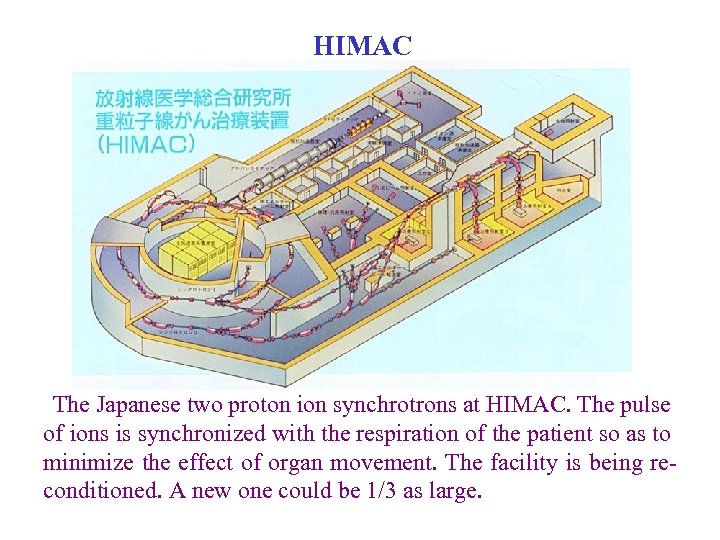
HIMAC The Japanese two proton ion synchrotrons at HIMAC. The pulse of ions is synchronized with the respiration of the patient so as to minimize the effect of organ movement. The facility is being reconditioned. A new one could be 1/3 as large.
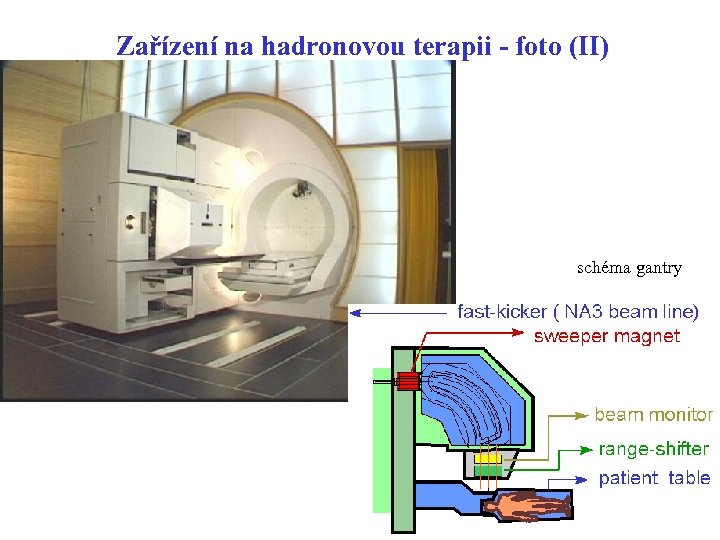
Zařízení na hadronovou terapii - foto (II) schéma gantry

• • • • In summary (spring 2008): Present facilities (roughly): Sub-atomic physics labs doing some therapy: 12 Hospital based proton therapy centers: 10 Under construction: 14 Patients treated: To date about 50, 000 patients have been treated with hadrons. (mostly with protons) At HIMAC 3, 000 patients treated with carbon beams At GSI 300 patients treated with ions
a3403d874edbd951703aca6e61a89ffe.ppt