Зависимость скорости реакции от температуры.pptx
- Количество слайдов: 21

Зависимость скорости реакции от температуры правило Вант-Гоффа γ – температурный коэффициент скорости реакции

Теория активных соударений • -столкновение частиц • - достаточный запас энергии • - определенная ориентация частиц

Число столкновений Z=f T) (e

достаточный запас энергии минимальная избыточная энергия, по сравнению со средней энергией частиц, необходимая для протекания реакции, называется энергия активации (обозначается Еа; выражается в к. Дж/моль).
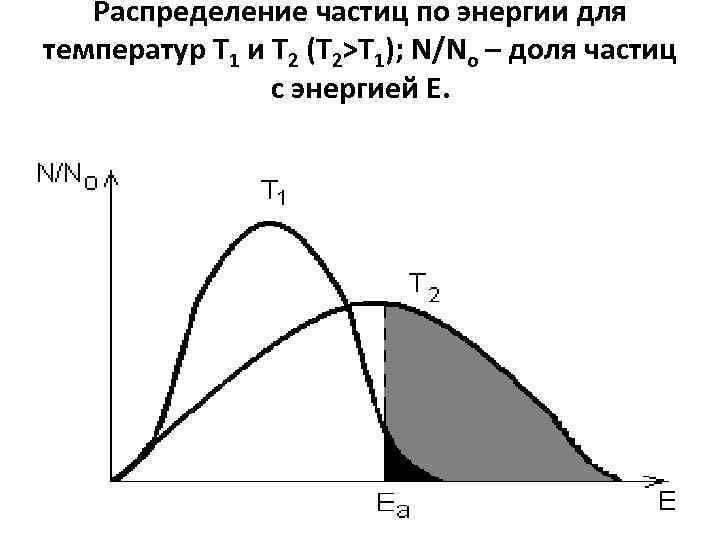
Распределение частиц по энергии для температур Т 1 и Т 2 (Т 2>T 1); N/No – доля частиц с энергией Е.
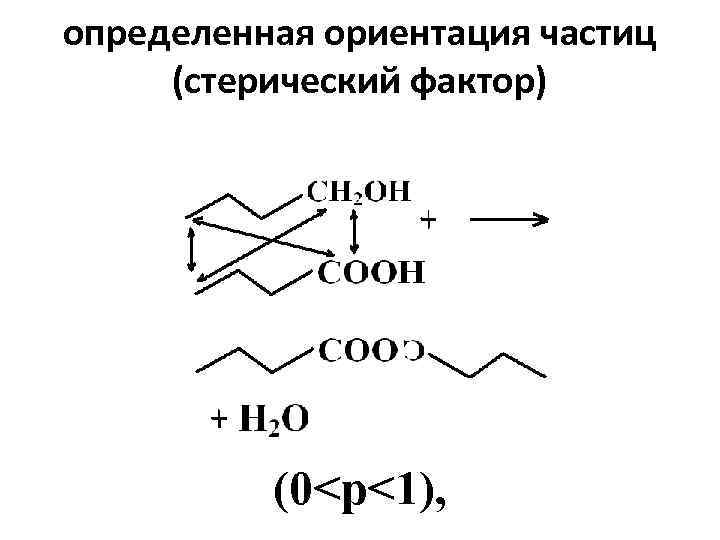
определенная ориентация частиц (стерический фактор) (0<p<1),

уравнение Аррениуса А – предэкспоненциальный множитель, A = p·Z; p – стерический фактор, показывающий вероятность столкновений в направлении, которое благоприятно для перераспределения связей, особенно этот фактор важен для больших разветвленных молекул органической природы (0<p<1), в остальных случаях р→ 1; Z – частотный фактор, пропорциональный общему числу соударений

уравнение Аррениуса для двух температур:

Расчет энергии активации
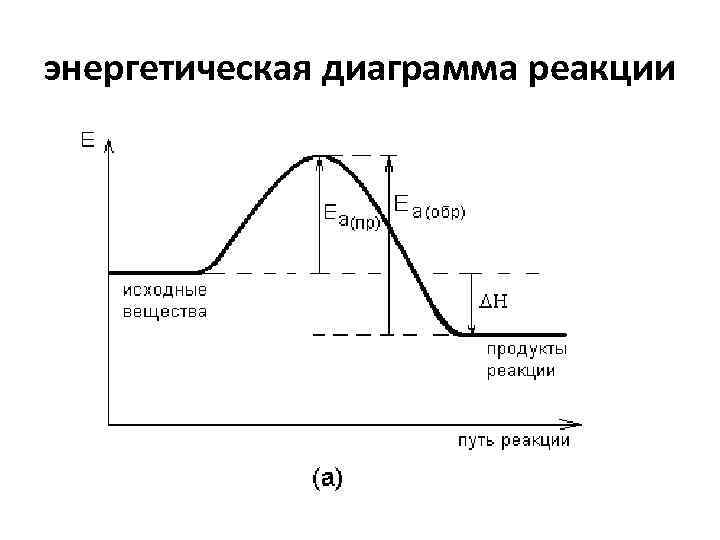
энергетическая диаграмма реакции

Катализ • Катализ – это явление изменения скорости реакции в присутствии веществ, не расходующихся в процессе взаимодействия (катализаторов). • В зависимости от фазового состояния реагирующих веществ и катализатора различают два вида катализа – гомогенный и гетерогенный.

• любая каталитическая реакция является реакцией сложной; • катализатор изменяет механизм процесса (иногда и порядок реакции), то есть в присутствии катализатора реакция проходит через другие промежуточные стадии, энергетически более выгодные; • катализатор, снижая энергию активации реакции, увеличивает скорость как прямой реакции, так и обратной; • катализатор не смещает положения равновесия реакции, а лишь уменьшает время достижения системой состояния равновесия; • катализатор не изменяет термодинамические характеристики процесса и ускоряет только термодинамически возможные реакции.
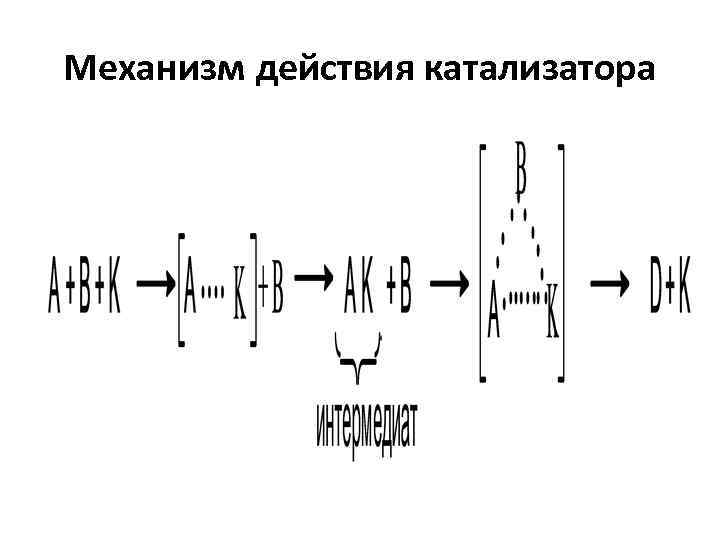
Механизм действия катализатора
![Энергетическая диаграмма процесса без катализатора (1) и с катализатором (2) Е [А…В] в Еа Энергетическая диаграмма процесса без катализатора (1) и с катализатором (2) Е [А…В] в Еа](https://present5.com/presentation/1/171332170_134388328.pdf-img/171332170_134388328.pdf-14.jpg)
Энергетическая диаграмма процесса без катализатора (1) и с катализатором (2) Е [А…В] в Еа А…К Еа 2 [А. . К]+В А+В+К Еа 1 Н АК+В С С+К КООРДИНАТА РЕАКЦИИ

Ферментативный катализ • Ферменты – сложные органические вещества белковой природы – значительно отличаются от неорганических катализаторов высокой активностью и специфичностью действия.

механизм ферментного катализа ES, фермент-субстратный комплекс
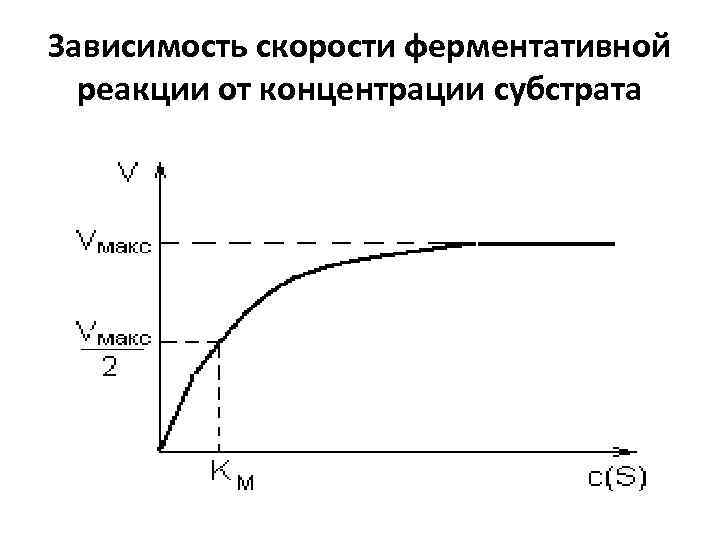
Зависимость скорости ферментативной реакции от концентрации субстрата

уравнение Михаэлиса — Ментен
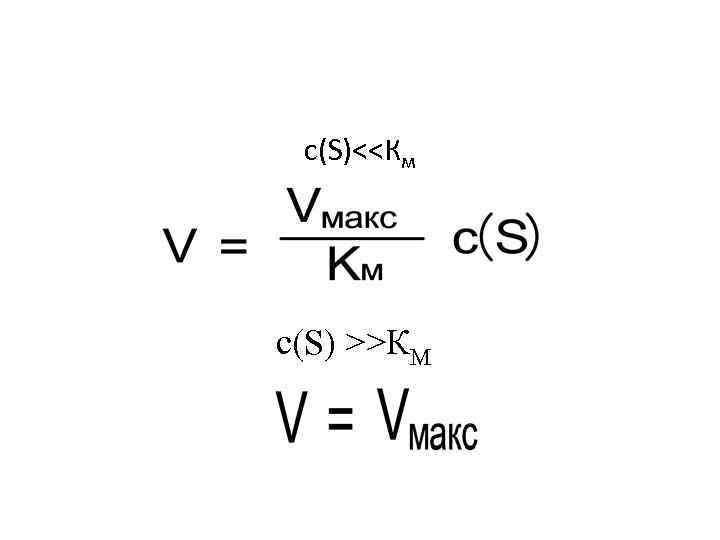
с(S)<<Км с(S) >>КМ

Влияние различных факторов на скорость ферментативных реакций • • • 1 – температура 2 – р. Н среды 3 – наличие ингибиторов (ионов и лигандов токсикантов) 4 – концентрация продукта катализа

Механизм обратного действия
Зависимость скорости реакции от температуры.pptx