През. адсорбция.ppt
- Количество слайдов: 9
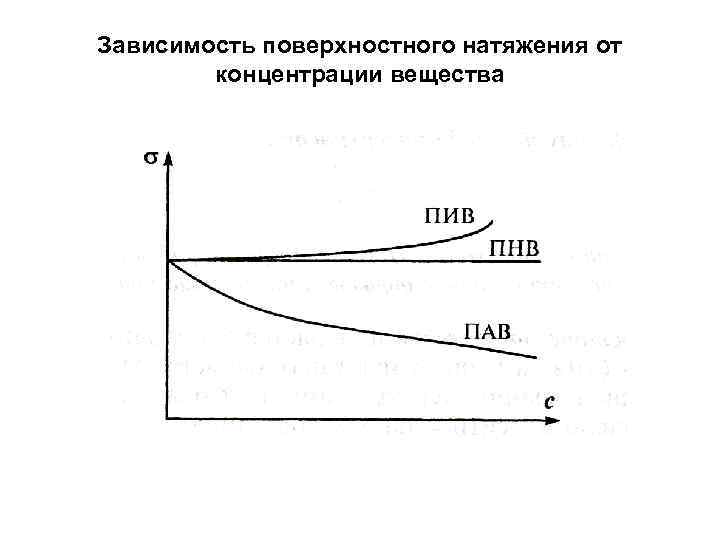
Зависимость поверхностного натяжения от концентрации вещества
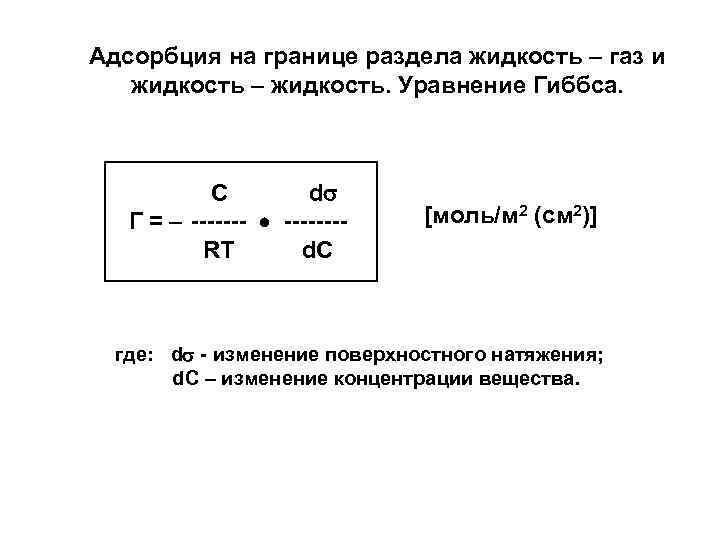
Адсорбция на границе раздела жидкость – газ и жидкость – жидкость. Уравнение Гиббса. С d Г = -------RT d. C [моль/м 2 (см 2)] где: d - изменение поверхностного натяжения; d. С – изменение концентрации вещества.

Анализ уравнения Гиббса. Из изотермы адсорбции Гиббса следует, что в зависимости от знака d / d. C направление процесса адсорбции может быть различным. Возможны три случая: d 1) ------- < 0, d. C d 2) ------- > 0, d. C d 3) ------- = 0, d. C тогда Г – положительная, происходит концентрирование компонента в поверхностном слое, так ведут себя ПАВ. тогда Г – отрицательная или десорбция, происходит уменьшение концентрации растворенного вещества в поверхностном слое, это характерно для ПНАВ. тогда Г = 0, адсорбция не идет.
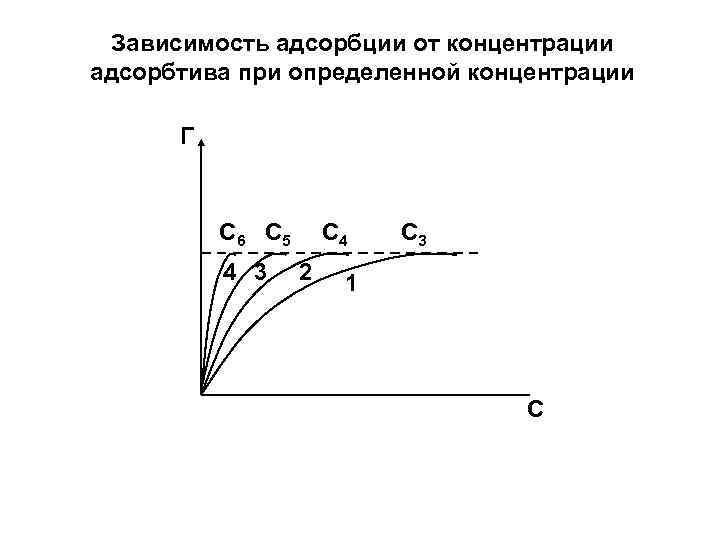
Зависимость адсорбции от концентрации адсорбтива при определенной концентрации Г С 6 С 5 4 3 С 4 2 С 3 1 С

Дифильные молекулы ПАВ определенным образом ориентируются на поверхности раздела вода – воздух. а) б) О О О при малых концентрациях ПАВ соблюдается правило Дюкло-Траубе. О при повышении концентрации ПАВ наблюдается переход отдельных молекул в «стоячее» положение. | | | | в) ООООООО при последующем повышении концентрации ПАВ в поверхностном слое приводит к образованию насыщенного слоя, т. н. частоколу Ленгмюра. ОООО ОО ОО О полярная группа О углеводородный радикал

Адсорбция на границе раздела твердое тело – газ и твердое тело – жидкость Уравнение Фрейндлиха Г = Кр1/n Г = КС 1/n жидкостей - для адсорбции газа - для адсорбции Г – адсорбция (ммоль/г) р – равновесное давление газа над адсорбентом С – равновесная концентрация жидкости над адсорбентом К, n = const, определяются экспериментально из логарифмического уравнения Фрейндлиха: lg Г = lg K + 1/n lg C (p)

Уравнение Ленгмюра Р Г = Г -------К+Р С Г = Г -------К+С адсорбтив - газ адсорбтив - жидкость Г – адсорбция Г - предельная адсорбция, которая соответствует полному заполнению поверхности адсорбента С – равновесная концентрация адсорбтива Р – равновесное давление адсорбтива К – const эмпирическая
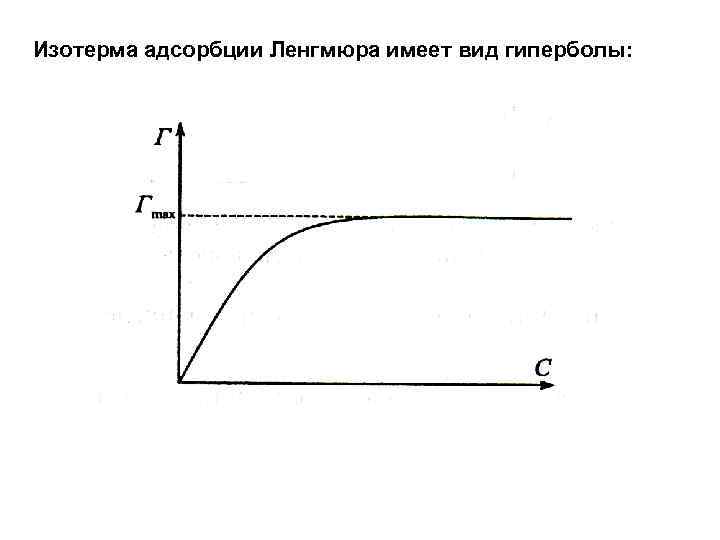
Изотерма адсорбции Ленгмюра имеет вид гиперболы:

Анализ изотермы адсорбции Ленгмюра 1) Если С адсорбтива мала, то количество адсорбируемого вещества прямо пропорционально его С: С Г = Г ------К 2) Если С большая, то адсорбируется предельно возможное количество вещества: Г = Г
През. адсорбция.ppt