алкены профиль.ppt
- Количество слайдов: 40
 Завершите начатые фразы: Непредельные углеводороды – это углеводороды, . . которые имеют в углеродной цепи кратные связи (двойные, тройные). Алкены – это непредельные углеводороды … содержащие в молекуле, помимо одинарных связей, одну двойную связь между атомами углерода и отвечают формуле H 2 n. n. С
Завершите начатые фразы: Непредельные углеводороды – это углеводороды, . . которые имеют в углеродной цепи кратные связи (двойные, тройные). Алкены – это непредельные углеводороды … содержащие в молекуле, помимо одинарных связей, одну двойную связь между атомами углерода и отвечают формуле H 2 n. n. С
 Простейший алкен –. . . этен (этилен). Молекулярная формула этилена. . . С 2 H 4 Структурная формула этилена. . . СН 2= СН 2 Электронное строение молекулы этилена обусловлено. . . гибридизацией атомов углерода.
Простейший алкен –. . . этен (этилен). Молекулярная формула этилена. . . С 2 H 4 Структурная формула этилена. . . СН 2= СН 2 Электронное строение молекулы этилена обусловлено. . . гибридизацией атомов углерода.
 Особенности строения алканов Атомы углерода при двойной связи находятся в sp 2 -гибридном состоянии и между ними образуется двойная связь, состоящая из π-связи и σ-связи. Длина двойной связи – 0, 134 нм. Все валентные углы близки к 120º.
Особенности строения алканов Атомы углерода при двойной связи находятся в sp 2 -гибридном состоянии и между ними образуется двойная связь, состоящая из π-связи и σ-связи. Длина двойной связи – 0, 134 нм. Все валентные углы близки к 120º.
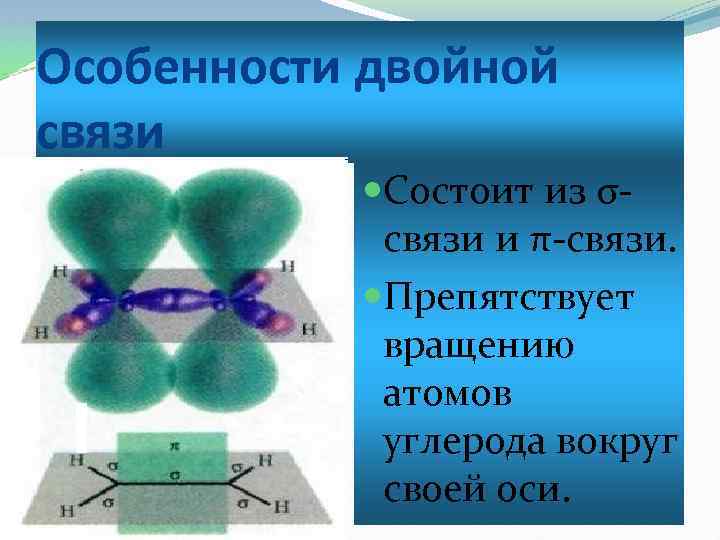 Особенности двойной связи Состоит из σсвязи и π-связи. Препятствует вращению атомов углерода вокруг своей оси.
Особенности двойной связи Состоит из σсвязи и π-связи. Препятствует вращению атомов углерода вокруг своей оси.
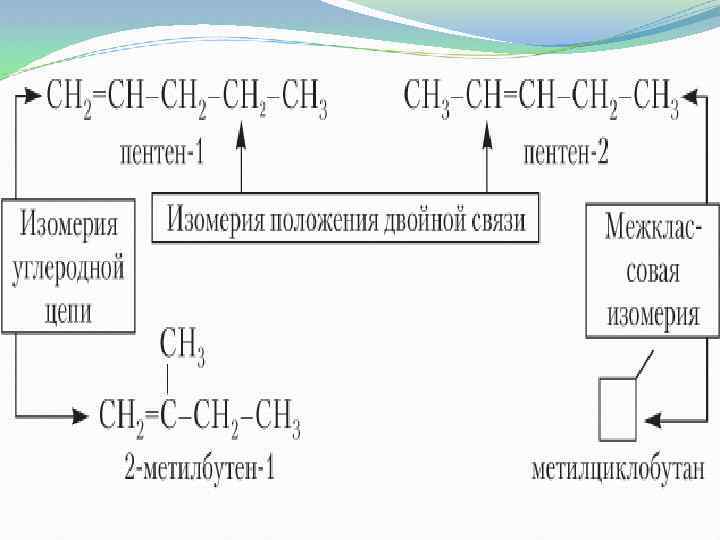
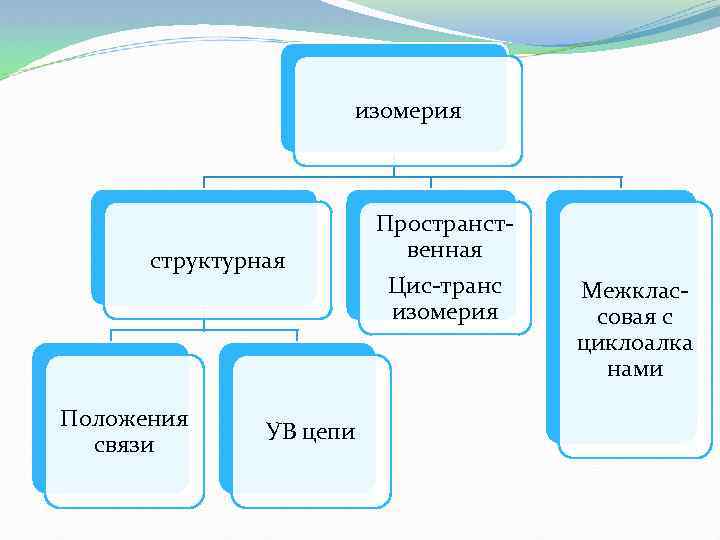 изомерия структурная Положения связи УВ цепи Пространственная Цис-транс изомерия Межклассовая с циклоалка нами
изомерия структурная Положения связи УВ цепи Пространственная Цис-транс изомерия Межклассовая с циклоалка нами
 Ациклические углеводороды, в молекулах которых содержится одна двойная связь, называются А) алканы Б) алкены В) алкины Г) арены. 2. Для алкенов характерна изомерия А) углеродного Б) положения скелета кратной связи В) пространственная Г) все ответы верны. 1.
Ациклические углеводороды, в молекулах которых содержится одна двойная связь, называются А) алканы Б) алкены В) алкины Г) арены. 2. Для алкенов характерна изомерия А) углеродного Б) положения скелета кратной связи В) пространственная Г) все ответы верны. 1.
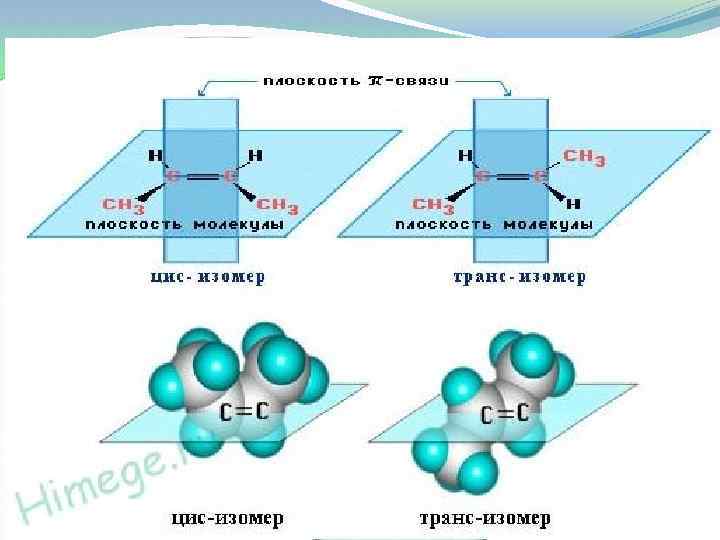
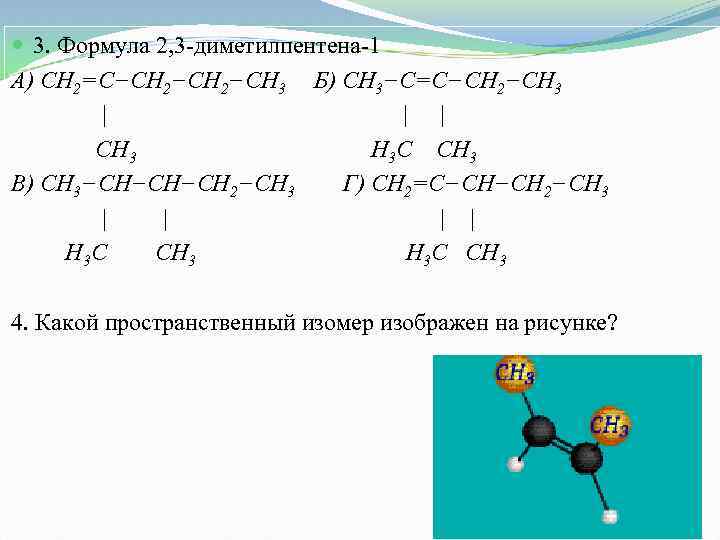 3. Формула 2, 3 -диметилпентена-1 А) СН 2=С−СН 2−СН 3 Б) СН 3−С=С−СН 2−СН 3 | | | СН 3 Н 3 С СН 3 В) СН 3−СН−СН−СН 2−СН 3 Г) СН 2=С−СН−СН 2−СН 3 | | Н 3 С СН 3 4. Какой пространственный изомер изображен на рисунке?
3. Формула 2, 3 -диметилпентена-1 А) СН 2=С−СН 2−СН 3 Б) СН 3−С=С−СН 2−СН 3 | | | СН 3 Н 3 С СН 3 В) СН 3−СН−СН−СН 2−СН 3 Г) СН 2=С−СН−СН 2−СН 3 | | Н 3 С СН 3 4. Какой пространственный изомер изображен на рисунке?
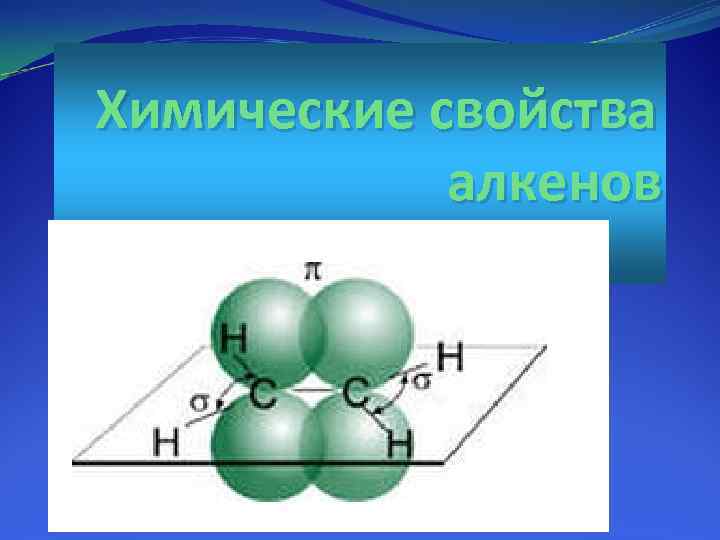 Химические свойства алкенов
Химические свойства алкенов
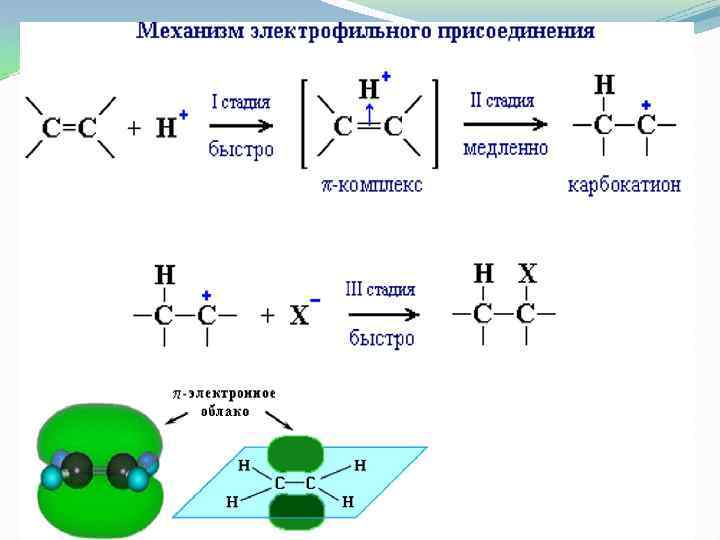
 Химические свойства Алкены вступают в реакции присоединени которые протекают я, по месту разрыванепрочной связи. Для алкенов характерны реакции электрофильного присоединения (АЕ). Механизм ионный.
Химические свойства Алкены вступают в реакции присоединени которые протекают я, по месту разрыванепрочной связи. Для алкенов характерны реакции электрофильного присоединения (АЕ). Механизм ионный.
 Реакции присоединения Гидрирование (+ Н ) 2 Галогенирование (+ Г) 2 Гидрогалогенирование (+НГ) Гидратация (+ Н О) 2
Реакции присоединения Гидрирование (+ Н ) 2 Галогенирование (+ Г) 2 Гидрогалогенирование (+НГ) Гидратация (+ Н О) 2
 Качественная реакция на связь Качественная реакция на -связь это обесцвечивание бромной воды.
Качественная реакция на связь Качественная реакция на -связь это обесцвечивание бромной воды.

 Гидрогалогенирование Гидратация Реакции гидрогалогенирования и гидратации несимметричных гомологов этилена идут легче по сравнению с этиленом и проходят в соответствии с правилом Марковникова.
Гидрогалогенирование Гидратация Реакции гидрогалогенирования и гидратации несимметричных гомологов этилена идут легче по сравнению с этиленом и проходят в соответствии с правилом Марковникова.
 Правило В. В. Марковникова При присоединении НГ или Н 2 О к несимметричному алкену водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген или (ОН ) к менее гидрированному атому углерода.
Правило В. В. Марковникова При присоединении НГ или Н 2 О к несимметричному алкену водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген или (ОН ) к менее гидрированному атому углерода.
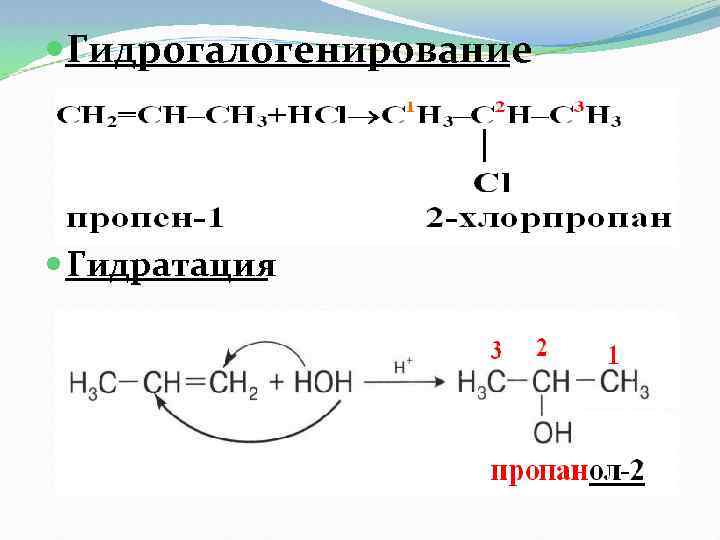 Гидрогалогенирование Гидратация
Гидрогалогенирование Гидратация
 Реакции окисления Полное окисление горение. Неполное окисление взаимодействие с окислителями : KMn. O 4 фиолетовый раствор
Реакции окисления Полное окисление горение. Неполное окисление взаимодействие с окислителями : KMn. O 4 фиолетовый раствор
 Горение красноватым светящимся Этилен горит пламенем, в то время как пламя предельных углеводородов голубое; это происходит потому, что массовая доля углерода в алкенах выше, чем в алканах с тем же числом атомов углерода.
Горение красноватым светящимся Этилен горит пламенем, в то время как пламя предельных углеводородов голубое; это происходит потому, что массовая доля углерода в алкенах выше, чем в алканах с тем же числом атомов углерода.

 Мягкое окисление Качественная реакция на связь обесцвечивание фиолетового раствора перманганата калия. этиленгликоль (этандиол-1, 2)
Мягкое окисление Качественная реакция на связь обесцвечивание фиолетового раствора перманганата калия. этиленгликоль (этандиол-1, 2)

 Полимеризация (особый тип реакций присоединения , в которых молекулы алкенов соединяются друг с другом с образованием больших длинных молекул, макромолекул. Реакция полимеризации алкенов и их производных протекает по свободнорадикальному механизму.
Полимеризация (особый тип реакций присоединения , в которых молекулы алкенов соединяются друг с другом с образованием больших длинных молекул, макромолекул. Реакция полимеризации алкенов и их производных протекает по свободнорадикальному механизму.

 Полимер это высокомолекулярное соединение (вмс) Мономер это низкомолекулярное соединение n степень полимеризации 1 группа структурное звено
Полимер это высокомолекулярное соединение (вмс) Мономер это низкомолекулярное соединение n степень полимеризации 1 группа структурное звено
 Сырье полиэтилен
Сырье полиэтилен
 Изделия из полиэтилена
Изделия из полиэтилена
 Сырье полипропилен
Сырье полипропилен
 Изделия из полипропилена
Изделия из полипропилена
 Свойства полиэтилена Полиэтилен полупрозрачный, эластичный, жирный на ощупь материал. При нагревании размягчается, в размягченном состоянии легко меняет форму, из расплава можно вытянуть нити.
Свойства полиэтилена Полиэтилен полупрозрачный, эластичный, жирный на ощупь материал. При нагревании размягчается, в размягченном состоянии легко меняет форму, из расплава можно вытянуть нити.
 Горит синеватым пламенем, распространяя запах расплавленного парафина, продолжает гореть вне пламени. Не изменяет окраску желтой бромной воды и фиолетового раствора перманганата калия. Данные растворы веществ не действуют на полимер, т. к. отсутствует в составе полимера - связь.
Горит синеватым пламенем, распространяя запах расплавленного парафина, продолжает гореть вне пламени. Не изменяет окраску желтой бромной воды и фиолетового раствора перманганата калия. Данные растворы веществ не действуют на полимер, т. к. отсутствует в составе полимера - связь.
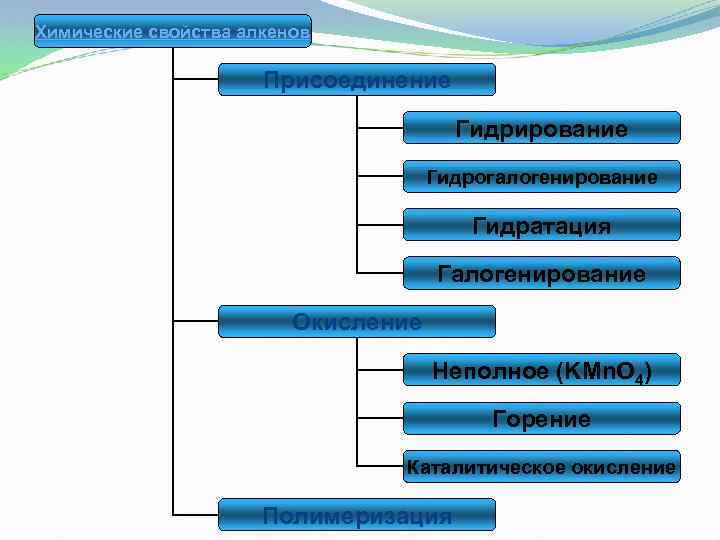 Химические свойства алкенов Присоединение Гидрирование Гидрогалогенирование Гидратация Галогенирование Окисление Неполное (KMn. O 4) Горение Каталитическое окисление Полимеризация
Химические свойства алкенов Присоединение Гидрирование Гидрогалогенирование Гидратация Галогенирование Окисление Неполное (KMn. O 4) Горение Каталитическое окисление Полимеризация
 1. Реакция присоединения водорода называется А) гидрирование Б) гидрогалогенирование В) гидратация В) дегидрирование 2. В реакции бромирования пропена образуется А) 1, 3 -дибромпропан Б) 1 -бромпропан В) 2 -бромпропан Г) 1, 2 -дибромпропан 3. Сумма коэффициентов в уравнении горения пропена равна: А) 11 Б) 15 В) 21 Г) 23 4. При гидрогалогенировании алкенов атом водорода присоединяется к … гидрированному атому углерода, а атом галогена – к … гидрированному. А) более Б) менее
1. Реакция присоединения водорода называется А) гидрирование Б) гидрогалогенирование В) гидратация В) дегидрирование 2. В реакции бромирования пропена образуется А) 1, 3 -дибромпропан Б) 1 -бромпропан В) 2 -бромпропан Г) 1, 2 -дибромпропан 3. Сумма коэффициентов в уравнении горения пропена равна: А) 11 Б) 15 В) 21 Г) 23 4. При гидрогалогенировании алкенов атом водорода присоединяется к … гидрированному атому углерода, а атом галогена – к … гидрированному. А) более Б) менее
 Реакция гидробромирования пропена протекает: 1) в соответствии с правилом В. В. Марковникова 2) в соответствии с правилом А. М. Зайцева 3) по радикальному механизму 4) по электрофильному механизму 5) с преимущественным образованием 2 бромпропана 6) с преимущественным образованием 1 бромпропана Ответы: 1, 4, 5
Реакция гидробромирования пропена протекает: 1) в соответствии с правилом В. В. Марковникова 2) в соответствии с правилом А. М. Зайцева 3) по радикальному механизму 4) по электрофильному механизму 5) с преимущественным образованием 2 бромпропана 6) с преимущественным образованием 1 бромпропана Ответы: 1, 4, 5
 Предложите способ очистки пропана от примесей этилена. Напишите уравнения соответствующих реакций. Ответ: пропустить смесь газов через раствор бромной воды или перманганата калия, этилен прореагирует с данными растворами.
Предложите способ очистки пропана от примесей этилена. Напишите уравнения соответствующих реакций. Ответ: пропустить смесь газов через раствор бромной воды или перманганата калия, этилен прореагирует с данными растворами.
 Назовите химические реакции, которые являются общими для алканов и алкенов. Ответ: реакции горения.
Назовите химические реакции, которые являются общими для алканов и алкенов. Ответ: реакции горения.
 Получение алкенов 1. Дегидратация спиртов: H 2 SO 4 H−CH 2−OH → CH 2=CH 2 + H 2 O 2. Из галогеналканов: H−CH 2−Br + KOHсп. р-р → СH 2=CH 2 + KBr + H 2 O 3. Крекинг алканов: t С 8 Н 18 → С 4 Н 10 + С 4 Н 8 4. Дегидрирование алканов: t, Cr 2 O 3 H−CH 2−H → CH 2=CH 2 + H 2
Получение алкенов 1. Дегидратация спиртов: H 2 SO 4 H−CH 2−OH → CH 2=CH 2 + H 2 O 2. Из галогеналканов: H−CH 2−Br + KOHсп. р-р → СH 2=CH 2 + KBr + H 2 O 3. Крекинг алканов: t С 8 Н 18 → С 4 Н 10 + С 4 Н 8 4. Дегидрирование алканов: t, Cr 2 O 3 H−CH 2−H → CH 2=CH 2 + H 2
 1. Бутен можно получить крекингом: А) бутана Б) пентана В) гексана Г) октана 2. Какие признаки характеризуют физические свойства этена: 1) бесцветная жидкость, 2) имеет резкий запах, 3) бесцветный газ, 4) немного легче воздуха, 5) почти без запаха, 6) плохо растворим в воде, 7) не горит, 8) с воздухом образует взрывоопасные смеси? А) 3, 4, 5, 6, 8 Б) 1, 2, 6, 7 В) 2, 3, 4, 6, 8 Г) 3, 4, 6, 8 3. Плотность паров алкена по водороду равна 49. Массовая доля углерода в нём – 85, 71%, массовая доля водорода – 14, 29%. Молекулярная формула этого углеводорода А) С 5 Н 10 Б) С 6 Н 12 В) С 7 Н 14 Г) С 8 Н 16
1. Бутен можно получить крекингом: А) бутана Б) пентана В) гексана Г) октана 2. Какие признаки характеризуют физические свойства этена: 1) бесцветная жидкость, 2) имеет резкий запах, 3) бесцветный газ, 4) немного легче воздуха, 5) почти без запаха, 6) плохо растворим в воде, 7) не горит, 8) с воздухом образует взрывоопасные смеси? А) 3, 4, 5, 6, 8 Б) 1, 2, 6, 7 В) 2, 3, 4, 6, 8 Г) 3, 4, 6, 8 3. Плотность паров алкена по водороду равна 49. Массовая доля углерода в нём – 85, 71%, массовая доля водорода – 14, 29%. Молекулярная формула этого углеводорода А) С 5 Н 10 Б) С 6 Н 12 В) С 7 Н 14 Г) С 8 Н 16



