Зав. кафедрой, д. м. н.








































































- Размер: 3.8 Mегабайта
- Количество слайдов: 79
Описание презентации Зав. кафедрой, д. м. н. по слайдам
 Зав. кафедрой, д. м. н. проф. Конопля Е. Н. Курск
Зав. кафедрой, д. м. н. проф. Конопля Е. Н. Курск
 Лабораторные и инструментальные методы исследования Основные клинические синдромы при заболеваниях печени
Лабораторные и инструментальные методы исследования Основные клинические синдромы при заболеваниях печени
 ФУНКЦИОНАЛЬНОЕ ИССЛЕДОВАНИЕ ПЕЧЕНИ • Исследование пигментного обмена. • Отражением пигментного обмена в печени является содержание в крови (а также в кале и моче) билирубина и продуктов его восстановления. • Определение нарушений пигментного обмена дает представление о функциональном состоянии гепатоцитов и помогает дифференцировать различные типы желтух. • Печень участвует в обмене билирубина, выполняя следующие функции: • 1) образование билирубина в звездчатых ретикулоэндотелиоцитах; • 2) захват свободного билирубина из крови; • 3) связывание билирубина с глюкуроновой кислотой; • 4) секреция в желчь билирубинглюкоронида (связанного билирубина).
ФУНКЦИОНАЛЬНОЕ ИССЛЕДОВАНИЕ ПЕЧЕНИ • Исследование пигментного обмена. • Отражением пигментного обмена в печени является содержание в крови (а также в кале и моче) билирубина и продуктов его восстановления. • Определение нарушений пигментного обмена дает представление о функциональном состоянии гепатоцитов и помогает дифференцировать различные типы желтух. • Печень участвует в обмене билирубина, выполняя следующие функции: • 1) образование билирубина в звездчатых ретикулоэндотелиоцитах; • 2) захват свободного билирубина из крови; • 3) связывание билирубина с глюкуроновой кислотой; • 4) секреция в желчь билирубинглюкоронида (связанного билирубина).
 • В сыворотке крови здорового человека определяется в основном свободный билирубин в количестве 8, 5 -20, 5 мкмоль/л (25% прямого и 75% непрямого билирубина), который дает непрямую реакцию с диазореактивом • Свободный билирубин, нерастворимый в воде, не выделяется почками; • После связывания с глюкуроновой кислотой он становится водорастворимым и дает прямую реакцию с диазореактивом и при накоплении в крови — при подпеченочной и печеночной желтухах он обнаруживается в моче. • В желчные пути выделяется только связанный билирубин (билирубинглюкуронид). В крупных желчных ходах и желчном пузыре и далее в кишечнике небольшая часть билирубина восстанавливается до уробилиногена, который резорбцируется в верхнем отделе тонкой кишки и с кровью воротной вены попадает в печень.
• В сыворотке крови здорового человека определяется в основном свободный билирубин в количестве 8, 5 -20, 5 мкмоль/л (25% прямого и 75% непрямого билирубина), который дает непрямую реакцию с диазореактивом • Свободный билирубин, нерастворимый в воде, не выделяется почками; • После связывания с глюкуроновой кислотой он становится водорастворимым и дает прямую реакцию с диазореактивом и при накоплении в крови — при подпеченочной и печеночной желтухах он обнаруживается в моче. • В желчные пути выделяется только связанный билирубин (билирубинглюкуронид). В крупных желчных ходах и желчном пузыре и далее в кишечнике небольшая часть билирубина восстанавливается до уробилиногена, который резорбцируется в верхнем отделе тонкой кишки и с кровью воротной вены попадает в печень.
 • Здоровая печень полностью улавливает его и окисляет, но поврежденный орган в состоянии выполнить эту функцию, уробилиноген переходит в кровь и выделяется с мочой. • Уробилинурия является тонким и ранним признаком функциональной недостаточности печени. Остальная, большая часть билирубина в кишечнике восстанавливается вплоть до стеркобилиногена. • Основная часть его выделяется с калом. • Небольшая часть стеркобилиногена, всасываясь в нижних отделах толстой кишки, минуя печень, по геморроидальным венам, попадает в общий круг кровообращения и выделяется почками.
• Здоровая печень полностью улавливает его и окисляет, но поврежденный орган в состоянии выполнить эту функцию, уробилиноген переходит в кровь и выделяется с мочой. • Уробилинурия является тонким и ранним признаком функциональной недостаточности печени. Остальная, большая часть билирубина в кишечнике восстанавливается вплоть до стеркобилиногена. • Основная часть его выделяется с калом. • Небольшая часть стеркобилиногена, всасываясь в нижних отделах толстой кишки, минуя печень, по геморроидальным венам, попадает в общий круг кровообращения и выделяется почками.
 • Исследование белкового обмена: • основано на методе электрофореза белков сыворотки крови, определении фибриногена и белковых осадочных пробах. • В норме количество общего белка составляет 65 -85 г / л • Альбумины составляют 50 -60% • Глобулины 40 -50%. Альбуминово-глобулиновый коэффециент состовляет 1 -1, 5 • Соотношение глобулинов α 1 — 4, α 2 – 8, β -12, γ -16 • Нарушение белковообразовательной функции печени ведет не только к уменьшению общего белка, альбуминов за счет снижения их синтеза, но и к диспротеинемии, в частности, гипергамма-глобулинемии, • Для заболеваний печени характерно сниже ние альбумино-глобулинового коэффициента. • Фибриноген синтезируется в печени. • В норме его количество в крови 2 -4 г / л • при тяжелом ее поражении количество фибриногена в плазме снижается, что может отразиться и на свертывании крови.
• Исследование белкового обмена: • основано на методе электрофореза белков сыворотки крови, определении фибриногена и белковых осадочных пробах. • В норме количество общего белка составляет 65 -85 г / л • Альбумины составляют 50 -60% • Глобулины 40 -50%. Альбуминово-глобулиновый коэффециент состовляет 1 -1, 5 • Соотношение глобулинов α 1 — 4, α 2 – 8, β -12, γ -16 • Нарушение белковообразовательной функции печени ведет не только к уменьшению общего белка, альбуминов за счет снижения их синтеза, но и к диспротеинемии, в частности, гипергамма-глобулинемии, • Для заболеваний печени характерно сниже ние альбумино-глобулинового коэффициента. • Фибриноген синтезируется в печени. • В норме его количество в крови 2 -4 г / л • при тяжелом ее поражении количество фибриногена в плазме снижается, что может отразиться и на свертывании крови.
 • Осадочные пробы. • Осадочные, или флоккуляционные, пробы это большая группа методов, основанных на взаимодействии различных реагентов с коллоидной системой белков сыворотки, при котором развивается преципитационное помутнение или флоккуляция. • Устойчивость коллоидной системы крови нарушается в основном из-за диспротеинемии и частично парапротеинемии, которая возникает при хронических диффузных болезнях печени. • Так γ — глобулины нормальной сыворотки имеют флоккулирующую активность, но в сыворотке больных гепатитом и циррозом эта активность значительно выше. • Антифлоккуляция происходит за счет альбуминов сыворотки и α 1 — глобулиновой фракции. • Ингибирующая способность этих белковых фракций уменьшается у больных диффузными заболеваниями печени.
• Осадочные пробы. • Осадочные, или флоккуляционные, пробы это большая группа методов, основанных на взаимодействии различных реагентов с коллоидной системой белков сыворотки, при котором развивается преципитационное помутнение или флоккуляция. • Устойчивость коллоидной системы крови нарушается в основном из-за диспротеинемии и частично парапротеинемии, которая возникает при хронических диффузных болезнях печени. • Так γ — глобулины нормальной сыворотки имеют флоккулирующую активность, но в сыворотке больных гепатитом и циррозом эта активность значительно выше. • Антифлоккуляция происходит за счет альбуминов сыворотки и α 1 — глобулиновой фракции. • Ингибирующая способность этих белковых фракций уменьшается у больных диффузными заболеваниями печени.
 • Фракция α 2 и β -глобулинов способствуют флоккуляции, а мукопротеиды играют роль ингибиторов. • Т. е. количественные или качественные изменения сывороточных протеиновых фракций, которые выражаются в увеличении флоккуляционной или уменьшением ингибиторной активности, становятся причиной измененных осадочных (флоккуляционных) проб. • Предложено много сравнительно простых осадочных проб. К ним относятся золотоколлоидальная (проба Ланге), фуксин-сулемовая (реакция Таката), кефалин-холестериновая, цинк-сульфатная реакция Иргля, коагуляционная проба (проба Вельтмана), тимоловая реакция Мак-Лагана.
• Фракция α 2 и β -глобулинов способствуют флоккуляции, а мукопротеиды играют роль ингибиторов. • Т. е. количественные или качественные изменения сывороточных протеиновых фракций, которые выражаются в увеличении флоккуляционной или уменьшением ингибиторной активности, становятся причиной измененных осадочных (флоккуляционных) проб. • Предложено много сравнительно простых осадочных проб. К ним относятся золотоколлоидальная (проба Ланге), фуксин-сулемовая (реакция Таката), кефалин-холестериновая, цинк-сульфатная реакция Иргля, коагуляционная проба (проба Вельтмана), тимоловая реакция Мак-Лагана.
 • Наибольшее распространение в клинической практике получила тимоловая проба , чувствительная к повышению уровня β и γ -глобулинов, а также ингибирующей способности β -липопротеидов и липидов сыворотки. • Нормальная величина тимоловой пробы 0 -4 ед. • Алиментарная гиперлипемия значительно влияет на результаты тимоловой пробы, поэтому кровь для исследования следует брать натощак. • При ОВГ тимоловая проба повышается в первые дни желтушного периода, но может стать положительной даже в дожелтушном периоде сывороточного гепатита.
• Наибольшее распространение в клинической практике получила тимоловая проба , чувствительная к повышению уровня β и γ -глобулинов, а также ингибирующей способности β -липопротеидов и липидов сыворотки. • Нормальная величина тимоловой пробы 0 -4 ед. • Алиментарная гиперлипемия значительно влияет на результаты тимоловой пробы, поэтому кровь для исследования следует брать натощак. • При ОВГ тимоловая проба повышается в первые дни желтушного периода, но может стать положительной даже в дожелтушном периоде сывороточного гепатита.
 • Показатели тимоловой пробы возвращаются к норме к концу 4 -5 -й недели желтушного периода. При затяжном вирусном гепатите или его переходе в хроническую форму показатели остаются постоянно повышенными. • У больных хроническим гепатитом и циррозом печени, тимоловая проба является одним из наиболее чувствительных и надежных функциональных показателей активности патологического процесса в печени. • Эта проба отрицательна при механической желтухе. • Большое преимущество тимоловой пробы перед другими осадочными пробами представляет ее цифровое выражение, позволяющее точно оценить динамику изменений.
• Показатели тимоловой пробы возвращаются к норме к концу 4 -5 -й недели желтушного периода. При затяжном вирусном гепатите или его переходе в хроническую форму показатели остаются постоянно повышенными. • У больных хроническим гепатитом и циррозом печени, тимоловая проба является одним из наиболее чувствительных и надежных функциональных показателей активности патологического процесса в печени. • Эта проба отрицательна при механической желтухе. • Большое преимущество тимоловой пробы перед другими осадочными пробами представляет ее цифровое выражение, позволяющее точно оценить динамику изменений.
 • Сулемовая проба наиболее показательна при ХАГ и циррозе печени. Резкое снижение уровня сулемовой пробы (1 мл и ниже) отмечается при далеко зашедшем процессе и свидетельствует о выраженной печеночно-клеточной недостаточности • Формоловая проба – превращение сыворотки в студнеобразную массу при значительном увеличении количества глобулинов и особенно фибриногена.
• Сулемовая проба наиболее показательна при ХАГ и циррозе печени. Резкое снижение уровня сулемовой пробы (1 мл и ниже) отмечается при далеко зашедшем процессе и свидетельствует о выраженной печеночно-клеточной недостаточности • Формоловая проба – превращение сыворотки в студнеобразную массу при значительном увеличении количества глобулинов и особенно фибриногена.
 • Факторы свертывания крови — протромбин, проконвертин, акцелерин, фибриноген, антигемофилический фактор — синтезируются преимущественно в печени. • Протромбиновый индекс или протромбиновая активность , определяемый по Квику, отражает суммарную активность ряда веществ — протромбина, проконвертина, акцелерина и фактора Стюарта — Прауэр. • Для получения достоверных результатов определения протромбиновой активности необходимо использовать стандартизованный тромбопластин. • Нормальные показатели в пределах 80 -100 %. • Клиническое значение пробы состоит в резком ее снижении при развитии субмассивных и массивных некрозов печени. Резкое падение протромбинового индекса у больных острыми хроническими болезнями печени указывает на выраженную печеночно-клеточную недостаточность, угрозу печеночной комы.
• Факторы свертывания крови — протромбин, проконвертин, акцелерин, фибриноген, антигемофилический фактор — синтезируются преимущественно в печени. • Протромбиновый индекс или протромбиновая активность , определяемый по Квику, отражает суммарную активность ряда веществ — протромбина, проконвертина, акцелерина и фактора Стюарта — Прауэр. • Для получения достоверных результатов определения протромбиновой активности необходимо использовать стандартизованный тромбопластин. • Нормальные показатели в пределах 80 -100 %. • Клиническое значение пробы состоит в резком ее снижении при развитии субмассивных и массивных некрозов печени. Резкое падение протромбинового индекса у больных острыми хроническими болезнями печени указывает на выраженную печеночно-клеточную недостаточность, угрозу печеночной комы.
 • У больных с выраженным внутрипеченочным холестазом снижение протромбиновой активности связывают не только с поражением гепатоцитов, но и с вторичным дефицитом витамина К. • Проконвертин — фактор VII — участвует в образовании тромбопластина. Нормальные показатели — 80 -120 %. Выявляется отчетливая зависимость между степенью печеночно-клеточной недостаточности и снижением уровня проконвертина у больных острыми гепатитами тяжелого течения и циррозами печени. • Проконвертин является тестом выбора для распознавания и контроля за течением печеночно-клеточной недостаточности у больных с прекомой и комой. • Недостаток пробы в затруднении оценки ее показателей при наличии внутри- и внепеченочного холестаза. • Для устранения возможного дефицита витамина К рекомендуется нагрузка этим витамином.
• У больных с выраженным внутрипеченочным холестазом снижение протромбиновой активности связывают не только с поражением гепатоцитов, но и с вторичным дефицитом витамина К. • Проконвертин — фактор VII — участвует в образовании тромбопластина. Нормальные показатели — 80 -120 %. Выявляется отчетливая зависимость между степенью печеночно-клеточной недостаточности и снижением уровня проконвертина у больных острыми гепатитами тяжелого течения и циррозами печени. • Проконвертин является тестом выбора для распознавания и контроля за течением печеночно-клеточной недостаточности у больных с прекомой и комой. • Недостаток пробы в затруднении оценки ее показателей при наличии внутри- и внепеченочного холестаза. • Для устранения возможного дефицита витамина К рекомендуется нагрузка этим витамином.
 • Исследование углеводного обмена. • В клетках печени при участии энзимных систем происходит синтез гликогена, его депонирование и гликогенолиз, и гликонеогенез. • Поддержание уровня глюкозы в крови обеспечивается, помимо печени, деятельностью других органов и систем поджелудочной железы, гипофизарно-надночечниковой системы и др. • Поэтому содержание глюкозы в крови натощак меняется лишь при крайне тяжелых поражениях печени, и выявление недостаточного участия ее в углеводном обмене возможно лишь с помощью функциональных проб. • Проба с нагрузкой глюкозой малоэффективна, так как на содержание глюкозы в крови, влияют и состояние вегетативной нервной системы, и запасы гликогена в печени и мышцах и т. д.
• Исследование углеводного обмена. • В клетках печени при участии энзимных систем происходит синтез гликогена, его депонирование и гликогенолиз, и гликонеогенез. • Поддержание уровня глюкозы в крови обеспечивается, помимо печени, деятельностью других органов и систем поджелудочной железы, гипофизарно-надночечниковой системы и др. • Поэтому содержание глюкозы в крови натощак меняется лишь при крайне тяжелых поражениях печени, и выявление недостаточного участия ее в углеводном обмене возможно лишь с помощью функциональных проб. • Проба с нагрузкой глюкозой малоэффективна, так как на содержание глюкозы в крови, влияют и состояние вегетативной нервной системы, и запасы гликогена в печени и мышцах и т. д.
 • Проба с нагрузкой галактозой представляет известную ценность (галактоза не усваивается никакими тканями и органами, кроме печени, и на содержание ее в крови не влияют гормоны). • Больному дают выпить раствор 40 г галактозы в 200 мл воды и определяют выделение ее с мочой. • В норме оно происходит в течение не более 4 ч и не превышает 3 г. • На выделение галактозы с мочой могут влиять функция почек и всасывательная способность кишечника, поэтому более показательным является определение содержания галактозы в крови. • При хорошей функции печени максимальный подъем содержания галактозы крови наблюдается через 30 -60 мин и не превышает 15% исходного уровня; последний снова достигается к 2 ч. • При плохой функции печени подъем уровня галактозы выше, снижение уровня галактозы в крови наступает медленнее.
• Проба с нагрузкой галактозой представляет известную ценность (галактоза не усваивается никакими тканями и органами, кроме печени, и на содержание ее в крови не влияют гормоны). • Больному дают выпить раствор 40 г галактозы в 200 мл воды и определяют выделение ее с мочой. • В норме оно происходит в течение не более 4 ч и не превышает 3 г. • На выделение галактозы с мочой могут влиять функция почек и всасывательная способность кишечника, поэтому более показательным является определение содержания галактозы в крови. • При хорошей функции печени максимальный подъем содержания галактозы крови наблюдается через 30 -60 мин и не превышает 15% исходного уровня; последний снова достигается к 2 ч. • При плохой функции печени подъем уровня галактозы выше, снижение уровня галактозы в крови наступает медленнее.
 • Жировой обмен. • Печень играет основную роль в синтезе и расщеплении жиров, фосфолипидов и холестерина. • Содержание липидов в крови изменяется при поражении печени. • В норме в сыворотке содержится 3, 9 — 5, 2 ммоль/л холестерина. У больных с тяжелыми формами острых и хронических гепатитов и циррозов вследствие нарушения синтеза содержание холестерина в снижается. • При большинстве холестатических желтух отмечается повышение его уровня.
• Жировой обмен. • Печень играет основную роль в синтезе и расщеплении жиров, фосфолипидов и холестерина. • Содержание липидов в крови изменяется при поражении печени. • В норме в сыворотке содержится 3, 9 — 5, 2 ммоль/л холестерина. У больных с тяжелыми формами острых и хронических гепатитов и циррозов вследствие нарушения синтеза содержание холестерина в снижается. • При большинстве холестатических желтух отмечается повышение его уровня.
 • Определение активности ферментов • Занимает особое место в диагностике заболеваний печени и желчевыводящих путей. • Исследуют уровень: трансаминаз- аспарагиновой трансаминазы ( A с. А T ), аланиновой трансаминазы (А л. А Т), γ -глутамил-транспептидазы ( γ -ГТП), щелочной фосфатазы (ЩФ), холинэстеразы (ХЭ). • Активность трансаминаз, особенно A с. А T , нарастает в активной фазе острых и хронических заболеваний печени. ( N 0, 1 -0, 45 ммоль / ч. л или 8 -40 ед. ) • Повышение активности γ -ГТП ( N 0, 6 -3, 96 ммоль / ч. л) характерно для холестаза, алкогольных поражений печени, • Повышение ЩФ ( N 1, 0 -3, 0 ммоль / ч. л) характерно для холестаза и опухолей. • Снижение активности холинэстеразы сыворотки свидетельствует о тяжелом поражении гепатоцитов.
• Определение активности ферментов • Занимает особое место в диагностике заболеваний печени и желчевыводящих путей. • Исследуют уровень: трансаминаз- аспарагиновой трансаминазы ( A с. А T ), аланиновой трансаминазы (А л. А Т), γ -глутамил-транспептидазы ( γ -ГТП), щелочной фосфатазы (ЩФ), холинэстеразы (ХЭ). • Активность трансаминаз, особенно A с. А T , нарастает в активной фазе острых и хронических заболеваний печени. ( N 0, 1 -0, 45 ммоль / ч. л или 8 -40 ед. ) • Повышение активности γ -ГТП ( N 0, 6 -3, 96 ммоль / ч. л) характерно для холестаза, алкогольных поражений печени, • Повышение ЩФ ( N 1, 0 -3, 0 ммоль / ч. л) характерно для холестаза и опухолей. • Снижение активности холинэстеразы сыворотки свидетельствует о тяжелом поражении гепатоцитов.
 • Лактатдегидрогенеза (ЛДГ) — фермент, участвующий в одном из конечных этапов превращения глюкозы с образованием молочной кислоты. • Находится во всех органах и тканях, поэтому диагностическое значение имеет определение изоферментов ЛДГ, так как отдельные изоформы характеризуют преимущественно определен ные органы. • Нормальный изоферментный спектр сыворотки крови: • ЛДГ 1 — 30 -36%, • ЛДГ 2 — 40 -50%, • ЛДГ 3 — 14 -20%, • ЛДГ 4 — 0 -4%, • ЛДГ 5 — 0 -2%, • ЛДГ 2 /ЛДГ 1 1, 2 -1, 5.
• Лактатдегидрогенеза (ЛДГ) — фермент, участвующий в одном из конечных этапов превращения глюкозы с образованием молочной кислоты. • Находится во всех органах и тканях, поэтому диагностическое значение имеет определение изоферментов ЛДГ, так как отдельные изоформы характеризуют преимущественно определен ные органы. • Нормальный изоферментный спектр сыворотки крови: • ЛДГ 1 — 30 -36%, • ЛДГ 2 — 40 -50%, • ЛДГ 3 — 14 -20%, • ЛДГ 4 — 0 -4%, • ЛДГ 5 — 0 -2%, • ЛДГ 2 /ЛДГ 1 1, 2 -1, 5.
 • Определение изоферментного спектра ЛДГ чаще всего назначается при патологии печени и сердца, реже — легких. • При инфаркте миокарда в течение первых 2 -3 суток активность ЛДГ 1 значительно возрастает и соотношение ЛДГ 2 /ЛДГ 1 становится равным 0, 6 -0, 8. Нормализация происходит спустя 2 -3 недели после инфаркта миокарда и зависит от объема поражения — чем обширнее был инфаркт, тем дольше сохраняются изменения в изоферментном спектре ЛДГ. • При других заболеваниях сердца этот показатель, как правило, не меняется. • При заболеваниях печени, сопровождающихся повреждением клеток (гепатиты, токсические воздействия, метастазы в печень), отмечается увеличение активности фракций ЛДГ 4 и ЛДГ 5.
• Определение изоферментного спектра ЛДГ чаще всего назначается при патологии печени и сердца, реже — легких. • При инфаркте миокарда в течение первых 2 -3 суток активность ЛДГ 1 значительно возрастает и соотношение ЛДГ 2 /ЛДГ 1 становится равным 0, 6 -0, 8. Нормализация происходит спустя 2 -3 недели после инфаркта миокарда и зависит от объема поражения — чем обширнее был инфаркт, тем дольше сохраняются изменения в изоферментном спектре ЛДГ. • При других заболеваниях сердца этот показатель, как правило, не меняется. • При заболеваниях печени, сопровождающихся повреждением клеток (гепатиты, токсические воздействия, метастазы в печень), отмечается увеличение активности фракций ЛДГ 4 и ЛДГ 5.
 • Исследование обезвреживающей функции печени. • Кровь воротной вены, поступающая от желудочно-кишечного тракта, содержит различные токсичные вещества, для которых печень служит барьером. • Здесь они не только задерживаются, но в большинстве своем и обезвреживаются с помощью ферментов, осуществляющих окисление, восстановление, дезаминирование, гидролиз, метилирование, образование сульфатов и глюкуронидов, соединение с глицином. • В результате этих преобразований получаются или менее токсичные, или более растворимые вещества, которые могут быть выведены с желчью или мочой. • Аммиак превращается в менее токсичную мочевину; • свободный билирубин, соединяясь с глюкуроновой кислотой, становится менее токсичным и водорастворимым и может выводиться с желчью и мочой. • Фенолы, индол, кетоны, спирты, сульфаниламидные препараты, пирамидон, камфора, морфин обезвреживаются путем образования глюкуронидов или сульфатов.
• Исследование обезвреживающей функции печени. • Кровь воротной вены, поступающая от желудочно-кишечного тракта, содержит различные токсичные вещества, для которых печень служит барьером. • Здесь они не только задерживаются, но в большинстве своем и обезвреживаются с помощью ферментов, осуществляющих окисление, восстановление, дезаминирование, гидролиз, метилирование, образование сульфатов и глюкуронидов, соединение с глицином. • В результате этих преобразований получаются или менее токсичные, или более растворимые вещества, которые могут быть выведены с желчью или мочой. • Аммиак превращается в менее токсичную мочевину; • свободный билирубин, соединяясь с глюкуроновой кислотой, становится менее токсичным и водорастворимым и может выводиться с желчью и мочой. • Фенолы, индол, кетоны, спирты, сульфаниламидные препараты, пирамидон, камфора, морфин обезвреживаются путем образования глюкуронидов или сульфатов.
 • Бензойный натрий — путем соединения с глицином; сантонин окисляется в оксисантонин; металлы вступают в связь с нуклеопрогеидами, звездчатые ретикулоэндотелиоциты задерживают и фагоцитируют микроорганизмы. • Проба с нагрузкой бензойно-кислым натрием. • Этот препарат, принятый внутрь или введенный внутривенно, соединяется в печени с глицином, образуя гиппуровую кислоту , и выводится с мочой. • Обезвреживающая функция печени оценивается по проценту выделенного с мочой бензойно-кислого натрия в виде гиппуровой кислоты. • При поражении паренхимы печени синтез гиппуровой кислоты нарушается и выделение ее замедляется. • Проба имеет ряд недостатков: она положительная при механических желтухах, опухолях, лихорадочных состояниях и ее можно проводить только при нормальной функ ции почек.
• Бензойный натрий — путем соединения с глицином; сантонин окисляется в оксисантонин; металлы вступают в связь с нуклеопрогеидами, звездчатые ретикулоэндотелиоциты задерживают и фагоцитируют микроорганизмы. • Проба с нагрузкой бензойно-кислым натрием. • Этот препарат, принятый внутрь или введенный внутривенно, соединяется в печени с глицином, образуя гиппуровую кислоту , и выводится с мочой. • Обезвреживающая функция печени оценивается по проценту выделенного с мочой бензойно-кислого натрия в виде гиппуровой кислоты. • При поражении паренхимы печени синтез гиппуровой кислоты нарушается и выделение ее замедляется. • Проба имеет ряд недостатков: она положительная при механических желтухах, опухолях, лихорадочных состояниях и ее можно проводить только при нормальной функ ции почек.
 • Исследование выделительной функции печени. • Среди веществ, подлежащих выведению из организма, водорастворимые выделяются преимущественно почками, нерастворимые в воде или связанные с белками — печенью. • Нормальная выделительная способность печени ограничена. • При значительном усилении гемолиза здоровая печень неспособна вывести весь билирубин из крови и он в ней накапливается. • При поражении паренхимы уменьшаются выделительные возможности печени, что, часто проявляется билирубинемией. • Для выявления нарушенной выделительной функции печени, особенно при безжелтушных формах заболевания, большое значение имеют пробы с введением в кровь веществ, подлежащих выведению с желчью.
• Исследование выделительной функции печени. • Среди веществ, подлежащих выведению из организма, водорастворимые выделяются преимущественно почками, нерастворимые в воде или связанные с белками — печенью. • Нормальная выделительная способность печени ограничена. • При значительном усилении гемолиза здоровая печень неспособна вывести весь билирубин из крови и он в ней накапливается. • При поражении паренхимы уменьшаются выделительные возможности печени, что, часто проявляется билирубинемией. • Для выявления нарушенной выделительной функции печени, особенно при безжелтушных формах заболевания, большое значение имеют пробы с введением в кровь веществ, подлежащих выведению с желчью.
 • Проба с бромсульфалеином является одной из наиболее специфичных. Препарат вводят больному внутривенно из расчета 5 мг/кг. Через 3 мин после введения, когда достигается максимальная концентрация препарата в крови, берут первую пробу крови, а через 45 мин — вторую. • В обеих порциях концентрацию бромсульфалеина. • При хорошей выделительной функции печени через 45 мин в крови содержится не более 5% препарата от первоначальной концентрации, принимаемой за 100%. • Краску через 15 мин после ее введения можно обнаружить и в желчи. • Проба очень чувствительна: небольшие нарушения функции органа, не улавливаемые другими методами, заметно сказываются на ее результатах. • Проба с зеленым индоцианом основана на аналогичном принципе. Препарат вводят внутривенно из расчета 0, 5 мг/кг; в норме через 20 мин в крови остается не более 4% введенной краски. • Проба более чувствительная, чем бромсульфалеиновая.
• Проба с бромсульфалеином является одной из наиболее специфичных. Препарат вводят больному внутривенно из расчета 5 мг/кг. Через 3 мин после введения, когда достигается максимальная концентрация препарата в крови, берут первую пробу крови, а через 45 мин — вторую. • В обеих порциях концентрацию бромсульфалеина. • При хорошей выделительной функции печени через 45 мин в крови содержится не более 5% препарата от первоначальной концентрации, принимаемой за 100%. • Краску через 15 мин после ее введения можно обнаружить и в желчи. • Проба очень чувствительна: небольшие нарушения функции органа, не улавливаемые другими методами, заметно сказываются на ее результатах. • Проба с зеленым индоцианом основана на аналогичном принципе. Препарат вводят внутривенно из расчета 0, 5 мг/кг; в норме через 20 мин в крови остается не более 4% введенной краски. • Проба более чувствительная, чем бромсульфалеиновая.
 • Иммунологические методы. • Используются для выявления неспецифических изменений • Определяют иммуноглобулины разных классов, комплемент, циркулирующие иммунные комплексы. • Проводится исследование α — фетопротеина — индикатора регенерации и опухолевого роста. • В последнее время широко используются методы, позволяющие обнаружить как инфицирование вирусами гепатита А, В, С, Д, Е, так и стадию репликации этих вирусов, особенно гепатита В и С (иммуноферментный и радиоиммунный анализ для выявления маркеров репликации, полимеразная цепная реакция для индикации ДНК ВГВ и РНК ВГС).
• Иммунологические методы. • Используются для выявления неспецифических изменений • Определяют иммуноглобулины разных классов, комплемент, циркулирующие иммунные комплексы. • Проводится исследование α — фетопротеина — индикатора регенерации и опухолевого роста. • В последнее время широко используются методы, позволяющие обнаружить как инфицирование вирусами гепатита А, В, С, Д, Е, так и стадию репликации этих вирусов, особенно гепатита В и С (иммуноферментный и радиоиммунный анализ для выявления маркеров репликации, полимеразная цепная реакция для индикации ДНК ВГВ и РНК ВГС).
 ИНСТРУМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ПЕЧЕНИ • Важное место принадлежит рентгенологическому исследованию верхних отделов желудочно-кишечного тракта и ФЭГД • Они позволяют выявить варикозное расширение вен пищевода, изменения слизистой оболочки желудка (что характерно для синдрома портальной гипертензии), эрозивный эзофагит, гастрит.
ИНСТРУМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ПЕЧЕНИ • Важное место принадлежит рентгенологическому исследованию верхних отделов желудочно-кишечного тракта и ФЭГД • Они позволяют выявить варикозное расширение вен пищевода, изменения слизистой оболочки желудка (что характерно для синдрома портальной гипертензии), эрозивный эзофагит, гастрит.
 • Высокоинформативными методами диагностики заболеваний печени служат ультразвуковое исследование, компьютерная томография, радиоизотопное сканирование. • Выбор метода определяется его возможностями и доступностью.
• Высокоинформативными методами диагностики заболеваний печени служат ультразвуковое исследование, компьютерная томография, радиоизотопное сканирование. • Выбор метода определяется его возможностями и доступностью.
 • Возможности специальных методов исследования печени Метод Показания Ультра- звуковое исследо- вание Очаговые поражения (кисты, гемангиомы). Цирроз печени, стеатоз печени. Исследование деталей анатомического строения (диагностика холестаза, портальной гипертензии, асцита, спленомегалии). Контроль при проведении Компью терная томогра-ф ия ия Исследование деталей анатомического строения, сосудистой системы, билиарного дерева (диагностика холелитиаза, абсцессов, кист, метастазов опухолей, гемангиом, аденом). Контроль при проведении пункции патологического очага Радиоизо- топное сканиро- вание Очаговые поражения (опухоли, метастазы, кисты, абсцессы). Диффузные поражения (цирроз в поздней стад. )
• Возможности специальных методов исследования печени Метод Показания Ультра- звуковое исследо- вание Очаговые поражения (кисты, гемангиомы). Цирроз печени, стеатоз печени. Исследование деталей анатомического строения (диагностика холестаза, портальной гипертензии, асцита, спленомегалии). Контроль при проведении Компью терная томогра-ф ия ия Исследование деталей анатомического строения, сосудистой системы, билиарного дерева (диагностика холелитиаза, абсцессов, кист, метастазов опухолей, гемангиом, аденом). Контроль при проведении пункции патологического очага Радиоизо- топное сканиро- вание Очаговые поражения (опухоли, метастазы, кисты, абсцессы). Диффузные поражения (цирроз в поздней стад. )
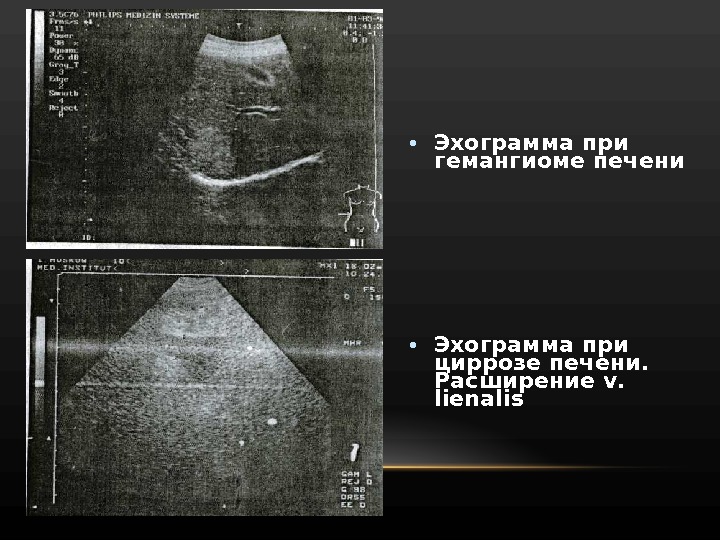
 • Эхограмма при гемангиоме печени • Эхограмма при циррозе печени. Расширение v. lienalis
• Эхограмма при гемангиоме печени • Эхограмма при циррозе печени. Расширение v. lienalis
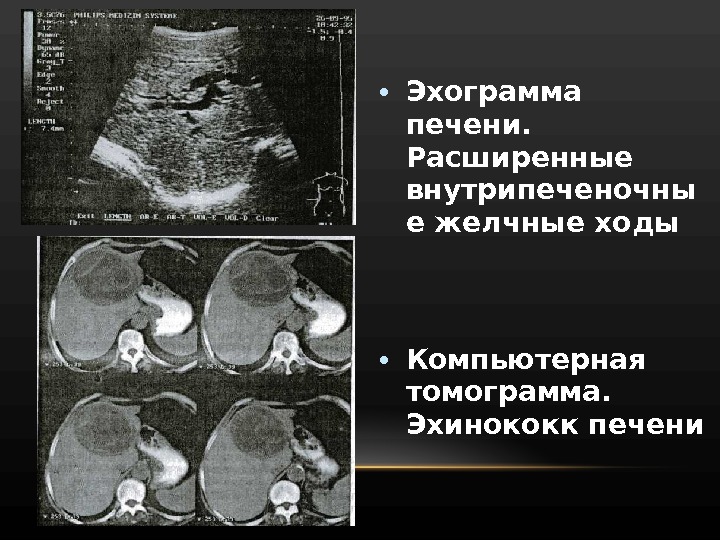
 • Эхограмма печени. Расширенные внутрипеченочны е желчные ходы • Компьютерная томограмма. Эхинококк печени
• Эхограмма печени. Расширенные внутрипеченочны е желчные ходы • Компьютерная томограмма. Эхинококк печени
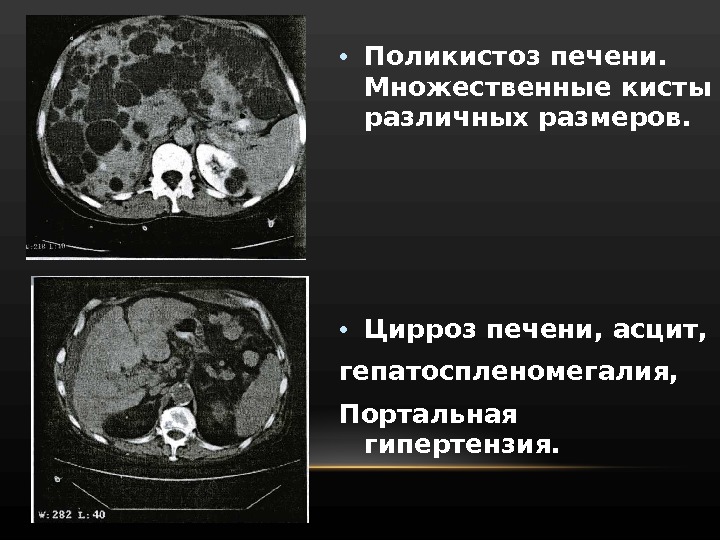
 • Поликистоз печени. Множественные кисты различных размеров. • Цирроз печени, асцит, гепатоспленомегалия, Портальная гипертензия.
• Поликистоз печени. Множественные кисты различных размеров. • Цирроз печени, асцит, гепатоспленомегалия, Портальная гипертензия.
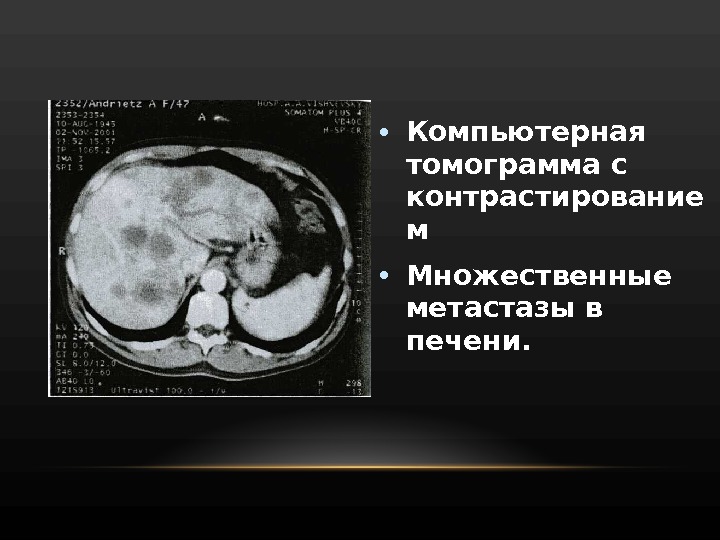
 • Компьютерная томограмма с контрастирование м • Множественные метастазы в печени.
• Компьютерная томограмма с контрастирование м • Множественные метастазы в печени.
 • Пункционная биопсия печени показана для диагностики диффузных заболеваний печени (хронический гепатит, жировой гепатоз, цирроз печени). • Исследование пунктата печени высокоинформативно для постановки диагноза и уточнения активности патологического процесса в печени Для диагностики очаговых поражений печени используется при цельная биопсия под контролем ультразвукового исследования и компьютерной томографии. • Лапароскопия — достаточно сложный и травматичный метод исследования, применяется, главным образом, для уточнения узловых очаговых образований в печени с последующей прицельной биопсией.
• Пункционная биопсия печени показана для диагностики диффузных заболеваний печени (хронический гепатит, жировой гепатоз, цирроз печени). • Исследование пунктата печени высокоинформативно для постановки диагноза и уточнения активности патологического процесса в печени Для диагностики очаговых поражений печени используется при цельная биопсия под контролем ультразвукового исследования и компьютерной томографии. • Лапароскопия — достаточно сложный и травматичный метод исследования, применяется, главным образом, для уточнения узловых очаговых образований в печени с последующей прицельной биопсией.
 • Исследование желчного пузыря и желчных путей • Пероральная холецистография сохраняет свое значение при определении количества, размеров и структуры камней, проходимости пузырного протока и оценке способности стенок желчного пузыря к сокращению. • Недостатками метода является лучевая нагрузка, невозможность проведения исследования при желтухе, а также аллергические реакции на йод.
• Исследование желчного пузыря и желчных путей • Пероральная холецистография сохраняет свое значение при определении количества, размеров и структуры камней, проходимости пузырного протока и оценке способности стенок желчного пузыря к сокращению. • Недостатками метода является лучевая нагрузка, невозможность проведения исследования при желтухе, а также аллергические реакции на йод.
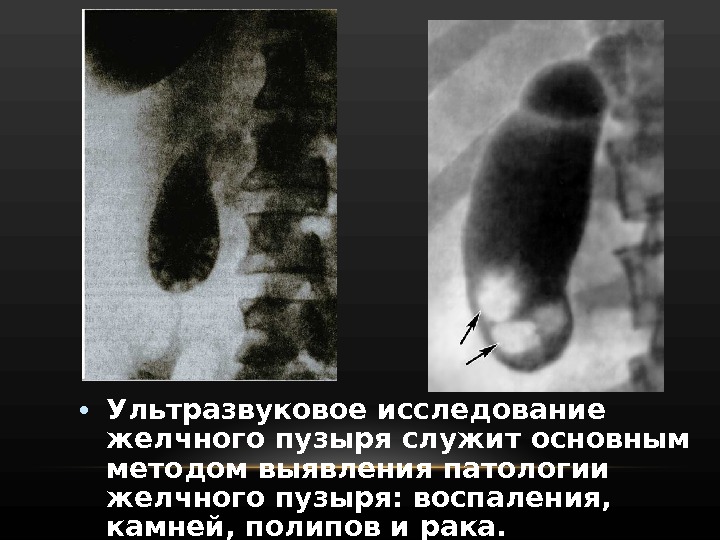
 • Ультразвуковое исследование желчного пузыря служит основным методом выявления патологии желчного пузыря: воспаления, камней, полипов и рака.
• Ультразвуковое исследование желчного пузыря служит основным методом выявления патологии желчного пузыря: воспаления, камней, полипов и рака.
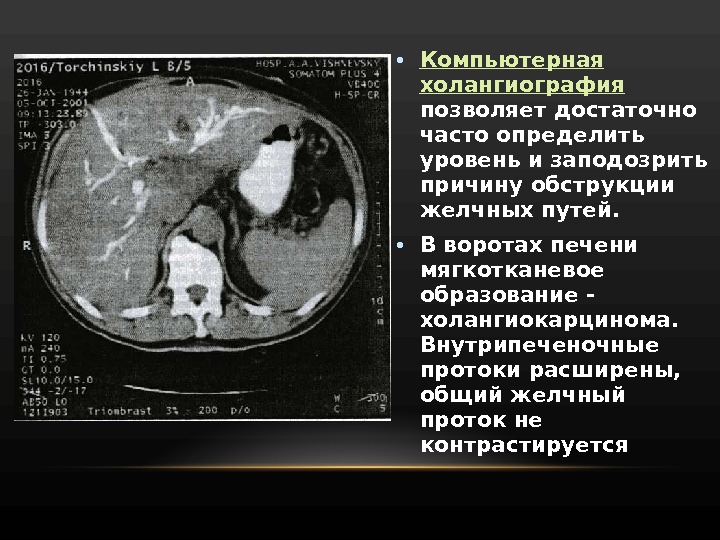
 • Компьютерная холангиография позволяет достаточно часто определить уровень и заподозрить причину обструкции желчных путей. • В воротах печени мягкотканевое образование — холангиокарцинома. Внутрипеченочные протоки расширены, общий желчный проток не контрастируется
• Компьютерная холангиография позволяет достаточно часто определить уровень и заподозрить причину обструкции желчных путей. • В воротах печени мягкотканевое образование — холангиокарцинома. Внутрипеченочные протоки расширены, общий желчный проток не контрастируется
 • Эндоскопическая ретроградная панкреатохолангиография • (ЭРПХГ) — восходящее (ретроградное) эндоскопическое введение контрастного вещества через большой дуоденальный сосок с одновременным рентгенологическим исследованием желчевыводящих путей и панкреатических протоков. ЭРПХГ применяется для выяснения причин подпеченочной желтухи, при наличии клинических и ультразвуковых признаков холедохолитиаза. • Дуоденальное зондирование в диагностике заболеваний желчного пузыря и желчных путей значительно утратило свою значимость в связи с широким использованием эндоскопии и ультразвукового исследования. • Многомоментное фракционное дуоденальное зондирование позволяет получить желчь из общего желчного протока, желчного пузыря и внутрипеченочных желчных протоков с последующим биохимическим и микроскопическим исследованием. • Этот метод дает представление о функции желчного пузыря и желчевыводящих протоков
• Эндоскопическая ретроградная панкреатохолангиография • (ЭРПХГ) — восходящее (ретроградное) эндоскопическое введение контрастного вещества через большой дуоденальный сосок с одновременным рентгенологическим исследованием желчевыводящих путей и панкреатических протоков. ЭРПХГ применяется для выяснения причин подпеченочной желтухи, при наличии клинических и ультразвуковых признаков холедохолитиаза. • Дуоденальное зондирование в диагностике заболеваний желчного пузыря и желчных путей значительно утратило свою значимость в связи с широким использованием эндоскопии и ультразвукового исследования. • Многомоментное фракционное дуоденальное зондирование позволяет получить желчь из общего желчного протока, желчного пузыря и внутрипеченочных желчных протоков с последующим биохимическим и микроскопическим исследованием. • Этот метод дает представление о функции желчного пузыря и желчевыводящих протоков
 ОСНОВНЫЕ СИНДРОМЫ ПРИ ПАТОЛОГИИ БИЛИАРНОЙ СИСТЕМЫ • Клинические синдромы: ▪ Желтухи и холестаза ▪ Синдром портальной гипертензии ▪ Гепатолиенальный синдром ▪ Геморрагический синдром ▪ Гепаторенальный синдром ▪ Синдром печеночной недостаточности • Лабораторные синдромы: ▪ синдром цитолиза ▪ синдром холестаза ▪ синдром неспецифического мезенхиального воспаления с выраженным иммунным компонентом. ▪ синдром печеночно-клеточной недостаточности • Обычно эти синдромы наблюдаются не изолировано, а в сочетании, но в клинической картине преобладают симптомы одного из них.
ОСНОВНЫЕ СИНДРОМЫ ПРИ ПАТОЛОГИИ БИЛИАРНОЙ СИСТЕМЫ • Клинические синдромы: ▪ Желтухи и холестаза ▪ Синдром портальной гипертензии ▪ Гепатолиенальный синдром ▪ Геморрагический синдром ▪ Гепаторенальный синдром ▪ Синдром печеночной недостаточности • Лабораторные синдромы: ▪ синдром цитолиза ▪ синдром холестаза ▪ синдром неспецифического мезенхиального воспаления с выраженным иммунным компонентом. ▪ синдром печеночно-клеточной недостаточности • Обычно эти синдромы наблюдаются не изолировано, а в сочетании, но в клинической картине преобладают симптомы одного из них.
 СИНДРОМ ЖЕЛТУХИ И ХОЛЕСТАЗА • Возникновение желтухи всегда обусловлено нарушением обмена билирубина, который образуется в результате распада гемоглобина, эритроцитов и разрушения гема. • Гемоглобин превращается в билирубин в ретикулоэндотелиальной системе, преимущественно в печени, селезенке и костном мозге в результате сложного комплекса окислительно-восстановительных реакций. • Клетки ретикулоэндотелиальной системы выделяют в кровь непрямой, свободный, несвязанный, неконъюгированный билирубин. • Всего за сутки синтезируется около 300 мг билирубина.
СИНДРОМ ЖЕЛТУХИ И ХОЛЕСТАЗА • Возникновение желтухи всегда обусловлено нарушением обмена билирубина, который образуется в результате распада гемоглобина, эритроцитов и разрушения гема. • Гемоглобин превращается в билирубин в ретикулоэндотелиальной системе, преимущественно в печени, селезенке и костном мозге в результате сложного комплекса окислительно-восстановительных реакций. • Клетки ретикулоэндотелиальной системы выделяют в кровь непрямой, свободный, несвязанный, неконъюгированный билирубин. • Всего за сутки синтезируется около 300 мг билирубина.
 • Печень выполняет три важнейших функции в обмене билирубина: ▪ захват билирубина из крови печеночной клеткой, ▪ связывание билирубина с глюкуроновой кислотой, ▪ выделение связанного билирубина из печеночной клетки в желчные капилляры. • Непрямой билирубин, образованный в результате распада гемоглобина переносится в мембраны эндоплазматической сети, где связывается с глюкороновой кислотой, это делает его растворимым в воде и обеспечивает переход в желчь, фильтрацию в почках и быструю (прямую реакцию с диазореактивом. • Он называется связанным, прямым, растворимым, конъюгированным.
• Печень выполняет три важнейших функции в обмене билирубина: ▪ захват билирубина из крови печеночной клеткой, ▪ связывание билирубина с глюкуроновой кислотой, ▪ выделение связанного билирубина из печеночной клетки в желчные капилляры. • Непрямой билирубин, образованный в результате распада гемоглобина переносится в мембраны эндоплазматической сети, где связывается с глюкороновой кислотой, это делает его растворимым в воде и обеспечивает переход в желчь, фильтрацию в почках и быструю (прямую реакцию с диазореактивом. • Он называется связанным, прямым, растворимым, конъюгированным.
 • Выделение билирубина в желчь – конечный этап обмена пигмента в печеночных клетках. • Билирубин выделяется из печени в желчь и выводится в тонкую кишку. Около 10% билирубина восстанавливается до уробилиногена на пути в тонкую кишку, во внепеченочных желчных ходах и желчном пузыре. • Из тонкой кишки часть образовавшегося уробилиногена всасывается ч/з кишечную стенку, попадает в портальную вену и током крови переносится в печень (печеночно-клеточная циркуляция уробилиногена), где полностью расщепляется и частично выделяется с мочой в виде уробилина.
• Выделение билирубина в желчь – конечный этап обмена пигмента в печеночных клетках. • Билирубин выделяется из печени в желчь и выводится в тонкую кишку. Около 10% билирубина восстанавливается до уробилиногена на пути в тонкую кишку, во внепеченочных желчных ходах и желчном пузыре. • Из тонкой кишки часть образовавшегося уробилиногена всасывается ч/з кишечную стенку, попадает в портальную вену и током крови переносится в печень (печеночно-клеточная циркуляция уробилиногена), где полностью расщепляется и частично выделяется с мочой в виде уробилина.
 • Уровень уробилиногена в моче у здоровых людей невысок (приблизительно 4 мг/сутки). Основное же количество уробилиногена из тонкой кишки попадает в толстую восстанавливается до стеркобилиногена, который выделяется с калом. превратившись в прямой кишке и на воздухе в стеркобилин. • Количество фекального стеркобилина варьирует от 47 до 276 мг в сутки • Соотношении стеркобилина к уробилину составляет 10: 1 или 20: 1. • Билирубин в моче (желчные пигменты) появляются только при повышении в крови прямого билирубина.
• Уровень уробилиногена в моче у здоровых людей невысок (приблизительно 4 мг/сутки). Основное же количество уробилиногена из тонкой кишки попадает в толстую восстанавливается до стеркобилиногена, который выделяется с калом. превратившись в прямой кишке и на воздухе в стеркобилин. • Количество фекального стеркобилина варьирует от 47 до 276 мг в сутки • Соотношении стеркобилина к уробилину составляет 10: 1 или 20: 1. • Билирубин в моче (желчные пигменты) появляются только при повышении в крови прямого билирубина.
 • Желтуха обусловлена отложением желтого пигмента билирубина в коже, склерах и слизистых оболочках при повышенном содержании его в крови. • Желтушное окрашивание кожи наблюдается при отложении других красящих веществ – кератина – при избыточном потреблении продуктов его содержащих – морковь, апельсины, но каротин не окрашивает слизистые и склеры. • Желтуха может быть: ◦ надпеченочная (гемолитическая) ◦ печеночная (паренхиматозная) ◦ подпеченочная (механическая)
• Желтуха обусловлена отложением желтого пигмента билирубина в коже, склерах и слизистых оболочках при повышенном содержании его в крови. • Желтушное окрашивание кожи наблюдается при отложении других красящих веществ – кератина – при избыточном потреблении продуктов его содержащих – морковь, апельсины, но каротин не окрашивает слизистые и склеры. • Желтуха может быть: ◦ надпеченочная (гемолитическая) ◦ печеночная (паренхиматозная) ◦ подпеченочная (механическая)
 НАДПЕЧЕНОЧНАЯ (ГЕМОЛИТИЧЕСКАЯ) ЖЕЛТУХА • Надпеченочная желтуха обусловлена чрезмерным распадом эритроцитов и значительным образованием свободного билирубина, который не успевает связываться в печени и накапливается в крови. • Гемолитическая желтуха является верным симптомом гемолитических анемий, одним из симптомов В 12 дефицитной анемии, малярии, застойном септическом эндокардите, инфаркте различных органов (чаще легких).
НАДПЕЧЕНОЧНАЯ (ГЕМОЛИТИЧЕСКАЯ) ЖЕЛТУХА • Надпеченочная желтуха обусловлена чрезмерным распадом эритроцитов и значительным образованием свободного билирубина, который не успевает связываться в печени и накапливается в крови. • Гемолитическая желтуха является верным симптомом гемолитических анемий, одним из симптомов В 12 дефицитной анемии, малярии, застойном септическом эндокардите, инфаркте различных органов (чаще легких).
 • При гемолитической желтухе кожа обычная лимонно – желтого цвета. Кожного зуда не бывает. • В крови повышается количество билирубина за счет непрямого. • Билирубин в моче отсутствует, но моча значительно пигментирована за счет резко возросшего уробилиногена, испражнения насыщенного темного цвета, в следствии повышенного содержания стеркобилиногена. • Соотношение стеркобилина к уробилину 300: 1 или даже 500: 1.
• При гемолитической желтухе кожа обычная лимонно – желтого цвета. Кожного зуда не бывает. • В крови повышается количество билирубина за счет непрямого. • Билирубин в моче отсутствует, но моча значительно пигментирована за счет резко возросшего уробилиногена, испражнения насыщенного темного цвета, в следствии повышенного содержания стеркобилиногена. • Соотношение стеркобилина к уробилину 300: 1 или даже 500: 1.
 ПЕЧЕНОЧНАЯ (ПАРЕНХИМАТОЗНАЯ) ЖЕЛТУХА • Печеночная желтуха обусловлена нарушением захвата, связывания и выделения билирубина печенью изолировано или комбинировано, что может быть при: • синдроме Жильбера, • приобретенных хронических гепатитах, • Циррозах печени, • вирусных гепатитах, • лептоспирозе, • отравлении грибами и другими печеночными ядами, • синдроме Дабина-Джонсона • синдроме Ротора.
ПЕЧЕНОЧНАЯ (ПАРЕНХИМАТОЗНАЯ) ЖЕЛТУХА • Печеночная желтуха обусловлена нарушением захвата, связывания и выделения билирубина печенью изолировано или комбинировано, что может быть при: • синдроме Жильбера, • приобретенных хронических гепатитах, • Циррозах печени, • вирусных гепатитах, • лептоспирозе, • отравлении грибами и другими печеночными ядами, • синдроме Дабина-Джонсона • синдроме Ротора.
 • Кожные покровы при печеночной желтухе имеют шафраново – желтый с красноватым оттенком цвет. • Кожный зуд бывает не часто. В сыворотке крови повышается содержание билирубина за счет обоих фракций. • Моча цвета пива, за счет появления желчных кислот. Уменьшается выделение стеркобилина с калом, т. к. меньше билирубина выделяется печенью в кишечник. • Соотношение стеркобилиногена к уробилиногену в тяжелых случаях достигает 1: 1.
• Кожные покровы при печеночной желтухе имеют шафраново – желтый с красноватым оттенком цвет. • Кожный зуд бывает не часто. В сыворотке крови повышается содержание билирубина за счет обоих фракций. • Моча цвета пива, за счет появления желчных кислот. Уменьшается выделение стеркобилина с калом, т. к. меньше билирубина выделяется печенью в кишечник. • Соотношение стеркобилиногена к уробилиногену в тяжелых случаях достигает 1: 1.
 ПОДПЕЧЕНОЧНАЯ (МЕХАНИЧЕСКАЯ) ЖЕЛТУХА • Подпеченочная или механическая желтуха – по существу холестатическая, но препятствие оттоку желчи находится во внепеченочных желчевыводящих путях, обычный желчный проток. • Чаще всего это конкременты, опухоли и стриктуры (рак головки поджелудочной железы, рак фатерова соска). • В результате нарушения оттока желчи билирубин диффундирует в печеночные клетки, а так же обратно в кровь.
ПОДПЕЧЕНОЧНАЯ (МЕХАНИЧЕСКАЯ) ЖЕЛТУХА • Подпеченочная или механическая желтуха – по существу холестатическая, но препятствие оттоку желчи находится во внепеченочных желчевыводящих путях, обычный желчный проток. • Чаще всего это конкременты, опухоли и стриктуры (рак головки поджелудочной железы, рак фатерова соска). • В результате нарушения оттока желчи билирубин диффундирует в печеночные клетки, а так же обратно в кровь.
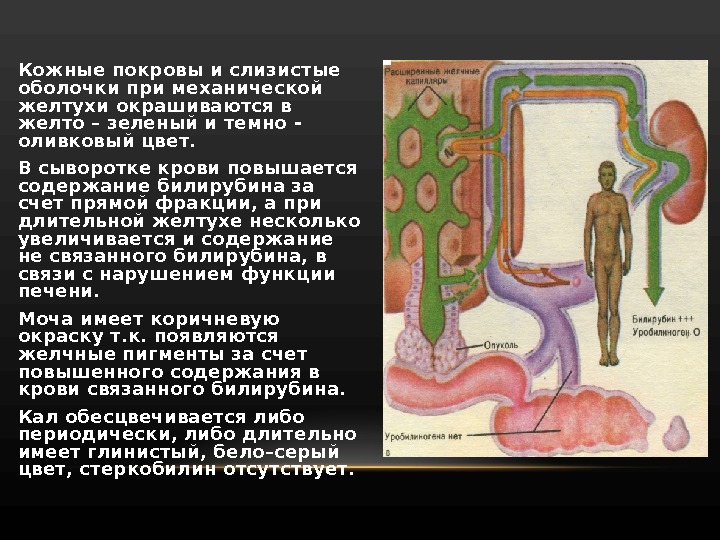
 • Кожные покровы и слизистые оболочки при механической желтухи окрашиваются в желто – зеленый и темно — оливковый цвет. • В сыворотке крови повышается содержание билирубина за счет прямой фракции, а при длительной желтухе несколько увеличивается и содержание не связанного билирубина, в связи с нарушением функции печени. • Моча имеет коричневую окраску т. к. появляются желчные пигменты за счет повышенного содержания в крови связанного билирубина. • Кал обесцвечивается либо периодически, либо длительно имеет глинистый, бело–серый цвет, стеркобилин отсутствует.
• Кожные покровы и слизистые оболочки при механической желтухи окрашиваются в желто – зеленый и темно — оливковый цвет. • В сыворотке крови повышается содержание билирубина за счет прямой фракции, а при длительной желтухе несколько увеличивается и содержание не связанного билирубина, в связи с нарушением функции печени. • Моча имеет коричневую окраску т. к. появляются желчные пигменты за счет повышенного содержания в крови связанного билирубина. • Кал обесцвечивается либо периодически, либо длительно имеет глинистый, бело–серый цвет, стеркобилин отсутствует.
 СИНДРОМ ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ (ПГ). • Портальная гипертензия – это внешнее давление в системе воротной вены. • У здоровых людей давление в системе портальной вены составляет 7 – 10 мм рт. ст. , а при портальной гипертензии оно превышает 20 мм ртутного столба. Различают три вида портальной гипертензии: • — надпеченочная ПГ; • — подпеченочная ПГ; • — внутрипеченочную ПГ.
СИНДРОМ ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ (ПГ). • Портальная гипертензия – это внешнее давление в системе воротной вены. • У здоровых людей давление в системе портальной вены составляет 7 – 10 мм рт. ст. , а при портальной гипертензии оно превышает 20 мм ртутного столба. Различают три вида портальной гипертензии: • — надпеченочная ПГ; • — подпеченочная ПГ; • — внутрипеченочную ПГ.
 • Надпеченочная ПГ развивается в результате полного или частичного блока печеночных вен (тромбоз) – болезнь Бадда-Киари или при сдавлении печеночных вен опухолью, рубцами, лимфатическими узлами (встречается в 2 -5% случаев). • Подпеченочная форма ПГ развивается за счет полной или частичной блокады воротной вены и ее крупных ветвей, которая возникает при травме живота, при сдавливании воротной вены в результате карциномы или кисты поджелудочной железы (встречается в 10 -12% случаев).
• Надпеченочная ПГ развивается в результате полного или частичного блока печеночных вен (тромбоз) – болезнь Бадда-Киари или при сдавлении печеночных вен опухолью, рубцами, лимфатическими узлами (встречается в 2 -5% случаев). • Подпеченочная форма ПГ развивается за счет полной или частичной блокады воротной вены и ее крупных ветвей, которая возникает при травме живота, при сдавливании воротной вены в результате карциномы или кисты поджелудочной железы (встречается в 10 -12% случаев).
 • Внутрипеченочная форма ПГ развивается в следствии поражения венозного русла в печени, возникает внутрипеченочный блок, что может быть при циррозах печени и реже при других ее поражениях: паразитарных инвазиях, внутрипеченочных опухолях или врожденных аномалиях портального русла в печени (встречается в 80 -87% случаев). • Причиной повышения давления в печеночной вене при циррозах является дезорганизация структуры внутрипеченочных долек в следствие фиброза и в большей степени, в результате узловой регенерации печеночной ткани. Повышение давления в системе портальной вены обуславливает раскрытие или расширение ранее имеющихся коллатералей.
• Внутрипеченочная форма ПГ развивается в следствии поражения венозного русла в печени, возникает внутрипеченочный блок, что может быть при циррозах печени и реже при других ее поражениях: паразитарных инвазиях, внутрипеченочных опухолях или врожденных аномалиях портального русла в печени (встречается в 80 -87% случаев). • Причиной повышения давления в печеночной вене при циррозах является дезорганизация структуры внутрипеченочных долек в следствие фиброза и в большей степени, в результате узловой регенерации печеночной ткани. Повышение давления в системе портальной вены обуславливает раскрытие или расширение ранее имеющихся коллатералей.
 • Существует три группы естественных портокавальных анастомозов: • В зоне геморроидальных венных сплетений – анастомозы между нижней брыжеечной веной и геморроидальными венами, впадающими в нижнюю полую вену – портокавальные. При ПГ развиваются геморроидальные узлы, разрыв некоторых, не редко, вызывает прямокишечные кровотечения. • В зоне пищеводно – желудочных сплетений – путь через левую желудочную вену, пищеводное сплетение и полунепарную вену в верхнюю полую вену – кава-кавальные анастомозы. При выраженной ПГ в нижней части пищевода и образуются значительные варикозные вены, которые при травме дают тяжелое кровотечение. • В системе околопупочных вен анастомозирующих с венами брюшной стенки и диафрагмы, несущими кровь в верхнюю и нижнюю полые вены – кава-кавальные анастомозы При ПГ расширеные и расходящиеся в разные стороны вены, образуют вокруг пупка своеобразную картину так называемую «голову медузы» .
• Существует три группы естественных портокавальных анастомозов: • В зоне геморроидальных венных сплетений – анастомозы между нижней брыжеечной веной и геморроидальными венами, впадающими в нижнюю полую вену – портокавальные. При ПГ развиваются геморроидальные узлы, разрыв некоторых, не редко, вызывает прямокишечные кровотечения. • В зоне пищеводно – желудочных сплетений – путь через левую желудочную вену, пищеводное сплетение и полунепарную вену в верхнюю полую вену – кава-кавальные анастомозы. При выраженной ПГ в нижней части пищевода и образуются значительные варикозные вены, которые при травме дают тяжелое кровотечение. • В системе околопупочных вен анастомозирующих с венами брюшной стенки и диафрагмы, несущими кровь в верхнюю и нижнюю полые вены – кава-кавальные анастомозы При ПГ расширеные и расходящиеся в разные стороны вены, образуют вокруг пупка своеобразную картину так называемую «голову медузы» .
 • Повышение давления в системе ВП приводит к появлению спленомегалии, при этом может развиться гепатолиенальный синдром. • Портальная гипертензия сопровождается асцитом, который в некоторых случаях при поражении печени может быть обусловлен и другими причинами – гипоальбуминемией и гиперальдостеронизмом, вследствие печеночно-клеточной недостаточности. • Чаще же имеется несколько факторов обуславливающих развитие асцита у больных с поражением печени. • Поступление крови из кишечника через анастомозы в общий кровоток минуя печень, может привести к интоксикации, проявлениями которой могут оказаться острая или хроническая энцефалопатия. • Ранними проявлениями портальной недостаточности может быть метиоризм и диспепсические расстройства – тошнота, снижение аппетита.
• Повышение давления в системе ВП приводит к появлению спленомегалии, при этом может развиться гепатолиенальный синдром. • Портальная гипертензия сопровождается асцитом, который в некоторых случаях при поражении печени может быть обусловлен и другими причинами – гипоальбуминемией и гиперальдостеронизмом, вследствие печеночно-клеточной недостаточности. • Чаще же имеется несколько факторов обуславливающих развитие асцита у больных с поражением печени. • Поступление крови из кишечника через анастомозы в общий кровоток минуя печень, может привести к интоксикации, проявлениями которой могут оказаться острая или хроническая энцефалопатия. • Ранними проявлениями портальной недостаточности может быть метиоризм и диспепсические расстройства – тошнота, снижение аппетита.
 • Клинические проявления. • Наиболее ранние симптомы портальной гипертензии: метеоризм, чувство переполненности кишечника, тошнота, боли по всему животу, снижение аппетита. • «Симптомы плохого питания» — плохо выраженная подкожная клетчатка, сухая кожа, атрофия мускулатуры. • При прогрессировании портальной гипертензии развивается асцит, отеки ног, кровотечения из варикозно-расширенных вен пищевода, прямой кишки. • Спленомегалия. • Гепатомегалия. • При прогрессировании – печеночная энцефалопатия. •
• Клинические проявления. • Наиболее ранние симптомы портальной гипертензии: метеоризм, чувство переполненности кишечника, тошнота, боли по всему животу, снижение аппетита. • «Симптомы плохого питания» — плохо выраженная подкожная клетчатка, сухая кожа, атрофия мускулатуры. • При прогрессировании портальной гипертензии развивается асцит, отеки ног, кровотечения из варикозно-расширенных вен пищевода, прямой кишки. • Спленомегалия. • Гепатомегалия. • При прогрессировании – печеночная энцефалопатия. •
 • Диагностика портальной гипертензии на УЗИ – увеличение диаметра воротной и селезеночной вен. • ЭФГДС – варикозное расширение вен пищевода. • Ректороманоскопия – для выявления варикозно-расширенных вен при развитии коллатералей по мезентерико-геморраидальному пути. • Лечение: Для устранения портальной гипертензии, которая опасна пищеводно- желудочным и геморроидальным кровотечением больным хирургическим путем накладывают соустье между системой воротной и нижней полой веной
• Диагностика портальной гипертензии на УЗИ – увеличение диаметра воротной и селезеночной вен. • ЭФГДС – варикозное расширение вен пищевода. • Ректороманоскопия – для выявления варикозно-расширенных вен при развитии коллатералей по мезентерико-геморраидальному пути. • Лечение: Для устранения портальной гипертензии, которая опасна пищеводно- желудочным и геморроидальным кровотечением больным хирургическим путем накладывают соустье между системой воротной и нижней полой веной
 ГЕМОРРАГИЧЕСКИЙ СИНДРОМ. • Геморрагический диатез – появление кровоизлияний и кровоподтеков на коже и в подкожной клетчатке, кровоточивость десен, носовых кровотечений, гематурий, в отдельных случаях маточных, геморроидальных кровотечений, а так же из варикозно-расширенных вен пищевода и желудка. • В основе этого синдрома лежат три группы причин: Уменьшение синтеза факторов свертывания крови. Повышенное потребление факторов свертывания. Уменьшение количества и изменение функциональных свойств тромбоцитов.
ГЕМОРРАГИЧЕСКИЙ СИНДРОМ. • Геморрагический диатез – появление кровоизлияний и кровоподтеков на коже и в подкожной клетчатке, кровоточивость десен, носовых кровотечений, гематурий, в отдельных случаях маточных, геморроидальных кровотечений, а так же из варикозно-расширенных вен пищевода и желудка. • В основе этого синдрома лежат три группы причин: Уменьшение синтеза факторов свертывания крови. Повышенное потребление факторов свертывания. Уменьшение количества и изменение функциональных свойств тромбоцитов.
 • Снижение факторов свертывания крови важная причина геморрагического диатеза. В начале снижается синтез фактора VII , затем II , IX , при тяжелой печеночно-клеточной недостаточности уменьшается синтез факторов I , V , XII. • Повышенное потребление факторов свертывания. Выделение из поврежденных клеток печени в кровь тромбопластических веществ ведет диссеминированному внутрисосудистому свертыванию крови с фибринолизином и образованием тромбоцитарных тромбов. Эти процессы требуют повышенного количества I , II , VII IX , XI факторов свертывания в результате чего развивается коагуляция потребления. • Уменьшение количества тромбоцитов так же имеет существенное значение для развития геморрагического диатеза при болезнях печени. Наиболее частой причиной тромбоцитопении является гиперспленизм и диссеминированное внутрисосудистое свертывание крови
• Снижение факторов свертывания крови важная причина геморрагического диатеза. В начале снижается синтез фактора VII , затем II , IX , при тяжелой печеночно-клеточной недостаточности уменьшается синтез факторов I , V , XII. • Повышенное потребление факторов свертывания. Выделение из поврежденных клеток печени в кровь тромбопластических веществ ведет диссеминированному внутрисосудистому свертыванию крови с фибринолизином и образованием тромбоцитарных тромбов. Эти процессы требуют повышенного количества I , II , VII IX , XI факторов свертывания в результате чего развивается коагуляция потребления. • Уменьшение количества тромбоцитов так же имеет существенное значение для развития геморрагического диатеза при болезнях печени. Наиболее частой причиной тромбоцитопении является гиперспленизм и диссеминированное внутрисосудистое свертывание крови
 ГЕПАТОЛИЕНАЛЬНЫЙ СИНДРОМ (ГЛС) • Гепатомегалия при заболеваниях печени обычно сочетается с увеличением селезенки, сочетание поражения печени и селезенки объясняется тесной связью обоих органов и системой воротной вены, близостью их иннервации и путей лимфаоттока. • ГЛС наблюдается при: • острых и хронических заболеваниях печени, • врожденных и приобретенных дефектах сосудов портальной системы, • некоторых болезнях нарушения обмена веществ, • системных заболеваниях крови, • хронических инфекциях и паразитарных заболеваниях, • инфекционном мононуклеозе, • брюшном тифе, • болезнях ССС.
ГЕПАТОЛИЕНАЛЬНЫЙ СИНДРОМ (ГЛС) • Гепатомегалия при заболеваниях печени обычно сочетается с увеличением селезенки, сочетание поражения печени и селезенки объясняется тесной связью обоих органов и системой воротной вены, близостью их иннервации и путей лимфаоттока. • ГЛС наблюдается при: • острых и хронических заболеваниях печени, • врожденных и приобретенных дефектах сосудов портальной системы, • некоторых болезнях нарушения обмена веществ, • системных заболеваниях крови, • хронических инфекциях и паразитарных заболеваниях, • инфекционном мононуклеозе, • брюшном тифе, • болезнях ССС.
 • Болезням печени принадлежит основная роль в развитии гепатолиенального синдрома, более чем в 90% случаев ГЛС обусловлен патологией печени. • Основным симптомом ГЛС служит увеличение печени и селезенки. • Размеры органов значительно варьируют при заболеваниях печени. Консистенция обоих органов плотная, величина колеблется в зависимости от стадии заболевания. • На далеко зашедшей стадии цирроза печень уменьшается. Селезенка увеличивается позднее чем печень. • В периоды обострения отмечается болезненность при пальпации органов. • Для ГЛС характерны анемия, лейкоцитопения и тромбоцитопения т. е. панцитопения, что происходит в результате повышенного разрушения форменных элементов крови прохождении через селезенку.
• Болезням печени принадлежит основная роль в развитии гепатолиенального синдрома, более чем в 90% случаев ГЛС обусловлен патологией печени. • Основным симптомом ГЛС служит увеличение печени и селезенки. • Размеры органов значительно варьируют при заболеваниях печени. Консистенция обоих органов плотная, величина колеблется в зависимости от стадии заболевания. • На далеко зашедшей стадии цирроза печень уменьшается. Селезенка увеличивается позднее чем печень. • В периоды обострения отмечается болезненность при пальпации органов. • Для ГЛС характерны анемия, лейкоцитопения и тромбоцитопения т. е. панцитопения, что происходит в результате повышенного разрушения форменных элементов крови прохождении через селезенку.
 СИНДРОМ ЦИТОЛИЗА ПЕЧЕНОЧНЫХ КЛЕТОК. • Синдром цитолиза печеночных клеток или нарушение целостности гепатоцитов очень часто сочетается с печеночно-клеточной недостаточностью. Синдром цитолиза возникает при наличии некроза печеночных клеток или тяжелом повреждении их мембран и характеризуется выходом внутриклеточных ферментов, в большом количестве в плазму крови. • При цитолизе гепатоцитов наблюдается повышение активности A л. А T и A с. А T , γ- глютамитранспептидазы, ЛДГ, в основном за счет пятой фракции. • Отмечается повышение уровня железа и цианокоболамина. • При выраженном цитолитическом синдроме возможно появление субфибрилетета и даже лихорадки, • Нередко развивается умеренная желтуха, обусловленная содержанием в крови прямого и непрямого билирубина.
СИНДРОМ ЦИТОЛИЗА ПЕЧЕНОЧНЫХ КЛЕТОК. • Синдром цитолиза печеночных клеток или нарушение целостности гепатоцитов очень часто сочетается с печеночно-клеточной недостаточностью. Синдром цитолиза возникает при наличии некроза печеночных клеток или тяжелом повреждении их мембран и характеризуется выходом внутриклеточных ферментов, в большом количестве в плазму крови. • При цитолизе гепатоцитов наблюдается повышение активности A л. А T и A с. А T , γ- глютамитранспептидазы, ЛДГ, в основном за счет пятой фракции. • Отмечается повышение уровня железа и цианокоболамина. • При выраженном цитолитическом синдроме возможно появление субфибрилетета и даже лихорадки, • Нередко развивается умеренная желтуха, обусловленная содержанием в крови прямого и непрямого билирубина.
 СИНДРОМ ХОЛЕСТАЗА. • Синдром холестаза. • Обусловлен нарушением желчевыделительной функции печеночных клеток с нарушением образования желчной мицеллы и поражением мельчайших желчных ходов. • Для синдром холестаза характерно: • 1. Повышение активности ферментных маркеров холестаза – щелочной фосфолипазы, лейцин-аминопептидазы, • 5 -нуклеотидазы, γ- глютаминтранспептидазы. • 2. Гиперхолистеринемия, повышение уровня фосфолипидов, β — липопротеидов, желчных кислот. • 3. Гипербилирубинемия.
СИНДРОМ ХОЛЕСТАЗА. • Синдром холестаза. • Обусловлен нарушением желчевыделительной функции печеночных клеток с нарушением образования желчной мицеллы и поражением мельчайших желчных ходов. • Для синдром холестаза характерно: • 1. Повышение активности ферментных маркеров холестаза – щелочной фосфолипазы, лейцин-аминопептидазы, • 5 -нуклеотидазы, γ- глютаминтранспептидазы. • 2. Гиперхолистеринемия, повышение уровня фосфолипидов, β — липопротеидов, желчных кислот. • 3. Гипербилирубинемия.
 СИНДРОМ ПЕЧЕНОЧНО-КЛЕТОЧНОЙ НЕДОСТАТОЧНОСТИ. • Синдром печеночно-клеточной недостаточности. • Отражает состояние основных функциональных проб печени, оценивающих поглатительно-экскреторно-метаболизтирующу ю и синтетическую функцию печени. • Для них характерно: • А) уменьшение содержания в сыворотке крови общего белка, особенно альбуминов, уменьшение протромбина, холестерина, повышение активности холинестеразы. • Б) снижение клиренса антипирина. Уменьшение содержания в сыворотке крови II , VII факторов свертывания. • В) задержка выделения бромсульфалена, гипербилирубинемия с прямой реакцией. • Г) повышение содержания аминов, фенолов, аминокислот.
СИНДРОМ ПЕЧЕНОЧНО-КЛЕТОЧНОЙ НЕДОСТАТОЧНОСТИ. • Синдром печеночно-клеточной недостаточности. • Отражает состояние основных функциональных проб печени, оценивающих поглатительно-экскреторно-метаболизтирующу ю и синтетическую функцию печени. • Для них характерно: • А) уменьшение содержания в сыворотке крови общего белка, особенно альбуминов, уменьшение протромбина, холестерина, повышение активности холинестеразы. • Б) снижение клиренса антипирина. Уменьшение содержания в сыворотке крови II , VII факторов свертывания. • В) задержка выделения бромсульфалена, гипербилирубинемия с прямой реакцией. • Г) повышение содержания аминов, фенолов, аминокислот.
 ИММУНОВОСПАЛИТЕЛЬНЫЙ СИНДРОМ. • Обусловлен сенсибилизацией клеток иммунокомпетентной ткани и активацией ретикулогистеоцитарной системы. • Для этого синдрома характерно: • А) повышение уровня γ- глобулинов сыворотки крови, • Б) изменение белково–осадочных проб (тимоловой, сулемовой, ) • В) Повышение уровня Jg Q , Jg M , Jg A , появление неспецифических антител в том числе и к ДНК, гладкомышечных волокнам митохондрий, изменение количества и соотношения субпопуляций лимфоцитов (хелперов и супрессоров).
ИММУНОВОСПАЛИТЕЛЬНЫЙ СИНДРОМ. • Обусловлен сенсибилизацией клеток иммунокомпетентной ткани и активацией ретикулогистеоцитарной системы. • Для этого синдрома характерно: • А) повышение уровня γ- глобулинов сыворотки крови, • Б) изменение белково–осадочных проб (тимоловой, сулемовой, ) • В) Повышение уровня Jg Q , Jg M , Jg A , появление неспецифических антител в том числе и к ДНК, гладкомышечных волокнам митохондрий, изменение количества и соотношения субпопуляций лимфоцитов (хелперов и супрессоров).
 ПЕЧЁНОЧНОКЛЕТОЧНАЯ НЕДОСТАТОЧНОСТЬ • Печёночноклеточная недостаточность может осложнять течение почти всех заболеваний печени. • Она может развиться при вирусном гепатите, циррозах, жировой печени беременных, лекарственном гепатите, передозировке некоторых препаратов (например, парацетамола), перевязке печёночной артерии вблизи печени, окклюзии печёночных вен. • Её возникновению может способствовать недостаточность кровообращения, сопровождающаяся артериальной гипотензией, особенно у больных циррозом печени.
ПЕЧЁНОЧНОКЛЕТОЧНАЯ НЕДОСТАТОЧНОСТЬ • Печёночноклеточная недостаточность может осложнять течение почти всех заболеваний печени. • Она может развиться при вирусном гепатите, циррозах, жировой печени беременных, лекарственном гепатите, передозировке некоторых препаратов (например, парацетамола), перевязке печёночной артерии вблизи печени, окклюзии печёночных вен. • Её возникновению может способствовать недостаточность кровообращения, сопровождающаяся артериальной гипотензией, особенно у больных циррозом печени.
 • Печёночноклеточная недостаточность при хроническом холестазе (первичный билиарный цирроз или злокачественная опухоль печени, а также острый холангит) может привести к фатальному исходу. К её диагностике при острой обструкции жёлчных путей следует подходить с осторожностью. • Хотя некоторые проявления синдрома печёночно-клеточной недостаточности при различных заболеваниях могут отличаться, в целом его клиническая картина и лечение одинаковы и не зависят от этиологии. • Постоянные морфологические признаки при этом синдроме отсутствуют; особенно важно, что при нём не всегда выявляется некроз. • Следовательно, синдром печёночно-клеточной недостаточности является скорее функциональным, чем анатомическим.
• Печёночноклеточная недостаточность при хроническом холестазе (первичный билиарный цирроз или злокачественная опухоль печени, а также острый холангит) может привести к фатальному исходу. К её диагностике при острой обструкции жёлчных путей следует подходить с осторожностью. • Хотя некоторые проявления синдрома печёночно-клеточной недостаточности при различных заболеваниях могут отличаться, в целом его клиническая картина и лечение одинаковы и не зависят от этиологии. • Постоянные морфологические признаки при этом синдроме отсутствуют; особенно важно, что при нём не всегда выявляется некроз. • Следовательно, синдром печёночно-клеточной недостаточности является скорее функциональным, чем анатомическим.
 • Он состоит из различных сочетаний перечисленных ниже признаков. • • Общие симптомы. • • Желтуха. • • Гипердинамический тип кровообращения и цианоз. • • Лихорадка и септицемия. • • Неврологические нарушения (печёночная энцефалопатия). • • Асцит. • • Нарушения азотистого обмена. • • Кожные и эндокринные изменения. • • Нарушения свёртывания крови
• Он состоит из различных сочетаний перечисленных ниже признаков. • • Общие симптомы. • • Желтуха. • • Гипердинамический тип кровообращения и цианоз. • • Лихорадка и септицемия. • • Неврологические нарушения (печёночная энцефалопатия). • • Асцит. • • Нарушения азотистого обмена. • • Кожные и эндокринные изменения. • • Нарушения свёртывания крови
 • Общие симптомы • Наиболее характерны слабость и быстрая утомляемость. Возможно истощение, связанное с нарушением обмена веществ • Лихорадка и септицемия • Постоянная лихорадка, обычно не превышающая 38 °С, выявляется приблизительно в трети случаев декомпенсированного цирроза печени. • На неё не влияют приём антибиотиков и уменьшение потребления белка. Вероятно, лихорадка связана не только с поражением печени. В её развитии (по крайней мере у страдающих алкоголизмом) могут играть роль цитокины, например фактор некроза опухолей. • Цитокины, выделяющиеся при воспалительных реакциях, приводят к некоторым нежелательным эффектам, в частности к вазодилатации, активации эндотелия и полиорганной недостаточности. • Печень человека стерильна, а в портальной крови микроорганизмы выявляются только в редких случаях. Однако при циррозе печени бактерии, особенно кишечные, могут попадать в системный кровоток либо через дефектный печёночный фильтр, либо через портосистемные коллатерали.
• Общие симптомы • Наиболее характерны слабость и быстрая утомляемость. Возможно истощение, связанное с нарушением обмена веществ • Лихорадка и септицемия • Постоянная лихорадка, обычно не превышающая 38 °С, выявляется приблизительно в трети случаев декомпенсированного цирроза печени. • На неё не влияют приём антибиотиков и уменьшение потребления белка. Вероятно, лихорадка связана не только с поражением печени. В её развитии (по крайней мере у страдающих алкоголизмом) могут играть роль цитокины, например фактор некроза опухолей. • Цитокины, выделяющиеся при воспалительных реакциях, приводят к некоторым нежелательным эффектам, в частности к вазодилатации, активации эндотелия и полиорганной недостаточности. • Печень человека стерильна, а в портальной крови микроорганизмы выявляются только в редких случаях. Однако при циррозе печени бактерии, особенно кишечные, могут попадать в системный кровоток либо через дефектный печёночный фильтр, либо через портосистемные коллатерали.
 • При терминальной печёночно-клеточной недостаточности часто развивается септицемия. Она обусловлена многими факторами: нарушением функции клеток Купффера и полиморфноядерных лейкоцитов, снижением содержания в сыворотке различных факторов (фибронектина, опсонинов и хемоаттрактантов, в том числе компонентов комплемента). • Системная токсемия кишечного происхождения нарушает поглотительную функцию ретикулоэндотелиальной системы и, кроме того, повреждает почки. • Все эти факторы приводят к эпизодам бактериемии с положительной гемокультурой. Особенно большое значение это имеет при спонтанном бактериальном перитоните, который при циррозе печени с асцитом развивается в 75% случаев.
• При терминальной печёночно-клеточной недостаточности часто развивается септицемия. Она обусловлена многими факторами: нарушением функции клеток Купффера и полиморфноядерных лейкоцитов, снижением содержания в сыворотке различных факторов (фибронектина, опсонинов и хемоаттрактантов, в том числе компонентов комплемента). • Системная токсемия кишечного происхождения нарушает поглотительную функцию ретикулоэндотелиальной системы и, кроме того, повреждает почки. • Все эти факторы приводят к эпизодам бактериемии с положительной гемокультурой. Особенно большое значение это имеет при спонтанном бактериальном перитоните, который при циррозе печени с асцитом развивается в 75% случаев.
 • Инфекции мочевых путей у больных циррозом печени развиваются особенно часто; обычно они обусловлены грамотрицательными бактериями. Некоторое значение имеют мочевые катетеры, оставляемые на длительный срок. • Пневмония особенно часто развивается у больных алкоголизмом. Внебольничные инфекции обычно хорошо поддаются лечению. • Госпитальные инфекции протекают более тяжело. • Кроме того, возможны другие инфекционные осложнения, включая лимфангаит и эндокардит. • При острой печёночной недостаточности инфекция развивается в 50% случаев, часто в мягких тканях, дыхательных или мочевых путях или в катетерах центральных вен. Клинически она может протекать атипично, без выраженной лихорадки, без озноба и лишь с небольшим лейкоцитозом. • Как при острой, так и при хронической печёночной недостаточности инфекции почти в двух третях случаев вызваны грамположительными бактериями, часто стафилококками; в трети случаев возбудителями являются грамотрицательные бактерии • Госпитальная смертность достигает 38%.
• Инфекции мочевых путей у больных циррозом печени развиваются особенно часто; обычно они обусловлены грамотрицательными бактериями. Некоторое значение имеют мочевые катетеры, оставляемые на длительный срок. • Пневмония особенно часто развивается у больных алкоголизмом. Внебольничные инфекции обычно хорошо поддаются лечению. • Госпитальные инфекции протекают более тяжело. • Кроме того, возможны другие инфекционные осложнения, включая лимфангаит и эндокардит. • При острой печёночной недостаточности инфекция развивается в 50% случаев, часто в мягких тканях, дыхательных или мочевых путях или в катетерах центральных вен. Клинически она может протекать атипично, без выраженной лихорадки, без озноба и лишь с небольшим лейкоцитозом. • Как при острой, так и при хронической печёночной недостаточности инфекции почти в двух третях случаев вызваны грамположительными бактериями, часто стафилококками; в трети случаев возбудителями являются грамотрицательные бактерии • Госпитальная смертность достигает 38%.
 • Прогностически неблагоприятными признаками являются отсутствие лихорадки, повышение уровня креатинина в сыворотке, значительный лейкоцитоз. • Рецидивирующая инфекция — грозный признак и является показанием к трансплантации печени. • При печёночной недостаточности проведению инвазивных процедур должна предшествовать профилактика антибиотиками. • При подозрении на инфекцию парентерально назначают антибиотики широкого спектра действия.
• Прогностически неблагоприятными признаками являются отсутствие лихорадки, повышение уровня креатинина в сыворотке, значительный лейкоцитоз. • Рецидивирующая инфекция — грозный признак и является показанием к трансплантации печени. • При печёночной недостаточности проведению инвазивных процедур должна предшествовать профилактика антибиотиками. • При подозрении на инфекцию парентерально назначают антибиотики широкого спектра действия.
 • Печёночный запах • Выдыхаемый больным воздух имеет сладковатый запах, слегка напоминающий запах фекалий; его можно сравнить с запахом от недавно вскрытого трупа или с мышиным запахом. Он развивается при тяжёлой печёночноклеточной болезни, особенно с выраженным коллатеральным кровообращением. • Печёночный запах имеет преимущественно кишечное происхождение, поскольку после дефекации или после изменения кишечной флоры антибиотиками широкого спектра действия он ослабевает. У больных с печёночной комой и с печёночным запахом в моче выявляется метилмеркаптан. • Это вещество образуется из метионина при подавлении нормального деметилирования поврежденной печенью и может выделяться с выдыхаемым воздухом. • При остром поражении печени печёночный запах, особенно распространяющийся на всю комнату, является неблагоприятным признаком; после его появления часто развивается кома. Он очень часто встречается при выраженном портоколлатеральном кровообращении и при этом не свидетельствует о столь неблагоприятном прогнозе. • Если причина комы неясна, выявление печёночного запаха может помочь диагностике.
• Печёночный запах • Выдыхаемый больным воздух имеет сладковатый запах, слегка напоминающий запах фекалий; его можно сравнить с запахом от недавно вскрытого трупа или с мышиным запахом. Он развивается при тяжёлой печёночноклеточной болезни, особенно с выраженным коллатеральным кровообращением. • Печёночный запах имеет преимущественно кишечное происхождение, поскольку после дефекации или после изменения кишечной флоры антибиотиками широкого спектра действия он ослабевает. У больных с печёночной комой и с печёночным запахом в моче выявляется метилмеркаптан. • Это вещество образуется из метионина при подавлении нормального деметилирования поврежденной печенью и может выделяться с выдыхаемым воздухом. • При остром поражении печени печёночный запах, особенно распространяющийся на всю комнату, является неблагоприятным признаком; после его появления часто развивается кома. Он очень часто встречается при выраженном портоколлатеральном кровообращении и при этом не свидетельствует о столь неблагоприятном прогнозе. • Если причина комы неясна, выявление печёночного запаха может помочь диагностике.
 ПЕЧЕНОЧНАЯ ЭНЦЕФАЛОПАТИЯ И КОМА. • Печеночная энцефалопатия развивается при острой и хронической печеночной недостаточности. • Патогенез печеночной недостаточности обусловлен прежде всего выпадением обезвреживающей функции печени и токсическим воздействием продуктов метаболизма азотистых соединений на мозг. • Они проникают из портального кровотока в мозг в следствии гибели паренхимы печени. Развивается печеночная энцефалопатия (ПЭП). • ПЭП связана с адсорбцией токсинов, появляющихся в кишечнике под воздействием бактериальной флоры на азотистые соединения. • Роль основных токсинов играют: аммиак, ароматические аминокислоты, а так же метионин, меркаптаны, образуемые при метаболизме метионина в кишечнике и производные фенола и индола.
ПЕЧЕНОЧНАЯ ЭНЦЕФАЛОПАТИЯ И КОМА. • Печеночная энцефалопатия развивается при острой и хронической печеночной недостаточности. • Патогенез печеночной недостаточности обусловлен прежде всего выпадением обезвреживающей функции печени и токсическим воздействием продуктов метаболизма азотистых соединений на мозг. • Они проникают из портального кровотока в мозг в следствии гибели паренхимы печени. Развивается печеночная энцефалопатия (ПЭП). • ПЭП связана с адсорбцией токсинов, появляющихся в кишечнике под воздействием бактериальной флоры на азотистые соединения. • Роль основных токсинов играют: аммиак, ароматические аминокислоты, а так же метионин, меркаптаны, образуемые при метаболизме метионина в кишечнике и производные фенола и индола.
 • Аммиак – продукт белкового обмена, в печень аммиак поступает из воротной вены и практически полный метаболизм аммиака и аминогрупп, аминокислот с образованием мочевины и глутамина происходит почти исключительно в печени во время первого пассажа крови, оттекающий из кишечника и поэтому • в норме в системной крови определяются лишь следы аммиака. • При ОПН содержание аммиака в крови повышается только при развитии массивных некрозов. • У больных с хронической печеночной недостаточностью аммиак поступает в кровь преимущественно по порто-кавальным анастомозам, по которым венозная кровь, обогащенная аммиаком и другими токсическими продуктами, попадает в систему большого круга кровообращения ускользая от метаболического печеночного процесса, также имеет значение нарушения способности печеночных клеток синтезировать мочевину.
• Аммиак – продукт белкового обмена, в печень аммиак поступает из воротной вены и практически полный метаболизм аммиака и аминогрупп, аминокислот с образованием мочевины и глутамина происходит почти исключительно в печени во время первого пассажа крови, оттекающий из кишечника и поэтому • в норме в системной крови определяются лишь следы аммиака. • При ОПН содержание аммиака в крови повышается только при развитии массивных некрозов. • У больных с хронической печеночной недостаточностью аммиак поступает в кровь преимущественно по порто-кавальным анастомозам, по которым венозная кровь, обогащенная аммиаком и другими токсическими продуктами, попадает в систему большого круга кровообращения ускользая от метаболического печеночного процесса, также имеет значение нарушения способности печеночных клеток синтезировать мочевину.
 • Важным звеном в патогенезе является снижение содержания аминокислот с разветвленной цепью в крови и спинномозговой жидкости. • У больных циррозом печени повышается метаболизм белка, для чего необходимо повышенное использование как источника энергии аминокислот – валина, лейцина, изолейцина, что сопровождается поступлением в кровь значительных количеств ароматических аминокислот – фенилаланина, тирозина и триптофана, метаболизм которых, в норме, происходит в печени. • Избыток ароматических аминокислот вызывает торможение ферментной системы. В результате чего в ЦНС накапливаются ложные нейротрансмиттеры. • К ним относятся – актопамин, фенилэтиламин, тирамин, фенилэтлколамин. • Ложные нейротрансмитторы, а так же серотанин (продукт метаболизма триптофана) приводят к угнетению нервной системы, истощению мозга и развитию энцефалопатии. • К факторам способствующим печеночной недостаточности относятся: повышенный распад белков, связанный с повышенным содержанием их в пище, применение седативных средств, алкоголя, диуретических препаратов, которые вызывают гипокалиемию или гипомагнезимию, хирургические вмешательства парацентез, сопутствующие инфекции.
• Важным звеном в патогенезе является снижение содержания аминокислот с разветвленной цепью в крови и спинномозговой жидкости. • У больных циррозом печени повышается метаболизм белка, для чего необходимо повышенное использование как источника энергии аминокислот – валина, лейцина, изолейцина, что сопровождается поступлением в кровь значительных количеств ароматических аминокислот – фенилаланина, тирозина и триптофана, метаболизм которых, в норме, происходит в печени. • Избыток ароматических аминокислот вызывает торможение ферментной системы. В результате чего в ЦНС накапливаются ложные нейротрансмиттеры. • К ним относятся – актопамин, фенилэтиламин, тирамин, фенилэтлколамин. • Ложные нейротрансмитторы, а так же серотанин (продукт метаболизма триптофана) приводят к угнетению нервной системы, истощению мозга и развитию энцефалопатии. • К факторам способствующим печеночной недостаточности относятся: повышенный распад белков, связанный с повышенным содержанием их в пище, применение седативных средств, алкоголя, диуретических препаратов, которые вызывают гипокалиемию или гипомагнезимию, хирургические вмешательства парацентез, сопутствующие инфекции.
 КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ ПЕЧЕНОЧНОЙ ЭНЦЕФАЛОПАТИИ. • Острая печеночная недостаточность очень быстро переходит в кому. • Энцефалопатия развивается как синдром хронической печеночной недостаточности. Она может быть эпизодической со спонтанным разрешением при исключении способствующих факторов или интермитирующей – длящейся многие месяцы и даже годы. • Клинические проявления печеночной недостаточности складываются из нарушений психики, нервно-мышечных расстройств и изменений ЭЭГ.
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ ПЕЧЕНОЧНОЙ ЭНЦЕФАЛОПАТИИ. • Острая печеночная недостаточность очень быстро переходит в кому. • Энцефалопатия развивается как синдром хронической печеночной недостаточности. Она может быть эпизодической со спонтанным разрешением при исключении способствующих факторов или интермитирующей – длящейся многие месяцы и даже годы. • Клинические проявления печеночной недостаточности складываются из нарушений психики, нервно-мышечных расстройств и изменений ЭЭГ.
 • Первая стадия продромальная. • У больных отмечается снижение аппетита, повышение кровоточивости, больные быстро худеют, снижается толерантность к алкоголю. • Появляются нарушения поведения, эмоциональная неустойчивость, чувство тревоги, тоски, апатии, эйфории, замедления мышления, ухудшение ориентировки, расстройство сна (сонливость днем, бессонница ночью). • Часто больные становятся слезливыми, слабодушными. • Замедляются психические реакции, речь, возможны некоторое психомоторное возбуждение, реже агрессивность с негативизмом, но ориентация и критика сохраняются. Отмечаются начальные нарушения речи, письма. • ЭЭГ, в большинстве случаев, нормальна.
• Первая стадия продромальная. • У больных отмечается снижение аппетита, повышение кровоточивости, больные быстро худеют, снижается толерантность к алкоголю. • Появляются нарушения поведения, эмоциональная неустойчивость, чувство тревоги, тоски, апатии, эйфории, замедления мышления, ухудшение ориентировки, расстройство сна (сонливость днем, бессонница ночью). • Часто больные становятся слезливыми, слабодушными. • Замедляются психические реакции, речь, возможны некоторое психомоторное возбуждение, реже агрессивность с негативизмом, но ориентация и критика сохраняются. Отмечаются начальные нарушения речи, письма. • ЭЭГ, в большинстве случаев, нормальна.
 • Вторая стадия – начинающаяся кома. Начинающаяся кома – характеризуется углублением психических и неврологических нарушений, характерных для первой стадии. • Нарастает общая слабость, диспепсические явления, метиоризм, боли в животе, полигиповитаминозы в результате нарушения усвояемости витаминов, лихорадка, желтуха, может появится гипопротеинемия, отеки, прогрессировать асцит. • Больные совершают бессмысленные поступки. Периодически возникают делириозные состояния с судорогами и моторным возбуждением. • Больнее становятся агрессивными, иногда опасными для окружающих. Рефлексы повышены. • У больных отмечается неопрятность. Развивается оглушенность, сознание частично спутано. Часто появляется лихорадка, возможна желтуха, печеночный запах изо рта, диспепсические нарушения. Дыхание учащается, становится глубоким. На ЭЭГ неравномерность α-ритма по частоте. •
• Вторая стадия – начинающаяся кома. Начинающаяся кома – характеризуется углублением психических и неврологических нарушений, характерных для первой стадии. • Нарастает общая слабость, диспепсические явления, метиоризм, боли в животе, полигиповитаминозы в результате нарушения усвояемости витаминов, лихорадка, желтуха, может появится гипопротеинемия, отеки, прогрессировать асцит. • Больные совершают бессмысленные поступки. Периодически возникают делириозные состояния с судорогами и моторным возбуждением. • Больнее становятся агрессивными, иногда опасными для окружающих. Рефлексы повышены. • У больных отмечается неопрятность. Развивается оглушенность, сознание частично спутано. Часто появляется лихорадка, возможна желтуха, печеночный запах изо рта, диспепсические нарушения. Дыхание учащается, становится глубоким. На ЭЭГ неравномерность α-ритма по частоте. •
 • III стадия – ступор. Выявляется комплекс общемозговых, пирамидальных и экстропирамидальных расстройств. • Выраженные нарушения сознания иногда прерываются кратковременным возбуждением. • Больные прибывают в длительном сне с периодическим пробуждением. • Отмечаются: недержание мочи, скрип зубов, тризм, фибриллярные подергивания мышц и судороги. • Лицо маскообразное, ригидность скелетной мускулатуры, замедление произвольных движений. • На ЭЭГ грубые изменения. ЭЭГ приближается к изолинии.
• III стадия – ступор. Выявляется комплекс общемозговых, пирамидальных и экстропирамидальных расстройств. • Выраженные нарушения сознания иногда прерываются кратковременным возбуждением. • Больные прибывают в длительном сне с периодическим пробуждением. • Отмечаются: недержание мочи, скрип зубов, тризм, фибриллярные подергивания мышц и судороги. • Лицо маскообразное, ригидность скелетной мускулатуры, замедление произвольных движений. • На ЭЭГ грубые изменения. ЭЭГ приближается к изолинии.
 • IV стадия – кома. • Сознание отсутствует. Раздражение на болевые рецепторы отсутствует. Ригидность мышц затылка и конечностей, зрачки расширены, реакция на свет исчезает, АД снижается, дыхание типа Кусмауля или Чейна – Стокса. • ССС – тахикардия, гипотония. • В крови – лейкоцитоз, анемия, гиперазотемия, высокий уровень желчных кислот, низкий уровень белка и альбуминов. • В большинстве случаев повышение содержания γ – глобулинов, повышается содержание факторов свертывания крови, холестерина, калия. • Нарастает уровень общего билирубина, снижается, ранее повышенные A л. А T , A с. А T , снижается содержание холинэстеразы, нарастает метаболический ацидоз.
• IV стадия – кома. • Сознание отсутствует. Раздражение на болевые рецепторы отсутствует. Ригидность мышц затылка и конечностей, зрачки расширены, реакция на свет исчезает, АД снижается, дыхание типа Кусмауля или Чейна – Стокса. • ССС – тахикардия, гипотония. • В крови – лейкоцитоз, анемия, гиперазотемия, высокий уровень желчных кислот, низкий уровень белка и альбуминов. • В большинстве случаев повышение содержания γ – глобулинов, повышается содержание факторов свертывания крови, холестерина, калия. • Нарастает уровень общего билирубина, снижается, ранее повышенные A л. А T , A с. А T , снижается содержание холинэстеразы, нарастает метаболический ацидоз.

