Теория строения орг соед.ppt
- Количество слайдов: 59
 Запорожский государственный медицинский университет Теория строения органических соединений Запорожье, 2011
Запорожский государственный медицинский университет Теория строения органических соединений Запорожье, 2011
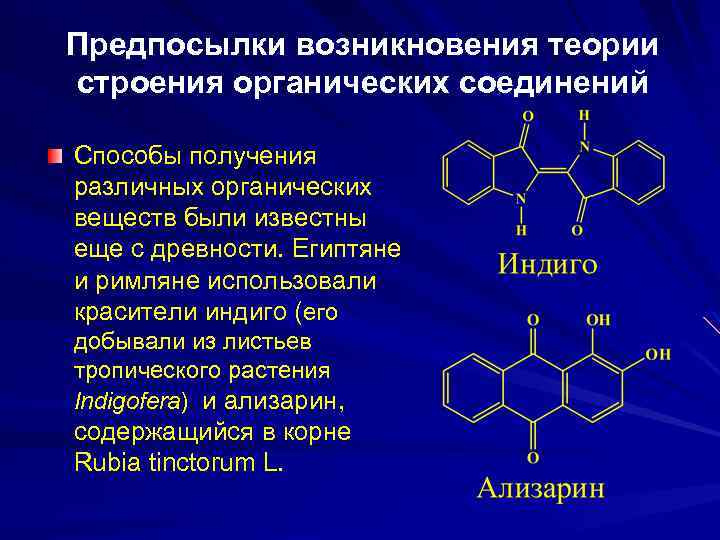 Предпосылки возникновения теории строения органических соединений Способы получения различных органических веществ были известны еще с древности. Египтяне и римляне использовали красители индиго (его добывали из листьев тропического растения Indigofera) и ализарин, содержащийся в корне Rubia tinctorum L.
Предпосылки возникновения теории строения органических соединений Способы получения различных органических веществ были известны еще с древности. Египтяне и римляне использовали красители индиго (его добывали из листьев тропического растения Indigofera) и ализарин, содержащийся в корне Rubia tinctorum L.
 Предпосылки возникновения теории строения органических соединений Некоторые технологии органической химии возникли еще в глубокой древности, например, спиртовое и уксуснокислое брожение. Во времена средневековья к этим знаниям ничего не прибавилось, некоторый прогресс начался только в 16 -17 в: были получены некоторые вещества, в основном путем перегонки c водяным паром некоторых растительных продуктов.
Предпосылки возникновения теории строения органических соединений Некоторые технологии органической химии возникли еще в глубокой древности, например, спиртовое и уксуснокислое брожение. Во времена средневековья к этим знаниям ничего не прибавилось, некоторый прогресс начался только в 16 -17 в: были получены некоторые вещества, в основном путем перегонки c водяным паром некоторых растительных продуктов.
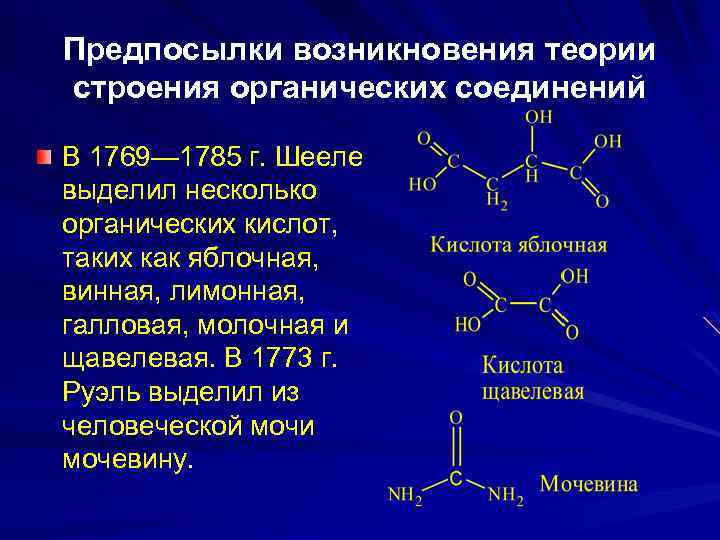 Предпосылки возникновения теории строения органических соединений В 1769— 1785 г. Шееле выделил несколько органических кислот, таких как яблочная, винная, лимонная, галловая, молочная и щавелевая. В 1773 г. Руэль выделил из человеческой мочи мочевину.
Предпосылки возникновения теории строения органических соединений В 1769— 1785 г. Шееле выделил несколько органических кислот, таких как яблочная, винная, лимонная, галловая, молочная и щавелевая. В 1773 г. Руэль выделил из человеческой мочи мочевину.
 Предпосылки возникновения теории строения органических соединений Выделенные из животного или растительного сырья продукты имели между собой много общего, но отличались от неорганических соединений. Так возник термин «Органическая химия» — раздел химии, изучающий вещества, выделенные из организмов (определение Берцелиуса, 1807 г. ). При этом полагали, что эти вещества могут быть получены только в живых организмах благодаря «жизненной силе» .
Предпосылки возникновения теории строения органических соединений Выделенные из животного или растительного сырья продукты имели между собой много общего, но отличались от неорганических соединений. Так возник термин «Органическая химия» — раздел химии, изучающий вещества, выделенные из организмов (определение Берцелиуса, 1807 г. ). При этом полагали, что эти вещества могут быть получены только в живых организмах благодаря «жизненной силе» .
 Предпосылки возникновения теории строения органических соединений Как принято считать, органическая химия как наука появилась в 1828 году когда немецкий химик Фридрих Вёлер впервые получил органическое вещество — мочевину — в результате упаривания водного раствора аммоний цианата (NH 4 OCN), полученного in situ взаимодействием калий цианата с аммоний сульфатом.
Предпосылки возникновения теории строения органических соединений Как принято считать, органическая химия как наука появилась в 1828 году когда немецкий химик Фридрих Вёлер впервые получил органическое вещество — мочевину — в результате упаривания водного раствора аммоний цианата (NH 4 OCN), полученного in situ взаимодействием калий цианата с аммоний сульфатом.
 Предпосылки возникновения теории строения органических соединений Важными этапами стали: - предложение шотландским химиком Арчибальдом Скоттом Купером и поныне используемого символа валентной черты, соединяющей атомы при изображении структурных формул. Например, для метилового спирта можно представить единственно возможную последовательность связей с учетом валентности связываемых атомов в виде следующей формулы:
Предпосылки возникновения теории строения органических соединений Важными этапами стали: - предложение шотландским химиком Арчибальдом Скоттом Купером и поныне используемого символа валентной черты, соединяющей атомы при изображении структурных формул. Например, для метилового спирта можно представить единственно возможную последовательность связей с учетом валентности связываемых атомов в виде следующей формулы:
 Предпосылки возникновения теории строения органических соединений установление немецким химиком-органиком Фридрихом Августом Кекуле 1857 г. четырёхвалентности карбона и строения бензола
Предпосылки возникновения теории строения органических соединений установление немецким химиком-органиком Фридрихом Августом Кекуле 1857 г. четырёхвалентности карбона и строения бензола
 19 сентября 1861 года - Съезд немецких естествоиспытателей и врачей в Шпейере – Александр Михайлович Бутлеров «О химическом строении вещества» Основой теории Бутлерова является идея о порядке химического взаимодействия атомов в молекуле. Этот порядок химического взаимодействия не включает представления о механизме химической связи и физическом расположении атомов. Эта важная особенность теории химического строения позволяет всегда опираться на нее при построении физической модели молекулы.
19 сентября 1861 года - Съезд немецких естествоиспытателей и врачей в Шпейере – Александр Михайлович Бутлеров «О химическом строении вещества» Основой теории Бутлерова является идея о порядке химического взаимодействия атомов в молекуле. Этот порядок химического взаимодействия не включает представления о механизме химической связи и физическом расположении атомов. Эта важная особенность теории химического строения позволяет всегда опираться на нее при построении физической модели молекулы.
 Теория строения органических соединений 1. Все атомы в молекуле органического соединения связаны друг с другом в определенной последовательности в соответствии с их валентностью. Изменение последовательности расположения атомов приводит к образованию нового вещества с новыми свойствами. Например, составу вещества С 2 Н 6 О отвечают два разных соединения: эфир диметиловый (СН 3 -О-СН 3) и спирт этиловый (С 2 Н 5 ОН).
Теория строения органических соединений 1. Все атомы в молекуле органического соединения связаны друг с другом в определенной последовательности в соответствии с их валентностью. Изменение последовательности расположения атомов приводит к образованию нового вещества с новыми свойствами. Например, составу вещества С 2 Н 6 О отвечают два разных соединения: эфир диметиловый (СН 3 -О-СН 3) и спирт этиловый (С 2 Н 5 ОН).
 Теория строения органических соединений 2. Свойства веществ зависят от их химического строения. Химическое строение - это определенный порядок в чередовании атомов в молекуле, во взаимодействии и взаимном влиянии атомов друг на друга - как соседних, так и через другие атомы. В результате каждое вещество имеет свои особые физические и химические свойства. Например, диметиловый эфир - это газ без запаха, нерастворимый в воде, t°пл. = -138°C, t°кип. = 23, 6°C; этиловый спирт - жидкость с запахом, растворимая в воде, t°пл. = -114, 5°C, t°кип. =78, 3°C. Данное положение теории строения органических веществ объяснило явление изомерии, широко распространенное в органической химии. Приведенная пара соединений - эфир диметиловый и спирт этиловый - один из примеров, иллюстрирующих явление изомерии.
Теория строения органических соединений 2. Свойства веществ зависят от их химического строения. Химическое строение - это определенный порядок в чередовании атомов в молекуле, во взаимодействии и взаимном влиянии атомов друг на друга - как соседних, так и через другие атомы. В результате каждое вещество имеет свои особые физические и химические свойства. Например, диметиловый эфир - это газ без запаха, нерастворимый в воде, t°пл. = -138°C, t°кип. = 23, 6°C; этиловый спирт - жидкость с запахом, растворимая в воде, t°пл. = -114, 5°C, t°кип. =78, 3°C. Данное положение теории строения органических веществ объяснило явление изомерии, широко распространенное в органической химии. Приведенная пара соединений - эфир диметиловый и спирт этиловый - один из примеров, иллюстрирующих явление изомерии.
 Теория строения органических соединений 3. Изучение свойств веществ позволяет определить их химическое строение, а химическое строение веществ определяет их физические и химические свойства. 4. Атомы карбона способны соединятся между собой, образовывая углеродные цепи различного вида. Они могут быть как открытыми, так и замкнутыми (циклическими), как прямыми, так и разветвленными. В зависимости от числа связей, затрачиваемых атомами карбона на соединение друг с другом, цепи могут быть насыщенными (с одинарными связями) или ненасыщенными (с двойными и тройными связями).
Теория строения органических соединений 3. Изучение свойств веществ позволяет определить их химическое строение, а химическое строение веществ определяет их физические и химические свойства. 4. Атомы карбона способны соединятся между собой, образовывая углеродные цепи различного вида. Они могут быть как открытыми, так и замкнутыми (циклическими), как прямыми, так и разветвленными. В зависимости от числа связей, затрачиваемых атомами карбона на соединение друг с другом, цепи могут быть насыщенными (с одинарными связями) или ненасыщенными (с двойными и тройными связями).
 Теория строения органических соединений 5. Каждое органическое соединение имеет одну определенную структурную формулу, строения которую или строят, основываясь на положении о четырехвалентном карбоне и способности его атомов образовывать цепи и циклы. Строение молекулы как реального объекта можно изучить экспериментально химическими и физическими методами.
Теория строения органических соединений 5. Каждое органическое соединение имеет одну определенную структурную формулу, строения которую или строят, основываясь на положении о четырехвалентном карбоне и способности его атомов образовывать цепи и циклы. Строение молекулы как реального объекта можно изучить экспериментально химическими и физическими методами.
 Понятие изомерии Изомерия - это явление существования соединений, имеющих одинаковый качественный и количественный состав, но различное строение и, следовательно, разные свойства. • Например, при содержании в молекуле 4 -х атомов карбона и 10 -ти атомов гидрогена возможно В зависимости от характера отличий в существование 2 -х строении изомеров изомерных соединений: различают структурную и пространственную изомерию.
Понятие изомерии Изомерия - это явление существования соединений, имеющих одинаковый качественный и количественный состав, но различное строение и, следовательно, разные свойства. • Например, при содержании в молекуле 4 -х атомов карбона и 10 -ти атомов гидрогена возможно В зависимости от характера отличий в существование 2 -х строении изомеров изомерных соединений: различают структурную и пространственную изомерию.
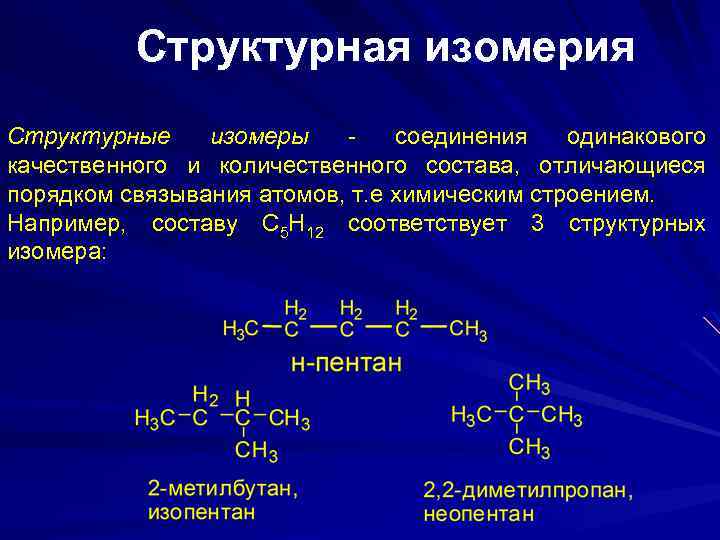 Структурная изомерия Структурные изомеры - соединения одинакового качественного и количественного состава, отличающиеся порядком связывания атомов, т. е химическим строением. Например, составу C 5 H 12 соответствует 3 структурных изомера:
Структурная изомерия Структурные изомеры - соединения одинакового качественного и количественного состава, отличающиеся порядком связывания атомов, т. е химическим строением. Например, составу C 5 H 12 соответствует 3 структурных изомера:
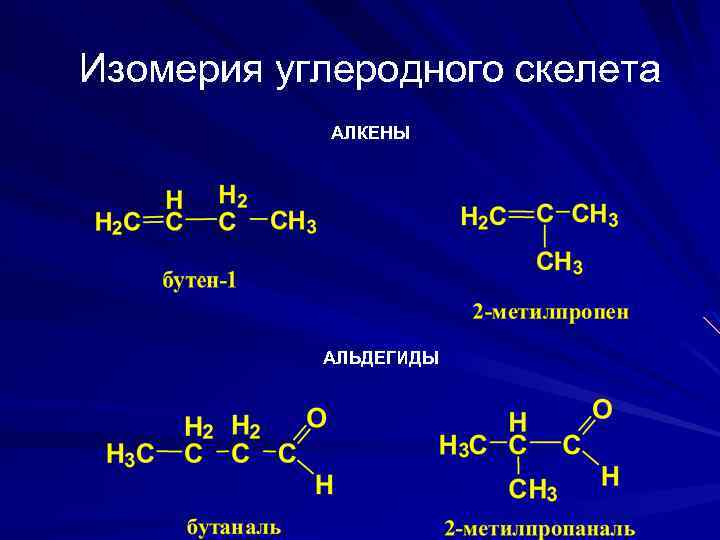 Изомерия углеродного скелета АЛКЕНЫ АЛЬДЕГИДЫ
Изомерия углеродного скелета АЛКЕНЫ АЛЬДЕГИДЫ
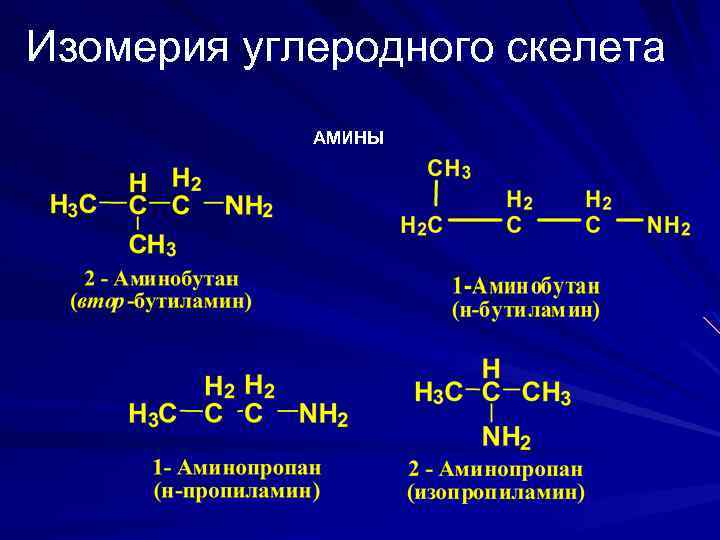 Изомерия углеродного скелета АМИНЫ
Изомерия углеродного скелета АМИНЫ
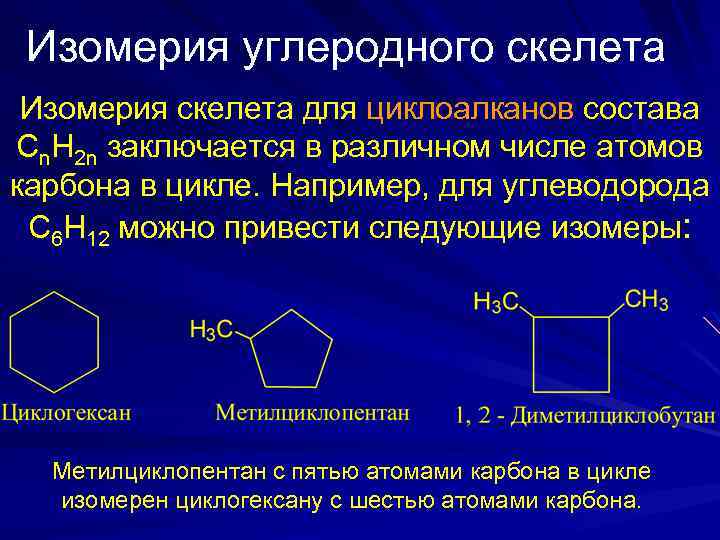 Изомерия углеродного скелета Изомерия скелета для циклоалканов состава Cn. H 2 n заключается в различном числе атомов карбона в цикле. Например, для углеводорода C 6 H 12 можно привести следующие изомеры: Метилциклопентан с пятью атомами карбона в цикле изомерен циклогексану с шестью атомами карбона.
Изомерия углеродного скелета Изомерия скелета для циклоалканов состава Cn. H 2 n заключается в различном числе атомов карбона в цикле. Например, для углеводорода C 6 H 12 можно привести следующие изомеры: Метилциклопентан с пятью атомами карбона в цикле изомерен циклогексану с шестью атомами карбона.
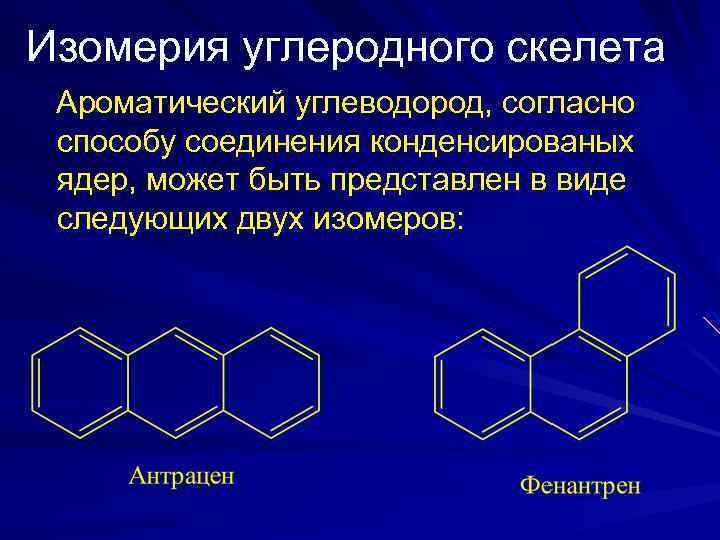 Изомерия углеродного скелета Ароматический углеводород, согласно способу соединения конденсированых ядер, может быть представлен в виде следующих двух изомеров:
Изомерия углеродного скелета Ароматический углеводород, согласно способу соединения конденсированых ядер, может быть представлен в виде следующих двух изомеров:
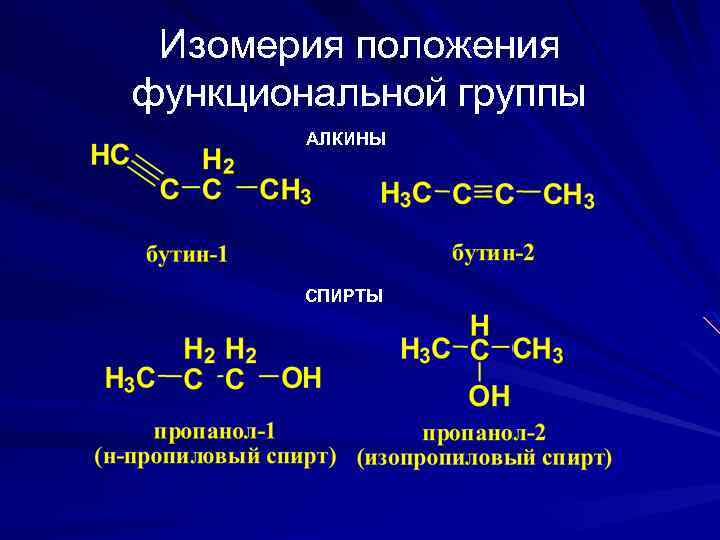 Изомерия положения функциональной группы АЛКИНЫ СПИРТЫ
Изомерия положения функциональной группы АЛКИНЫ СПИРТЫ
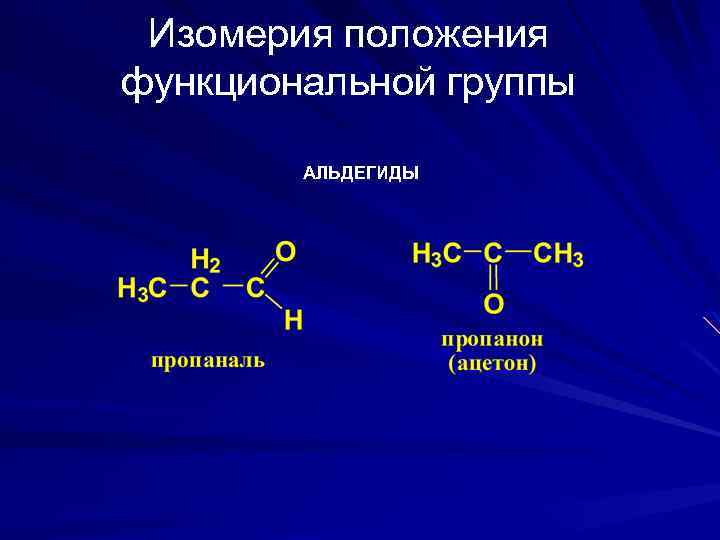 Изомерия положения функциональной группы АЛЬДЕГИДЫ
Изомерия положения функциональной группы АЛЬДЕГИДЫ
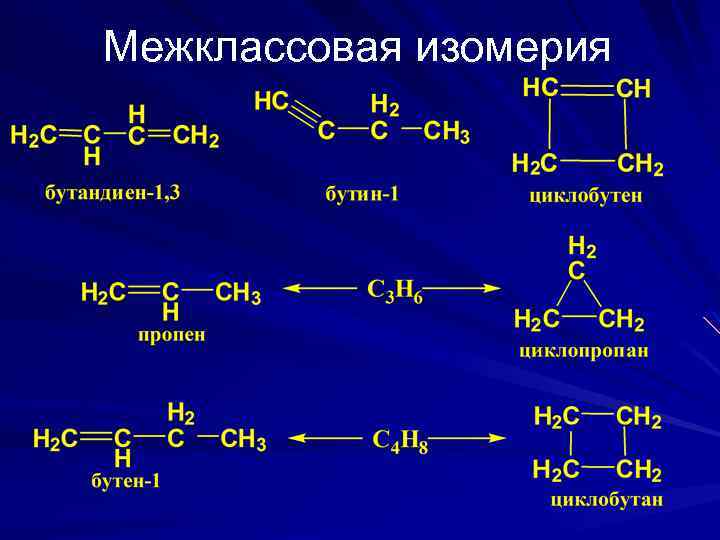 Межклассовая изомерия
Межклассовая изомерия
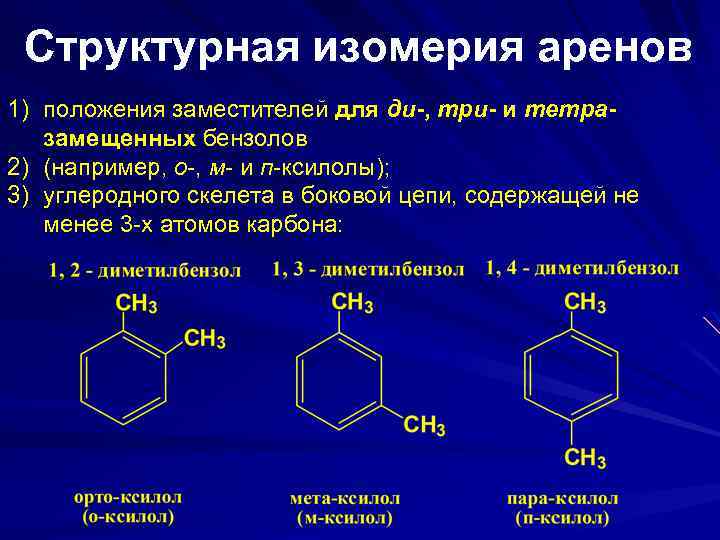 Структурная изомерия аренов 1) положения заместителей для ди-, три- и тетразамещенных бензолов 2) (например, о-, м- и п-ксилолы); 3) углеродного скелета в боковой цепи, содержащей не менее 3 -х атомов карбона:
Структурная изомерия аренов 1) положения заместителей для ди-, три- и тетразамещенных бензолов 2) (например, о-, м- и п-ксилолы); 3) углеродного скелета в боковой цепи, содержащей не менее 3 -х атомов карбона:
 Конформации Различные пространственные формы молекулы, переходящие друг в друга путем вращения вокруг sсвязей С–С, называют конформациями или поворотными изомерами (конформерами). Рассмотрим поворотные изомеры на примере этана Н 3 С–СН 3:
Конформации Различные пространственные формы молекулы, переходящие друг в друга путем вращения вокруг sсвязей С–С, называют конформациями или поворотными изомерами (конформерами). Рассмотрим поворотные изомеры на примере этана Н 3 С–СН 3:
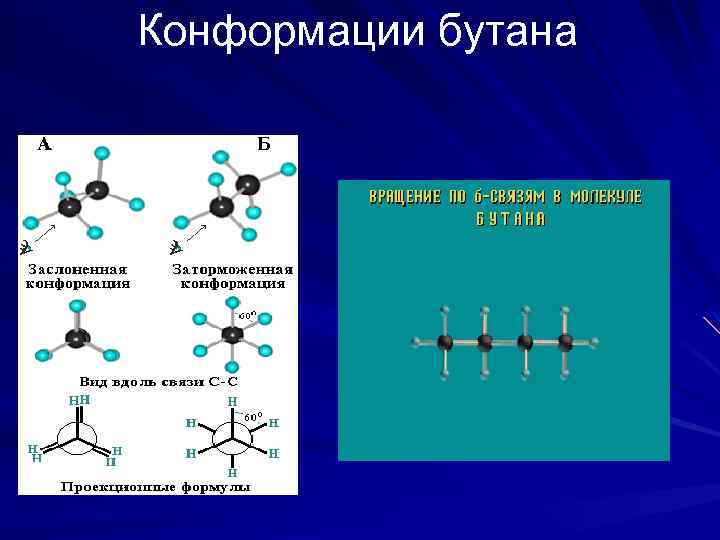 Конформации бутана
Конформации бутана
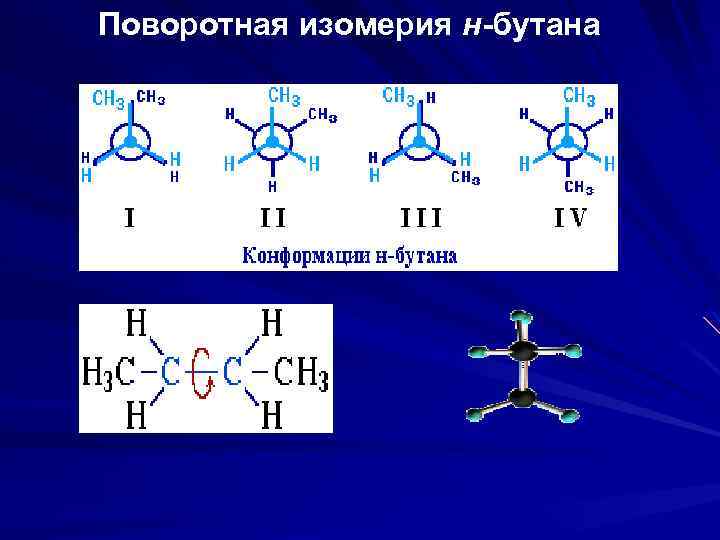 Поворотная изомерия н-бутана
Поворотная изомерия н-бутана
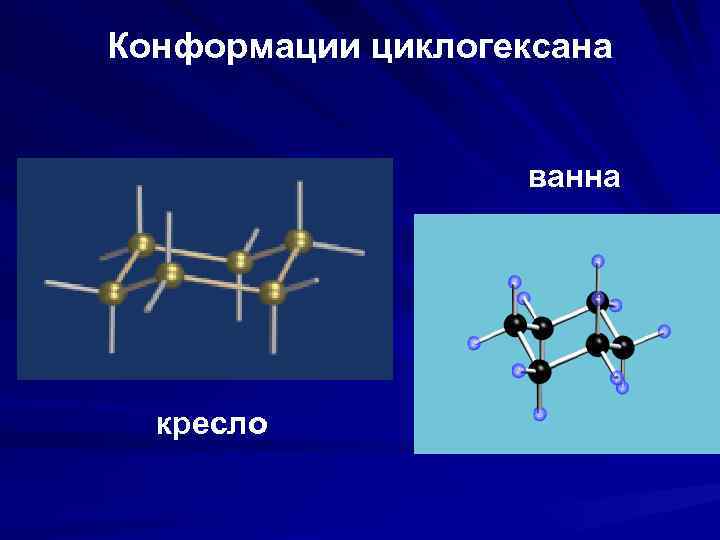 Конформации циклогексана ванна кресло
Конформации циклогексана ванна кресло
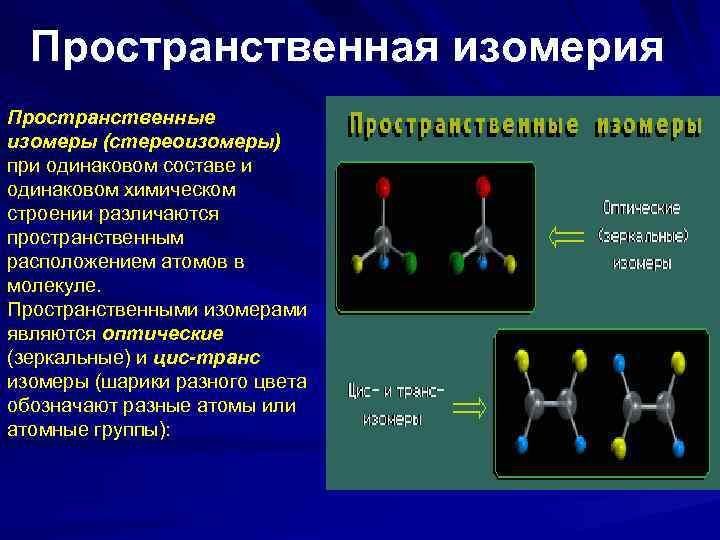 Пространственная изомерия Пространственные изомеры (стереоизомеры) при одинаковом составе и одинаковом химическом строении различаются пространственным расположением атомов в молекуле. Пространственными изомерами являются оптические (зеркальные) и цис-транс изомеры (шарики разного цвета обозначают разные атомы или атомные группы):
Пространственная изомерия Пространственные изомеры (стереоизомеры) при одинаковом составе и одинаковом химическом строении различаются пространственным расположением атомов в молекуле. Пространственными изомерами являются оптические (зеркальные) и цис-транс изомеры (шарики разного цвета обозначают разные атомы или атомные группы):
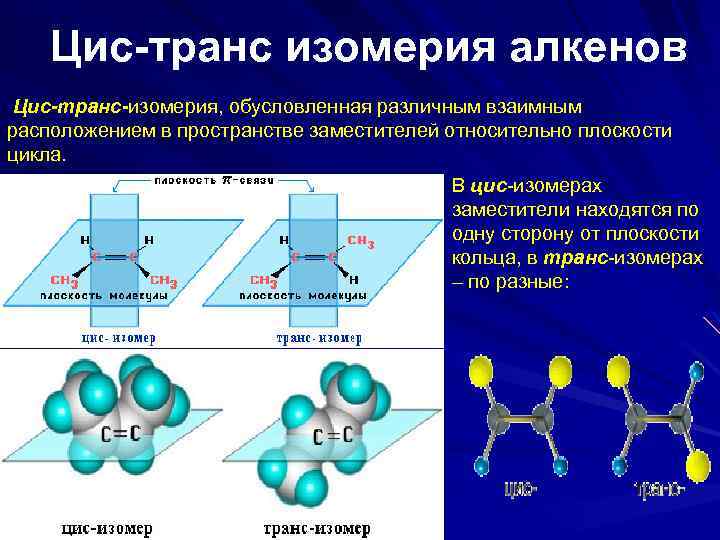 Цис-транс изомерия алкенов Цис-транс-изомерия, обусловленная различным взаимным расположением в пространстве заместителей относительно плоскости цикла. В цис-изомерах заместители находятся по одну сторону от плоскости кольца, в транс-изомерах – по разные:
Цис-транс изомерия алкенов Цис-транс-изомерия, обусловленная различным взаимным расположением в пространстве заместителей относительно плоскости цикла. В цис-изомерах заместители находятся по одну сторону от плоскости кольца, в транс-изомерах – по разные:
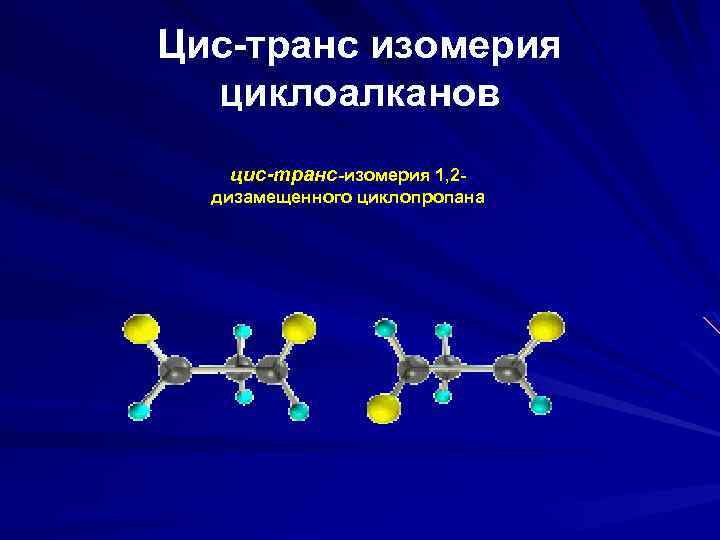 Цис-транс изомерия циклоалканов цис-транс-изомерия 1, 2 дизамещенного циклопропана
Цис-транс изомерия циклоалканов цис-транс-изомерия 1, 2 дизамещенного циклопропана
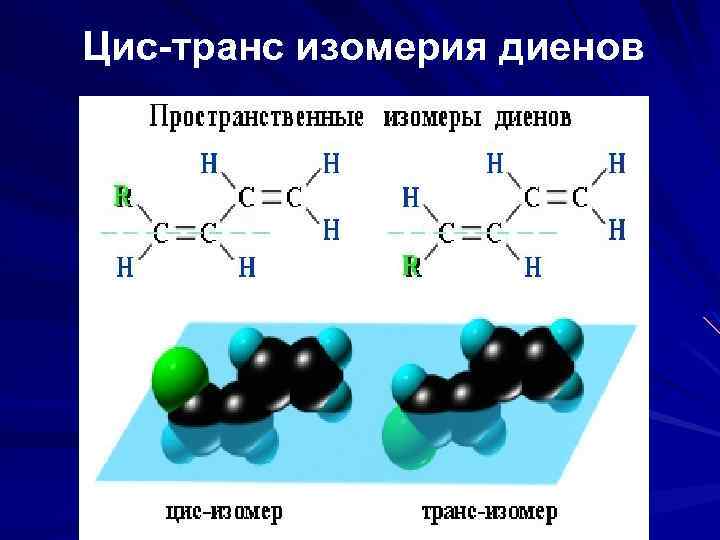 Цис-транс изомерия диенов
Цис-транс изомерия диенов
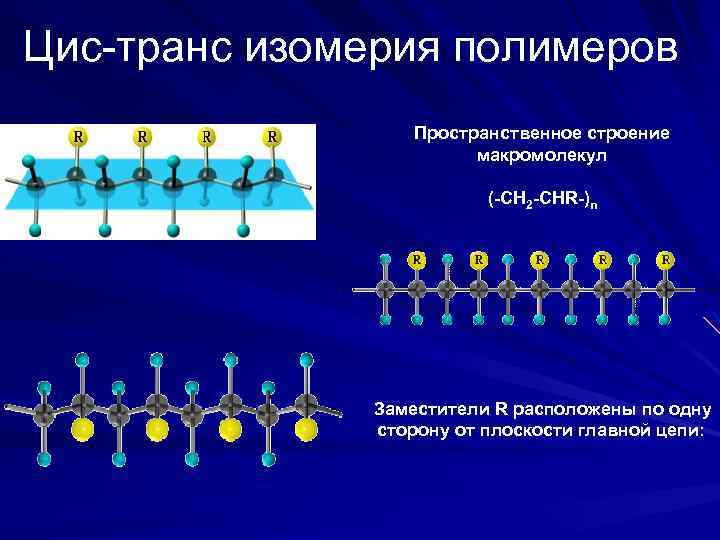 Цис-транс изомерия полимеров Пространственное строение макромолекул (-CH 2 -CHR-)n Заместители R расположены по одну сторону от плоскости главной цепи:
Цис-транс изомерия полимеров Пространственное строение макромолекул (-CH 2 -CHR-)n Заместители R расположены по одну сторону от плоскости главной цепи:
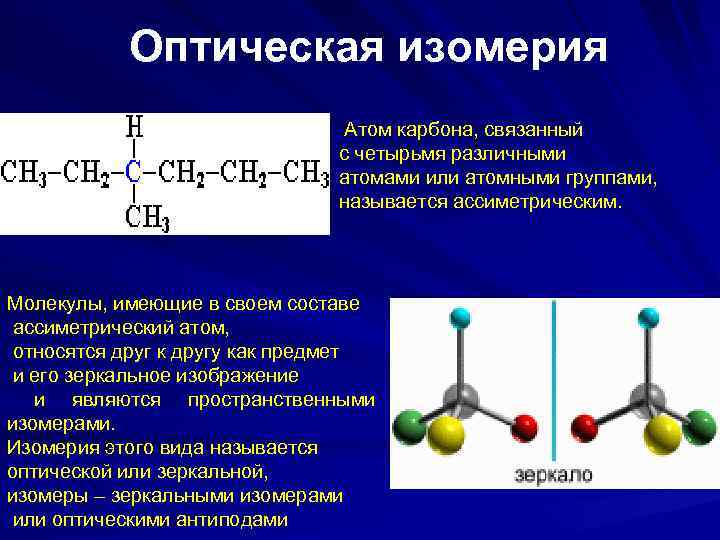 Оптическая изомерия Атом карбона, связанный с четырьмя различными атомами или атомными группами, называется ассиметрическим. Молекулы, имеющие в своем составе ассиметрический атом, относятся друг к другу как предмет и его зеркальное изображение и являются пространственными изомерами. Изомерия этого вида называется оптической или зеркальной, изомеры – зеркальными изомерами или оптическими антиподами
Оптическая изомерия Атом карбона, связанный с четырьмя различными атомами или атомными группами, называется ассиметрическим. Молекулы, имеющие в своем составе ассиметрический атом, относятся друг к другу как предмет и его зеркальное изображение и являются пространственными изомерами. Изомерия этого вида называется оптической или зеркальной, изомеры – зеркальными изомерами или оптическими антиподами
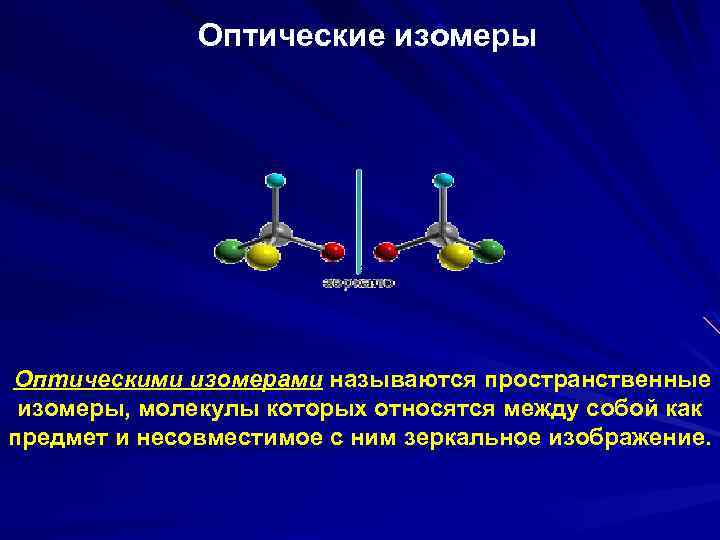 Оптические изомеры Оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение.
Оптические изомеры Оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение.
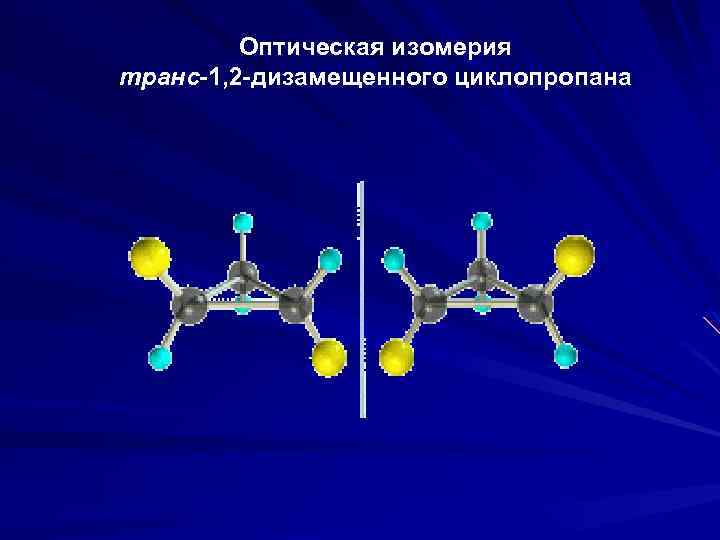 Оптическая изомерия транс-1, 2 -дизамещенного циклопропана
Оптическая изомерия транс-1, 2 -дизамещенного циклопропана
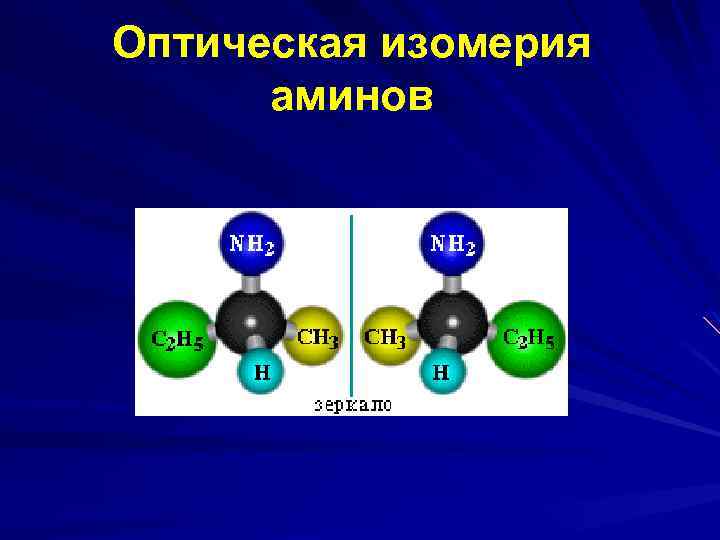 Оптическая изомерия аминов
Оптическая изомерия аминов
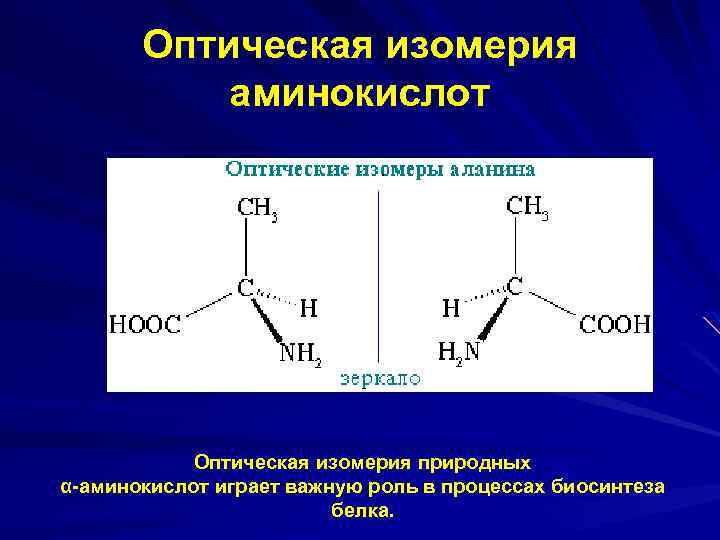 Оптическая изомерия аминокислот Оптическая изомерия природных α-аминокислот играет важную роль в процессах биосинтеза белка.
Оптическая изомерия аминокислот Оптическая изомерия природных α-аминокислот играет важную роль в процессах биосинтеза белка.
 Взаимное влияние атомов в органических соединениях При образовании ковалентной связи между двумя атомами с одинаковой электроотрицательностью электронная пара в равной мере принадлежит связанным атомом (неполярная связь). Если же атомы имеют разную электроотрицательность, электронная плотность ковалентной связи смещается к более электроотрицательному атому (полярная связь). В сложных органических молекулах полярная ковалентная связь оказывает влияние на соседние связи: приводит к изменению их электронного состояния, вызывая поляризацию:
Взаимное влияние атомов в органических соединениях При образовании ковалентной связи между двумя атомами с одинаковой электроотрицательностью электронная пара в равной мере принадлежит связанным атомом (неполярная связь). Если же атомы имеют разную электроотрицательность, электронная плотность ковалентной связи смещается к более электроотрицательному атому (полярная связь). В сложных органических молекулах полярная ковалентная связь оказывает влияние на соседние связи: приводит к изменению их электронного состояния, вызывая поляризацию:
 Например, в молекуле н-бутана все углерод-углеродные связи неполярны, электронная плотность распределена симметрично и молекула не имеет дипольного момента. Введение в молекулу н-бутана атома хлора (1 -хлорбутан) приводит к поляризации не только связи С-Сl, но и соседних углерод-углеродных связей. Атом хлора, имея большую электроотрицательность, чем карбон, оттягивает электроны σ -связи С-Сl в свою сторону. В результате такого смещения на атоме хлора появляется частичный отрицательный заряд (δ-), а на углеродном атоме – равные по значению положительный заряд (δ+). Понижение электронной плотности на С 1 частично компенсируется оттягиванием в его сторону электронов с соседнего атома карбона, что приводит к поляризации связи С 2 -С 1 и возникновению частичного положительно заряда на атоме С 2. Тот, в свою очередь, вызывает поляризацию связи. С 2 -С 3 и т. д. По мере удаления связи дробный заряд на атомах карбона уменьшается: δ+> δ’’+> δ’’’+. Таким образом, поляризация связи С-Сl вызывает электронную асимметрию молекулы и появление дипольного момента.
Например, в молекуле н-бутана все углерод-углеродные связи неполярны, электронная плотность распределена симметрично и молекула не имеет дипольного момента. Введение в молекулу н-бутана атома хлора (1 -хлорбутан) приводит к поляризации не только связи С-Сl, но и соседних углерод-углеродных связей. Атом хлора, имея большую электроотрицательность, чем карбон, оттягивает электроны σ -связи С-Сl в свою сторону. В результате такого смещения на атоме хлора появляется частичный отрицательный заряд (δ-), а на углеродном атоме – равные по значению положительный заряд (δ+). Понижение электронной плотности на С 1 частично компенсируется оттягиванием в его сторону электронов с соседнего атома карбона, что приводит к поляризации связи С 2 -С 1 и возникновению частичного положительно заряда на атоме С 2. Тот, в свою очередь, вызывает поляризацию связи. С 2 -С 3 и т. д. По мере удаления связи дробный заряд на атомах карбона уменьшается: δ+> δ’’+> δ’’’+. Таким образом, поляризация связи С-Сl вызывает электронную асимметрию молекулы и появление дипольного момента.
 Индуктивный эффект Передача электронного влияния заместителя вдоль цепи σсвязей называется индуктивным (индукционным) эффектом. Обозначается индуктивный эффект буквой «I» . Направление смещения электронной плотности σ-связей изображают прямой стрелкой (→). Действие индуктивного эффекта наиболее сильно проявляется на двух ближайших σ-связях. Из-за слабой поляризуемости σ-связей индуктивный эффект через 3 -4 связи затухает. В зависимости от направления электронного влияния заместителя различают индуктивный положительный (+I) и отрицательный (-I). В качестве стандарта для оценки направления индуктивного эффекта заместителя принят индуктивный эффект атома гидрогена, который из-за небольшого дипольного момента связи С-Н считается равным нулю.
Индуктивный эффект Передача электронного влияния заместителя вдоль цепи σсвязей называется индуктивным (индукционным) эффектом. Обозначается индуктивный эффект буквой «I» . Направление смещения электронной плотности σ-связей изображают прямой стрелкой (→). Действие индуктивного эффекта наиболее сильно проявляется на двух ближайших σ-связях. Из-за слабой поляризуемости σ-связей индуктивный эффект через 3 -4 связи затухает. В зависимости от направления электронного влияния заместителя различают индуктивный положительный (+I) и отрицательный (-I). В качестве стандарта для оценки направления индуктивного эффекта заместителя принят индуктивный эффект атома гидрогена, который из-за небольшого дипольного момента связи С-Н считается равным нулю.
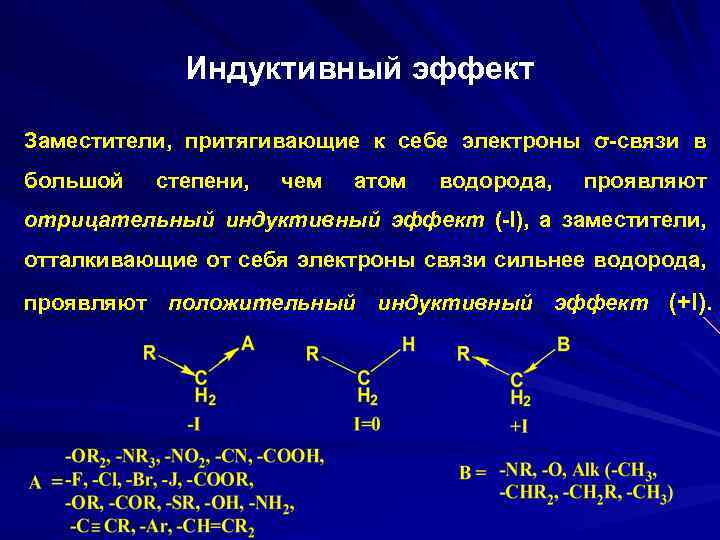 Индуктивный эффект Заместители, притягивающие к себе электроны σ-связи в большой степени, чем атом водорода, проявляют отрицательный индуктивный эффект (-I), а заместители, отталкивающие от себя электроны связи сильнее водорода, проявляют положительный индуктивный эффект (+I).
Индуктивный эффект Заместители, притягивающие к себе электроны σ-связи в большой степени, чем атом водорода, проявляют отрицательный индуктивный эффект (-I), а заместители, отталкивающие от себя электроны связи сильнее водорода, проявляют положительный индуктивный эффект (+I).
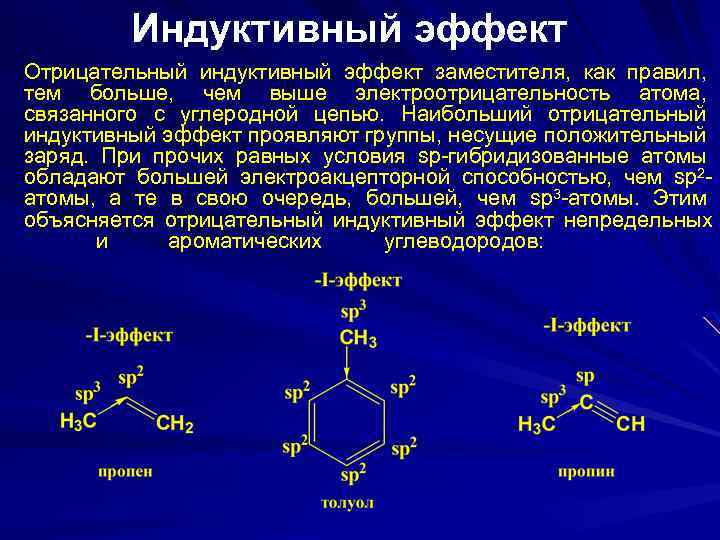 Индуктивный эффект Отрицательный индуктивный эффект заместителя, как правил, тем больше, чем выше электроотрицательность атома, связанного с углеродной цепью. Наибольший отрицательный индуктивный эффект проявляют группы, несущие положительный заряд. При прочих равных условия sp-гибридизованные атомы обладают большей электроакцепторной способностью, чем sp 2 атомы, а те в свою очередь, большей, чем sp 3 -атомы. Этим объясняется отрицательный индуктивный эффект непредельных и ароматических углеводородов:
Индуктивный эффект Отрицательный индуктивный эффект заместителя, как правил, тем больше, чем выше электроотрицательность атома, связанного с углеродной цепью. Наибольший отрицательный индуктивный эффект проявляют группы, несущие положительный заряд. При прочих равных условия sp-гибридизованные атомы обладают большей электроакцепторной способностью, чем sp 2 атомы, а те в свою очередь, большей, чем sp 3 -атомы. Этим объясняется отрицательный индуктивный эффект непредельных и ароматических углеводородов:
 Наибольший положительный индуктивный эффект проявляют заместители, несущие отрицательный заряд. Среди алкильных групп большими электроннодонорными свойствами обладают третичные радикалы, затем вторичные и, наконец, первичные: В ряду первичных алкильных радикалов положительный индуктивный эффект возрастает с увеличением углеродной цепи: С 4 Н 9 ->С 3 Н 7 ->С 2 Н 5 ->СН 3 Таким образом, на основании изложенного можно сделать следующие выводы: 1. Индуктивный эффект проявляется всегда при наличии в молекуле атома с различной электроотрицательностью. 2. Индуктивный эффект распространяется только через σ-связи и всегда в одном направлении. 3. Индуктивный эффект затухает в цепи через 3 -4 σ-связи.
Наибольший положительный индуктивный эффект проявляют заместители, несущие отрицательный заряд. Среди алкильных групп большими электроннодонорными свойствами обладают третичные радикалы, затем вторичные и, наконец, первичные: В ряду первичных алкильных радикалов положительный индуктивный эффект возрастает с увеличением углеродной цепи: С 4 Н 9 ->С 3 Н 7 ->С 2 Н 5 ->СН 3 Таким образом, на основании изложенного можно сделать следующие выводы: 1. Индуктивный эффект проявляется всегда при наличии в молекуле атома с различной электроотрицательностью. 2. Индуктивный эффект распространяется только через σ-связи и всегда в одном направлении. 3. Индуктивный эффект затухает в цепи через 3 -4 σ-связи.
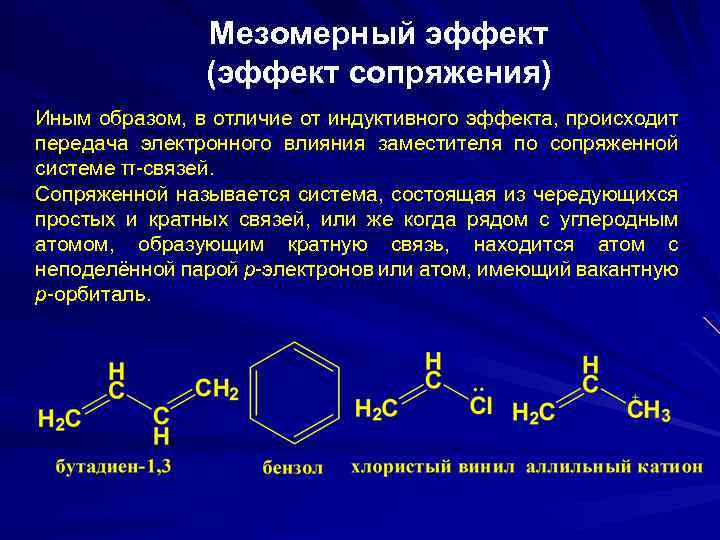 Мезомерный эффект (эффект сопряжения) Иным образом, в отличие от индуктивного эффекта, происходит передача электронного влияния заместителя по сопряженной системе π-связей. Сопряженной называется система, состоящая из чередующихся простых и кратных связей, или же когда рядом с углеродным атомом, образующим кратную связь, находится атом с неподелённой парой р-электронов или атом, имеющий вакантную р-орбиталь.
Мезомерный эффект (эффект сопряжения) Иным образом, в отличие от индуктивного эффекта, происходит передача электронного влияния заместителя по сопряженной системе π-связей. Сопряженной называется система, состоящая из чередующихся простых и кратных связей, или же когда рядом с углеродным атомом, образующим кратную связь, находится атом с неподелённой парой р-электронов или атом, имеющий вакантную р-орбиталь.
 Мезомерный эффект (эффект сопряжения) Сопряженные системы делятся на системы с открытой и замкнутой цепью. В спряженных системах имеет место дополнительного перекрывания π- и р-орбиталей, которое называют сопряжением. Различают π, π-сопряжение (перекрывание двух π-орбиталей) и р, π-сопряжение (перекрывание р-орбитали с π-орбиталью). Сопряжение возможно лишь в случае параллельности осей симметрии взаимодействующих орбиталей. В результате сопряжения образуется единая π-электронная система и происходит перераспределение (делокализация) π-электронной плотности.
Мезомерный эффект (эффект сопряжения) Сопряженные системы делятся на системы с открытой и замкнутой цепью. В спряженных системах имеет место дополнительного перекрывания π- и р-орбиталей, которое называют сопряжением. Различают π, π-сопряжение (перекрывание двух π-орбиталей) и р, π-сопряжение (перекрывание р-орбитали с π-орбиталью). Сопряжение возможно лишь в случае параллельности осей симметрии взаимодействующих орбиталей. В результате сопряжения образуется единая π-электронная система и происходит перераспределение (делокализация) π-электронной плотности.
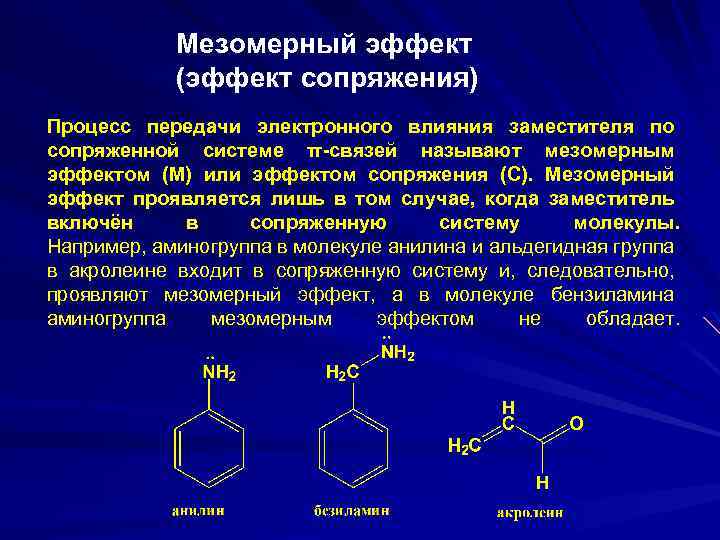 Мезомерный эффект (эффект сопряжения) Процесс передачи электронного влияния заместителя по сопряженной системе π-связей называют мезомерным эффектом (М) или эффектом сопряжения (С). Мезомерный эффект проявляется лишь в том случае, когда заместитель включён в сопряженную систему молекулы. Например, аминогруппа в молекуле анилина и альдегидная группа в акролеине входит в сопряженную систему и, следовательно, проявляют мезомерный эффект, а в молекуле бензиламина аминогруппа мезомерным эффектом не обладает.
Мезомерный эффект (эффект сопряжения) Процесс передачи электронного влияния заместителя по сопряженной системе π-связей называют мезомерным эффектом (М) или эффектом сопряжения (С). Мезомерный эффект проявляется лишь в том случае, когда заместитель включён в сопряженную систему молекулы. Например, аминогруппа в молекуле анилина и альдегидная группа в акролеине входит в сопряженную систему и, следовательно, проявляют мезомерный эффект, а в молекуле бензиламина аминогруппа мезомерным эффектом не обладает.
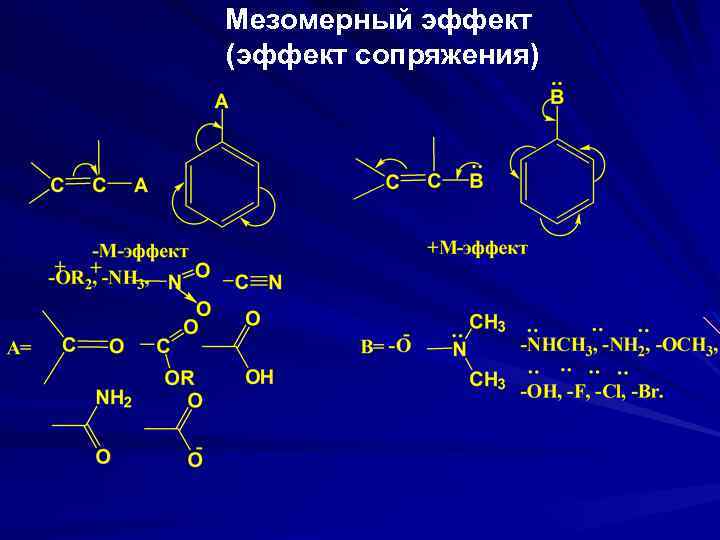
 Различают мезомерный эффект заместителя положительный (+М) и отрицательный (-М). Положительный мезомерный эффект проявляют заместители, подающие электроны в сопряженную систему. К ним относят атомы, содержащие неподелённые пары электронов или отрицательный заряд, а также атомные группы, имеющие на первом атоме неподелённые электронные пары или отрицательный заряд. Отрицательный мезомерный эффект проявляют заместители, оттягивающие на себя электронную плотность сопряженной системы. -М-эффектом облают заместители, первый атом которых несет положительный заряд, а также атомные группы, в которых первый атом связан кратной связью с более электроотрицательным атомом, чем он сам. Направление смещения электронной плотности π-связей и неподеленных пар электронов изображают изогнутой стрелкой, начало которой указывает, какие электроны смещаются, а конец - связь или атом, к которым они смещаются.
Различают мезомерный эффект заместителя положительный (+М) и отрицательный (-М). Положительный мезомерный эффект проявляют заместители, подающие электроны в сопряженную систему. К ним относят атомы, содержащие неподелённые пары электронов или отрицательный заряд, а также атомные группы, имеющие на первом атоме неподелённые электронные пары или отрицательный заряд. Отрицательный мезомерный эффект проявляют заместители, оттягивающие на себя электронную плотность сопряженной системы. -М-эффектом облают заместители, первый атом которых несет положительный заряд, а также атомные группы, в которых первый атом связан кратной связью с более электроотрицательным атомом, чем он сам. Направление смещения электронной плотности π-связей и неподеленных пар электронов изображают изогнутой стрелкой, начало которой указывает, какие электроны смещаются, а конец - связь или атом, к которым они смещаются.
 Мезомерный эффект (эффект сопряжения)
Мезомерный эффект (эффект сопряжения)
 Наибольший отрицательный мезомерный эффект проявляют заместители, несущие положительный заряд. –М-эффект ненасыщенных группировок тем больше, чем больше разность электроотрицательность атомов, связанных кратной связью. Наибольшим положительным мезомерным эффектом обладают атомы, несущие отрицательный заряд. +М-эффект заместителей, содержащих атомы с неподелёнными парами электронов тем больше, чем меньше в пределах группы периода электроотрицательность атома, несущего неподелённую пару, например: -NH 2>-OH> -F. В пределах группы периодической системы +Мэффект заместителей ослабевает сверху вниз (-F>Cl>-Br), что объясняют большей выгодностью при перекрывании близких по размерам р-орбиталей.
Наибольший отрицательный мезомерный эффект проявляют заместители, несущие положительный заряд. –М-эффект ненасыщенных группировок тем больше, чем больше разность электроотрицательность атомов, связанных кратной связью. Наибольшим положительным мезомерным эффектом обладают атомы, несущие отрицательный заряд. +М-эффект заместителей, содержащих атомы с неподелёнными парами электронов тем больше, чем меньше в пределах группы периода электроотрицательность атома, несущего неподелённую пару, например: -NH 2>-OH> -F. В пределах группы периодической системы +Мэффект заместителей ослабевает сверху вниз (-F>Cl>-Br), что объясняют большей выгодностью при перекрывании близких по размерам р-орбиталей.
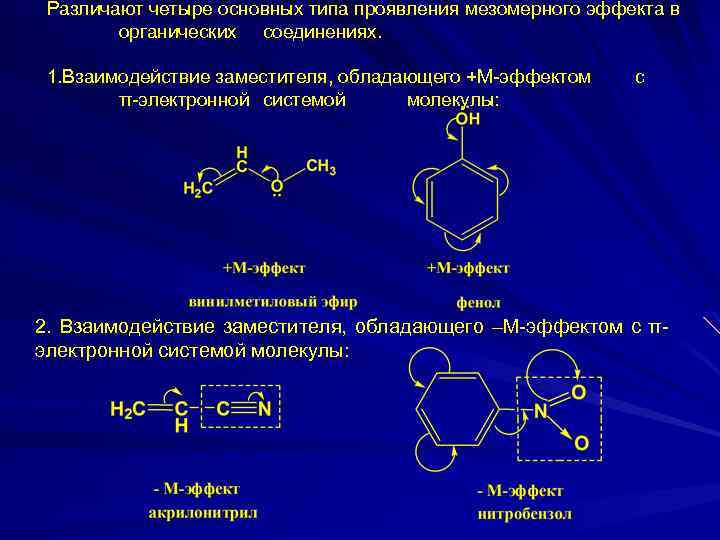 Различают четыре основных типа проявления мезомерного эффекта в органических соединениях. 1. Взаимодействие заместителя, обладающего +М-эффектом π-электронной системой молекулы: с 2. Взаимодействие заместителя, обладающего –М-эффектом с πэлектронной системой молекулы:
Различают четыре основных типа проявления мезомерного эффекта в органических соединениях. 1. Взаимодействие заместителя, обладающего +М-эффектом π-электронной системой молекулы: с 2. Взаимодействие заместителя, обладающего –М-эффектом с πэлектронной системой молекулы:
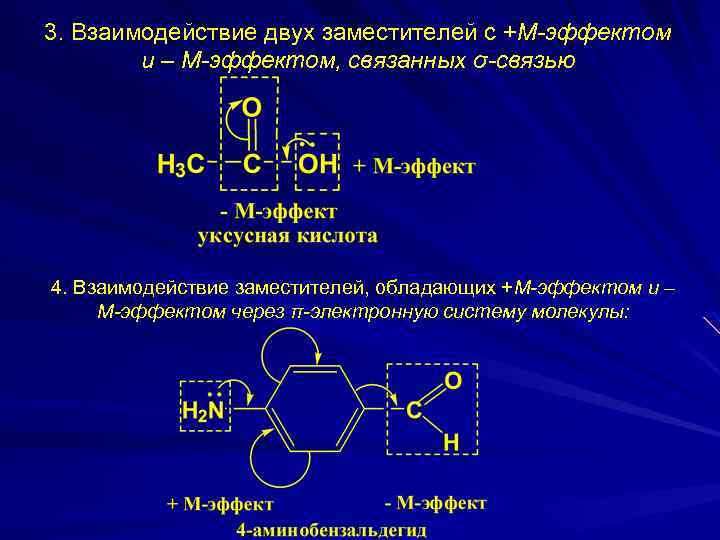 3. Взаимодействие двух заместителей с +М-эффектом и – М-эффектом, связанных σ-связью 4. Взаимодействие заместителей, обладающих +М-эффектом и – М-эффектом через π-электронную систему молекулы:
3. Взаимодействие двух заместителей с +М-эффектом и – М-эффектом, связанных σ-связью 4. Взаимодействие заместителей, обладающих +М-эффектом и – М-эффектом через π-электронную систему молекулы:
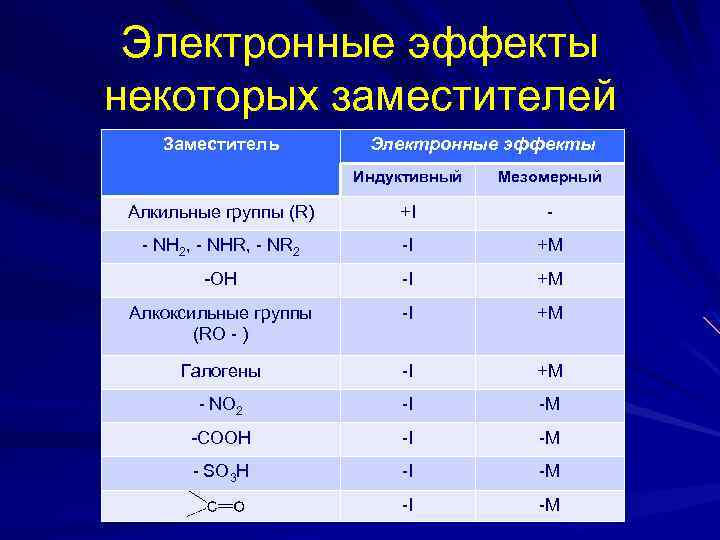 Электронные эффекты некоторых заместителей Заместитель Электронные эффекты Индуктивный Мезомерный Алкильные группы (R) +I - - NH 2, - NHR, - NR 2 -I +M -OH -I +M Алкоксильные группы (RO - ) -I +M Галогены -I +M - NO 2 -I -M -COOH -I -M - SO 3 H -I -M
Электронные эффекты некоторых заместителей Заместитель Электронные эффекты Индуктивный Мезомерный Алкильные группы (R) +I - - NH 2, - NHR, - NR 2 -I +M -OH -I +M Алкоксильные группы (RO - ) -I +M Галогены -I +M - NO 2 -I -M -COOH -I -M - SO 3 H -I -M
 Тест-контроль 1. Изомерами называются. . . Ответ 1 : вещества, имеющие сходное строение и сходные химические свойства, но разный количественный состав Ответ 2 : вещества, имеющие одинаковый качественный состав, но различные свойства Ответ 3 : вещества, имеющие одинаковый качественный и количественный состав, но различное строение молекул Ответ 4 : вещества, молекулы которых содержат одинаковое количество атомов карбона, но разное количество атомов других элементов
Тест-контроль 1. Изомерами называются. . . Ответ 1 : вещества, имеющие сходное строение и сходные химические свойства, но разный количественный состав Ответ 2 : вещества, имеющие одинаковый качественный состав, но различные свойства Ответ 3 : вещества, имеющие одинаковый качественный и количественный состав, но различное строение молекул Ответ 4 : вещества, молекулы которых содержат одинаковое количество атомов карбона, но разное количество атомов других элементов
 2. Какие из представленных на рисунке соединений являются изомерами? Ответ 1 : 1, 2 и 1, 5 Ответ 2 : 1, 2 и 3, 6 Ответ 3 : 3, 6 и 1, 5 Ответ 4 : 2, 3 и 1, 5
2. Какие из представленных на рисунке соединений являются изомерами? Ответ 1 : 1, 2 и 1, 5 Ответ 2 : 1, 2 и 3, 6 Ответ 3 : 3, 6 и 1, 5 Ответ 4 : 2, 3 и 1, 5
 3. Сколько изомерных алкенов соответствует формуле С 4 Н 8 Ответ 1: изомеров нет Ответ 2: два Ответ 3: три Ответ 4: четыре
3. Сколько изомерных алкенов соответствует формуле С 4 Н 8 Ответ 1: изомеров нет Ответ 2: два Ответ 3: три Ответ 4: четыре
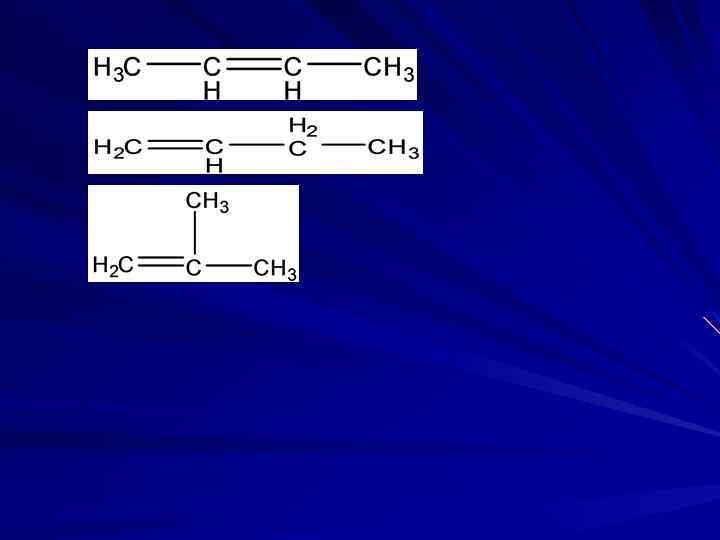
 4. Какие из перечисленных диенов могут существовать в виде цис- и транс-изомеров: а) бутадиен-1, 3; б) 2 -метилбутадиен-1, 3; в) пентадиен-1, 3; г) гексадиен-2, 4; д) 2, 3 -диметилбутадиен-1, 3 Ответ 1: а) и б) Ответ 2: а) и д) Ответ 3: в) и г) Ответ 4: б) и д)
4. Какие из перечисленных диенов могут существовать в виде цис- и транс-изомеров: а) бутадиен-1, 3; б) 2 -метилбутадиен-1, 3; в) пентадиен-1, 3; г) гексадиен-2, 4; д) 2, 3 -диметилбутадиен-1, 3 Ответ 1: а) и б) Ответ 2: а) и д) Ответ 3: в) и г) Ответ 4: б) и д)
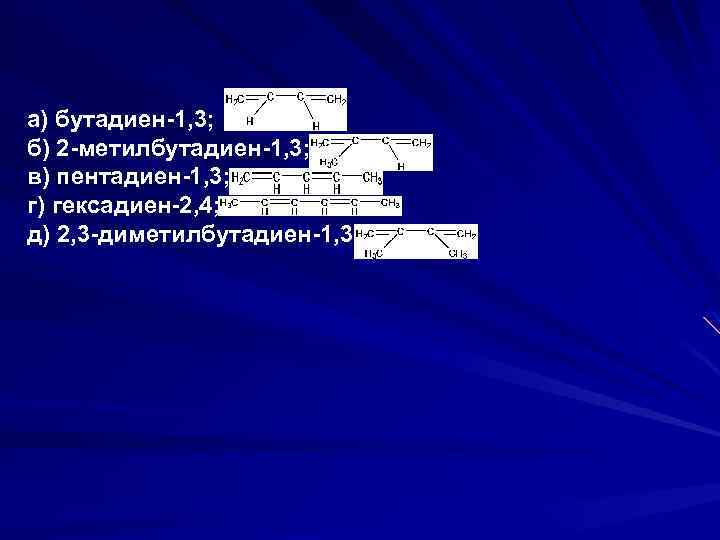 а) бутадиен-1, 3; б) 2 -метилбутадиен-1, 3; в) пентадиен-1, 3; г) гексадиен-2, 4; д) 2, 3 -диметилбутадиен-1, 3
а) бутадиен-1, 3; б) 2 -метилбутадиен-1, 3; в) пентадиен-1, 3; г) гексадиен-2, 4; д) 2, 3 -диметилбутадиен-1, 3
 5. Какие арены изомерны другу: а) орто-ксилол; б) этилбензол; в) метилбензол; г) 1 -метил-3 -этилбензол; д) мета-ксилол; е) изопропилбензол ? Ответ 1: а, б, д Ответ 2: а, г, е Ответ 3: б, в, г Ответ 4: а, в, е
5. Какие арены изомерны другу: а) орто-ксилол; б) этилбензол; в) метилбензол; г) 1 -метил-3 -этилбензол; д) мета-ксилол; е) изопропилбензол ? Ответ 1: а, б, д Ответ 2: а, г, е Ответ 3: б, в, г Ответ 4: а, в, е


