3fa38b49d38d0a83fe4222a4e8c234b8.ppt
- Количество слайдов: 66

ЗАПОРОЖСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ Кафедра клинической лабораторной диагностики НАСЛЕДСТВЕННЫЕ НАРУШЕНИЯ ОБМЕНА АМИНОКИСЛОТ кандидат медицинских наук, доцент Беленький Сергей Андреевич ЗАПОРОЖЬЕ 2016

Метаболические болезни – группа заболеваний, связанных с различными нарушениями метаболизма вследствие отсутствия определённого фермента или его недостаточности.

Причины метаболических болезней: v наследственные нарушения метаболизма (энзимопатии); v заболевания эндокринной системы; v нарушения в работе метаболически важных органов (например, печени).

Первое заболевание среди врожденных нарушений метаболизма – ОХРОНОЗ (АЛКАПТОНУРИЯ) Изучая алкаптонурию, английский врач Арчибальд Эдвард Гарро (Sir Archibald Edward Garrod, 1857 -1936) разработал в 1909 г. концепцию метаболического блока, положив начало исследованиям врожденных болезней метаболизма.

Наследственные нарушения метаболизма – 22 подкласса в зависимости от пораженного метаболического пути. Подклассы: Частота Аминоацидопатии 31% Органические ацидурии 27% Дефекты цикла мочевины 21% Дефекты дыхательной цепи 12% Гликогенозы 8% Дефекты митохондриального β-окисления 8% Перокисомные заболевания 4%

Наследственные нарушения обмена аминокислот представляют собой наиболее изученную группу генетически детерминированных энзимопатий. Они обусловлены рецессивными мутациями генов, локализованных в аутосомах.

В результате энзиматического дефекта аминокислоты не утилизируются в организме, а в тканях и биологических жидкостях накапливаются недоокисленные продукты нарушенного метаболизма, обладающие токсическим действием на ткани и органы, в первую очередь на нервную систему.

Большинство нарушений проявляется в первые недели и месяцы жизни (диспептический синдром, неврологические расстройства и изменения кожи). Совершенствование методов диагностики позволило установить частоту этой группы заболеваний, определить их значение и удельный вес в структуре патологии раннего возраста.

Частота наследственных нарушений обмена аминокислот колеблется от 1 : 10 000 до 1 : 100 000 новорожденных. Частота гетерозиготных носителей патологического гена составляет в общей популяции 1 : 100 — 1 : 400.

НАРУШЕНИЯ ТРАНСПОРТА АМИНОКИСЛОТ 1. АНОМАЛИИ ГРУППОВЫХ 2. СУБСТРАТ-СПЕЦИФИЧНЫЕ ПЕРМЕАЗНЫХ СИСТЕМ ДВУХОСНОВНАЯ АМИНОАЦИДУРИЯ, ГИСТИДИНУРИЯ, ЛИЗИНУРИЯ, ЦИСТИН-ЛИЗИНУРИЯ, БОЛЕЗНЬ ГИПЕРЦИСТЕИНУРИЯ, ХАРТНУПА МАЛЬАБСОРБЦИИ ТРИПТОФАНА И МЕТИОНИНА ДИКАРБОКСИЛАМИНОАЦИДУРИЯ, ИМИНОГЛИЦИНУРИЯ

ЦИСТИН-ЛИЗИН-УРИЯ Дефект переносчика цистеина и основных аминокислот. Относительно доброкачественное течение (уровень этих аминокислот в крови обычно не изменяется, поскольку они синтезируются в организме); возможно образование цистиновых камней в почках.

Болезнь ХАРТНУПА Нарушение переноса незаменимых нейтральных аминокислот (валин, лейцин, изолейцин, фенилаланин, триптофан, аланин, серин, тирозин). Гипераминоацидурия, признаки пеллагры (дерматит открытых участков кожи, нервно-психические расстройства) из-за недостатка витамина РР, синтезируемого из триптофана.

В настоящее время апробирована и внедряется в практику лечебных учреждений этапная биохимическая система диагностики наследственных нарушений обмена аминокислот.

Первый этап обследования (тотальный скрининг) – качественные пробы и полуколичественные методы для выявления групп детей с повышенным содержанием определённых аминокислот в крови и увеличенной экскрецией их с мочой.

Второй этап обследования Осуществление динамического наблюдения за такими детьми. Проведение количественного биохимического исследования крови и мочи, целью которого является конечная идентификация патологии.

Своевременная диагностика делает возможной раннюю патогенетическую терапию, основной принцип которой – «разгрузка» дефектной ферментной системы посредством исключения из рациона аминокислоты, не метаболизирующейся в организме.

Профилактика заболеваний, обусловленных нарушением обмена аминокислот – медико-генетическое консультирование, выявление гетерозиготных носителей патологического гена, антенатальная диагностика (определение концентрации аминокислоты в амниотической жидкости).

Гетерозиготные носители определяются с помощью нагрузочных тестов. При гетерозиготности мутантного гена активность детерминируемого им фермента, хотя и обеспечивает нормальную жизнедеятельность организма, но ниже, чем у гомозигот по нормальному гену.

Метаболизм аминокислот и нейтрализация аммониака
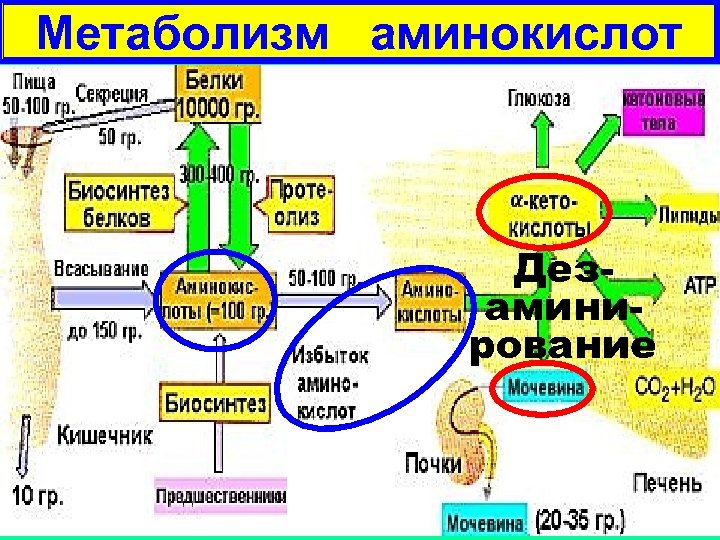
Метаболизм аминокислот Дезаминирование 20
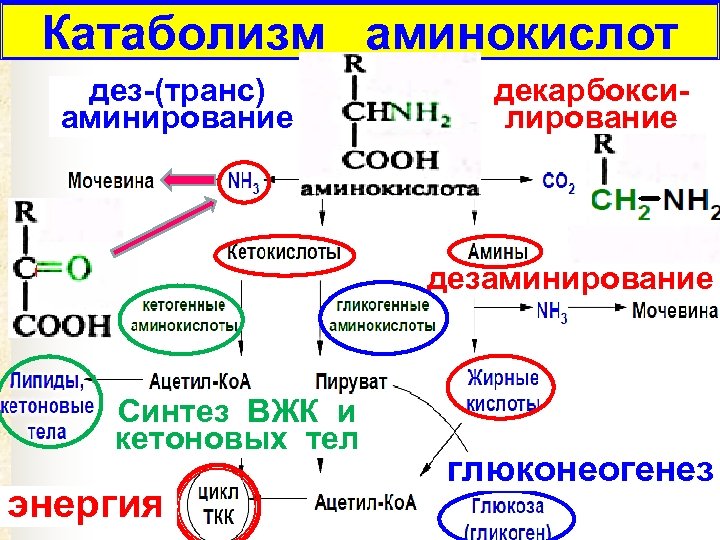
Катаболизм аминокислот дез-(транс) аминирование декарбоксилирование дезаминирование Синтез ВЖК и кетоновых тел энергия глюконеогенез 21

БИОГЕННЫЕ АМИНЫ Исходная АК Гистидин Триптофан Фенилаланин, тирозин Глутамат Биогенный амин Биологическая роль Гистамин Тканевый гормон, медиатор воспаления и аллергии Серотонин Тканевый гормон, медиатор, нейротрансмиттер Дофамин, норадреналин, адреналин Нейротрансмиттер, гормоны надпочечников (стрессассоциированные) ГАМК Тормозной нейро 22 трансмиттер ЦНС
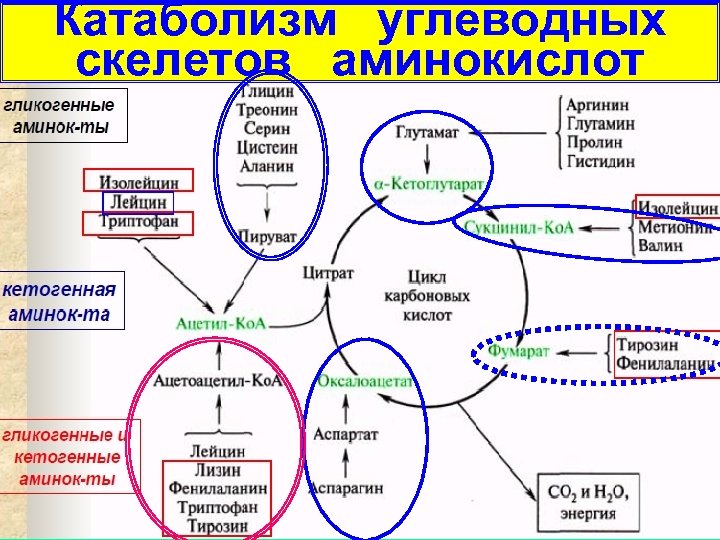
Катаболизм углеводных скелетов аминокислот 23

ТОКСИЧНОСТЬ АММОНИАКА 1. Аммониак в митохондриях сдвигает катализируемую глутаматдегидрогеназой реакцию в сторону образования глутамата: α-Кетоглутарат + NAD-H + NH 3 +. → Глутамат + NAD (снижение концентрации метаболитов ЦТК – гипоэнергетическое состояние).

ТОКСИЧНОСТЬ АММОНИАКА 2. Высокие концентрации аммониака стимулируют синтез глутамина (при участии глутаминсинтетазы): Глутамат + NH 3 + АТФ → Глутамин + АДФ + Н 3 Р 04. Накопление глутамина в астроцитах повышает в них осмотическое давление, что может вызвать отёк мозга.

ТОКСИЧНОСТЬ АММОНИАКА 3. Снижение концентрации глутамата нарушает синтез основного тормозного медиатора ГАМК (γ-аминомасляной кислоты), а также обмен аминокислот (реакций трансаминирования). При недостатке ГАМК и других медиаторов нарушается проведение нервного импульса, возникают судороги.

ТОКСИЧНОСТЬ АММОНИАКА 4. Избыток иона аммония нарушает трансмембранный перенос одновалентных катионов Na+ и К+, конкурируя с ними за ионные каналы (NH 4+ не способен проникать через мембраны), что также влияет на проведение нервных импульсов.

ТОКСИЧНОСТЬ АММОНИАКА 5. Снижение концентрации метаболитов ЦТК вызывает компенсаторное усиление синтеза оксалоацетата из пирувата, сопровождающееся интенсивным потреблением СО 2. Гипокапния из-за повышенного потребления СО 2 при гипераммониемии особенно характерна для клеток головного мозга.

ТОКСИЧНОСТЬ АММОНИАКА 6. Повышение концентрации аммониака в крови вызывает алкалоз (сдвиг р. Н в щелочную сторону), что увеличивает сродство гемоглобина к кислороду и ведёт к гипоксии тканей, от которой главным образом страдает головной мозг.

НЕЙТРАЛИЗАЦИЯ (ОБЕЗВРЕЖИВАНИЕ) АММОНИАКА Поскольку аммониак является чрезвычайно токсичным соединением, в тканях существует несколько путей его обезвреживания: 1. Синтез глутамина (взаимодействие глутамата с аммониаком) 2. Синтез аспарагина (взаимодействие аспартата с аммониаком) 3. Синтез глутамата (взаимодействие α-кетоглутарата с аммониаком) 4. Синтез карбамоилфосфата (образование мочевины, синтез нуклеотидов) 5. Синтез солей аммония (NH 4 Cl)
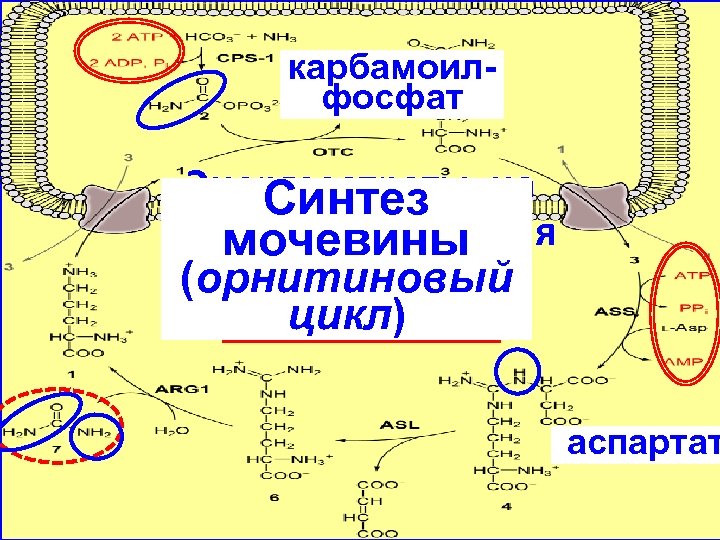
карбамоилфосфат Энергозатраты на Синтез образование 1 моля мочевины (орнитиновый мочевины – цикл) 4 моля АТФ! аспартат

Эффективность работы орнитинового цикла при нормальном питании человека и умеренных нагрузках – около 60% его мощности. Это необходимо для избежания гипераммониемии при изменении количества белка в пище, при продолжительной интенсивной физической работе или длительном голодании, при патологических состояниях, сопровождающихся интенсивным распадом белков тканей (сахарный диабет и др. ). Известны врожденные метаболические нарушения, связанные с недостатком одного из ферментов, участвующих в синтезе мочевины.
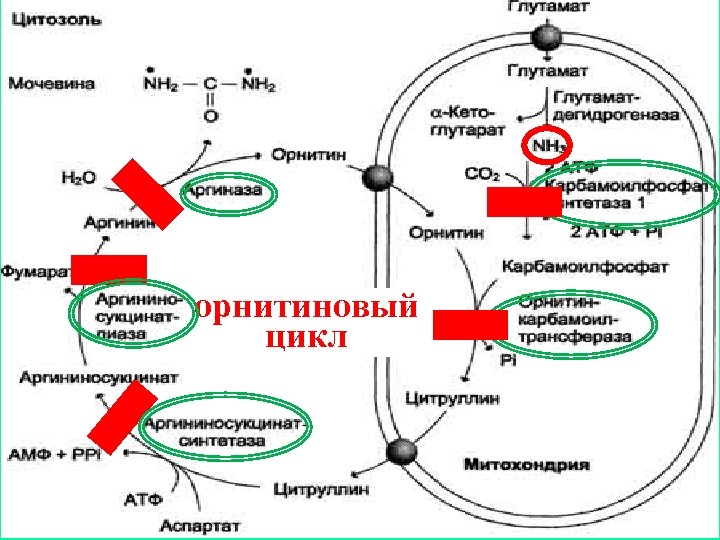
орнитиновый цикл
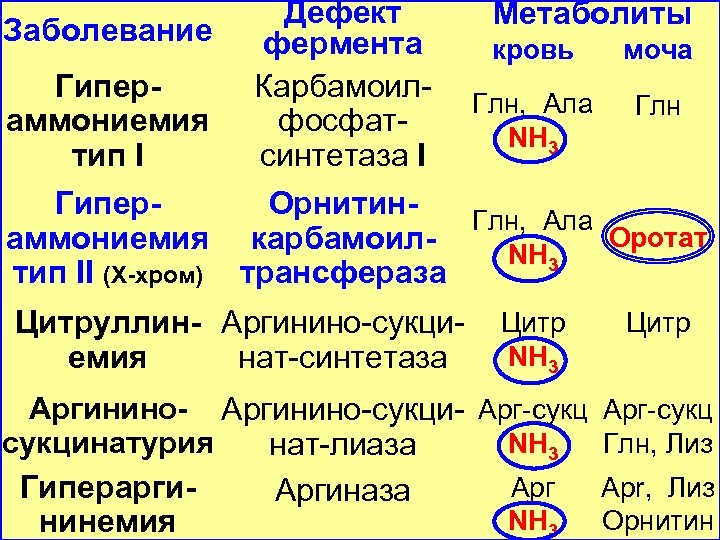
Дефект Заболевание фермента Гипер. Карбамоиламмониемия фосфаттип I синтетаза I Метаболиты кровь моча Глн, Ала NH 3 Глн Гипер- Орнитин. Глн, Ала Оротат аммониемия карбамоил. NH 3 тип II (Х-хром) трансфераза Цитруллин- Аргинино-сукциемия нат-синтетаза Цитр NH 3 Цитр Аргинино-сукци- Арг-сукцинатурия NH 3 Глн, Лиз нат-лиаза Apг Apr, Лиз Гиперарги. Аргиназа NH 3 Орнитин нинемия
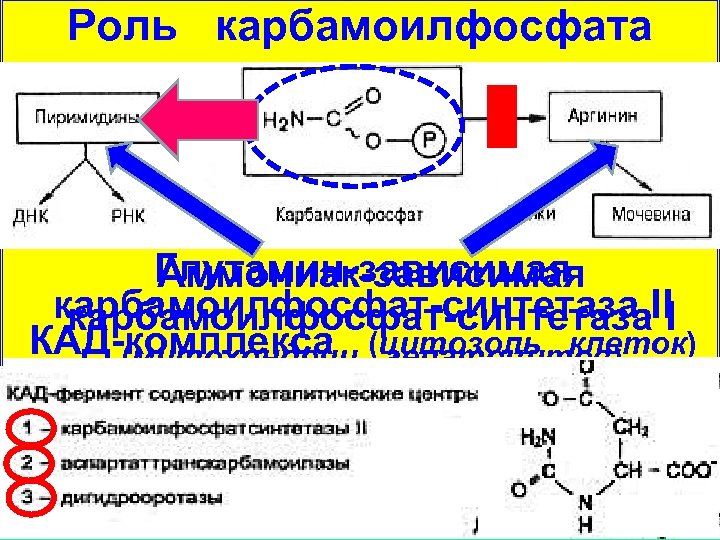
Роль карбамоилфосфата Глутамин-зависимая Аммониак-зависимая карбамоилфосфат-синтетаза ІІ карбамоилфосфат-синтетаза І КАД-комплекса (цитозоль клеток) (митохондрии гепатоцитов)

Диетическая коррекция гипераммониемий

1. Фенилпировиноградная олигофрения (фенилкетонурия).
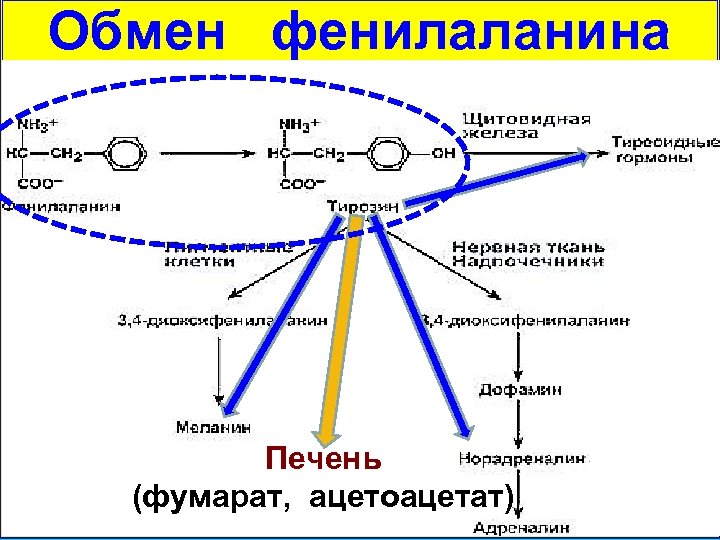
Обмен фенилаланина Печень (фумарат, ацетоацетат)
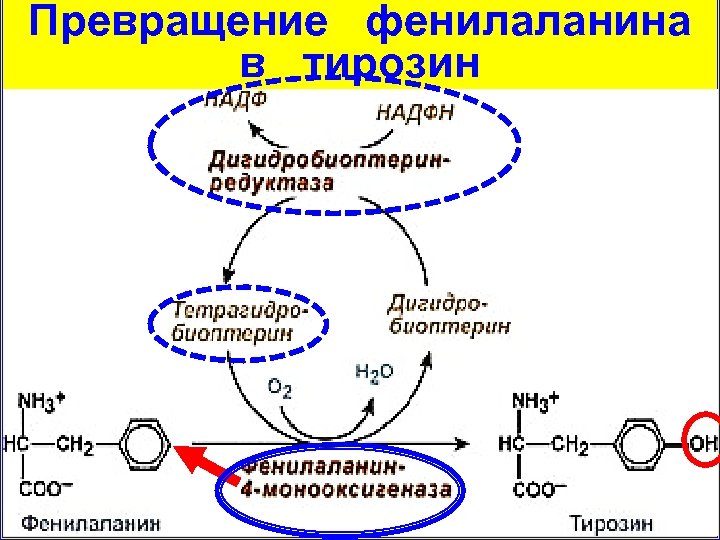
Превращение фенилаланина в тирозин

Фенилпировиноградная олигофрения Классическая форма аутосомнорецессивный генетичесий дефект фенилаланин-4 гидроксилазы (кофермент – тетрагидробиоптерин) Вариантная форма аутосомнорецессивный генетичесий дефект дигидробиоптеринредуктазы
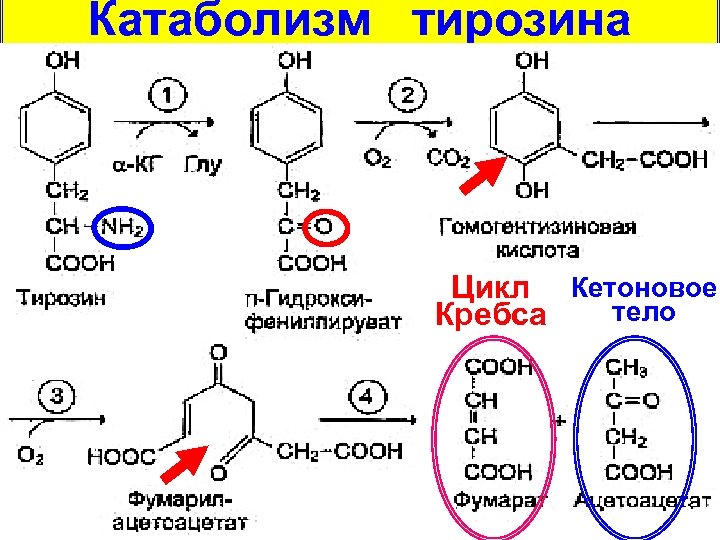
Катаболизм тирозина Цикл Кетоновое тело Кребса
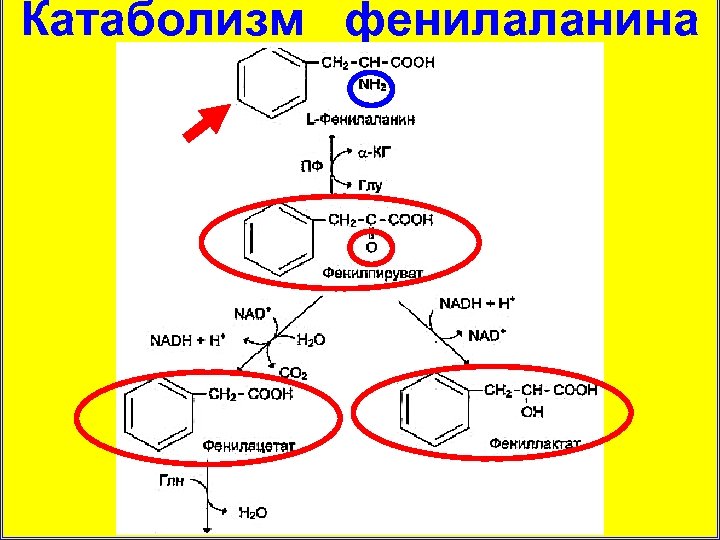
Катаболизм фенилаланина

Патогенез – увеличение содержания фенилаланина более 0, 2 г/л (норма 0, 01 -0, 02 г/л) и его прямое токсическое действие; – накопление токсичных производных – фенилпируват, фениллактат, фенилэтиламин и о-фенилацетат (нарушение метаболизма липидов в головном мозгу); – недостаточный синтез катехоламинов и меланина; – относительное снижение количества тирозина и других «больших» аминокислот, конкурирующих с фенилаланином при переносе через ГЭБ.

Клиника – сочетание деменции с атаксией, гиперкинезами (часто судороги); – вялость, артериальная гипотония (недостаточное образование катехоламинов); – светлая окраска волос, кожи и голубой цвет радужки (недостаточное образование меланинов); – экзематозные проявления (выделение аномальных метаболитов через кожу); – запах плесени или «мышиный» запах (наличие фенилуксусной кислоты в моче).

Диетическая коррекция Тирозин пищи

2. Тирозинозы.
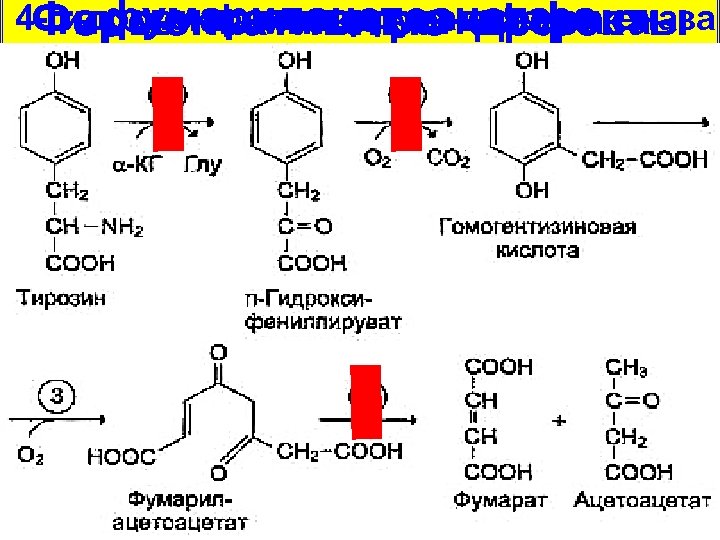
4 -гидроксифенилпируватдиоксигеназа фумарилацетоацетаза тирозинаминотрансфераза Ферментативные дефекты

Патогенез тирозинозов – увеличение содержания тирозина до 0, 06 -0, 12 г/л (норма 0, 0080, 015 г/л) и его прямое токсическое действие; – накопление тирозина в печени и других тканях, отложение его кристаллов в коже и роговице; – накопление токсичных производных (n-гидроксифенилпируват, n-гидроксифениллактат, n-гидроксифенилацетат, сукцинилацетон).

Проявления тирозинозов Отложение в тканях кристаллов тирозина (II тип) из-за превышения пределов его растворимости (помутнение роговицы, гиперкератоз кожи ладоней и подошв) или его метаболитов (I и III типы); гепатоспленомегалия, цирроз, карцинома печени, остеопороз, понос, рвота, «капустный» запах; умеренная умственная отсталость (NB! уровень фенилаланина в крови не увеличивается, т. к. катализируемая гидрокилазой фенилаланина реакция необратима!)

3. Охроноз (алкаптонурия).
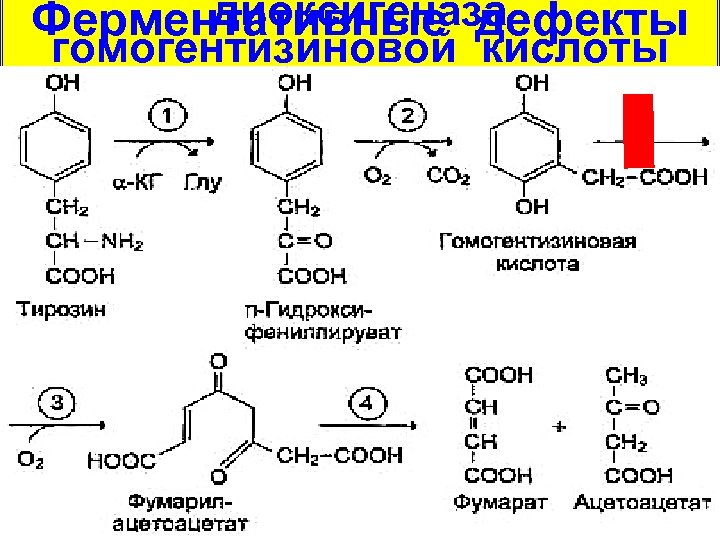
диоксигеназа Ферментативные дефекты гомогентизиновой кислоты

Проявления охроноза Избыток гомогентизиновой кислоты (частично выводясь с мочой) откладывается в соединительной ткани, особенно в коже и хрящах. Окисляясь, она полимеризуется с образованием темно-коричневого пигмента (от греч. оchros – темножелтый, nosos – болезнь). Накапливающие пигмент ткани приобретают соответствующую окраску (склеры, хрящи ушных раковин, слизистые); развиваются артриты. Пропитанные пигментом участки в последующем нередко кальцифицируются.
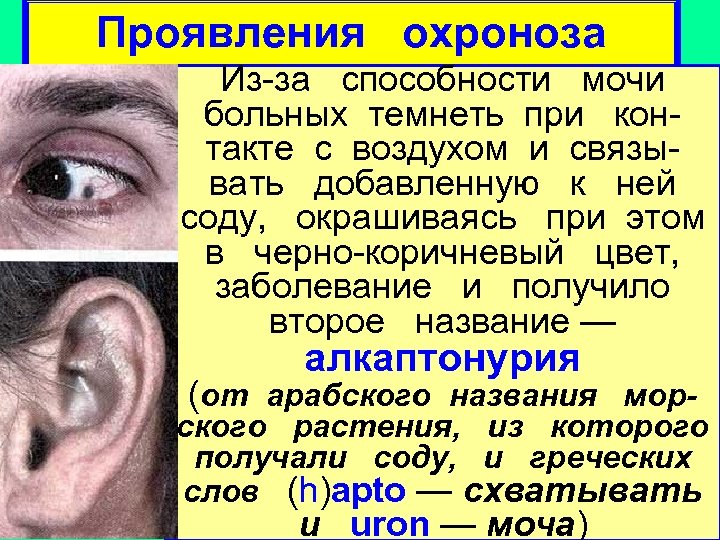
Проявления охроноза Из-за способности мочи больных темнеть при контакте с воздухом и связывать добавленную к ней соду, окрашиваясь при этом в черно-коричневый цвет, заболевание и получило второе название — алкаптонурия (от арабского названия мор- ского растения, из которого получали соду, и греческих слов (h)apto — схватывать и uron — моча)

4. Альбинизм.

Патогенез альбинизма Дефект специфической тирозиназы (кофактор – ионы Сu+) – нарушение образования пигментов (меланинов) в коже и ее придатках; часто снижена острота зрения, светобоязнь. NB! Синтез катехоламинов не нарушен, т. к. в нем участвует другой фермент (Fе 2+-зависимая гидроксилаза, кофермент которой Н 4 БП – аналогичен фенилаланингидроксилазе).
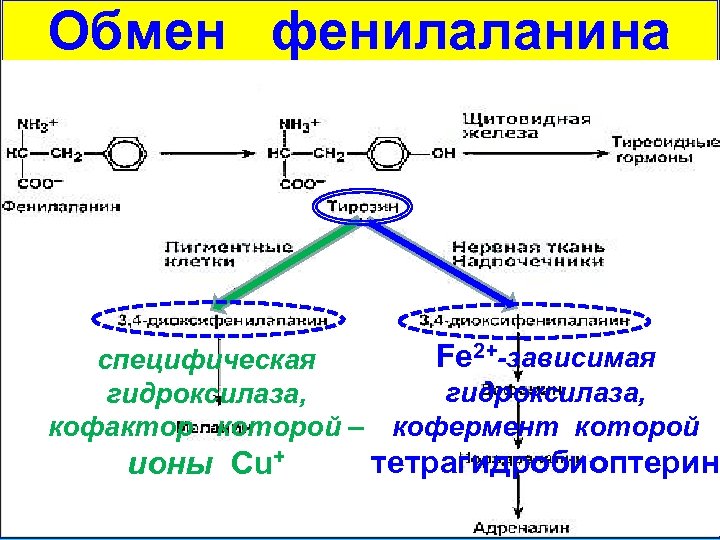
Обмен фенилаланина Fе 2+-зависимая специфическая гидроксилаза, кофактор которой – гидроксилаза, кофермент которой ионы Сu+ тетрагидробиоптерин
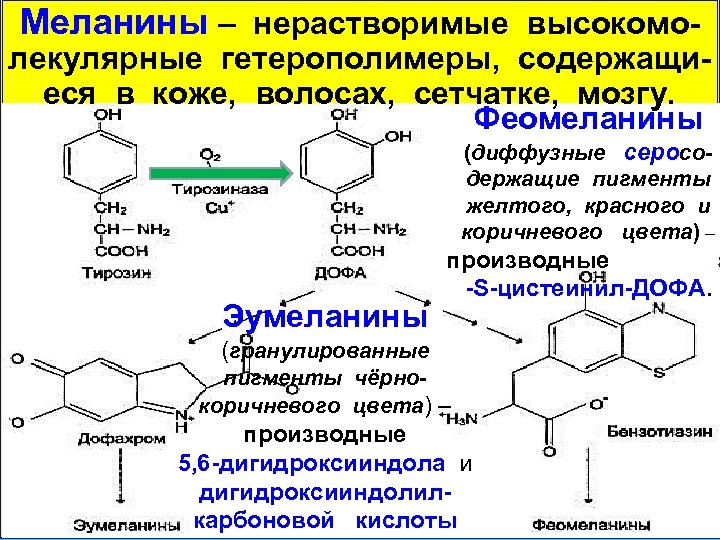
Меланины – нерастворимые высокомо- лекулярные гетерополимеры, содержащиеся в коже, волосах, сетчатке, мозгу. Феомеланины (диффузные серосодержащие пигменты желтого, красного и коричневого цвета) – Эумеланины производные 5 -S-цистеинил-ДОФА. (гранулированные пигменты чёрнокоричневого цвета) – производные 5, 6 -дигидроксииндола и дигидроксииндолилкарбоновой кислоты

5. Лейцино з (кетонурия разветвлённоцепочечных амино-, кето- и гидроксикислот; болезнь мочи с запахом кленового сиропа).

Патогенез лейциноза Энзиматический дефект – отсутствие или резкое снижение активности ферментативной системы, обеспечивающей окислительное декарбоксилирование аминокислот с разветвлённой цепью – лейцина, изолейцина и валина. Эти кислоты и продукты их дезаминирования накапливаются в организме. Наиболее патогенно накопление лейцина.
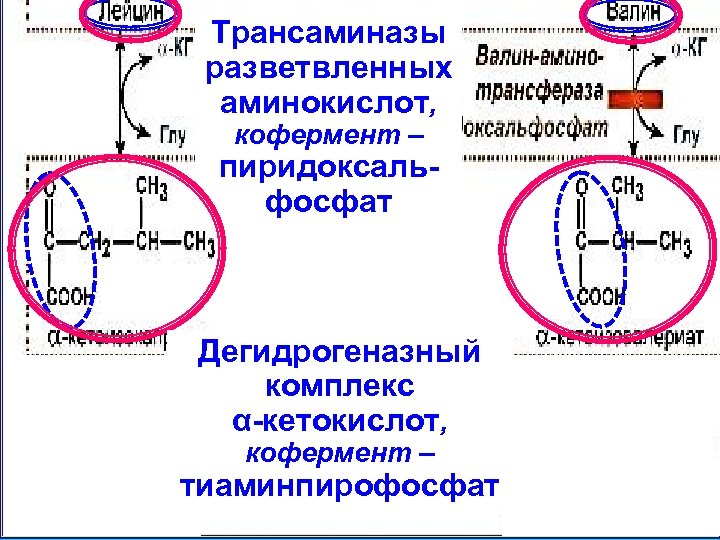
Трансаминазы Катаболизм разветвленных аминокислот с аминокислот, кофермент – разветвлённой цепью пиридоксальфосфат Дегидрогеназный комплекс α-кетокислот, кофермент – тиаминпирофосфат

Проявления лейциноза Задержка умственного развития, угнетение ЦНС, может развиваться летаргия, кома; двигательные нарушения, опистотонус; гипогликемия, кетоацидоз; гипотония; рвота, обезвоживание; своеобразный, напоминающий кленовый сироп, запах мочи, в которой обнаруживается присутствие аминокислот с разветвлённой цепью.

6. Гистидинемия
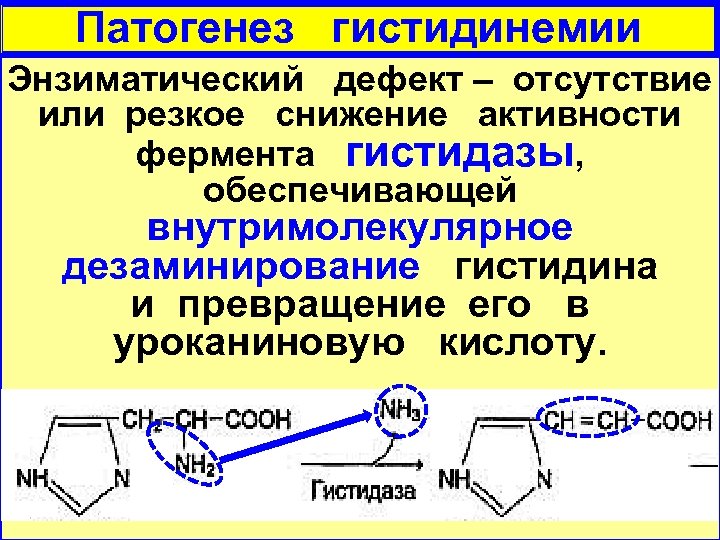
Патогенез гистидинемии Энзиматический дефект – отсутствие или резкое снижение активности фермента гистидазы, обеспечивающей внутримолекулярное дезаминирование гистидина и превращение его в уроканиновую кислоту.

Патогенез гистидинемии Потребность в гистидине для детей раннего возраста (16 -34 мг/кг) покрывается за счет молочного питания (в 100 мл молока около 30 мг гистидина), а избыток в норме полностью утилизируется гистидазой. При отсутствии или дефиците фермента в тканях накапливаются продукты окислительного(!!) дезаминирования гистидина – имидазолпировиноградная, имидазолмолочная и имидазолуксусная кислоты, оказывающие токсическое действие на ЦНС. В крови также повышается содержание гистидина.

Проявления гистидинемии Патология проявляется на первом году жизни. Дети светловолосые, голубоглазые (как при ФКУ). Тяжесть клинических проявлений вариабельна. При полном отсутствии фермента в первые 3 -4 месяца жизни – задержка психического развития, отрицательный эмоциональный комплекс; мышечная гипотония, задержка становления двигательных функций; полиморфный судорожный синдром, постепенно нарастающая клиника отека мозга.

Проявления гистидинемии При частичной недостаточности фермента в первые месяцы жизни дети развиваются нормально, в некоторых случаях наблюдается задержка становления статических и двигательных функций. Характерные симптомы – задержка формирования речевых навыков, снижение слуха, легкая возбудимость, агрессивность, боязнь новых ситуаций. В крови повышено содержание гистидина до 0, 1 -0, 15 г/л и выше.
3fa38b49d38d0a83fe4222a4e8c234b8.ppt