Минералогия_занятие_5_классификация.ppt
- Количество слайдов: 11
 Занятие № 5 КЛАССИФИКАЦИЯ МИНЕРАЛОВ Минерал – природное химическое соединение кристаллической структуры, образовавшееся в ходе геологических процессов. Минеральные индивиды Различны Алмаз (С) Анатаз (Ti. O 2) Сходны Пирит (Fe. S 2) Молибденит (Mo. S 2) Минеральный вид
Занятие № 5 КЛАССИФИКАЦИЯ МИНЕРАЛОВ Минерал – природное химическое соединение кристаллической структуры, образовавшееся в ходе геологических процессов. Минеральные индивиды Различны Алмаз (С) Анатаз (Ti. O 2) Сходны Пирит (Fe. S 2) Молибденит (Mo. S 2) Минеральный вид
 Минеральный вид – это отвлеченное понятие, которое обобщает все сходные по химическому составу и кристаллической структуре многочисленные минеральные индивиды (соответствие с понятием «биологический вид). Известно около 3500 минеральных видов Систематизация в более крупные объединения Классификации минералов
Минеральный вид – это отвлеченное понятие, которое обобщает все сходные по химическому составу и кристаллической структуре многочисленные минеральные индивиды (соответствие с понятием «биологический вид). Известно около 3500 минеральных видов Систематизация в более крупные объединения Классификации минералов
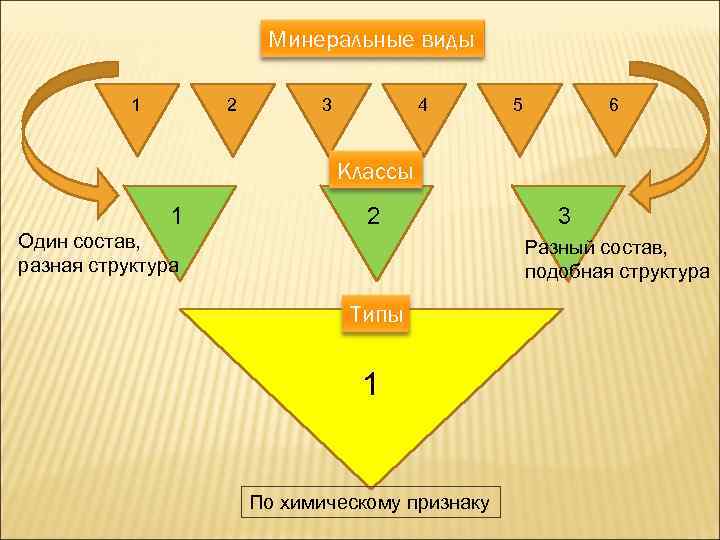 Минеральные виды 1 2 3 4 5 6 Классы 1 2 Один состав, разная структура 3 Разный состав, подобная структура Типы 1 По химическому признаку
Минеральные виды 1 2 3 4 5 6 Классы 1 2 Один состав, разная структура 3 Разный состав, подобная структура Типы 1 По химическому признаку
 КЛАССИФИКАЦИЯ МИНЕРАЛОВ Тип III Простые вещества Сернистые соединения и их аналоги Кислородные соединения Класс 1 Простые оксиды Класс 2 Сложные оксиды Класс 3 Гидроксиды Класс 4 Силикаты и их аналоги Класс 5 Фосфаты, арсенаты, ванадаты Класс 6 Сульфаты Класс 7 Хроматы, вольфраматы, молибдаты Тип IV Класс 8 Карбонаты Галогениды
КЛАССИФИКАЦИЯ МИНЕРАЛОВ Тип III Простые вещества Сернистые соединения и их аналоги Кислородные соединения Класс 1 Простые оксиды Класс 2 Сложные оксиды Класс 3 Гидроксиды Класс 4 Силикаты и их аналоги Класс 5 Фосфаты, арсенаты, ванадаты Класс 6 Сульфаты Класс 7 Хроматы, вольфраматы, молибдаты Тип IV Класс 8 Карбонаты Галогениды
 ХАРАКТЕР ХИМИЧЕСКИХ СВЯЗЕЙ В МИНЕРАЛАХ По типу кристаллохимических связей химические элементы разделяются на 3 главные группы: vс металлической связью; vс атомными (ковалентными) и отчасти с металлическими или вандервальсовыми связями; vисключительно с вандервальсовыми связями.
ХАРАКТЕР ХИМИЧЕСКИХ СВЯЗЕЙ В МИНЕРАЛАХ По типу кристаллохимических связей химические элементы разделяются на 3 главные группы: vс металлической связью; vс атомными (ковалентными) и отчасти с металлическими или вандервальсовыми связями; vисключительно с вандервальсовыми связями.
 металлические связи физические свойства: ØНепрозрачность ØМеталлический блеск ØНизкая твердость ØКовкость ØХорошая тепло- и электропроводность ковалентные связи физические свойства: ØПрозрачность ØСтеклянный блеск ØВысокая твердость ØСлабая тепло- и электропроводность Вандервальсовые связи = ковалентные связи
металлические связи физические свойства: ØНепрозрачность ØМеталлический блеск ØНизкая твердость ØКовкость ØХорошая тепло- и электропроводность ковалентные связи физические свойства: ØПрозрачность ØСтеклянный блеск ØВысокая твердость ØСлабая тепло- и электропроводность Вандервальсовые связи = ковалентные связи
 ФОРМУЛЫ МИНЕРАЛОВ Существуют разные способы написания формул При написании идеальных формул минералов мы будем придерживаться следующих правил: ØСначала указываем катионы, затем анионы или анионные радикалы - Fe. S 2 Na. Cl Mg[Si. O 4] Na[Al. Si 3 O 8] Ø Анионные радикалы записываются в квадратных скобках – Mg 2[Si. O 4], Na[Al. Si 3 O 8] Ø Катионы, занимающие разную структурную позицию, записываем в порядке убывания их координационного числа (валентности) – Ca 2 Mg 5[Si 8 O 22](OH)2 (Ca – к. ч. 8, Mg – к. ч. 6).
ФОРМУЛЫ МИНЕРАЛОВ Существуют разные способы написания формул При написании идеальных формул минералов мы будем придерживаться следующих правил: ØСначала указываем катионы, затем анионы или анионные радикалы - Fe. S 2 Na. Cl Mg[Si. O 4] Na[Al. Si 3 O 8] Ø Анионные радикалы записываются в квадратных скобках – Mg 2[Si. O 4], Na[Al. Si 3 O 8] Ø Катионы, занимающие разную структурную позицию, записываем в порядке убывания их координационного числа (валентности) – Ca 2 Mg 5[Si 8 O 22](OH)2 (Ca – к. ч. 8, Mg – к. ч. 6).
 Ø Катионы, занимающие одну и ту же структурную позицию, заключаем в круглые скобки и пишем через запятую – (Mg, Fe)2[Si. O 4]. Ø Анионы, занимающие разную структурную позицию, записываются в следующем порядке: v комплексные анионы [PO 4]3 -, [Si. O 4]4 -, [Si 2 O 7]6 -, [As. O 4]3 - – сразу за катионами – Ca [PO ] (F, Cl, OH); 5 4 3 v если анионов несколько, их располагают в порядке уменьшения коэффициента – везувиан Ca 10 Al 4 Mg 2[Si. O 4]5[Si 2 O 7]2(OH)4; Ø Гидроксильные группы обычно пишутся после комплексных анионов в круглых скобках. Ø Число молекул кристаллизационной воды указывают в конце формулы, через точку – Ca[SO 4]× 2 H 2 O (гипс).
Ø Катионы, занимающие одну и ту же структурную позицию, заключаем в круглые скобки и пишем через запятую – (Mg, Fe)2[Si. O 4]. Ø Анионы, занимающие разную структурную позицию, записываются в следующем порядке: v комплексные анионы [PO 4]3 -, [Si. O 4]4 -, [Si 2 O 7]6 -, [As. O 4]3 - – сразу за катионами – Ca [PO ] (F, Cl, OH); 5 4 3 v если анионов несколько, их располагают в порядке уменьшения коэффициента – везувиан Ca 10 Al 4 Mg 2[Si. O 4]5[Si 2 O 7]2(OH)4; Ø Гидроксильные группы обычно пишутся после комплексных анионов в круглых скобках. Ø Число молекул кристаллизационной воды указывают в конце формулы, через точку – Ca[SO 4]× 2 H 2 O (гипс).
 ЧАСТНЫЕ ФОРМУЛЫ МИНЕРАЛОВ В природе широко проявлен изоморфизм химических элементов, и минералы имеют переменный состав. Например, сфалерит (Zn. S) часто содержит в своем составе Fe. Если Fe в сфалерите 20%, то его частная формула будет (Zn 0. 8 Fe 0. 2)S. Такую формулу часто называют эмпирической, т. е. выведенной из результатов анализа данной пробы минерала. В скобках указаны атомы одной структурной позиции, они располагаются в порядке убывания коэффициентов.
ЧАСТНЫЕ ФОРМУЛЫ МИНЕРАЛОВ В природе широко проявлен изоморфизм химических элементов, и минералы имеют переменный состав. Например, сфалерит (Zn. S) часто содержит в своем составе Fe. Если Fe в сфалерите 20%, то его частная формула будет (Zn 0. 8 Fe 0. 2)S. Такую формулу часто называют эмпирической, т. е. выведенной из результатов анализа данной пробы минерала. В скобках указаны атомы одной структурной позиции, они располагаются в порядке убывания коэффициентов.
 ОПИСАНИЕ И ДИАГНОСТИКА МИНЕРАЛОВ Тип I. Простые вещества. Группа Чистые или самородные элементы Твердые растворы Интерметаллиды Минерал Медь Cu Серебро Ag Сера S Графит C Алмаз C Платина Pt Золото (Au, Ag) Осмистый иридий (Os, Jr) Купроаурид Au 2 Cu 3
ОПИСАНИЕ И ДИАГНОСТИКА МИНЕРАЛОВ Тип I. Простые вещества. Группа Чистые или самородные элементы Твердые растворы Интерметаллиды Минерал Медь Cu Серебро Ag Сера S Графит C Алмаз C Платина Pt Золото (Au, Ag) Осмистый иридий (Os, Jr) Купроаурид Au 2 Cu 3
 Спасибо за внимание! Роза кальцита
Спасибо за внимание! Роза кальцита


