3. Практика. Теория атома водорода.ppt
- Количество слайдов: 14
 Занятие 3 : Теория атома водорода 1. 1. Правило квантования орбит (для момента импульса электрона : ОСНОВНЫЕ ФОРМУЛЫ ДЛЯ РЕШЕНИЯ ЗАДАЧ 1. Первый и второй постулаты Бора Радиус n-й стационарной орбиты электрона : Радиус невозбужденного атома водорода: Скорость электрона на n-й стационарной орбите: 1. 2. Потенциальная энергия электрона в атоме водорода (водородоподобном ионе): 1. 3. Собственное значение энергии электрона Еn в водородоподобном атоме: R - постоянная Ридберга : Энергия ионизации невозбужденного атома водорода (Z = 1, n = 1) :
Занятие 3 : Теория атома водорода 1. 1. Правило квантования орбит (для момента импульса электрона : ОСНОВНЫЕ ФОРМУЛЫ ДЛЯ РЕШЕНИЯ ЗАДАЧ 1. Первый и второй постулаты Бора Радиус n-й стационарной орбиты электрона : Радиус невозбужденного атома водорода: Скорость электрона на n-й стационарной орбите: 1. 2. Потенциальная энергия электрона в атоме водорода (водородоподобном ионе): 1. 3. Собственное значение энергии электрона Еn в водородоподобном атоме: R - постоянная Ридберга : Энергия ионизации невозбужденного атома водорода (Z = 1, n = 1) :
 Потенциал ионизации атома Ui (где Ei - работа удаления электрона с i -й орбиты в бесконечность) : 2. Третий постулат Бора 2. 1. Частота кванта излучения при переходе электрона с n-й орбиты на m–ю орбиту: Здесь n – исходная, m – конечная орбиты; Еm и Еn – соответствующие значения энергии электрона. 2. 2. Длин волн, соответствующих линиям водородного спектра: При m = 1, n = 2, 3, 4, . . . - серия Лаймана (ультрафиолетовая область); При m = 2, n = 3, 4, 5, . . . - серия Бальмера (видимая область); При m = 3, n = 4, 5, 6, . . . - серия Пашена (инфракрасная область). Вывод: видимая область спектра соответствует значениям : m = 2 и n = 3, 4, 5, . . .
Потенциал ионизации атома Ui (где Ei - работа удаления электрона с i -й орбиты в бесконечность) : 2. Третий постулат Бора 2. 1. Частота кванта излучения при переходе электрона с n-й орбиты на m–ю орбиту: Здесь n – исходная, m – конечная орбиты; Еm и Еn – соответствующие значения энергии электрона. 2. 2. Длин волн, соответствующих линиям водородного спектра: При m = 1, n = 2, 3, 4, . . . - серия Лаймана (ультрафиолетовая область); При m = 2, n = 3, 4, 5, . . . - серия Бальмера (видимая область); При m = 3, n = 4, 5, 6, . . . - серия Пашена (инфракрасная область). Вывод: видимая область спектра соответствует значениям : m = 2 и n = 3, 4, 5, . . .
 1 А. (20. 1) Найти радиусы rn трёх первых боровских электронных орбит (n = 1, 2, 3) в атоме водорода (Z = 1) и скорости электрона n на этих орбитах. Z = 1 n = 1, 2, 3 rn - ? 1. Для нахождения радиусов боровских орбит и скоростей электрона на этих орбитах воспользуемся правилом квантования орбит, постулированное Н. Бором : (1) Из уравнения (1) следует, что устойчивыми являются лишь те орбиты, для которых момент импульса электрона кратен постоянной Планка. Здесь m = 9, 11 10 – 31 кг – масса электрона; n – главное квантовое число (положительный целочисленный параметр); ћ = 1, 05 10 – 34 Дж с – приведенная постоянная Планка. 2. Вторым уравнением относительно неизвестных переменных rn и n является уравнение движения, отражающее баланс сил кулоновского взаимодействия ядра с электроном и центростремительной силы : Здесь е = 1, 6 10 – 19 Кл – модуль заряда электрона; 0 = 8, 85 10 – 12 Ф/м – электрическая постоянная; Z – порядковый номер атома в таблице Менделеева (для водорода Z = 1). Решая уравнения (1) и (2), получаем: (3) (4) Численные значения для случая n = 1 : (2)
1 А. (20. 1) Найти радиусы rn трёх первых боровских электронных орбит (n = 1, 2, 3) в атоме водорода (Z = 1) и скорости электрона n на этих орбитах. Z = 1 n = 1, 2, 3 rn - ? 1. Для нахождения радиусов боровских орбит и скоростей электрона на этих орбитах воспользуемся правилом квантования орбит, постулированное Н. Бором : (1) Из уравнения (1) следует, что устойчивыми являются лишь те орбиты, для которых момент импульса электрона кратен постоянной Планка. Здесь m = 9, 11 10 – 31 кг – масса электрона; n – главное квантовое число (положительный целочисленный параметр); ћ = 1, 05 10 – 34 Дж с – приведенная постоянная Планка. 2. Вторым уравнением относительно неизвестных переменных rn и n является уравнение движения, отражающее баланс сил кулоновского взаимодействия ядра с электроном и центростремительной силы : Здесь е = 1, 6 10 – 19 Кл – модуль заряда электрона; 0 = 8, 85 10 – 12 Ф/м – электрическая постоянная; Z – порядковый номер атома в таблице Менделеева (для водорода Z = 1). Решая уравнения (1) и (2), получаем: (3) (4) Численные значения для случая n = 1 : (2)
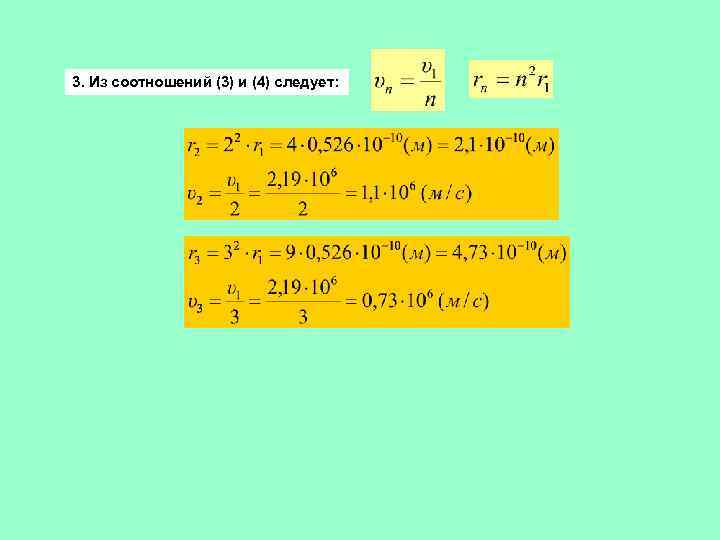 3. Из соотношений (3) и (4) следует:
3. Из соотношений (3) и (4) следует:
 2 А. (20. 4) Найти период Т обращения электрона на первой боровской орбите (n = 1) атома водорода и его угловую скорость . Z = 1 n = 1 Т - ? 1. Период обращения электрона по любой боровской орбите определим, разделив длину орбиты на скорость электрона на ней: Воспользуемся полученными в задаче 1 А выражениями для радиуса боровской орбиты и скорости электрона на ней : Подстановкой (2) и (3) в (1) получаем : 2. За один период электрон совершает вокруг ядра полный оборот, которому соответствует угол поворота 2 радиан. Для угловой частоты получаем : (1) (2) (3) (4) (5)
2 А. (20. 4) Найти период Т обращения электрона на первой боровской орбите (n = 1) атома водорода и его угловую скорость . Z = 1 n = 1 Т - ? 1. Период обращения электрона по любой боровской орбите определим, разделив длину орбиты на скорость электрона на ней: Воспользуемся полученными в задаче 1 А выражениями для радиуса боровской орбиты и скорости электрона на ней : Подстановкой (2) и (3) в (1) получаем : 2. За один период электрон совершает вокруг ядра полный оборот, которому соответствует угол поворота 2 радиан. Для угловой частоты получаем : (1) (2) (3) (4) (5)
 3 А. (20. 5) Найти наименьшую min и наибольшую max длины волн спектральных линий водорода (Z = 1) в видимой области спектра. Z = 1 min - ? max - ? 1. К видимой области спектра относятся первые линии серии Бальмера, соответствующие переходам электрона на 2 -й энергетический уровень (k = 2) с вышележащих уровней (n 3). Длины волн спектральных линий найдем из 2 -го постулата Бора: энергия излучаемого кванта ЭМ-волны при переходе электрона из n-го стационарного состояния в k-е состояние, равна разности энергий этих состояний электрона: Формула Планка для энергии фотона: (1) 2. Энергия фотона на n-й боровской орбите состоит из суммы кинетической энергии Т и потенциальной энергии U взаимодействия электрона с ядром : Отрицательный знак перед 2 -м слагаемым (2) отражает отрицательный заряд электрона (- е). Потенциал, создаваемый ядром на расстоянии rn : (2) (3) 3. Подставим (3) в (2) и воспользуемся полученными в задаче 1 А выражениями для радиуса n-й боровской орбиты rn и скорости электрона на ней n : (4)
3 А. (20. 5) Найти наименьшую min и наибольшую max длины волн спектральных линий водорода (Z = 1) в видимой области спектра. Z = 1 min - ? max - ? 1. К видимой области спектра относятся первые линии серии Бальмера, соответствующие переходам электрона на 2 -й энергетический уровень (k = 2) с вышележащих уровней (n 3). Длины волн спектральных линий найдем из 2 -го постулата Бора: энергия излучаемого кванта ЭМ-волны при переходе электрона из n-го стационарного состояния в k-е состояние, равна разности энергий этих состояний электрона: Формула Планка для энергии фотона: (1) 2. Энергия фотона на n-й боровской орбите состоит из суммы кинетической энергии Т и потенциальной энергии U взаимодействия электрона с ядром : Отрицательный знак перед 2 -м слагаемым (2) отражает отрицательный заряд электрона (- е). Потенциал, создаваемый ядром на расстоянии rn : (2) (3) 3. Подставим (3) в (2) и воспользуемся полученными в задаче 1 А выражениями для радиуса n-й боровской орбиты rn и скорости электрона на ней n : (4)
 4. Подставим (4) в (1). Получаем уравнение относительно длин волн спектральных линий kn , излучаемых при переходе электрона с n-й боровской орбиты на k-ю орбиту: (5) В полученной формуле Бальмера (5) использована постоянная Ридберга R : 5. Наименьшей разности энергий, а следовательно, наибольшей длине волны, соответствует переход с 3 -го на 2 -й уровень (n = 3, k = 2), Z = 1 : 6. В видимый диапазон попадают = 0, 4 … 0, 76 мкм. Поэтому наименьшей длине видимой волны в спектре атома водорода соответствует 4 -я линия Бальмера, min = 0, 41 мкм (переход n = 6 k = 2 ).
4. Подставим (4) в (1). Получаем уравнение относительно длин волн спектральных линий kn , излучаемых при переходе электрона с n-й боровской орбиты на k-ю орбиту: (5) В полученной формуле Бальмера (5) использована постоянная Ридберга R : 5. Наименьшей разности энергий, а следовательно, наибольшей длине волны, соответствует переход с 3 -го на 2 -й уровень (n = 3, k = 2), Z = 1 : 6. В видимый диапазон попадают = 0, 4 … 0, 76 мкм. Поэтому наименьшей длине видимой волны в спектре атома водорода соответствует 4 -я линия Бальмера, min = 0, 41 мкм (переход n = 6 k = 2 ).
 4 А. (20. 6) Найти наибольшую длину волны max ультрафиолетовой серии спектра (k = 1) водорода (серия Лаймана). Какую наименьшую скорость min должны иметь электроны, чтобы при возбуждении атомов водорода ударами электронов появилась эта линия? Z = 1 k = 1 min - ? max - ? 1. Все линии серии Лаймана (k = 1, n 2) являются ультрафиолетовыми. Наибольшей длине волны соответствует переход между ближайшими энергетическими уровнями, т. е. переход со 2 -го на 1 -й уровень (k = 1, n = 2). Для вычисления длины волны используем формулу (5) задачи 3 А : (1) 2. При нахождении минимальной скорости min налетающих электронов считаем, что вся их кинетическая энергия при соударении передается электрону атома. В результате этот электрон переходит с k - го уровня на n - й уровень: 3. Используем формулу Планка для энергии кванта: (2) (3) 4. Решим совместно уравнения (2) и (3): (1)
4 А. (20. 6) Найти наибольшую длину волны max ультрафиолетовой серии спектра (k = 1) водорода (серия Лаймана). Какую наименьшую скорость min должны иметь электроны, чтобы при возбуждении атомов водорода ударами электронов появилась эта линия? Z = 1 k = 1 min - ? max - ? 1. Все линии серии Лаймана (k = 1, n 2) являются ультрафиолетовыми. Наибольшей длине волны соответствует переход между ближайшими энергетическими уровнями, т. е. переход со 2 -го на 1 -й уровень (k = 1, n = 2). Для вычисления длины волны используем формулу (5) задачи 3 А : (1) 2. При нахождении минимальной скорости min налетающих электронов считаем, что вся их кинетическая энергия при соударении передается электрону атома. В результате этот электрон переходит с k - го уровня на n - й уровень: 3. Используем формулу Планка для энергии кванта: (2) (3) 4. Решим совместно уравнения (2) и (3): (1)
 5 А. (20. 10) В каких пределах должна лежать энергия W бомбардирующих электронов, чтобы при возбуждении атомов водорода (Z = 1) ударами этих электронов спектр водорода имел только одну спектральную линию (k = 1) ? Z = 1 k = 1 Wmin - ? Wmax - ? 1. Для получения одной линии в спектре излучения водорода необходимо и достаточно, чтобы электрон в возбужденном атоме находился на 2 -м (n = 1) уровне и после излучения фотона переходил на 1 -й (k = 1) уровень. При этом энергия налетающих электров W должна удовлетворять неравенству : (1) 2. Воспользуемся формулой энергии электрона, находящегося на n - м уровне (задача 3 А), и выразим Ek через E 1 : 3. Найдем энергию, необходимую для перехода электрона с k - го уровня n - й уровень Ekn : (2)
5 А. (20. 10) В каких пределах должна лежать энергия W бомбардирующих электронов, чтобы при возбуждении атомов водорода (Z = 1) ударами этих электронов спектр водорода имел только одну спектральную линию (k = 1) ? Z = 1 k = 1 Wmin - ? Wmax - ? 1. Для получения одной линии в спектре излучения водорода необходимо и достаточно, чтобы электрон в возбужденном атоме находился на 2 -м (n = 1) уровне и после излучения фотона переходил на 1 -й (k = 1) уровень. При этом энергия налетающих электров W должна удовлетворять неравенству : (1) 2. Воспользуемся формулой энергии электрона, находящегося на n - м уровне (задача 3 А), и выразим Ek через E 1 : 3. Найдем энергию, необходимую для перехода электрона с k - го уровня n - й уровень Ekn : (2)
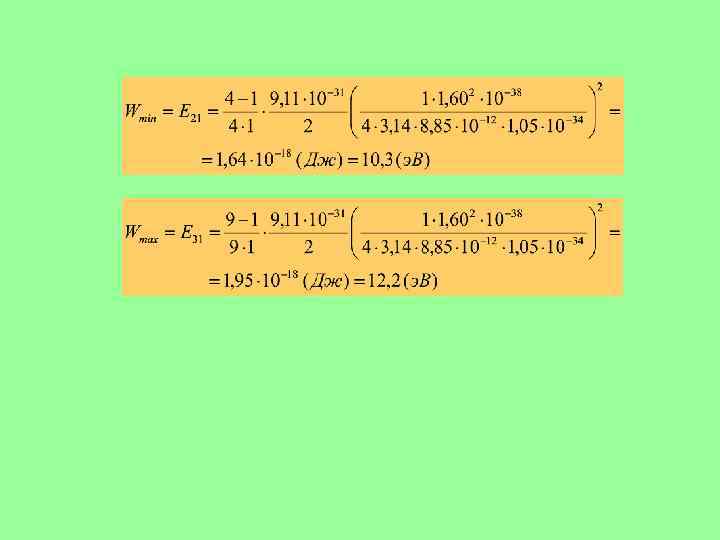
 6 А. (20. 12) В каких пределах должны лежать длины волн монохроматического света, чтобы при возбуждении атомов водорода (Z = 1) квантами этого света наблюдались три спектральные линии (k = 1) ? Z = 1 k = 1 min - ? max - ? 1. Наблюдение только трех линий спектра возможно, если электроны будут располагаться в атомах водорода на первых трех энергетических уровнях. В спектре будут присутствовать линии, соответствующие переходам: 2. Для перевода электрона из основного состояния (n = 1) не далее 3 -го уровня (k = 3), нужно, чтобы энергия фотона W не была меньше энергии перехода между 1 -м и 3 -м уровнями Е 31: 3. Но для этого длина возбуждающей волны света С должна быть короче или равна длине волны 31 кванта, излучаемого при переходе с 3 -го на 1 -й энергетический уровень : 4. Чтобы электрон не достиг 4 -го уровня, энергия фотона W не должна достигать величины энергии перехода электрона Е 41 : 5. Но для этого длина возбуждающей волны света С должна быть больше длины волны 41 фотона. С учетом (1) получим: В расчетах используем формулу Бальмера : (1)
6 А. (20. 12) В каких пределах должны лежать длины волн монохроматического света, чтобы при возбуждении атомов водорода (Z = 1) квантами этого света наблюдались три спектральные линии (k = 1) ? Z = 1 k = 1 min - ? max - ? 1. Наблюдение только трех линий спектра возможно, если электроны будут располагаться в атомах водорода на первых трех энергетических уровнях. В спектре будут присутствовать линии, соответствующие переходам: 2. Для перевода электрона из основного состояния (n = 1) не далее 3 -го уровня (k = 3), нужно, чтобы энергия фотона W не была меньше энергии перехода между 1 -м и 3 -м уровнями Е 31: 3. Но для этого длина возбуждающей волны света С должна быть короче или равна длине волны 31 кванта, излучаемого при переходе с 3 -го на 1 -й энергетический уровень : 4. Чтобы электрон не достиг 4 -го уровня, энергия фотона W не должна достигать величины энергии перехода электрона Е 41 : 5. Но для этого длина возбуждающей волны света С должна быть больше длины волны 41 фотона. С учетом (1) получим: В расчетах используем формулу Бальмера : (1)
 7 А. (20. 16) Найти длину волны де Бройля для электрона, движущегося по первой (k = 1) боровской орбите атома водорода (Z = 1). Z = 1 k - ? По де Бройлю движению любой частицы соответствует волна (волна вероятности), длина которой описывается формулой : (1) См. задачу 1 А: скорость электрона на 1 -й (k = 1) боровской орбите атома водорода (Z = 1): (2) С учетом полученного результат скорость электрона можно считать нерелятивистской ( << c). Подстановкой (2) в (1) получаем : (3)
7 А. (20. 16) Найти длину волны де Бройля для электрона, движущегося по первой (k = 1) боровской орбите атома водорода (Z = 1). Z = 1 k - ? По де Бройлю движению любой частицы соответствует волна (волна вероятности), длина которой описывается формулой : (1) См. задачу 1 А: скорость электрона на 1 -й (k = 1) боровской орбите атома водорода (Z = 1): (2) С учетом полученного результат скорость электрона можно считать нерелятивистской ( << c). Подстановкой (2) в (1) получаем : (3)
 8 А. (6. 115) Математический маятник массой m = 10 мг и длиной l = 1 см. Найти: а) энергию Е 0 нулевых колебаний маятника; б) классическую амплитуду колебаний а маятника, соответствующую энергии Е 0. m = 10 мг l = 1 см Е 0 - ? а - ? Энергию Е 0 нулевых колебаний маятника определяет выражение: ( - угловая частота колебаний) (1) Амплитуду колебаний маятника (длина дуги АВ) можно характеризовать углом отклонения от вертикали и проекцией дуги на горизонтальную ось а. Для малых колебаний ( << /2) проекция перемещения на горизонтальную ось а практически совпадает с дугой АВ: В точке наибольшего отклонения (т. В) из точки покоя (т. А) кинетическая энергия равна нулю (Т = 0), а полная энергия равна потенциальной энергии (U) в поле сил тяжести : (2) Найдем высоту подъема маятника h и подставим в (2) и далее в (1): (3) (4)
8 А. (6. 115) Математический маятник массой m = 10 мг и длиной l = 1 см. Найти: а) энергию Е 0 нулевых колебаний маятника; б) классическую амплитуду колебаний а маятника, соответствующую энергии Е 0. m = 10 мг l = 1 см Е 0 - ? а - ? Энергию Е 0 нулевых колебаний маятника определяет выражение: ( - угловая частота колебаний) (1) Амплитуду колебаний маятника (длина дуги АВ) можно характеризовать углом отклонения от вертикали и проекцией дуги на горизонтальную ось а. Для малых колебаний ( << /2) проекция перемещения на горизонтальную ось а практически совпадает с дугой АВ: В точке наибольшего отклонения (т. В) из точки покоя (т. А) кинетическая энергия равна нулю (Т = 0), а полная энергия равна потенциальной энергии (U) в поле сил тяжести : (2) Найдем высоту подъема маятника h и подставим в (2) и далее в (1): (3) (4)
 9 А. (6. 119) Чему равен квадрат орбитального момента импульса М 2 электрона в состояниях а) 2 р ; б) 5 f ? 2 р: n = 2, l = 1 5 f: n = 5, l = 3 М 2 - ? Модуль орбитального момента импульса описывается выражением: Орбитальное (азимутальное) квантовое число: (1) Область изменений орбитального квантового числа : Совокупность электронов с одним и тем же значением главного квантового числа n образует электронную оболочку (обозначается буквами: s, p, d, f, g, … ). Электроны с одинаковыми значениями главного n и азимутального l квантовых чисел образуют электронную подоболочку (обозначается цифрами: 1, 2, 3, 4, … ). В обозначении состояния электрона номер главного квантового числа n указывают перед обозначением азимутального l квантового числа (1 s, 2 p, …). Число l всегда меньше на единицу числа n. Возможны следующие состояния электрона: Воспользуемся выражением (1):
9 А. (6. 119) Чему равен квадрат орбитального момента импульса М 2 электрона в состояниях а) 2 р ; б) 5 f ? 2 р: n = 2, l = 1 5 f: n = 5, l = 3 М 2 - ? Модуль орбитального момента импульса описывается выражением: Орбитальное (азимутальное) квантовое число: (1) Область изменений орбитального квантового числа : Совокупность электронов с одним и тем же значением главного квантового числа n образует электронную оболочку (обозначается буквами: s, p, d, f, g, … ). Электроны с одинаковыми значениями главного n и азимутального l квантовых чисел образуют электронную подоболочку (обозначается цифрами: 1, 2, 3, 4, … ). В обозначении состояния электрона номер главного квантового числа n указывают перед обозначением азимутального l квантового числа (1 s, 2 p, …). Число l всегда меньше на единицу числа n. Возможны следующие состояния электрона: Воспользуемся выражением (1):


