ЗАНЯТИЕ 1 ПРЕДМЕТ И ЗАДАЧИ СОВРЕМЕННОЙ ИММУНОЛОГИИ. ОСНОВНЫЕ





















































































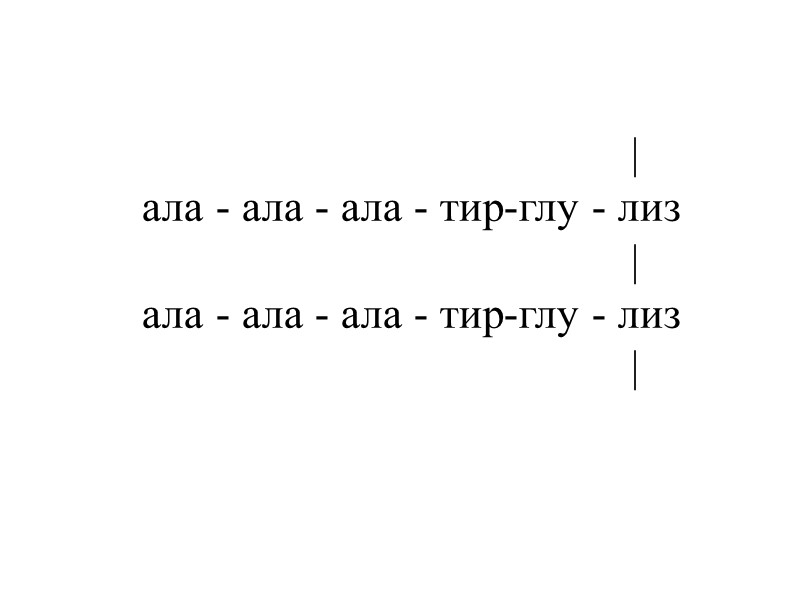
















23612-zan_1_2_lechfac.ppt
- Количество слайдов: 137
 ЗАНЯТИЕ 1 ПРЕДМЕТ И ЗАДАЧИ СОВРЕМЕННОЙ ИММУНОЛОГИИ. ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ. ИСТОРИЯ
ЗАНЯТИЕ 1 ПРЕДМЕТ И ЗАДАЧИ СОВРЕМЕННОЙ ИММУНОЛОГИИ. ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ. ИСТОРИЯ
 Современная иммунология как наука изучает молекулярные, клеточные, генетические механизмы функционирования иммунной системы. Главная функция иммунной системы – поддержание генетического (фенотипического) постоянства (однородности, индивидуальности, гомеостаза) организма.
Современная иммунология как наука изучает молекулярные, клеточные, генетические механизмы функционирования иммунной системы. Главная функция иммунной системы – поддержание генетического (фенотипического) постоянства (однородности, индивидуальности, гомеостаза) организма.
 Реализация этой функции иммунной системы в норме обеспечивается за счет: 1) распознавания «чужого» и «измененного своего»; 2) их элиминации в результате эффекторных механизмов врожденного и приобретенного иммунитета; 3) сохранения способности к более высокому ответу при повторном контакте с теми же антигенами (иммунологическая память)
Реализация этой функции иммунной системы в норме обеспечивается за счет: 1) распознавания «чужого» и «измененного своего»; 2) их элиминации в результате эффекторных механизмов врожденного и приобретенного иммунитета; 3) сохранения способности к более высокому ответу при повторном контакте с теми же антигенами (иммунологическая память)
 Реализуя эту функцию иммунная система обеспечивает: - противоинфекционный иммунитет (противовирусный, антибактериальный, противопаразитарный иммунитет); - противоопухолевый иммунитет, элиминацию стареющих и измененных в результате мутаций клеток, контроль за пролиферацией и дифференцировкой клеток; - реакции против антигенов гистосовместимости (отторжение органов и тканей при трансплантации и иммунология репродукции);
Реализуя эту функцию иммунная система обеспечивает: - противоинфекционный иммунитет (противовирусный, антибактериальный, противопаразитарный иммунитет); - противоопухолевый иммунитет, элиминацию стареющих и измененных в результате мутаций клеток, контроль за пролиферацией и дифференцировкой клеток; - реакции против антигенов гистосовместимости (отторжение органов и тканей при трансплантации и иммунология репродукции);
 При нарушении функций иммунной системы возможны: - реакции против своих собственных антигенов (аутоиммунная патология); -избыточные реакции против экзогенных антигенов (аллергенов) - аллергические реакции.
При нарушении функций иммунной системы возможны: - реакции против своих собственных антигенов (аутоиммунная патология); -избыточные реакции против экзогенных антигенов (аллергенов) - аллергические реакции.
 Врожденные и приобретенные дефекты функционирования отдельных компонентов иммунной системы – первичные иммунодефициты и вторичная иммунная недостаточность – лежат в основе тяжелых, не поддающихся терапии инфекционных процессов.
Врожденные и приобретенные дефекты функционирования отдельных компонентов иммунной системы – первичные иммунодефициты и вторичная иммунная недостаточность – лежат в основе тяжелых, не поддающихся терапии инфекционных процессов.
 В своем историческом развитии иммунология как наука прошла 3 основных этапа: Первый - открытие иммунитета как повышенной устойчивости к повторному заражению теми или иными инфекционными заболеваниями. ИСТОРИЯ ИММУНОЛОГИИ
В своем историческом развитии иммунология как наука прошла 3 основных этапа: Первый - открытие иммунитета как повышенной устойчивости к повторному заражению теми или иными инфекционными заболеваниями. ИСТОРИЯ ИММУНОЛОГИИ
 Древний Китай Турция Черкесы Леди Мэри Монтегю, жена британского посла в Константинополе, заразила оспой ребенка, который родился у нее в Турции (1721 г). Вариоляция
Древний Китай Турция Черкесы Леди Мэри Монтегю, жена британского посла в Константинополе, заразила оспой ребенка, который родился у нее в Турции (1721 г). Вариоляция
 В том же 18-м веке в Англии было известно, что доярки, которым приходилось сталкиваться с коровьей оспой, редко заболевали натуральной оспой. В 1774 г. английский крестьянин Беджамин Джести, чтобы защитить свою жену от оспы, нанес ей на кожу предплечья содержимое больных оспой коров. Вакцинация
В том же 18-м веке в Англии было известно, что доярки, которым приходилось сталкиваться с коровьей оспой, редко заболевали натуральной оспой. В 1774 г. английский крестьянин Беджамин Джести, чтобы защитить свою жену от оспы, нанес ей на кожу предплечья содержимое больных оспой коров. Вакцинация
 Днем рождения иммунологии считается 14 мая 1796 года, когда Эдвард Дженнер перенес содержимое оспенных пустул от доярки Сары Нельмс 8-летнему мальчику Джемсу Филлипсу. Спустя 1,5 месяца он публично перенес ему содержимое пустул от больного натуральной оспой, мальчик не заболел. Через несколько месяцев и через 5 лет - повторные заражения – заболевания не последовало - развился стойкий иммунитет. С тех пор по всему миру были созданы оспопрививальные пункты. Это было рождением научного подхода к применению активной иммунизации и началом развития иммунологии. К сожалению, Дженнер не сумел увидеть в открытом им способе борьбы с оспой общего принципа предохранения от инфекционных заболеваний и не сделал попытки, объяснить почему его вакцина создает иммунитет.
Днем рождения иммунологии считается 14 мая 1796 года, когда Эдвард Дженнер перенес содержимое оспенных пустул от доярки Сары Нельмс 8-летнему мальчику Джемсу Филлипсу. Спустя 1,5 месяца он публично перенес ему содержимое пустул от больного натуральной оспой, мальчик не заболел. Через несколько месяцев и через 5 лет - повторные заражения – заболевания не последовало - развился стойкий иммунитет. С тех пор по всему миру были созданы оспопрививальные пункты. Это было рождением научного подхода к применению активной иммунизации и началом развития иммунологии. К сожалению, Дженнер не сумел увидеть в открытом им способе борьбы с оспой общего принципа предохранения от инфекционных заболеваний и не сделал попытки, объяснить почему его вакцина создает иммунитет.
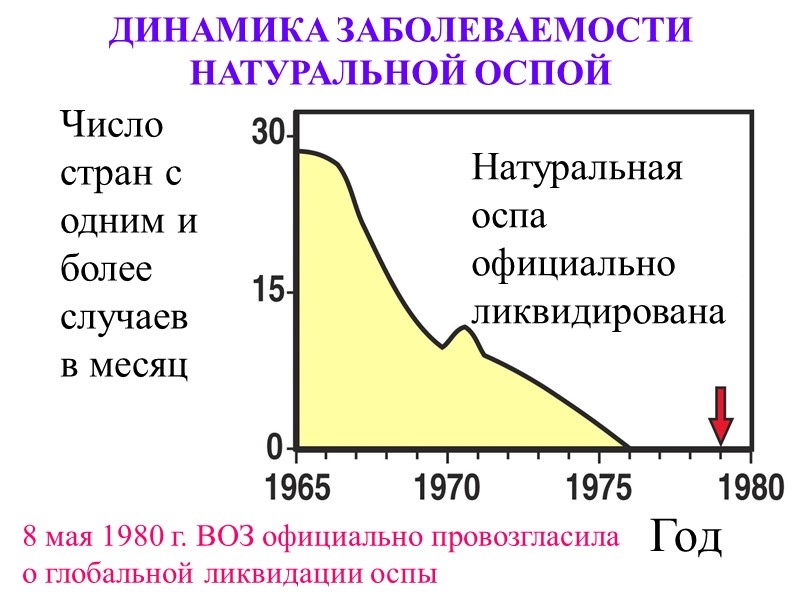
 ДИНАМИКА ЗАБОЛЕВАЕМОСТИ НАТУРАЛЬНОЙ ОСПОЙ Год Число стран с одним и более случаев в месяц Натуральная оспа официально ликвидирована 8 мая 1980 г. ВОЗ официально провозгласила о глобальной ликвидации оспы
ДИНАМИКА ЗАБОЛЕВАЕМОСТИ НАТУРАЛЬНОЙ ОСПОЙ Год Число стран с одним и более случаев в месяц Натуральная оспа официально ликвидирована 8 мая 1980 г. ВОЗ официально провозгласила о глобальной ликвидации оспы
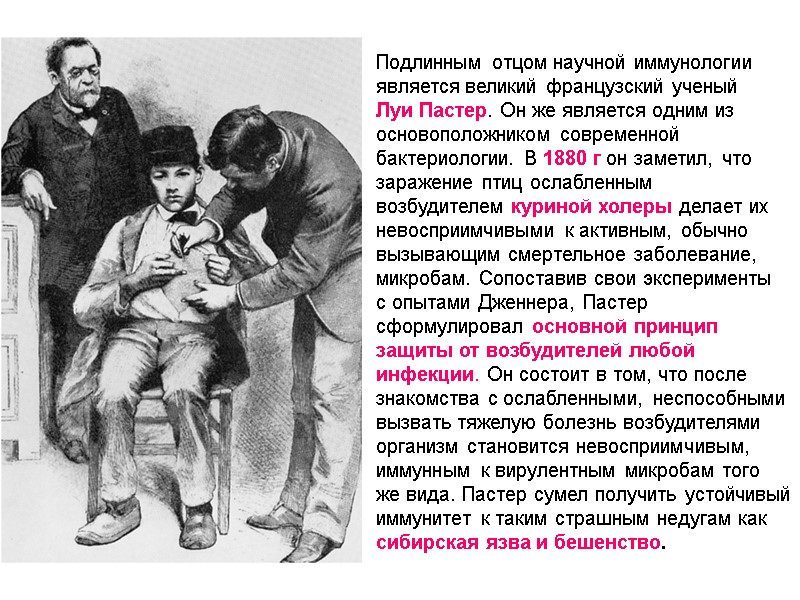
 Figure 1-1 Подлинным отцом научной иммунологии является великий французский ученый Луи Пастер. Он же является одним из основоположником современной бактериологии. В 1880 г он заметил, что заражение птиц ослабленным возбудителем куриной холеры делает их невосприимчивыми к активным, обычно вызывающим смертельное заболевание, микробам. Сопоставив свои эксперименты с опытами Дженнера, Пастер сформулировал основной принцип защиты от возбудителей любой инфекции. Он состоит в том, что после знакомства с ослабленными, неспособными вызвать тяжелую болезнь возбудителями организм становится невосприимчивым, иммунным к вирулентным микробам того же вида. Пастер сумел получить устойчивый иммунитет к таким страшным недугам как сибирская язва и бешенство.
Figure 1-1 Подлинным отцом научной иммунологии является великий французский ученый Луи Пастер. Он же является одним из основоположником современной бактериологии. В 1880 г он заметил, что заражение птиц ослабленным возбудителем куриной холеры делает их невосприимчивыми к активным, обычно вызывающим смертельное заболевание, микробам. Сопоставив свои эксперименты с опытами Дженнера, Пастер сформулировал основной принцип защиты от возбудителей любой инфекции. Он состоит в том, что после знакомства с ослабленными, неспособными вызвать тяжелую болезнь возбудителями организм становится невосприимчивым, иммунным к вирулентным микробам того же вида. Пастер сумел получить устойчивый иммунитет к таким страшным недугам как сибирская язва и бешенство.
 Второй этап, приходящийся на конец 19-го и начало 20-го веков, охарактеризовался открытием основных иммунологических феноменов: 1) антителообразования или гуморального иммунного ответа, 2) реакции гиперчувствительности замедленного типа (ГЗТ), 3) фагоцитоза, роли комплемента в иммунных реакциях. Этот этап продолжился до конца 50-х годов 20 века.
Второй этап, приходящийся на конец 19-го и начало 20-го веков, охарактеризовался открытием основных иммунологических феноменов: 1) антителообразования или гуморального иммунного ответа, 2) реакции гиперчувствительности замедленного типа (ГЗТ), 3) фагоцитоза, роли комплемента в иммунных реакциях. Этот этап продолжился до конца 50-х годов 20 века.
 1) Нобелевская премия 1901 г. Эмиль фон Беринг (Emil von Behring) Первой Нобелевской премии по физиологии и медицине был удостоен Эмиль Адольф фон Беринг. Свои исследования фон Беринг проводил у Роберта Коха в Коховском институте в Берлине. После того как в 1883 г. Леффлер выделил дифтерийную бациллу, а Ру и Йерсин в 1888 г. обнаружили дифтерийный экзотоксин, фон Беринг со своими сотрудникам Китасато и Вернике в 1890-1892 гг. показали, что иммунитет к дифтерии и столбняку зависит от образования антитоксинов, циркулирующих в крови. Он показал, что пассивное введение антитоксической сыворотки может обеспечить выздоровление больных, и этим положил начало сывороточной иммунотерапии разнообразных болезней.
1) Нобелевская премия 1901 г. Эмиль фон Беринг (Emil von Behring) Первой Нобелевской премии по физиологии и медицине был удостоен Эмиль Адольф фон Беринг. Свои исследования фон Беринг проводил у Роберта Коха в Коховском институте в Берлине. После того как в 1883 г. Леффлер выделил дифтерийную бациллу, а Ру и Йерсин в 1888 г. обнаружили дифтерийный экзотоксин, фон Беринг со своими сотрудникам Китасато и Вернике в 1890-1892 гг. показали, что иммунитет к дифтерии и столбняку зависит от образования антитоксинов, циркулирующих в крови. Он показал, что пассивное введение антитоксической сыворотки может обеспечить выздоровление больных, и этим положил начало сывороточной иммунотерапии разнообразных болезней.
 Беринг (Behring) вместе со своими коллегами Вернике (Wernicke) слева и Фрошем (Frosch) в центре в лаборатории Роберта Коха в Берлине. В 1890 г. вместе со своим университетским другом Эрихом Вернике он сумел создать первую эффективную терапевтическую сыворотку против дифтерии.
Беринг (Behring) вместе со своими коллегами Вернике (Wernicke) слева и Фрошем (Frosch) в центре в лаборатории Роберта Коха в Берлине. В 1890 г. вместе со своим университетским другом Эрихом Вернике он сумел создать первую эффективную терапевтическую сыворотку против дифтерии.
 Шибасабуро Китазато (Shibasaburo Kitasato) Вместе с Shibasaburo Kitasato он разработал эффективную терапевтическую сыворотку против столбняка.
Шибасабуро Китазато (Shibasaburo Kitasato) Вместе с Shibasaburo Kitasato он разработал эффективную терапевтическую сыворотку против столбняка.
 В Перми промышленное производство первых лечебных сывороток против дифтерии было начато под руководством профессора Владимира Михайловича Здравосмыслова в 1900 году.
В Перми промышленное производство первых лечебных сывороток против дифтерии было начато под руководством профессора Владимира Михайловича Здравосмыслова в 1900 году.
 2) Нобелевская премия 1905 г. Роберт Кох (Robert Koch) Премия присуждена “за его исследования и открытия, связанные с туберкулёзом”. Р. Кох является основоположником современной бактериологии, им разработаны методы культивирования бактерий в агаровых средах. Для иммунологии наиболее важное значение имеют работы по реакции гиперчувствительности замедленного типа (ГЗТ). Иммунодиагностика с помощью туберкулинового теста и “феномен Коха”, который состоит в повышенной кожной реакции на микобактерии туберкулеза при введении их в кожу сенсибилизированных животных, сыграли решающую роль в изучении механизмов клеточного иммунитета. Как было доказано впоследствии в 1970-х гг. эти реакции опосредуются Т-эффекторами ГЗТ (или активированными Тh1-клетками), а не антителами, т.е. фактически в 1890 г. при изучении туберкулеза им был открыт новый тип иммунных реакций – реакции клеточноопосредованного иммунитета.
2) Нобелевская премия 1905 г. Роберт Кох (Robert Koch) Премия присуждена “за его исследования и открытия, связанные с туберкулёзом”. Р. Кох является основоположником современной бактериологии, им разработаны методы культивирования бактерий в агаровых средах. Для иммунологии наиболее важное значение имеют работы по реакции гиперчувствительности замедленного типа (ГЗТ). Иммунодиагностика с помощью туберкулинового теста и “феномен Коха”, который состоит в повышенной кожной реакции на микобактерии туберкулеза при введении их в кожу сенсибилизированных животных, сыграли решающую роль в изучении механизмов клеточного иммунитета. Как было доказано впоследствии в 1970-х гг. эти реакции опосредуются Т-эффекторами ГЗТ (или активированными Тh1-клетками), а не антителами, т.е. фактически в 1890 г. при изучении туберкулеза им был открыт новый тип иммунных реакций – реакции клеточноопосредованного иммунитета.
 Илья Ильич Мечников Пауль Эрлих (Paul Ehrlich) 3) Нобелевская премия 1908 г.
Илья Ильич Мечников Пауль Эрлих (Paul Ehrlich) 3) Нобелевская премия 1908 г.
 Пауль Эрлих (Paul Ehrlich)
Пауль Эрлих (Paul Ehrlich)
 Во время круиза на яхте принца Монако при исследовании реакций, возникающих при введении животным ядов, полученных от морских беспозвоночных, вместе с Полем Портье он в 1902 г. открыл явление анафилаксии или реакции гиперчувствительности немедленного типа. 4) Нобелевская премия 1913 г. Шарль Рише (Charles Richet)
Во время круиза на яхте принца Монако при исследовании реакций, возникающих при введении животным ядов, полученных от морских беспозвоночных, вместе с Полем Портье он в 1902 г. открыл явление анафилаксии или реакции гиперчувствительности немедленного типа. 4) Нобелевская премия 1913 г. Шарль Рише (Charles Richet)
 В 1896 году роль комплемента и антител в механизме комплементзависимого бактериолиза, а в 1898 году открыл феномен специфического иммунного гемолиза. Таким образом был открыт классический путь активации белков системы комплемента. 5) Нобелевская премия 1919 г. Жюль Борде (Jules Bordet)
В 1896 году роль комплемента и антител в механизме комплементзависимого бактериолиза, а в 1898 году открыл феномен специфического иммунного гемолиза. Таким образом был открыт классический путь активации белков системы комплемента. 5) Нобелевская премия 1919 г. Жюль Борде (Jules Bordet)
 В своих ранних исследованиях по антиэритроцитарным антителам он описал в 1901 г. ряд изогемагглютининов человека, которые в наше время составляют систему групп крови АВО. В 1926 г. Ландштейнер и Фелип Левин открыли систему MNP, а в 1940 г. вместе с Альбертом Винером – систему групп крови Rh. Большую роль сыграли работы по антигенной специфичности, выполненные в 1930-1940 гг. 6) Нобелевская премия 1930 г. Карл Ландштейнер (Karl Landsteiner)
В своих ранних исследованиях по антиэритроцитарным антителам он описал в 1901 г. ряд изогемагглютининов человека, которые в наше время составляют систему групп крови АВО. В 1926 г. Ландштейнер и Фелип Левин открыли систему MNP, а в 1940 г. вместе с Альбертом Винером – систему групп крови Rh. Большую роль сыграли работы по антигенной специфичности, выполненные в 1930-1940 гг. 6) Нобелевская премия 1930 г. Карл Ландштейнер (Karl Landsteiner)
 7) Нобелевская премия 1951 г. Макс Тейлор (Max Theiler) Премия присуждена Максу Тейлору “ за разработку вакцины против желтой лихорадки”. В конце 30-х годов ему удалось получить аттенуированные штаммы вируса жёлтой лихорадки; для этого он применил серийные пассажи in vitro на культурах ткани мышей и куриных эмбрионов. Этими методами были созданы штаммы, которые сохраняли свою иммуногенность, но были лишены патогенности и составили основу современных эффективных вакцин против жёлтой лихорадки.
7) Нобелевская премия 1951 г. Макс Тейлор (Max Theiler) Премия присуждена Максу Тейлору “ за разработку вакцины против желтой лихорадки”. В конце 30-х годов ему удалось получить аттенуированные штаммы вируса жёлтой лихорадки; для этого он применил серийные пассажи in vitro на культурах ткани мышей и куриных эмбрионов. Этими методами были созданы штаммы, которые сохраняли свою иммуногенность, но были лишены патогенности и составили основу современных эффективных вакцин против жёлтой лихорадки.
 8) Нобелевская премия 1957 г. Даниэль Бове (Daniel Bovet) Премия присуждена Д. Бове, швейцарскому физиологу и фармакологу, “за разработку антигистаминовых препаратов для лечения аллергии”. Среди факторов, которые освобождаются при анафилаксии, наиболее важными являются гистамин, серотонин и другие, это привело его к поиску веществ, способных подавлять действие гистамина; в результате появились лекарственные препараты, оказавшиеся эффективным средством лечения астмы и сенной лихорадки
8) Нобелевская премия 1957 г. Даниэль Бове (Daniel Bovet) Премия присуждена Д. Бове, швейцарскому физиологу и фармакологу, “за разработку антигистаминовых препаратов для лечения аллергии”. Среди факторов, которые освобождаются при анафилаксии, наиболее важными являются гистамин, серотонин и другие, это привело его к поиску веществ, способных подавлять действие гистамина; в результате появились лекарственные препараты, оказавшиеся эффективным средством лечения астмы и сенной лихорадки
 Питер Медавар (Peter Medawar) Ф. Макфарлейн Бернет (Frank Macfarlane Burnet) 9) Нобелевская премия 1960 г. за открытие приобретённой иммунологической толерантности
Питер Медавар (Peter Medawar) Ф. Макфарлейн Бернет (Frank Macfarlane Burnet) 9) Нобелевская премия 1960 г. за открытие приобретённой иммунологической толерантности
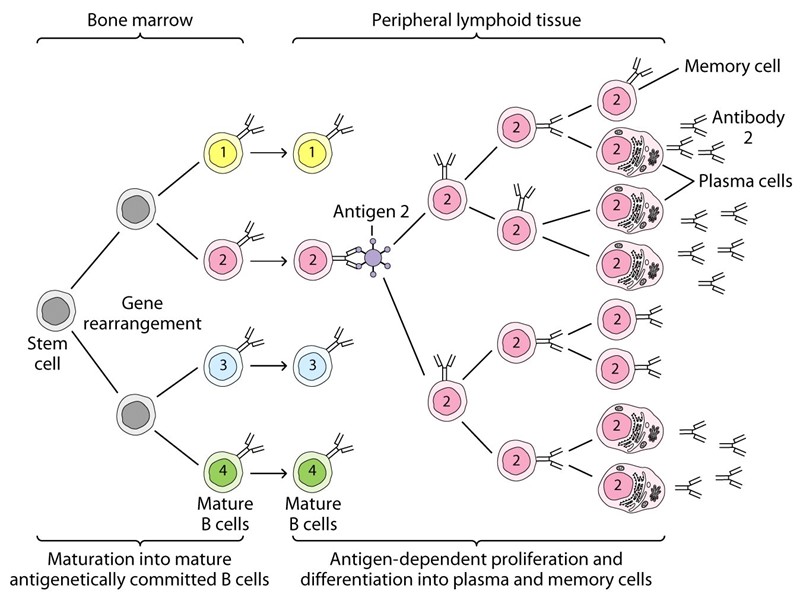
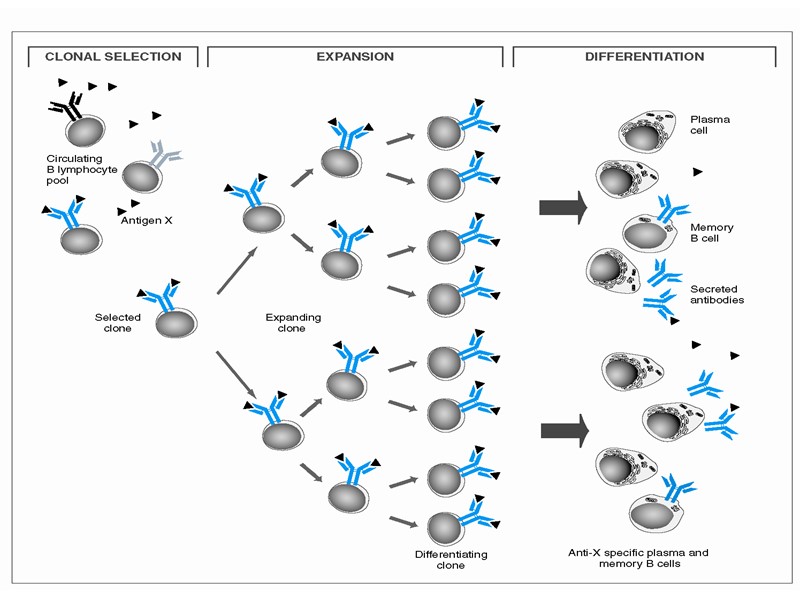
 Клонально-селекционная теория иммунитета 1. Вся совокупность лимфоцитов клонирована по специфичности антигенраспознающих рецепторов. 2. Формирование клонального разнообразия происходит на этапе антигеннезависимой дифференцировки в результате рекомбинации генов, кодирующих антигенраспознающие рецепторы. .
Клонально-селекционная теория иммунитета 1. Вся совокупность лимфоцитов клонирована по специфичности антигенраспознающих рецепторов. 2. Формирование клонального разнообразия происходит на этапе антигеннезависимой дифференцировки в результате рекомбинации генов, кодирующих антигенраспознающие рецепторы. .

 3. При поступлении малых количеств антигена он связывается с рецепторами тех клонов, которые специфичны для данного антигена. Это приводит к клональной активации, пролиферации и дифференцировке в эффекторные клетки или клетки памяти.
3. При поступлении малых количеств антигена он связывается с рецепторами тех клонов, которые специфичны для данного антигена. Это приводит к клональной активации, пролиферации и дифференцировке в эффекторные клетки или клетки памяти.

 4. Контакт лимфоцитов с большим количеством антигена приводит к гибели соответствующих клонов (отрицательная селекция), что лежит в основе иммунологической толерантности (специфической иммунной неотвечаемости) к своим собственным антигенам.
4. Контакт лимфоцитов с большим количеством антигена приводит к гибели соответствующих клонов (отрицательная селекция), что лежит в основе иммунологической толерантности (специфической иммунной неотвечаемости) к своим собственным антигенам.
 Третий этап - с 60-х годов 20 века по настоящее время - глубокое познание клеточных, а с начала 70-80-х годов и молекулярных механизмов функционирования иммунной системы.
Третий этап - с 60-х годов 20 века по настоящее время - глубокое познание клеточных, а с начала 70-80-х годов и молекулярных механизмов функционирования иммунной системы.
 Walter and Eliza Hall Institute (WEHI), Melbourne, Australia Основан в 1915 г. Eliza и Walter Russell Hall Директора: Dr. Sydney Patterson (1919-1923) Charles Kellaway (1924-1944) Sir Frank Macfarlane Burnet (1944-1965) Sir Gustav Nossal (1965-1996) Professor Suzanne Cory (1996-2009) Professor Doug Hilton (2009-настоящее время)
Walter and Eliza Hall Institute (WEHI), Melbourne, Australia Основан в 1915 г. Eliza и Walter Russell Hall Директора: Dr. Sydney Patterson (1919-1923) Charles Kellaway (1924-1944) Sir Frank Macfarlane Burnet (1944-1965) Sir Gustav Nossal (1965-1996) Professor Suzanne Cory (1996-2009) Professor Doug Hilton (2009-настоящее время)
 Miller JF. Immunological function of the thymus. Lancet. 1961 Sep 30;2:748-9. Miller JF. The thymus and the development of immunologic responsiveness. Science. 1964 Jun 26;144:1544-51. Miller JF, Mitchell GF. The thymus and the precursors of antigen reactive cells. Nature. 1967 Nov 18;216(5116):659-63. Miller JF, Sprent J. Cell-to-cell interaction in the immune response. VI. Contribution of thymus-derived cells and antibody-forming cell precursors to immunological memory. J Exp Med. 1971 Jul 1;134(1):66-82. Jacques Francis Albert Pierre Miller (Жак Миллер, родился 2.04.1931)
Miller JF. Immunological function of the thymus. Lancet. 1961 Sep 30;2:748-9. Miller JF. The thymus and the development of immunologic responsiveness. Science. 1964 Jun 26;144:1544-51. Miller JF, Mitchell GF. The thymus and the precursors of antigen reactive cells. Nature. 1967 Nov 18;216(5116):659-63. Miller JF, Sprent J. Cell-to-cell interaction in the immune response. VI. Contribution of thymus-derived cells and antibody-forming cell precursors to immunological memory. J Exp Med. 1971 Jul 1;134(1):66-82. Jacques Francis Albert Pierre Miller (Жак Миллер, родился 2.04.1931)
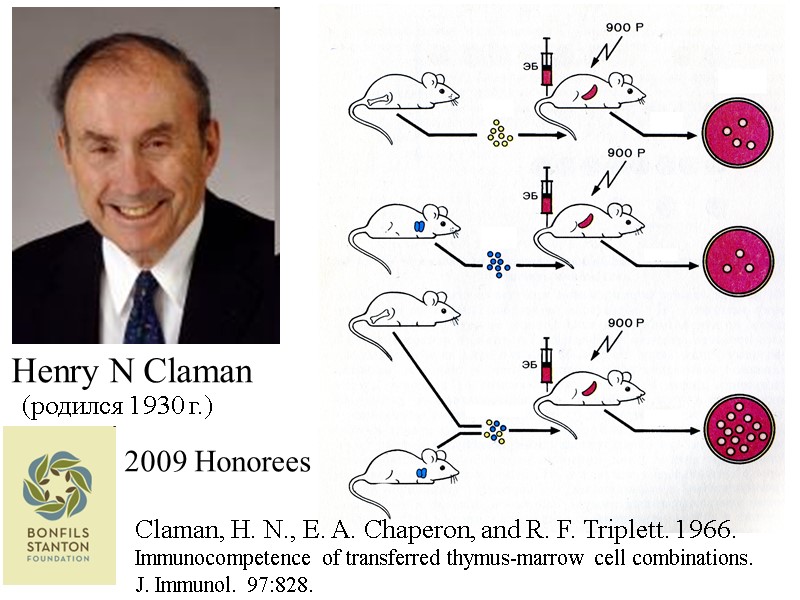
 Henry N Claman 2009 Honorees Claman, H. N., E. A. Chaperon, and R. F. Triplett. 1966. Immunocompetence of transferred thymus-marrow cell combinations. J. Immunol. 97:828. (родился 1930 г.)
Henry N Claman 2009 Honorees Claman, H. N., E. A. Chaperon, and R. F. Triplett. 1966. Immunocompetence of transferred thymus-marrow cell combinations. J. Immunol. 97:828. (родился 1930 г.)

 Professor Jacques Miller (centre) in 1996, the year of his retirement from the Walter and Eliza Hall Institute for Medical Research. Professor Donald Metcalf (left) and Sir Gustav Nossal also retired from WEHI in the same year. Photo: Courtesy of the Walter and Eliza Hall Institute of Medical Research.
Professor Jacques Miller (centre) in 1996, the year of his retirement from the Walter and Eliza Hall Institute for Medical Research. Professor Donald Metcalf (left) and Sir Gustav Nossal also retired from WEHI in the same year. Photo: Courtesy of the Walter and Eliza Hall Institute of Medical Research.
 Джеральд М. Эдельман (Gerald M. Edelman) 10) Нобелевская премия 1972 г. Родней Р. Портер (Rodney R. Porter) - за исследования химической структуры антител
Джеральд М. Эдельман (Gerald M. Edelman) 10) Нобелевская премия 1972 г. Родней Р. Портер (Rodney R. Porter) - за исследования химической структуры антител
 Розалин Яллоу (Rosalyn R. Yallow) - за разработку метода радиоиммунологического анализа 11) Нобелевская премия 1977 г.
Розалин Яллоу (Rosalyn R. Yallow) - за разработку метода радиоиммунологического анализа 11) Нобелевская премия 1977 г.
 Барух Бенацерраф (Baruj Benacerraf) Жан Доссе (Jean Dausset) Джордж Снелл (George D. Snell) 12) Ноб. пр. 1980 г. - за открытие генетически детерминированных структур клеточной поверхности, регулирующих иммунный ответ
Барух Бенацерраф (Baruj Benacerraf) Жан Доссе (Jean Dausset) Джордж Снелл (George D. Snell) 12) Ноб. пр. 1980 г. - за открытие генетически детерминированных структур клеточной поверхности, регулирующих иммунный ответ
 Нильс К. Ерне (Niels K. Jerne ) Цехарь Мильстейн (Cesar Milstein) Георг Джин Франц Кёллер (Georges J.F. Kohler) 13) Нобелевская премия 1984 г.
Нильс К. Ерне (Niels K. Jerne ) Цехарь Мильстейн (Cesar Milstein) Георг Джин Франц Кёллер (Georges J.F. Kohler) 13) Нобелевская премия 1984 г.
 Сузуму Тонегава (Susumu Tonegawa) 14) Нобелевская премия 1987 г.
Сузуму Тонегава (Susumu Tonegawa) 14) Нобелевская премия 1987 г.
 Джозеф Э. Мюррей (Joseph E. Murray) E. Донниел Томас (E. Donnall Thomas) 15) Нобелевская премия 1990 г.
Джозеф Э. Мюррей (Joseph E. Murray) E. Донниел Томас (E. Donnall Thomas) 15) Нобелевская премия 1990 г.
 Питер К. Догерти (Peter C. Doherty) Рольф М. Цинкернагель (Rolf M. Zinkernagel) 16) Нобелевская премия 1996 г.
Питер К. Догерти (Peter C. Doherty) Рольф М. Цинкернагель (Rolf M. Zinkernagel) 16) Нобелевская премия 1996 г.
 17) 6 октября 2008 года Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины Гарольду цур Хаузену за открытие того, что вирус папилломы может вызывать рак шейки матки (1/2), и Франсуазе Барре-Синусси (1/4) и Люку Монтанье (1/4) за открытие вируса иммунодефицита человека.
17) 6 октября 2008 года Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины Гарольду цур Хаузену за открытие того, что вирус папилломы может вызывать рак шейки матки (1/2), и Франсуазе Барре-Синусси (1/4) и Люку Монтанье (1/4) за открытие вируса иммунодефицита человека.
 1000000 US$ 7 июня 2011 г., Гонконг Жюль Хоффман Руслан Меджитов Брюс Бётлер 7 июня 2011 присуждена премия Шао (азиатский аналог Нобелевской премии) за работы по врожденному иммунитету
1000000 US$ 7 июня 2011 г., Гонконг Жюль Хоффман Руслан Меджитов Брюс Бётлер 7 июня 2011 присуждена премия Шао (азиатский аналог Нобелевской премии) за работы по врожденному иммунитету
 18) 3 октября 2011 г. Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины: 1/2 Брюсу Бетлеру и Жюлю Хоффману и 1/2 Ральфу Стейнману
18) 3 октября 2011 г. Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины: 1/2 Брюсу Бетлеру и Жюлю Хоффману и 1/2 Ральфу Стейнману
 Первое научное определение иммунитета дал в 1903 году И.И. Мечников, обозначивший этим термином "общую систему явлений, благодаря которым организм выдерживает нападение болезнетворных микробов".
Первое научное определение иммунитета дал в 1903 году И.И. Мечников, обозначивший этим термином "общую систему явлений, благодаря которым организм выдерживает нападение болезнетворных микробов".
 Фрэнк Макфарлейн Бернет (Frank Macfarlane Burnet) Концепция иммунного надзора за соматическими мутациями, опухолевой трансформацией клеток, процессами клеточной пролиферации и дифференцировки
Фрэнк Макфарлейн Бернет (Frank Macfarlane Burnet) Концепция иммунного надзора за соматическими мутациями, опухолевой трансформацией клеток, процессами клеточной пролиферации и дифференцировки
 По определению академика Р.В. Петрова, иммунитет - это способ защиты организма от живых тел и веществ, несущих на себе признаки генетически чужеродной информации.
По определению академика Р.В. Петрова, иммунитет - это способ защиты организма от живых тел и веществ, несущих на себе признаки генетически чужеродной информации.
 Чужеродными (без добавления слова "генетически") являются все вещества, которые не могут быть утилизированы живой системой ни для производства энергии, ни для формирования своих собственных структур.
Чужеродными (без добавления слова "генетически") являются все вещества, которые не могут быть утилизированы живой системой ни для производства энергии, ни для формирования своих собственных структур.
 Известно 3 группы таких веществ: 1) неорганические соединения; 2) простые органические соединения, не являющиеся продуктами обмена веществ, например, лекарственные препараты; 3) биополимеры животного, растительного и микробного происхождения.
Известно 3 группы таких веществ: 1) неорганические соединения; 2) простые органические соединения, не являющиеся продуктами обмена веществ, например, лекарственные препараты; 3) биополимеры животного, растительного и микробного происхождения.
 В зависимости от того какими рецепторами и эффекторными молекулами распознаются генетически чужеродные соединения в современной литературе их разделяют на две большие группы: 1) патоген-ассоциированные молекулярные паттерны (англ. PAMP; pathogen-associated molecular pattern) и молекулярные паттерны повреждения (англ. DAMP; damage-associated molecular pattern) - распознаются паттерн- распознающими рецепторами и эффекторными молекулами врожденного иммунитета; 2) антигены - распознаются антиген- распознающими рецепторами Т- и В-лимфоцитов и антителами.
В зависимости от того какими рецепторами и эффекторными молекулами распознаются генетически чужеродные соединения в современной литературе их разделяют на две большие группы: 1) патоген-ассоциированные молекулярные паттерны (англ. PAMP; pathogen-associated molecular pattern) и молекулярные паттерны повреждения (англ. DAMP; damage-associated molecular pattern) - распознаются паттерн- распознающими рецепторами и эффекторными молекулами врожденного иммунитета; 2) антигены - распознаются антиген- распознающими рецепторами Т- и В-лимфоцитов и антителами.
 Патоген-ассоциированные молекулярные паттерны (PAMP), молекулярные паттерны повреждения (DAMP) и паттерн-распознающие рецепторы (PRR)
Патоген-ассоциированные молекулярные паттерны (PAMP), молекулярные паттерны повреждения (DAMP) и паттерн-распознающие рецепторы (PRR)
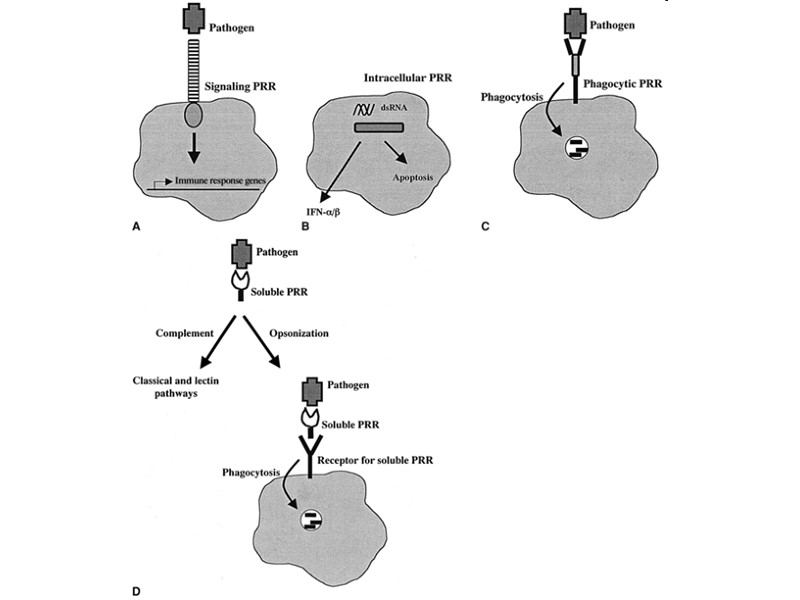
 ПЕРВАЯ ГРУППА ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ - сигнальные мембранные и внутриклеточные рецепторы
ПЕРВАЯ ГРУППА ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ - сигнальные мембранные и внутриклеточные рецепторы
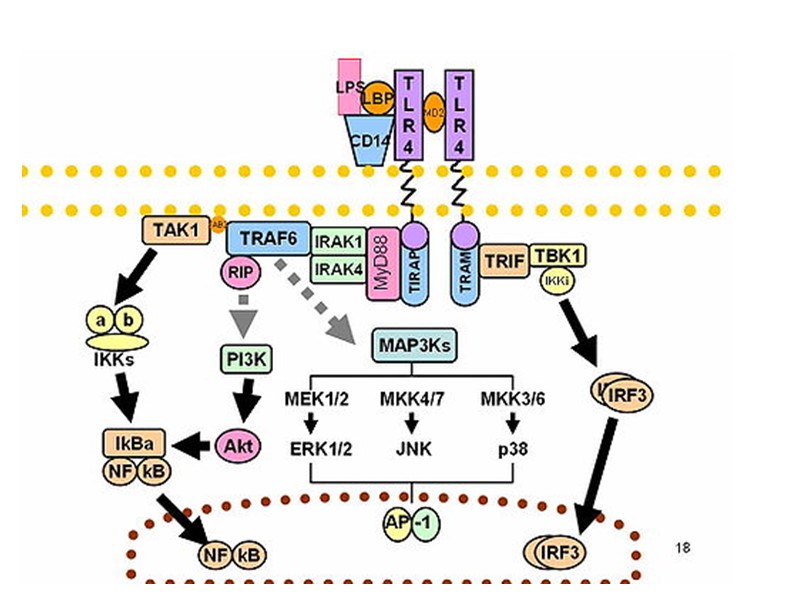
 1. Сигнальные мембранные и внутриклеточные рецепторы I. Распознают вне- и внутриклеточные PAMP и DAMP II. Распознавание ведет к запуску: 1) провоспалительных внутриклеточных сигнальных путей с образованием NF-B; 2) путей с активацией интерфероновых регуляторных факторов (IRFs) - IRF3 и IRF7; 3) компонентов MAP-киназного сигнального каскада: JUN N-терминальной киназы (JNK), p38 MAP киназы, ведущих к образованию ядерного фактора AP-1 III. Активация этих ядерных факторов приводит к повышению экспрессии генов, кодирующих: 1) антимикробные пептиды и белки; 2) провоспалительные цитокины (IL-1β, TNF-α), хемокины (IL-8 и др.); 3) мембранные молекулы (CD80/86, MHC II класса) и цитокины (IL-12 и др.), запускающие иммунный ответ; 4) при распознавании внутриклеточных вирусных РНК и ДНК помимо этого запускается синтез интреферонов I типа и апоптоз вирус-инфицированных клеток.
1. Сигнальные мембранные и внутриклеточные рецепторы I. Распознают вне- и внутриклеточные PAMP и DAMP II. Распознавание ведет к запуску: 1) провоспалительных внутриклеточных сигнальных путей с образованием NF-B; 2) путей с активацией интерфероновых регуляторных факторов (IRFs) - IRF3 и IRF7; 3) компонентов MAP-киназного сигнального каскада: JUN N-терминальной киназы (JNK), p38 MAP киназы, ведущих к образованию ядерного фактора AP-1 III. Активация этих ядерных факторов приводит к повышению экспрессии генов, кодирующих: 1) антимикробные пептиды и белки; 2) провоспалительные цитокины (IL-1β, TNF-α), хемокины (IL-8 и др.); 3) мембранные молекулы (CD80/86, MHC II класса) и цитокины (IL-12 и др.), запускающие иммунный ответ; 4) при распознавании внутриклеточных вирусных РНК и ДНК помимо этого запускается синтез интреферонов I типа и апоптоз вирус-инфицированных клеток.
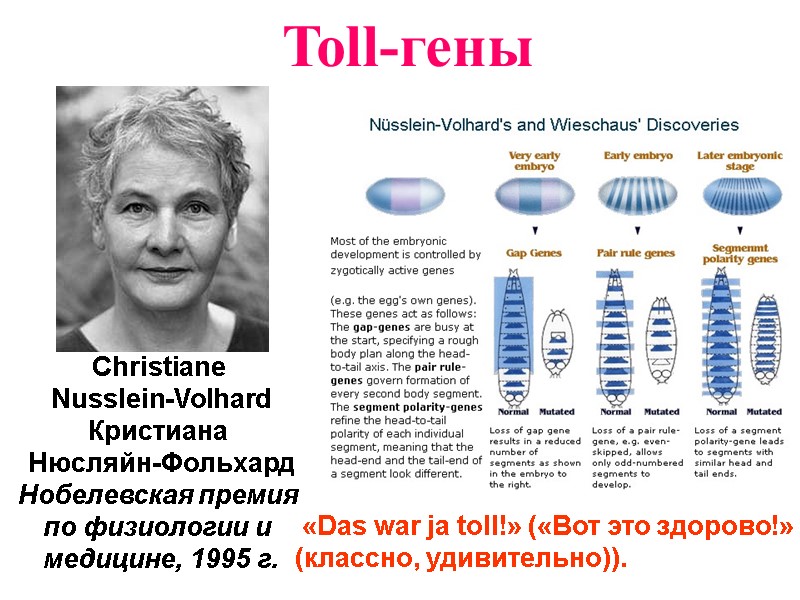
 Toll-гены «Das war ja toll!» («Вот это здорово!» (классно, удивительно)).
Toll-гены «Das war ja toll!» («Вот это здорово!» (классно, удивительно)).
 Lemaitre B, Nicolas E, Michaut L, Reichhart J-M, Hoffmann JA. The Dorsoventral Regulatory Gene Cassette spatzle/Toll/cactus Controls the Potent Antifungal Response in Drosophila Adults. Cell. 1996;86(6):973–983. 1996 - Toll-рецепторы Жюль А. Хоффманн (Jules A. Hoffmann), род. 2 августа 1941 г. Past Président de l’Académie des Sciences (2007-2008), Иностранный член РАН
Lemaitre B, Nicolas E, Michaut L, Reichhart J-M, Hoffmann JA. The Dorsoventral Regulatory Gene Cassette spatzle/Toll/cactus Controls the Potent Antifungal Response in Drosophila Adults. Cell. 1996;86(6):973–983. 1996 - Toll-рецепторы Жюль А. Хоффманн (Jules A. Hoffmann), род. 2 августа 1941 г. Past Président de l’Académie des Sciences (2007-2008), Иностранный член РАН
 С 1994 по 2005 гг. - директор Института молекулярной и клеточной биологии (IBMC) Французского национального центра научных исследований (CNRS) Страсбургского университета Лаборатория иммунного ответа и развития насекомых
С 1994 по 2005 гг. - директор Института молекулярной и клеточной биологии (IBMC) Французского национального центра научных исследований (CNRS) Страсбургского университета Лаборатория иммунного ответа и развития насекомых
 Чарльз Джэнэвэй (Charles A. Janeway, 1943-2003) и Руслан Меджитов Toll-подобные рецепторы (TLR1-TLR10 у человека; TLR1-9 и TLR11-13 у мыши) 2. Medzhitov R, Preston-Hurlburt P, Janeway CA. A human homologue of the Drosophila Toll protein signals activation of adaptive immunity // Nature. 1997. Vol. 388 (6640) July P. 394–397. 1. Janeway C.A. Jr. (1989). Approaching the asymptote? Evolution and revolution in immunology. Cold Spring Harb. Symp. Quant. Biol. 54, 1–13
Чарльз Джэнэвэй (Charles A. Janeway, 1943-2003) и Руслан Меджитов Toll-подобные рецепторы (TLR1-TLR10 у человека; TLR1-9 и TLR11-13 у мыши) 2. Medzhitov R, Preston-Hurlburt P, Janeway CA. A human homologue of the Drosophila Toll protein signals activation of adaptive immunity // Nature. 1997. Vol. 388 (6640) July P. 394–397. 1. Janeway C.A. Jr. (1989). Approaching the asymptote? Evolution and revolution in immunology. Cold Spring Harb. Symp. Quant. Biol. 54, 1–13
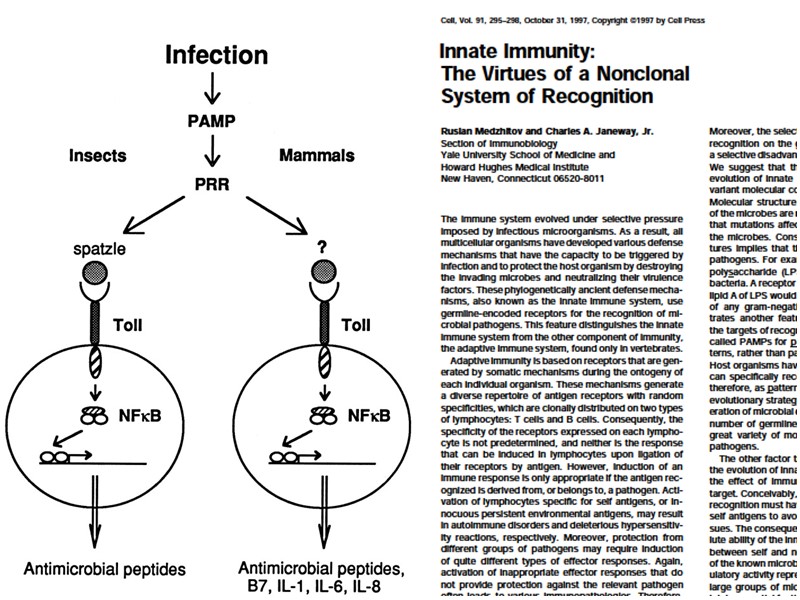
 R Medzhitov; P Preston-Hurlburt; C A Janeway A human homologue of the Drosophila Toll protein signals activation of adaptive immunity. Nature 1997;388( 6640):394- 397. Клонирован и охарактеризован человеческий гомолог Toll-рецептора Drosophila. 1. Человеческий Toll-подобный рецептор (англ. TLR, Toll-like receptor) также как и у Drosophila содержит внеклеточный распознающий домен с лейциновыми повторами (англ. LRR, leucine- rich repeat domain) и внутриклеточный TIR-домен (англ. Toll/IL-1R domain) для передачи активационного сигнала. 2. Передача сигнала также как и у Drosophila осуществляется через NF- kappaB сигнальный путь. 3. Трансфекция гена TLR в человеческие клеточные линии приводит к экспрессии контролируемых NF- kappaB генов: IL-1, IL-6 и IL-8, а также костимулирующих молекул B7 (CD80/CD86), необходимых для активации наивных Т-лимфоцитов.
R Medzhitov; P Preston-Hurlburt; C A Janeway A human homologue of the Drosophila Toll protein signals activation of adaptive immunity. Nature 1997;388( 6640):394- 397. Клонирован и охарактеризован человеческий гомолог Toll-рецептора Drosophila. 1. Человеческий Toll-подобный рецептор (англ. TLR, Toll-like receptor) также как и у Drosophila содержит внеклеточный распознающий домен с лейциновыми повторами (англ. LRR, leucine- rich repeat domain) и внутриклеточный TIR-домен (англ. Toll/IL-1R domain) для передачи активационного сигнала. 2. Передача сигнала также как и у Drosophila осуществляется через NF- kappaB сигнальный путь. 3. Трансфекция гена TLR в человеческие клеточные линии приводит к экспрессии контролируемых NF- kappaB генов: IL-1, IL-6 и IL-8, а также костимулирующих молекул B7 (CD80/CD86), необходимых для активации наивных Т-лимфоцитов.

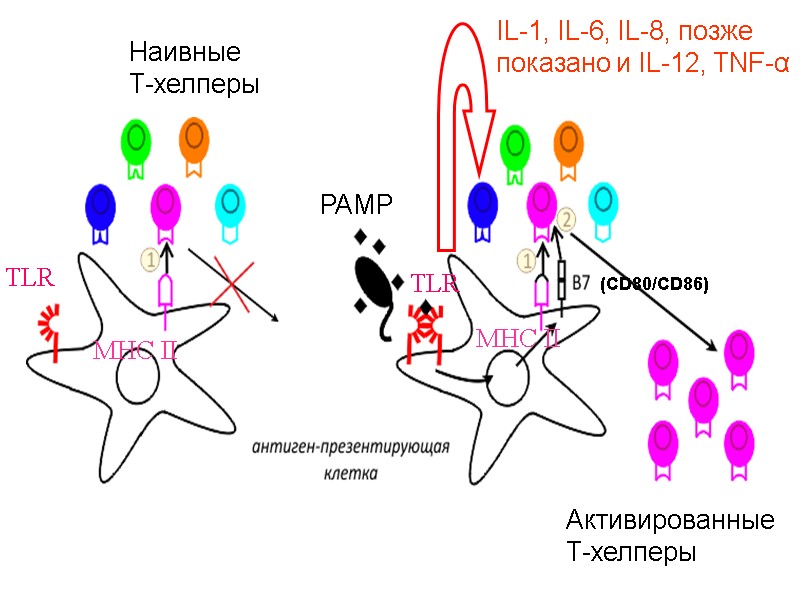
 Наивные Т-хелперы MHC II TLR TLR PAMP IL-1, IL-6, IL-8, позже показано и IL-12, TNF-α Активированные Т-хелперы MHC II (CD80/CD86)
Наивные Т-хелперы MHC II TLR TLR PAMP IL-1, IL-6, IL-8, позже показано и IL-12, TNF-α Активированные Т-хелперы MHC II (CD80/CD86)
 1998 г. - Брюс Бетлер (Bruce Beutler) - LPS через TLR4 у мышей повышает TNF
1998 г. - Брюс Бетлер (Bruce Beutler) - LPS через TLR4 у мышей повышает TNF
 Шизуо Акира Shizuo Akira (審良 静男) Department of Host Defense, Osaka University, Japan
Шизуо Акира Shizuo Akira (審良 静男) Department of Host Defense, Osaka University, Japan
 1000000 US$ 7 июня 2011 г., Гонконг Жюль Хоффман Руслан Меджитов Брюс Бётлер 7 июня 2011 присуждена премия Шао (азиатский аналог Нобелевской премии) за работы по врожденному иммунитету
1000000 US$ 7 июня 2011 г., Гонконг Жюль Хоффман Руслан Меджитов Брюс Бётлер 7 июня 2011 присуждена премия Шао (азиатский аналог Нобелевской премии) за работы по врожденному иммунитету
 18) 3 октября 2011 г. Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины: 1/2 Брюсу Бетлеру и Жюлю Хоффману и 1/2 Ральфу Стейнману
18) 3 октября 2011 г. Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины: 1/2 Брюсу Бетлеру и Жюлю Хоффману и 1/2 Ральфу Стейнману
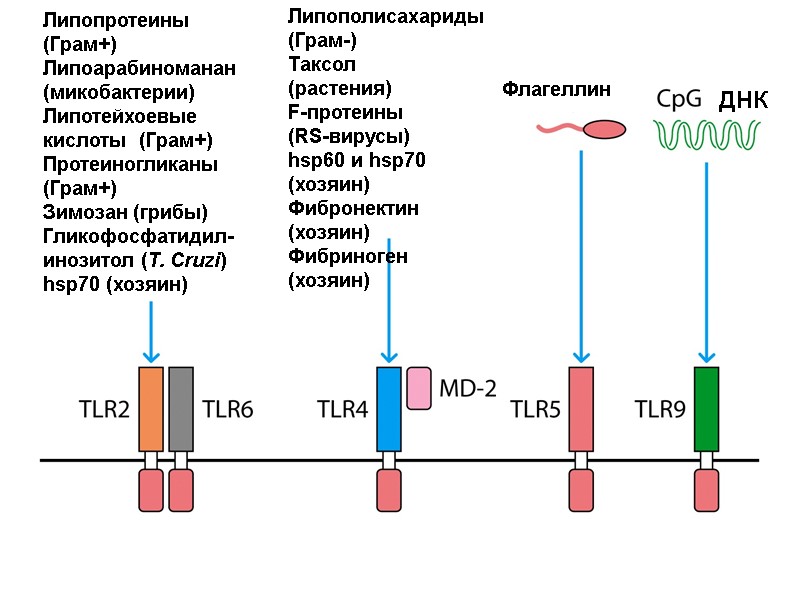
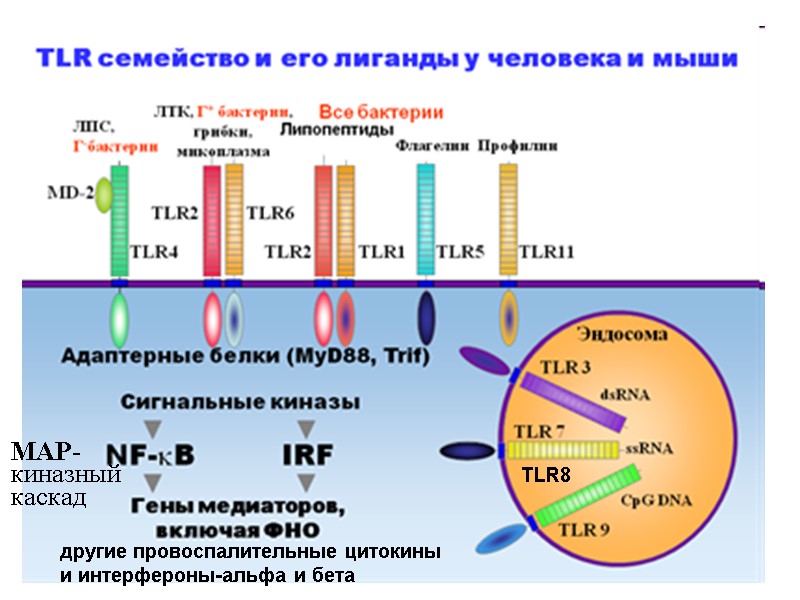
 Липопротеины (Грам+) Липоарабиноманан (микобактерии) Липотейхоевые кислоты (Грам+) Протеиногликаны (Грам+) Зимозан (грибы) Гликофосфатидил- инозитол (T. Cruzi) hsp70 (хозяин) Липополисахариды (Грам-) Таксол (растения) F-протеины (RS-вирусы) hsp60 и hsp70 (хозяин) Фибронектин (хозяин) Фибриноген (хозяин) Флагеллин ДНК
Липопротеины (Грам+) Липоарабиноманан (микобактерии) Липотейхоевые кислоты (Грам+) Протеиногликаны (Грам+) Зимозан (грибы) Гликофосфатидил- инозитол (T. Cruzi) hsp70 (хозяин) Липополисахариды (Грам-) Таксол (растения) F-протеины (RS-вирусы) hsp60 и hsp70 (хозяин) Фибронектин (хозяин) Фибриноген (хозяин) Флагеллин ДНК
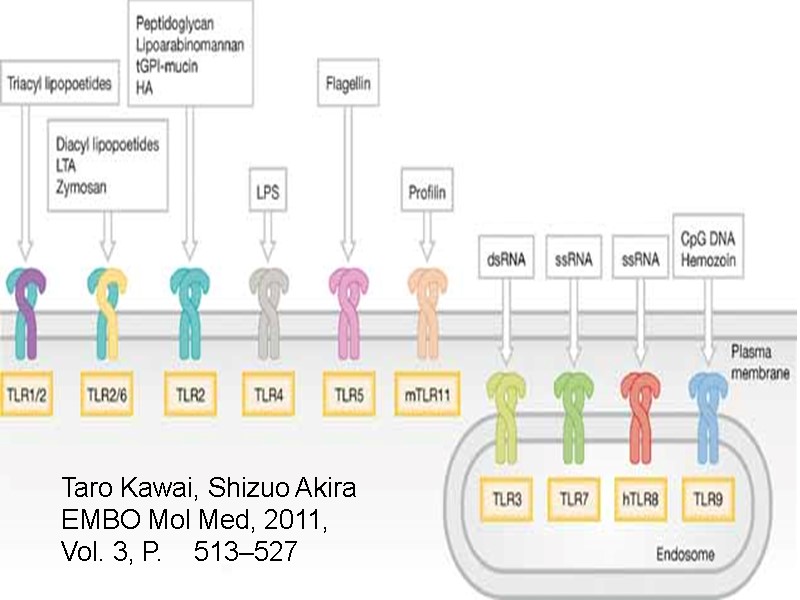
 TLR1 - в комплексе с TLR2 распознает триациллипопептиды (бактерии и микобактерии) TLR3 - двухспиральные РНК (вирусы) TLR7 и TLR8 - одноцепочечные РНК (вирусы) и некоторые противовирусные препараты TLR10 - (только у людей) лиганд не известен TLR11 - (только у мышей) профилин (Toxoplasma gondii); у человека ген репрессирован (стоп-кодоны) TLR12 (только у мышей) - профилин (Toxoplasma gondii) TLR-13 (только у мышей) - последовательность CGGAAAGACC бактериальной рибосомальной РНК
TLR1 - в комплексе с TLR2 распознает триациллипопептиды (бактерии и микобактерии) TLR3 - двухспиральные РНК (вирусы) TLR7 и TLR8 - одноцепочечные РНК (вирусы) и некоторые противовирусные препараты TLR10 - (только у людей) лиганд не известен TLR11 - (только у мышей) профилин (Toxoplasma gondii); у человека ген репрессирован (стоп-кодоны) TLR12 (только у мышей) - профилин (Toxoplasma gondii) TLR-13 (только у мышей) - последовательность CGGAAAGACC бактериальной рибосомальной РНК
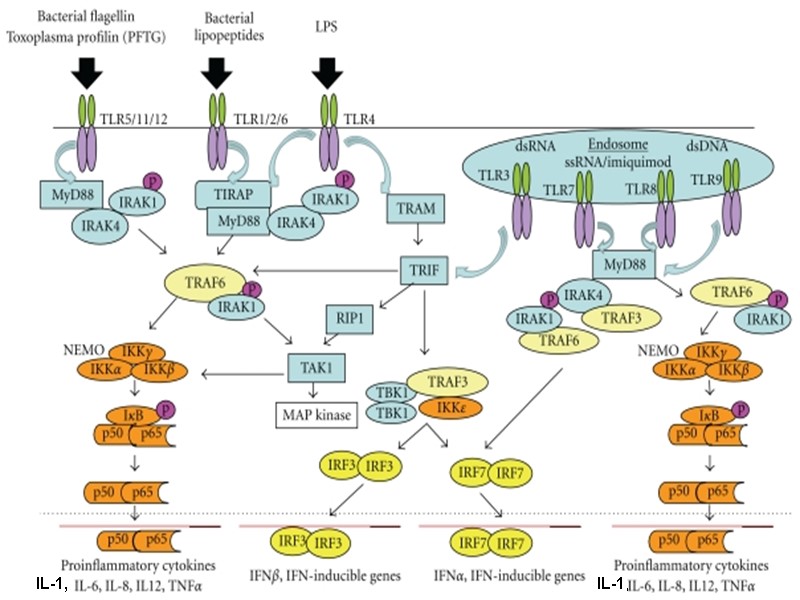
 Taro Kawai, Shizuo Akira EMBO Mol Med, 2011, Vol. 3, P. 513–527
Taro Kawai, Shizuo Akira EMBO Mol Med, 2011, Vol. 3, P. 513–527
 TLR8 другие провоспалительные цитокины и интерфероны-альфа и бета MAP- киназный каскад
TLR8 другие провоспалительные цитокины и интерфероны-альфа и бета MAP- киназный каскад

 IL-1, IL-1,
IL-1, IL-1,
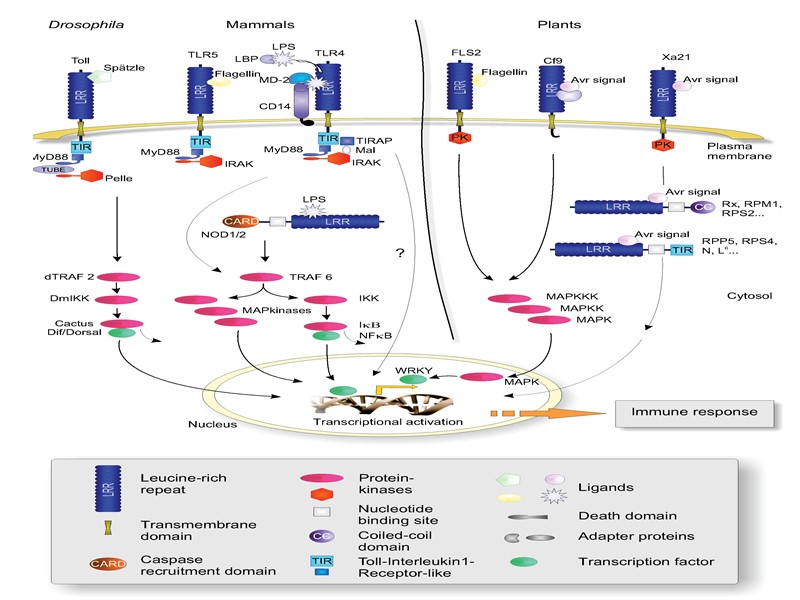
 Wen-Yuan Song, Guo-Liang Wang, Li-Li Chen, Han-Suk Kim, Li-Ya Pi, Tom Holsten, J. Gardner, Bei Wang, Wen-Xue Zhai, Li-Huang Zhu, Claude Fauquet, Pamela Ronald A receptor kinase-like protein encoded by the rice disease resistance gene, Xa21. Science 15 December 1995: Vol. 270 no. 5243 pp. 1804-1806 1995 - Памела Рональд (Pamela Ronald) - идентификация Xa21-рецепторов риса, сходных с Toll
Wen-Yuan Song, Guo-Liang Wang, Li-Li Chen, Han-Suk Kim, Li-Ya Pi, Tom Holsten, J. Gardner, Bei Wang, Wen-Xue Zhai, Li-Huang Zhu, Claude Fauquet, Pamela Ronald A receptor kinase-like protein encoded by the rice disease resistance gene, Xa21. Science 15 December 1995: Vol. 270 no. 5243 pp. 1804-1806 1995 - Памела Рональд (Pamela Ronald) - идентификация Xa21-рецепторов риса, сходных с Toll

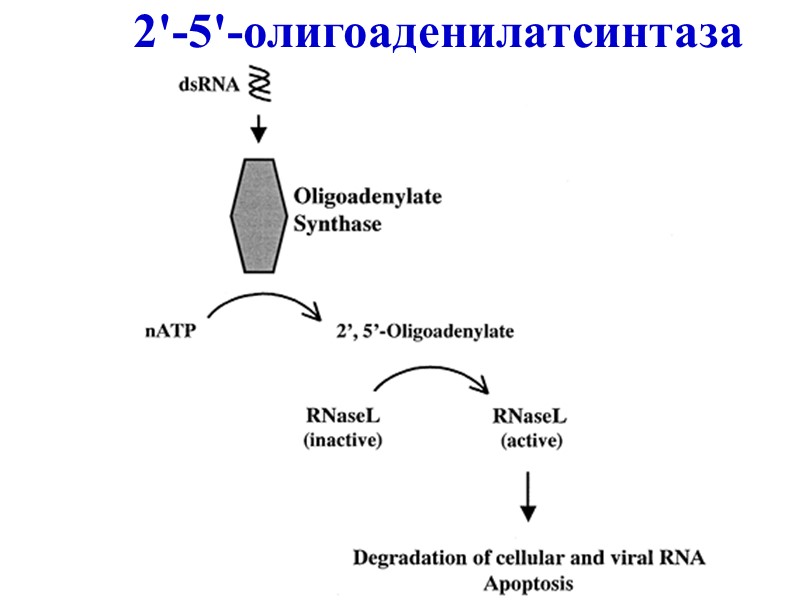
 КЛАССИФИКАЦИЯ ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ 1. Сигнальные мембранные и внутриклеточные рецепторы: 1) Toll, TLR1-TLR13 и аналоги у растений, 2) RLR-семейство (англ. RIG-I-like receptors), включает 3 сенсора: RIG-I (англ. retinoic acid-inducible gene 1), MDA5 (англ. melanoma Differentiation-Associated protein 5), LGP2 (англ. laboratory of genetics and physiology 2), распознающие вирусные 5'-трифосфат РНК и двухспиральные РНК и являющиеся хеликазами, расплетающими двухспиральные РНК с участием АТФ; 3) NLR-семейство (англ. NOD-like receptors; около 20; синоним: NBS-LRR от англ. nucleotide-binding site leucine-rich repeat) включает: а) NOD1 и NOD2, которые содержат нуклеотид-связывающий олигомеризационный домен (англ. nucleotide-binding oligomerization domain) и домен с лейциновыми повторами; б) подсемество NALP1-NALP14; в) другие представители; 4) 2'-5'-олигоаденилатсинтаза; 5) протеинкиназа, активируемая двухспиральной РНК (PKR).
КЛАССИФИКАЦИЯ ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ 1. Сигнальные мембранные и внутриклеточные рецепторы: 1) Toll, TLR1-TLR13 и аналоги у растений, 2) RLR-семейство (англ. RIG-I-like receptors), включает 3 сенсора: RIG-I (англ. retinoic acid-inducible gene 1), MDA5 (англ. melanoma Differentiation-Associated protein 5), LGP2 (англ. laboratory of genetics and physiology 2), распознающие вирусные 5'-трифосфат РНК и двухспиральные РНК и являющиеся хеликазами, расплетающими двухспиральные РНК с участием АТФ; 3) NLR-семейство (англ. NOD-like receptors; около 20; синоним: NBS-LRR от англ. nucleotide-binding site leucine-rich repeat) включает: а) NOD1 и NOD2, которые содержат нуклеотид-связывающий олигомеризационный домен (англ. nucleotide-binding oligomerization domain) и домен с лейциновыми повторами; б) подсемество NALP1-NALP14; в) другие представители; 4) 2'-5'-олигоаденилатсинтаза; 5) протеинкиназа, активируемая двухспиральной РНК (PKR).
 КЛАССИФИКАЦИЯ ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ 2. Паттерн-распознающие рецепторы, участвующие в фагоцитозе и эндоцитозе: scavenger рецепторы (рецепторы-мусорщики, SR-A, MARCO), макрофагальный маннозный рецептор, бета-глюкановые рецепторы. 3. Секретируемые паттерн-распознающие рецепторные молекулы: коллектины (маннозосвязывающий протеин, сурфактантные протеины A и D), пентраксины (С-реактивный протеин и сывороточный амилоид А), белки семейства липидных трансфераз (липополисахаридсвязывающий протеин и др.), пептидогликан-распознающие протеины.
КЛАССИФИКАЦИЯ ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ 2. Паттерн-распознающие рецепторы, участвующие в фагоцитозе и эндоцитозе: scavenger рецепторы (рецепторы-мусорщики, SR-A, MARCO), макрофагальный маннозный рецептор, бета-глюкановые рецепторы. 3. Секретируемые паттерн-распознающие рецепторные молекулы: коллектины (маннозосвязывающий протеин, сурфактантные протеины A и D), пентраксины (С-реактивный протеин и сывороточный амилоид А), белки семейства липидных трансфераз (липополисахаридсвязывающий протеин и др.), пептидогликан-распознающие протеины.

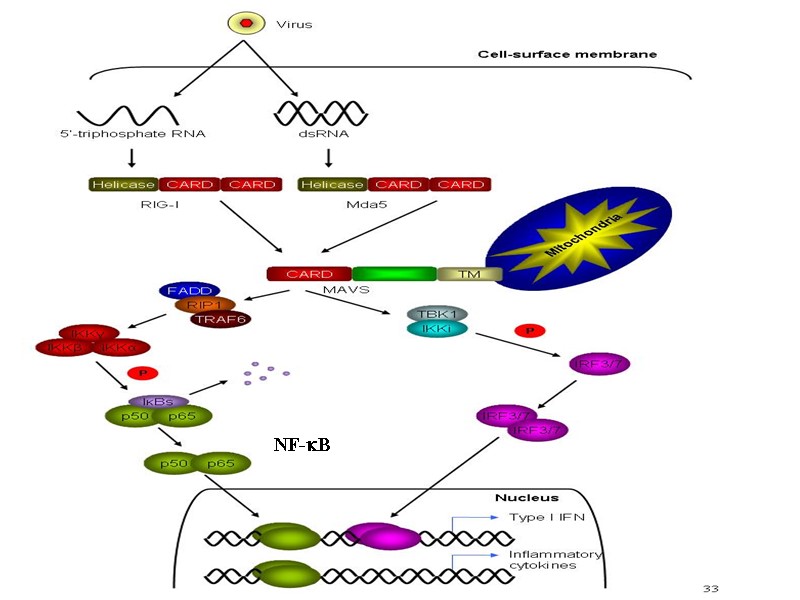
 RLR-семейство (англ. RIG-I-like receptors) RIG-I (англ. retinoic acid-inducible gene 1) распознает вирусные 5'-трифосфат-РНК MDA5 (англ. melanoma differentiation-associated protein 5) распознает вирусные двухспиральные РНК LGP2 (англ. laboratory of genetics and physiology 2) ингибирует действие RIG-I и MDA5 Являются хеликазами - ферментами расплетающими двухспиральные РНК с участием АТФ.
RLR-семейство (англ. RIG-I-like receptors) RIG-I (англ. retinoic acid-inducible gene 1) распознает вирусные 5'-трифосфат-РНК MDA5 (англ. melanoma differentiation-associated protein 5) распознает вирусные двухспиральные РНК LGP2 (англ. laboratory of genetics and physiology 2) ингибирует действие RIG-I и MDA5 Являются хеликазами - ферментами расплетающими двухспиральные РНК с участием АТФ.
 NF-B
NF-B
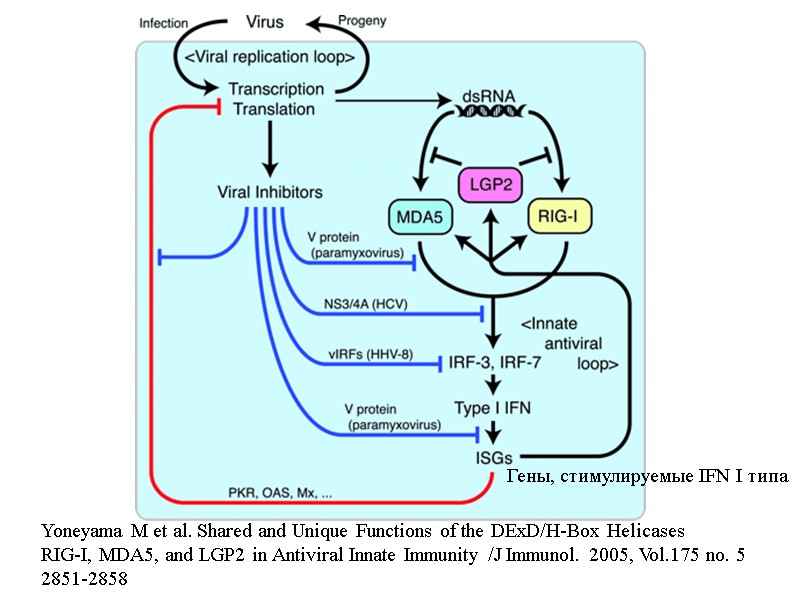
 Yoneyama M et al. Shared and Unique Functions of the DExD/H-Box Helicases RIG-I, MDA5, and LGP2 in Antiviral Innate Immunity /J Immunol. 2005, Vol.175 no. 5 2851-2858 Гены, стимулируемые IFN I типа
Yoneyama M et al. Shared and Unique Functions of the DExD/H-Box Helicases RIG-I, MDA5, and LGP2 in Antiviral Innate Immunity /J Immunol. 2005, Vol.175 no. 5 2851-2858 Гены, стимулируемые IFN I типа
 PKR - серин/треониновая протеинкиназа, содержит три домена, связывающих dsРНК, в N-концевой части и C- концевой киназный домен. PKR активируется dsРНК, является внутриклеточным сенсором вирусных инфекций, т.к. dsРНК содержат многие вирусы, но не клетки хозяина. PKR экспрессируется постоянно, экспрессия может значительно усиливаться интерферонами. Активированная PKR фосфорилирует фактор инициации трансляции eIF-2α по остатку Ser 51. Результат - блокирование трансляции вирусных и собственных белков. PKR также индуцирует апоптоз инфицированных клеток, что предупреждает дальнейшее распространение вирусов. Протеин-киназа R, активируемая двух- спиральными РНК (PKR)
PKR - серин/треониновая протеинкиназа, содержит три домена, связывающих dsРНК, в N-концевой части и C- концевой киназный домен. PKR активируется dsРНК, является внутриклеточным сенсором вирусных инфекций, т.к. dsРНК содержат многие вирусы, но не клетки хозяина. PKR экспрессируется постоянно, экспрессия может значительно усиливаться интерферонами. Активированная PKR фосфорилирует фактор инициации трансляции eIF-2α по остатку Ser 51. Результат - блокирование трансляции вирусных и собственных белков. PKR также индуцирует апоптоз инфицированных клеток, что предупреждает дальнейшее распространение вирусов. Протеин-киназа R, активируемая двух- спиральными РНК (PKR)
 2'-5'-олигоаденилатсинтаза
2'-5'-олигоаденилатсинтаза
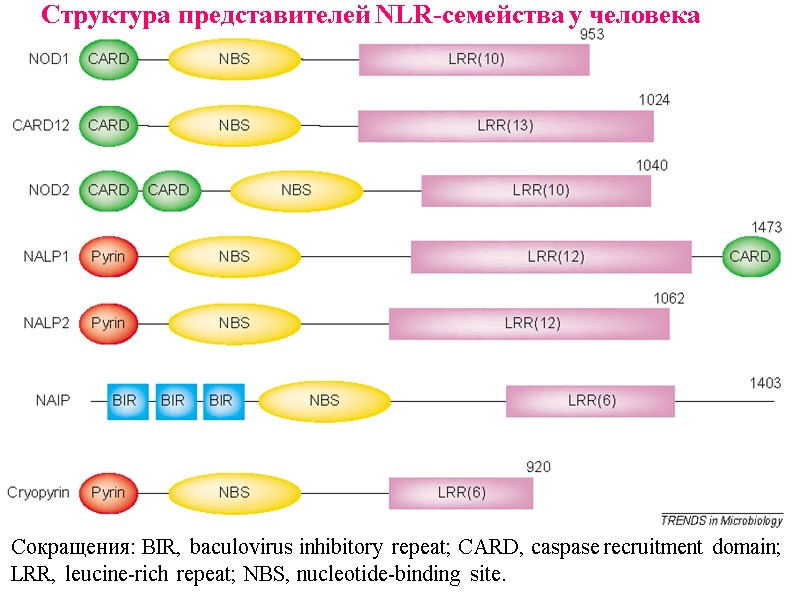
 Известно по крайней мере 23 Nod-подобных рецепторов. Все они были идентифицированы на основе анализа генома человека по их гомологии с белком-регулятором апоптоза Apaf-1. Nod-подобные рецепторы классифицируются по их эффекторному домену. Подсемейство NOD (NLRC): NOD1 и NOD2, содержат один или два CARD-домена (домен, рекрутирующий каспазы), и помимо них домен с лейциновыми повторами (LRR) и нуклеотид-связывающий олигомеризационный домен (англ. nucleotide-binding oligomerization domain), от которого произошло их название, связывающего нуклеозидтрифосаты. Подсемейство NALP (NLRP): рецепторы, содержащие пириновый домен (PYR): NALP1, NALP2, NALP3 и т.д. до NALP14 у человека; всего около 18 членов подсемейства; Подсемейство NAIP — рецепторы с BIR (англ. baculovirus inhibitory repeat) доменом: собственно NAIP. NLR-семейство (англ. NOD-like receptors; cиноним: NBS-LRR-семейство (англ. nucleotide-binding site leucine-rich repeat)
Известно по крайней мере 23 Nod-подобных рецепторов. Все они были идентифицированы на основе анализа генома человека по их гомологии с белком-регулятором апоптоза Apaf-1. Nod-подобные рецепторы классифицируются по их эффекторному домену. Подсемейство NOD (NLRC): NOD1 и NOD2, содержат один или два CARD-домена (домен, рекрутирующий каспазы), и помимо них домен с лейциновыми повторами (LRR) и нуклеотид-связывающий олигомеризационный домен (англ. nucleotide-binding oligomerization domain), от которого произошло их название, связывающего нуклеозидтрифосаты. Подсемейство NALP (NLRP): рецепторы, содержащие пириновый домен (PYR): NALP1, NALP2, NALP3 и т.д. до NALP14 у человека; всего около 18 членов подсемейства; Подсемейство NAIP — рецепторы с BIR (англ. baculovirus inhibitory repeat) доменом: собственно NAIP. NLR-семейство (англ. NOD-like receptors; cиноним: NBS-LRR-семейство (англ. nucleotide-binding site leucine-rich repeat)
 Сокращения: BIR, baculovirus inhibitory repeat; CARD, caspase recruitment domain; LRR, leucine-rich repeat; NBS, nucleotide-binding site. Структура представителей NLR-семейства у человека
Сокращения: BIR, baculovirus inhibitory repeat; CARD, caspase recruitment domain; LRR, leucine-rich repeat; NBS, nucleotide-binding site. Структура представителей NLR-семейства у человека
 NOD1 распознает пептидогликан грамнегативных бактерий с диаминопимелиновой кислотой (мезо-ДАПК, DAP, meso-DAP). NOD2 распознает внутриклеточные мурамилдипептиды - пептидогликаны как грампозитивных, так и грамнегативных бактерий. Аналог мурумилдипептида используется как лекарственный препарат - ликопид. NOD1/2 распознают микробные молекулы через C-концевой LRR-домен, обогащенный лециновыми повторами. Через CARD домен через каспазы запускается ряд сигнальных путей. Выявлена повышенная частота мутации гена CARD15 (ген NOD2) при болезни Крона. В передаче сигнала с NOD1/2 на пути с NF-κB and MAP-киназы участвует серин-треониновая киназа RIP2.
NOD1 распознает пептидогликан грамнегативных бактерий с диаминопимелиновой кислотой (мезо-ДАПК, DAP, meso-DAP). NOD2 распознает внутриклеточные мурамилдипептиды - пептидогликаны как грампозитивных, так и грамнегативных бактерий. Аналог мурумилдипептида используется как лекарственный препарат - ликопид. NOD1/2 распознают микробные молекулы через C-концевой LRR-домен, обогащенный лециновыми повторами. Через CARD домен через каспазы запускается ряд сигнальных путей. Выявлена повышенная частота мутации гена CARD15 (ген NOD2) при болезни Крона. В передаче сигнала с NOD1/2 на пути с NF-κB and MAP-киназы участвует серин-треониновая киназа RIP2.
 КЛАССИФИКАЦИЯ ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ 2-я группа. Паттерн-распознающие рецепторы, участвующие в фагоцитозе и эндоцитозе: scavenger рецепторы (рецепторы-мусорщики, SR-A, MARCO), макрофагальный маннозный рецептор, бета-глюкановые рецепторы.
КЛАССИФИКАЦИЯ ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ 2-я группа. Паттерн-распознающие рецепторы, участвующие в фагоцитозе и эндоцитозе: scavenger рецепторы (рецепторы-мусорщики, SR-A, MARCO), макрофагальный маннозный рецептор, бета-глюкановые рецепторы.
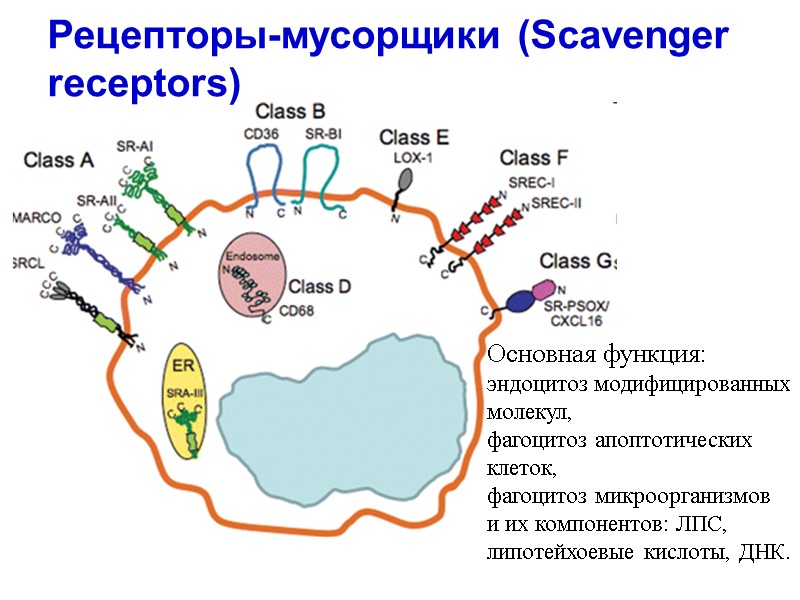
 Рецепторы-мусорщики (Scavenger receptors) Основная функция: эндоцитоз модифицированных молекул, фагоцитоз апоптотических клеток, фагоцитоз микроорганизмов и их компонентов: ЛПС, липотейхоевые кислоты, ДНК.
Рецепторы-мусорщики (Scavenger receptors) Основная функция: эндоцитоз модифицированных молекул, фагоцитоз апоптотических клеток, фагоцитоз микроорганизмов и их компонентов: ЛПС, липотейхоевые кислоты, ДНК.
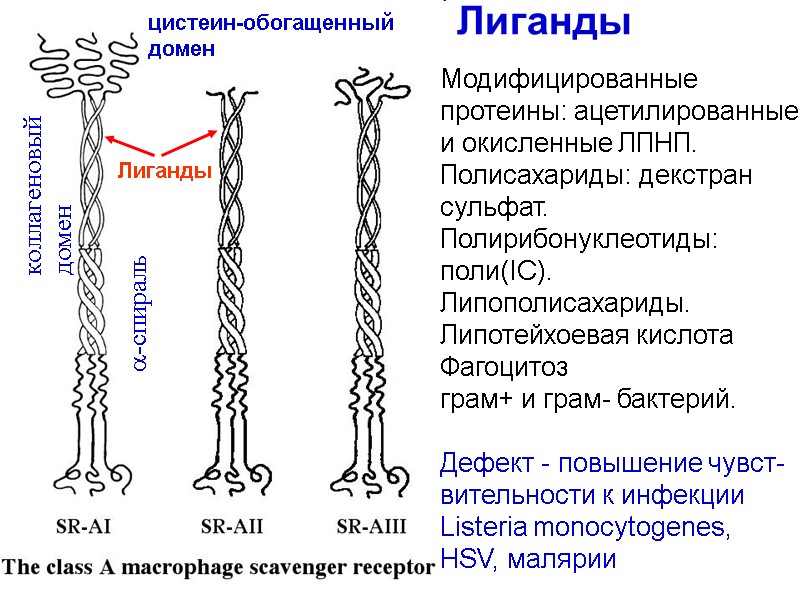
 Лиганды Модифицированные протеины: ацетилированные и окисленные ЛПНП. Полисахариды: декстран сульфат. Полирибонуклеотиды: поли(IC). Липополисахариды. Липотейхоевая кислота Фагоцитоз грам+ и грам- бактерий. Дефект - повышение чувст- вительности к инфекции Listeria monocytogenes, HSV, малярии -спираль коллагеновый домен цистеин-обогащенный домен Лиганды
Лиганды Модифицированные протеины: ацетилированные и окисленные ЛПНП. Полисахариды: декстран сульфат. Полирибонуклеотиды: поли(IC). Липополисахариды. Липотейхоевая кислота Фагоцитоз грам+ и грам- бактерий. Дефект - повышение чувст- вительности к инфекции Listeria monocytogenes, HSV, малярии -спираль коллагеновый домен цистеин-обогащенный домен Лиганды
 MARCO - макрофагальный рецептор с коллагеноподобной структурой По структуре похож на SC-A, но не содержит α-спирального региона. Лиганды присоединяется к цистеин-обогащенному домену. Связывает грам+ и грам- бактерии, но не зимозан грибов. Экспрессируется преимущественно на макрофагах краевой зоны селезенки, но под действием LPS и провоспалительных цитокинов на других макрофагах.
MARCO - макрофагальный рецептор с коллагеноподобной структурой По структуре похож на SC-A, но не содержит α-спирального региона. Лиганды присоединяется к цистеин-обогащенному домену. Связывает грам+ и грам- бактерии, но не зимозан грибов. Экспрессируется преимущественно на макрофагах краевой зоны селезенки, но под действием LPS и провоспалительных цитокинов на других макрофагах.
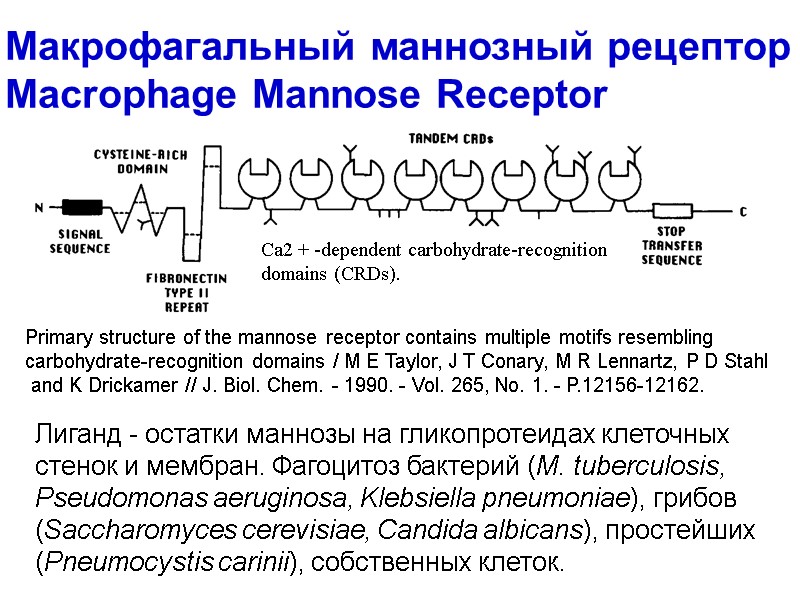
 Макрофагальный маннозный рецептор Macrophage Mannose Receptor Са2 + -dependent carbohydrate-recognition domains (CRDs). Лиганд - остатки маннозы на гликопротеидах клеточных стенок и мембран. Фагоцитоз бактерий (M. tuberculosis, Pseudomonas aeruginosa, Klebsiella pneumoniae), грибов (Saccharomyces cerevisiae, Candida albicans), простейших (Pneumocystis carinii), собственных клеток. Primary structure of the mannose receptor contains multiple motifs resembling carbohydrate-recognition domains / M E Taylor, J T Conary, M R Lennartz, P D Stahl and K Drickamer // J. Biol. Chem. - 1990. - Vol. 265, No. 1. - P.12156-12162.
Макрофагальный маннозный рецептор Macrophage Mannose Receptor Са2 + -dependent carbohydrate-recognition domains (CRDs). Лиганд - остатки маннозы на гликопротеидах клеточных стенок и мембран. Фагоцитоз бактерий (M. tuberculosis, Pseudomonas aeruginosa, Klebsiella pneumoniae), грибов (Saccharomyces cerevisiae, Candida albicans), простейших (Pneumocystis carinii), собственных клеток. Primary structure of the mannose receptor contains multiple motifs resembling carbohydrate-recognition domains / M E Taylor, J T Conary, M R Lennartz, P D Stahl and K Drickamer // J. Biol. Chem. - 1990. - Vol. 265, No. 1. - P.12156-12162.
 Дектин-1 (Dectin-1) относится к типу II трансмембранных рецепторов, содержащих один CRD в C-концевой части белка и атипичный ITAM мотив в N-концевом цитоплазматическом участке. CRD относится к субсемейству C-типу лектиноподобных доменов. В отличие от классических доменов С-типа лектиноподобный CDR домен не содержит аминокислот, необходимых для связывания Ca2+, поэтому связывает лиганды без участия Ca2+. Дектин-1 - первый идентифицированный лектин дендритных клеток, который присутствует и на макрофагах. Дектин-1 специфичен для углеводов, содержащих β-1,3– и β-1,6–связи, которые являются PAMPs, найденными в клеточных стенках грибов и других микроорганизмов. Он связывает и активирует фагоцитоз обогащенного β-глюканами зимозана и выполняет функции фагоцитозного PRR макрофагов и дендритных клеток. β-глюкановые рецепторы
Дектин-1 (Dectin-1) относится к типу II трансмембранных рецепторов, содержащих один CRD в C-концевой части белка и атипичный ITAM мотив в N-концевом цитоплазматическом участке. CRD относится к субсемейству C-типу лектиноподобных доменов. В отличие от классических доменов С-типа лектиноподобный CDR домен не содержит аминокислот, необходимых для связывания Ca2+, поэтому связывает лиганды без участия Ca2+. Дектин-1 - первый идентифицированный лектин дендритных клеток, который присутствует и на макрофагах. Дектин-1 специфичен для углеводов, содержащих β-1,3– и β-1,6–связи, которые являются PAMPs, найденными в клеточных стенках грибов и других микроорганизмов. Он связывает и активирует фагоцитоз обогащенного β-глюканами зимозана и выполняет функции фагоцитозного PRR макрофагов и дендритных клеток. β-глюкановые рецепторы
 КЛАССИФИКАЦИЯ ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ 3 группа. Секретируемые паттерн-распознающие рецепторные молекулы: коллектины (маннозосвязывающий протеин, сурфактантные протеины A и D), пентраксины (С-реактивный протеин и сывороточный амилоид А), белки семейства липидных трансфераз (липополисахаридсвязывающий протеин и др.), пептидогликан-распознающие протеины.
КЛАССИФИКАЦИЯ ПАТТЕРН-РАСПОЗНАЮЩИХ РЕЦЕПТОРОВ 3 группа. Секретируемые паттерн-распознающие рецепторные молекулы: коллектины (маннозосвязывающий протеин, сурфактантные протеины A и D), пентраксины (С-реактивный протеин и сывороточный амилоид А), белки семейства липидных трансфераз (липополисахаридсвязывающий протеин и др.), пептидогликан-распознающие протеины.
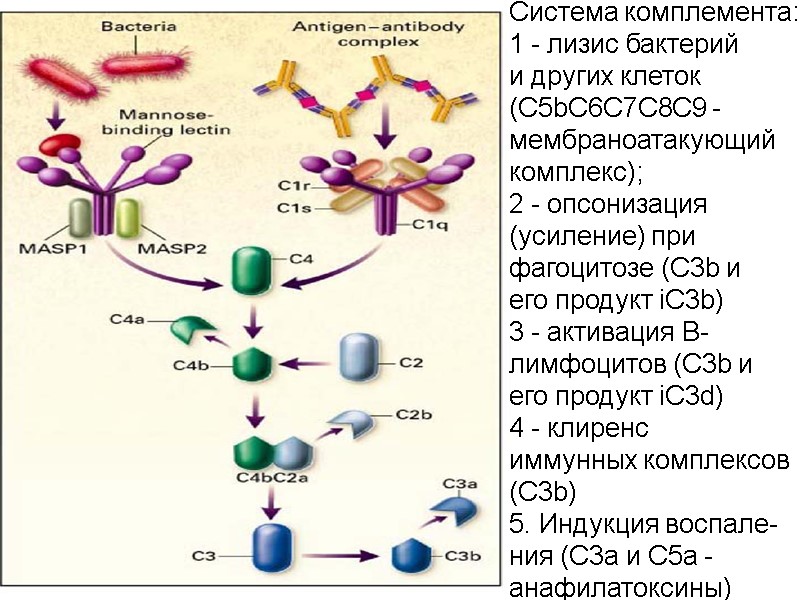
 Система комплемента: 1 - лизис бактерий и других клеток (C5bС6С7С8С9 - мембраноатакующий комплекс); 2 - опсонизация (усиление) при фагоцитозе (C3b и его продукт iC3b) 3 - активация В- лимфоцитов (C3b и его продукт iC3d) 4 - клиренс иммунных комплексов (С3b) 5. Индукция воспале- ния (C3a и C5a - анафилатоксины)
Система комплемента: 1 - лизис бактерий и других клеток (C5bС6С7С8С9 - мембраноатакующий комплекс); 2 - опсонизация (усиление) при фагоцитозе (C3b и его продукт iC3b) 3 - активация В- лимфоцитов (C3b и его продукт iC3d) 4 - клиренс иммунных комплексов (С3b) 5. Индукция воспале- ния (C3a и C5a - анафилатоксины)

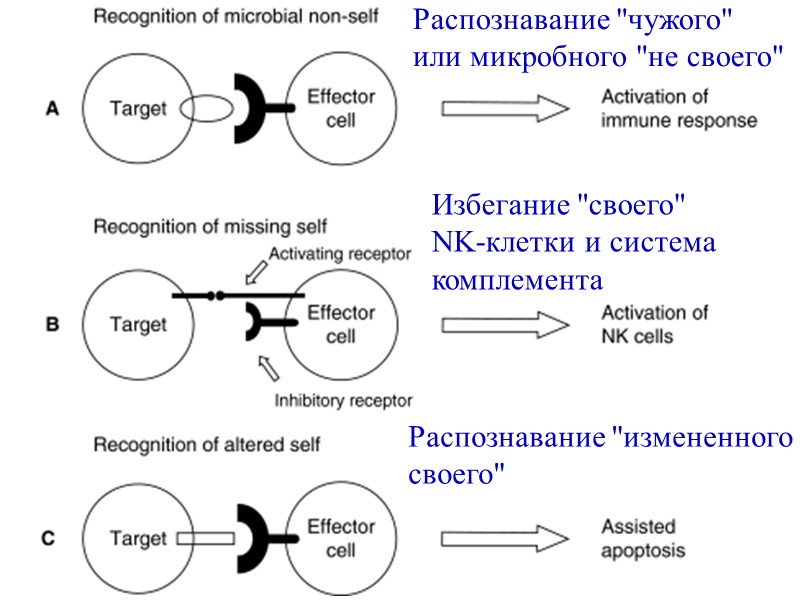
 Распознавание "чужого" или микробного "не своего" Избегание "своего" NK-клетки и система комплемента Распознавание "измененного своего"
Распознавание "чужого" или микробного "не своего" Избегание "своего" NK-клетки и система комплемента Распознавание "измененного своего"
 Защищает все виды живых существ, в то время как приобретенный иммунитет есть только у позвоночных. 2. Является первой линией защиты, включающей в защиту как собственные эффекторные механизмы, так и подсистему приобретенного (Т- и В-лимфоцитарного) иммунитета. 3. Распознающие структуры кодируются относительно небольшим числом генов, которые не могут увеличивать разнообразия рецепторов с помощью соматических перестроек (как это происходит в приобретенном иммунитете). 4. Из-за ограниченности числа генов рецепторы (сенсоры) распознают не индивидуальный патоген, а целые классы патогенных молекул, жизненно необходимых для выживания соответствующих микроорганизмов, либо молекулы, образующиеся при повреждении. 5. У позвоночных механизмы врожденного иммунитета вовлечены в эффекторные механизмы приобретенного иммунитета. Врожденный иммунитет (innate immunity, палеоиммунитет, конституциональный, примордиальный, естественный)
Защищает все виды живых существ, в то время как приобретенный иммунитет есть только у позвоночных. 2. Является первой линией защиты, включающей в защиту как собственные эффекторные механизмы, так и подсистему приобретенного (Т- и В-лимфоцитарного) иммунитета. 3. Распознающие структуры кодируются относительно небольшим числом генов, которые не могут увеличивать разнообразия рецепторов с помощью соматических перестроек (как это происходит в приобретенном иммунитете). 4. Из-за ограниченности числа генов рецепторы (сенсоры) распознают не индивидуальный патоген, а целые классы патогенных молекул, жизненно необходимых для выживания соответствующих микроорганизмов, либо молекулы, образующиеся при повреждении. 5. У позвоночных механизмы врожденного иммунитета вовлечены в эффекторные механизмы приобретенного иммунитета. Врожденный иммунитет (innate immunity, палеоиммунитет, конституциональный, примордиальный, естественный)
 1. Принципиально разные стратегии распознавания: во врожденном - рецептор узнает инвариантные химические структуры целого класса патогенов в адаптивном – генерируется набор рецепторов со случайной специфичностью, которые потом отбираются. 2. За каждую из двух ветвей иммунитета, в первом приближении, отвечают разные виды клеток иммунной системы (иммуноцитов). Клетки адаптивного иммунитета - Т и В лимфоциты (а также NKT клетки). Клетки врожденного иммунитета – моноциты/макрофаги, гранулоциты (нейтрофилы, эозинофилы, базофилы и тучные клетки), дендритные клетки, NK-клетки. Дополнительные факты про врожденный иммунитет
1. Принципиально разные стратегии распознавания: во врожденном - рецептор узнает инвариантные химические структуры целого класса патогенов в адаптивном – генерируется набор рецепторов со случайной специфичностью, которые потом отбираются. 2. За каждую из двух ветвей иммунитета, в первом приближении, отвечают разные виды клеток иммунной системы (иммуноцитов). Клетки адаптивного иммунитета - Т и В лимфоциты (а также NKT клетки). Клетки врожденного иммунитета – моноциты/макрофаги, гранулоциты (нейтрофилы, эозинофилы, базофилы и тучные клетки), дендритные клетки, NK-клетки. Дополнительные факты про врожденный иммунитет
 РАЗЛИЧИЯ ПОДСИСТЕМ ПАЛЕО- И НЕОИММУНИТЕТА Характеристика рецепторов Палео- иммунитет Неоиммунитет 1. Разнообразие (количество) десятки- сотни более 1022 вариантов 2. Формирование разнообразия кодируются зародышевыми генами V-, (D-), J- реаранжировка 3. Включение в защиту немедленно спустя несколько дней (необходима пролиферация и дифференцировка) 4. Распознавание патогенов да да 5. Элиминация да да Иммунологическая память да нет
РАЗЛИЧИЯ ПОДСИСТЕМ ПАЛЕО- И НЕОИММУНИТЕТА Характеристика рецепторов Палео- иммунитет Неоиммунитет 1. Разнообразие (количество) десятки- сотни более 1022 вариантов 2. Формирование разнообразия кодируются зародышевыми генами V-, (D-), J- реаранжировка 3. Включение в защиту немедленно спустя несколько дней (необходима пролиферация и дифференцировка) 4. Распознавание патогенов да да 5. Элиминация да да Иммунологическая память да нет
 Антигены – это вещества и надмолекулярные компоненты, взаимодействующие с антиген- специфическими распознающими и эффекторными белками иммунной системы. К последним относятся антитела, их мембранная форма – В-клеточные рецепторы (мембранные иммуноглобулины) и Т-клеточные рецепторы.
Антигены – это вещества и надмолекулярные компоненты, взаимодействующие с антиген- специфическими распознающими и эффекторными белками иммунной системы. К последним относятся антитела, их мембранная форма – В-клеточные рецепторы (мембранные иммуноглобулины) и Т-клеточные рецепторы.
 Термин «антигены» введен в 1899 г. Л. Детре (сотрудник И.И. Мечникова). Происхождение термина. Антитоксины (Беринг с сотрудниками) Антитела (нем.: antikorper, в 1891 г. Пауль Эрлих, korper - микроскопические тельца, бактерии, англ.: antibody, в последующем было показано, что антитела образуются не только против бактерий) Антигены (вещества, индуцирующие образование антител и взаимодействующие с ними)
Термин «антигены» введен в 1899 г. Л. Детре (сотрудник И.И. Мечникова). Происхождение термина. Антитоксины (Беринг с сотрудниками) Антитела (нем.: antikorper, в 1891 г. Пауль Эрлих, korper - микроскопические тельца, бактерии, англ.: antibody, в последующем было показано, что антитела образуются не только против бактерий) Антигены (вещества, индуцирующие образование антител и взаимодействующие с ними)
 В последующем выяснилось, что антигены также распознаются В-клеточными рецепторами (их распознающей частью – мембранными иммуноглобулинами) и Т-клеточными рецепторами.
В последующем выяснилось, что антигены также распознаются В-клеточными рецепторами (их распознающей частью – мембранными иммуноглобулинами) и Т-клеточными рецепторами.
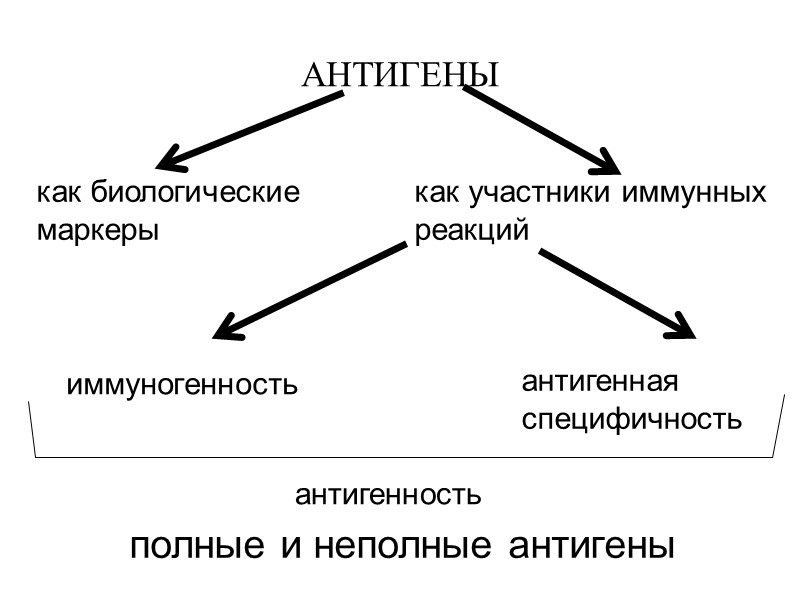
 АНТИГЕНЫ как биологические маркеры как участники иммунных реакций иммуногенность антигенная специфичность антигенность полные и неполные антигены
АНТИГЕНЫ как биологические маркеры как участники иммунных реакций иммуногенность антигенная специфичность антигенность полные и неполные антигены
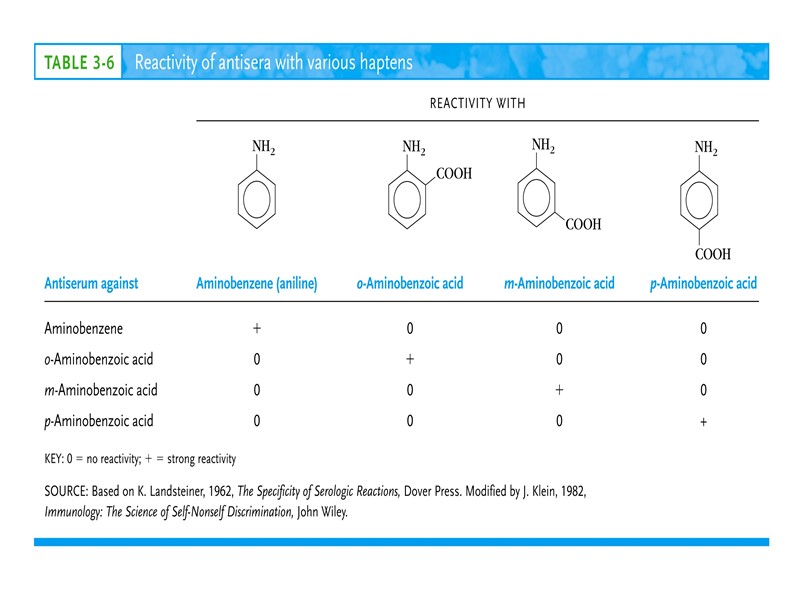
 В своих ранних исследованиях по антиэритроцитарным антителам он описал в 1901 г. ряд изогемагглютининов человека, которые в наше время составляют систему групп крови АВО. В 1926 г. Ландштейнер и Фелип Левин открыли систему MNP, а в 1940 г. вместе с Альбертом Винером – систему групп крови Rh. Большую роль сыграли работы по антигенной специфичности, выполненные в 1930-1940 гг. 1930 год Карл Ландштейнер (Karl Landsteiner)
В своих ранних исследованиях по антиэритроцитарным антителам он описал в 1901 г. ряд изогемагглютининов человека, которые в наше время составляют систему групп крови АВО. В 1926 г. Ландштейнер и Фелип Левин открыли систему MNP, а в 1940 г. вместе с Альбертом Винером – систему групп крови Rh. Большую роль сыграли работы по антигенной специфичности, выполненные в 1930-1940 гг. 1930 год Карл Ландштейнер (Karl Landsteiner)
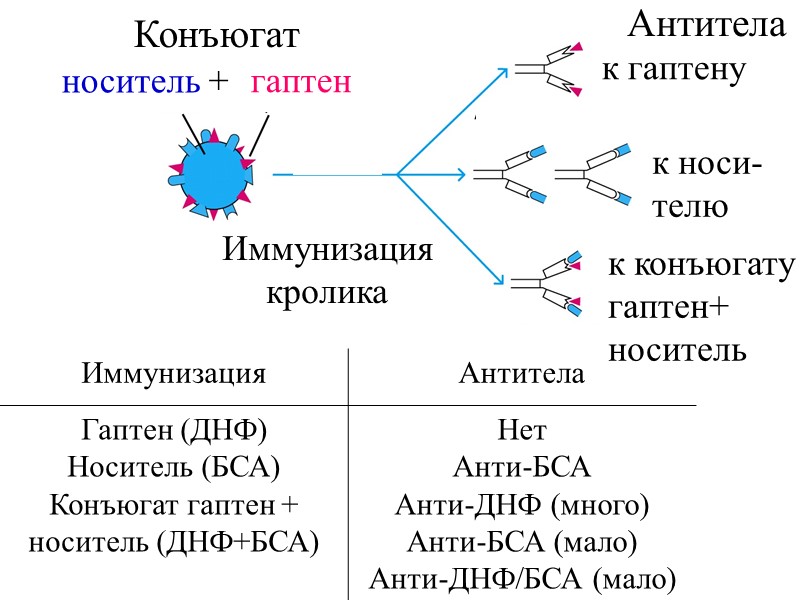
 гаптен носитель + Иммунизация кролика Конъюгат Антитела к гаптену к носи- телю к конъюгату гаптен+ носитель
гаптен носитель + Иммунизация кролика Конъюгат Антитела к гаптену к носи- телю к конъюгату гаптен+ носитель

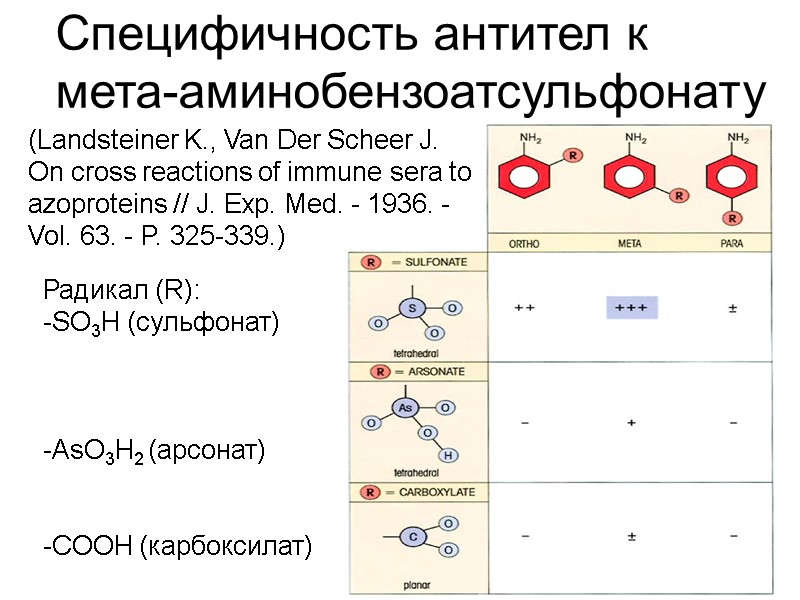
 Специфичность антител к мета-аминобензоатсульфонату (Landsteiner K., Van Der Scheer J. On cross reactions of immune sera to azoproteins // J. Exp. Med. - 1936. - Vol. 63. - P. 325-339.) Радикал (R): -SO3H (сульфонат) -AsO3H2 (арсонат) -COOH (карбоксилат)
Специфичность антител к мета-аминобензоатсульфонату (Landsteiner K., Van Der Scheer J. On cross reactions of immune sera to azoproteins // J. Exp. Med. - 1936. - Vol. 63. - P. 325-339.) Радикал (R): -SO3H (сульфонат) -AsO3H2 (арсонат) -COOH (карбоксилат)
 Получение антител к биологически важным гаптенам Гормоны Нейромедиаторы Простагландины Лейкотриены Тромбоксаны Биогенные амины и другие
Получение антител к биологически важным гаптенам Гормоны Нейромедиаторы Простагландины Лейкотриены Тромбоксаны Биогенные амины и другие
 Антигенные детерминанты конформационные секвенционные
Антигенные детерминанты конформационные секвенционные
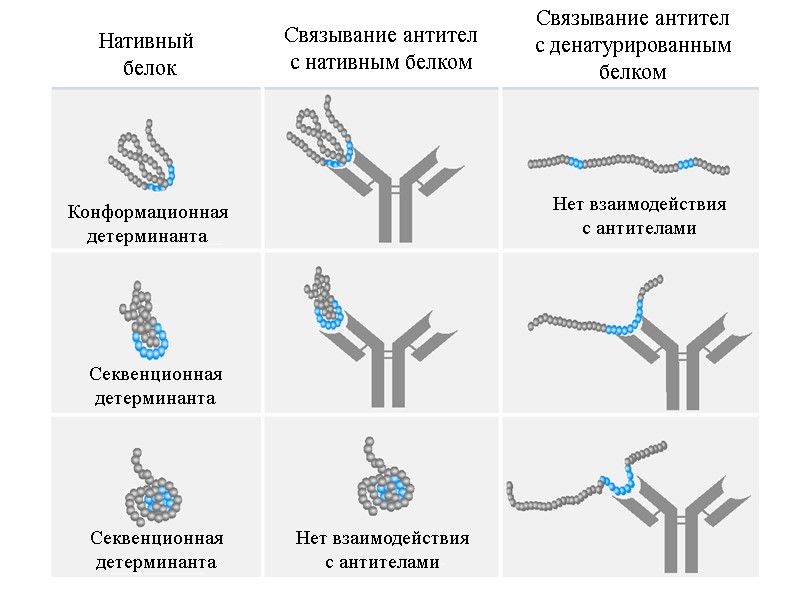
 Нативный белок Конформационная детерминанта Секвенционная детерминанта Секвенционная детерминанта Нет взаимодействия с антителами Нет взаимодействия с антителами Связывание антител с нативным белком Связывание антител с денатурированным белком
Нативный белок Конформационная детерминанта Секвенционная детерминанта Секвенционная детерминанта Нет взаимодействия с антителами Нет взаимодействия с антителами Связывание антител с нативным белком Связывание антител с денатурированным белком
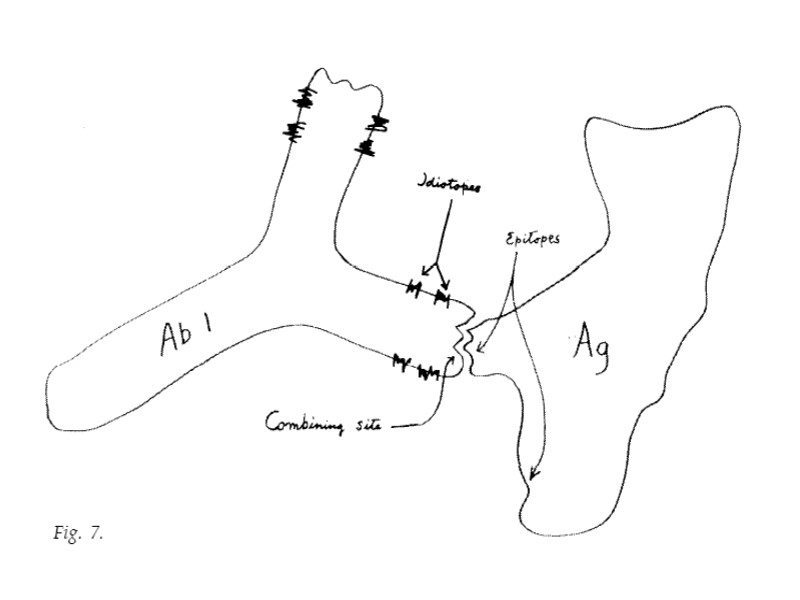
 Нильс К. Ерне (Niels K. Jerne ) (Нобелевская премия, 1984 г.) Эпитоп = синоним антигенной детерминанте Паратоп - участок активного центра антител, взаимодействующий с эпитопом
Нильс К. Ерне (Niels K. Jerne ) (Нобелевская премия, 1984 г.) Эпитоп = синоним антигенной детерминанте Паратоп - участок активного центра антител, взаимодействующий с эпитопом

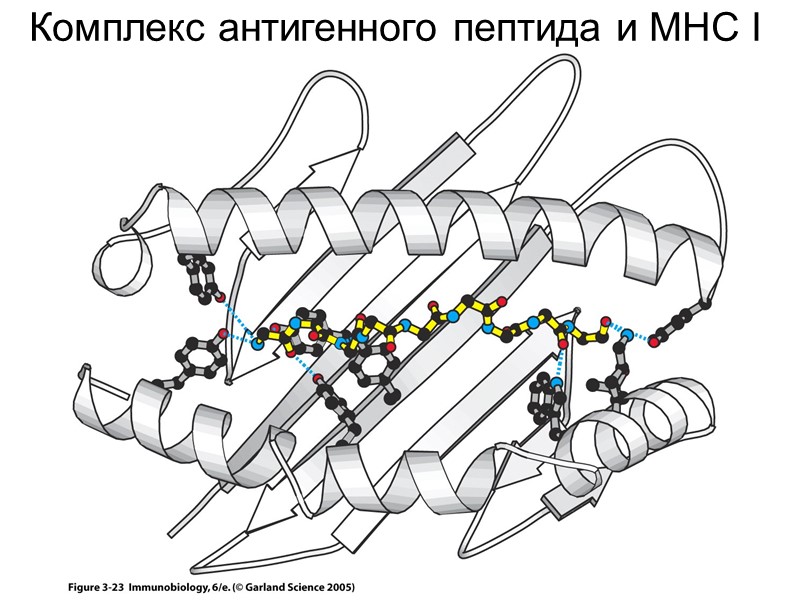
 Figure 3-23 Комплекс антигенного пептида и MHC I
Figure 3-23 Комплекс антигенного пептида и MHC I
 Валентность антигенов - определяется количеством антигенных детерминант (эпитопов)
Валентность антигенов - определяется количеством антигенных детерминант (эпитопов)
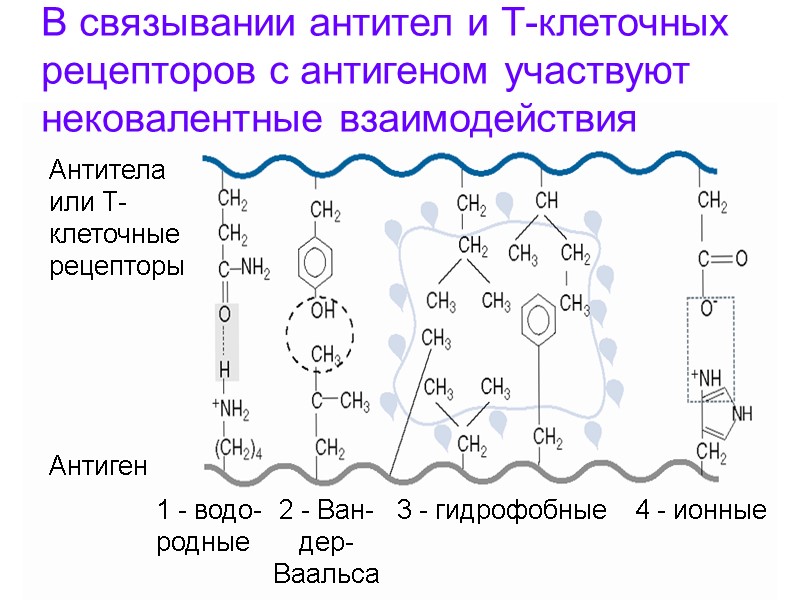
 Антитела или Т- клеточные рецепторы Антиген 1 - водо- родные 2 - Ван- дер- Ваальса 3 - гидрофобные 4 - ионные В связывании антител и Т-клеточных рецепторов с антигеном участвуют нековалентные взаимодействия
Антитела или Т- клеточные рецепторы Антиген 1 - водо- родные 2 - Ван- дер- Ваальса 3 - гидрофобные 4 - ионные В связывании антител и Т-клеточных рецепторов с антигеном участвуют нековалентные взаимодействия
 Иммуногенность - большая или меньшая способность антигена вызывать иммунный ответ. Толерогенность Протективная активность
Иммуногенность - большая или меньшая способность антигена вызывать иммунный ответ. Толерогенность Протективная активность
 Адъюванты - повышают иммуногенность полного антигена (т.е. уже обладающего иммуногенностью) за счет его депонирования и дополнительной активации клеток иммунной системы Примеры: - полный адъювант Фрейнда (ланолин, вазелиновое масло и бактерии вакцины БЦЖ); - неполный адъювант Фрейнда (без БЦЖ); - гидроокись алюминия
Адъюванты - повышают иммуногенность полного антигена (т.е. уже обладающего иммуногенностью) за счет его депонирования и дополнительной активации клеток иммунной системы Примеры: - полный адъювант Фрейнда (ланолин, вазелиновое масло и бактерии вакцины БЦЖ); - неполный адъювант Фрейнда (без БЦЖ); - гидроокись алюминия
 Факторы, влияющие на иммуногенность антигенов - молекулярная масса; - структурная гетерогенность; - жесткость конформации
Факторы, влияющие на иммуногенность антигенов - молекулярная масса; - структурная гетерогенность; - жесткость конформации
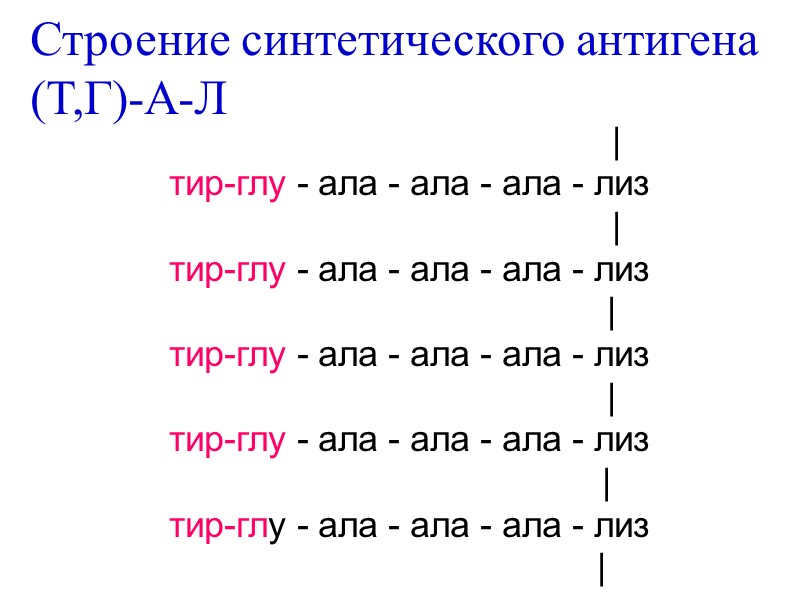
 | тир-глу - ала - ала - ала - лиз | тир-глу - ала - ала - ала - лиз | тир-глу - ала - ала - ала - лиз | тир-глу - ала - ала - ала - лиз | тир-глу - ала - ала - ала - лиз | Строение синтетического антигена (Т,Г)-А-Л
| тир-глу - ала - ала - ала - лиз | тир-глу - ала - ала - ала - лиз | тир-глу - ала - ала - ала - лиз | тир-глу - ала - ала - ала - лиз | тир-глу - ала - ала - ала - лиз | Строение синтетического антигена (Т,Г)-А-Л
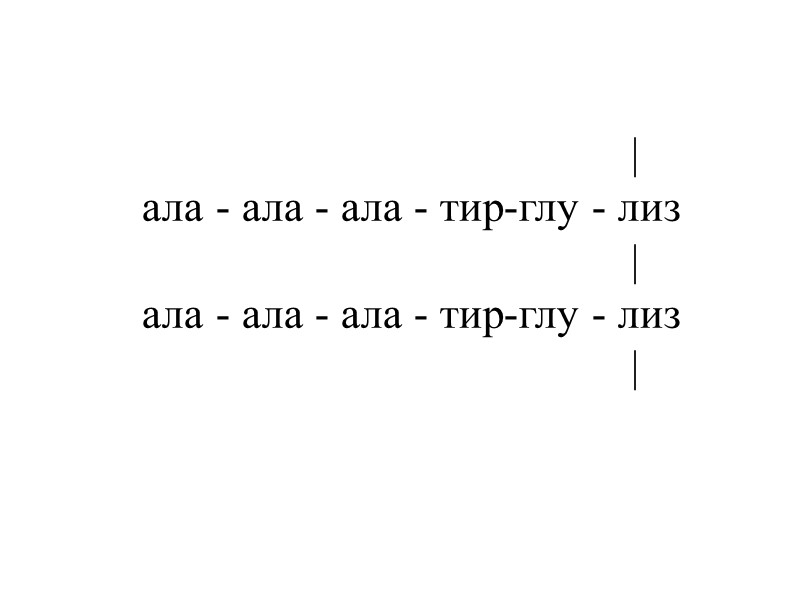 | ала - ала - ала - тир-глу - лиз | ала - ала - ала - тир-глу - лиз |
| ала - ала - ала - тир-глу - лиз | ала - ала - ала - тир-глу - лиз |
 Факторы, влияющие на иммуногенность антигенов - молекулярная масса; - структурная гетерогенность; - жесткость конформации
Факторы, влияющие на иммуногенность антигенов - молекулярная масса; - структурная гетерогенность; - жесткость конформации
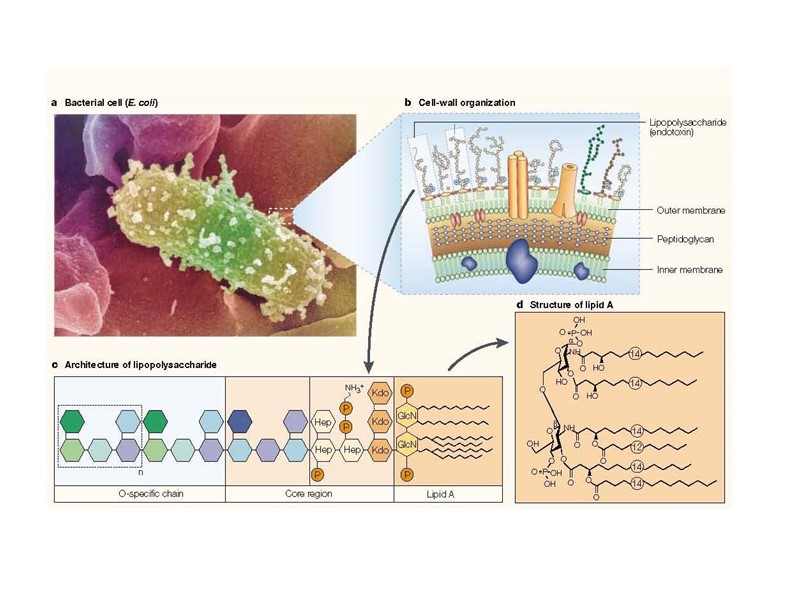
 состоящие из повторяющихся звеньев, содержащих остатки разных амино- и моносахаридов, обладают при достаточной молекулярной массе свойствами полных антигенов. Особенно высокой иммуногенностью обладают комплексы бактериальных гетерополисахаридов с липидами. Гетерополисариды,
состоящие из повторяющихся звеньев, содержащих остатки разных амино- и моносахаридов, обладают при достаточной молекулярной массе свойствами полных антигенов. Особенно высокой иммуногенностью обладают комплексы бактериальных гетерополисахаридов с липидами. Гетерополисариды,

 Тимуснезависимые антигены Как правило, имеют наряду с высокой молекулярной массой и структурной гетерогенностью: 1) достаточно жесткую структуру; 2) большое количество часто повторяющихся детерминант. В результате они способны к перекрестному связыванию большого количества антительных или иммуноглобулиновых рецепторов на поверхности В-лимфоцитов.
Тимуснезависимые антигены Как правило, имеют наряду с высокой молекулярной массой и структурной гетерогенностью: 1) достаточно жесткую структуру; 2) большое количество часто повторяющихся детерминант. В результате они способны к перекрестному связыванию большого количества антительных или иммуноглобулиновых рецепторов на поверхности В-лимфоцитов.
 В результате соответствующие клоны В-лимфоцитов получают мощный активационный сигнал и вступают в пролиферацию и дифференцировку с образованием антителообразующих клеток без участия Т-хелперов.
В результате соответствующие клоны В-лимфоцитов получают мощный активационный сигнал и вступают в пролиферацию и дифференцировку с образованием антителообразующих клеток без участия Т-хелперов.
 Тимуснезависимые антигены 1 типа - LPS E. coli. Характерно адъювантное действие. 2 типа - вызывают перекрестную сшивку рецепторов - поливинилпирролидон и полимеры D-аминокислот.
Тимуснезависимые антигены 1 типа - LPS E. coli. Характерно адъювантное действие. 2 типа - вызывают перекрестную сшивку рецепторов - поливинилпирролидон и полимеры D-аминокислот.
 Гомополисахариды Декстран состоит из остатков α-D-глюкозы, соединенных как и в крахмале 1-4- и 1-6-гликозидными связями. При молекулярной массе 75000 не обладает иммуногенностью и используется как кровезаменитель. При молекулярной массе 600000 и выше приобретает иммуногенность.
Гомополисахариды Декстран состоит из остатков α-D-глюкозы, соединенных как и в крахмале 1-4- и 1-6-гликозидными связями. При молекулярной массе 75000 не обладает иммуногенностью и используется как кровезаменитель. При молекулярной массе 600000 и выше приобретает иммуногенность.
 Нуклеиновые кислоты Обычно неиммуногенны, но если их присоединить, например, к белкам, то, иммунизируя конъюгатами можно получить антитела к ДНК и РНК. Особенно хорошо антитела образуются при иммунизации отрицательно заряженными нуклеиновыми кислотами в комплексе с положительно заряженными белками.
Нуклеиновые кислоты Обычно неиммуногенны, но если их присоединить, например, к белкам, то, иммунизируя конъюгатами можно получить антитела к ДНК и РНК. Особенно хорошо антитела образуются при иммунизации отрицательно заряженными нуклеиновыми кислотами в комплексе с положительно заряженными белками.
 Липиды Как правило, неиммуногенны и антител к простым липидам, таким как жиры и воска получить не удается. Однако многие липиды являются гаптенами, что положено в основу получения антител к стероидам и фосфолипидам.
Липиды Как правило, неиммуногенны и антител к простым липидам, таким как жиры и воска получить не удается. Однако многие липиды являются гаптенами, что положено в основу получения антител к стероидам и фосфолипидам.
 Природные антигены относятся к смешанным соединениям. Например, антигены групп крови являются гликофосфолипидами, специфичность которых связана с углеводной частью молекулы, являющейся гетерополисахаридом. Наследование групп крови связано с наследованием различных ферментов - гликозилтрансфераз.
Природные антигены относятся к смешанным соединениям. Например, антигены групп крови являются гликофосфолипидами, специфичность которых связана с углеводной частью молекулы, являющейся гетерополисахаридом. Наследование групп крови связано с наследованием различных ферментов - гликозилтрансфераз.
 Антигены групп крови системы ABO
Антигены групп крови системы ABO
 Иммуногенность антигенов помимо рассмотренных выше структурных особенностей: - молекулярной массы; - структурной гетерогенности; - жесткости конформации зависит и от их способности к катаболизму.
Иммуногенность антигенов помимо рассмотренных выше структурных особенностей: - молекулярной массы; - структурной гетерогенности; - жесткости конформации зависит и от их способности к катаболизму.
 Иммуногенность антигенов и их способность к катаболизму С одной стороны, легко катаболизируемые вещества не являются антигенами. С другой - таковыми не являются вообще некатаболизируемые соединения. Общая закономерность - чем дольше находится антиген в организме - тем выше его иммуногенность.
Иммуногенность антигенов и их способность к катаболизму С одной стороны, легко катаболизируемые вещества не являются антигенами. С другой - таковыми не являются вообще некатаболизируемые соединения. Общая закономерность - чем дольше находится антиген в организме - тем выше его иммуногенность.
 Классификация антигенов по происхождению Антигены микробного и паразитарного происхождения (вирусные, бактериальные, грибковые, простейших, гельминтов и др.) 2. Растительные антигены 3. Антигены тканей животных и человека -ксеноантигены -аллоантигены -изоантигены -эмбриоспецифические -опухолевоспецифические 4. Аутоантигены 5. Синтетические антигены
Классификация антигенов по происхождению Антигены микробного и паразитарного происхождения (вирусные, бактериальные, грибковые, простейших, гельминтов и др.) 2. Растительные антигены 3. Антигены тканей животных и человека -ксеноантигены -аллоантигены -изоантигены -эмбриоспецифические -опухолевоспецифические 4. Аутоантигены 5. Синтетические антигены
 Итак, главная функция иммунной системы – поддержание генетического постоянства (однородности, индивидуальности, гомеостаза) организма.
Итак, главная функция иммунной системы – поддержание генетического постоянства (однородности, индивидуальности, гомеостаза) организма.
 Реализация этой функции иммунной системы обеспечивается за счет: 1) распознавания «чужого» и «измененного своего»; 2) их элиминации в результате эффекторных механизмов врожденного и приобретенного иммунитета; 3) сохранения способности к более высокому ответу при повторном контакте с теми же антигенами (иммунологическая память)
Реализация этой функции иммунной системы обеспечивается за счет: 1) распознавания «чужого» и «измененного своего»; 2) их элиминации в результате эффекторных механизмов врожденного и приобретенного иммунитета; 3) сохранения способности к более высокому ответу при повторном контакте с теми же антигенами (иммунологическая память)
 ИММУНИТЕТ = распознавание + элиминация + память
ИММУНИТЕТ = распознавание + элиминация + память

