 Законы идеального газа
Законы идеального газа
 Идеальный газ n 1. Идеальным газом называется газ, в котором отсутствуют силы межмолекулярного взаимодействия. С достаточной степенью точности газы можно считать идеальными в тех случаях, когда рассматриваются их состояния, далекие от областей фазовых превращений. Для идеальных газов справедливы следующие законы :
Идеальный газ n 1. Идеальным газом называется газ, в котором отсутствуют силы межмолекулярного взаимодействия. С достаточной степенью точности газы можно считать идеальными в тех случаях, когда рассматриваются их состояния, далекие от областей фазовых превращений. Для идеальных газов справедливы следующие законы :
 Закон Бойля - Mаpиоттa n Это один из основных газовых законов, описывает изотермические процессы (T=const) в идеальных газах. Установлен независимо друг от друга при экспериментальном изучении зависимости давления газа от его объема при постоянной температуре Р. Бойлем в 1662 и Э. Мариоттом в 1676. n При неизменных температуре и массе произведение численных значений давления и объема газа постоянно: n p. V = const
Закон Бойля - Mаpиоттa n Это один из основных газовых законов, описывает изотермические процессы (T=const) в идеальных газах. Установлен независимо друг от друга при экспериментальном изучении зависимости давления газа от его объема при постоянной температуре Р. Бойлем в 1662 и Э. Мариоттом в 1676. n При неизменных температуре и массе произведение численных значений давления и объема газа постоянно: n p. V = const
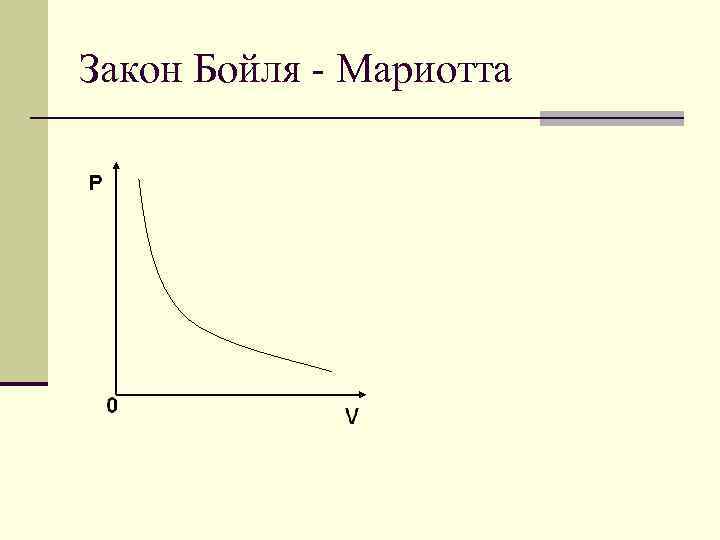 Закон Бойля - Mаpиоттa
Закон Бойля - Mаpиоттa
 Закон Гей-Люссака n Это один из основных газовых законов, описывает изобарные процессы(p=const) в идеальных газах. Закон открыт независимо Ж. Л. Гей-Люссаком в 1802 г. и Дж. Дальтоном в 1801 г. n при постоянном давлении объем данной массы газа прямо пропорционален его абсолютной температуре: n V = V 0(1 + at) где V - объем газа при температуре t, °С V 0 – его объем при 0°С a -температурный коэффициент объемного расширения. Для всех газов a = (1/273°С– 1). Следовательно, V = V 0(1 +(1/273)t)
Закон Гей-Люссака n Это один из основных газовых законов, описывает изобарные процессы(p=const) в идеальных газах. Закон открыт независимо Ж. Л. Гей-Люссаком в 1802 г. и Дж. Дальтоном в 1801 г. n при постоянном давлении объем данной массы газа прямо пропорционален его абсолютной температуре: n V = V 0(1 + at) где V - объем газа при температуре t, °С V 0 – его объем при 0°С a -температурный коэффициент объемного расширения. Для всех газов a = (1/273°С– 1). Следовательно, V = V 0(1 +(1/273)t)
 Закон Гей-Люссака Графически зависимость объема от температуры изображается прямой линией – изобарой. При очень низких температурах (близких к – 273°С) закон Гей-Люссака не выполняется, поэтому сплошная линия на графике заменена пунктиром.
Закон Гей-Люссака Графически зависимость объема от температуры изображается прямой линией – изобарой. При очень низких температурах (близких к – 273°С) закон Гей-Люссака не выполняется, поэтому сплошная линия на графике заменена пунктиром.
 Закон Шарля n Закон Шарля, один из основных газовых законов, описывает изохорные процессы(V=const) в идеальных газах. n при постоянном объеме давление данной массы газа прямо пропорционально его абсолютной температуре: n p = p 0(1+gt) где р0 - давление газа при температуре t = 273, 15 К. g -температурный коэффициент давления. Его значение не зависит от природы газа; для всех газов = 1/273 °С– 1. Таким образом, p = p 0(1 +(1/273)t)
Закон Шарля n Закон Шарля, один из основных газовых законов, описывает изохорные процессы(V=const) в идеальных газах. n при постоянном объеме давление данной массы газа прямо пропорционально его абсолютной температуре: n p = p 0(1+gt) где р0 - давление газа при температуре t = 273, 15 К. g -температурный коэффициент давления. Его значение не зависит от природы газа; для всех газов = 1/273 °С– 1. Таким образом, p = p 0(1 +(1/273)t)
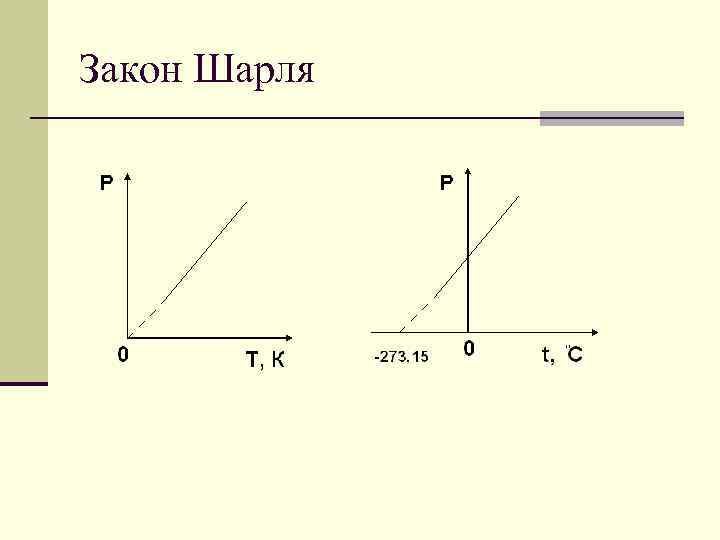 Закон Шарля
Закон Шарля
 Закон Авогадро n Закон Авогадро, один из основных законов идеальных газов. Закон был открыт А. Авогадро в 1811. n при одинаковых давлениях и одинаковых температурах и равных объемах различных идеальных газов содержится одинаковое число молекул; или, что то же самое: при одинаковых давлениях и одинаковых температурах грамм-молекулы различных идеальных газов занимают одинаковые объемы. n Согласно закону Авогадро, 1 моль любого идеального газа при нормальных условиях занимает одинаковый объем. При давлении р =101, 325 к. Па и температуре Т = 273, 15 К этот объем равен 22, 41383 м 3. Следовательно, моль любого вещества содержит одно и то же число молекул, равное числу Авогадро 6, 022045(31). 1023 моль-1.
Закон Авогадро n Закон Авогадро, один из основных законов идеальных газов. Закон был открыт А. Авогадро в 1811. n при одинаковых давлениях и одинаковых температурах и равных объемах различных идеальных газов содержится одинаковое число молекул; или, что то же самое: при одинаковых давлениях и одинаковых температурах грамм-молекулы различных идеальных газов занимают одинаковые объемы. n Согласно закону Авогадро, 1 моль любого идеального газа при нормальных условиях занимает одинаковый объем. При давлении р =101, 325 к. Па и температуре Т = 273, 15 К этот объем равен 22, 41383 м 3. Следовательно, моль любого вещества содержит одно и то же число молекул, равное числу Авогадро 6, 022045(31). 1023 моль-1.