Простой обратимый процесс.ppt
- Количество слайдов: 19

Закономерности управления простым обратимым процессом

простой обратимый процесс а. А + b. В c. С + d. D, где С – целевой продукт Химическое равновесие Константа равновесия Кс или Кр * - равновесная конверсия реагента * - равновесный выход целевого продукта
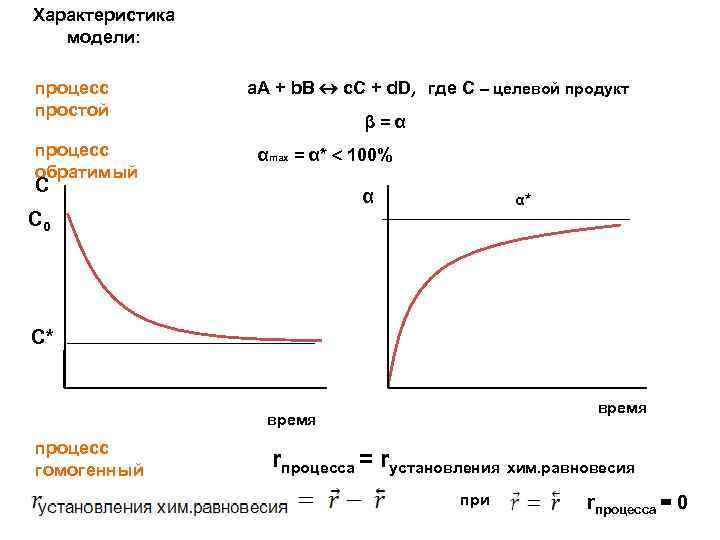
Характеристика модели: процесс простой процесс обратимый а. А + b. В c. С + d. D, где С – целевой продукт β=α αmax = α* 100% С α α* С 0 С* время процесс гомогенный rпроцесса = rустановления хим. равновесия при rпроцесса = 0

Объекты управления: rустановления хим. равновесия положение равновесия - * Инструменты управления: кинетические параметры rустановления хим. равновесия = f 1(C, p, t, kat) * = f 2(C, p, t) Принцип Ле-Шателье «Если на систему, находящуюся в равновесии, воздействовать извне, изменяя какое-нибудь из условий, определяющих равновесие, то равновесие смещается в направлении уменьшения эффекта воздействия»
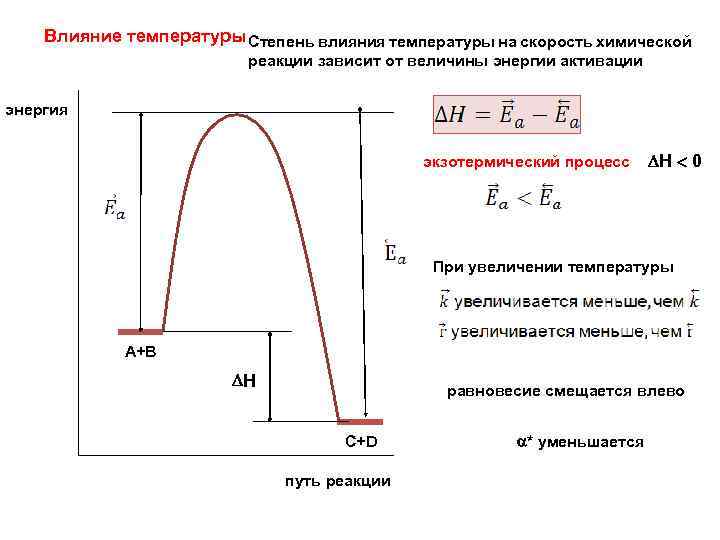
Влияние температуры Степень влияния температуры на скорость химической реакции зависит от величины энергии активации энергия экзотермический процесс Н 0 При увеличении температуры А+В H равновесие смещается влево C+D путь реакции * уменьшается
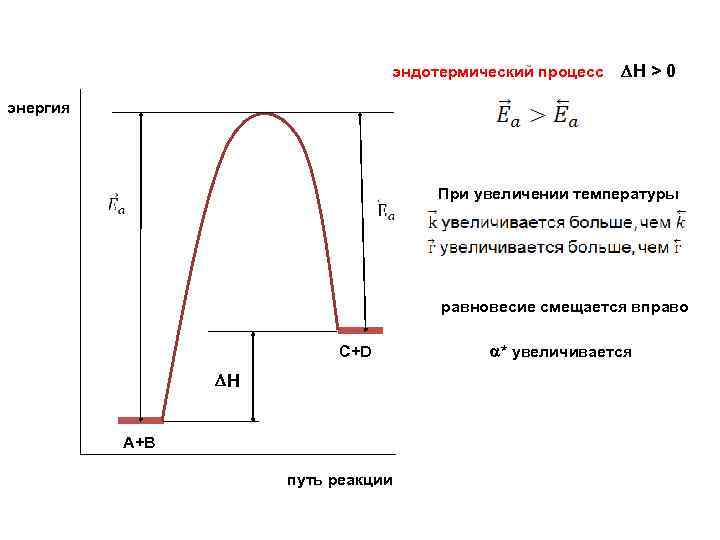
эндотермический процесс Н > 0 энергия При увеличении температуры равновесие смещается вправо C+D H А+В путь реакции * увеличивается
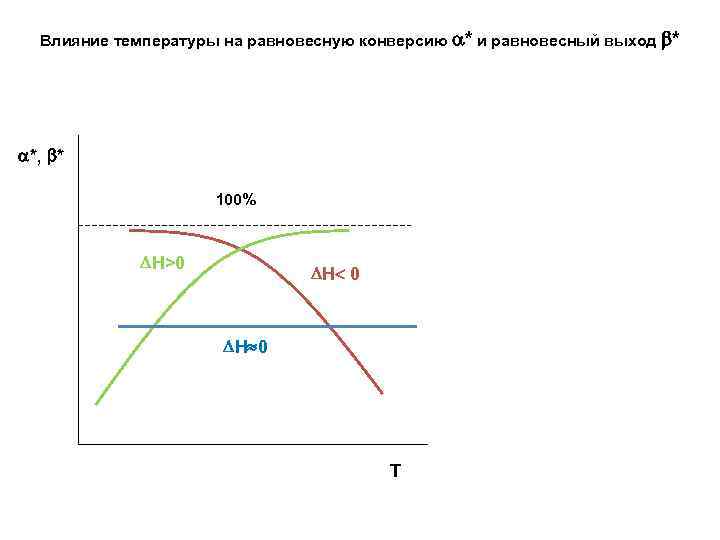
Влияние температуры на равновесную конверсию * и равновесный выход * *, * 100% Н>0 Н 0 Т
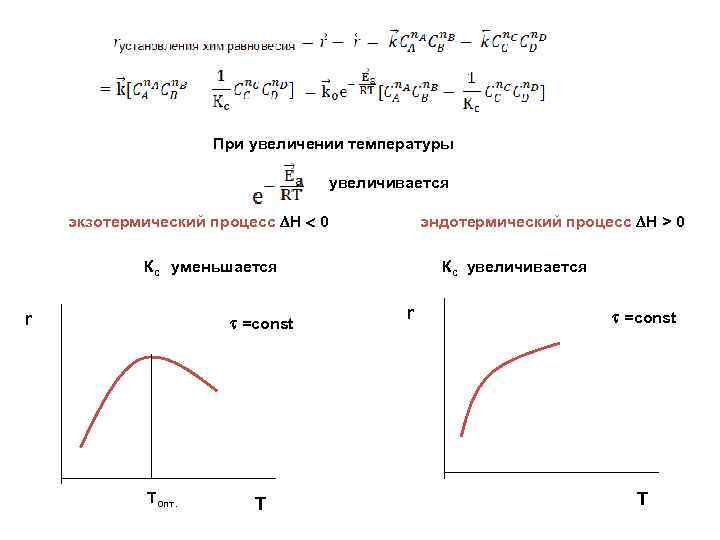
При увеличении температуры увеличивается экзотермический процесс Н 0 эндотермический процесс Н > 0 Кс уменьшается r =const Tопт. T Кс увеличивается r =const T
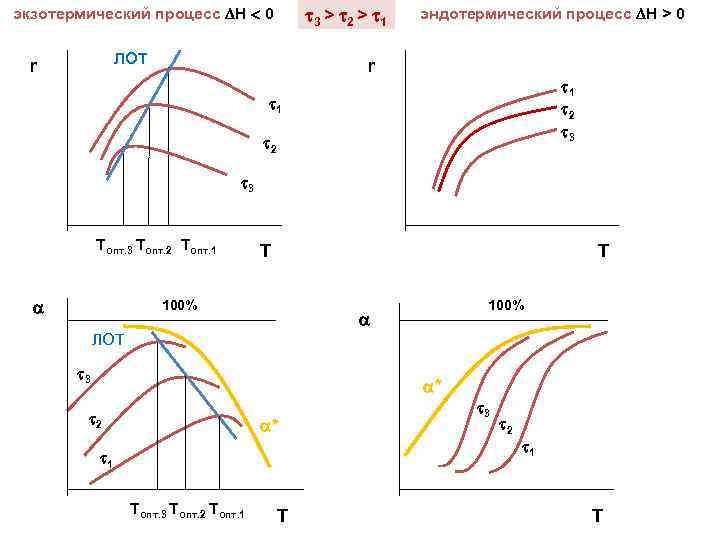
3 > 2 > 1 экзотермический процесс Н 0 ЛОТ r эндотермический процесс Н > 0 r 1 2 3 Tопт. 2 Tопт. 1 T T 100% ЛОТ 3 * 2 * 3 2 1 1 Tопт. 3 Tопт. 2 Tопт. 1 T T

экзотермический процесс Н 0 эндотермический процесс Н > 0 Сначала реакционную смесь нагревают для обеспечения высокой скорости процесса, а затем охлаждают по линии оптимальных температур (ЛОТ) для достижения более высокого значения конверсии при максимально возможных скоростях – режим понижающихся температур Процесс проводят при максимальной температуре постоянной температуры оптимально – режим
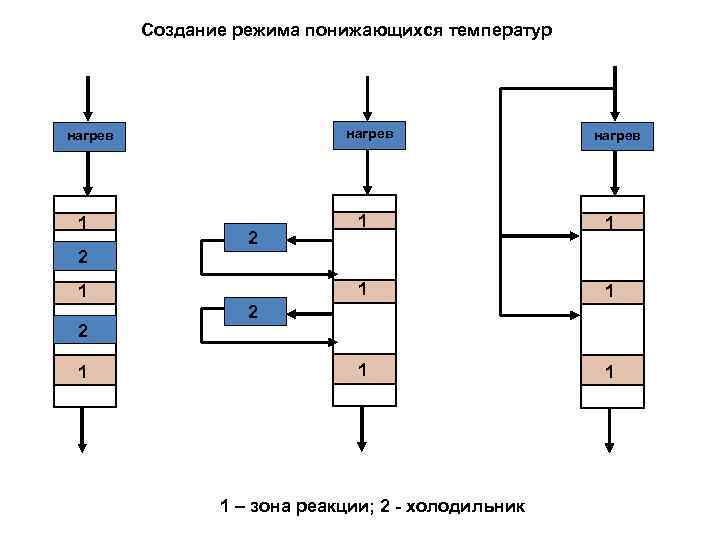
Создание режима понижающихся температур нагрев 1 2 1 1 1 2 1 2 нагрев 1 2 1 – зона реакции; 2 - холодильник
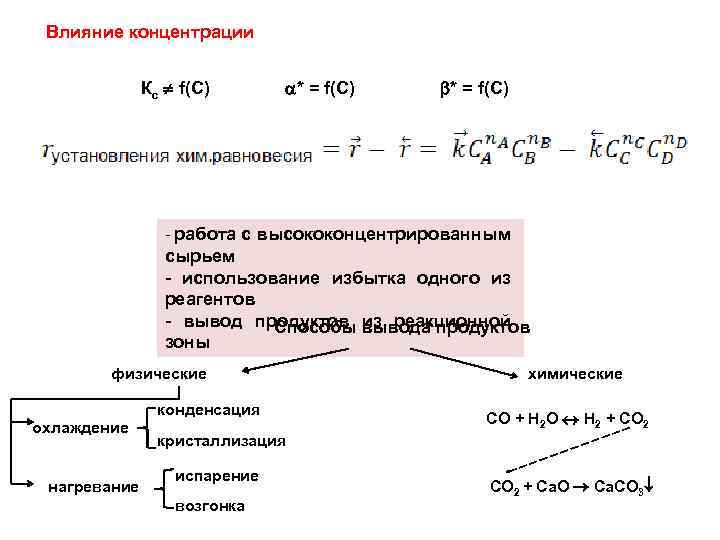
Влияние концентрации Кс f(С) * = f(С) - работа с высококонцентрированным сырьем - использование избытка одного из реагентов - вывод продуктов вывода продуктов Способы из реакционной зоны физические охлаждение нагревание конденсация химические СО + Н 2 О Н 2 + CO 2 кристаллизация испарение возгонка CO 2 + Ca. O Cа. CO 3

Влияние давления Давление влияет на газофазные реакции Степень влияния давления зависит от порядка реакции При увеличении давления равновесие не смещается * = const равновесие смещается вправо * увеличивается равновесие смещается влево * уменьшается

Окисление SO 2 до SO 3 2 SO 2(г) + O 2(г) 2 SO 3(г), Н = -94, 23 к. Дж/моль, kat –V 2 O 5 Технологическая классификация процесса: Объекты управления: простой, обратимый, каталитический, газофазный, но гетерогенный, экзотермический процесс rпроцесса положение равновесия Катализаторы: БАВ, СВД, CВC, ИК, содержащие 8% V 2 O 5 /носитель, очистка сырья Лимитирующая стадия – диффузия молекул в поры катализатора Т = 400 -6000 С, режим понижающихся температур 300% избыток кислорода, разбавление обжигового газа (14 -15% об. SO 2) воздухом Вывод продуктов из реакционной зоны (метод двойного контактирования) Абсорбция SO 3 98, 3%-ной Н 2 SO 4 (моногидратом) при Т 1000 C
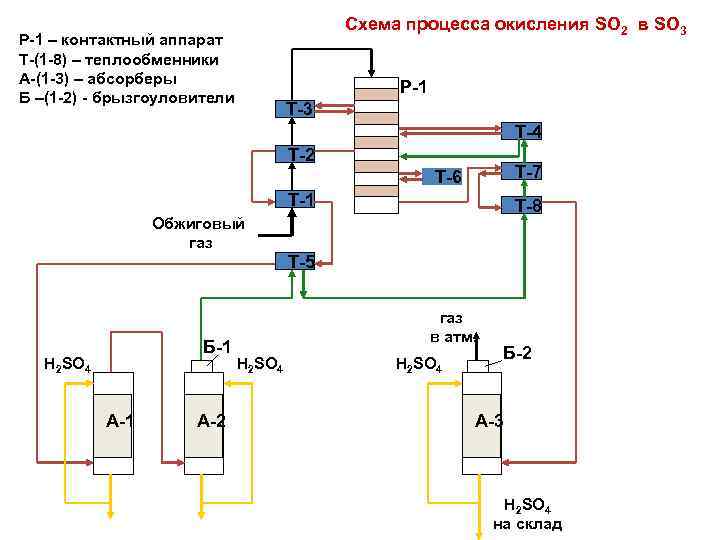
Схема процесса окисления SO 2 в SO 3 Р-1 – контактный аппарат Т-(1 -8) – теплообменники А-(1 -3) – абсорберы Б –(1 -2) - брызгоуловители Р-1 Т-3 Т-4 Т-2 Т-7 Т-6 Т-1 Т-8 Обжиговый газ Т-5 Б-1 Н 2 SO 4 А-1 А-2 газ в атм. Н 2 SO 4 Б-2 А-3 Н 2 SO 4 на склад
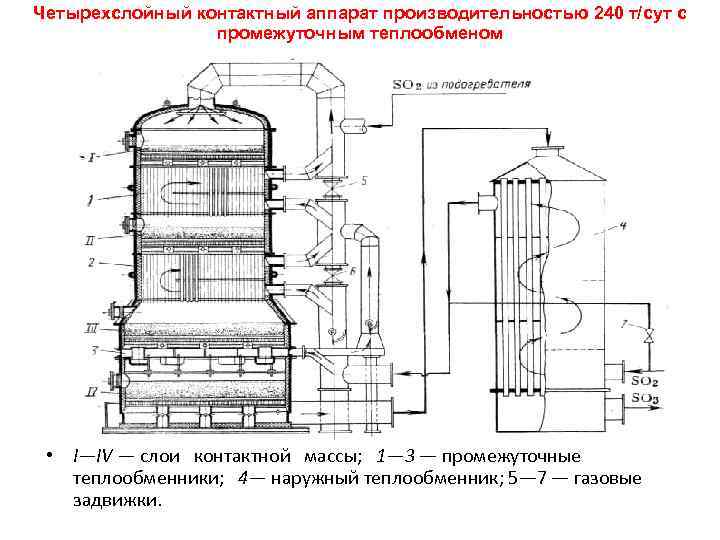
Четырехслойный контактный аппарат производительностью 240 т/сут с промежуточным теплообменом • I—IV — слои контактной массы; 1— 3 — промежуточные теплообменники; 4— наружный теплообменник; 5— 7 — газовые задвижки.
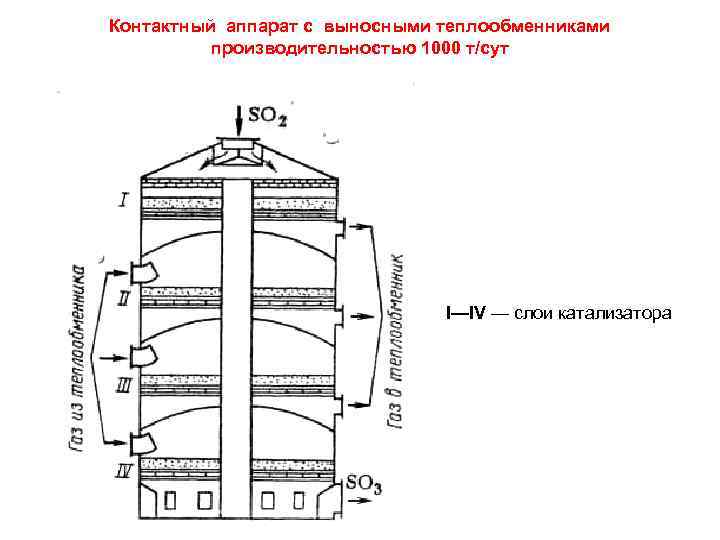
Контактный аппарат с выносными теплообменниками производительностью 1000 т/сут I—IV — слои катализатора
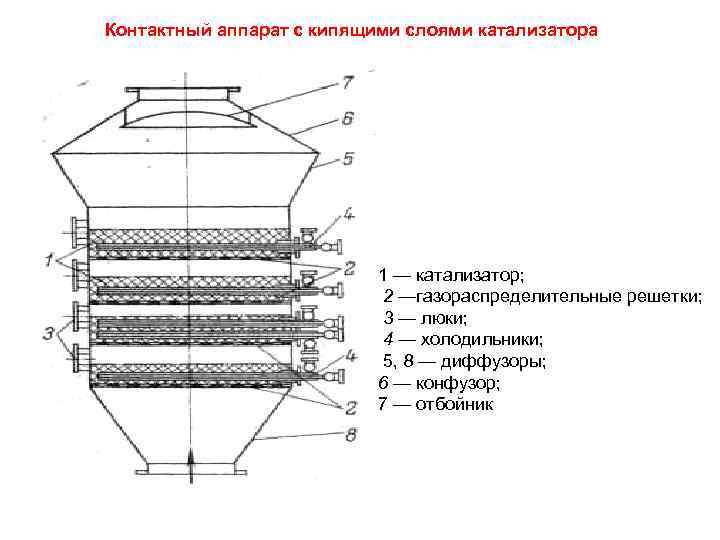
Контактный аппарат с кипящими слоями катализатора 1 — катализатор; 2 —газораспределительные решетки; 3 — люки; 4 — холодильники; 5, 8 — диффузоры; 6 — конфузор; 7 — отбойник

• Схема производства серной кислоты из колчедана 1 — печь; 2 — система гидроудаления огарка; 3 — котел-утилизатор; 4 — циклон с пересыпным устройством; 5 — сухой электрофильтр; 6 — первая промывная башня; 7 — вторая промывная башня; 8 — первый мокрый электрофильтр; 9 — второй мокрый электрофильтр; 10— сушильная башня; 11 — газодувка; 12 — фильтр-брызгоуловитель; 13 — теплообменники контактного узла; 14 — контактный аппарат; 15 — олеумный абсорбер; 16 — первый моногидратный абсорбер; 17 — второй моногидратный абсорбер; 18 — сборники кислоты; 19 — холодильники; 20 — холодильник воздушного охлаждения кислоты; 21 — пусковой подогреватель.
Простой обратимый процесс.ppt