Материал_К_Лекции.ppt
- Количество слайдов: 55
 ЗАКОН ДЕЙСТВУЮЩИХ МАСС. • Скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, возведенных в степень их стехиометрических коэффициентов (v) • v=k[A]m[B]n • k – константа скорости, постоянная при данной реакции ( при определенной температуре) величина, характеризующая влияние природы реагирующих веществ на скорость их взаимодействия друг с другом; • [ ] – означают концентрацию реагирующих веществ в моль/л • В случае обратимых реакций устанавливается подвижное химическое равновесие, при котором в системе одновременно присутствуют как исходные, так и образующиеся вещества. 1 2/1/2018
ЗАКОН ДЕЙСТВУЮЩИХ МАСС. • Скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, возведенных в степень их стехиометрических коэффициентов (v) • v=k[A]m[B]n • k – константа скорости, постоянная при данной реакции ( при определенной температуре) величина, характеризующая влияние природы реагирующих веществ на скорость их взаимодействия друг с другом; • [ ] – означают концентрацию реагирующих веществ в моль/л • В случае обратимых реакций устанавливается подвижное химическое равновесие, при котором в системе одновременно присутствуют как исходные, так и образующиеся вещества. 1 2/1/2018
 Химическим равновесием называют такое состояние системы реагирующих веществ, при котором скорости прямой и обратной реакции равны. • Для системы • • • a. A+b. B =c. C +d. D скорость прямой реакции v 1= k[A]a[B]b, а скорость обратной реакции v 2= k[C]c[D]d. При химическом равновесии v 1= v 2. Поэтому можно написать : k 1[A]a[B]b= k 2[C]c[D]d. После преобразования получим k 2 / k 1 =([C]c[D]d) / ([A]a[B]b). Но отношение двух постоянных величин k 1/ k 2, есть величина постоянная, которую обозначают К и называют константой равновесия, т. е. К =([C]c[D]d) / ([A]a[B]b). 2/1/2018 2
Химическим равновесием называют такое состояние системы реагирующих веществ, при котором скорости прямой и обратной реакции равны. • Для системы • • • a. A+b. B =c. C +d. D скорость прямой реакции v 1= k[A]a[B]b, а скорость обратной реакции v 2= k[C]c[D]d. При химическом равновесии v 1= v 2. Поэтому можно написать : k 1[A]a[B]b= k 2[C]c[D]d. После преобразования получим k 2 / k 1 =([C]c[D]d) / ([A]a[B]b). Но отношение двух постоянных величин k 1/ k 2, есть величина постоянная, которую обозначают К и называют константой равновесия, т. е. К =([C]c[D]d) / ([A]a[B]b). 2/1/2018 2
 Константа равновесия • Константа равновесия(К) показывает во сколько раз скорость прямой реакции больше скорости обратной реакции (приданной температуре и одинаковой концентрации). • Если К=1, → то скорость прямой реакции равна скорости обратной реакции, • если К >1, то преобладает прямая реакция и динамическое равновесие сдвинуто вправо, • К меньше 1 динамическое равновесие сдвинуто влево и преобладает обратная реакция. • • • Например для обратимой реакции уравнение имеет вид: Fe. Cl 3 + 3 NH 4 SCN = Fe(SCN)3 + 3 NH 4 Cl уравнение константы равновесия имеет вид: К=[Fe(SCN)3][NH 4 Cl]3 [Fe. Cl 3][ NH 4 SCN]3 Однако з-н действующих масс и понятие о химическом равновесии применимы только к неэлектролитам и к слабым электролитам в разбавленных водных ( или неводных ) растворах. 2/1/2018 3
Константа равновесия • Константа равновесия(К) показывает во сколько раз скорость прямой реакции больше скорости обратной реакции (приданной температуре и одинаковой концентрации). • Если К=1, → то скорость прямой реакции равна скорости обратной реакции, • если К >1, то преобладает прямая реакция и динамическое равновесие сдвинуто вправо, • К меньше 1 динамическое равновесие сдвинуто влево и преобладает обратная реакция. • • • Например для обратимой реакции уравнение имеет вид: Fe. Cl 3 + 3 NH 4 SCN = Fe(SCN)3 + 3 NH 4 Cl уравнение константы равновесия имеет вид: К=[Fe(SCN)3][NH 4 Cl]3 [Fe. Cl 3][ NH 4 SCN]3 Однако з-н действующих масс и понятие о химическом равновесии применимы только к неэлектролитам и к слабым электролитам в разбавленных водных ( или неводных ) растворах. 2/1/2018 3
 • ТЕОРЕТИЧЕСКИЕ ОСНОВЫ АНАЛИТИКИ Некоторые положения теории электролитов и закона действующих масс, применяемых в аналитике. а) Положения теории электролитов Электролиты – вещества, способные, распадаться на ионы ( более точная формулировка: проводники, через которые электрического тока вызывает перемещение ионов ( ионная проводимость) и химические реакции ) электрохимические реакции. Раствор - гомогенная смесь двух или нескольких веществ, способная непрерывно изменять свои свойства. Центральной теорией аналитической химии можно назвать теорию электролитической диссоциации Шведского ученого Свант Август Аррениус, созданной в 1887 году. « Электролиты в растворах (диссоциируют) на ионы вследствие взаимодействия с ионами растворителя » Количественно ионизация ( диссоциация на ионы) электролита в растворе характеризуется степенью диссоциации( ионизации) – (греческая). • • • 2/1/2018 4
• ТЕОРЕТИЧЕСКИЕ ОСНОВЫ АНАЛИТИКИ Некоторые положения теории электролитов и закона действующих масс, применяемых в аналитике. а) Положения теории электролитов Электролиты – вещества, способные, распадаться на ионы ( более точная формулировка: проводники, через которые электрического тока вызывает перемещение ионов ( ионная проводимость) и химические реакции ) электрохимические реакции. Раствор - гомогенная смесь двух или нескольких веществ, способная непрерывно изменять свои свойства. Центральной теорией аналитической химии можно назвать теорию электролитической диссоциации Шведского ученого Свант Август Аррениус, созданной в 1887 году. « Электролиты в растворах (диссоциируют) на ионы вследствие взаимодействия с ионами растворителя » Количественно ионизация ( диссоциация на ионы) электролита в растворе характеризуется степенью диссоциации( ионизации) – (греческая). • • • 2/1/2018 4
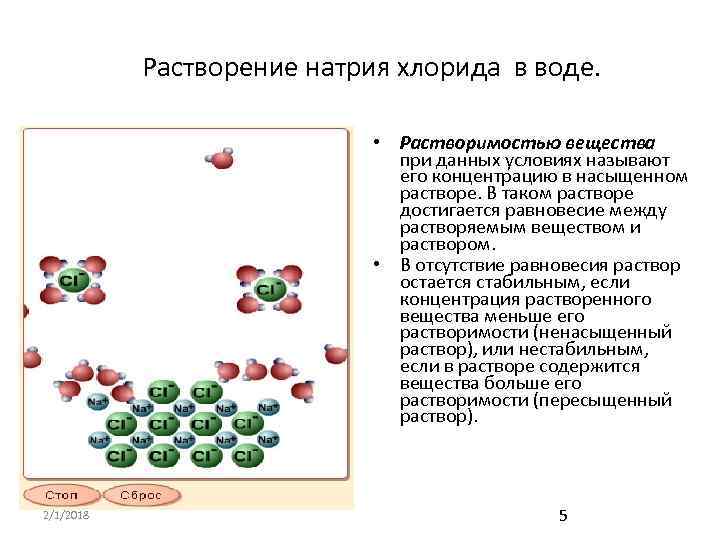 Растворение натрия хлорида в воде. • Растворимостью вещества при данных условиях называют его концентрацию в насыщенном растворе. В таком растворе достигается равновесие между растворяемым веществом и раствором. • В отсутствие равновесия раствор остается стабильным, если концентрация растворенного вещества меньше его растворимости (ненасыщенный раствор), или нестабильным, если в растворе содержится вещества больше его растворимости (пересыщенный раствор). 2/1/2018 5
Растворение натрия хлорида в воде. • Растворимостью вещества при данных условиях называют его концентрацию в насыщенном растворе. В таком растворе достигается равновесие между растворяемым веществом и раствором. • В отсутствие равновесия раствор остается стабильным, если концентрация растворенного вещества меньше его растворимости (ненасыщенный раствор), или нестабильным, если в растворе содержится вещества больше его растворимости (пересыщенный раствор). 2/1/2018 5
 Химическое равновесие в реальных системах • Фундаментальные законы термодинамики описывают равновесие в идеальных системах (идеальных растворах). Однако можно адаптировать этот математический аппарат для описания реальных растворов. • Факторы влияющие на равновесие в реальной системе: а) электростатические б) химические взаимодействия Границы между ними условны. Например, сольватационные эффекты, обусловленные взаимодействием растворенных частиц с молекулами растворителя, обычно имеют частично электростатическую, частично химическую природу. 2/1/2018 6
Химическое равновесие в реальных системах • Фундаментальные законы термодинамики описывают равновесие в идеальных системах (идеальных растворах). Однако можно адаптировать этот математический аппарат для описания реальных растворов. • Факторы влияющие на равновесие в реальной системе: а) электростатические б) химические взаимодействия Границы между ними условны. Например, сольватационные эффекты, обусловленные взаимодействием растворенных частиц с молекулами растворителя, обычно имеют частично электростатическую, частично химическую природу. 2/1/2018 6
 Электростатические взаимодействия • К ним относятся (в порядке убываний энергий взаимодействий): • Кулоновские взаимодействия между ионами • Ион-дипольные и диполь-дипольные взаимодействия с участием полярных молекул • Ван-дер-ваальсовы взаимодействия между любыми частицами присутствующими в растворе. Очевидно также, что энергия электростатического взаимодействия зависит от химической природы частиц: Еаа≠Евв ≠Еав. Тогда как для идеальных растворов Еаа=Евв=Еав. Для нейтральных молекул силы электростатического взаимодействия малы и проявляются только на коротких расстояниях, поэтому отклонение свойств неэлектролитов от идеальности становятся заметными лишь при высоких расстояниях. Напротив, взаимодействия между ионами весьма сильны и проявляются даже на больших расстояниях. Поэтому для растворов электролитов отклонения от идеальности выражены значительно сильнее и проявляются в разбавленных растворах. Учет электростатических взаимодействий проводят с помощью приема, называемого метода активности. 2/1/2018 7
Электростатические взаимодействия • К ним относятся (в порядке убываний энергий взаимодействий): • Кулоновские взаимодействия между ионами • Ион-дипольные и диполь-дипольные взаимодействия с участием полярных молекул • Ван-дер-ваальсовы взаимодействия между любыми частицами присутствующими в растворе. Очевидно также, что энергия электростатического взаимодействия зависит от химической природы частиц: Еаа≠Евв ≠Еав. Тогда как для идеальных растворов Еаа=Евв=Еав. Для нейтральных молекул силы электростатического взаимодействия малы и проявляются только на коротких расстояниях, поэтому отклонение свойств неэлектролитов от идеальности становятся заметными лишь при высоких расстояниях. Напротив, взаимодействия между ионами весьма сильны и проявляются даже на больших расстояниях. Поэтому для растворов электролитов отклонения от идеальности выражены значительно сильнее и проявляются в разбавленных растворах. Учет электростатических взаимодействий проводят с помощью приема, называемого метода активности. 2/1/2018 7
 Активность ионов в растворах электролитов • Понятие "активность" введено для того, чтобы количественными соотношениями, справедливыми для идеальных растворов, можно было описать свойства реальных растворов. В частности, закон действующих масс применительно к растворам электролитов выполняется в том случае, если вместо концентраций частиц подразумевать их активности. • Таким образом, активность (а) — эффективная '(действующая) концентрация частиц в растворе, , пропорциональная их аналитической концентрации. α=f*C, • где С — аналитическая моляльная или молярная концентрация частиц, f— коэффициент активности. Размерность активности совпадает с размерностью моляльной (моль/кг) или молярной (моль/дм 3) концентрации частиц. 2/1/2018 8
Активность ионов в растворах электролитов • Понятие "активность" введено для того, чтобы количественными соотношениями, справедливыми для идеальных растворов, можно было описать свойства реальных растворов. В частности, закон действующих масс применительно к растворам электролитов выполняется в том случае, если вместо концентраций частиц подразумевать их активности. • Таким образом, активность (а) — эффективная '(действующая) концентрация частиц в растворе, , пропорциональная их аналитической концентрации. α=f*C, • где С — аналитическая моляльная или молярная концентрация частиц, f— коэффициент активности. Размерность активности совпадает с размерностью моляльной (моль/кг) или молярной (моль/дм 3) концентрации частиц. 2/1/2018 8
 Коэффициент активности (f) • Коэффициент активности (f) характеризует степень отклонения свойств реальных растворов от свойств идеальных растворов и определяется как f=al. C. В идеальных растворах коэффициент активности равен единице, а активность частиц равна их концентрации. Свойства очень разбавленных растворов, в которых взаимодействие между частицами (ионами) растворенного вещества минимально, близки к свойствам идеальных растворов. Поэтому для очень разбавленных растворов принимают, что f» 1, а» С. • Коэффициенты активности ионов в водных растворах электролитов зависят от температуры, ионной силы раствора, заряда иона, а также (для концентрированных растворов) от размера иона. 2/1/2018 9
Коэффициент активности (f) • Коэффициент активности (f) характеризует степень отклонения свойств реальных растворов от свойств идеальных растворов и определяется как f=al. C. В идеальных растворах коэффициент активности равен единице, а активность частиц равна их концентрации. Свойства очень разбавленных растворов, в которых взаимодействие между частицами (ионами) растворенного вещества минимально, близки к свойствам идеальных растворов. Поэтому для очень разбавленных растворов принимают, что f» 1, а» С. • Коэффициенты активности ионов в водных растворах электролитов зависят от температуры, ионной силы раствора, заряда иона, а также (для концентрированных растворов) от размера иона. 2/1/2018 9
 Ионная сила раствора • Ионная сила раствора (/) — мера электростатического взаимодействия всех ионов в растворе электролитов, определяемая как: • I=½Σ Cι *zι • где С, — моляльная концентрация ионов i-го типа, zi, : — заряд ионов i-го типа в единицах заряда электрона (в безразмерных единицах). При расчете ионной силы разбавленных растворов значения моляльной концентрации ионов обычно приближенно принимают равным значению их молярной концентрации. 2/1/2018 10
Ионная сила раствора • Ионная сила раствора (/) — мера электростатического взаимодействия всех ионов в растворе электролитов, определяемая как: • I=½Σ Cι *zι • где С, — моляльная концентрация ионов i-го типа, zi, : — заряд ионов i-го типа в единицах заряда электрона (в безразмерных единицах). При расчете ионной силы разбавленных растворов значения моляльной концентрации ионов обычно приближенно принимают равным значению их молярной концентрации. 2/1/2018 10
 Расчет коэффициента активности • Коэффициент активности иона в водном растворе при 25 °С также можно рассчитать самостоятельно по следующим формулам: • Для растворов с ионной силой меньше 0, 01 на основании предельного закона Дебая. Хюккеля: lgƒι=-0, 5*zι²*√I • Для растворов с ионной силой меньше 0, 1 по расширенному уравнению Дебая-Хюккеля: lgƒι=-0, 5*zι²*√I • 1 + √I • Если ионная сила раствора меньше 0, 0005, то коэффициенты активности ионов в этом растворе можно принять равными единице и, соответственно, вместо активностей ионов использовать их молярные концентрации. 2/1/2018 11
Расчет коэффициента активности • Коэффициент активности иона в водном растворе при 25 °С также можно рассчитать самостоятельно по следующим формулам: • Для растворов с ионной силой меньше 0, 01 на основании предельного закона Дебая. Хюккеля: lgƒι=-0, 5*zι²*√I • Для растворов с ионной силой меньше 0, 1 по расширенному уравнению Дебая-Хюккеля: lgƒι=-0, 5*zι²*√I • 1 + √I • Если ионная сила раствора меньше 0, 0005, то коэффициенты активности ионов в этом растворе можно принять равными единице и, соответственно, вместо активностей ионов использовать их молярные концентрации. 2/1/2018 11
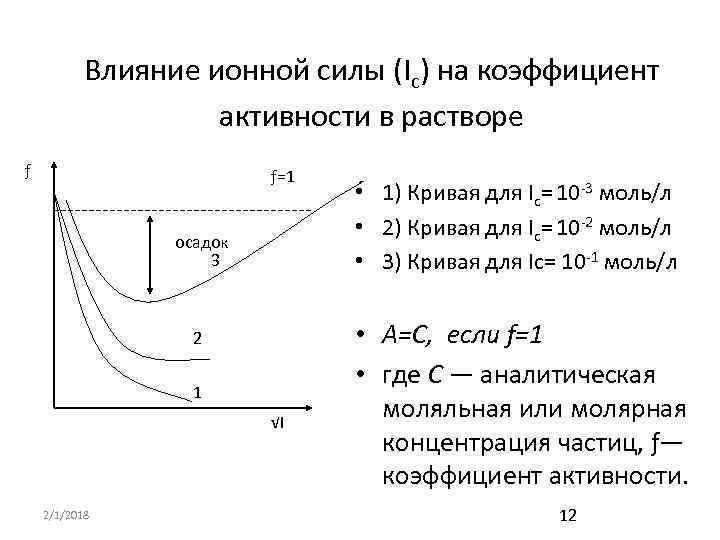 Влияние ионной силы (Iс) на коэффициент активности в растворе ƒ ƒ=1 осадок 3 2 1 √I 2/1/2018 • 1) Кривая для Iс= 10 -3 моль/л • 2) Кривая для Iс= 10 -2 моль/л • 3) Кривая для Iс= 10 -1 моль/л • A=C, если f=1 • где С — аналитическая моляльная или молярная концентрация частиц, ƒ— коэффициент активности. 12
Влияние ионной силы (Iс) на коэффициент активности в растворе ƒ ƒ=1 осадок 3 2 1 √I 2/1/2018 • 1) Кривая для Iс= 10 -3 моль/л • 2) Кривая для Iс= 10 -2 моль/л • 3) Кривая для Iс= 10 -1 моль/л • A=C, если f=1 • где С — аналитическая моляльная или молярная концентрация частиц, ƒ— коэффициент активности. 12
 Реальная и условная константа равновесия • Если константу равновесия выразить через активности реагирующих частиц, то такую константу называют термодинамической или реальной : • К =а(С)cа(D)d а (A)aа(B)b • А если константа равновесия записана через равновесные концентрации, то такая константа называется концентрационная или условная. • К =[С]c[D]d [A]a[B]b 2/1/2018 13
Реальная и условная константа равновесия • Если константу равновесия выразить через активности реагирующих частиц, то такую константу называют термодинамической или реальной : • К =а(С)cа(D)d а (A)aа(B)b • А если константа равновесия записана через равновесные концентрации, то такая константа называется концентрационная или условная. • К =[С]c[D]d [A]a[B]b 2/1/2018 13
 Типы химических реакций используемых в аналитике С точки зрения химика-аналитика целесообразно выделить следующие типы химических реакций: 1) С переносом протона – кислотноосновные; 2) С переносом электрона – окислительно -восстановительные; 3) С переносом электронных пар с образованием донорно-акцепторных связей – реакции комплексообразования. • 2/1/2018 14
Типы химических реакций используемых в аналитике С точки зрения химика-аналитика целесообразно выделить следующие типы химических реакций: 1) С переносом протона – кислотноосновные; 2) С переносом электрона – окислительно -восстановительные; 3) С переносом электронных пар с образованием донорно-акцепторных связей – реакции комплексообразования. • 2/1/2018 14
 Процессы в химическом анализе • Процессы с изменением агрегатного состояния (осаждение, дистиляция, растворение)- гетерогенное равновесие (или равновесие в системе осадокраствор). • Процессы распределения (экстракция, хроматография) – равновесия экстракционных систем. 2/1/2018 15
Процессы в химическом анализе • Процессы с изменением агрегатного состояния (осаждение, дистиляция, растворение)- гетерогенное равновесие (или равновесие в системе осадокраствор). • Процессы распределения (экстракция, хроматография) – равновесия экстракционных систем. 2/1/2018 15
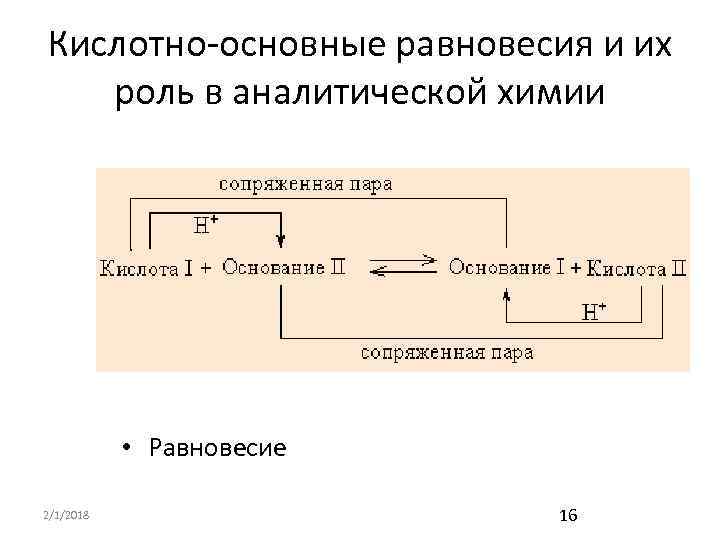 Кислотно-основные равновесия и их роль в аналитической химии • Равновесие 2/1/2018 16
Кислотно-основные равновесия и их роль в аналитической химии • Равновесие 2/1/2018 16
 Протолитические равновесия Согласно теории электролитической диссоциации С. А. Арениуса: • Кислота – это вещество, выделяющее при ионизации ион водорода. • Основание – это вещество, выделяющее при ионизации гидроксид-ион. 2/1/2018 17
Протолитические равновесия Согласно теории электролитической диссоциации С. А. Арениуса: • Кислота – это вещество, выделяющее при ионизации ион водорода. • Основание – это вещество, выделяющее при ионизации гидроксид-ион. 2/1/2018 17
 Согласно протолилической теории кислот и оснований Бренстенда-Лоури: • Кислота – это вещество, выделяющее при основании протон, а основание – вещество, присоединяющее протоны. НВ Н + + ВКислота Основание НВ и В- - сопряженные кислота и основание. 2/1/2018 18
Согласно протолилической теории кислот и оснований Бренстенда-Лоури: • Кислота – это вещество, выделяющее при основании протон, а основание – вещество, присоединяющее протоны. НВ Н + + ВКислота Основание НВ и В- - сопряженные кислота и основание. 2/1/2018 18
 Протолитическое равновесие • Равновесие, в котором участвует протон – ион водорода • Равновесие реакций, в которых участвуют молекулы воды, отдающее или принимающие протоны: Н 2 О = Н+ + ОНН 2 О + Н + = Н 3 О + Н 2 О = Н 3 О+ + ОН 2/1/2018 19
Протолитическое равновесие • Равновесие, в котором участвует протон – ион водорода • Равновесие реакций, в которых участвуют молекулы воды, отдающее или принимающие протоны: Н 2 О = Н+ + ОНН 2 О + Н + = Н 3 О + Н 2 О = Н 3 О+ + ОН 2/1/2018 19
 Амфотерные вещества • Амфолиты – вещества, способные присоединять и отдавать ионы(вода, дикарбонат-ион, гидросульфид-ион) НСО 3 - = Н+ + СО 32 НСО 3 - + Н+ = Н 2 СО 3 = Н 2 О +СО 2 2/1/2018 20
Амфотерные вещества • Амфолиты – вещества, способные присоединять и отдавать ионы(вода, дикарбонат-ион, гидросульфид-ион) НСО 3 - = Н+ + СО 32 НСО 3 - + Н+ = Н 2 СО 3 = Н 2 О +СО 2 2/1/2018 20
 Теория Льюиса: • Кислота – соединение, способное принимать электронную пару с оброзованием ковалентной связи, а основание – соединение, способное предоставить электронную пару для образования ковалентной связи NH 3 + H+ =NH 4+ 2/1/2018 21
Теория Льюиса: • Кислота – соединение, способное принимать электронную пару с оброзованием ковалентной связи, а основание – соединение, способное предоставить электронную пару для образования ковалентной связи NH 3 + H+ =NH 4+ 2/1/2018 21
 Протолитическое равновесие в воде Н 2 О = Н+ + ОН • Вода – слабый электролит, поэтому за константу химического равновесия можно принять: Кс = [Н 3 О+][ОН-] /[Н 2 О]2 Кс[Н 2 О]2 = const = Kw Kw = [Н+][ОН-]. Kw = 10 -14 2/1/2018 22
Протолитическое равновесие в воде Н 2 О = Н+ + ОН • Вода – слабый электролит, поэтому за константу химического равновесия можно принять: Кс = [Н 3 О+][ОН-] /[Н 2 О]2 Кс[Н 2 О]2 = const = Kw Kw = [Н+][ОН-]. Kw = 10 -14 2/1/2018 22
![Для воды: • • - [Н 3 О+]=[ОН-]= 10 -7 р. Н = - Для воды: • • - [Н 3 О+]=[ОН-]= 10 -7 р. Н = -](https://present5.com/presentation/3/61173249_154472087.pdf-img/61173249_154472087.pdf-23.jpg) Для воды: • • - [Н 3 О+]=[ОН-]= 10 -7 р. Н = - lg [Н 3 О+] = - lg 10 -7= 7, р. ОН = - lg [ОН-] = - lg 10 -7= 7, р. Kw = р. Н + р. ОН = 14. В кислых растворах р. Н<7 В Нейтральных р. Н=7 В щелочных р. Н>7. 2/1/2018 23
Для воды: • • - [Н 3 О+]=[ОН-]= 10 -7 р. Н = - lg [Н 3 О+] = - lg 10 -7= 7, р. ОН = - lg [ОН-] = - lg 10 -7= 7, р. Kw = р. Н + р. ОН = 14. В кислых растворах р. Н<7 В Нейтральных р. Н=7 В щелочных р. Н>7. 2/1/2018 23
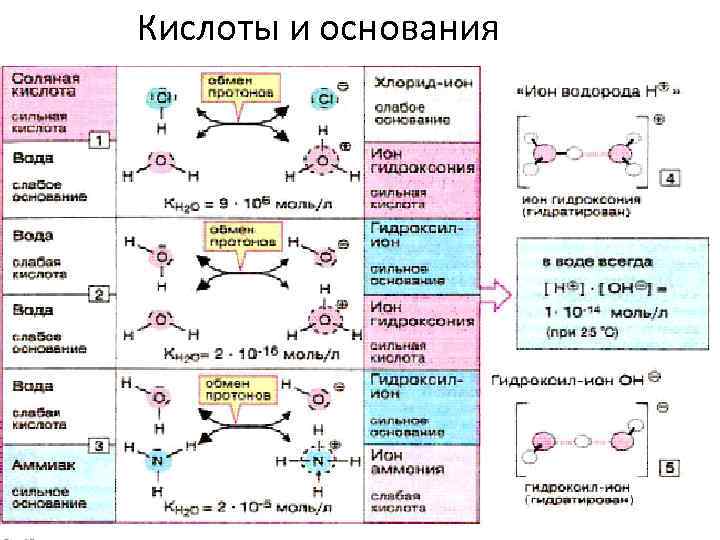 Кислоты и основания 2/1/2018 24
Кислоты и основания 2/1/2018 24
 Слабые кислоты и основания • Будучи слабыми электролитами, в водных растворах распадаются на ионы лишь в незначительной мере(степень диссоциации на ионы << 1). В их растворах устанавливаются равновесие между ионами и непродиссоциированными молекулами. 2/1/2018 25
Слабые кислоты и основания • Будучи слабыми электролитами, в водных растворах распадаются на ионы лишь в незначительной мере(степень диссоциации на ионы << 1). В их растворах устанавливаются равновесие между ионами и непродиссоциированными молекулами. 2/1/2018 25
 Константа кислотности и р. Н растворов слабых кислот • НВ+Н 2 О= Н 3 О+ + В • Ка = [Н 3 О+][В-]/[НВ], • р. Ка= -lg. Ка, чем больше Ка (меньше р. Ка), тем сильнее кислота, 2/1/2018 26
Константа кислотности и р. Н растворов слабых кислот • НВ+Н 2 О= Н 3 О+ + В • Ка = [Н 3 О+][В-]/[НВ], • р. Ка= -lg. Ка, чем больше Ка (меньше р. Ка), тем сильнее кислота, 2/1/2018 26
![Константа кислотности и р. Н растворов слабых кислот • Ка = [Н 3 О+][В-]/[НВ]= Константа кислотности и р. Н растворов слабых кислот • Ка = [Н 3 О+][В-]/[НВ]=](https://present5.com/presentation/3/61173249_154472087.pdf-img/61173249_154472087.pdf-27.jpg) Константа кислотности и р. Н растворов слабых кислот • Ка = [Н 3 О+][В-]/[НВ]= α 2 сα/1 -α, • Если вместо концентрации сα величину V – разведение, выражаемое в л/моль, V=1/сα, то формула будет иметь следующий вид: • Ка= α 2 /V(1 -α) или Ка= α 2 сα /1 -α 2/1/2018 27
Константа кислотности и р. Н растворов слабых кислот • Ка = [Н 3 О+][В-]/[НВ]= α 2 сα/1 -α, • Если вместо концентрации сα величину V – разведение, выражаемое в л/моль, V=1/сα, то формула будет иметь следующий вид: • Ка= α 2 /V(1 -α) или Ка= α 2 сα /1 -α 2/1/2018 27
 Константа основности и р. Н растворов слабых оснований • • • Ионизация однокислотного слабого основания В+Н 2 О= ОН- + НВ+ , Кв = [НВ+][ОН-]/[В], Кв=Кw/Ка, р. Кw=р. Ка+р. Кв. Ионное произведение воды равно произведению констант кислотности и основности сопряженной пары кислоты и основания. 2/1/2018 28
Константа основности и р. Н растворов слабых оснований • • • Ионизация однокислотного слабого основания В+Н 2 О= ОН- + НВ+ , Кв = [НВ+][ОН-]/[В], Кв=Кw/Ка, р. Кw=р. Ка+р. Кв. Ионное произведение воды равно произведению констант кислотности и основности сопряженной пары кислоты и основания. 2/1/2018 28
 Кв= α 2 св/1 -α • Где α – степень ионизации однокислотного слабого основания, а св – его исходная концентрация, поскольку для слабого основания α<< 1, то Кв= α 2 св 2/1/2018 29
Кв= α 2 св/1 -α • Где α – степень ионизации однокислотного слабого основания, а св – его исходная концентрация, поскольку для слабого основания α<< 1, то Кв= α 2 св 2/1/2018 29
 Гидролиз • Сольволиз – это процесс взаимодействия растворенного вещества с ионами, образующимися при ионизации молекул растворителя во время этого процесса. • Гидролиз – взаимодействие ионов растворенной соли с протонами или гидроксильными группами нейтральных молекул воды. 2/1/2018 30
Гидролиз • Сольволиз – это процесс взаимодействия растворенного вещества с ионами, образующимися при ионизации молекул растворителя во время этого процесса. • Гидролиз – взаимодействие ионов растворенной соли с протонами или гидроксильными группами нейтральных молекул воды. 2/1/2018 30
 Сольватация и сольволиз Сольватация – процесс образования сольватокомплексов при взаимодействии ионов растворенного вещества с молекулами растворителя без разрушения молекул растворителя Гидратация – процесс образования аквокомплексов при взаимодействии ионов растворенного вещества с молекулами воды Mn+ + m. H 2 O = [M(H 2 O)m]n+ Сольволиз – процесс взаимодействия растворенного вещества с ионами, образующимися при разрушении молекул растворителя (ионизации) Гидролиз – процесс взаимодействия растворенного вещества с протонами или гидроксильными группами непродиссоциировавших молекул воды 2/1/2018 31
Сольватация и сольволиз Сольватация – процесс образования сольватокомплексов при взаимодействии ионов растворенного вещества с молекулами растворителя без разрушения молекул растворителя Гидратация – процесс образования аквокомплексов при взаимодействии ионов растворенного вещества с молекулами воды Mn+ + m. H 2 O = [M(H 2 O)m]n+ Сольволиз – процесс взаимодействия растворенного вещества с ионами, образующимися при разрушении молекул растворителя (ионизации) Гидролиз – процесс взаимодействия растворенного вещества с протонами или гидроксильными группами непродиссоциировавших молекул воды 2/1/2018 31
 Гидролизу в водных растворах подвергаются соли, содержащие катионы слабых оснований и анионы слабых кислот CH 3 COONa Na+ + CH 3 COO- I. CH 3 COO- + H 2 O CH 3 COOH + OH- При гидролизе аниона соли выделяются гидроксильные группы и реакция среды становится слабо щелочной II. NH 4 Cl NH 4+ + Cl- NH 4+ + H 2 O NH 3 + H 3 O+ При гидролизе катиона соли выделяются катионы гидроксония и реакция среды становится слабо кислой III. NH 4 CN NH 4 + + CN- NH 4+ + H 2 O NH 3 + H 3 O+ CN- + H 2 O HCN + OH- Реакция среды в подобных случаях может быть различной 2/1/2018 32
Гидролизу в водных растворах подвергаются соли, содержащие катионы слабых оснований и анионы слабых кислот CH 3 COONa Na+ + CH 3 COO- I. CH 3 COO- + H 2 O CH 3 COOH + OH- При гидролизе аниона соли выделяются гидроксильные группы и реакция среды становится слабо щелочной II. NH 4 Cl NH 4+ + Cl- NH 4+ + H 2 O NH 3 + H 3 O+ При гидролизе катиона соли выделяются катионы гидроксония и реакция среды становится слабо кислой III. NH 4 CN NH 4 + + CN- NH 4+ + H 2 O NH 3 + H 3 O+ CN- + H 2 O HCN + OH- Реакция среды в подобных случаях может быть различной 2/1/2018 32
 Гидролитическое равновесие В растворах солей, в которых протекают гидролитические процессы устанавливается гидролитическое равновесие, которое характеризуется константой гидролитического равновесия Kh Степень гидролиза h – величина, равная отношению числа прогидролизовавшихся ионов nh к общему числу n исходных ионов: Степень гидролиза h – увеличивается с уменьшением концентрации раствора и с ростом температуры Обычно гидрализуется очень малая часть ионов и 2/1/2018 h << 1 33
Гидролитическое равновесие В растворах солей, в которых протекают гидролитические процессы устанавливается гидролитическое равновесие, которое характеризуется константой гидролитического равновесия Kh Степень гидролиза h – величина, равная отношению числа прогидролизовавшихся ионов nh к общему числу n исходных ионов: Степень гидролиза h – увеличивается с уменьшением концентрации раствора и с ростом температуры Обычно гидрализуется очень малая часть ионов и 2/1/2018 h << 1 33
 Гидролиз аниона слабой кислоты B- + H 2 O = HB + OHПреобразуем: Т. о. , константа гидролиза равна константе основности основания, сопряженного с кислотой, анион которой гидролизуется h << 1: h = (Kh/cb)1/2; [OH-] = hcb = (Kh/cb)1/2 cb = (Khcb)1/2 = (Kwcb/Ka)1/2 В соответствии с законом Оствальда при p. OH = – lg(Kwcb/Ka)1/2 = 0, 5(14 + pcb – p. Ka) = 7 + 0, 5(pcb – p. Ka) 2/1/2018 p. H = 14 – (7 + 0, 5(pcb – p. Ka)) = 7 + 0, 5(p. Ka – pcb) 34
Гидролиз аниона слабой кислоты B- + H 2 O = HB + OHПреобразуем: Т. о. , константа гидролиза равна константе основности основания, сопряженного с кислотой, анион которой гидролизуется h << 1: h = (Kh/cb)1/2; [OH-] = hcb = (Kh/cb)1/2 cb = (Khcb)1/2 = (Kwcb/Ka)1/2 В соответствии с законом Оствальда при p. OH = – lg(Kwcb/Ka)1/2 = 0, 5(14 + pcb – p. Ka) = 7 + 0, 5(pcb – p. Ka) 2/1/2018 p. H = 14 – (7 + 0, 5(pcb – p. Ka)) = 7 + 0, 5(p. Ka – pcb) 34
 Гидролиз катиона слабого основания BН+ + H 2 O = B + H 3 O+ Преобразуем: Т. о. , константа гидролиза равна константе кислотности кислоты, сопряженной с основанием, катион которого гидролизуется h << 1: h = (Kh/ca)1/2; [H 3 O+] = hca = (Kh/ca)1/2 ca = (Khca)1/2 = (Kwca/Kb)1/2 В соответствии с законом Оствальда при p. H = – lg(Kwca/Kb)1/2 = 0, 5(14 + pca – p. Kb) = 7 + 0, 5(pca – p. Kb) 2/1/2018 p. H = 7 – 0, 5(p. Kb – pca) 35
Гидролиз катиона слабого основания BН+ + H 2 O = B + H 3 O+ Преобразуем: Т. о. , константа гидролиза равна константе кислотности кислоты, сопряженной с основанием, катион которого гидролизуется h << 1: h = (Kh/ca)1/2; [H 3 O+] = hca = (Kh/ca)1/2 ca = (Khca)1/2 = (Kwca/Kb)1/2 В соответствии с законом Оствальда при p. H = – lg(Kwca/Kb)1/2 = 0, 5(14 + pca – p. Kb) = 7 + 0, 5(pca – p. Kb) 2/1/2018 p. H = 7 – 0, 5(p. Kb – pca) 35
 Буферные системы (растворы) • Это растворы, способные сохранять приблизительно постоянное значение р. Н при добавлении к ним небольших количеств сильных кислот или оснований. 2/1/2018 36
Буферные системы (растворы) • Это растворы, способные сохранять приблизительно постоянное значение р. Н при добавлении к ним небольших количеств сильных кислот или оснований. 2/1/2018 36
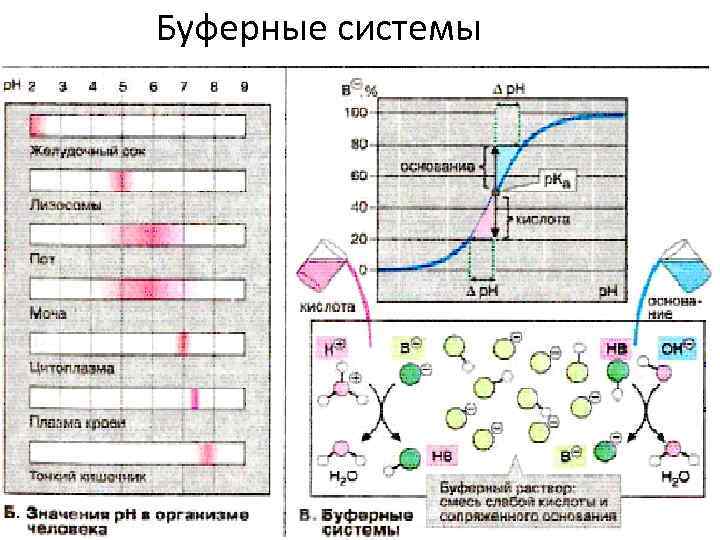 Буферные системы 2/1/2018 37
Буферные системы 2/1/2018 37
 Буферные системы (растворы) Буферные системы (или буферные растворы) – это растворы, способные сохранять приблизительно постоянное значение p. H при добавлении к ним небольших количеств сильных кислот или сильных оснований Содержащие индивидуальное вещество Гидротартрат калия KHC 4 H 4 O 6 p. H = 3, 567 Гидрофталат калия KHC 8 H 4 O 4 0, 05 М p. H = 4, 008 Тетраборат натрия (бура) Na 2 B 4 O 7 10 H 2 O 0, 05 М p. H = 9, 18 2/1/2018 Содержащие смесь веществ Хлороводородная к-та – глицин HCl + NH 2 COOH p. H = 1, 10 – 3, 50 Гидроксид натрия – гидрофталат калия Na. OH + KHC 8 H 4 O 4 p. H = 4, 00 – 6, 20 Ацетатный буфер Фосфатный буфер CH 3 COOH + CH 3 COONa Na 2 HPO 4 + KH 2 PO 4 p. H = 3, 80 – 6, 30 p. H = 4, 80 – 8, 00 Аммиачный буфер NH 4 OH + NH 4 Cl p. H ~ 10 38
Буферные системы (растворы) Буферные системы (или буферные растворы) – это растворы, способные сохранять приблизительно постоянное значение p. H при добавлении к ним небольших количеств сильных кислот или сильных оснований Содержащие индивидуальное вещество Гидротартрат калия KHC 4 H 4 O 6 p. H = 3, 567 Гидрофталат калия KHC 8 H 4 O 4 0, 05 М p. H = 4, 008 Тетраборат натрия (бура) Na 2 B 4 O 7 10 H 2 O 0, 05 М p. H = 9, 18 2/1/2018 Содержащие смесь веществ Хлороводородная к-та – глицин HCl + NH 2 COOH p. H = 1, 10 – 3, 50 Гидроксид натрия – гидрофталат калия Na. OH + KHC 8 H 4 O 4 p. H = 4, 00 – 6, 20 Ацетатный буфер Фосфатный буфер CH 3 COOH + CH 3 COONa Na 2 HPO 4 + KH 2 PO 4 p. H = 3, 80 – 6, 30 p. H = 4, 80 – 8, 00 Аммиачный буфер NH 4 OH + NH 4 Cl p. H ~ 10 38
 Буферная система, содержащая слабую кислоту и ее соль CH 3 COOH + CH 3 COONa CH 3 COO- + Na+ CH 3 COOH CH 3 COO- + H+ Действие буферной системы: CH 3 COO- + H 3 O+ CH 3 COOH + H 2 O CH 3 COOH + OH- CH 3 COO- + H 2 O p. H буферной системы: 2/1/2018 39
Буферная система, содержащая слабую кислоту и ее соль CH 3 COOH + CH 3 COONa CH 3 COO- + Na+ CH 3 COOH CH 3 COO- + H+ Действие буферной системы: CH 3 COO- + H 3 O+ CH 3 COOH + H 2 O CH 3 COOH + OH- CH 3 COO- + H 2 O p. H буферной системы: 2/1/2018 39
 Буферная система, содержащая слабое основание и его соль NH 4 OH + NH 4 Cl NH 4+ + Cl- NH 4 OH NH 4+ + OH- Действие буферной системы: OH- + H 3 O+ 2 H 2 O NH 4+ + OH- NH 3 H 2 O p. H буферной системы: 2/1/2018 40
Буферная система, содержащая слабое основание и его соль NH 4 OH + NH 4 Cl NH 4+ + Cl- NH 4 OH NH 4+ + OH- Действие буферной системы: OH- + H 3 O+ 2 H 2 O NH 4+ + OH- NH 3 H 2 O p. H буферной системы: 2/1/2018 40
 Буферная емкость определяется количеством сильной кислоты или сильного основания, которые при добавлении к одному литру буферного раствора изменяют значение р. Н этого раствора на единицу По ГФ XI «Буферной емкостью (β) называют выраженное в грамм-эквивалентах количество сильного основания (В), прибавление которого к 1 л буферного раствора вызывает возрастание величины р. Н этого раствора на единицу» β = d. B/dp. H ΔB/Δp. H Для буферной системы слабая кислота/соль слабой кислоты: р. Н 2/1/2018 дистиллированной воды для приготовления буферных растворов 5, 8 - 7, 0 41
Буферная емкость определяется количеством сильной кислоты или сильного основания, которые при добавлении к одному литру буферного раствора изменяют значение р. Н этого раствора на единицу По ГФ XI «Буферной емкостью (β) называют выраженное в грамм-эквивалентах количество сильного основания (В), прибавление которого к 1 л буферного раствора вызывает возрастание величины р. Н этого раствора на единицу» β = d. B/dp. H ΔB/Δp. H Для буферной системы слабая кислота/соль слабой кислоты: р. Н 2/1/2018 дистиллированной воды для приготовления буферных растворов 5, 8 - 7, 0 41
 Равновесия в растворах комплексных соединений 2/1/2018 42
Равновесия в растворах комплексных соединений 2/1/2018 42
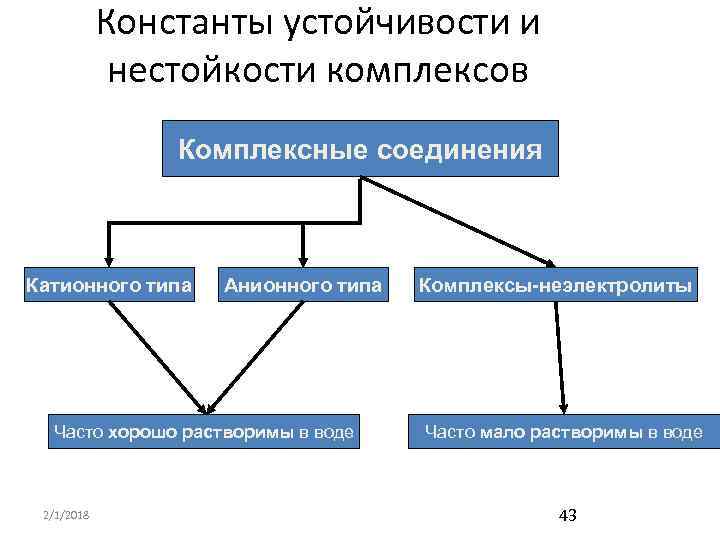 Константы устойчивости и нестойкости комплексов Комплексные соединения Катионного типа Анионного типа Часто хорошо растворимы в воде 2/1/2018 Комплексы-неэлектролиты Часто мало растворимы в воде 43
Константы устойчивости и нестойкости комплексов Комплексные соединения Катионного типа Анионного типа Часто хорошо растворимы в воде 2/1/2018 Комплексы-неэлектролиты Часто мало растворимы в воде 43
 Константы устойчивости и нестойкости комплексов Комплексные соединения Катионного типа Анионного типа Первичная электролитическая диссоциация отщепляются ионы внешней сферы: [Ag(NH 3)2]Cl 2/1/2018 [Ag(NH 3)2]+ + Cl- K 4[Fe(CN)6] 4 K+ + [Fe(CN)6]444
Константы устойчивости и нестойкости комплексов Комплексные соединения Катионного типа Анионного типа Первичная электролитическая диссоциация отщепляются ионы внешней сферы: [Ag(NH 3)2]Cl 2/1/2018 [Ag(NH 3)2]+ + Cl- K 4[Fe(CN)6] 4 K+ + [Fe(CN)6]444
![Константы устойчивости и нестойкости комплексов Вторичная электролитическая диссоциация [Ag(NH 3)2]+ + Н 2 О Константы устойчивости и нестойкости комплексов Вторичная электролитическая диссоциация [Ag(NH 3)2]+ + Н 2 О](https://present5.com/presentation/3/61173249_154472087.pdf-img/61173249_154472087.pdf-45.jpg) Константы устойчивости и нестойкости комплексов Вторичная электролитическая диссоциация [Ag(NH 3)2]+ + Н 2 О [Ag(NH 3)(H 2 O)]+ + NH 3 [Ag(H 2 O)2]+ + NH 3 отщепляются ионы внутренней сферы: Каждая ступень диссоциации внутренней сферы комплекса характеризуется своей константой химического равновесия 2/1/2018 45
Константы устойчивости и нестойкости комплексов Вторичная электролитическая диссоциация [Ag(NH 3)2]+ + Н 2 О [Ag(NH 3)(H 2 O)]+ + NH 3 [Ag(H 2 O)2]+ + NH 3 отщепляются ионы внутренней сферы: Каждая ступень диссоциации внутренней сферы комплекса характеризуется своей константой химического равновесия 2/1/2018 45
 Константы устойчивости и нестойкости комплексов Равновесие комплексообразования в общем виде: M + n. L = MLn характеризуется константой образования комплекса (константой устойчивости комплекса) I. M + L = ML III. ML 2 + L = ML 3 II. ML + L = ML 2 n MLn-1 + L = MLn 2/1/2018 46 Чем больше константа устойчивости, тем прочнее комплекс в растворе!
Константы устойчивости и нестойкости комплексов Равновесие комплексообразования в общем виде: M + n. L = MLn характеризуется константой образования комплекса (константой устойчивости комплекса) I. M + L = ML III. ML 2 + L = ML 3 II. ML + L = ML 2 n MLn-1 + L = MLn 2/1/2018 46 Чем больше константа устойчивости, тем прочнее комплекс в растворе!
 Константы устойчивости и нестойкости комплексов Реакция диссоциации комплекса в общем виде: MLn= M + n. L характеризуется константой диссоциации комплекса (константой нестойкости, константой неустойчивости) Полная константа нестойкости равна произведению ступенчатых констант нестойкости: Константа нестойкости (полная и ступенчатая) обратно пропорциональна константе устойчивости: Константы нестойкости и устойчивости обычно представляют в виде: Kн = 1/ p. Kн = -lg. Kн -p = lg Экспериментально установлено, что b комплексов различных металлов однотипного состава и строения с лигандами, образующими координационные связи через донорные атомы O или N, часто изменяются в последовательности: Ряд 2/1/2018 Ирвинга Уильямса Mn 2+
Константы устойчивости и нестойкости комплексов Реакция диссоциации комплекса в общем виде: MLn= M + n. L характеризуется константой диссоциации комплекса (константой нестойкости, константой неустойчивости) Полная константа нестойкости равна произведению ступенчатых констант нестойкости: Константа нестойкости (полная и ступенчатая) обратно пропорциональна константе устойчивости: Константы нестойкости и устойчивости обычно представляют в виде: Kн = 1/ p. Kн = -lg. Kн -p = lg Экспериментально установлено, что b комплексов различных металлов однотипного состава и строения с лигандами, образующими координационные связи через донорные атомы O или N, часто изменяются в последовательности: Ряд 2/1/2018 Ирвинга Уильямса Mn 2+
 Условные константы устойчивости комплексов Сумма равновесных концентраций всех форм лиганда, присутствующих в растворе, за исключением лигандов, связанных во внутренней сфере комплекса L = [L]/[c. L] Активная доля лиганда (коэффициент конкурирующих реакций). Характеризует мольную долю лигандов, не участвующих в побочных реакциях, за исключением лигандов, связанных во внутренней сфере комплекса Концентрационная и условная константы устойчивости комплекса связаны междйу собой следующим образом: 2/1/2018 48
Условные константы устойчивости комплексов Сумма равновесных концентраций всех форм лиганда, присутствующих в растворе, за исключением лигандов, связанных во внутренней сфере комплекса L = [L]/[c. L] Активная доля лиганда (коэффициент конкурирующих реакций). Характеризует мольную долю лигандов, не участвующих в побочных реакциях, за исключением лигандов, связанных во внутренней сфере комплекса Концентрационная и условная константы устойчивости комплекса связаны междйу собой следующим образом: 2/1/2018 48
 Условные константы устойчивости комплексов Пример: L + H+ = HL+ L – основание по Бренстеду-Лоури [HL+] = [H+][L]/K 1 HL+ + H+ = H 2 L 2+ [H 2 L 2+] = [H+][HL+]/K 2 = [H+]2[L]/K 1 K 2 [c. L] = [L]+[HL+]+[H 2 L 2+] = [L]+[H+][L]/K 1+ [H+]2[L]/K 1 K 2 = [L](1+[H+]/K 1+ [H+]2/K 1 K 2) L = [L]/[c. L] 2/1/2018 L= [L]/[L](1+[H+]/K 1+ [H+]2/K 1 K 2)= 1/(1+[H+]/K 1+ [H+]2/K 1 K 2) 49
Условные константы устойчивости комплексов Пример: L + H+ = HL+ L – основание по Бренстеду-Лоури [HL+] = [H+][L]/K 1 HL+ + H+ = H 2 L 2+ [H 2 L 2+] = [H+][HL+]/K 2 = [H+]2[L]/K 1 K 2 [c. L] = [L]+[HL+]+[H 2 L 2+] = [L]+[H+][L]/K 1+ [H+]2[L]/K 1 K 2 = [L](1+[H+]/K 1+ [H+]2/K 1 K 2) L = [L]/[c. L] 2/1/2018 L= [L]/[L](1+[H+]/K 1+ [H+]2/K 1 K 2)= 1/(1+[H+]/K 1+ [H+]2/K 1 K 2) 49
 Понятия, используемые при описании комплексообразования в растворах Аналитическая концентрация ионов металла, т. е. металла сумма равновесных концентраций всех форм ионов металла, присутствующих в растворе Аналитическая концентрация лиганда F(L) = [c. М]/[M] = 1/ M Функция закомплексованности i = [MLi]/[c. М] Функция распределения Функция образования 50 2/1/2018
Понятия, используемые при описании комплексообразования в растворах Аналитическая концентрация ионов металла, т. е. металла сумма равновесных концентраций всех форм ионов металла, присутствующих в растворе Аналитическая концентрация лиганда F(L) = [c. М]/[M] = 1/ M Функция закомплексованности i = [MLi]/[c. М] Функция распределения Функция образования 50 2/1/2018
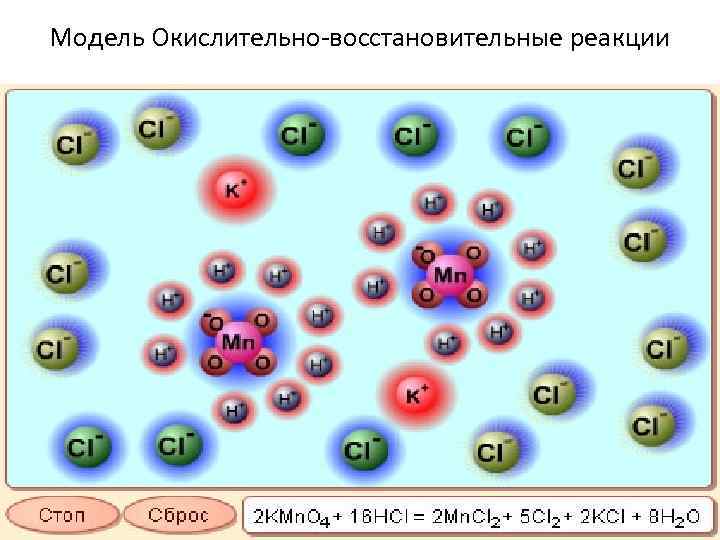 Модель Окислительно-восстановительные реакции 2/1/2018 51
Модель Окислительно-восстановительные реакции 2/1/2018 51
 Комплексонаты 2/1/2018 52
Комплексонаты 2/1/2018 52
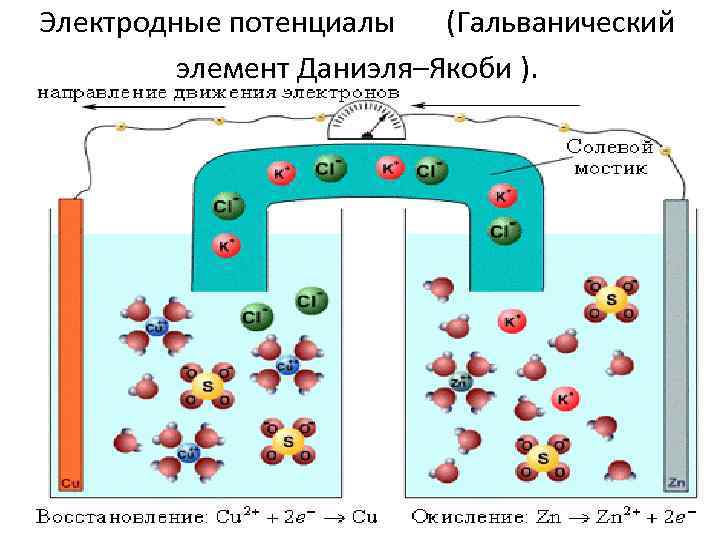 Электродные потенциалы (Гальванический элемент Даниэля–Якоби ). 2/1/2018 53
Электродные потенциалы (Гальванический элемент Даниэля–Якоби ). 2/1/2018 53
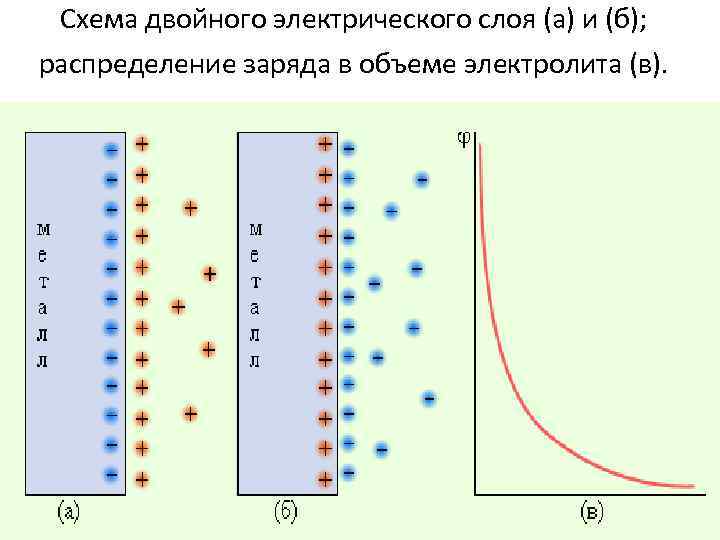 Схема двойного электрического слоя (а) и (б); распределение заряда в объеме электролита (в). 2/1/2018 54
Схема двойного электрического слоя (а) и (б); распределение заряда в объеме электролита (в). 2/1/2018 54
 уравнение Нернста для электродного процесса 2/1/2018 55
уравнение Нернста для электродного процесса 2/1/2018 55


