1 lekcie chemie.ppt
- Количество слайдов: 97
 Základy anorganické chemie RNDr. Kristýna Vondráčková kristyna. vondrackova@email. cz
Základy anorganické chemie RNDr. Kristýna Vondráčková kristyna. vondrackova@email. cz
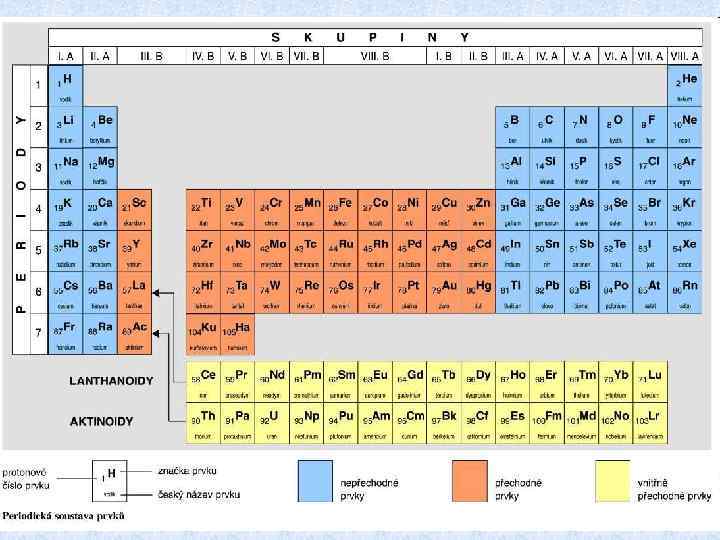
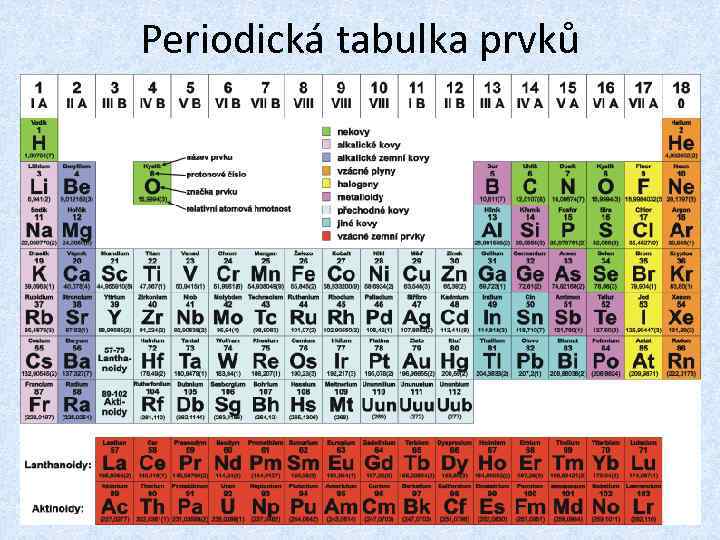 Periodická tabulka prvků
Periodická tabulka prvků
 PSP- periodická soustava prvků • Dnes 115 prvků • Řazeny podle protonového čísla řádky = periody (7) sloupce = skupiny Názvy skupin: lanthanoidy, aktinoidy, alkalické kovy, kovy alk. zemin, halogenidy, vzácné plyny
PSP- periodická soustava prvků • Dnes 115 prvků • Řazeny podle protonového čísla řádky = periody (7) sloupce = skupiny Názvy skupin: lanthanoidy, aktinoidy, alkalické kovy, kovy alk. zemin, halogenidy, vzácné plyny
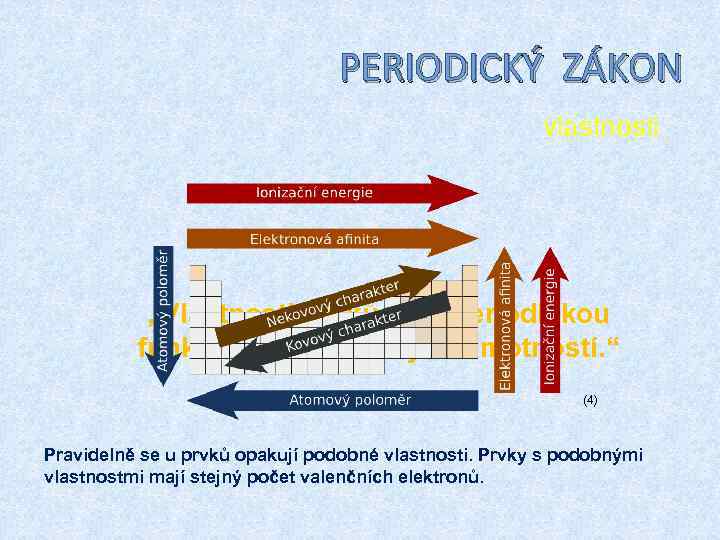 PERIODICKÝ ZÁKON vlastnosti „Vlastnosti prvků jsou periodickou funkcí jejich atomových hmotností. “ (4) Pravidelně se u prvků opakují podobné vlastnosti. Prvky s podobnými vlastnostmi mají stejný počet valenčních elektronů.
PERIODICKÝ ZÁKON vlastnosti „Vlastnosti prvků jsou periodickou funkcí jejich atomových hmotností. “ (4) Pravidelně se u prvků opakují podobné vlastnosti. Prvky s podobnými vlastnostmi mají stejný počet valenčních elektronů.
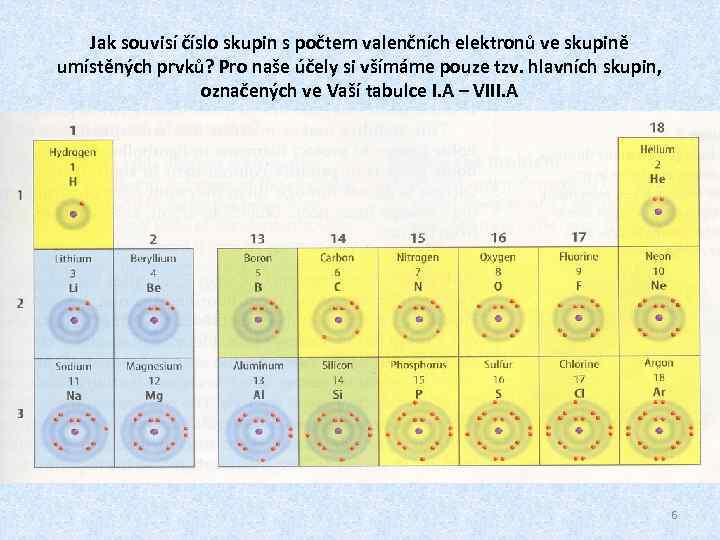 Jak souvisí číslo skupin s počtem valenčních elektronů ve skupině umístěných prvků? Pro naše účely si všímáme pouze tzv. hlavních skupin, označených ve Vaší tabulce I. A – VIII. A 6
Jak souvisí číslo skupin s počtem valenčních elektronů ve skupině umístěných prvků? Pro naše účely si všímáme pouze tzv. hlavních skupin, označených ve Vaší tabulce I. A – VIII. A 6
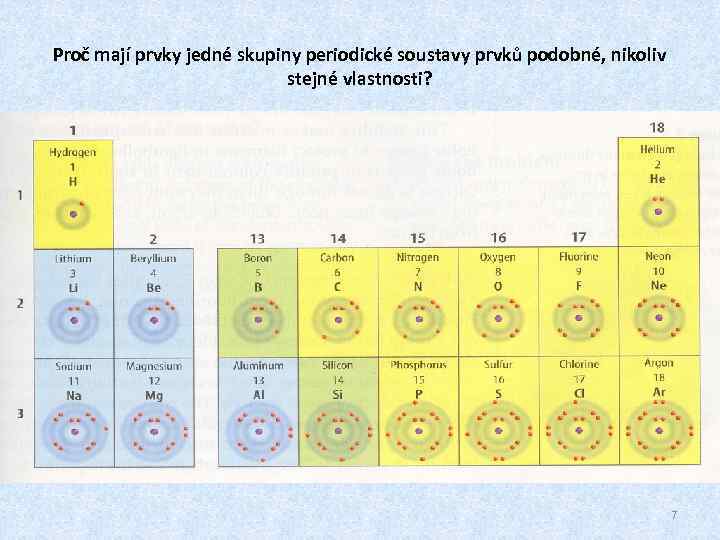 Proč mají prvky jedné skupiny periodické soustavy prvků podobné, nikoliv stejné vlastnosti? 7
Proč mají prvky jedné skupiny periodické soustavy prvků podobné, nikoliv stejné vlastnosti? 7
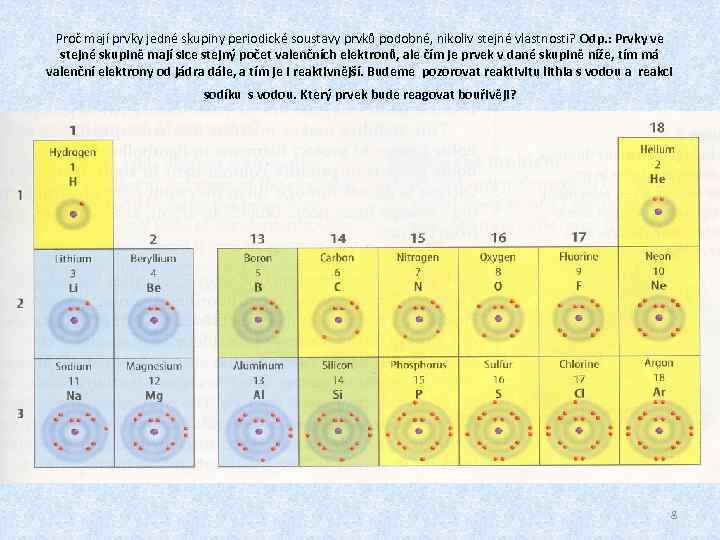 Proč mají prvky jedné skupiny periodické soustavy prvků podobné, nikoliv stejné vlastnosti? Odp. : Prvky ve stejné skupině mají sice stejný počet valenčních elektronů, ale čím je prvek v dané skupině níže, tím má valenční elektrony od jádra dále, a tím je i reaktivnější. Budeme pozorovat reaktivitu lithia s vodou a reakci sodíku s vodou. Který prvek bude reagovat bouřivěji? 8
Proč mají prvky jedné skupiny periodické soustavy prvků podobné, nikoliv stejné vlastnosti? Odp. : Prvky ve stejné skupině mají sice stejný počet valenčních elektronů, ale čím je prvek v dané skupině níže, tím má valenční elektrony od jádra dále, a tím je i reaktivnější. Budeme pozorovat reaktivitu lithia s vodou a reakci sodíku s vodou. Který prvek bude reagovat bouřivěji? 8
 Ø PRVKY: Název prvku tvoří 1 až 2 písmenová zkratka, 2. písmeno je malé. Názvy jsou v PSP (periodické soustavě prvků). Př. : kobalt je Co, ne CO Pozn. : PSP je nejdůležitější chemická tabulka.
Ø PRVKY: Název prvku tvoří 1 až 2 písmenová zkratka, 2. písmeno je malé. Názvy jsou v PSP (periodické soustavě prvků). Př. : kobalt je Co, ne CO Pozn. : PSP je nejdůležitější chemická tabulka.
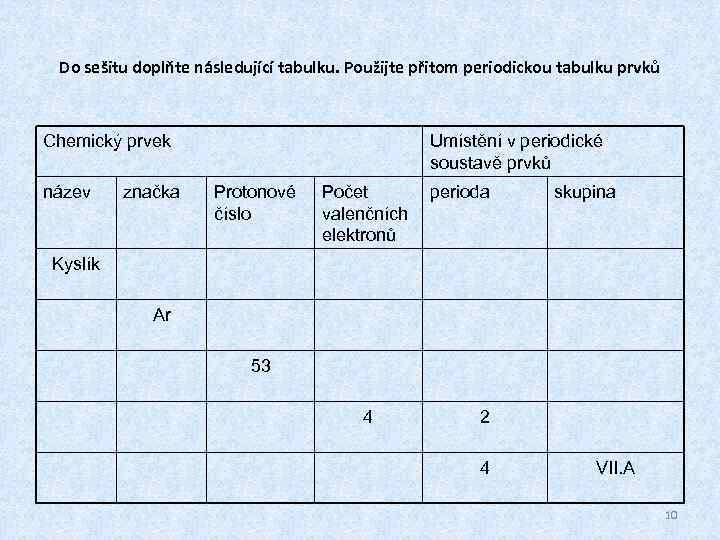 Do sešitu doplňte následující tabulku. Použijte přitom periodickou tabulku prvků Chemický prvek název značka Umístění v periodické soustavě prvků Protonové číslo Počet perioda valenčních elektronů skupina Kyslík Ar 53 4 2 4 VII. A 10
Do sešitu doplňte následující tabulku. Použijte přitom periodickou tabulku prvků Chemický prvek název značka Umístění v periodické soustavě prvků Protonové číslo Počet perioda valenčních elektronů skupina Kyslík Ar 53 4 2 4 VII. A 10
 Ø SLOUČENINY - OBECNĚ: A) OXIDAČNÍ ČÍSLO: souvisí s nábojem atomu prvku ve sloučenině. Značí se římskou číslicí. Na+I Cl-I Vysvětlení (zjednodušené): Atom je složen z jádra (+) a obalu (elektrony -). Nejdůležitější z nich jsou valenční elektrony, jsou nejdál od jádra. Chemická vazba (jde o elektrostatické síly): Ø atomy se přibliží, dráhy valenčních el. se překryjí, Ø valenční elektrony utvoří elektronový pár; el. pár přitahují jádra obou atomů, tj. el. pár tvoří chemickou vazbu. Když je jádro 1 atomu silnější, posune se vazebný el. pár k němu a vzniká na tomto atomu - náboj, na 2. atomu pak + náboj. Tento náboj určuje oxidační číslo atomu.
Ø SLOUČENINY - OBECNĚ: A) OXIDAČNÍ ČÍSLO: souvisí s nábojem atomu prvku ve sloučenině. Značí se římskou číslicí. Na+I Cl-I Vysvětlení (zjednodušené): Atom je složen z jádra (+) a obalu (elektrony -). Nejdůležitější z nich jsou valenční elektrony, jsou nejdál od jádra. Chemická vazba (jde o elektrostatické síly): Ø atomy se přibliží, dráhy valenčních el. se překryjí, Ø valenční elektrony utvoří elektronový pár; el. pár přitahují jádra obou atomů, tj. el. pár tvoří chemickou vazbu. Když je jádro 1 atomu silnější, posune se vazebný el. pár k němu a vzniká na tomto atomu - náboj, na 2. atomu pak + náboj. Tento náboj určuje oxidační číslo atomu.
 Rozdělení anorganických sloučenin Dvouprvkové - halogenidy, hydridy, oxidy, sulfidy , selenidy, telluridy, bezkyslíkaté kyseliny - jsou složeny ze dvou prvků Tříprvkové - hydroxidy, kyanidy, kyslíkaté kyseliny, soli - jsou složeny ze tří prvků
Rozdělení anorganických sloučenin Dvouprvkové - halogenidy, hydridy, oxidy, sulfidy , selenidy, telluridy, bezkyslíkaté kyseliny - jsou složeny ze dvou prvků Tříprvkové - hydroxidy, kyanidy, kyslíkaté kyseliny, soli - jsou složeny ze tří prvků
 Zásady chemického názvosloví sloučenin • chemický vzorec • je zápis za použití značek prvků, který uvádí počet a druh atomů přítomných v molekule látky • název anorganické sloučeniny : • podstatné jméno - typ sloučeniny, např. oxid, chlorid, kyselina charakterizuje negativní část sloučeniny = anion • přídavné jméno - udává, od kterého prvku je sloučenina odvozena, např. draselný, železitý, amonný charakterizuje elektropozitivní složku sloučeniny = kation
Zásady chemického názvosloví sloučenin • chemický vzorec • je zápis za použití značek prvků, který uvádí počet a druh atomů přítomných v molekule látky • název anorganické sloučeniny : • podstatné jméno - typ sloučeniny, např. oxid, chlorid, kyselina charakterizuje negativní část sloučeniny = anion • přídavné jméno - udává, od kterého prvku je sloučenina odvozena, např. draselný, železitý, amonný charakterizuje elektropozitivní složku sloučeniny = kation
 Chemický vzorec užití pro jednoduchou a názornou charakterizaci sloučenin. Některé z druhů chemických vzorců (společné i pro organické sloučeniny): 1) Stechiometrické (empirické) vzorce - udává druh atomů v molekule - udává vzájemný poměr atomů v molekule - omezené využití Příklad: ethanol C 2 H 6 O dusitan amonný NH 2 O glukosa CH 2 O peroxid vodíku HO 2) Souhrnné (sumární) vzorce - udává druh atomů v molekule - udává počet atomů v molekule Příklad: ethanol C 2 H 6 O dusitan amonný NH 4 NO 2 glukosa C 6 H 12 O 6 peroxid vodíku H 2 O 2 14
Chemický vzorec užití pro jednoduchou a názornou charakterizaci sloučenin. Některé z druhů chemických vzorců (společné i pro organické sloučeniny): 1) Stechiometrické (empirické) vzorce - udává druh atomů v molekule - udává vzájemný poměr atomů v molekule - omezené využití Příklad: ethanol C 2 H 6 O dusitan amonný NH 2 O glukosa CH 2 O peroxid vodíku HO 2) Souhrnné (sumární) vzorce - udává druh atomů v molekule - udává počet atomů v molekule Příklad: ethanol C 2 H 6 O dusitan amonný NH 4 NO 2 glukosa C 6 H 12 O 6 peroxid vodíku H 2 O 2 14
 3) Funkční vzorec - již částečně vychází ze struktury sloučeniny - zachycení charakteristických uskupení (tzv. funkčních skupin) - používá se v anorganické chemii nejčastěji. Příklad: ethanol C 2 H 5 OH dusitan amonný NH 4 NO 2 peroxid vodíku H 2 O 2 4) Konstituční vzorce - udává které prvky a jakými vazbami jsou propojeny - též vychází ze struktury sloučeniny 4 a) rozvinutá forma 4 b) racionální forma Příklad: ethanol CH 3 CH 2 OH 5)Elektronové konstituční vzorce - udává které prvky a jakými vazbami jsou propojeny - též vychází ze struktury sloučeniny - navíc jsou znázorněny nevazebné elektronové páry 6) Geometrické vzorce (prostorové) - udává jak jsou atomy orientovány v prostoru Příklad: ethanol 15
3) Funkční vzorec - již částečně vychází ze struktury sloučeniny - zachycení charakteristických uskupení (tzv. funkčních skupin) - používá se v anorganické chemii nejčastěji. Příklad: ethanol C 2 H 5 OH dusitan amonný NH 4 NO 2 peroxid vodíku H 2 O 2 4) Konstituční vzorce - udává které prvky a jakými vazbami jsou propojeny - též vychází ze struktury sloučeniny 4 a) rozvinutá forma 4 b) racionální forma Příklad: ethanol CH 3 CH 2 OH 5)Elektronové konstituční vzorce - udává které prvky a jakými vazbami jsou propojeny - též vychází ze struktury sloučeniny - navíc jsou znázorněny nevazebné elektronové páry 6) Geometrické vzorce (prostorové) - udává jak jsou atomy orientovány v prostoru Příklad: ethanol 15
 Chemický název 2 typy: 1) triviální – bez souvislosti se složením látky. Většinou souvislost s nějakou vlastností. Příklady: HCl kyselina solná, Na. Cl sůl kamenná, H 2 O voda, NH 3 čpavek, Mn. O 2 burel. . . 2) Racionální – vychází ze SLOŽENÍ látky. je založeno na OXIDAČNÍM ČÍSLE Racionální název se většinou skládá z podstatného jména a přídavného jména: Podstatné jméno: určuje typ sloučenin. (oxid, peroxid, kyselina, hydroxid, sulfid, nitrid. . . ) Přídavné jméno: udává, od kterého prvku je sloučenina odvozena. 16
Chemický název 2 typy: 1) triviální – bez souvislosti se složením látky. Většinou souvislost s nějakou vlastností. Příklady: HCl kyselina solná, Na. Cl sůl kamenná, H 2 O voda, NH 3 čpavek, Mn. O 2 burel. . . 2) Racionální – vychází ze SLOŽENÍ látky. je založeno na OXIDAČNÍM ČÍSLE Racionální název se většinou skládá z podstatného jména a přídavného jména: Podstatné jméno: určuje typ sloučenin. (oxid, peroxid, kyselina, hydroxid, sulfid, nitrid. . . ) Přídavné jméno: udává, od kterého prvku je sloučenina odvozena. 16
 Oxidační číslo • zapisujeme vpravo nahoře • součet oxidačních čísel ve vzorci = 0 Oxidační číslo: • nulové (u prvků v nesloučeném stavu) • záporné (-I až –IV) • kladné (I – VIII) vyjadřujeme příslušnou koncovkou
Oxidační číslo • zapisujeme vpravo nahoře • součet oxidačních čísel ve vzorci = 0 Oxidační číslo: • nulové (u prvků v nesloučeném stavu) • záporné (-I až –IV) • kladné (I – VIII) vyjadřujeme příslušnou koncovkou
 Oxidační číslo je elektrický náboj, který by byl přítomen na atomu určitého prvku, kdyby elektrony každé vazby byly přiděleny elektronegativnějšímu atomu. Značí se římskými číslicemi vpravo nahoře u symbolu prvku, H 2 I SVI O 4 -II Pravidla odvozování: 1) Atomy prvků ve volném stavu (vzácné plyny) nebo ve své molekule (N 2, O 2. . . ) mají oxidační číslo rovno nule. 2) Oxidační číslo prvku v jednoatomovém iontu je rovno náboji iontu. 3) V elektroneutrální molekule (např. H 2 SO 4) je součet oxidačních čísel roven nule, u iontu (např. (SO 4)2– odpovídá jeho náboji. 4) Některé prvky mají ve většině sloučenin stejné oxidační číslo: HI Na. I KI Ca. II Mg. II Ca. II O-II CIV (v organických látkách) 5) Maximální kladné číslo, kterého může NEPŘECHODNÝ PRVEK dosáhnout, je rovno číslu skupiny, ve které prvek leží. 18
Oxidační číslo je elektrický náboj, který by byl přítomen na atomu určitého prvku, kdyby elektrony každé vazby byly přiděleny elektronegativnějšímu atomu. Značí se římskými číslicemi vpravo nahoře u symbolu prvku, H 2 I SVI O 4 -II Pravidla odvozování: 1) Atomy prvků ve volném stavu (vzácné plyny) nebo ve své molekule (N 2, O 2. . . ) mají oxidační číslo rovno nule. 2) Oxidační číslo prvku v jednoatomovém iontu je rovno náboji iontu. 3) V elektroneutrální molekule (např. H 2 SO 4) je součet oxidačních čísel roven nule, u iontu (např. (SO 4)2– odpovídá jeho náboji. 4) Některé prvky mají ve většině sloučenin stejné oxidační číslo: HI Na. I KI Ca. II Mg. II Ca. II O-II CIV (v organických látkách) 5) Maximální kladné číslo, kterého může NEPŘECHODNÝ PRVEK dosáhnout, je rovno číslu skupiny, ve které prvek leží. 18
 PRAVIDLA pro VÝPOČET OXID. ČÍSLA (nejdůležitější): 1) součet oxid. čísel atomů v molekule = 0 2) obvyklá oxid. čísla: Tab. 1: prvek obvyklá ox. č. výjimka F -I H +I -I v hydridech O -II -I v peroxidech 1. sk. PSP(Na, K. . ) +I 2. sk. PSP(Mg, Ca. . ) +II Ag +I Zn, Cd +II Al , B +III
PRAVIDLA pro VÝPOČET OXID. ČÍSLA (nejdůležitější): 1) součet oxid. čísel atomů v molekule = 0 2) obvyklá oxid. čísla: Tab. 1: prvek obvyklá ox. č. výjimka F -I H +I -I v hydridech O -II -I v peroxidech 1. sk. PSP(Na, K. . ) +I 2. sk. PSP(Mg, Ca. . ) +II Ag +I Zn, Cd +II Al , B +III
 B) TVORBA VZORCE a NÁZVU Známe: Na. Cl - chlorid sodný Z Tab. 1 plynou oxid. čísla: Na+I Cl-I VZOREC: • prvek se záporným ox. č. je obvykle zcela vpravo • prvek s kladným ox. č. je obvykle zcela vlevo NÁZEV tvoří: • podstatné jméno s koncovkou (chlorid) – odvozeno od prvku se záporným oxid. číslem • přídavné jméno s koncovkou (sodný) – odvozeno od prvku s kladným oxid. číslem;
B) TVORBA VZORCE a NÁZVU Známe: Na. Cl - chlorid sodný Z Tab. 1 plynou oxid. čísla: Na+I Cl-I VZOREC: • prvek se záporným ox. č. je obvykle zcela vpravo • prvek s kladným ox. č. je obvykle zcela vlevo NÁZEV tvoří: • podstatné jméno s koncovkou (chlorid) – odvozeno od prvku se záporným oxid. číslem • přídavné jméno s koncovkou (sodný) – odvozeno od prvku s kladným oxid. číslem;
 Př. : Určete oxidační čísla prvků v HCl. O 4 H: je ve vzorci zcela vlevo, proto má + oxidační číslo, z Tab. 1 (obvyklá ox. č. ) plyne, že má ox. č. +I O: je ve vzorci zcela vpravo, proto má – oxid. číslo, z Tab. 1 (obvyklá ox. č. ) plyne, že má ox. č. -II Cl: ox. číslo (neznámá x) určíme dle Pravidla 1) (součet oxid. čísel všech atomů v molekule = 0), tzn: H Cl O 1*(+1) + 1*(x) + 4*(-2) = 0 x = +7 Výsledek: H+I Cl+VII O 4 -II.
Př. : Určete oxidační čísla prvků v HCl. O 4 H: je ve vzorci zcela vlevo, proto má + oxidační číslo, z Tab. 1 (obvyklá ox. č. ) plyne, že má ox. č. +I O: je ve vzorci zcela vpravo, proto má – oxid. číslo, z Tab. 1 (obvyklá ox. č. ) plyne, že má ox. č. -II Cl: ox. číslo (neznámá x) určíme dle Pravidla 1) (součet oxid. čísel všech atomů v molekule = 0), tzn: H Cl O 1*(+1) + 1*(x) + 4*(-2) = 0 x = +7 Výsledek: H+I Cl+VII O 4 -II.
 Oxidační čísla a jejich koncovky I II IV V VI VIII -ný -natý -ičitý -ečný, -ičný -ový -istý -ičelý
Oxidační čísla a jejich koncovky I II IV V VI VIII -ný -natý -ičitý -ečný, -ičný -ový -istý -ičelý
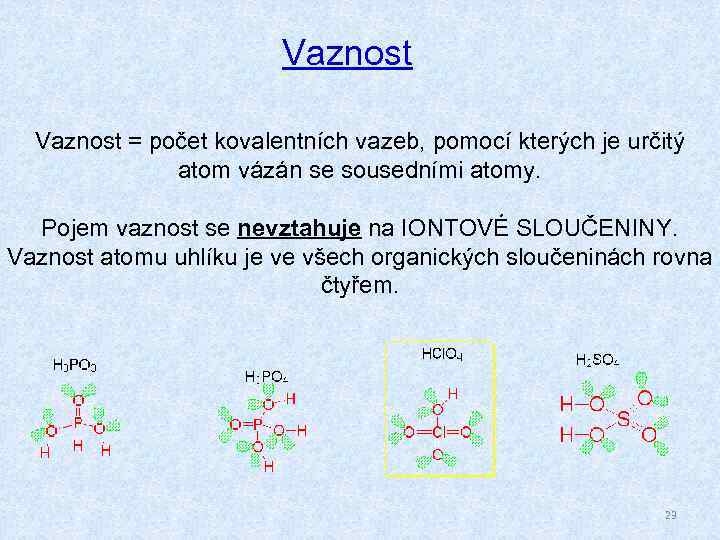 Vaznost = počet kovalentních vazeb, pomocí kterých je určitý atom vázán se sousedními atomy. Pojem vaznost se nevztahuje na IONTOVÉ SLOUČENINY. Vaznost atomu uhlíku je ve všech organických sloučeninách rovna čtyřem. 23
Vaznost = počet kovalentních vazeb, pomocí kterých je určitý atom vázán se sousedními atomy. Pojem vaznost se nevztahuje na IONTOVÉ SLOUČENINY. Vaznost atomu uhlíku je ve všech organických sloučeninách rovna čtyřem. 23
 Binární sloučeniny • halogenidy • hydridy • oxidy • sulfidy (selenidy, telluridy) • halogenvodíkové kyseliny • … • ve vzorcích binárních sloučenin má jeden prvek kladné a druhý záporné oxidační číslo Binární sloučeniny jsou nejjednodušší anorganické sloučeniny, které se skládají právě ze dvou prvků.
Binární sloučeniny • halogenidy • hydridy • oxidy • sulfidy (selenidy, telluridy) • halogenvodíkové kyseliny • … • ve vzorcích binárních sloučenin má jeden prvek kladné a druhý záporné oxidační číslo Binární sloučeniny jsou nejjednodušší anorganické sloučeniny, které se skládají právě ze dvou prvků.
 Názvy binárních sloučenin: 1. triviální Burel, kyselina solná HCl 2. Podstatné jméno + přídavné jméno (racionální) Podstatné jméno: od prvku se záporným oxidačním číslem; koncovka –ID Přídavné jméno: odvozeno od prvku s kladným ox. číslem; Podle hodnoty oxidačního čísla má jednu z osmi koncovek: -ný, -natý, -ičitý, - ičný (-ečný), -ový, -istý, -ičelý 3. Koncovka –AN sloučeniny vodíku s prvky III. A – VI. A skupiny: alan Al. H 3 fosfan PH 3 silan Si. H 4 sulfan H 2 S 4. Jednoslovo složenina z názvů obou prvků: 25 HCl chlorovodík, HBr bromovodík
Názvy binárních sloučenin: 1. triviální Burel, kyselina solná HCl 2. Podstatné jméno + přídavné jméno (racionální) Podstatné jméno: od prvku se záporným oxidačním číslem; koncovka –ID Přídavné jméno: odvozeno od prvku s kladným ox. číslem; Podle hodnoty oxidačního čísla má jednu z osmi koncovek: -ný, -natý, -ičitý, - ičný (-ečný), -ový, -istý, -ičelý 3. Koncovka –AN sloučeniny vodíku s prvky III. A – VI. A skupiny: alan Al. H 3 fosfan PH 3 silan Si. H 4 sulfan H 2 S 4. Jednoslovo složenina z názvů obou prvků: 25 HCl chlorovodík, HBr bromovodík
 Druhy binárních sloučenin: 1. oxidy 2. sulfidy 3. nitridy 4. hydridy 5. halogenidy 6. bezkyslíkaté kyseliny 7. peroxidy 8. hyperoxidy 9. …(selenidy, telluridy) Víceprvkové sloučeniny: 1. hydroxidy 2. kyanidy 3. kyseliny 4. soli 26
Druhy binárních sloučenin: 1. oxidy 2. sulfidy 3. nitridy 4. hydridy 5. halogenidy 6. bezkyslíkaté kyseliny 7. peroxidy 8. hyperoxidy 9. …(selenidy, telluridy) Víceprvkové sloučeniny: 1. hydroxidy 2. kyanidy 3. kyseliny 4. soli 26
 Oxidy: O-II - Dvouprvkové sloučeniny kyslíku s libovolným prvkem. - Sloučeniny odvozené od vody (H 2 O) náhradou obou atomů vodíku jiným prvkem. Název: -Podstatné jméno: OXID 27
Oxidy: O-II - Dvouprvkové sloučeniny kyslíku s libovolným prvkem. - Sloučeniny odvozené od vody (H 2 O) náhradou obou atomů vodíku jiným prvkem. Název: -Podstatné jméno: OXID 27
 Oxidy • jsou dvouprvkové sloučeniny kyslíku s jiným prvkem • kyslík v oxidech má oxidační číslo vždy –II • koncovka – id • oxid Cvičení 1: Ze sloučenin vyber oxidy: • Na. OH, KBr, Li 2 O, H 2 SO 3, Mg. O, Zn. S, Cr 2 O 3, KOH, CO 2, Ca. O
Oxidy • jsou dvouprvkové sloučeniny kyslíku s jiným prvkem • kyslík v oxidech má oxidační číslo vždy –II • koncovka – id • oxid Cvičení 1: Ze sloučenin vyber oxidy: • Na. OH, KBr, Li 2 O, H 2 SO 3, Mg. O, Zn. S, Cr 2 O 3, KOH, CO 2, Ca. O
 Odvození vzorce oxid vápenatý • napíšeme značky prvků v obráceném pořadí než v názvu CO • ke značkám napíšeme vpravo nahoru oxidační čísla Ca. IIO-II • sepíšeme oxidační čísla do kříže arabskými číslicemi Ca 2 O 2 • jsou – li ve vzorci soudělná čísla, krátíme: Ca 2 O 2 = Ca. O
Odvození vzorce oxid vápenatý • napíšeme značky prvků v obráceném pořadí než v názvu CO • ke značkám napíšeme vpravo nahoru oxidační čísla Ca. IIO-II • sepíšeme oxidační čísla do kříže arabskými číslicemi Ca 2 O 2 • jsou – li ve vzorci soudělná čísla, krátíme: Ca 2 O 2 = Ca. O
 Odvození názvu CO 2 • název je tvořen podstatným jménem oxid a přídavným jménem odvozeným od prvku s příslušnou koncovkou • napíšeme ke kyslíku oxidační číslo CO 2 -II • součet oxidačních čísel ve sloučenině = 0, je CIV x + 2 · (-2) = 0 x = 4 • název je oxid uhličitý
Odvození názvu CO 2 • název je tvořen podstatným jménem oxid a přídavným jménem odvozeným od prvku s příslušnou koncovkou • napíšeme ke kyslíku oxidační číslo CO 2 -II • součet oxidačních čísel ve sloučenině = 0, je CIV x + 2 · (-2) = 0 x = 4 • název je oxid uhličitý
 BINÁRNÍ SLOUČENINY 1 - Oxidy binární sloučeniny prvků s kyslíkem vznikají např. hořením Př. : S + O 2 = SO 2 -II XO
BINÁRNÍ SLOUČENINY 1 - Oxidy binární sloučeniny prvků s kyslíkem vznikají např. hořením Př. : S + O 2 = SO 2 -II XO
 1 - Oxidy -II XO Př: napište vzorec: oxid sodný +I -II Na 2 O 1 Slyším-li oxid, automaticky píšu O-II Oxid je SODNÝ, proto kationtem je sodík se značkou Na Podle koncovky = NÝ (SODNÝ) přiřadím sodíku ox. číslo +I Ox. čísla sepíšu do kříže případně zkrátím (křížové pravidlo) Křížové pravidlo zajišťuje, aby součet oxidačních čísel v molekule = 0 2 * (+1) + 1 * (-2) = 0
1 - Oxidy -II XO Př: napište vzorec: oxid sodný +I -II Na 2 O 1 Slyším-li oxid, automaticky píšu O-II Oxid je SODNÝ, proto kationtem je sodík se značkou Na Podle koncovky = NÝ (SODNÝ) přiřadím sodíku ox. číslo +I Ox. čísla sepíšu do kříže případně zkrátím (křížové pravidlo) Křížové pravidlo zajišťuje, aby součet oxidačních čísel v molekule = 0 2 * (+1) + 1 * (-2) = 0
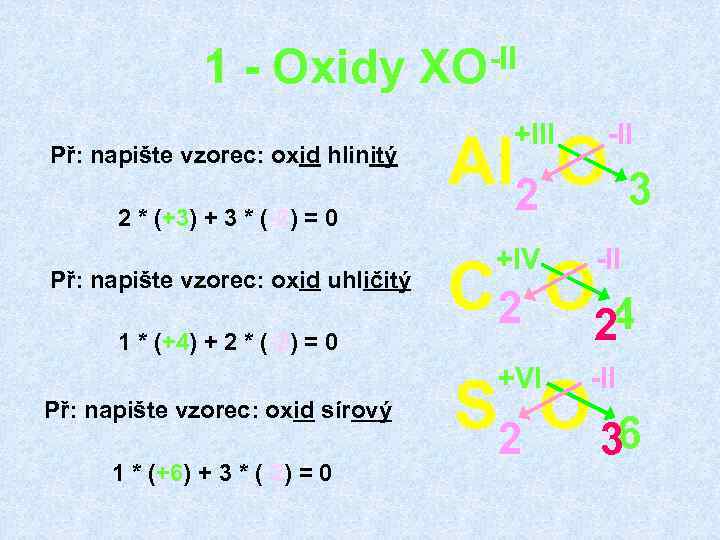 1 - Oxidy XO-II Př: napište vzorec: oxid hlinitý 2 * (+3) + 3 * (-2) = 0 +III -II Al 2 O 3 1 * (+4) + 2 * (-2) = 0 Př: napište vzorec: oxid sírový 1 * (+6) + 3 * (-2) = 0 -II +VI Př: napište vzorec: oxid uhličitý +IV -II C 2 O 24 S 2 O 36
1 - Oxidy XO-II Př: napište vzorec: oxid hlinitý 2 * (+3) + 3 * (-2) = 0 +III -II Al 2 O 3 1 * (+4) + 2 * (-2) = 0 Př: napište vzorec: oxid sírový 1 * (+6) + 3 * (-2) = 0 -II +VI Př: napište vzorec: oxid uhličitý +IV -II C 2 O 24 S 2 O 36
 Př. : Utvoř název ke vzorci Ca. O. Ca je prvek s jednoznačným + oxid. číslem +II, proto koncovka pro vápník - natý platí, že součet oxidačních čísel = 0 2 + (x) = 0 → x = - 2 O-II : OXID Výsledek: Ca. O je oxid vápenatý. Př. : Utvoř název ke vzorci P 2 O 5 P je chemická značka fosforu ze zpětného křížového pravidla vyplývá oxid. číslo +V pro fosfor (a –II pro kyslík) proto koncovka pro fosfor - ečný O-II : OXID Výsledek: P 2 O 5 je oxid fosforečný.
Př. : Utvoř název ke vzorci Ca. O. Ca je prvek s jednoznačným + oxid. číslem +II, proto koncovka pro vápník - natý platí, že součet oxidačních čísel = 0 2 + (x) = 0 → x = - 2 O-II : OXID Výsledek: Ca. O je oxid vápenatý. Př. : Utvoř název ke vzorci P 2 O 5 P je chemická značka fosforu ze zpětného křížového pravidla vyplývá oxid. číslo +V pro fosfor (a –II pro kyslík) proto koncovka pro fosfor - ečný O-II : OXID Výsledek: P 2 O 5 je oxid fosforečný.
 Cvičení 2: Urči oxidační čísla a napiš Názvy • • Cu. O Br 2 O 7 Xe. O 4 Cr. O 3 Li 2 O Zn. O Fe 2 O 3 Si. O 2 Vzorce • • Oxid sodný Oxid sírový Oxid dusičný Oxid hořečnatý Oxid cíničitý Oxid vápenatý Oxid rtuťný Oxid manganistý
Cvičení 2: Urči oxidační čísla a napiš Názvy • • Cu. O Br 2 O 7 Xe. O 4 Cr. O 3 Li 2 O Zn. O Fe 2 O 3 Si. O 2 Vzorce • • Oxid sodný Oxid sírový Oxid dusičný Oxid hořečnatý Oxid cíničitý Oxid vápenatý Oxid rtuťný Oxid manganistý
 Sulfidy: S-II - Obdoba oxidů. - Sloučeniny odvozené od sulfanu (H 2 S) náhradou obou atomů vodíku jiným prvkem (většinou kovem). Název: -Podstatné jméno: SULFID 36
Sulfidy: S-II - Obdoba oxidů. - Sloučeniny odvozené od sulfanu (H 2 S) náhradou obou atomů vodíku jiným prvkem (většinou kovem). Název: -Podstatné jméno: SULFID 36
 Sulfidy (selenidy, telluridy) • sulfidy (selenidy, telluridy) jsou dvouprvkové sloučeniny síry (selenu, telluru) s jiným prvkem • oxidační číslo síry (selenu, telluru) je vždy –II • postup při tvorbě vzorců a názvů sulfidů, selenidů a telluridů je obdobný jako u oxidů Cvičení 3: Z následujících sloučenin vyber sulfidy, selenidy, telluridy. H 2 SO 4, Ca. O, Fe. Se, Na 2 O, SCl 4, Pb. Te, Al. Cl 3, Na 2 S, Fe 2 Te 3, Pb. S
Sulfidy (selenidy, telluridy) • sulfidy (selenidy, telluridy) jsou dvouprvkové sloučeniny síry (selenu, telluru) s jiným prvkem • oxidační číslo síry (selenu, telluru) je vždy –II • postup při tvorbě vzorců a názvů sulfidů, selenidů a telluridů je obdobný jako u oxidů Cvičení 3: Z následujících sloučenin vyber sulfidy, selenidy, telluridy. H 2 SO 4, Ca. O, Fe. Se, Na 2 O, SCl 4, Pb. Te, Al. Cl 3, Na 2 S, Fe 2 Te 3, Pb. S
 Cvičení 4: Odvození názvů a vzorců Vzorce • sulfid hořečnatý • selenid sodný • tellurid cíničitý • sulfid vápenatý • selenid fosforečný • sulfid rtuťný • tellurid chromitý Názvy • • Cu. Se Ag 2 S Fe 2 Te 3 Pb. S K 2 Se Bi 2 Te 3 Ge. Se 2 As 2 S 5
Cvičení 4: Odvození názvů a vzorců Vzorce • sulfid hořečnatý • selenid sodný • tellurid cíničitý • sulfid vápenatý • selenid fosforečný • sulfid rtuťný • tellurid chromitý Názvy • • Cu. Se Ag 2 S Fe 2 Te 3 Pb. S K 2 Se Bi 2 Te 3 Ge. Se 2 As 2 S 5
 Nitridy: N-III - Dvouprvkové sloučeniny dusíku s kovy (především alkalickými a kovy alkalických zemin - Ca, Sr, Ba a Ra). - Sloučeniny odvozené od amoniaku (NH 3) náhradou všech atomů vodíku jiným prvkem. Název: -Podstatné jméno: NITRID 39
Nitridy: N-III - Dvouprvkové sloučeniny dusíku s kovy (především alkalickými a kovy alkalických zemin - Ca, Sr, Ba a Ra). - Sloučeniny odvozené od amoniaku (NH 3) náhradou všech atomů vodíku jiným prvkem. Název: -Podstatné jméno: NITRID 39
 Dvouprvkové sloučeniny s vodíkem - Dvouprvkové sloučeniny vodíku s nepřechodnými prvky. a) sloučeniny vodíku s prvky I a II skupiny -Podstatné jméno : HYDRID H-I b) sloučeniny vodíku s prvky III. A – VI. A skupiny: Koncovka –AN III. A IV. A VI. A MH 3 MH 4 MH 3 H 2 M boran BH 3 silan Si. H 4 fosfan PH 3 sulfan H 2 S alan Al. H 3 german Ge. H 4 arsan As. H 3 selan H 2 Se stannan Sn. H 4 stiban Sb. H 3 tellan H 2 Te c) sloučeniny vodíku s prvky VII. A skupiny halogenvodík 40
Dvouprvkové sloučeniny s vodíkem - Dvouprvkové sloučeniny vodíku s nepřechodnými prvky. a) sloučeniny vodíku s prvky I a II skupiny -Podstatné jméno : HYDRID H-I b) sloučeniny vodíku s prvky III. A – VI. A skupiny: Koncovka –AN III. A IV. A VI. A MH 3 MH 4 MH 3 H 2 M boran BH 3 silan Si. H 4 fosfan PH 3 sulfan H 2 S alan Al. H 3 german Ge. H 4 arsan As. H 3 selan H 2 Se stannan Sn. H 4 stiban Sb. H 3 tellan H 2 Te c) sloučeniny vodíku s prvky VII. A skupiny halogenvodík 40
 Dvouprvkové sloučeniny vodíku • • Prvky I. a II. A: název hydridy, ox. č. H: -I např. hydrid sodný, hydrid vápenatý Prvky III. – IV. A: triviální názvy kořen názvu prvku + koncovka – an ox. č. prvku – odpovídá číslu skupiny • III. A - boran, alan, gallan, indan, thallan • IV. A - methan, silan, german, stanan, plumban •
Dvouprvkové sloučeniny vodíku • • Prvky I. a II. A: název hydridy, ox. č. H: -I např. hydrid sodný, hydrid vápenatý Prvky III. – IV. A: triviální názvy kořen názvu prvku + koncovka – an ox. č. prvku – odpovídá číslu skupiny • III. A - boran, alan, gallan, indan, thallan • IV. A - methan, silan, german, stanan, plumban •
 Dvouprvkové sloučeniny vodíku • Prvky V. - VI. A: ox. č. : max ox. číslo VIII – číslo skupiny (V až VI) V. A ox. č. III vodík je vpravo od značky prvku – azan, fosfan, arsan, stiban, bismutan VI. A ox. č. II vodík je vlevo od značky prvku – oxidan, sulfan, sellan, tellan • Prvky VII. A halogenvodíky, HX – fluorovodík, chlorovodík, bromovodík, jodovodík
Dvouprvkové sloučeniny vodíku • Prvky V. - VI. A: ox. č. : max ox. číslo VIII – číslo skupiny (V až VI) V. A ox. č. III vodík je vpravo od značky prvku – azan, fosfan, arsan, stiban, bismutan VI. A ox. č. II vodík je vlevo od značky prvku – oxidan, sulfan, sellan, tellan • Prvky VII. A halogenvodíky, HX – fluorovodík, chlorovodík, bromovodík, jodovodík
 4 - Hydridy -I XH Př: napište vzorec: hydrid vápenatý +II -I Ca 1 H 2 Slyším-li hydrid, automaticky píšu vodík vpravo H-I Hydrid je VÁPENATÝ, proto kationtem je vápník se značkou Ca Podle koncovky = NATÝ přiřadím vápníku ox. číslo +II Ox. čísla sepíšu do kříže (křížové pravidlo) Křížové pravidlo opět zajišťuje, aby součet oxidačních čísel v molekule = 0 1 * (+2) + 2 * (-1) = 0
4 - Hydridy -I XH Př: napište vzorec: hydrid vápenatý +II -I Ca 1 H 2 Slyším-li hydrid, automaticky píšu vodík vpravo H-I Hydrid je VÁPENATÝ, proto kationtem je vápník se značkou Ca Podle koncovky = NATÝ přiřadím vápníku ox. číslo +II Ox. čísla sepíšu do kříže (křížové pravidlo) Křížové pravidlo opět zajišťuje, aby součet oxidačních čísel v molekule = 0 1 * (+2) + 2 * (-1) = 0
 Př. : Utvoř název ke vzorci KH K je chemická značka draslíku draslík má jednoznačné oxid. číslo +I, proto koncovka pro draslík - ný oxid. číslo x u Hx dopočíme dle pravidla 1: 1*(1) + x = 0 x = -1, H-I : HYDRID Výsledek: KH je hydrid draselný.
Př. : Utvoř název ke vzorci KH K je chemická značka draslíku draslík má jednoznačné oxid. číslo +I, proto koncovka pro draslík - ný oxid. číslo x u Hx dopočíme dle pravidla 1: 1*(1) + x = 0 x = -1, H-I : HYDRID Výsledek: KH je hydrid draselný.
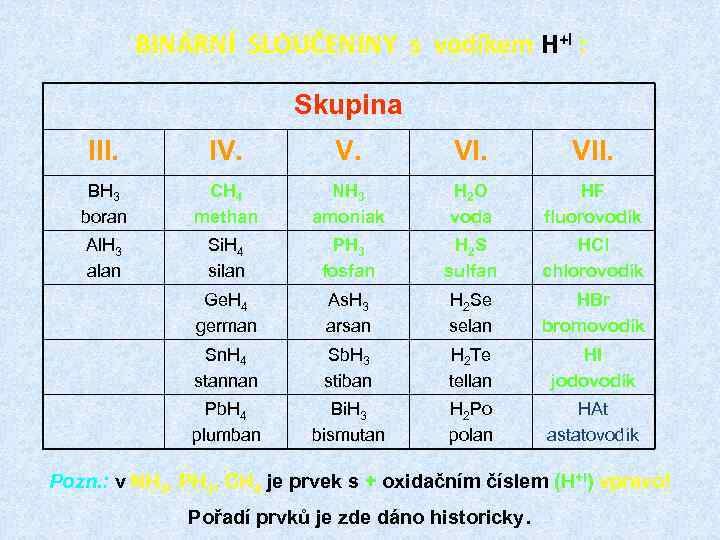 BINÁRNÍ SLOUČENINY s vodíkem H+I : Skupina III. IV. VII. BH 3 boran CH 4 methan NH 3 amoniak H 2 O voda HF fluorovodík Al. H 3 alan Si. H 4 silan PH 3 fosfan H 2 S sulfan HCl chlorovodík Ge. H 4 german As. H 3 arsan H 2 Se selan HBr bromovodík Sn. H 4 stannan Sb. H 3 stiban H 2 Te tellan HI jodovodík Pb. H 4 plumban Bi. H 3 bismutan H 2 Po polan HAt astatovodík Pozn. : v NH 3, PH 3, CH 4 je prvek s + oxidačním číslem (H+I) vpravo! Pořadí prvků je zde dáno historicky.
BINÁRNÍ SLOUČENINY s vodíkem H+I : Skupina III. IV. VII. BH 3 boran CH 4 methan NH 3 amoniak H 2 O voda HF fluorovodík Al. H 3 alan Si. H 4 silan PH 3 fosfan H 2 S sulfan HCl chlorovodík Ge. H 4 german As. H 3 arsan H 2 Se selan HBr bromovodík Sn. H 4 stannan Sb. H 3 stiban H 2 Te tellan HI jodovodík Pb. H 4 plumban Bi. H 3 bismutan H 2 Po polan HAt astatovodík Pozn. : v NH 3, PH 3, CH 4 je prvek s + oxidačním číslem (H+I) vpravo! Pořadí prvků je zde dáno historicky.
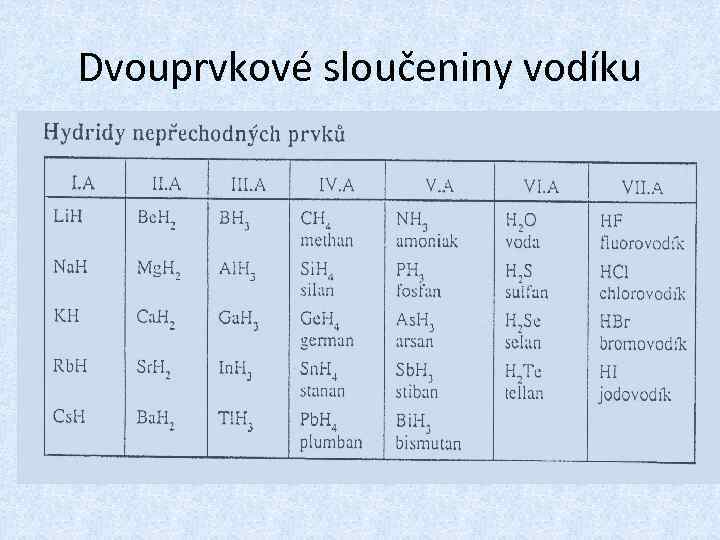 Dvouprvkové sloučeniny vodíku
Dvouprvkové sloučeniny vodíku
 Cvičení 5: Napiš názvy a vzorce • • • Li. H Pb. H 4 As. H 3 H 2 Se Ba. H 2 BH 3 HCl PH 3 H 2 Te • • • alan fosfan bismutan stannan jodovodík silan hydrid sodný azan hydrid vápenatý
Cvičení 5: Napiš názvy a vzorce • • • Li. H Pb. H 4 As. H 3 H 2 Se Ba. H 2 BH 3 HCl PH 3 H 2 Te • • • alan fosfan bismutan stannan jodovodík silan hydrid sodný azan hydrid vápenatý
 Halogenidy: X-I - Dvouprvkové sloučeniny halogenů s jiným prvkem. -Sloučeniny odvozené od halogenvodíků (HX) náhradou atomu vodíku jiným prvkem. -Halogenidy jsou SOLI, které jsou odvozené od bezkyslíkatých kyselin) Název: -Podstatné jméno: FLUORID, CHLORID, BROMID, JODID 48
Halogenidy: X-I - Dvouprvkové sloučeniny halogenů s jiným prvkem. -Sloučeniny odvozené od halogenvodíků (HX) náhradou atomu vodíku jiným prvkem. -Halogenidy jsou SOLI, které jsou odvozené od bezkyslíkatých kyselin) Název: -Podstatné jméno: FLUORID, CHLORID, BROMID, JODID 48
 Halogenidy • jsou dvouprvkové sloučeniny halogenů (F, Cl, Br, I) s jiným prvkem • oxidační číslo halogenů je –I • koncovka – id • fluorid, chlorid, bromid, jodid Cvičení 1: Ze sloučenin vyber halogenidy: KCl, Ca. CO 3, Na. OH, Li 2 O, Pb. S, CCl 4, Fe. Cl 3, Na. Br. O 3, H 2 O, H 3 As. O 4, I 2 O 5, PCl 5, Ca. F 2
Halogenidy • jsou dvouprvkové sloučeniny halogenů (F, Cl, Br, I) s jiným prvkem • oxidační číslo halogenů je –I • koncovka – id • fluorid, chlorid, bromid, jodid Cvičení 1: Ze sloučenin vyber halogenidy: KCl, Ca. CO 3, Na. OH, Li 2 O, Pb. S, CCl 4, Fe. Cl 3, Na. Br. O 3, H 2 O, H 3 As. O 4, I 2 O 5, PCl 5, Ca. F 2
 Odvození vzorce Chlorid hořečnatý • napíšeme značky prvků v obráceném pořadí než v názvu: Mg. Cl • k prvkům napíšeme vpravo nahoru oxidační čísla Mg. IICl-I • sepíšeme oxidační čísla do kříže arabskými číslicemi Mg 1 Cl 2 • v chemii jedničky ve vzorci nepíšeme Mg. Cl 2
Odvození vzorce Chlorid hořečnatý • napíšeme značky prvků v obráceném pořadí než v názvu: Mg. Cl • k prvkům napíšeme vpravo nahoru oxidační čísla Mg. IICl-I • sepíšeme oxidační čísla do kříže arabskými číslicemi Mg 1 Cl 2 • v chemii jedničky ve vzorci nepíšeme Mg. Cl 2
 Odvození názvu CBr 4 • název halogenidu je tvořen podstatným jménem fluorid, chlorid, bromid, jodid a přídavným jménem odvozeným od druhého prvku • napíšeme oxidační číslo halogenu: CBr 4 -I • součet oxidačních čísel ve sloučenině je roven 0, musí být oxidační číslo CIV x + 4 · (-1) = 0 x = 4 • název je bromid uhličitý
Odvození názvu CBr 4 • název halogenidu je tvořen podstatným jménem fluorid, chlorid, bromid, jodid a přídavným jménem odvozeným od druhého prvku • napíšeme oxidační číslo halogenu: CBr 4 -I • součet oxidačních čísel ve sloučenině je roven 0, musí být oxidační číslo CIV x + 4 · (-1) = 0 x = 4 • název je bromid uhličitý
 Cvičení 2: Urči oxidační čísla a napiš Názvy • Hg. I 2 • SCl 4 • Ca. Br 2 • Li. F • Ag. Br • Al. I 3 • Ca. Cl 2 • Cu. F Vzorce • fluorid osmičelý • jodid draselný • chlorid železitý • fluorid sírový • fluorid hořečnatý • chlorid uhličitý • bromid fosforečný • fluorid jodistý
Cvičení 2: Urči oxidační čísla a napiš Názvy • Hg. I 2 • SCl 4 • Ca. Br 2 • Li. F • Ag. Br • Al. I 3 • Ca. Cl 2 • Cu. F Vzorce • fluorid osmičelý • jodid draselný • chlorid železitý • fluorid sírový • fluorid hořečnatý • chlorid uhličitý • bromid fosforečný • fluorid jodistý
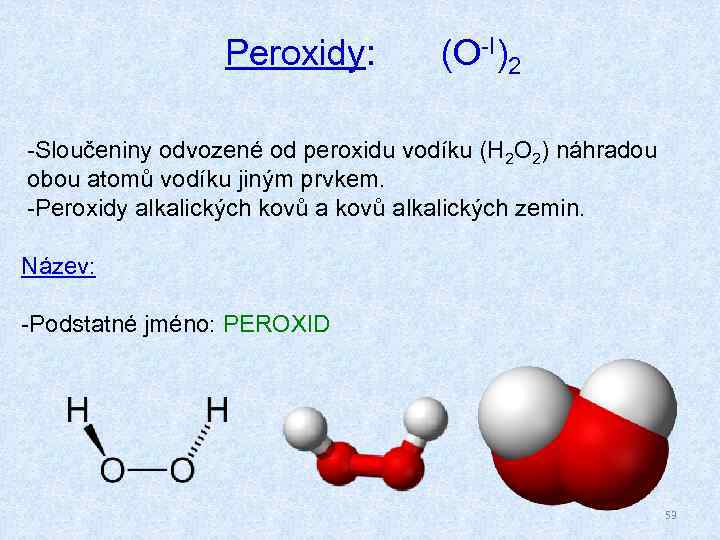 Peroxidy: (O-I)2 -Sloučeniny odvozené od peroxidu vodíku (H 2 O 2) náhradou obou atomů vodíku jiným prvkem. -Peroxidy alkalických kovů alkalických zemin. Název: -Podstatné jméno: PEROXID 53
Peroxidy: (O-I)2 -Sloučeniny odvozené od peroxidu vodíku (H 2 O 2) náhradou obou atomů vodíku jiným prvkem. -Peroxidy alkalických kovů alkalických zemin. Název: -Podstatné jméno: PEROXID 53
 3 - Peroxidy -II X(O 2) Př: napište vzorec: Peroxid sodný +I -II Na 2 (O 2) 1 Slyším-li peroxid, automaticky píšu (O 2)-II Peroxid je sodný, proto kationtem je sodík se značkou Na Podle koncovky = NÝ (SODNÝ) přiřadím sodíku ox. číslo +I Ox. čísla sepíšu do kříže (křížové pravidlo) Dvojky se v peroxidech nekrátí ! 2 * (+1) + 1 * (-2) = 0
3 - Peroxidy -II X(O 2) Př: napište vzorec: Peroxid sodný +I -II Na 2 (O 2) 1 Slyším-li peroxid, automaticky píšu (O 2)-II Peroxid je sodný, proto kationtem je sodík se značkou Na Podle koncovky = NÝ (SODNÝ) přiřadím sodíku ox. číslo +I Ox. čísla sepíšu do kříže (křížové pravidlo) Dvojky se v peroxidech nekrátí ! 2 * (+1) + 1 * (-2) = 0
 Proto POZOR na názvosloví PEROXIDŮ. Prakticky se používá 6 peroxidů: H 2 O 2 peroxid vodíku Mg. O 2 peroxid hořečnatý Na 2 O 2 peroxid sodný Ca. O 2 peroxid vápenatý K 2 O 2 peroxid draselný Ba. O 2 peroxid barnatý Proč se dvojky se v peroxidech nekrátí ? Důvod: peroxidy charakterizuje chemická vazba mezi 2 atomy kyslíku - O – O - (kde vodorovná čárka znamená chem. vazbu), proto ve vzorci 2 atomy kyslíku musí zůstat.
Proto POZOR na názvosloví PEROXIDŮ. Prakticky se používá 6 peroxidů: H 2 O 2 peroxid vodíku Mg. O 2 peroxid hořečnatý Na 2 O 2 peroxid sodný Ca. O 2 peroxid vápenatý K 2 O 2 peroxid draselný Ba. O 2 peroxid barnatý Proč se dvojky se v peroxidech nekrátí ? Důvod: peroxidy charakterizuje chemická vazba mezi 2 atomy kyslíku - O – O - (kde vodorovná čárka znamená chem. vazbu), proto ve vzorci 2 atomy kyslíku musí zůstat.
 Př. : Utvoř název ke vzorci Ba. O 2. O-II je oxid. číslo x u Bax určíme dle pravidla 1: 1*(x) + 2*(-2) = 0 x = +4, tzn. koncovka –ičitý Výsledek: Ba. O 2 je oxid baryčitý. A je to špatně. Proč? CHYBA proto, že Ba je ve 2. sk. PSP, má tedy oxidační číslo +II (nelze mít Ba+IV)
Př. : Utvoř název ke vzorci Ba. O 2. O-II je oxid. číslo x u Bax určíme dle pravidla 1: 1*(x) + 2*(-2) = 0 x = +4, tzn. koncovka –ičitý Výsledek: Ba. O 2 je oxid baryčitý. A je to špatně. Proč? CHYBA proto, že Ba je ve 2. sk. PSP, má tedy oxidační číslo +II (nelze mít Ba+IV)
 Znova: Hledáme název ke vzorci Ba. O 2. oxid. číslo pro kyslík též O-I , tzn. peroxid. základ vzorce: Bax. O-I 2 oxid. číslo x určíme opět dle pravidla 1: 1*x + 2*(-1) = 0 x = 2 a to čekáme Výsledek: Ba. O 2 je peroxid barnatý.
Znova: Hledáme název ke vzorci Ba. O 2. oxid. číslo pro kyslík též O-I , tzn. peroxid. základ vzorce: Bax. O-I 2 oxid. číslo x určíme opět dle pravidla 1: 1*x + 2*(-1) = 0 x = 2 a to čekáme Výsledek: Ba. O 2 je peroxid barnatý.
 Hyperoxidy: (O 2)-I -Sloučeniny kyslíku s alkalickými kovy (s výjimkou Li) -hyperoxid sodný Na. O 2 -hyperoxid draselný KO 2 -hyperoxid rubidný Rb. O 2 -hyperoxid cesný Cs. O 2 Název: -Podstatné jméno: HYPEROXID Selenidy: (Se)-II Azidy: (N 3)-I Telluridy: (Te)-II Karbidy: (C)-IV 58
Hyperoxidy: (O 2)-I -Sloučeniny kyslíku s alkalickými kovy (s výjimkou Li) -hyperoxid sodný Na. O 2 -hyperoxid draselný KO 2 -hyperoxid rubidný Rb. O 2 -hyperoxid cesný Cs. O 2 Název: -Podstatné jméno: HYPEROXID Selenidy: (Se)-II Azidy: (N 3)-I Telluridy: (Te)-II Karbidy: (C)-IV 58
 Tříprvkové sloučeniny • hydroxidy • kyslíkaté kyseliny (oxokyseliny) • polykyseliny • thiokyseliny • soli kyslíkatých kyselin
Tříprvkové sloučeniny • hydroxidy • kyslíkaté kyseliny (oxokyseliny) • polykyseliny • thiokyseliny • soli kyslíkatých kyselin
 Hydroxidy: (OH)-I Sloučeniny odvozené od vody (H 2 O) náhradou jednoho atomu vodíku jiným elektropozitivním prvkem. Název: -Podstatné jméno: HYDROXID 60
Hydroxidy: (OH)-I Sloučeniny odvozené od vody (H 2 O) náhradou jednoho atomu vodíku jiným elektropozitivním prvkem. Název: -Podstatné jméno: HYDROXID 60
 Pravidla • ve vzorcích tříprvkových sloučenin má kyslík záporné • vodík a třetí prvek kladné oxidační číslo – Oxidační číslo kyslíku ve sloučeninách je vždy -II (O-II). – Oxidační číslo vodíku ve sloučeninách je vždy +I (H+I). • Součet oxidačních čísel ve vzorci = 0.
Pravidla • ve vzorcích tříprvkových sloučenin má kyslík záporné • vodík a třetí prvek kladné oxidační číslo – Oxidační číslo kyslíku ve sloučeninách je vždy -II (O-II). – Oxidační číslo vodíku ve sloučeninách je vždy +I (H+I). • Součet oxidačních čísel ve vzorci = 0.
 Hydroxidy • hydroxidy jsou tříprvkové sloučeniny kovu, kyslíku a vodíku • kyslík a vodík tvoří v hydroxidu hydroxidovou skupinu OH-I (OH-I, protože je O-II a H-I) • podstatné jméno = hydroxid • přídavné jméno má zakončení, které odpovídá oxidačnímu číslu kovu • oxidační číslo kovu je vždy kladné • Cvičení 7: Vyber ze sloučenin hydroxidy. Al(OH)3, KCl, Na. OH, K 2 O, CCl 4, Zn. S, Al. Cl 3, H 2 O, KCl. O 3, Mg(OH)2, P 2 O 5, H 2 SO 3, PCl 3
Hydroxidy • hydroxidy jsou tříprvkové sloučeniny kovu, kyslíku a vodíku • kyslík a vodík tvoří v hydroxidu hydroxidovou skupinu OH-I (OH-I, protože je O-II a H-I) • podstatné jméno = hydroxid • přídavné jméno má zakončení, které odpovídá oxidačnímu číslu kovu • oxidační číslo kovu je vždy kladné • Cvičení 7: Vyber ze sloučenin hydroxidy. Al(OH)3, KCl, Na. OH, K 2 O, CCl 4, Zn. S, Al. Cl 3, H 2 O, KCl. O 3, Mg(OH)2, P 2 O 5, H 2 SO 3, PCl 3
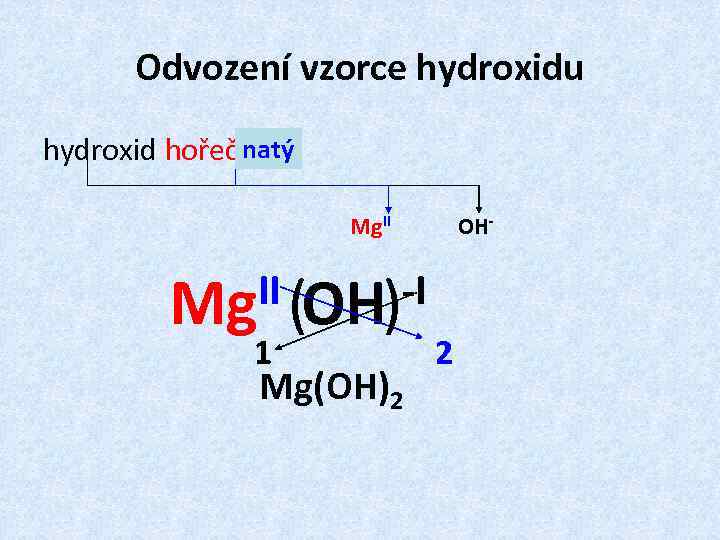 Odvození vzorce hydroxidu natý hydroxid hořečnatý: OH- Mg. II II (OH) -I Mg 1 Mg(OH)2 2
Odvození vzorce hydroxidu natý hydroxid hořečnatý: OH- Mg. II II (OH) -I Mg 1 Mg(OH)2 2
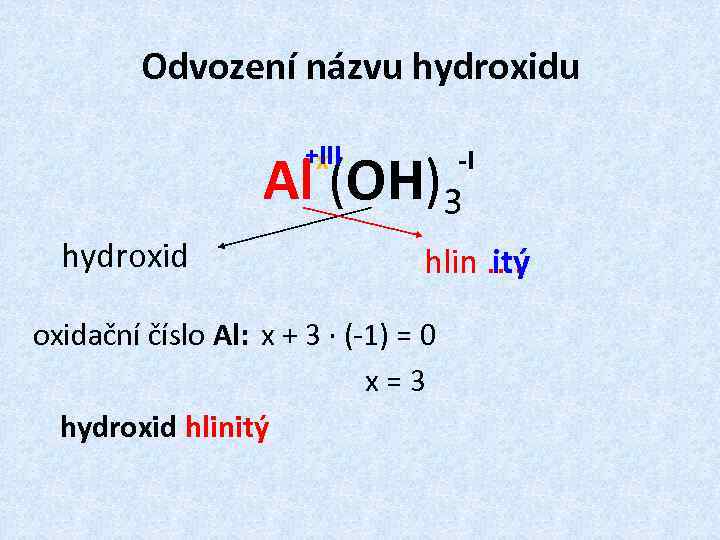 Odvození názvu hydroxidu +III x Al (OH)3 hydroxid -I hlin. . itý oxidační číslo Al: x + 3 · (-1) = 0 x = 3 hydroxid hlinitý
Odvození názvu hydroxidu +III x Al (OH)3 hydroxid -I hlin. . itý oxidační číslo Al: x + 3 · (-1) = 0 x = 3 hydroxid hlinitý
 BINÁRNÍ SLOUČENINY 2 - Hydroxidy obsahují skupinu (OH)-I. Vznikají reakcí oxidů kovů s nízkým oxid. číslem (I až III) s vodou Př. Ca. O + H 2 O = Ca(OH)2 X(OH)-I
BINÁRNÍ SLOUČENINY 2 - Hydroxidy obsahují skupinu (OH)-I. Vznikají reakcí oxidů kovů s nízkým oxid. číslem (I až III) s vodou Př. Ca. O + H 2 O = Ca(OH)2 X(OH)-I
 2 - Hydroxidy -I X(OH) Př: napište vzorec: hydroxid vápenatý +II -I Ca 1 (OH) 2 Slyším-li hydroxid, automaticky píšu (OH)-I Hydroxid je VÁPENATÝ, proto kationtem je vápník se značkou Ca Podle koncovky = NATÝ přiřadím vápníku ox. číslo +II Ox. čísla sepíšu do kříže případně zkrátím (křížové pravidlo) Křížové pravidlo opět zajišťuje, aby součet oxidačních čísel v molekule = 0 1 * (+2) + 2 * (-1) = 0
2 - Hydroxidy -I X(OH) Př: napište vzorec: hydroxid vápenatý +II -I Ca 1 (OH) 2 Slyším-li hydroxid, automaticky píšu (OH)-I Hydroxid je VÁPENATÝ, proto kationtem je vápník se značkou Ca Podle koncovky = NATÝ přiřadím vápníku ox. číslo +II Ox. čísla sepíšu do kříže případně zkrátím (křížové pravidlo) Křížové pravidlo opět zajišťuje, aby součet oxidačních čísel v molekule = 0 1 * (+2) + 2 * (-1) = 0
 2 - Hydroxidy X(OH)-I Př: napište vzorec: hydroxid železitý +III Fe 1 (OH) 1 * (+3) + 3 * (-1) = 0 Př: napište vzorec: hydroxid draselný 1 * (+1) + 1 * (-1) = 0 -I +I 3 -I K 1 (OH) 1
2 - Hydroxidy X(OH)-I Př: napište vzorec: hydroxid železitý +III Fe 1 (OH) 1 * (+3) + 3 * (-1) = 0 Př: napište vzorec: hydroxid draselný 1 * (+1) + 1 * (-1) = 0 -I +I 3 -I K 1 (OH) 1
 Př. : Utvoř název ke vzorci Cu(OH)2 (OH)-I : HYDROXID Cu je chemická značka mědi ze zpětného křížového pravidla vyplývá oxid. číslo +II, proto koncovka - natý Výsledek: Cu(OH)2 je hydroxid měďnatý. Př. : Utvoř název ke vzorci KOH (OH)-I : HYDROXID K je chemická značka draslíku draslík má jednoznačné oxid. číslo +I, proto koncovka - ný Výsledek: KOH nebo K(OH) je hydroxid draselný.
Př. : Utvoř název ke vzorci Cu(OH)2 (OH)-I : HYDROXID Cu je chemická značka mědi ze zpětného křížového pravidla vyplývá oxid. číslo +II, proto koncovka - natý Výsledek: Cu(OH)2 je hydroxid měďnatý. Př. : Utvoř název ke vzorci KOH (OH)-I : HYDROXID K je chemická značka draslíku draslík má jednoznačné oxid. číslo +I, proto koncovka - ný Výsledek: KOH nebo K(OH) je hydroxid draselný.
 Cvičení 8: Urči oxidační čísla a napiš • • hydroxid železitý hydroxid sodný hydroxid thoričitý hydroxid cíničitý hydroxid draselný hydroxid barnatý hydroxid vápenatý hydroxid amonný • • Pb(OH)4 Hg(OH)2 Ag. OH Cr(OH)3 Li. OH Zn(OH)2 Rb. OH Sr(OH)2
Cvičení 8: Urči oxidační čísla a napiš • • hydroxid železitý hydroxid sodný hydroxid thoričitý hydroxid cíničitý hydroxid draselný hydroxid barnatý hydroxid vápenatý hydroxid amonný • • Pb(OH)4 Hg(OH)2 Ag. OH Cr(OH)3 Li. OH Zn(OH)2 Rb. OH Sr(OH)2
 Názvosloví kyselin: Obsahují vždy VODÍK HI Podle počtu odštěpitelných vodíků dělíme kyseliny na: Jednosytné HCl. O 4 HCl Dvousytné H 2 SO 4 H 2 S H 3 PO 3 Vícesytné H 3 PO 4 = sytnost kyselin Podle obsahu kyslíků dělíme kyseliny na: Bezkyslíkaté HCl H 2 S Kyslíkaté H 2 SO 4 H 3 PO 3 H 3 PO 4 70
Názvosloví kyselin: Obsahují vždy VODÍK HI Podle počtu odštěpitelných vodíků dělíme kyseliny na: Jednosytné HCl. O 4 HCl Dvousytné H 2 SO 4 H 2 S H 3 PO 3 Vícesytné H 3 PO 4 = sytnost kyselin Podle obsahu kyslíků dělíme kyseliny na: Bezkyslíkaté HCl H 2 S Kyslíkaté H 2 SO 4 H 3 PO 3 H 3 PO 4 70
 Bezkyslíkaté kyseliny: Vznikají rozpuštěním plynu ve vodě! Název: Kyselina PLYN + OVÁ HF HCl HBr HI H 2 S kyselina fluorovodíková kyselina chlorovodíková kyselina bromovodíková kyselina jodovodíková kyselina sirovodíková plyn: fluorovodík plyn: chlorovodík plyn: bromovodík plyn: jodovodík plyn: sirovodík (sulfan) 71
Bezkyslíkaté kyseliny: Vznikají rozpuštěním plynu ve vodě! Název: Kyselina PLYN + OVÁ HF HCl HBr HI H 2 S kyselina fluorovodíková kyselina chlorovodíková kyselina bromovodíková kyselina jodovodíková kyselina sirovodíková plyn: fluorovodík plyn: chlorovodík plyn: bromovodík plyn: jodovodík plyn: sirovodík (sulfan) 71
 Bezkyslíkaté kyseliny • neobsahují kyslík • dvou nebo tříprvkové sloučeniny • halogenvodíkové kyseliny – vznikají zaváděním halogenvodíků do vody – fluorovodíková – chlorovodíková – bromovodíková – jodovodíková • kyselina kyanovodíková HCN • kyselina sulfanová H 2 S • kyselina selenovodíková H 2 Se
Bezkyslíkaté kyseliny • neobsahují kyslík • dvou nebo tříprvkové sloučeniny • halogenvodíkové kyseliny – vznikají zaváděním halogenvodíků do vody – fluorovodíková – chlorovodíková – bromovodíková – jodovodíková • kyselina kyanovodíková HCN • kyselina sulfanová H 2 S • kyselina selenovodíková H 2 Se
 Názvosloví bezkyslíkatých kyselin Název: • podstatné jméno - kyselina • přídavné jméno - odvozeného od názvu nekovu + přípona –ovodíková Vzorec: • atom vodíku jako první • atom nekovu vpravo za vodíkem • oxidační číslo nekovu je záporné, vodíku +I. • součet oxidačních čísel v molekule je roven 0 Cvičení 6: Odvoď název kyseliny HCl a vzorec kyseliny jodovodíkové.
Názvosloví bezkyslíkatých kyselin Název: • podstatné jméno - kyselina • přídavné jméno - odvozeného od názvu nekovu + přípona –ovodíková Vzorec: • atom vodíku jako první • atom nekovu vpravo za vodíkem • oxidační číslo nekovu je záporné, vodíku +I. • součet oxidačních čísel v molekule je roven 0 Cvičení 6: Odvoď název kyseliny HCl a vzorec kyseliny jodovodíkové.
 Kyslíkaté kyseliny (oxokyseliny): Vznikají reakcí příslušného oxidu s vodou. SO 2 + H 2 O H 2 SO 3 Název: Podstatné jméno: Kyselina Přídavné jméno: charakterizuje centrální atom a jeho oxidační číslo, které je vždy kladné. 74
Kyslíkaté kyseliny (oxokyseliny): Vznikají reakcí příslušného oxidu s vodou. SO 2 + H 2 O H 2 SO 3 Název: Podstatné jméno: Kyselina Přídavné jméno: charakterizuje centrální atom a jeho oxidační číslo, které je vždy kladné. 74
 Kyslíkaté kyseliny – tvorba VZORCŮ: Kyselina chloristá 1. Napíšeme značky prvků podle názvu I VII -II H Cl O 4 2. Doplníme oxidační čísla kyslík –II, vodík +I, chlor: podle názvu 3. Dopočítáme počet KYSLÍKŮ: molekula musí být elektroneutrální, tzn. , že součet oxidačních čísel = 0. Sečteme kladná oxidační čísla a vydělíme 2 (1+7)/2=4 Je-li součet kladných oxidačních čísel lichý doplníme vodík!!! Např. u kyseliny siřičité 75
Kyslíkaté kyseliny – tvorba VZORCŮ: Kyselina chloristá 1. Napíšeme značky prvků podle názvu I VII -II H Cl O 4 2. Doplníme oxidační čísla kyslík –II, vodík +I, chlor: podle názvu 3. Dopočítáme počet KYSLÍKŮ: molekula musí být elektroneutrální, tzn. , že součet oxidačních čísel = 0. Sečteme kladná oxidační čísla a vydělíme 2 (1+7)/2=4 Je-li součet kladných oxidačních čísel lichý doplníme vodík!!! Např. u kyseliny siřičité 75
 Kyslíkaté kyseliny – tvorba NÁZVŮ: I VI -II 1. Doplníme oxidační čísla H Cr O 4 2 kyslík –II, vodík +I, chlor: vypočteme (molekula musí být elektroneutrální) 2. 1 + x + 4. (-2) = 0 X = 6 2. Vytvoříme název kyseliny. Kyselina chromová Některé prvky tvoří pro určité oxidační číslo více kyselin, jejichž molekuly se liší počtem atomů vodíku a kyslíku!!! Odlišení v názvu pomocí předpony vyjadřující počet atomů vodíků + předpona hydrogen!!! Mono- ditritetrapenta- hexa- … Kyselina dihydrogenchromová Pokud je od určitého oxidačního čísla známá pouze jedna kyselina, není nutné počet atomů vodíku uvádět!!! Kyselina chromová 76
Kyslíkaté kyseliny – tvorba NÁZVŮ: I VI -II 1. Doplníme oxidační čísla H Cr O 4 2 kyslík –II, vodík +I, chlor: vypočteme (molekula musí být elektroneutrální) 2. 1 + x + 4. (-2) = 0 X = 6 2. Vytvoříme název kyseliny. Kyselina chromová Některé prvky tvoří pro určité oxidační číslo více kyselin, jejichž molekuly se liší počtem atomů vodíku a kyslíku!!! Odlišení v názvu pomocí předpony vyjadřující počet atomů vodíků + předpona hydrogen!!! Mono- ditritetrapenta- hexa- … Kyselina dihydrogenchromová Pokud je od určitého oxidačního čísla známá pouze jedna kyselina, není nutné počet atomů vodíku uvádět!!! Kyselina chromová 76
 Kyslíkaté kyseliny • dělení podle počtu vázaných atomů vodíku: jednosytné x dvojsytné x vícesytné • atom vodíku má vždy oxidační číslo I • atom kyslíku v kyselinách má vždy oxidační číslo –II • oxidační číslo základního prvku je určeno zakončením v názvu kyseliny
Kyslíkaté kyseliny • dělení podle počtu vázaných atomů vodíku: jednosytné x dvojsytné x vícesytné • atom vodíku má vždy oxidační číslo I • atom kyslíku v kyselinách má vždy oxidační číslo –II • oxidační číslo základního prvku je určeno zakončením v názvu kyseliny
 Postup při tvorbě vzorce • zapíšeme atomy tvořící kyselinu v pořadí vodík, základní prvek, kyslík • napíšeme jejich oxidační čísla • sečteme všechna kladná a záporná oxidační čísla • součet kladných i záporných oxidačních čísel musí být roven nule • v kyselinách obsahujících základní prvek s lichým oxidačním číslem bývá obvykle jeden atom vodíku • v kyselinách obsahujících základní prvek se sudým oxidačním číslem bývají dva atomy vodíku
Postup při tvorbě vzorce • zapíšeme atomy tvořící kyselinu v pořadí vodík, základní prvek, kyslík • napíšeme jejich oxidační čísla • sečteme všechna kladná a záporná oxidační čísla • součet kladných i záporných oxidačních čísel musí být roven nule • v kyselinách obsahujících základní prvek s lichým oxidačním číslem bývá obvykle jeden atom vodíku • v kyselinách obsahujících základní prvek se sudým oxidačním číslem bývají dva atomy vodíku
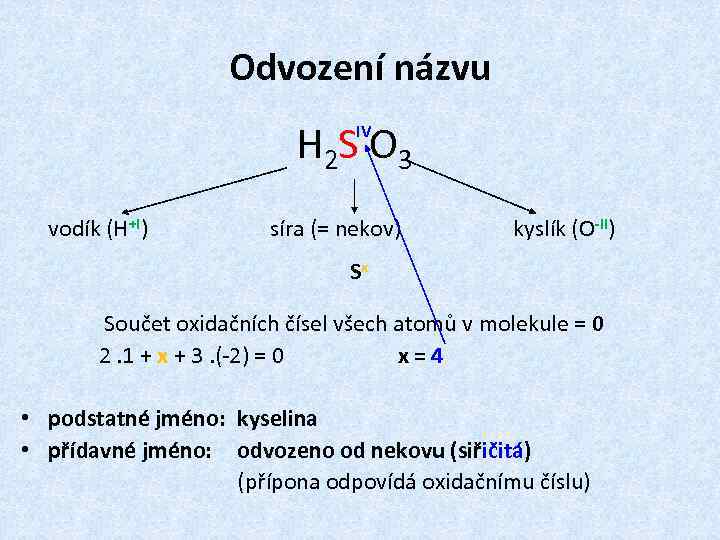 Odvození názvu H 2 S O 3 IV vodík (H+I) síra (= nekov) kyslík (O-II) Sx Součet oxidačních čísel všech atomů v molekule = 0 2. 1 + x + 3. (-2) = 0 x = 4 • podstatné jméno: kyselina • přídavné jméno: odvozeno od nekovu (siřičitá) (přípona odpovídá oxidačnímu číslu)
Odvození názvu H 2 S O 3 IV vodík (H+I) síra (= nekov) kyslík (O-II) Sx Součet oxidačních čísel všech atomů v molekule = 0 2. 1 + x + 3. (-2) = 0 x = 4 • podstatné jméno: kyselina • přídavné jméno: odvozeno od nekovu (siřičitá) (přípona odpovídá oxidačnímu číslu)
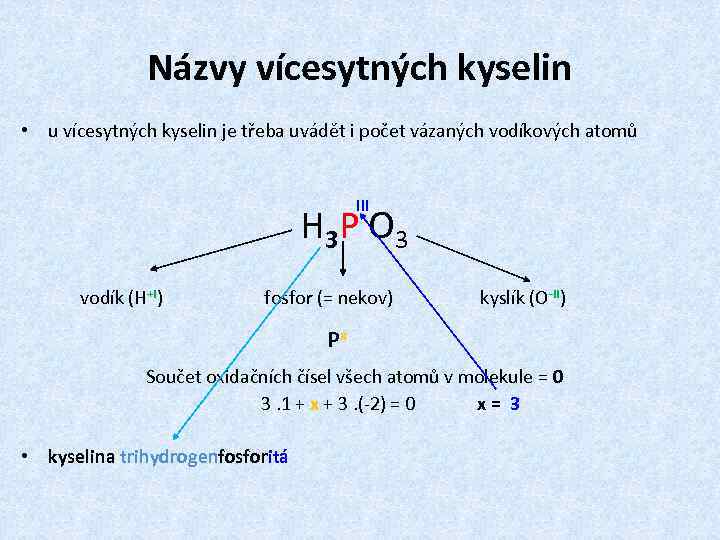 Názvy vícesytných kyselin • u vícesytných kyselin je třeba uvádět i počet vázaných vodíkových atomů III H 3 P O 3 vodík (H+I) fosfor (= nekov) kyslík (O-II) Px Součet oxidačních čísel všech atomů v molekule = 0 3. 1 + x + 3. (-2) = 0 x= 3 • kyselina trihydrogenfosforitá
Názvy vícesytných kyselin • u vícesytných kyselin je třeba uvádět i počet vázaných vodíkových atomů III H 3 P O 3 vodík (H+I) fosfor (= nekov) kyslík (O-II) Px Součet oxidačních čísel všech atomů v molekule = 0 3. 1 + x + 3. (-2) = 0 x= 3 • kyselina trihydrogenfosforitá
 Cvičení 9: Napiš vzorce kyselin • kyselina chlorná • kyselina uhličitá • kyselina chromitá • kyselina dusičná • kyselina manganistá • kyselina chromová
Cvičení 9: Napiš vzorce kyselin • kyselina chlorná • kyselina uhličitá • kyselina chromitá • kyselina dusičná • kyselina manganistá • kyselina chromová
 Číslovkové předpony • • 1 – mono 2 – di 3 – tri 4 – tetra 5 – penta 6 – hexa 7 – hepta trihydrogen tetrahydrogen pentahydrogen hexahydrogen
Číslovkové předpony • • 1 – mono 2 – di 3 – tri 4 – tetra 5 – penta 6 – hexa 7 – hepta trihydrogen tetrahydrogen pentahydrogen hexahydrogen
 Cvičení 10: Napiš vzorce a názvy • kyselina trihydrogenboritá • HBr. O • kyselina dihydrogenselenová • H 2 SO 3 • kyselina trihydrogenaseničná • HNO 2 • kyselina tetrahydrogenkřemičitá • H 2 Te. O 4 • kyselina pentahydrogenjodistá • kyselina trihydrogenxenoničelá • HIO 4 • kyselina dihydrogenuhličitá • H 3 PO 4 • HCl. O 3
Cvičení 10: Napiš vzorce a názvy • kyselina trihydrogenboritá • HBr. O • kyselina dihydrogenselenová • H 2 SO 3 • kyselina trihydrogenaseničná • HNO 2 • kyselina tetrahydrogenkřemičitá • H 2 Te. O 4 • kyselina pentahydrogenjodistá • kyselina trihydrogenxenoničelá • HIO 4 • kyselina dihydrogenuhličitá • H 3 PO 4 • HCl. O 3
 Polykyseliny • obsahují-li více atomů centrál. prvku • • H 2 Cr 2 VIO 7 H 2 S 2 VIO 7 H 2 Cr 3 VIO 10 H 4 P 2 V O 7 k. dichromová k. disírová k. trichromová k. tetrahydrogendifosforečná
Polykyseliny • obsahují-li více atomů centrál. prvku • • H 2 Cr 2 VIO 7 H 2 S 2 VIO 7 H 2 Cr 3 VIO 10 H 4 P 2 V O 7 k. dichromová k. disírová k. trichromová k. tetrahydrogendifosforečná
 Sůl: Sloučeniny odvozené od kyseliny náhradou jednoho či více atomů vodíku jiným elektropozitivním prvkem. Vznikají celou řadou reakcí: Nejčastěji NEUTRALIZACÍ, což je reakce kyseliny s hydroxidem za vzniku soli a vody. H 2 SO 3 + Ca(OH)2 → Ca 2 SO 3 + 2 H 2 O 1. Soli bezkyslíkatých kyselin (viz dříve - halogenidy, sulfidy, selenidy, telluridy, kyanidy…) 2. Soli kyslíkatých kyselin 85
Sůl: Sloučeniny odvozené od kyseliny náhradou jednoho či více atomů vodíku jiným elektropozitivním prvkem. Vznikají celou řadou reakcí: Nejčastěji NEUTRALIZACÍ, což je reakce kyseliny s hydroxidem za vzniku soli a vody. H 2 SO 3 + Ca(OH)2 → Ca 2 SO 3 + 2 H 2 O 1. Soli bezkyslíkatých kyselin (viz dříve - halogenidy, sulfidy, selenidy, telluridy, kyanidy…) 2. Soli kyslíkatých kyselin 85
 Názvy solí kyslíkatých kyselin: Název: Podstatné jméno: charakterizuje ANION kyseliny, od níž je sůl odvozena. koncovka -AN Ox. č. kyselina anion I -ná -nan II -natá -natan III -itá -itan IV -ičitá -ičitan V -ičná; -ečná -ičnan; -ečnan VI -ová -an !!! VII -istá -istan VII -ičelá -ičelan K 2 SO 4 Síran draselný Přídavné jméno: charakterizuje KATION (centrální atom) a jeho oxidační číslo. 86
Názvy solí kyslíkatých kyselin: Název: Podstatné jméno: charakterizuje ANION kyseliny, od níž je sůl odvozena. koncovka -AN Ox. č. kyselina anion I -ná -nan II -natá -natan III -itá -itan IV -ičitá -ičitan V -ičná; -ečná -ičnan; -ečnan VI -ová -an !!! VII -istá -istan VII -ičelá -ičelan K 2 SO 4 Síran draselný Přídavné jméno: charakterizuje KATION (centrální atom) a jeho oxidační číslo. 86
 Kyslíkaté kyseliny – tvorba VZORCŮ: Siřičitan vápenatý 1. Vzorec kyseliny → anion kyseliny 2. Kation – podle přídavného jména (vápenatý) H 2 SO 3 ↓ 2+ Ca SO 32 - 3. Doplníme oxidační číslo: -natý 4. Křížové pravidlo Ca. SO 3 87
Kyslíkaté kyseliny – tvorba VZORCŮ: Siřičitan vápenatý 1. Vzorec kyseliny → anion kyseliny 2. Kation – podle přídavného jména (vápenatý) H 2 SO 3 ↓ 2+ Ca SO 32 - 3. Doplníme oxidační číslo: -natý 4. Křížové pravidlo Ca. SO 3 87
 Kyslíkaté kyseliny – tvorba NÁZVŮ !!!: -II III 1. Ze vzorce odvodím název SÍRAN: Al 2 (SO 4)3 ↓ x + 4. (-2) = -2 X = 6 VI -II SO 42 - 2. Křížové pravidlo → náboj kationtu hliníku. Určíme koncovku přídavného jména: hlinitý Síran hlinitý 88
Kyslíkaté kyseliny – tvorba NÁZVŮ !!!: -II III 1. Ze vzorce odvodím název SÍRAN: Al 2 (SO 4)3 ↓ x + 4. (-2) = -2 X = 6 VI -II SO 42 - 2. Křížové pravidlo → náboj kationtu hliníku. Určíme koncovku přídavného jména: hlinitý Síran hlinitý 88
 Soli kyslíkatých kyselin • odvozeny náhradou atomu/ů vodíku/ů jiným atomem (kovem) nebo skupinou NH 4+ • podstatné jméno: odvozené od kyselin • zakončení –an • přídavné jméno: je odvozeno od kovu • má zakončení podle oxidačního čísla
Soli kyslíkatých kyselin • odvozeny náhradou atomu/ů vodíku/ů jiným atomem (kovem) nebo skupinou NH 4+ • podstatné jméno: odvozené od kyselin • zakončení –an • přídavné jméno: je odvozeno od kovu • má zakončení podle oxidačního čísla
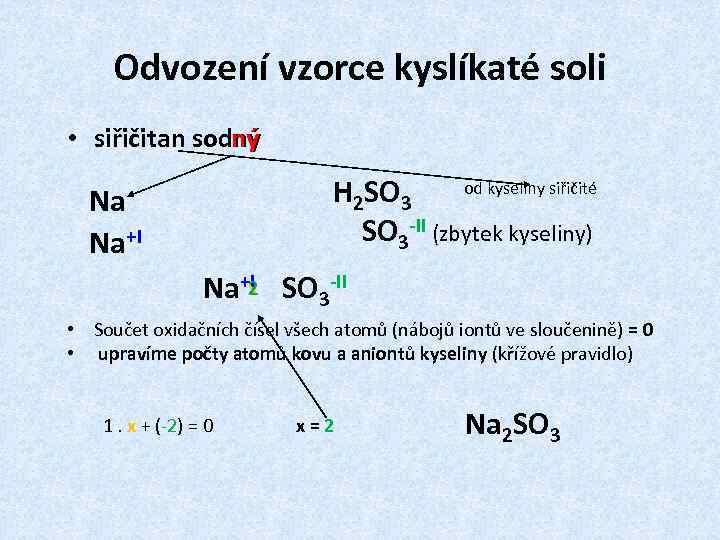 Odvození vzorce kyslíkaté soli ný • siřičitan sodný od kyseliny siřičité H 2 SO 3 -II (zbytek kyseliny) Na Na+I 2 x Na+I SO 3 -II • Součet oxidačních čísel všech atomů (nábojů iontů ve sloučenině) = 0 • upravíme počty atomů kovu a aniontů kyseliny (křížové pravidlo) 1. x + (-2) = 0 x = 2 Na 2 SO 3
Odvození vzorce kyslíkaté soli ný • siřičitan sodný od kyseliny siřičité H 2 SO 3 -II (zbytek kyseliny) Na Na+I 2 x Na+I SO 3 -II • Součet oxidačních čísel všech atomů (nábojů iontů ve sloučenině) = 0 • upravíme počty atomů kovu a aniontů kyseliny (křížové pravidlo) 1. x + (-2) = 0 x = 2 Na 2 SO 3
 Cvičení 11: Pojmenuj soli • • dusičnan draselný uhličitan vápenatý síran hořečnatý fosforečnan hlinitý hlinitan barnatý chlornan stříbrný manganistan draselný
Cvičení 11: Pojmenuj soli • • dusičnan draselný uhličitan vápenatý síran hořečnatý fosforečnan hlinitý hlinitan barnatý chlornan stříbrný manganistan draselný
 Odvození názvu kyslíkaté soli Al 2(SO 4)3 • sůl je odvozena od H 2 SO 4 síran • napíšeme oxidační číslo aniontu = náboj kyseliny (SO 4)-II • vypočteme oxidační číslo Al 2 · x + 3 · (-2) = 0 x = 3 • doplníme do vzorce Al. III 2(SO 4)-II 3 • oxidačnímu číslu III náleží koncovka –itý • název síran hlinitý
Odvození názvu kyslíkaté soli Al 2(SO 4)3 • sůl je odvozena od H 2 SO 4 síran • napíšeme oxidační číslo aniontu = náboj kyseliny (SO 4)-II • vypočteme oxidační číslo Al 2 · x + 3 · (-2) = 0 x = 3 • doplníme do vzorce Al. III 2(SO 4)-II 3 • oxidačnímu číslu III náleží koncovka –itý • název síran hlinitý
 Cvičení 12: Odvoď názvy solí • • Na 3 PO 4 Cu. CO 3 Mg 3(PO 4)2 Zn(NO 3)2 Ag 2 SO 4 KNO 3 Na 2 SO 4 KCl. O 3
Cvičení 12: Odvoď názvy solí • • Na 3 PO 4 Cu. CO 3 Mg 3(PO 4)2 Zn(NO 3)2 Ag 2 SO 4 KNO 3 Na 2 SO 4 KCl. O 3
 Amonné soli • mají místo kovu amonný kation NH 4+ • přídavné jméno - amonný • postup při tvoření názvu a vzorce u amonných solí je obdobný jako u ostatních solí Cvičení 13: Napiš vzorec fosforečnanu amonného: Napiš název (NH 4)2 SO 4:
Amonné soli • mají místo kovu amonný kation NH 4+ • přídavné jméno - amonný • postup při tvoření názvu a vzorce u amonných solí je obdobný jako u ostatních solí Cvičení 13: Napiš vzorec fosforečnanu amonného: Napiš název (NH 4)2 SO 4:
 Názvosloví kyselých solí Kyselé soli = soli, jejichž molekuly obsahují atomy vodíku (tzv. kyselé vodíky), které lze nahradit atomem (atomy) kovu. Přítomnost kyselých vodíků se vyjadřuje: 1. V NÁZVU: Před názvem aniontu číselným údajem (mono-, di -, tri-…) a předponou HYDROGEN. Vznikají pouze od více sytných kyselin: H 2 SO 4: sírany (SO 4)2 -, H 3 PO 4: fosforečnany (PO 4)3 hydrogensírany (HSO 4) - hydrogenfosforečnany (HPO 4)2 -, dihydrogenfosforečnany (H 2 PO 4)- Příklady: Ca(HCO 3)2 KH 2 PO 4 Na. HCO 3 Ca(H 2 PO 4)2 Hydrogenuhličitan vápenatý Dihydrogenfosforečnan draselný Hydrogenuhličitan sodný Dihydrogenfosforečnan vápenatý KHS Na 2 HAs. O 4 Ba. HPO 4 Cs 2 H 4 Te. O 6
Názvosloví kyselých solí Kyselé soli = soli, jejichž molekuly obsahují atomy vodíku (tzv. kyselé vodíky), které lze nahradit atomem (atomy) kovu. Přítomnost kyselých vodíků se vyjadřuje: 1. V NÁZVU: Před názvem aniontu číselným údajem (mono-, di -, tri-…) a předponou HYDROGEN. Vznikají pouze od více sytných kyselin: H 2 SO 4: sírany (SO 4)2 -, H 3 PO 4: fosforečnany (PO 4)3 hydrogensírany (HSO 4) - hydrogenfosforečnany (HPO 4)2 -, dihydrogenfosforečnany (H 2 PO 4)- Příklady: Ca(HCO 3)2 KH 2 PO 4 Na. HCO 3 Ca(H 2 PO 4)2 Hydrogenuhličitan vápenatý Dihydrogenfosforečnan draselný Hydrogenuhličitan sodný Dihydrogenfosforečnan vápenatý KHS Na 2 HAs. O 4 Ba. HPO 4 Cs 2 H 4 Te. O 6
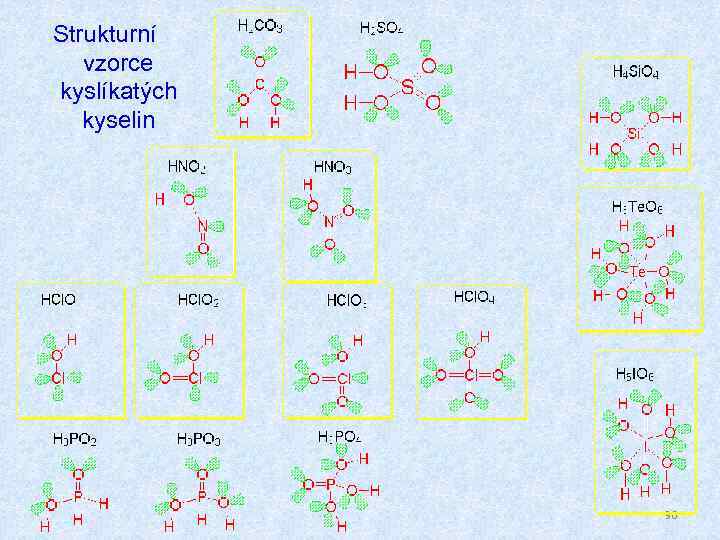 Strukturní vzorce kyslíkatých kyselin 96
Strukturní vzorce kyslíkatých kyselin 96
 Názvosloví krystalohydrátů Krystalohydráty = soli, které krystalizují z vodného roztoku tak, že váží určitý počet molekul VODY. Počet molekul vody se vyjadřuje: 1. V NÁZVU: Před názvem soli číselným údajem (mono-, di-, tri -…) a předpony hydrát. 2. VE VZORCI: . H 2 O Příklady: Cu. SO 4. 5 H 2 O Fe. SO 4. 7 H 2 O Zn. SO 4. 2 H 2 O Ca. SO 4. 2 H 2 O Pentahydrát síranu měďnatého Heptahydrát síranu železnatého Dihydrát síranu zinečnatého Dihydrát síranu vápenatého 97
Názvosloví krystalohydrátů Krystalohydráty = soli, které krystalizují z vodného roztoku tak, že váží určitý počet molekul VODY. Počet molekul vody se vyjadřuje: 1. V NÁZVU: Před názvem soli číselným údajem (mono-, di-, tri -…) a předpony hydrát. 2. VE VZORCI: . H 2 O Příklady: Cu. SO 4. 5 H 2 O Fe. SO 4. 7 H 2 O Zn. SO 4. 2 H 2 O Ca. SO 4. 2 H 2 O Pentahydrát síranu měďnatého Heptahydrát síranu železnatého Dihydrát síranu zinečnatého Dihydrát síranu vápenatého 97


