Загрязнение окружающей среды воздуха и воды.ppt
- Количество слайдов: 45
 ЗАГРЯЗНЕНИЯ ОКРУЖАЮЩЕЙ СРЕДЫ • ЗАГРЯЗНЕНИЕ - ЭТО ПРИВНЕСЕНИЕ В ЭКОЛОГИЧЕСКУЮ СИСТЕМУ НОВЫХ, НЕ ХАРАКТЕРНЫХ ДЛЯ НЕЕ ФИЗИЧЕСКИХ, ХИМИЧЕСКИХ И БИОЛОГИЧЕСКИХ АГЕНТОВ ИЛИ ПРЕВЫШЕНИЕ ЕСТЕСТВЕННОГО СРЕДНЕМНОГОЛЕТНЕГО УРОВНЯ ЭТИХ АГЕНТОВ В ПРИРОДНОЙ СРЕДЕ.
ЗАГРЯЗНЕНИЯ ОКРУЖАЮЩЕЙ СРЕДЫ • ЗАГРЯЗНЕНИЕ - ЭТО ПРИВНЕСЕНИЕ В ЭКОЛОГИЧЕСКУЮ СИСТЕМУ НОВЫХ, НЕ ХАРАКТЕРНЫХ ДЛЯ НЕЕ ФИЗИЧЕСКИХ, ХИМИЧЕСКИХ И БИОЛОГИЧЕСКИХ АГЕНТОВ ИЛИ ПРЕВЫШЕНИЕ ЕСТЕСТВЕННОГО СРЕДНЕМНОГОЛЕТНЕГО УРОВНЯ ЭТИХ АГЕНТОВ В ПРИРОДНОЙ СРЕДЕ.
 ИСТОЧНИКИ ЗАГРЯЗНЕНИЯ • ПРИРОДНОГО ПРОИСХОЖДЕНИЯ • ВУЛКАНЫ • ГЕЙЗЕРЫ • ЛЕСНЫЕ ПОЖАРЫ • ПЫЛЬНЫЕ БУРИ • АНТРОПОГЕННОГО ПРОИСХОЖДЕНИЯ • ПРОМЫШЛЕННЫЕ ПРЕДПРИЯТИЯ • ПРЕДПРИЯТИЯ ТЕПЛОЭНЕРГЕТИЧЕ СКОГО КОМПЛЕКСА • КОММУНАЛЬНОБЫТОВОЕ ХОЗЯЙСТВО • ЖИВОТНОВОДСТВО • ТРАНСПОРТ • СЕЛЬСКОЕ ХОЗЯЙСТВО
ИСТОЧНИКИ ЗАГРЯЗНЕНИЯ • ПРИРОДНОГО ПРОИСХОЖДЕНИЯ • ВУЛКАНЫ • ГЕЙЗЕРЫ • ЛЕСНЫЕ ПОЖАРЫ • ПЫЛЬНЫЕ БУРИ • АНТРОПОГЕННОГО ПРОИСХОЖДЕНИЯ • ПРОМЫШЛЕННЫЕ ПРЕДПРИЯТИЯ • ПРЕДПРИЯТИЯ ТЕПЛОЭНЕРГЕТИЧЕ СКОГО КОМПЛЕКСА • КОММУНАЛЬНОБЫТОВОЕ ХОЗЯЙСТВО • ЖИВОТНОВОДСТВО • ТРАНСПОРТ • СЕЛЬСКОЕ ХОЗЯЙСТВО
 Состав атмосферы Атмосфера – это газовая оболочка Земли, состоящая из Азота – на 78, 08% Кислорода – на 20, 95% Аргона – на 0, 93%, Углекислого газа – на 0, 03% Других газов – на 0, 01%
Состав атмосферы Атмосфера – это газовая оболочка Земли, состоящая из Азота – на 78, 08% Кислорода – на 20, 95% Аргона – на 0, 93%, Углекислого газа – на 0, 03% Других газов – на 0, 01%
 Загрязнение атмосферы • В зависимости от объемов выбросов загрязняющие вещества могут быть массовыми и специфическими. • К массовым загрязнителям относятся: • Диоксид серы • Оксиды азота • Оксид углерода • Углеводороды • Пыль
Загрязнение атмосферы • В зависимости от объемов выбросов загрязняющие вещества могут быть массовыми и специфическими. • К массовым загрязнителям относятся: • Диоксид серы • Оксиды азота • Оксид углерода • Углеводороды • Пыль
 Мировые источники загрязнений атмосферы сосредоточены в индустриально развитых странах Северной Америки, Европы, Восточной Азии. В России – промышленные центры расположены в городах Норильск, Магнитогорск, Липецк, Череповец, Новокузнецк, Нижний Тагил, Москва, Санкт-Петербург, Екатеринбург, Челябинск, Новосибирск, Самара, Омск, Кемерово, Барнаул, Хабаровск, атмосфера загрязняется в результате отсутствия или неэффективной работы очистных установок. Трансграничный перенос аэрополлютантов происходит из Центральной Европы – Украины, Польши, ФРГ, а также Великобритании. Наибольший вклад в загрязнение атмосферы России вносят электроэнергетика, металлургия (особенно цветная), нефтедобыча и нефтепереработка.
Мировые источники загрязнений атмосферы сосредоточены в индустриально развитых странах Северной Америки, Европы, Восточной Азии. В России – промышленные центры расположены в городах Норильск, Магнитогорск, Липецк, Череповец, Новокузнецк, Нижний Тагил, Москва, Санкт-Петербург, Екатеринбург, Челябинск, Новосибирск, Самара, Омск, Кемерово, Барнаул, Хабаровск, атмосфера загрязняется в результате отсутствия или неэффективной работы очистных установок. Трансграничный перенос аэрополлютантов происходит из Центральной Европы – Украины, Польши, ФРГ, а также Великобритании. Наибольший вклад в загрязнение атмосферы России вносят электроэнергетика, металлургия (особенно цветная), нефтедобыча и нефтепереработка.
 ПДК - предельно допустимая концентрация • Количество вредного вещества в окружающей среде, при постоянном контакте или воздействии за определенный промежуток времени практически не влияющее на здоровье человека и не вызывающее неблагоприятных последствий у его потомства
ПДК - предельно допустимая концентрация • Количество вредного вещества в окружающей среде, при постоянном контакте или воздействии за определенный промежуток времени практически не влияющее на здоровье человека и не вызывающее неблагоприятных последствий у его потомства
 Диоксид серы – SO 2 – загрязнитель № 1 • Источники образования: • В природных условиях – извержение вулканов и гейзеров, окисление серы и ее соединений в Мировом океане (до 150 млн. т в год) • В антропогенных условиях - при сжигании сернистых топлив (мазута и угля) (до 300 млн. т в год) • ПДК SO 2=0, 05 мг/куб. м
Диоксид серы – SO 2 – загрязнитель № 1 • Источники образования: • В природных условиях – извержение вулканов и гейзеров, окисление серы и ее соединений в Мировом океане (до 150 млн. т в год) • В антропогенных условиях - при сжигании сернистых топлив (мазута и угля) (до 300 млн. т в год) • ПДК SO 2=0, 05 мг/куб. м
 • Химические реакции в атмосфере: • SO 2 + 0, 5 O 2 → SO 3 – сернистый ангидрид, • SO 3 + H 2 O → H 2 SO 4 – серная кислота • 60% SO 2 превращается в серную кислоту
• Химические реакции в атмосфере: • SO 2 + 0, 5 O 2 → SO 3 – сернистый ангидрид, • SO 3 + H 2 O → H 2 SO 4 – серная кислота • 60% SO 2 превращается в серную кислоту
 Последствия загрязнения SO 2 • Вред здоровью людей – вдыхание диоксида серы в малых концентрациях вызывает неприятный вкус во рту, раздражает слизистые оболочки, приводит к потере аппетита, воспалению дыхательных путей, росту заболевания бронхитом. • Снижение р. Н воды, почвы, что вызывает гибель лесов, рыбы в водоемах, снижается урожайность сельскохозяйственных культур.
Последствия загрязнения SO 2 • Вред здоровью людей – вдыхание диоксида серы в малых концентрациях вызывает неприятный вкус во рту, раздражает слизистые оболочки, приводит к потере аппетита, воспалению дыхательных путей, росту заболевания бронхитом. • Снижение р. Н воды, почвы, что вызывает гибель лесов, рыбы в водоемах, снижается урожайность сельскохозяйственных культур.
 Последствия выпадения кислотных дождей
Последствия выпадения кислотных дождей
 Наносится ущерб коммунальному хозяйству и памятникам архитектуры (мрамор превращается в гипс) SO 2 + H 2 O → H 2 SO 3, H 2 SO 3 + 0, 5 O 2 → H 2 SO 4, H 2 SO 4 + Ca. CO 3 → Ca SO 4 + CO 2 +H 2 O Ca SO 4 + 2 H 2 O → Ca SO 4 * 2 H 2 O
Наносится ущерб коммунальному хозяйству и памятникам архитектуры (мрамор превращается в гипс) SO 2 + H 2 O → H 2 SO 3, H 2 SO 3 + 0, 5 O 2 → H 2 SO 4, H 2 SO 4 + Ca. CO 3 → Ca SO 4 + CO 2 +H 2 O Ca SO 4 + 2 H 2 O → Ca SO 4 * 2 H 2 O
 Образование смога лондонского типа (восстановительный смог) • Условия образования: • • • Высокие концентрации SO 2 Высокая влажность Температура порядка 0 градусов Цельсия • Механизм образования: • • • Твердые частицы (зола, сажа) конденсируют пары воды и образуют микрочастицы тумана Диоксид серы растворяется в капельках тумана с образованием сернистой кислоты Сернистая кислота окисляется кислородом в серную кислоту Образуется кислый, разъедающий все туман В 1952 г. в Лондоне содержание диоксида серы и сернистого ангидрида в воздухе достигло 4 мг/куб. м, что стало причиной гибели более 4000 человек.
Образование смога лондонского типа (восстановительный смог) • Условия образования: • • • Высокие концентрации SO 2 Высокая влажность Температура порядка 0 градусов Цельсия • Механизм образования: • • • Твердые частицы (зола, сажа) конденсируют пары воды и образуют микрочастицы тумана Диоксид серы растворяется в капельках тумана с образованием сернистой кислоты Сернистая кислота окисляется кислородом в серную кислоту Образуется кислый, разъедающий все туман В 1952 г. в Лондоне содержание диоксида серы и сернистого ангидрида в воздухе достигло 4 мг/куб. м, что стало причиной гибели более 4000 человек.
 Меры по снижению концентрации SO 2 • Эффективная работа ГОУ (газоочистных установок) • Обессеривание ископаемого топлива (мазута, каменного угля) • Перевод потребителей топлива на газ • Применение альтернативных видов топлива
Меры по снижению концентрации SO 2 • Эффективная работа ГОУ (газоочистных установок) • Обессеривание ископаемого топлива (мазута, каменного угля) • Перевод потребителей топлива на газ • Применение альтернативных видов топлива
 Оксиды азота - NOx • Источники образования: • В природных условиях – извержение вулканов, лесные пожары, грозовые разряды, а также в почве и поверхностных слоях океана вследствие протекания анаэробных процессов (до 700 млн. т /год). • В антропогенных условиях - производственная деятельность человека (75 млн. т/год) • Процессы горения топлива; • Получение и применение азотной кислоты; • Производство взрывчатых веществ; • Производство азотных удобрений; • Производство анилиновых красителей; • Производство вискозного волокна; • Газовые выбросы химической промышленности
Оксиды азота - NOx • Источники образования: • В природных условиях – извержение вулканов, лесные пожары, грозовые разряды, а также в почве и поверхностных слоях океана вследствие протекания анаэробных процессов (до 700 млн. т /год). • В антропогенных условиях - производственная деятельность человека (75 млн. т/год) • Процессы горения топлива; • Получение и применение азотной кислоты; • Производство взрывчатых веществ; • Производство азотных удобрений; • Производство анилиновых красителей; • Производство вискозного волокна; • Газовые выбросы химической промышленности
 Оксиды азота • N 2 O (оксид азота I валентный) • NO (оксид азота II валентный) • NO 2 (диоксид азота, валентность IV)
Оксиды азота • N 2 O (оксид азота I валентный) • NO (оксид азота II валентный) • NO 2 (диоксид азота, валентность IV)
 • N 2 O (оксид азота I валентный) – «веселящий газ» • Малотоксичный бесцветный газ со слабым запахом и сладковатым вкусом • Выделяется из почвы при внесении азотных удобрений • При высоких концентрациях может вызвать удушье (вследствие вытеснения кислорода из легких) • При соотношении 80% N 2 O и 20% О 2 применяется для наркоза • При температурах выше 500 градусов Цельсия разлагается 2 N 2 O → 2 N 2 + O 2
• N 2 O (оксид азота I валентный) – «веселящий газ» • Малотоксичный бесцветный газ со слабым запахом и сладковатым вкусом • Выделяется из почвы при внесении азотных удобрений • При высоких концентрациях может вызвать удушье (вследствие вытеснения кислорода из легких) • При соотношении 80% N 2 O и 20% О 2 применяется для наркоза • При температурах выше 500 градусов Цельсия разлагается 2 N 2 O → 2 N 2 + O 2
 NO (оксид азота II валентный) • Бесцветный токсичный газ образуется при сгорании ископаемого топлива • ПДК = 0, 06 мг/куб. м • Легко окисляется кислородом и озоном
NO (оксид азота II валентный) • Бесцветный токсичный газ образуется при сгорании ископаемого топлива • ПДК = 0, 06 мг/куб. м • Легко окисляется кислородом и озоном
 NO 2 (диоксид азота, валентность IV) • Токсичный газ бурого цвета • Образуется при сгорании ископаемого топлива • ПДК = 0, 04 мг/куб. м • Растворяется в воде с образованием азотной и азотистой кислот (40% оксида превращается в кислоту) • 2 NO 2 + H 2 O → HNO 3 + HNO 2
NO 2 (диоксид азота, валентность IV) • Токсичный газ бурого цвета • Образуется при сгорании ископаемого топлива • ПДК = 0, 04 мг/куб. м • Растворяется в воде с образованием азотной и азотистой кислот (40% оксида превращается в кислоту) • 2 NO 2 + H 2 O → HNO 3 + HNO 2
 Последствия загрязнения NOx • Отрицательное влияние на здоровье человека (неблагоприятная реакция с гемоглобином) • Закисление воды, почвы • Разрушение озонового слоя (1 молекула оксида азота может уничтожить 10 молекул озона) • Образование смога лос-анджелесского типа (фотохимический смог)
Последствия загрязнения NOx • Отрицательное влияние на здоровье человека (неблагоприятная реакция с гемоглобином) • Закисление воды, почвы • Разрушение озонового слоя (1 молекула оксида азота может уничтожить 10 молекул озона) • Образование смога лос-анджелесского типа (фотохимический смог)
 Образование смога лос-анджелесского типа (фотохимический смог) • Условия возникновения: • Наличие в воздухе углеводородов • Высокая солнечная активность • Температура воздуха 20 -25 градусов Цельсия
Образование смога лос-анджелесского типа (фотохимический смог) • Условия возникновения: • Наличие в воздухе углеводородов • Высокая солнечная активность • Температура воздуха 20 -25 градусов Цельсия
 Смог вызывает резь в глазах, раздражает легочную ткань, влияет на сердечнососудистую систему человека
Смог вызывает резь в глазах, раздражает легочную ткань, влияет на сердечнососудистую систему человека
 Меры по снижению концентрации NOx • Эффективная работа ГОУ (газоочистных установок) • Применение альтернативных видов топлива
Меры по снижению концентрации NOx • Эффективная работа ГОУ (газоочистных установок) • Применение альтернативных видов топлива
 Оксид углерода – СО ядовитый газ без цвета и запаха • Источники образования: • В природных условиях –лесные пожары, выделения океанов, неполное окисление органики (до 32 млн. т /год). • В антропогенных условиях • производственная деятельность - тепловые электростанции, металлургическая и химическая промышленности (150 млн. т в год) • Автотранспорт (460 млн. т/год) • ПДК = 1 мг/куб. м
Оксид углерода – СО ядовитый газ без цвета и запаха • Источники образования: • В природных условиях –лесные пожары, выделения океанов, неполное окисление органики (до 32 млн. т /год). • В антропогенных условиях • производственная деятельность - тепловые электростанции, металлургическая и химическая промышленности (150 млн. т в год) • Автотранспорт (460 млн. т/год) • ПДК = 1 мг/куб. м
 Последствия загрязнения СО • Рост сердечно-сосудистых заболеваний (стенокардия, поражение коронарных сосудов, атеросклероз) • Поражение нервной системы • При содержании в воздухе больших концентраций СО уменьшается доступ кислорода к тканям организма, что вызывает кислородное голодание и смерть.
Последствия загрязнения СО • Рост сердечно-сосудистых заболеваний (стенокардия, поражение коронарных сосудов, атеросклероз) • Поражение нервной системы • При содержании в воздухе больших концентраций СО уменьшается доступ кислорода к тканям организма, что вызывает кислородное голодание и смерть.
 Углеводороды (CH 4 и другие) • Природные источники (2 млрд. 600 млн. тонн в год) • разложение органики (болотные выделения и выделения рисовых полей, свалок, при жизнедеятельности жвачных животных), • лесные пожары, • месторождения каменного угля, нефти • Антропогенные источники (80 млн. тонн в год) • Промышленность – нефтяная, газовая, нефтехимическая • Автотранспорт • ПДК для углеводородов – от 150 до 300 мг/куб. м
Углеводороды (CH 4 и другие) • Природные источники (2 млрд. 600 млн. тонн в год) • разложение органики (болотные выделения и выделения рисовых полей, свалок, при жизнедеятельности жвачных животных), • лесные пожары, • месторождения каменного угля, нефти • Антропогенные источники (80 млн. тонн в год) • Промышленность – нефтяная, газовая, нефтехимическая • Автотранспорт • ПДК для углеводородов – от 150 до 300 мг/куб. м
 Последствия загрязнения углеводородами • Метан способствует усилению парникового эффекта (поглощает инфракрасное излучение нагретой земной поверхности) • Углеводороды способствуют образованию фотохимического смога
Последствия загрязнения углеводородами • Метан способствует усилению парникового эффекта (поглощает инфракрасное излучение нагретой земной поверхности) • Углеводороды способствуют образованию фотохимического смога
 Пыль • Природные источники • Космическая пыль (от 2 до 5 млн. тонн в год) • Земная пыль (3 млрд. 760 млн. тонн в год) органического и неорганического происхождения • Разрушение и выветривание горных пород и почвы • Вулканические извержения • Лесные, степные, торфяные пожары • Пыльные бури • Частицы соли, образующиеся при высыхании мельчайших капель морской и океанической воды • Антропогенные источники (2, 4 млрд. тонн в год) • Промышленность – горнорудная, металлургическая, угольная, деревообрабатывающая, производство автомобильных шин и резиновых технических изделий, технического углерода, цемента. • Минеральных удобрений • Тепловые электростанции • Строительство • ПДК для пыли – 0, 5 мг/куб. м
Пыль • Природные источники • Космическая пыль (от 2 до 5 млн. тонн в год) • Земная пыль (3 млрд. 760 млн. тонн в год) органического и неорганического происхождения • Разрушение и выветривание горных пород и почвы • Вулканические извержения • Лесные, степные, торфяные пожары • Пыльные бури • Частицы соли, образующиеся при высыхании мельчайших капель морской и океанической воды • Антропогенные источники (2, 4 млрд. тонн в год) • Промышленность – горнорудная, металлургическая, угольная, деревообрабатывающая, производство автомобильных шин и резиновых технических изделий, технического углерода, цемента. • Минеральных удобрений • Тепловые электростанции • Строительство • ПДК для пыли – 0, 5 мг/куб. м
 Значение пыли • • Положительное Поглощает прямую солнечную радиацию, защищает живые организмы от ее вредного влияния Рассеивает прямые солнечные лучи, создает более равномерное освещение поверхности Земли Способствует конденсации в атмосфере водяных паров и образованию осадков • Отрицательное Физическое загрязнение растений, поверхности почвы Усиление «парникового» эффекта Способствует образованию смога лондонского типа
Значение пыли • • Положительное Поглощает прямую солнечную радиацию, защищает живые организмы от ее вредного влияния Рассеивает прямые солнечные лучи, создает более равномерное освещение поверхности Земли Способствует конденсации в атмосфере водяных паров и образованию осадков • Отрицательное Физическое загрязнение растений, поверхности почвы Усиление «парникового» эффекта Способствует образованию смога лондонского типа
 Самоочищение и вторичное загрязнение атмосферы • Если в результате физико-химических превращений происходит образование менее вредных веществ и их последующее вымывание атмосферными осадками, то такой процесс называют самоочищением атмосферы. • Если в результате физико-химических превращений или взаимодействий вредных веществ друг с другом образовались более вредные вещества, то такой процесс называют вторичным загрязнением атмосферы
Самоочищение и вторичное загрязнение атмосферы • Если в результате физико-химических превращений происходит образование менее вредных веществ и их последующее вымывание атмосферными осадками, то такой процесс называют самоочищением атмосферы. • Если в результате физико-химических превращений или взаимодействий вредных веществ друг с другом образовались более вредные вещества, то такой процесс называют вторичным загрязнением атмосферы
 • Пример самоочищения • H 2 S + 1, 5 O 2 → H 2 O +SO 2 • ПДК H 2 S = 0, 008 мг/куб. м • ПДК SO 2 = 0, 05 мг/куб. м • SO 2 + H 2 O → H 2 SO 3 • H 2 SO 3 + 0, 5 O 2 → H 2 SO 4 • Во время дождя водяной пар с серной кислотой вымывается из атмосферы
• Пример самоочищения • H 2 S + 1, 5 O 2 → H 2 O +SO 2 • ПДК H 2 S = 0, 008 мг/куб. м • ПДК SO 2 = 0, 05 мг/куб. м • SO 2 + H 2 O → H 2 SO 3 • H 2 SO 3 + 0, 5 O 2 → H 2 SO 4 • Во время дождя водяной пар с серной кислотой вымывается из атмосферы
 Пример вторичного загрязнения атмосферы • Образование озона в воздухе в присутствии диоксида азота с последующим их взаимодействием с углеводородами с последующим образованием фотохимического смога • Разложение молекул хлорфторуглеводородов в озоновом слое с выделением радикала хлора, интенсивно разрушающего молекулы озона.
Пример вторичного загрязнения атмосферы • Образование озона в воздухе в присутствии диоксида азота с последующим их взаимодействием с углеводородами с последующим образованием фотохимического смога • Разложение молекул хлорфторуглеводородов в озоновом слое с выделением радикала хлора, интенсивно разрушающего молекулы озона.
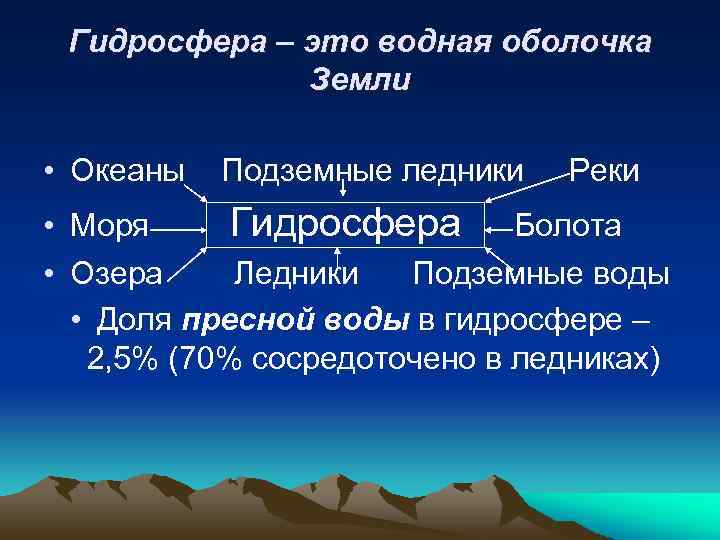 Гидросфера – это водная оболочка Земли • Океаны Подземные ледники Реки • Моря Гидросфера Болота • Озера Ледники Подземные воды • Доля пресной воды в гидросфере – 2, 5% (70% сосредоточено в ледниках)
Гидросфера – это водная оболочка Земли • Океаны Подземные ледники Реки • Моря Гидросфера Болота • Озера Ледники Подземные воды • Доля пресной воды в гидросфере – 2, 5% (70% сосредоточено в ледниках)
 Источники загрязнения гидросферы • 1. Атмосферные осадки (кислотные дожди, фенолы, соли тяжелых металлов, нефтепродукты) • 2. Бытовые (городские) сточные воды (ПАВ – шампунь, мыло, СМС, нитраты, жиры, масла, пищевые отходы, микроорганизмы). • 3. Промышленные сточные воды (металлургическая, химическая, • нефтехимическая, лесохимическая промышленности) • Водоемкость некоторых производств: • На 1 т угля расходуется 0, 6 куб. м воды • На 1 т нефти – 3 куб. м воды • На 1 т стали – 40 куб. м воды • На 1 т синтетического волокна – 300 куб. м воды • На 1 т бумаги- 900 куб. м воды • На 1 т резины – 2300 куб. м воды Для охлаждения энергоблоков мощностью 1 ГВт ТЭС – 1, 2 - 1, 6 куб. км воды в год, АЭС – до 3 куб. км в год.
Источники загрязнения гидросферы • 1. Атмосферные осадки (кислотные дожди, фенолы, соли тяжелых металлов, нефтепродукты) • 2. Бытовые (городские) сточные воды (ПАВ – шампунь, мыло, СМС, нитраты, жиры, масла, пищевые отходы, микроорганизмы). • 3. Промышленные сточные воды (металлургическая, химическая, • нефтехимическая, лесохимическая промышленности) • Водоемкость некоторых производств: • На 1 т угля расходуется 0, 6 куб. м воды • На 1 т нефти – 3 куб. м воды • На 1 т стали – 40 куб. м воды • На 1 т синтетического волокна – 300 куб. м воды • На 1 т бумаги- 900 куб. м воды • На 1 т резины – 2300 куб. м воды Для охлаждения энергоблоков мощностью 1 ГВт ТЭС – 1, 2 - 1, 6 куб. км воды в год, АЭС – до 3 куб. км в год.
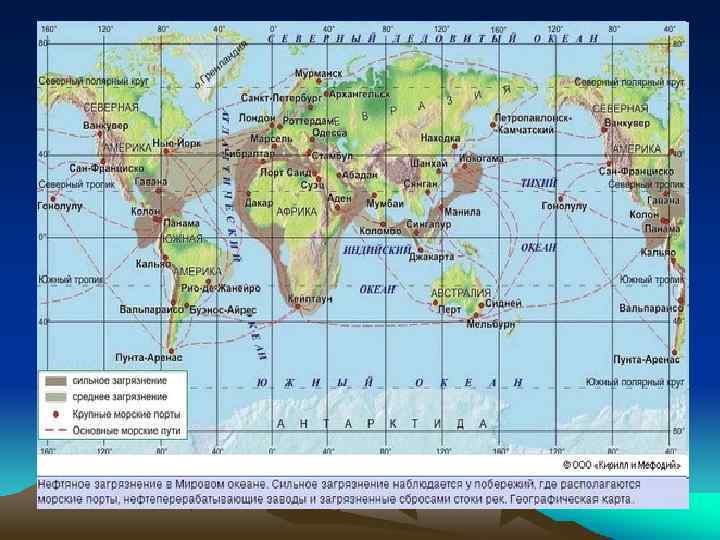
 • 4. Нефть и нефтепродукты (утечки при добыче и транспортировке) • 5. Сточные воды сельского хозяйства (пестициды, минеральные и органические удобрения) • Последствия загрязнения • Недостаток чистой воды, в том числе, питьевой • эвтрофирование и токсикофикация водных объектов • Заболевания людей (болезнь «Минамата» , «Итай-итай» )
• 4. Нефть и нефтепродукты (утечки при добыче и транспортировке) • 5. Сточные воды сельского хозяйства (пестициды, минеральные и органические удобрения) • Последствия загрязнения • Недостаток чистой воды, в том числе, питьевой • эвтрофирование и токсикофикация водных объектов • Заболевания людей (болезнь «Минамата» , «Итай-итай» )
 Способы использования природных вод • Водопользование (разведение и улов рыбы, водный транспорт, гидроэнергетика, отдых на воде) • Водопотребление (нужды сельского хозяйства, промышленности, коммунального хозяйства) • - Это использование воды без ее изъятия из мест естественной локализации • - Это использование воды с ее изъятием из мест локализации с частичным или полным безвозвратным расходованием или с возвратом в водоемы в загрязненном состоянии
Способы использования природных вод • Водопользование (разведение и улов рыбы, водный транспорт, гидроэнергетика, отдых на воде) • Водопотребление (нужды сельского хозяйства, промышленности, коммунального хозяйства) • - Это использование воды без ее изъятия из мест естественной локализации • - Это использование воды с ее изъятием из мест локализации с частичным или полным безвозвратным расходованием или с возвратом в водоемы в загрязненном состоянии
 • Водный объект считается загрязненным, если в результате сброса сточных вод или вредных веществ стал непригодным для частичного или полного водопотребления и водопользования. • ПДК (мг/л или г/л) – это такая концентрация вредных веществ в воде, при превышении которой вода становится непригодной для одного или нескольких видов водопользования и водопотребления
• Водный объект считается загрязненным, если в результате сброса сточных вод или вредных веществ стал непригодным для частичного или полного водопотребления и водопользования. • ПДК (мг/л или г/л) – это такая концентрация вредных веществ в воде, при превышении которой вода становится непригодной для одного или нескольких видов водопользования и водопотребления
 • ПДС (предельно допустимый сброс) – нормативная масса вещества в сточных водах, максимально допустимая к отведению с установленным режимом в данном пункте водного объекта в единицу времени с целью обеспечения норм качества воды в контрольном пункте.
• ПДС (предельно допустимый сброс) – нормативная масса вещества в сточных водах, максимально допустимая к отведению с установленным режимом в данном пункте водного объекта в единицу времени с целью обеспечения норм качества воды в контрольном пункте.
 Загрязнение вод России • Воды делятся на: • 1) нормативно-чистые – условно относится 50% вод России • 2) нормативно-очищенные – 10% от всех вод, низкая эффективность очистных сооружений и их перегруженность • 3) загрязненные – 40%, загрязняются взвешенными веществами, нефтепродуктами, СПАВ, соединениями фосфора, аммонийного азота, фенолами, органическими солями тяжелых металлов
Загрязнение вод России • Воды делятся на: • 1) нормативно-чистые – условно относится 50% вод России • 2) нормативно-очищенные – 10% от всех вод, низкая эффективность очистных сооружений и их перегруженность • 3) загрязненные – 40%, загрязняются взвешенными веществами, нефтепродуктами, СПАВ, соединениями фосфора, аммонийного азота, фенолами, органическими солями тяжелых металлов
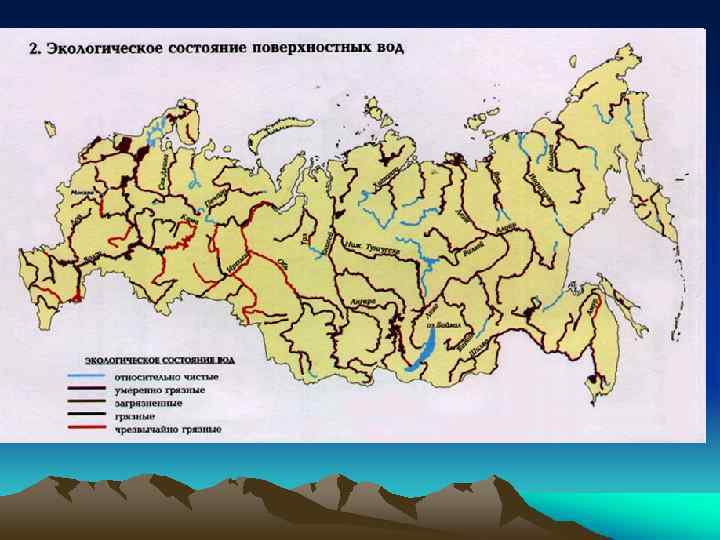
 • Загрязненные реки – Волга, Дон, Урал, Обь, Енисей, Лена, Печора. • Сильно загрязненные – Ока, Кама, Томь, Иртыш, Тобол, Тура. • Морские воды Черноморского побережья от Анапы до Сочи характеризуются классами «загрязненные» и «умеренно загрязненные» , а воды Финского залива Балтийского моря – «грязные» и «очень грязные» . Во многих морях превышены ПДК по нефтяному загрязнению, фенолам, аммонийному азоту, пестицидам, СПАВ, ртути, радиоактивному загрязнению.
• Загрязненные реки – Волга, Дон, Урал, Обь, Енисей, Лена, Печора. • Сильно загрязненные – Ока, Кама, Томь, Иртыш, Тобол, Тура. • Морские воды Черноморского побережья от Анапы до Сочи характеризуются классами «загрязненные» и «умеренно загрязненные» , а воды Финского залива Балтийского моря – «грязные» и «очень грязные» . Во многих морях превышены ПДК по нефтяному загрязнению, фенолам, аммонийному азоту, пестицидам, СПАВ, ртути, радиоактивному загрязнению.
 Самоочищение водных объектов • Разрушение загрязняющих веществ в воде под действием физико-химических и биологических процессов с образованием менее вредных продуктов называют самоочищением водных объектов • Самоочищение сопровождается процессами окисления, т. е. , в водных объектах для успешного самоочищения необходимо достаточное количество растворенного кислорода.
Самоочищение водных объектов • Разрушение загрязняющих веществ в воде под действием физико-химических и биологических процессов с образованием менее вредных продуктов называют самоочищением водных объектов • Самоочищение сопровождается процессами окисления, т. е. , в водных объектах для успешного самоочищения необходимо достаточное количество растворенного кислорода.
 Возможность самоочищения в водных объектов определяется через два показателя • ХПК – химическое потребление кислорода – количество кислорода в миллиграммах на 1 литр воды, необходимое для окисления углеродсодержащих веществ - до СО 2 И Н 2 О, азотсодержащих веществ – до нитратов, серосодержащих веществ – до сульфатов, фосфорсодержащих веществ – до фосфатов. Единица измерения – миллиграмм О 2/л.
Возможность самоочищения в водных объектов определяется через два показателя • ХПК – химическое потребление кислорода – количество кислорода в миллиграммах на 1 литр воды, необходимое для окисления углеродсодержащих веществ - до СО 2 И Н 2 О, азотсодержащих веществ – до нитратов, серосодержащих веществ – до сульфатов, фосфорсодержащих веществ – до фосфатов. Единица измерения – миллиграмм О 2/л.
 • БПК – биологическое потребление кислорода – это количество кислорода, израсходованное в определенный промежуток времени (5, 20 суток) на аэробное (кислородное) окисление нестойких органических соединений, содержащихся в воде. • Единица измерения – миллиграмм О 2/л.
• БПК – биологическое потребление кислорода – это количество кислорода, израсходованное в определенный промежуток времени (5, 20 суток) на аэробное (кислородное) окисление нестойких органических соединений, содержащихся в воде. • Единица измерения – миллиграмм О 2/л.
 • Но процессы самоочищения в водной среде проходят медленнее, чем в атмосферном воздухе по следующим причинам: • - источники загрязнения вод более разнообразны; • - физико-химические процессы в воде сильно замедлены из-за ее высокой вязкости и затруднения диффузионных и кинетических процессов; • - воздействие загрязнений на объекты водной среды оказывает сильное воздействие на многие естественные процессы. • Последствия загрязнения – накопление в воде солей тяжелых металлов, нитратов, сульфатов, органических веществ, приводящие к эвтрофированию и токсикофикации.
• Но процессы самоочищения в водной среде проходят медленнее, чем в атмосферном воздухе по следующим причинам: • - источники загрязнения вод более разнообразны; • - физико-химические процессы в воде сильно замедлены из-за ее высокой вязкости и затруднения диффузионных и кинетических процессов; • - воздействие загрязнений на объекты водной среды оказывает сильное воздействие на многие естественные процессы. • Последствия загрязнения – накопление в воде солей тяжелых металлов, нитратов, сульфатов, органических веществ, приводящие к эвтрофированию и токсикофикации.


