Бензол 2.ppt
- Количество слайдов: 28

Загадка бензола профессор СПб. ГУ, доктор химических наук Карцова Анна Алексеевна Санкт-Петербург 2010

2 1825 г. Майкл Фарадей из светильного газа С 6 Н 6 «карбюрированный водород»

Майкл Фарадей (1791 - 1867) v. Английский физик и химик, v член Лондонского королевского общества. v Один из основателей количественной электрохимии. 1823 г. впервые получил жидкие хлор, сероводород, оксид углерода(IV), аммиак, оксид азота(IV). 1825 г. - открыл бензол, изучил его физические и химические свойства. v. Положил начало исследованиям каучука. 1833 - 1836 гг. - установил количественные законы электролиза. 3

1825 г. Майкл Фарадей из светильного газа С 6 Н 6 «карбюрированный водород» Митчерлих «бензин» О. Лоран «фенол» (греч. «файно» - «освещать» ) С 6 Н 5 – «фенил» Либих - «бензол» 4

Бензол. Физические свойства Бесцветная, летучая жидкость Температура кипения +80 °С Плотность 0, 86 г/см 3 Tпл = +5, 50 С C 6 H 6 Тпл (толуола) = - 950 С C 6 H 5–CH 3 Горит коптящим пламенем «С» =93% Характерный запах! 5

«…Я сидел и писал учебник, но работа продвигалась плохо. Я подвинул мое кресло к камину и задремал. Снова атомы запрыгали перед моими глазами… Длинные цепи иногда тесно группировались и поворачивались подобно змеям. Но что это? Одна из змей ухватила свой собственный хвост. И эта фигура завертелась перед моими глазами, как бы насмехаясь надо мной. Как от вспышки молнии, я пробудился. Остаток ночи я провел, обдумывая следствие из гипотезы …» А. Кекуле 6
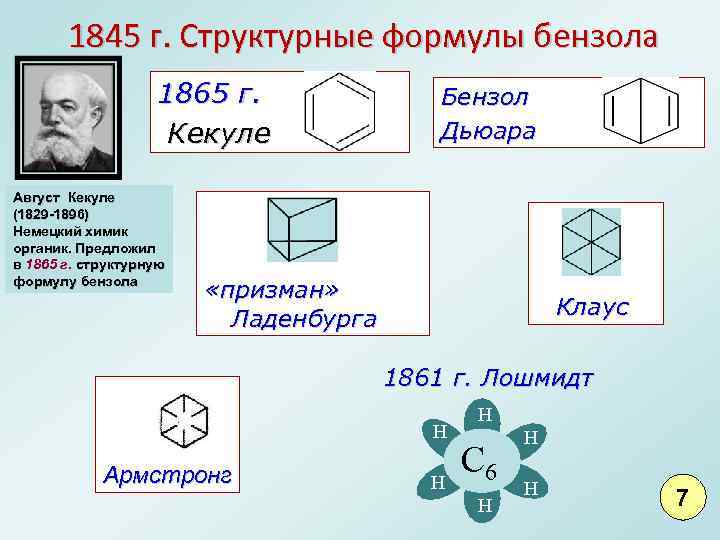
1845 г. Структурные формулы бензола 1865 г. Кекуле Август Кекуле (1829 -1896) Немецкий химик органик. Предложил в 1865 г. структурную формулу бензола Бензол Дьюара «призман» Ладенбурга Клаус 1861 г. Лошмидт Н Армстронг Н Н С 6 Н Н Н 7
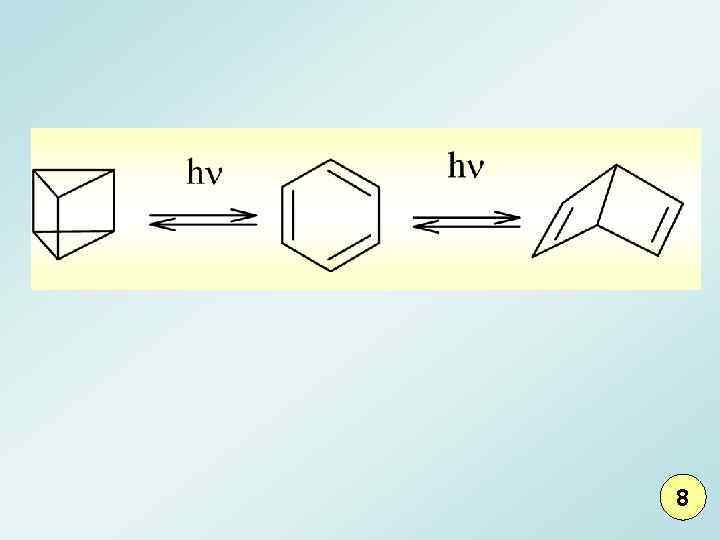
8
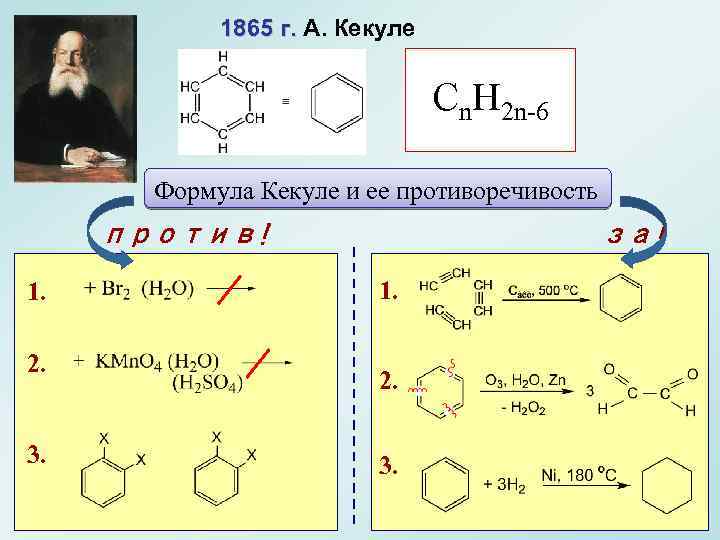
1865 г. А. Кекуле Cn. H 2 n-6 Формула Кекуле и ее противоречивость против! 1. 2. 3. за! 1. 2. 3. 9
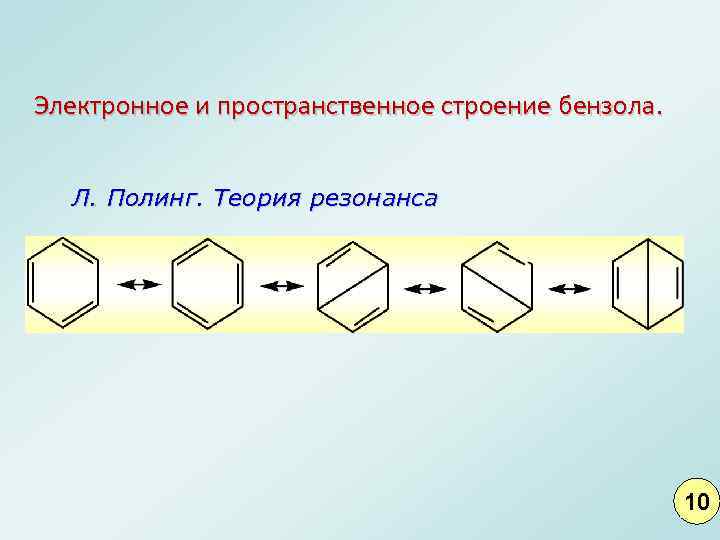
Электронное и пространственное строение бензола. Л. Полинг. Теория резонанса 10
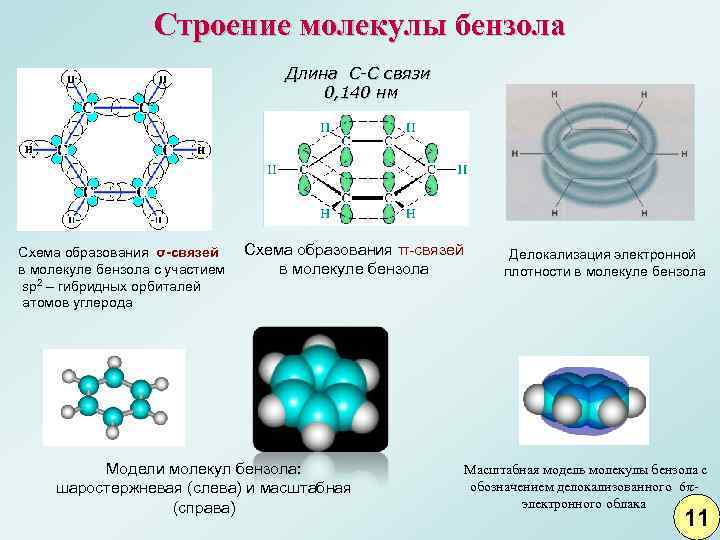
Строение молекулы бензола Длина C-C связи 0, 140 нм Схема образования σ-связей в молекуле бензола с участием sp 2 – гибридных орбиталей атомов углерода Схема образования π-связей в молекуле бензола Модели молекул бензола: шаростержневая (слева) и масштабная (справа) Делокализация электронной плотности в молекуле бензола Масштабная модель молекулы бензола с обозначением делокализованного 6 электронного облака 11
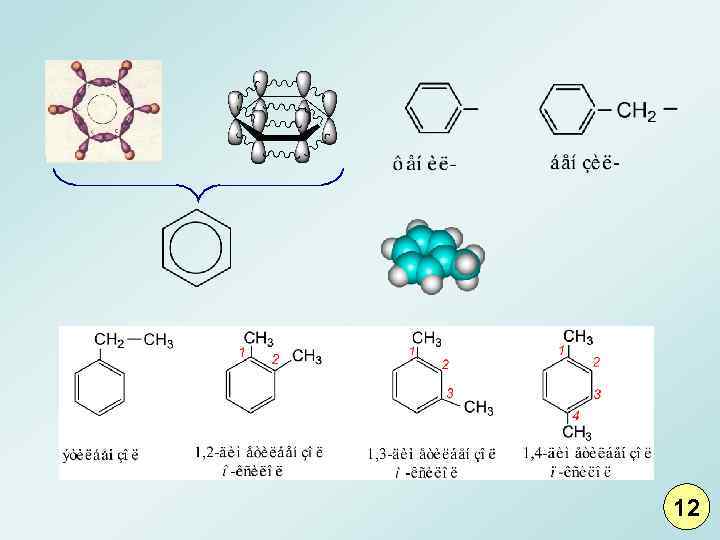
12
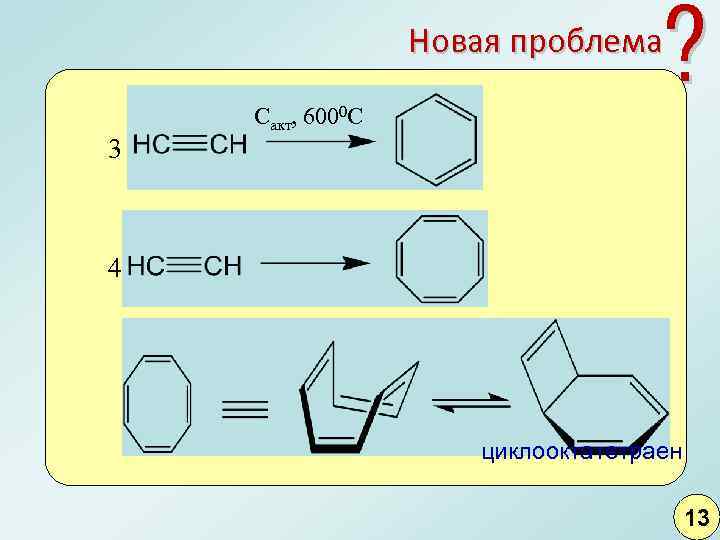
? Новая проблема 3 Сакт, 6000 С 4 циклооктатетраен 13
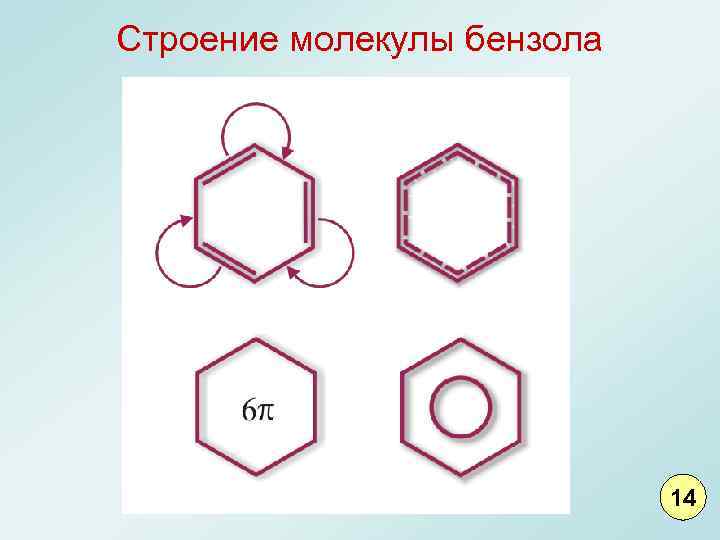
Строение молекулы бензола 14
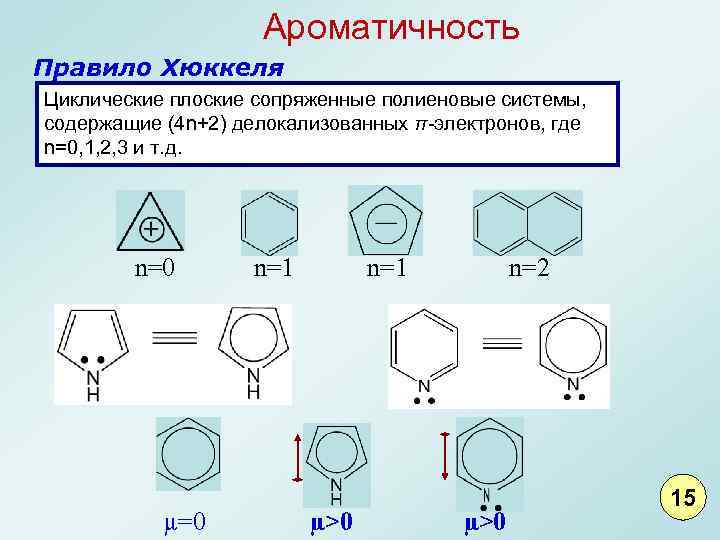
Ароматичность Правило Хюккеля Циклические плоские сопряженные полиеновые системы, содержащие (4 n+2) делокализованных π-электронов, где n=0, 1, 2, 3 и т. д. n=0 µ=0 n=1 µ>0 n=2 µ>0 15
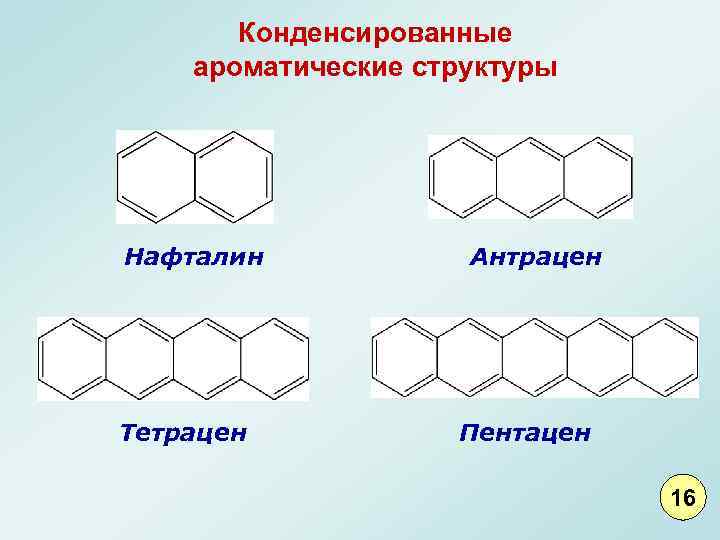
Конденсированные ароматические структуры Нафталин Тетрацен Антрацен Пентацен 16
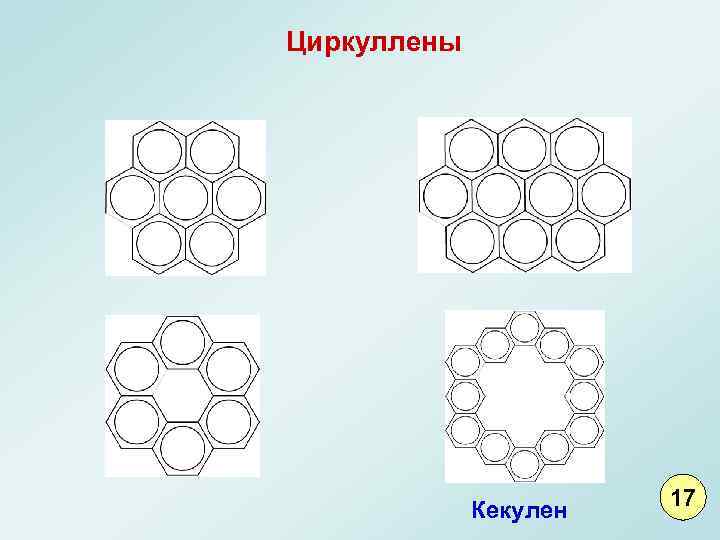
Циркуллены Кекулен 17
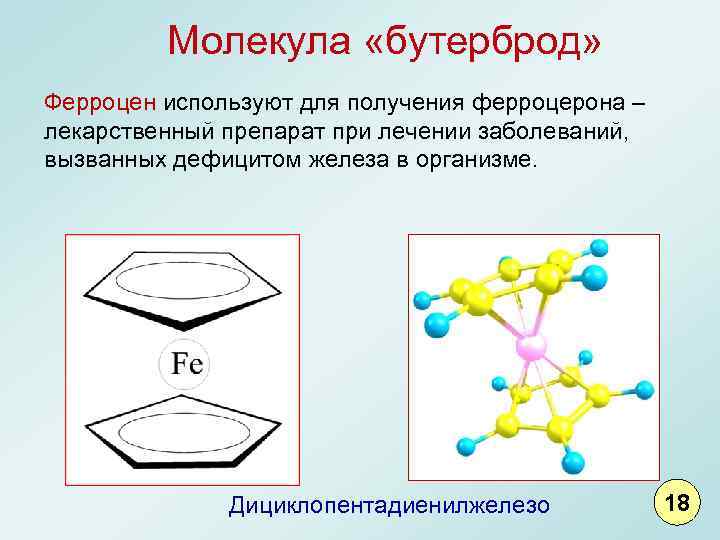
Молекула «бутерброд» Ферроцен используют для получения ферроцерона – лекарственный препарат при лечении заболеваний, вызванных дефицитом железа в организме. Дициклопентадиенилжелезо 18
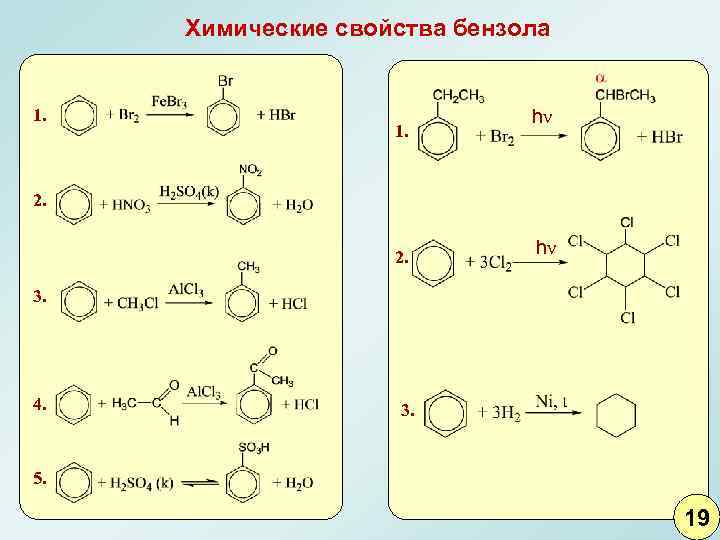
Химические свойства бензола 1. hν 2. 2. hν 3. 4. 3. 5. 19
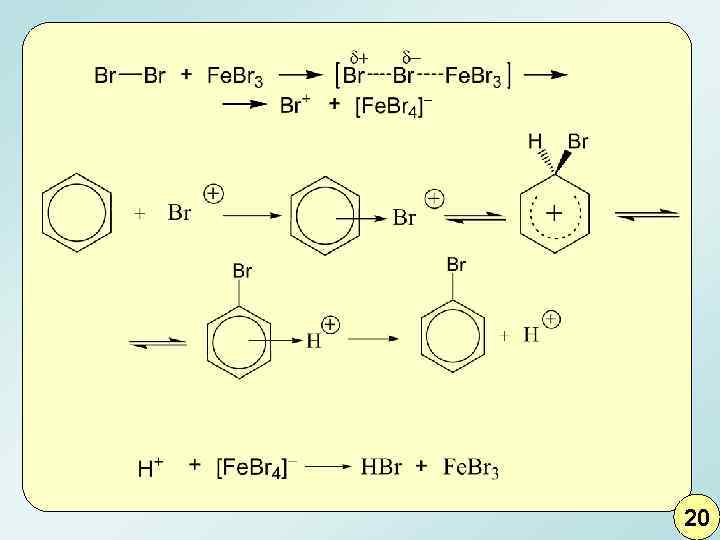
20
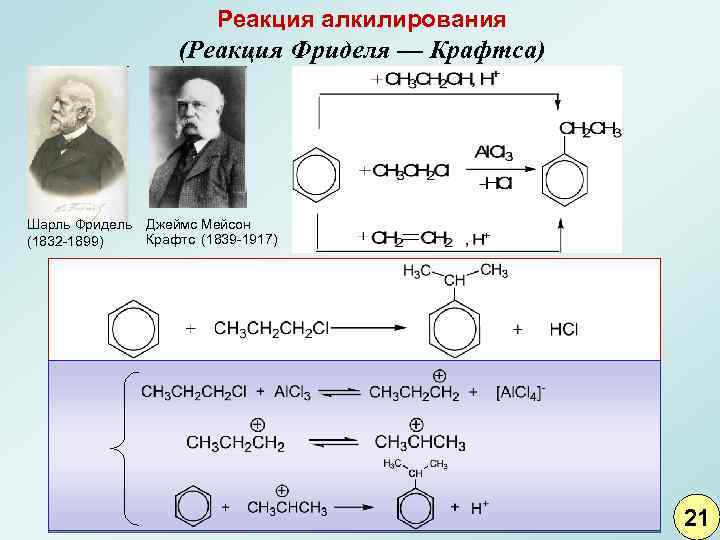
Реакция алкилирования (Реакция Фриделя — Крафтса) Шарль Фридель Джеймс Мейсон Крафтс (1839 -1917) (1832 -1899) 21
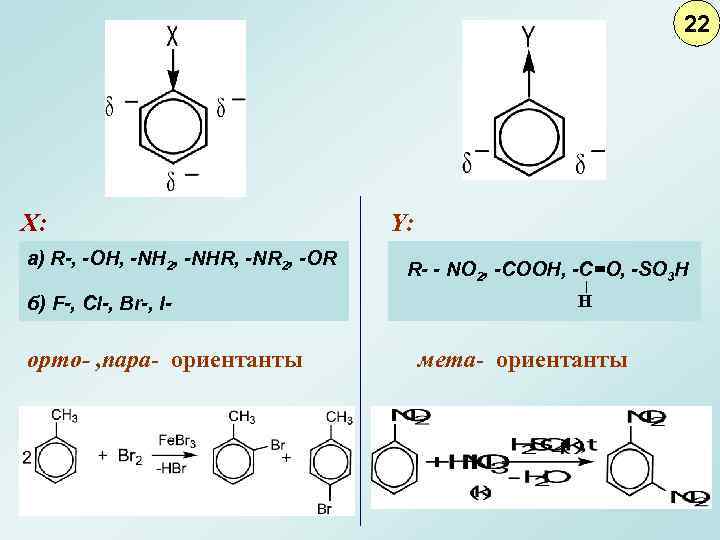
22 X: а) R-, -OH, -NH 2, -NHR, -NR 2, -OR б) F-, Cl-, Br-, I- орто- , пара- ориентанты Y: R- - NO 2, -COOH, -C=O, -SO 3 H H мета- ориентанты
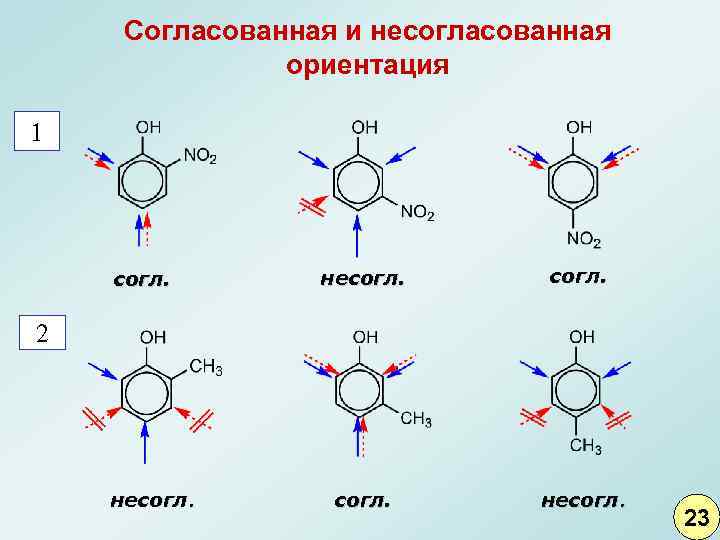
Согласованная и несогласованная ориентация 1 согл. несогл. 23
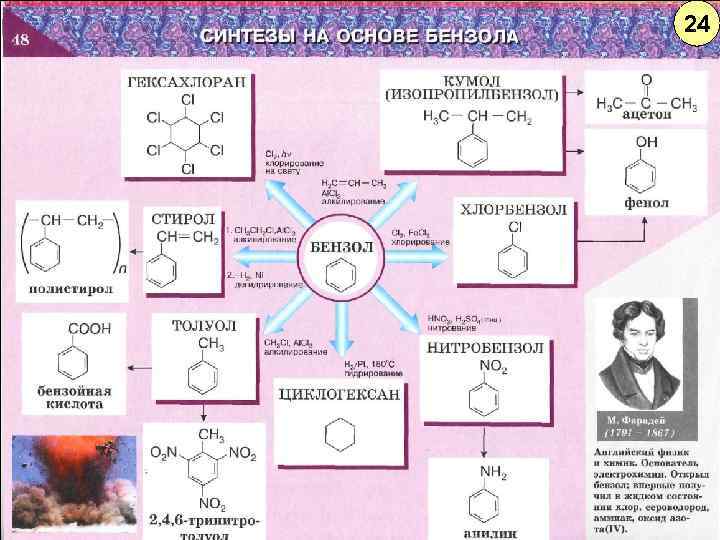
24
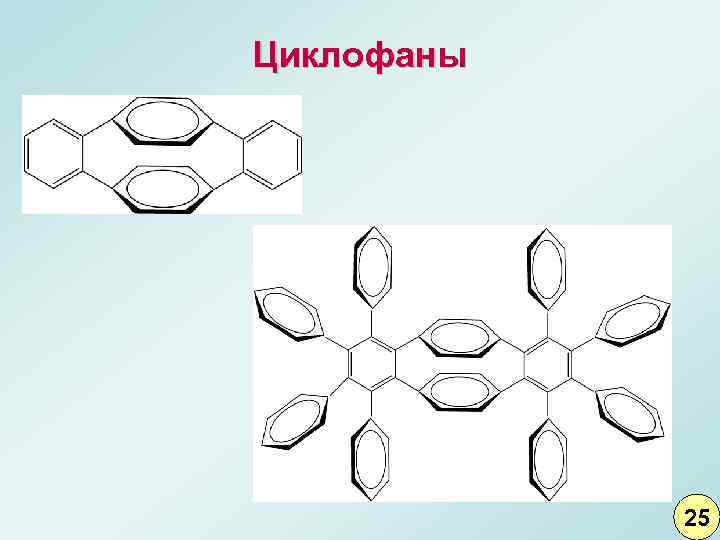
Циклофаны 25
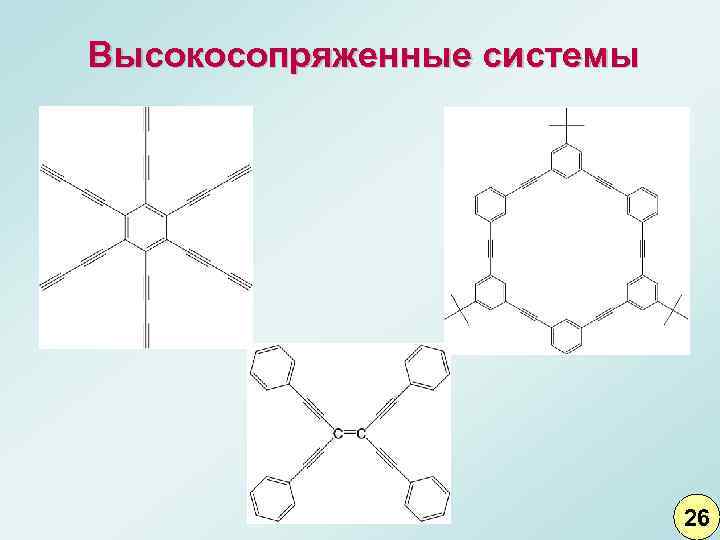
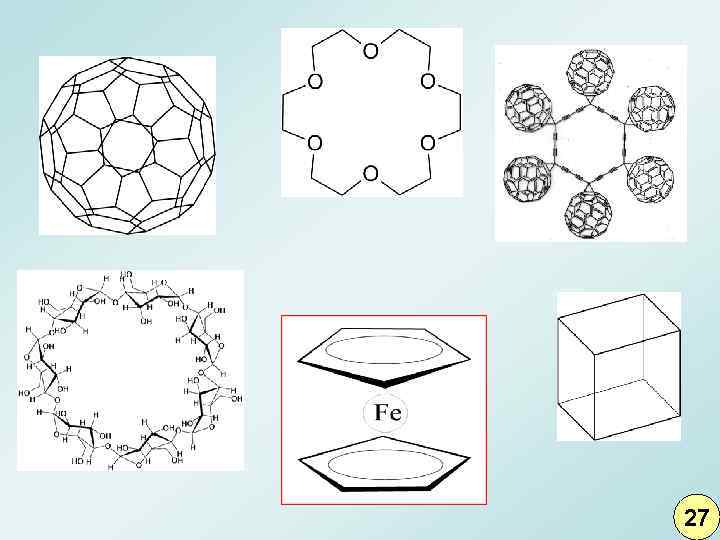
Высокосопряженные системы 26
27

Спасибо за внимание!
Бензол 2.ppt