8e9aa93f0a50ea5c06b6951269454e7a.ppt
- Количество слайдов: 38
 Задание № 1 Определить формулу углеводорода, класса Сn. H 2 n, если плотность его по водороду равна 28 Определить формулу углеводорода, плотность которого по воздуху равна 0, 9655, массовая доля углерода 85, 71%, а водорода 14, 29%
Задание № 1 Определить формулу углеводорода, класса Сn. H 2 n, если плотность его по водороду равна 28 Определить формулу углеводорода, плотность которого по воздуху равна 0, 9655, массовая доля углерода 85, 71%, а водорода 14, 29%

 План урока • Состав и строение алкенов • Номенклатура и изомерия алкенов • Получение алкенов • Химические свойства алкенов • Генетическая связь между УВ
План урока • Состав и строение алкенов • Номенклатура и изомерия алкенов • Получение алкенов • Химические свойства алкенов • Генетическая связь между УВ
 Задачи урока • Закрепить знания о гомологических рядах углеводородов. • Ознакомиться с новым классом УВ –алкены • Продолжить формировать представления о связи строения вещества с его свойствами. • Ознакомиться с химическими свойствами апкенов способами их получения. • Продолжить отрабатывать навыки и умения в составлении названий, написании структурных формул изомеров, уравнений химических реакций. • Закрепить и углубить знания, полученные на предыдущих уроках
Задачи урока • Закрепить знания о гомологических рядах углеводородов. • Ознакомиться с новым классом УВ –алкены • Продолжить формировать представления о связи строения вещества с его свойствами. • Ознакомиться с химическими свойствами апкенов способами их получения. • Продолжить отрабатывать навыки и умения в составлении названий, написании структурных формул изомеров, уравнений химических реакций. • Закрепить и углубить знания, полученные на предыдущих уроках
 Состав алкенов Алкены(олефины, этиленовые УВ) – это УВ, в молекулах которых два атома углерода находятся в состоянии sp 2 гибридизации и связаны друг с другом двойной связью. ОБЩАЯ ФОРМУЛА Cn. H 2 n, где n > 2
Состав алкенов Алкены(олефины, этиленовые УВ) – это УВ, в молекулах которых два атома углерода находятся в состоянии sp 2 гибридизации и связаны друг с другом двойной связью. ОБЩАЯ ФОРМУЛА Cn. H 2 n, где n > 2
 Строение алкенов Двойная связь является сочетанием - и -связей (хотя она изображаетс двумя одинаковыми черточками, всегда следует учитывать их неравноценность).
Строение алкенов Двойная связь является сочетанием - и -связей (хотя она изображаетс двумя одинаковыми черточками, всегда следует учитывать их неравноценность).
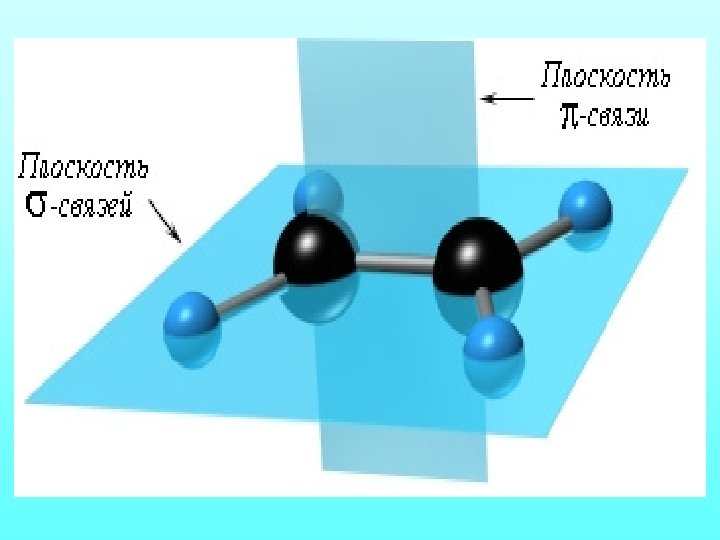
 Строение алкенов -Связь возникает при осевом перекрывании sp 2 -гибридных орбиталей, а -связь – при боковом перекрывании р-орбиталей соседних атомов углерода.
Строение алкенов -Связь возникает при осевом перекрывании sp 2 -гибридных орбиталей, а -связь – при боковом перекрывании р-орбиталей соседних атомов углерода.
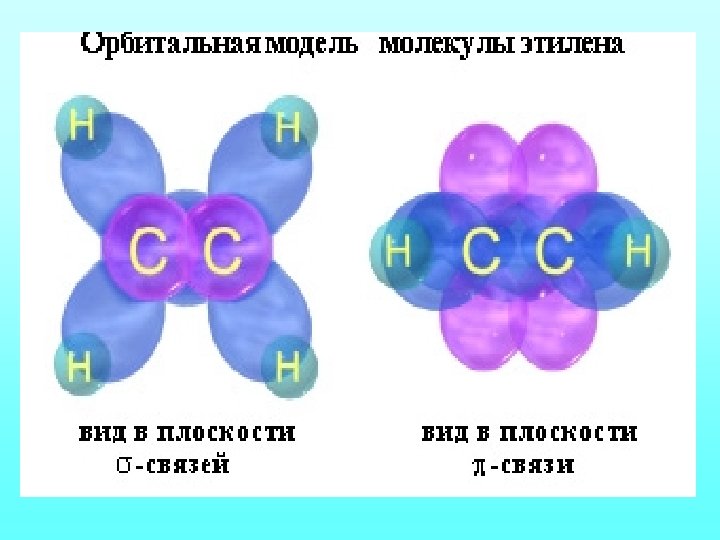
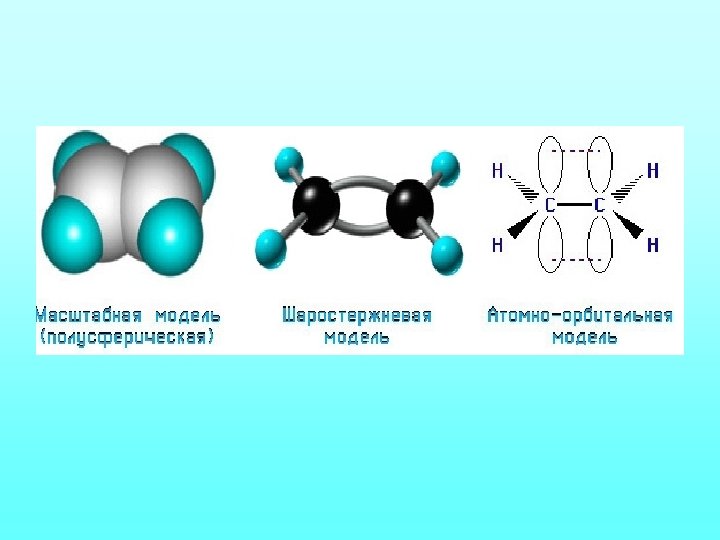
 Строение алкенов Образование связей в молекуле этилена можно изобразить следующей схемой: С=С -связь (перекрывание 2 sp 2 -2 sp 2) и -связь (2 рz-2 рz) С–Н -связь (перекрывание 2 sp 2 -АО углерода и 1 s-АО водорода)
Строение алкенов Образование связей в молекуле этилена можно изобразить следующей схемой: С=С -связь (перекрывание 2 sp 2 -2 sp 2) и -связь (2 рz-2 рz) С–Н -связь (перекрывание 2 sp 2 -АО углерода и 1 s-АО водорода)
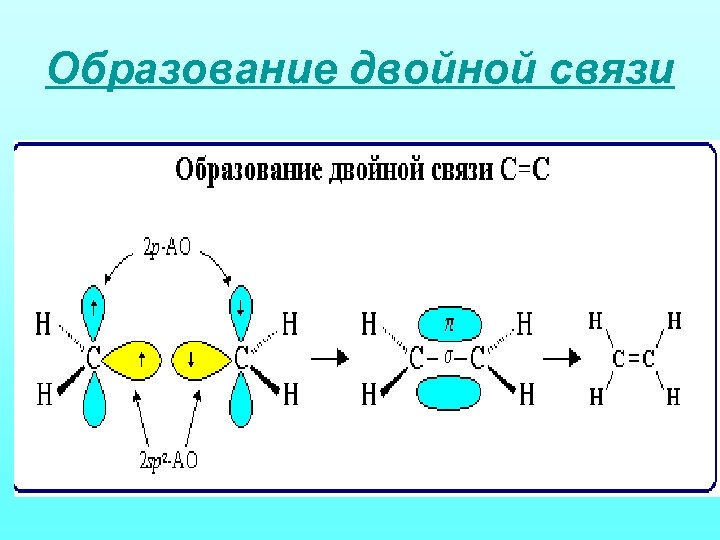 Образование двойной связи
Образование двойной связи
 Номенклатура Название алкена = корень названия ПУВ + суффикс ЕН + локант
Номенклатура Название алкена = корень названия ПУВ + суффикс ЕН + локант
 Номенклатура алкенов • Двойная связь должна входить в главную цепь • Нумерация начинается с той стороны молекулы, ближе к которой находится двойная связь • После корня используется суффикс –ен с указанием положения двойной связи СН 3 -С-СН 2 -СН-СН 3 ║ СН 2 │ СН 3
Номенклатура алкенов • Двойная связь должна входить в главную цепь • Нумерация начинается с той стороны молекулы, ближе к которой находится двойная связь • После корня используется суффикс –ен с указанием положения двойной связи СН 3 -С-СН 2 -СН-СН 3 ║ СН 2 │ СН 3
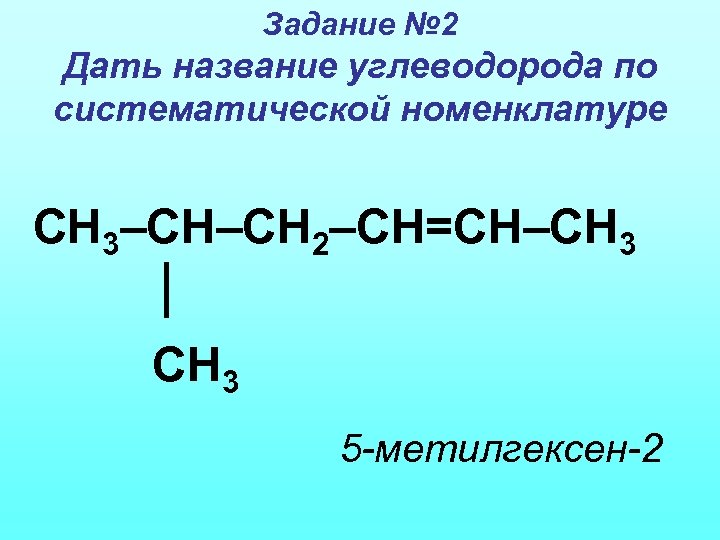 Задание № 2 Дать название углеводорода по систематической номенклатуре СН 3–СН–СН 2–СН=СН–СН 3 5 -метилгексен-2
Задание № 2 Дать название углеводорода по систематической номенклатуре СН 3–СН–СН 2–СН=СН–СН 3 5 -метилгексен-2
 Задание № 3 Построить 4, 5 -диметилгексен-2 Построить 2, 3, 3 -триметилпентен-1 Чем они являются по отношению к другу?
Задание № 3 Построить 4, 5 -диметилгексен-2 Построить 2, 3, 3 -триметилпентен-1 Чем они являются по отношению к другу?
 Изомерия алкенов Структурная: • Углеродного скелета • Положения двойной связи • Межклассовая Пространственная • Геометрическая (цис-транс)
Изомерия алкенов Структурная: • Углеродного скелета • Положения двойной связи • Межклассовая Пространственная • Геометрическая (цис-транс)
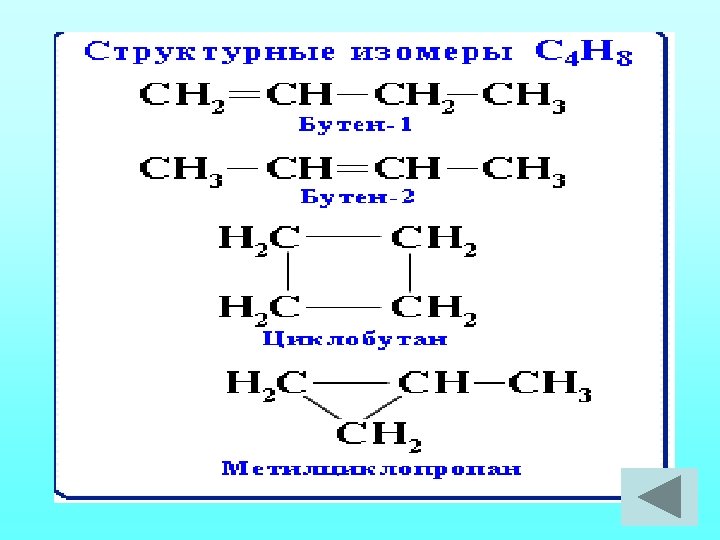
 Задание № 4 Составить все возможные изомеры для углеводорода С 5 Н 10 и дать им названия
Задание № 4 Составить все возможные изомеры для углеводорода С 5 Н 10 и дать им названия
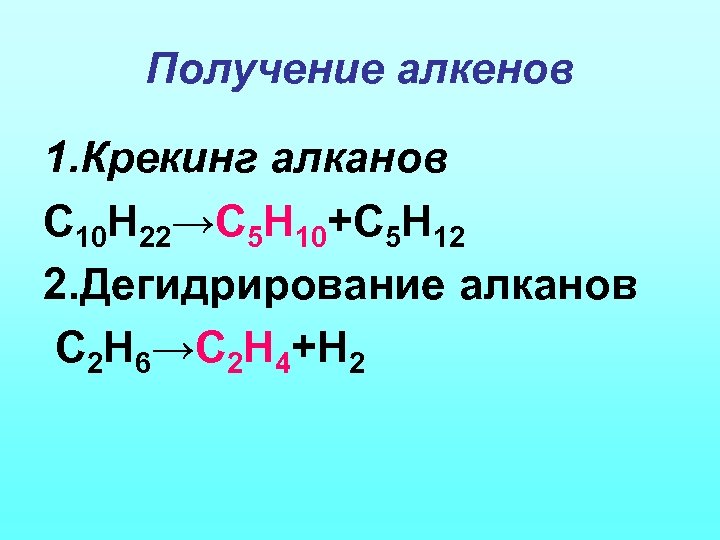 Получение алкенов 1. Крекинг алканов С 10 Н 22→С 5 Н 10+С 5 Н 12 2. Дегидрирование алканов С 2 Н 6→С 2 Н 4+Н 2
Получение алкенов 1. Крекинг алканов С 10 Н 22→С 5 Н 10+С 5 Н 12 2. Дегидрирование алканов С 2 Н 6→С 2 Н 4+Н 2
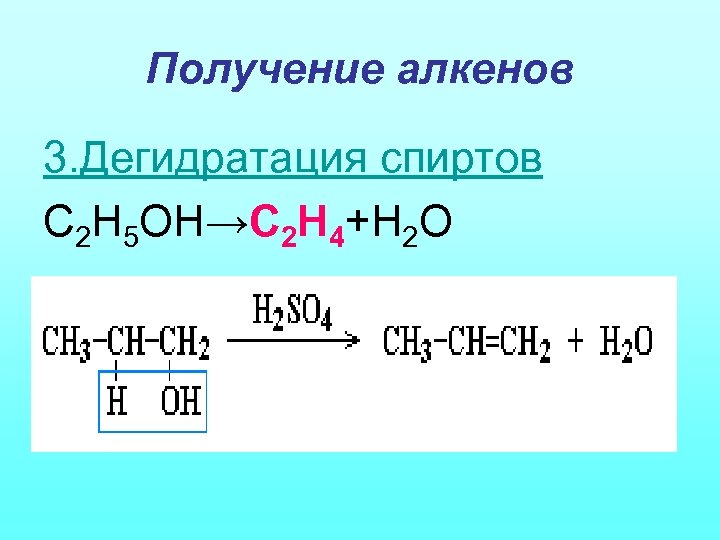 Получение алкенов 3. Дегидратация спиртов С 2 Н 5 ОН→С 2 Н 4+Н 2 О
Получение алкенов 3. Дегидратация спиртов С 2 Н 5 ОН→С 2 Н 4+Н 2 О
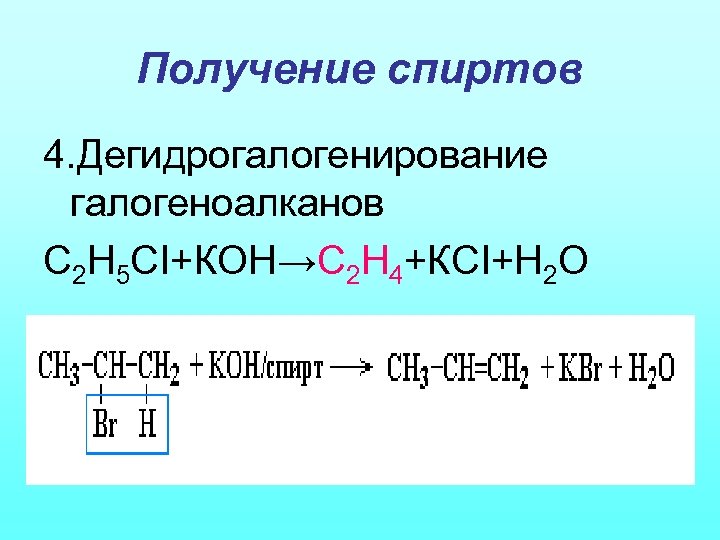 Получение спиртов 4. Дегидрогалогенирование галогеноалканов С 2 Н 5 CI+КОН→С 2 Н 4+КСI+Н 2 О
Получение спиртов 4. Дегидрогалогенирование галогеноалканов С 2 Н 5 CI+КОН→С 2 Н 4+КСI+Н 2 О
 Водород преимущественно отрывается от менее гидрогенезированных атомов углерода
Водород преимущественно отрывается от менее гидрогенезированных атомов углерода
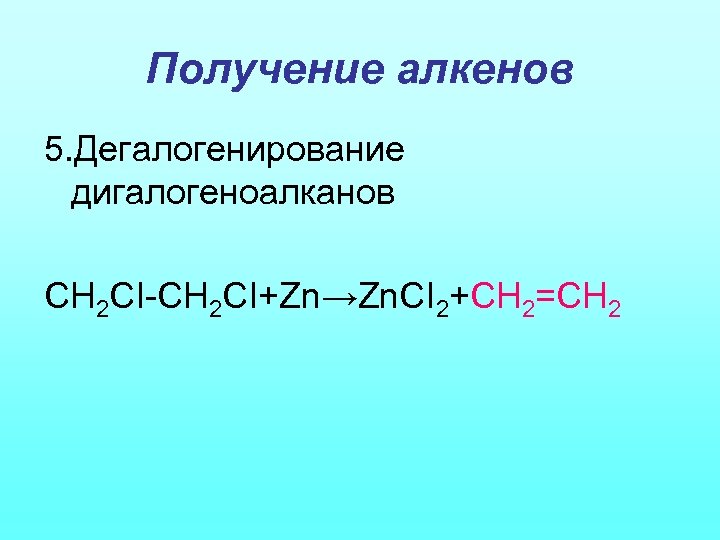 Получение алкенов 5. Дегалогенирование дигалогеноалканов СН 2 CI-CH 2 CI+Zn→Zn. CI 2+CH 2=CH 2
Получение алкенов 5. Дегалогенирование дигалогеноалканов СН 2 CI-CH 2 CI+Zn→Zn. CI 2+CH 2=CH 2
 Задание № 5 Написать уравнения реакций получения: а)пропена из пропана б)пропена из хлорпропана в)бутен-2 из бутанола-2 г)пропена из 1, 2 - дихлорпропана
Задание № 5 Написать уравнения реакций получения: а)пропена из пропана б)пропена из хлорпропана в)бутен-2 из бутанола-2 г)пропена из 1, 2 - дихлорпропана
 Химические свойства Чем объясняются химические свойства алкенов? Химические свойства объясняются наличием -связи, которая легко разрывается, вызывая реакции присоединения и окисления
Химические свойства Чем объясняются химические свойства алкенов? Химические свойства объясняются наличием -связи, которая легко разрывается, вызывая реакции присоединения и окисления
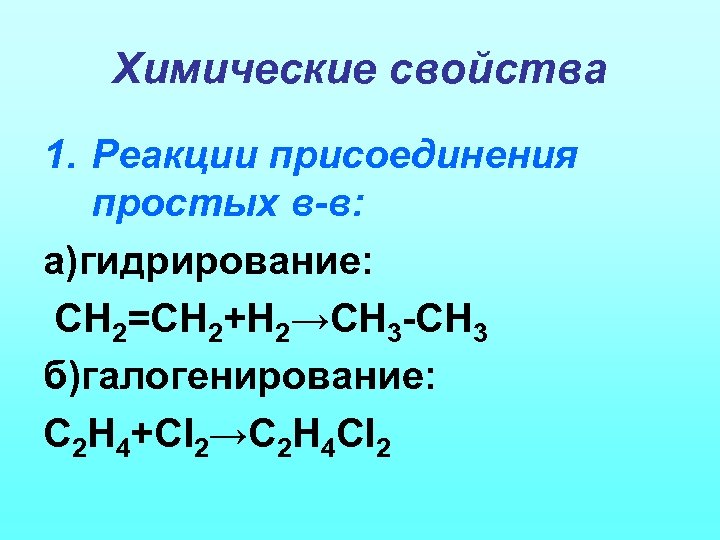 Химические свойства 1. Реакции присоединения простых в-в: а)гидрирование: СН 2=СН 2+Н 2→СН 3 -СН 3 б)галогенирование: С 2 Н 4+CI 2→C 2 H 4 CI 2
Химические свойства 1. Реакции присоединения простых в-в: а)гидрирование: СН 2=СН 2+Н 2→СН 3 -СН 3 б)галогенирование: С 2 Н 4+CI 2→C 2 H 4 CI 2
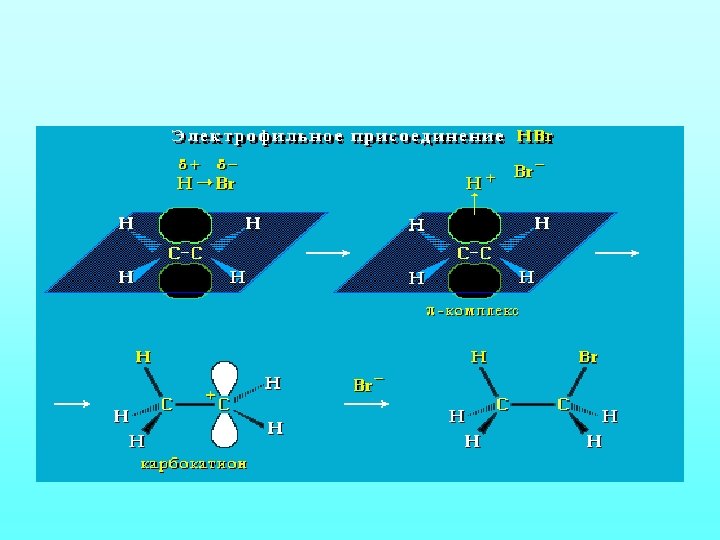
 Химические свойства 2. Присоединение сложных веществ: а)гидратация С 2 Н 4+Н 2 О→С 2 Н 5 ОН б)гидрогалогенирование С 2 Н 4+НBr→C 2 H 5 Br в)реакция полимеризации Правило Марковникова
Химические свойства 2. Присоединение сложных веществ: а)гидратация С 2 Н 4+Н 2 О→С 2 Н 5 ОН б)гидрогалогенирование С 2 Н 4+НBr→C 2 H 5 Br в)реакция полимеризации Правило Марковникова
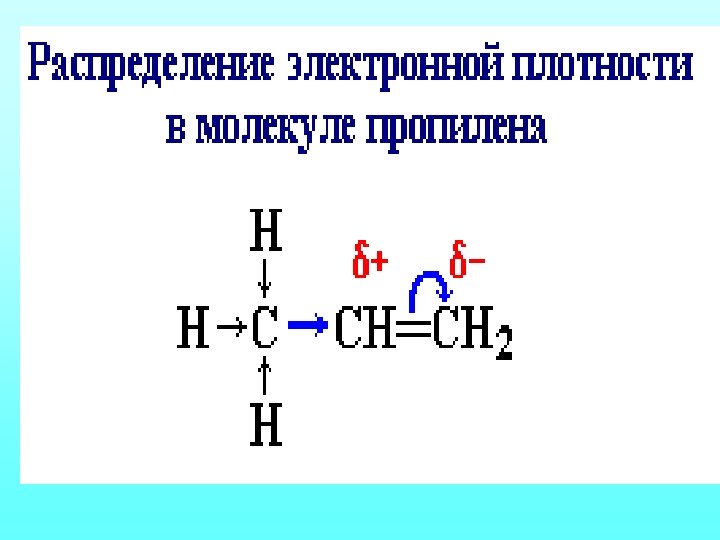
 Реакции окисления. а) алкены горят светящимся пламенем С 2 Н 4+3 О 2→ 2 СО 2+2 Н 2 О
Реакции окисления. а) алкены горят светящимся пламенем С 2 Н 4+3 О 2→ 2 СО 2+2 Н 2 О
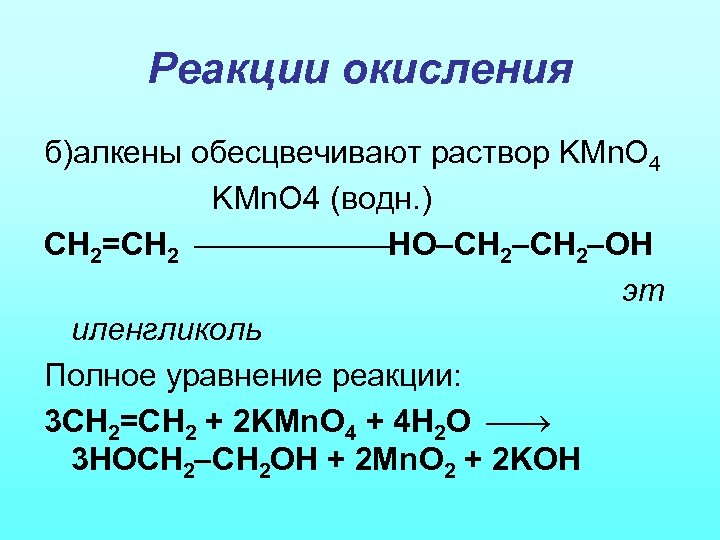 Реакции окисления б)алкены обесцвечивают раствор KMn. O 4 (водн. ) CH 2=CH 2 HO CH 2 OH эт иленгликоль Полное уравнение реакции: 3 CH 2=CH 2 + 2 KMn. O 4 + 4 H 2 O 3 HOCH 2 OH + 2 Mn. O 2 + 2 KOH
Реакции окисления б)алкены обесцвечивают раствор KMn. O 4 (водн. ) CH 2=CH 2 HO CH 2 OH эт иленгликоль Полное уравнение реакции: 3 CH 2=CH 2 + 2 KMn. O 4 + 4 H 2 O 3 HOCH 2 OH + 2 Mn. O 2 + 2 KOH
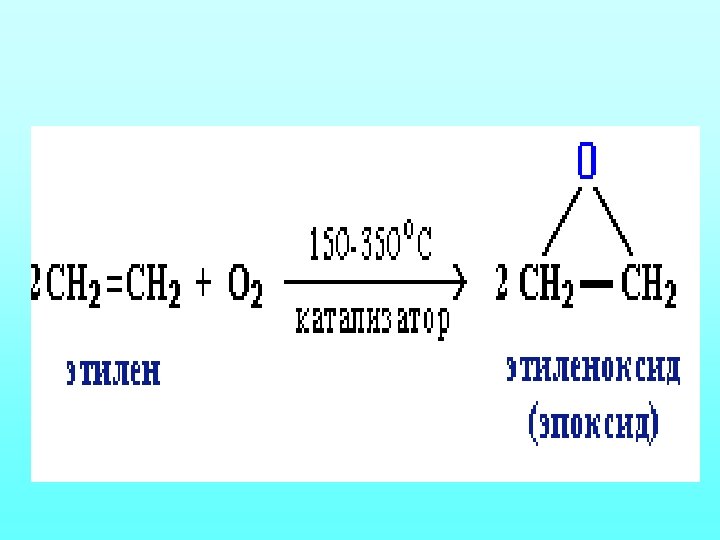
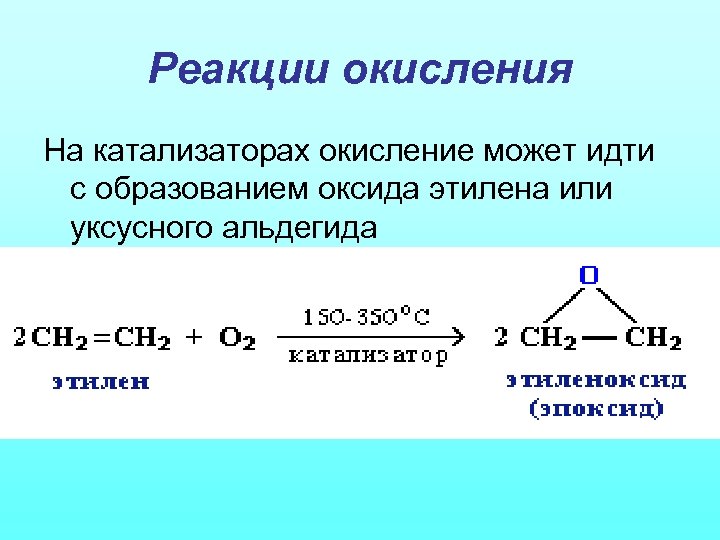 Реакции окисления На катализаторах окисление может идти с образованием оксида этилена или уксусного альдегида
Реакции окисления На катализаторах окисление может идти с образованием оксида этилена или уксусного альдегида
 Задание № 6 1. Как можно распознать этан и этилен? 2. Составьте уравнения реакций, соответствующих схеме: алкан А→? →алкен→алкан А 3. Написать уравнения реакций: а)гидрирование пропена б)гидратация бутен-1 в)гидратация бутен-2 г) горение пропена, бутена
Задание № 6 1. Как можно распознать этан и этилен? 2. Составьте уравнения реакций, соответствующих схеме: алкан А→? →алкен→алкан А 3. Написать уравнения реакций: а)гидрирование пропена б)гидратация бутен-1 в)гидратация бутен-2 г) горение пропена, бутена
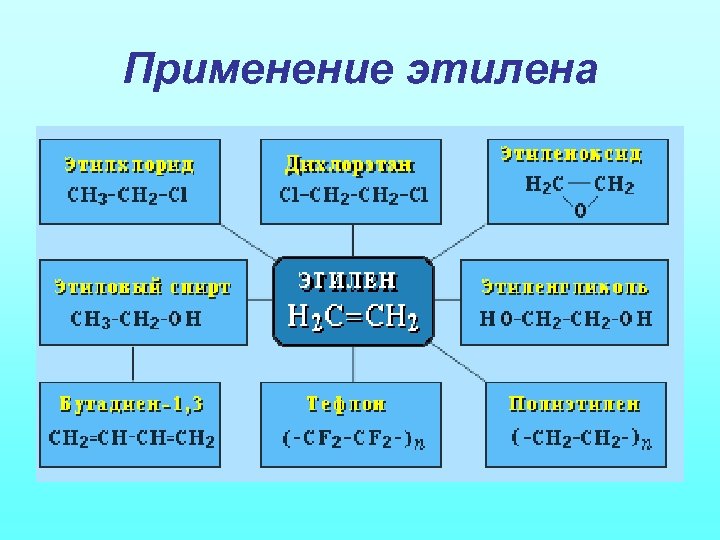 Применение этилена
Применение этилена

 Задание на дом § 12, упражнения: 1, 2, 3, 4
Задание на дом § 12, упражнения: 1, 2, 3, 4