!!!свойства,строение белков.ppt
- Количество слайдов: 119


Задачи: • сформировать понятия: «белки, или протеины» , «аминокислоты» , «денатурация» , «ренатурация» ; • познакомить учащихся со строением, структурной организацией и свойствами белковых молекул.

Химический состав организма человека Несмотря на огромное разнообразие и сложность строения, белки построены из 20 видов различных аминокислот.

Белки обладают огромной молекулярной массой: молекулярная масса альбумина (одного из белков яйца) — 36000, гемоглобина — 152000, миозина (одного из белков мышц) — 500000. Для сравнения: молекулярная масса спирта — 46, уксусной кислоты — 60, бензола — 78.

СЛОВАРЬ Белки (протеи ны, полипепти ды) — высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью аминокислот. Википедия Белки – это нерегулярные полимеры, мономерами которых являются аминокислоты. http: //bannikov. narod. ru/Belok. html

Белки В состав белков входят: С, Н, О, N, S. Часть белков образует комплексы с другими молекулами, содержащими фосфор, железо, цинк и медь. • Белки - (протеины, полипептиды) высокомолекулярные органические соединения, состоящие из остатков аминокислот, соединённых в цепочку пептидной связью. Белки –гетерополимеры, мономерами котрых являются α-аминокислоты.

Белки - сложные высокомолекулярные природные соединения, построенные из остатков α-аминокислот. Аминокислоты в белках связаны пептидными связями. Около 20 видов аминокислот входят в состав белков.

Классификация белков белки простые сложные состоят из кроме аминокислот содержат небелковую остатков простетическую группу: аминокислот атомы металла – металлопротеины молекулу липида – липопротеины молекулу углевода – гликопротеины остаток фосфорной кислоты – фосфопротеины молекулу нуклеиновой кислоты – нуклеопротеины
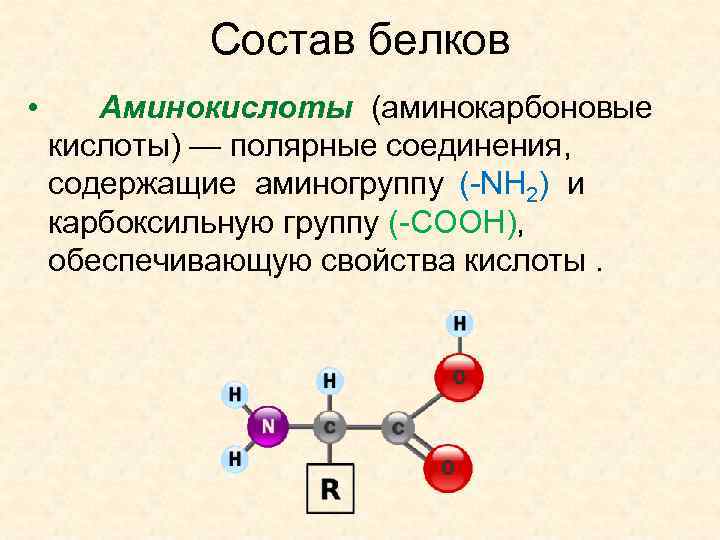
Состав белков • Аминокислоты (аминокарбоновые кислоты) — полярные соединения, содержащие аминогруппу (-NH 2) и карбоксильную группу (-COOH), обеспечивающую свойства кислоты.

Состав белков • В клетках и тканях обнаружено свыше 170 различных аминокислот, но в состав белков входит лишь 26. • Причем 6 из 26 аминокислот являются нестандартными. Они образуются в результате модификации стандартных аминокислот уже после их включения в полипептидную цепь. Поэтому обычными компонентами белков считают лишь 20 аминокислот. Аминокислоты Заменимые синтезируются в организме (10) Незаменимые в организме не синтезируются (10)
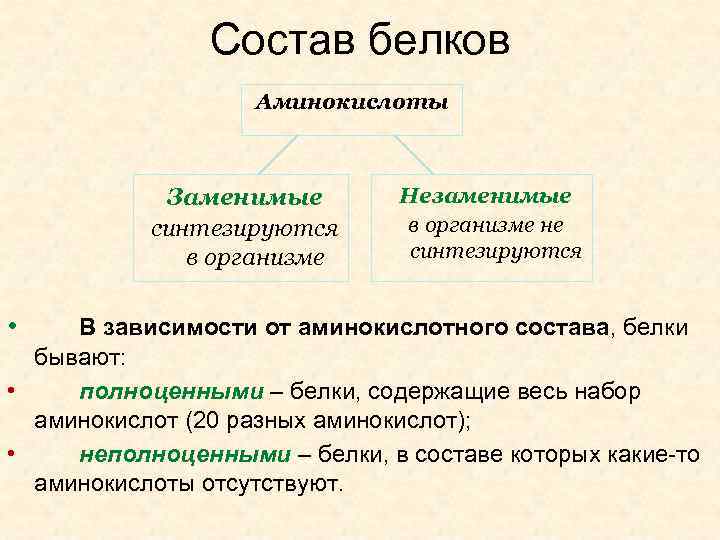
Состав белков Аминокислоты Заменимые синтезируются в организме • Незаменимые в организме не синтезируются В зависимости от аминокислотного состава, белки бывают: • полноценными – белки, содержащие весь набор аминокислот (20 разных аминокислот); • неполноценными – белки, в составе которых какие-то аминокислоты отсутствуют.
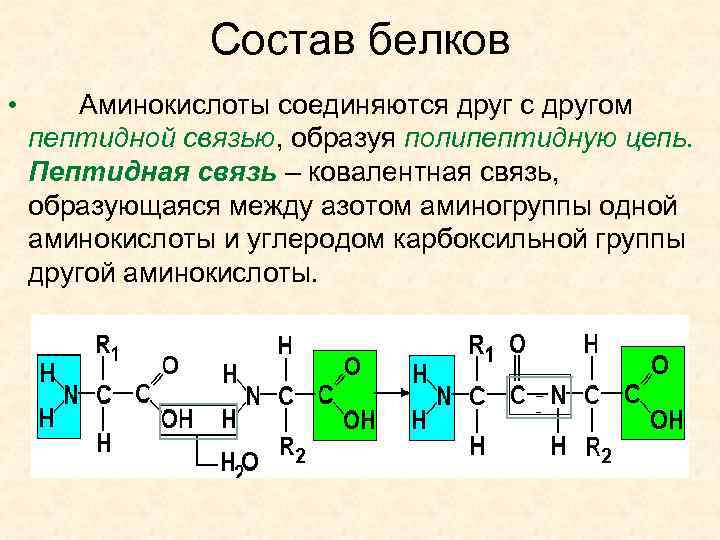
Состав белков • Аминокислоты соединяются друг с другом пептидной связью, образуя полипептидную цепь. Пептидная связь – ковалентная связь, образующаяся между азотом аминогруппы одной аминокислоты и углеродом карбоксильной группы другой аминокислоты.
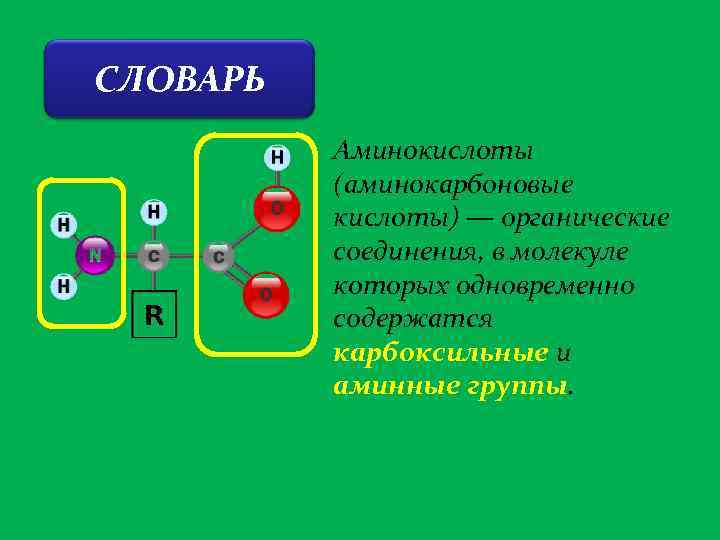
СЛОВАРЬ Аминокислоты (аминокарбоновые кислоты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.

Аминокислоты • аминокислоты содержат карбоксильную группу СООН и аминогруппу - NН 2, а отличаются радикалом • Аминогруппа - обладает свойствами оснований, а карбоксильная группа - кислотными свойствами. Аминокислоты - амфотерные соединения, поэтому могут взаимодействовать друг с другом, образуя полипептидную цепь. Связь между углеродом кислотной и азотом основной групп называется пептидной. Заменимые Незаменимые синтезируются в организме не синтезируются в организме

О С Н О Карбоксильная группа (карбоксил) СООН — функциональная одновалентная группировка, входящая в состав карбоновых кислот и определяющая их кислотные свойства. Википедия http: //upload. wikimedia. org/wikipedia/commons/thumb/0/09/Car boxylic-acid-group-3 D. png/771 px-Carboxylic-acid-group-3 D. png

Аминогру ппа — одновалентная группа —NH 2, остаток аммиака (NH 3). Википедия

Радикалы определяют структурные и функциональные особенности аминокислот.

СЛОВАРЬ Макромолекулой называют гигантскую молекулу, построенную из многих повторяющихся единиц – мономеров

Антуан Франсуа де Фуркруа основоположник изучения белков
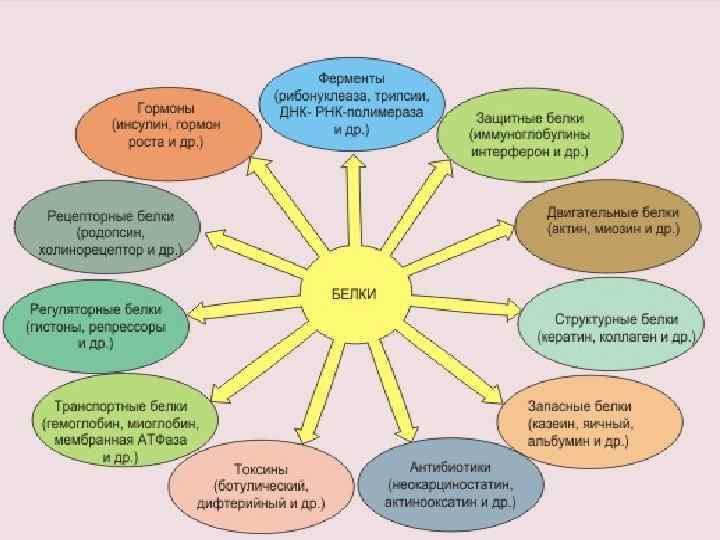
Функции белков

Источники белка. Белки — важнейшие компоненты пищи человека и корма животных. Совокупность непрерывно протекающих химический превращений белков занимает ведущее место в обмене веществ организмов. Скорость обновления белков у живых организмов зависит от содержания белков в пище, а также его биологической ценности, которая определяется наличием и соотношением незаменимых аминокислот.

Химическое строение белка. В основе жизнедеятельности любого организма лежат химические процессы. В каждой клетке вашего тела происходят тысячи химических реакций, и совокупность этих реакций определяет вашу индивидуальность. В этой грандиозной химической системе важнейшую роль играют молекулы белков.
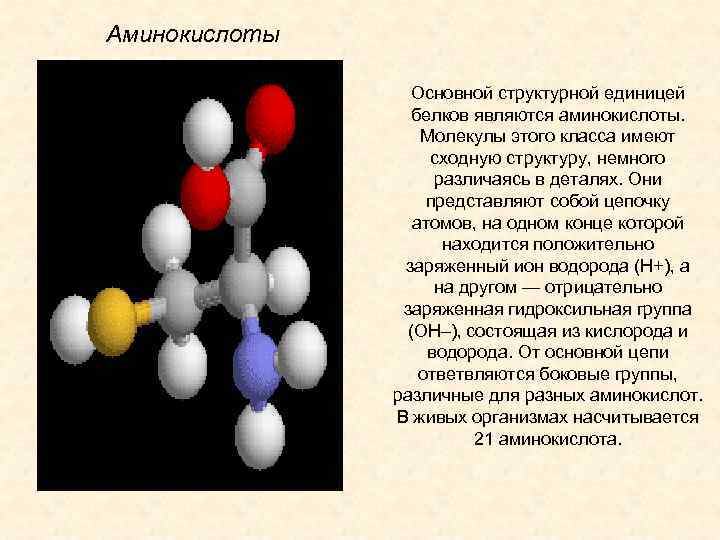
Аминокислоты Основной структурной единицей белков являются аминокислоты. Молекулы этого класса имеют сходную структуру, немного различаясь в деталях. Они представляют собой цепочку атомов, на одном конце которой находится положительно заряженный ион водорода (Н+), а на другом — отрицательно заряженная гидроксильная группа (ОН–), состоящая из кислорода и водорода. От основной цепи ответвляются боковые группы, различные для разных аминокислот. В живых организмах насчитывается 21 аминокислота.

Выделяют 4 уровня структуры белков. Все структуры формируются в каналах эндоплазматической цепи. При воздействии неблагоприятных факторов структуры белка могут разрушаться.
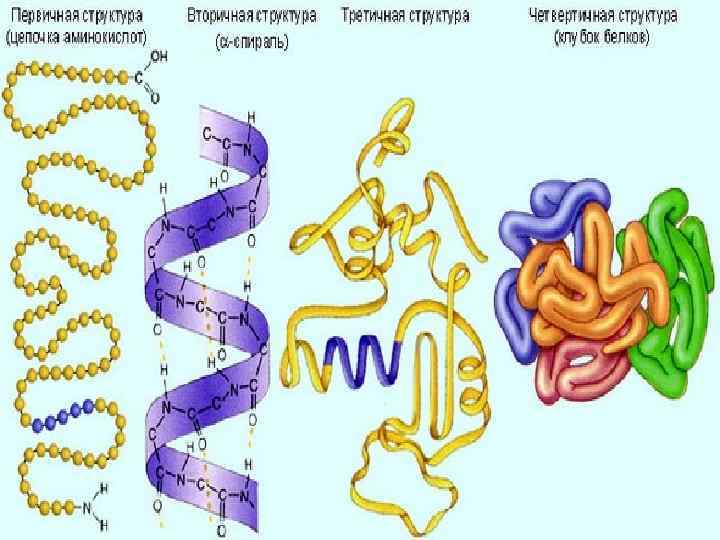
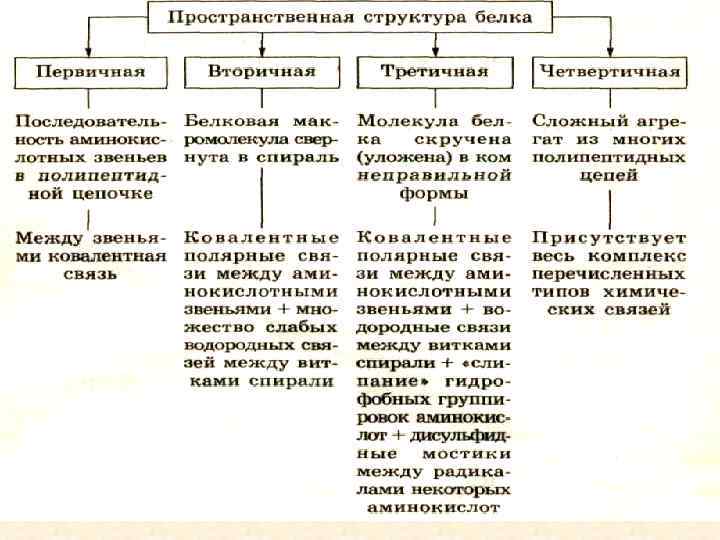
Структура Первичная Вторичная Третичная Четвертична я Характеристика структуры Химические связи

Структура молекулы белка Выделяют 4 уровня пространственной организации белков. • Первичная структура – последовательность расположения аминокислотных остатков в полипептидной цепи.

Структура молекулы белка • В организме человека обнаружено порядка 10 тыс. различных белков. Имея всего лишь 20 аминокислот, можно составить из них огромное количество самых разнообразных комбинаций. • Так, если молекула белка состоит всего из 10 аминокислотных остатков, то число теоретически возможных вариантов белковых молекул, отличающихся порядком чередования аминокислот, — 1020. Белки же, выделенные из живых организмов, образованы сотнями, а иногда и тысячами аминокислот.

Структура молекулы белка • Первым белком, у которого была выявлена аминокислотная последовательность, стал гормон инсулин. • Было выявлено, что молекула инсулина состоит из двух полипептидных цепей • (21 и 30 аминокислотных остатков), удерживаемых около друга дисульфидными мостиками. За свой кропотливый труд Ф. Сэнгер был удостоен Нобелевской премии.

Структура молекулы белка Первичная структура белковой молекулы определяет свойства молекул белка и ее пространственную конфигурацию. Замена всего лишь одной аминокислоты на другую в полипептидной цепочке может привести к изменению свойств и функций белка. Лишь незначительное количество белков имеет строго линейную структуру. Основная масса белков подвергается дальнейшей укладке, что приводит к образованию вторичной структуры белковой молекулы.

Первичная структура. • Структура - линейная последовательность аминокислот в полипептидной цепи. • Связи ковалентные пептидные.
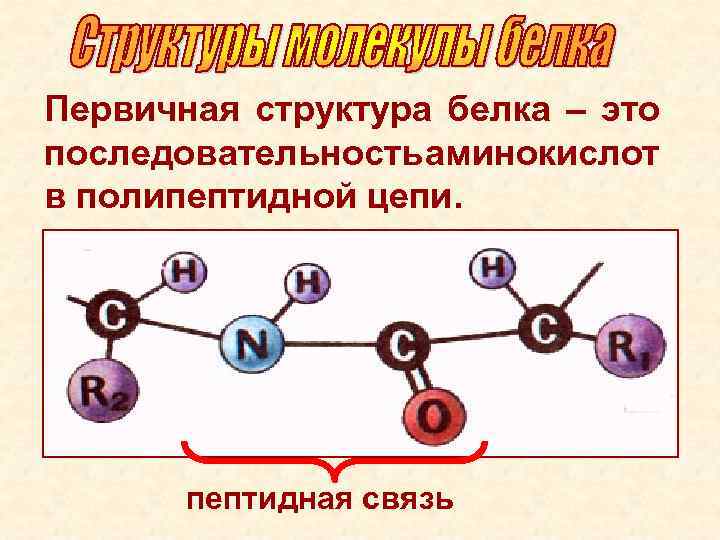
Первичная структура белка – это последовательность аминокислот в полипептидной цепи. пептидная связь

Первичная структура белка • Полипептидная цепь из последовательно соединенных аминокислотных остатков Связи: • пептидные

Вторичная структура спираль, удерживаемая водородными связями.

Вторичная структура • Структура: альфа-спираль; беттаспирали с параметрами, отличные от параметров спиралей глобулярных белков. • Связи: водородные, между остатками карбоксильных и аминогрупп.

Вторичная структура белка Полипептидная нить закручена в спираль • α-спираль – из одной полипептидной цепи • β –спираль – из нескольких полипептидных цепей Связи: • водородные
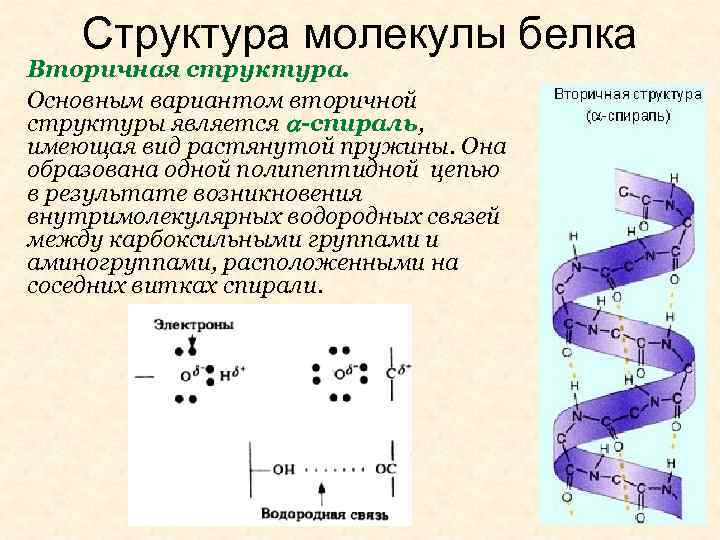
Структура молекулы белка Вторичная структура. Основным вариантом вторичной структуры является -спираль, имеющая вид растянутой пружины. Она образована одной полипептидной цепью в результате возникновения внутримолекулярных водородных связей между карбоксильными группами и аминогруппами, расположенными на соседних витках спирали.
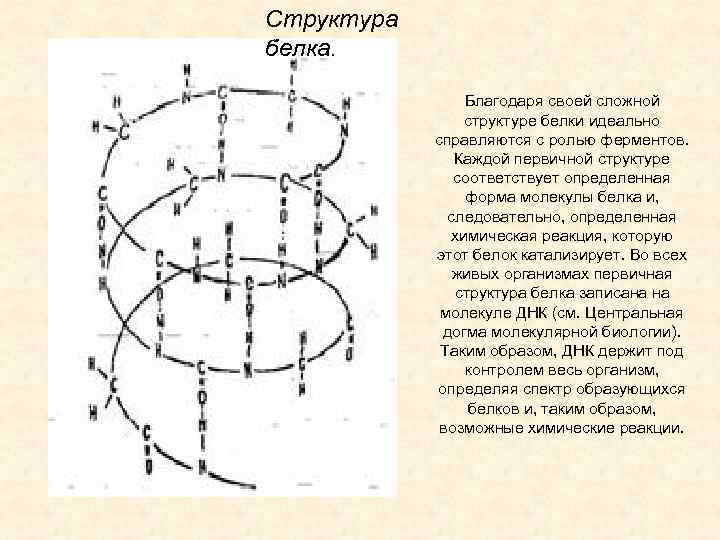
Структура белка. Благодаря своей сложной структуре белки идеально справляются с ролью ферментов. Каждой первичной структуре соответствует определенная форма молекулы белка и, следовательно, определенная химическая реакция, которую этот белок катализирует. Во всех живых организмах первичная структура белка записана на молекуле ДНК (см. Центральная догма молекулярной биологии). Таким образом, ДНК держит под контролем весь организм, определяя спектр образующихся белков и, таким образом, возможные химические реакции.

Третичная структура • Глобулярный тип белков: глобула, образующаяся в результате компактной укладки альфа-спирали (ионные, водородные, ковалентные и гидрофобные взаимодействия) • Фиббилярный тип белков: беттаструктуры, уложенные параллельными слоями, либо несколько скрученных спиралей (водородные и ковалентные связи)
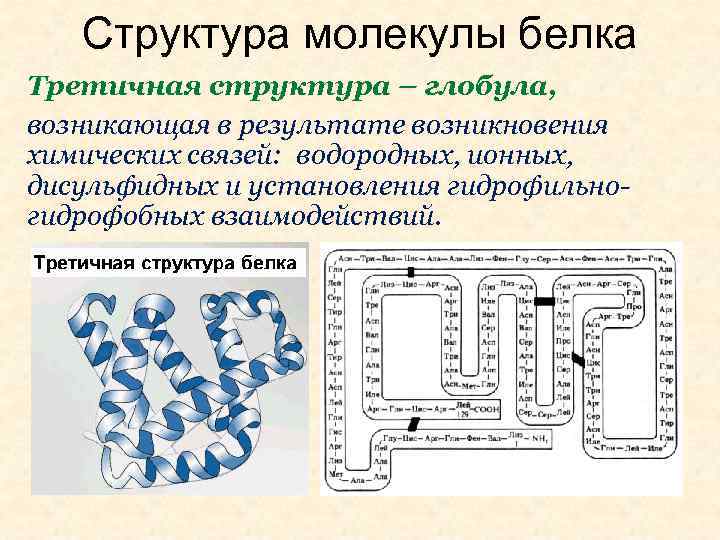
Структура молекулы белка Третичная структура – глобула, возникающая в результате возникновения химических связей: водородных, ионных, дисульфидных и установления гидрофильногидрофобных взаимодействий.

Третичная структура – имеет вид клубка, удерживаемого взаимодействием различных остатков аминокислот.

Третичная структура белка • Нить аминокислот свёртывается и образует клубок или фибриллу, специфичную для каждого белка. Связи: водородные • дисульфидные • гидрофобное взаимодействие

Структура белковой молекулы • • Четвертичная структура. Характерна для сложных белков, молекулы которых образованы двумя и более глобулами. • Глобулы удерживаются вместе благодаря ионным, гидрофильно-гидрофобным электростатическим взаимодействиям. и
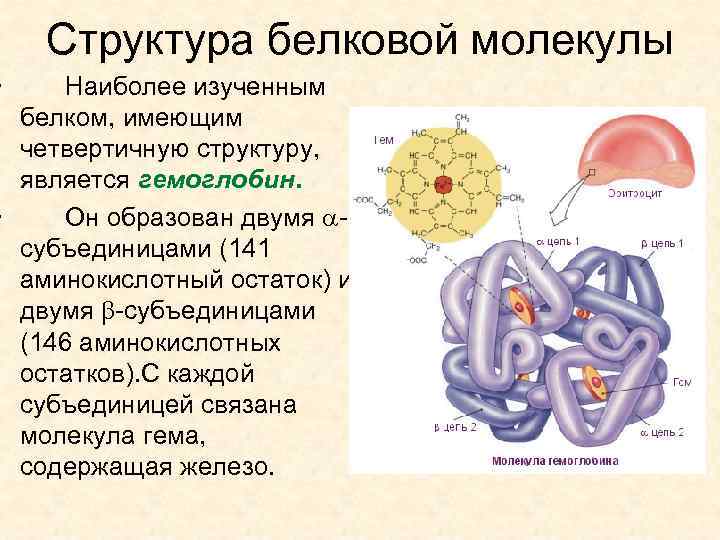
• Структура белковой молекулы Наиболее изученным белком, имеющим четвертичную структуру, является гемоглобин. • Он образован двумя субъединицами (141 аминокислотный остаток) и двумя -субъединицами (146 аминокислотных остатков). С каждой субъединицей связана молекула гема, содержащая железо.

Четвертичная структура • Глобулярный тип: агрегат из нескольких глобул (силы межмолекулярного притяжения) • Фибриллярный тип: микрофибриллы, состоящие из соответствующих эл-тов третичной структуры (силы межмолекулярного притяжения, а также ковалентные, водородные и ионные)

Четвертичная структура – характерна только для некоторых белков, соединяет несколько полипептидных цепей.

Четвертичная структура белка • молекулы белков четвертичной структуры состоят из нескольких макромолекул белков третичной структур, свёрнутых в клубок вместе Связи: • Ионные • Водородные • Гидрофобные связи
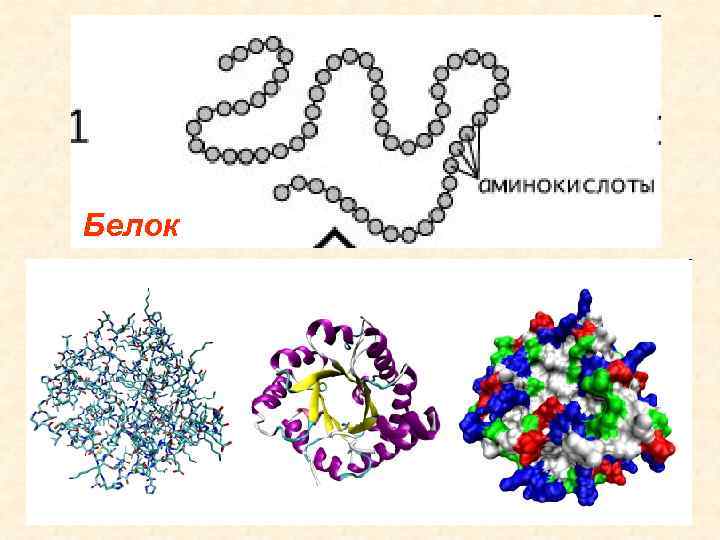
Белок
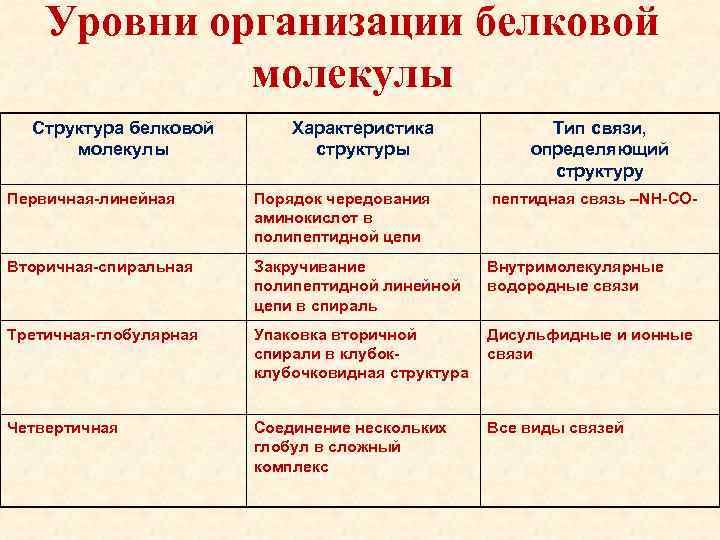
Уровни организации белковой молекулы Структура белковой молекулы Характеристика структуры Тип связи, определяющий структуру Первичная-линейная Порядок чередования аминокислот в полипептидной цепи пептидная связь –NH-CO- Вторичная-спиральная Закручивание полипептидной линейной цепи в спираль Внутримолекулярные водородные связи Третичная-глобулярная Упаковка вторичной спирали в клубокклубочковидная структура Дисульфидные и ионные связи Четвертичная Соединение нескольких глобул в сложный комплекс Все виды связей
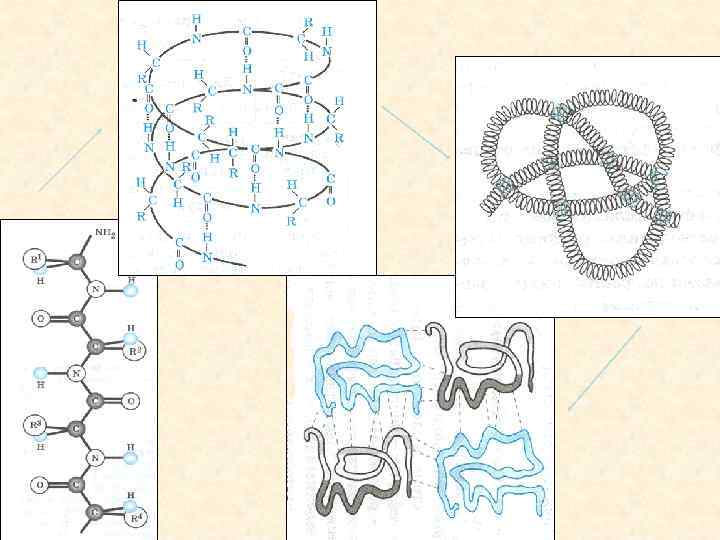

Белки чрезвычайно разнообразны по своим свойствам. Есть белки, растворимые (например, фибриноген) и нерастворимые (например, фибрин) в воде. Есть белки очень устойчивые (например, кератин) и неустойчивые (например, фермент каталаза с легко изменяющейся структурой). У белков встречается разнообразная форма молекул — от нитей (миозин - белок мышечных волокон) до шариков (гемоглобин)
Белки Простые состоят только из аминокислот Сложные содержат белковую и небелковую части • Процесс нарушения естественной структуры белка называется денатурацией. • Процесс восстановления естественной структуры белка называется ренатурацией. Возможна, если не разрушена первичная структура белка.
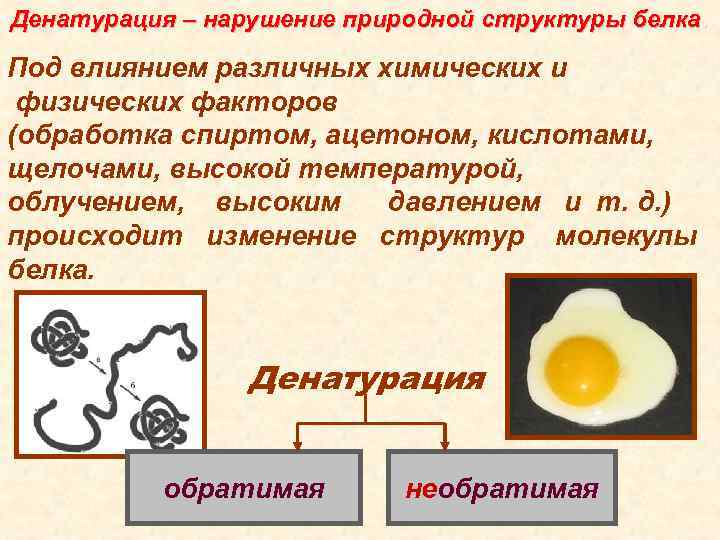
Денатурация – нарушение природной структуры белка. Под влиянием различных химических и физических факторов (обработка спиртом, ацетоном, кислотами, щелочами, высокой температурой, облучением, высоким давлением и т. д. ) происходит изменение структур молекулы белка. Денатурация обратимая необратимая
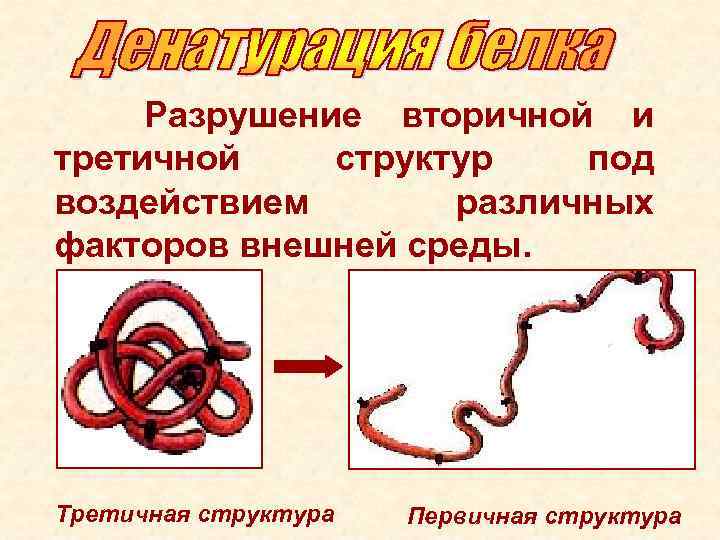
Разрушение вторичной и третичной структур под воздействием различных факторов внешней среды. Третичная структура Первичная структура
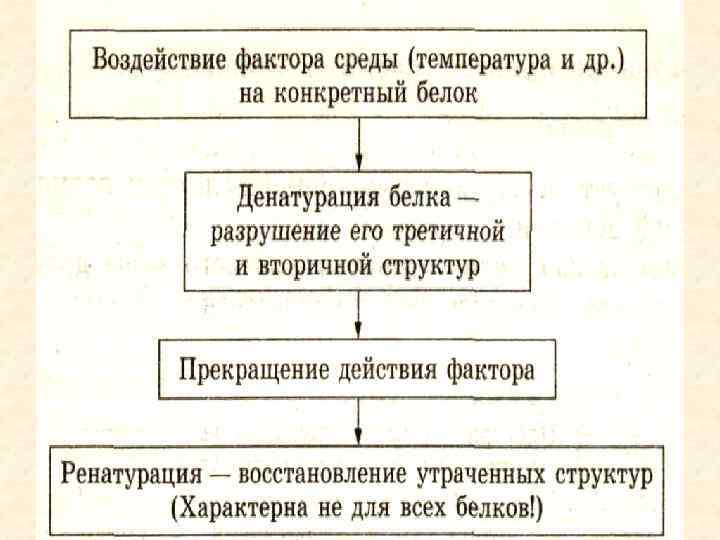

Денатурация белков (от лат. de- — приставка, означающая отделение, удаление и лат. nature — природа) — потеря белковыми веществами их естественных свойств (растворимости, гидрофильности и др. ) вследствие нарушения пространственной структуры их молекул. СЛОВАРЬ

под воздействием высоких температур

под воздействием высоких температур

под действием солей металлов

под действием спиртов

Под действием химических веществ – щелочей, кислот, солей тяжелых металлов, спиртов.

Ренатурация белков Полное восстановление структуры белка СЛОВАРЬ

биуретовая реакция

Ксантопротеиновая реакция – желтое окрашивание в присутствии НNO 3 при нагревании. Биуретовая реакция – красно – фиолетовое окрашивание в присутствии Cu. SO 4.

Свойства белков Белки имеют высокую молекулярную массу, некоторые растворимы в воде, способны к набуханию, характеризуются оптической активностью, подвижностью в электрическом поле и некоторыми другими свойствами.

• Белки активно вступают в химические реакции. Это свойство связано с тем, что аминокислоты, входящие в состав белков, содержат разные функциональные группы, способные реагировать с другими веществами. Важно, что такие взаимодействия происходят и внутри белковой молекулы, в результате чего образуется пептидная, водородная дисульфидная и другие виды связей.

• К радикалам аминокислот, а следовательно и белков, могут присоединяться различные соединения и ионы, что обеспечивает их транспорт по крови. Белки являются высокомолекулярными соединениями. Это полимеры, состоящие из сотен и тысяч аминокислотных остатков - мономеров. Соответственно и молекулярная масса белков находится в пределах 10 000 - 1 000. Так, в составе рибонуклеазы (фермента, расщепляющего РНК) содержится 124 аминокислотных остатка и ее

• молекулярная масса составляет примерно 14 000. Миоглобин (белок мышц), состоящий из 153 аминокислотных остатков, имеет молекулярную массу 17 000, а гемоглобин - 64 500 (574 аминокислотных остатка). Молекулярные массы других белков более высокие: -глобулин (образует антитела) состоит из 1250 аминокислот и имеет молекулярную массу около 150 000, а молекулярная масса фермента глутаматдегидрогеназы превышает 1 000.

• Определение молекулярной массы проводится различными методами: осмометрическим, гельфильтрационным, оптическим и др. однако наиболее точным является метод седиментации, предложенный Т. Сведбергом. Он основан на том, что при ультрацентрифугировании ускорением до 900 000 g скорость осаждения белков зависит от их молекулярной массы. Важнейшим свойством белков является их способность проявлять как кислые так и основные, то есть выступать в роли амфотерных электролитов.

• Это обеспечивается за счет различных диссоциирующих группировок, входящих в состав радикалов аминокислот. Например, кислотные свойства белку придают карбоксильные группы аспарагиновой глутаминовой аминокислот, а щелочные - радикалы аргинина, лизина и гистидина. Чем больше дикарбоновых аминокислот содержится в белке, тем сильнее проявляются его кислотные свойства и наоборот.

Роль белков в жизни клетки огромна. Современная биология показала, что сходство и различие организмов определяется в конечном счете набором белков.

Энергетическая Структурная Каталитическая Защитная Транспортная Сократительная Сигнальная Регуляторная
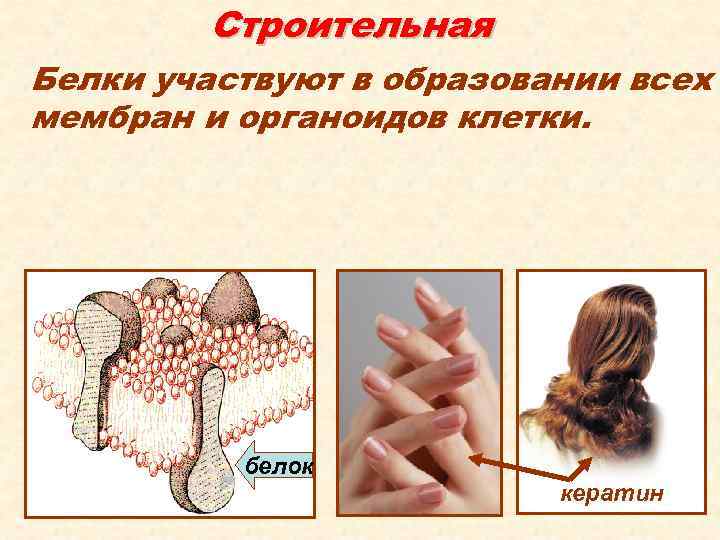
Строительная Белки участвуют в образовании всех мембран и органоидов клетки. белок кератин
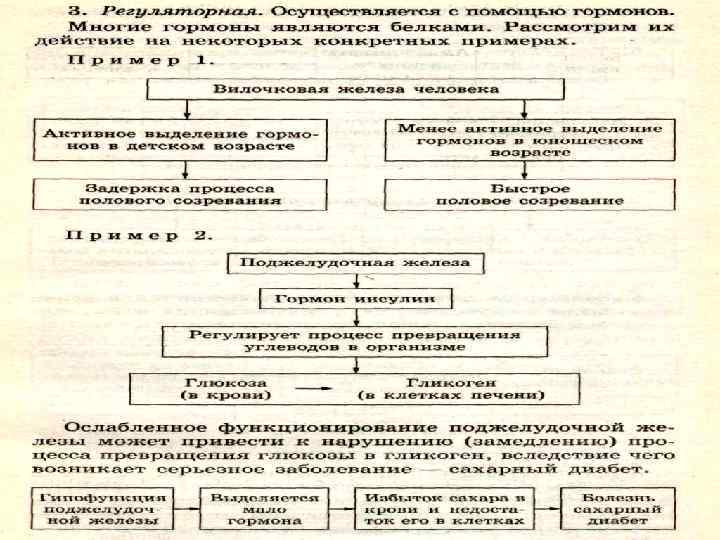
Каталитическая В каждой клетке имеются сотни ферментов. Они помогают осуществлять биохимические реакции, действуя как катализаторы.



• Ферменты (от латинского fermentum – закваска) • Ферменты - энзимы • Ферменты белковые специфические катализаторы • Ферменты стимулируют обмен веществ
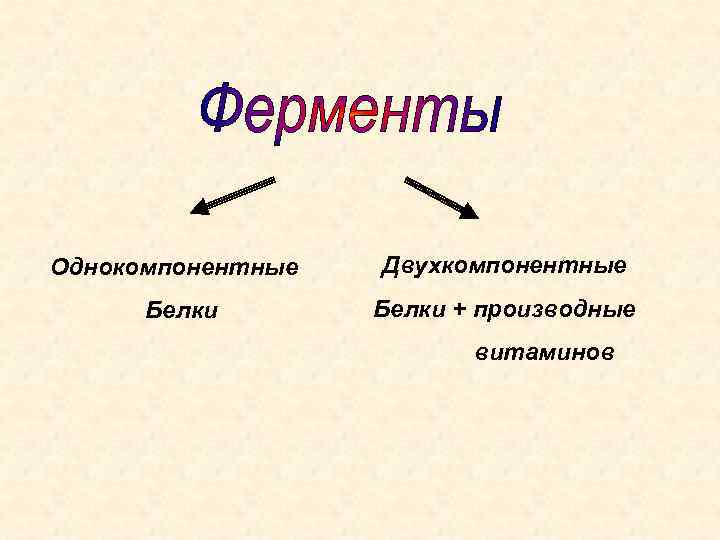
Однокомпонентные Белки Двухкомпонентные Белки + производные витаминов

Условия действия ферментов: • температура 30 – 50 • реакция среды (р. Н) • избирательность действия
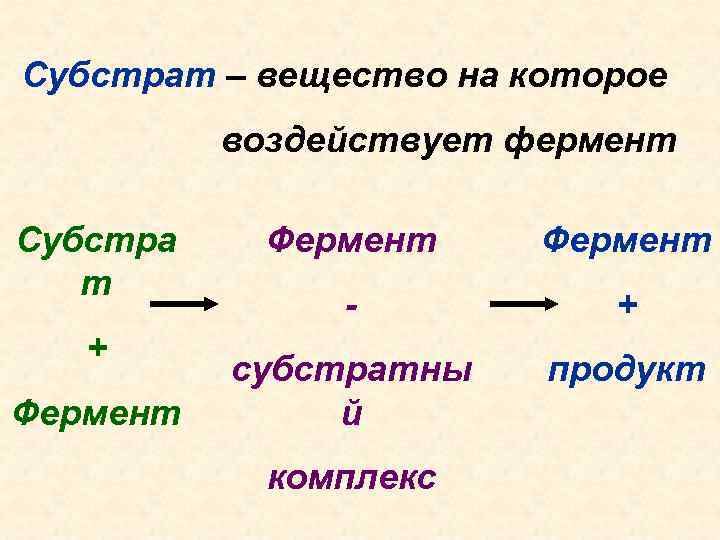
Субстрат – вещество на которое воздействует фермент Субстра т + Фермент - + субстратны й продукт комплекс

Практическое значение ферментов: • хлебопечение • виноделие, пивоварение • сыроделие • производство спирта, уксуса, чая
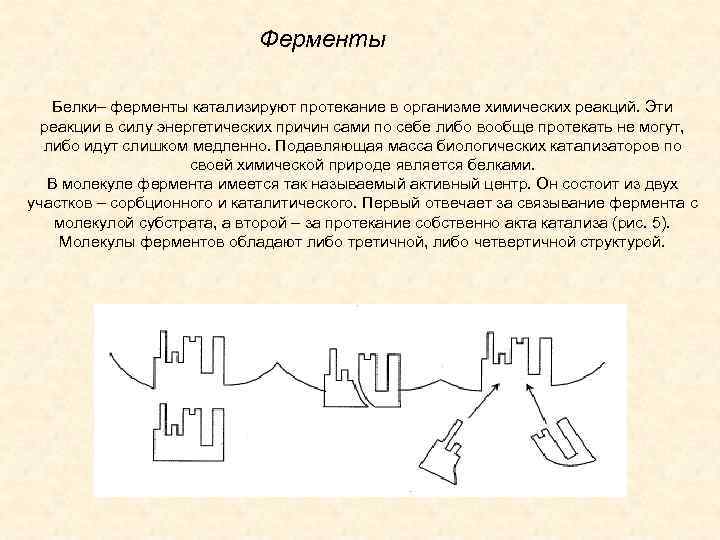
Ферменты Белки– ферменты катализируют протекание в организме химических реакций. Эти реакции в силу энергетических причин сами по себе либо вообще протекать не могут, либо идут слишком медленно. Подавляющая масса биологических катализаторов по своей химической природе является белками. В молекуле фермента имеется так называемый активный центр. Он состоит из двух участков – сорбционного и каталитического. Первый отвечает за связывание фермента с молекулой субстрата, а второй – за протекание собственно акта катализа (рис. 5). Молекулы ферментов обладают либо третичной, либо четвертичной структурой.

КАТАЛИТИЧЕСКАЯ ФУНКЦИЯ БЕЛКОВ наблюдение расщепления пероксида водорода ферментом пероксидазой (каталазой)

СВЕДЕНИЯ О ФЕРМЕНТЕ ПЕРОКСИДАЗА • В процессе жизнедеятельности в клетках образуется пероксид водорода (Н 2 О 2), который является ядовитым веществом для клетки. • В каждой растительной и животной клетке находится белок - фермент пероксидаза, который расщепляет пероксид водорода.

1. Приготовим клубни картофеля – сырой и вареный. 2. Отрежем по небольшому кусочку от каждого из них. Общий вид клубней сырого картофеля. 3. Проведём исследование на работу фермента пероксидаза с каждым кусочком. 4. Подтвердим или опровергнем выводы, полученные в результате исследований, используя другие

Капнем 2 -3 капли пероксида водорода на кусочек сырого картофеля. Что наблюдаем?
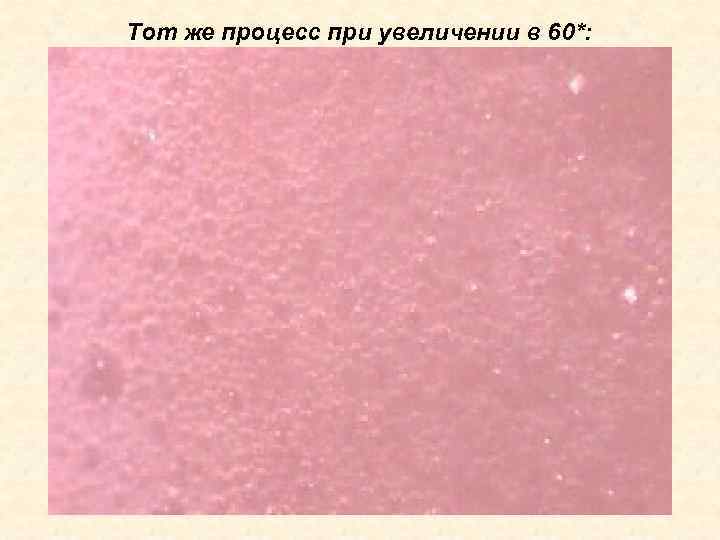
Тот же процесс при увеличении в 60*:

1. На какие вещества расщепляется пероксид водорода под влиянием пероксидазы? 2 Н 2 О 2 пероксидаза 2 Н 2 О+ О 2 2. Какое значение имеет реакция расщепления пероксида водорода под влиянием пероксидазы?

Капнем 2 -3 капли пероксида водорода на кусочек вареного картофеля. Наблюдается ли расщепление Н 2 О 2 ?

1. Почему в случае с вареным картофелем фермент пероксидаза не выполняет свою каталитическую функцию? 2. Какие уровни организации молекулы белка - фермента разрушились при варке картофеля? 3. Что такое денатурация белков? 4. Что вызывает денатурацию белков?

Будет ли идти процесс в клетках листа эпипремнума золотистого?
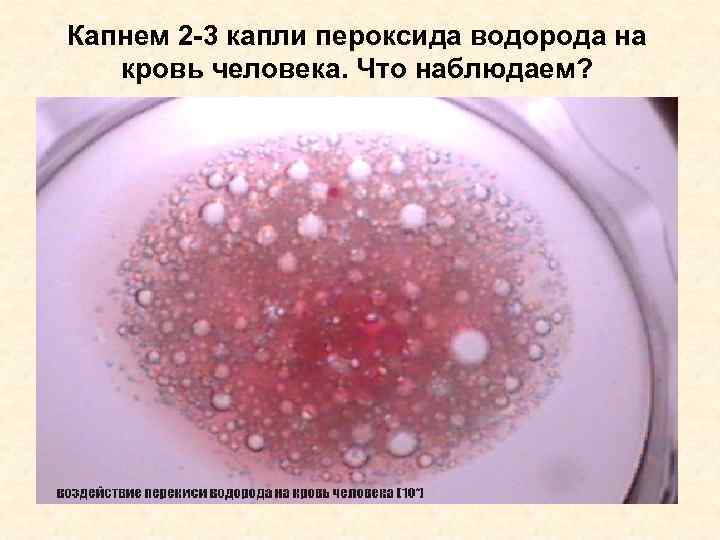
Капнем 2 -3 капли пероксида водорода на кровь человека. Что наблюдаем?
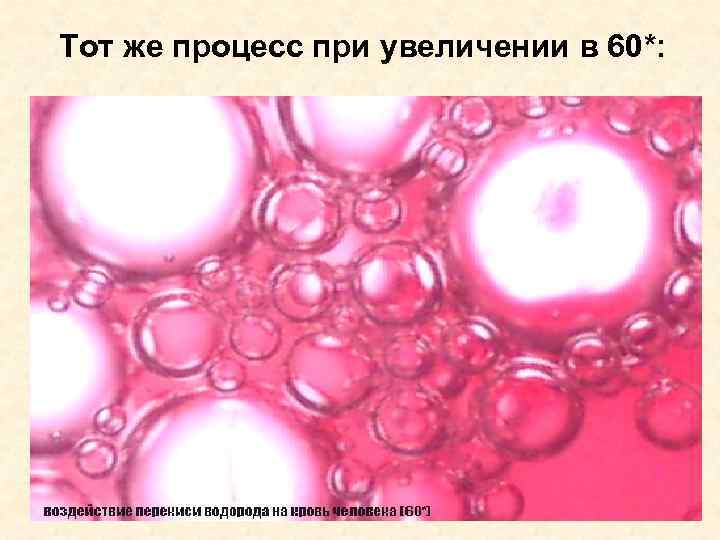
Тот же процесс при увеличении в 60*:
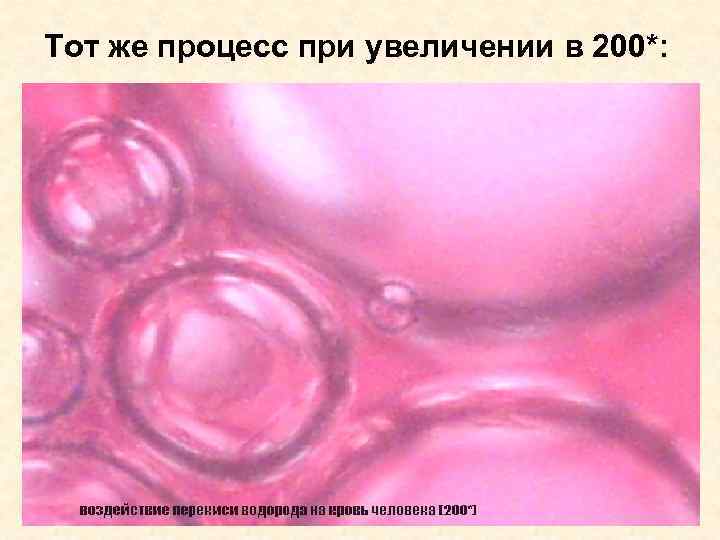
Тот же процесс при увеличении в 200*:

1. Попробуйте провести подобные исследования на других объектах. 2. Зафиксируйте результаты любым способом (фото-, видео- или микроскопическая съёмка) и принесите на следующий урок. 3. Сделайте выводы о работе ферментов в живой клетке и их роли для живых организмов.

Транспортная Белки связывают и переносят различные вещества и внутри клетки, и по всему организму. Например, г е м о г л о б и н крови переносит кислород.
Регуляторная Белки гормоны регулируют различные физиологические процессы. Например, инсулин Регулирует уровень углеводов в крови.
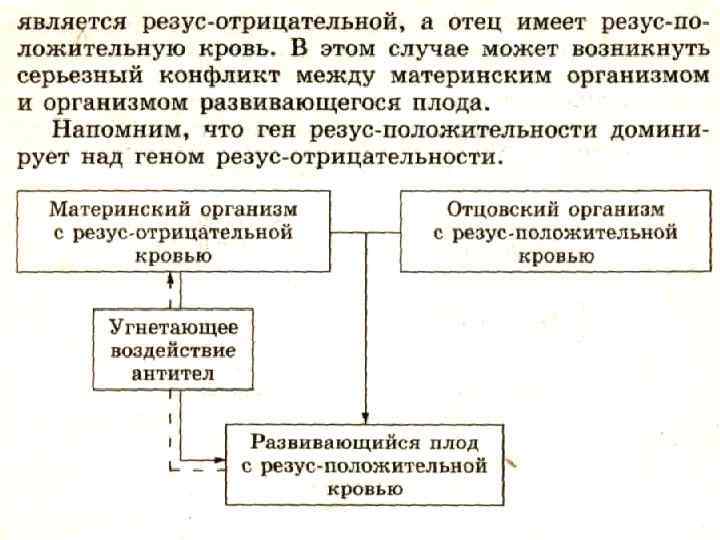
Защитная Предохраняют организм от вторжения чужеродных организмов и от повреждений Антитела блокируют чужеродные белки Например, фибриноген и протромбин обеспечивают свертываемость крови


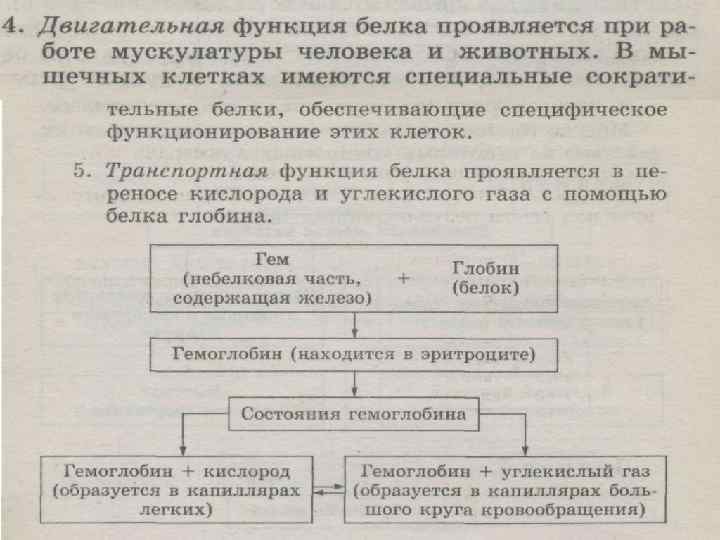

Сократительная Белки - участвуют в сокращении мышечных волокон. Актин и миозин – белки мышц

Энергетическая При недостатке углеводов или жиров окисляются молекулы аминокислот. При полном расщеплении белка до конечных продуктов выделяется энергия: 1 г белка - 17. 6 к. Дж Но в качестве источника энергии белки используются крайне редко.
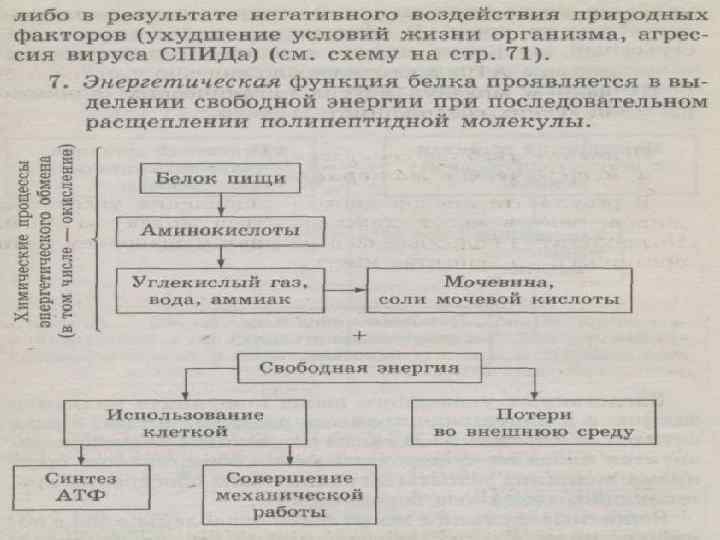

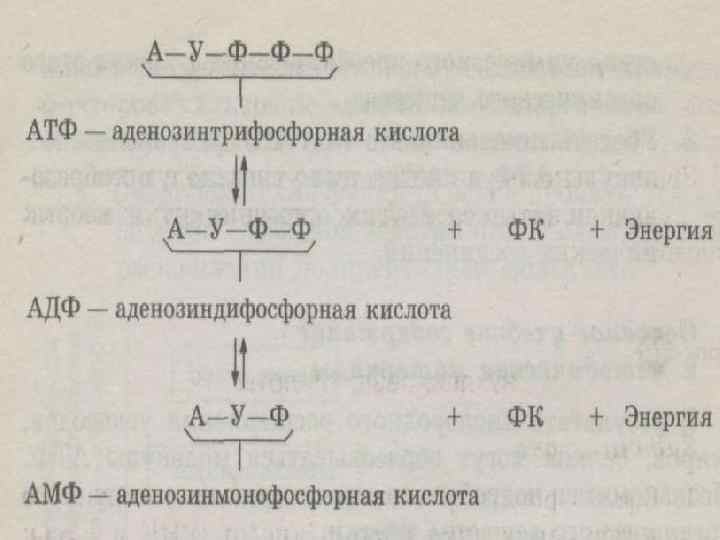
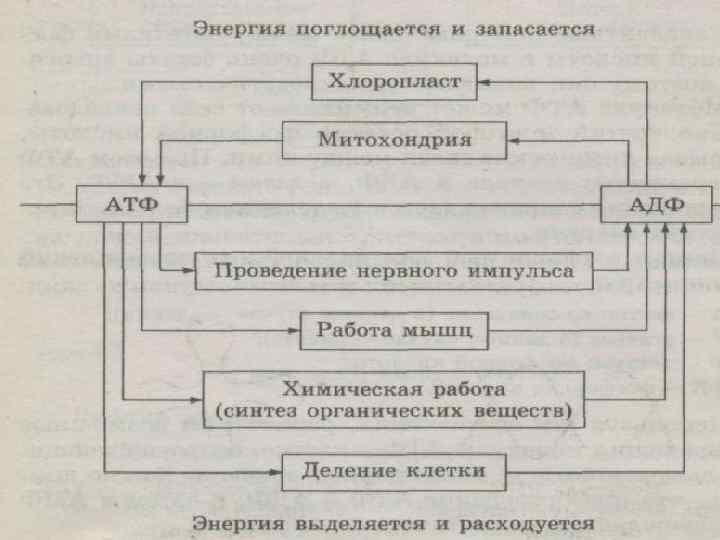
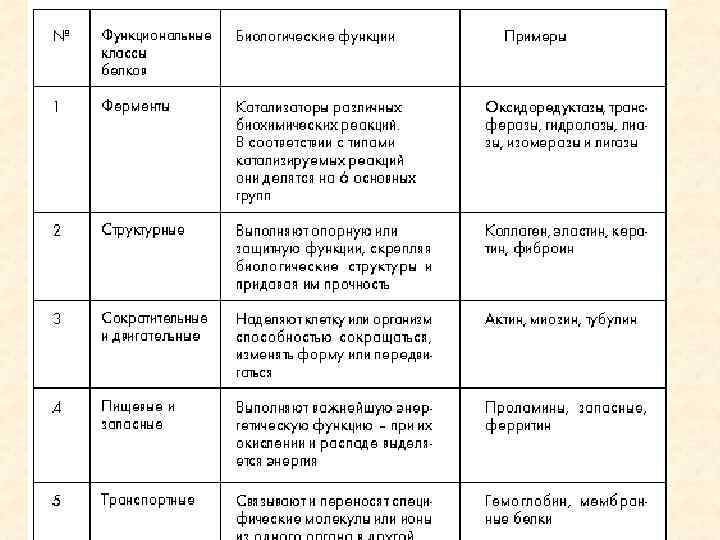
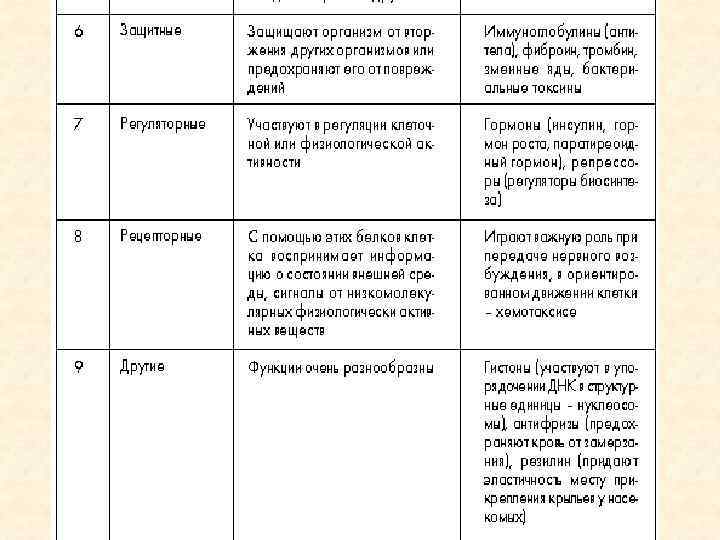
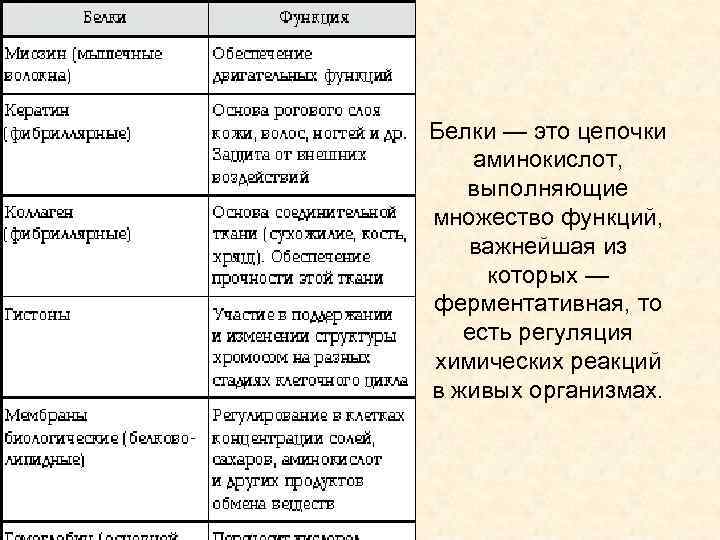
Белки — это цепочки аминокислот, выполняющие множество функций, важнейшая из которых — ферментативная, то есть регуляция химических реакций в живых организмах.
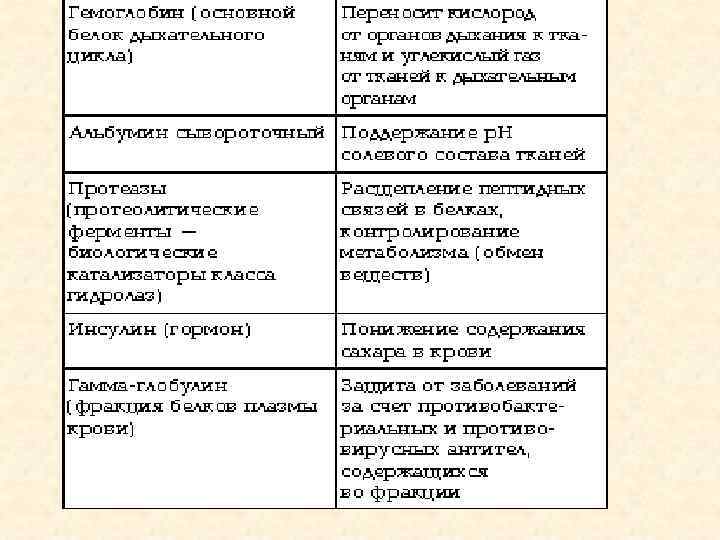

Вывод • Белки в клетке выполняют множество функций, имеют сложное строение. • Без белков жизнь клетки невозможна

Задание на дом: § 1. 4 «Состав и строение белков» , ответить на вопросы в конце параграфа

Использованные ресурсы http: //medzdravnica. ru/images/Med. Zdrav. Nizza/Ga. Zim/28. 02 Klet. Ka/Klet. Ka 113. jpg - белковая молекула http: //www. happynews. com/show. Image. aspx? fn=7312009/proteins-provide-cataract-protection. jpg&catid=5 структура белка http: //upload. wikimedia. org/wikipedia/commons/thumb/c/ce/Amino. Acidball. svg/702 px-Amino. Acidball. svg. png молекула аминокислоты http: //www. ebio. ru/images/08010502. jpg - структуры белка http: //upload. wikimedia. org/wikipedia/commons/thumb/8/88/Antoine_François%2 C_comte_de_Fourcroy. jpg/180 px. Antoine_François%2 C_comte_de_Fourcroy. jpg - портрет Антуана Франсуа де Фуркруа http: //www. medbiol. ru/medbiol/biology_sk/images/010. jpg - функции белков http: //bannikov. narod. ru/images/belok 1. jpg - первичная структура белка http: //bannikov. narod. ru/images/belok 2. jpg - вторичная структура белка http: //bannikov. narod. ru/images/belok 3. jpg - третичная структура белка http: //bannikov. narod. ru/images/belok 4. jpg - четвертичная структура белка

http: //upload. wikimedia. org/wikipedia/commons/0/02/Fried_egg%2 C_sunny_side_up. jpg - яичница http: //www. darwin. museum. ru/expos/floor 3/Evol/img/dnk_b. jpg - модель ДНК http: //su. okis. ru/img/su/445435 ssg. JPG- ДНК и РНК http: //nauka. relis. ru/08/0402/rna 2. jpg - сравнение ДНК и РНК Википедия - http: //ru. wikipedia. org http: //de. academic. ru/pictures/dewiki/49/180 px-Friedrich_Miescher. jpg - Фридрих Мишер http: //www. membrana. ru/images/articles/1039448450 -4. jpeg- нуклеотид http: //img 1. liveinternet. ru/images/attach/b/3/13/466/13466026_geni. jpg - ДНК http: //luts. ucoz. ru/load/8 - Занимательная биология http: //luts. ucoz. ru/_ld/0/63839. jpg - белки
!!!свойства,строение белков.ppt