порошки.ppt
- Количество слайдов: 64

Зачем необходимы наноматериалы? 1. Катализ 2. Сорбенты 3. Покрытия
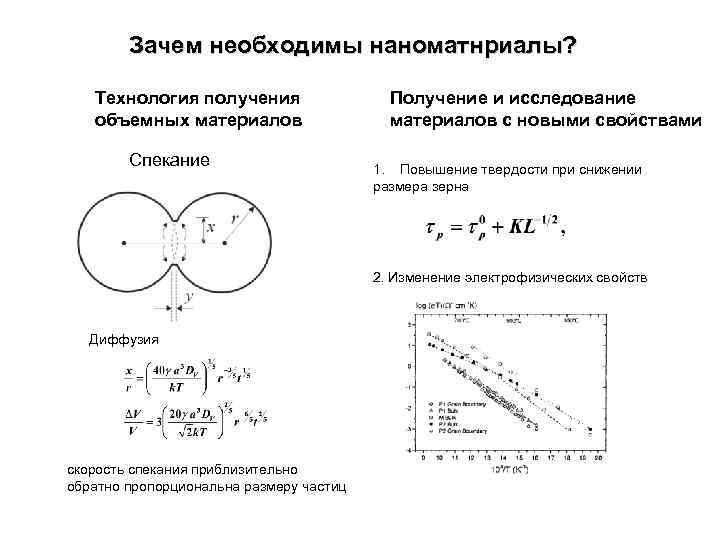
Зачем необходимы наноматнриалы? Технология получения объемных материалов Спекание Получение и исследование материалов с новыми свойствами 1. Повышение твердости при снижении размера зерна 2. Изменение электрофизических свойств Диффузия скорость спекания приблизительно обратно пропорциональна размеру частиц

Grootzevert W. F. M. , Winnubst A. J. A. , Theunissen G. S. , Burggraaf A. J. Powder Preparation and Compaction Behavior of Fine-grained Y-TZP. // Journal of Material Science. 1990. V. 25. P. 3449 -3455. These elements are: (1) primary crystallites; (2) aggregates in which the primary crystallites are held together by neck areas which are formed by reaction, e. g. sintering of the powder by surface diffusion or even diffusion and precipitation at necks in the suspension, (3) agglomerates (4) The aggregates or the individual primary crystallites are held together in an agglomerate structure by relatively weak (e. g. Van der Waals. capillary) attractive forces. During wetchemical preparation these crystallite "clusters" (2 and 3) are essentially formed in the early stages of the preparation cycle Кабанова М. И. , Дубок В. А. Влияние характеристик порошков на микроструктуру и механические свойства спеченной керамики в Zr. O 2 – 3 мол% Y 2 O 3. // Порошковая металлургия. 1996. № 1/2. С. 103 -109. элементарный монокристалл - область когерентного рассеяния лучей (ОКР) кристаллит - сросток ОКР агрегат - конструкция из кристаллитов и межкристаллитных пор) агломерат - конструкция из агрегатов и межагрегатных пор) гранула -элемент, сформированный из агломератов для улучшения технологических свойств порошка
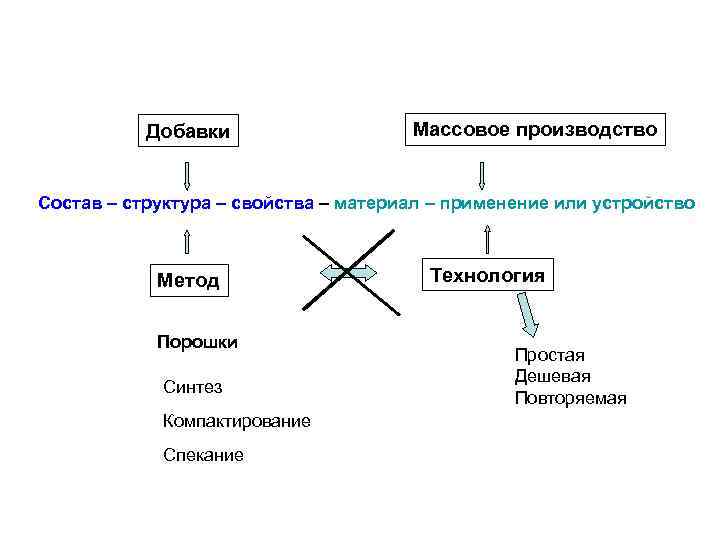
Добавки Массовое производство Состав – структура – свойства – материал – применение или устройство Метод Порошки Синтез Компактирование Спекание Технология Простая Дешевая Повторяемая

Методы синтеза нанопорошков Деструктивные Конструктивные 1. 2. 3. 4. Медленные 1. Золь-гель 2. Осаждение 3. Гидротермальный Измельчение Лучевое испарение Взрывной Молекулярное разложение Экономика Быстрые 1. Кристаллизация 2. Метод «Печини» 3. Разложение солей 4. Плазменно-химический синтез Низкая стоимость прекурсоров Низкая стоимость порошков Высокий % выхода Физико-химические свойства Масштабирование Простое оборудование Соответствие поставленной цели Автоматизация Нано Высокая удельная поверхность Низкая агломерируемость
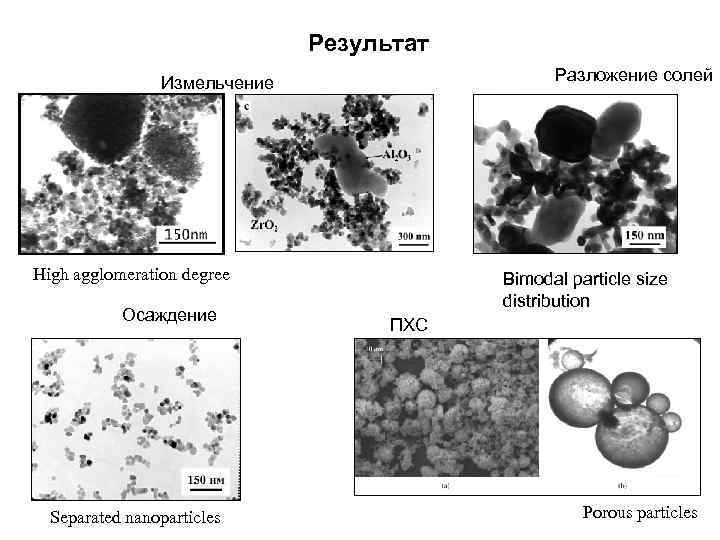
Результат Разложение солей Измельчение High agglomeration degree Осаждение Separated nanoparticles Bimodal particle size distribution ПХС Porous particles
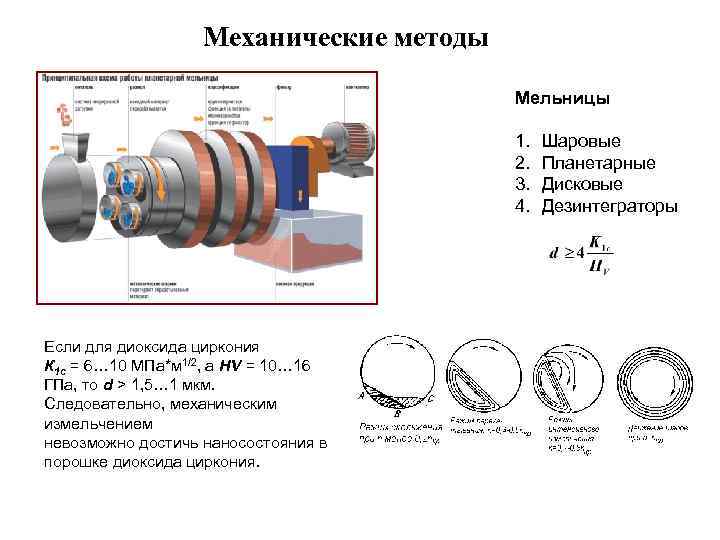
Механические методы Мельницы 1. 2. 3. 4. Если для диоксида циркония К 1 с = 6… 10 МПа*м 1/2, а НV = 10… 16 ГПа, то d > 1, 5… 1 мкм. Следовательно, механическим измельчением невозможно достичь наносостояния в порошке диоксида циркония. Шаровые Планетарные Дисковые Дезинтеграторы
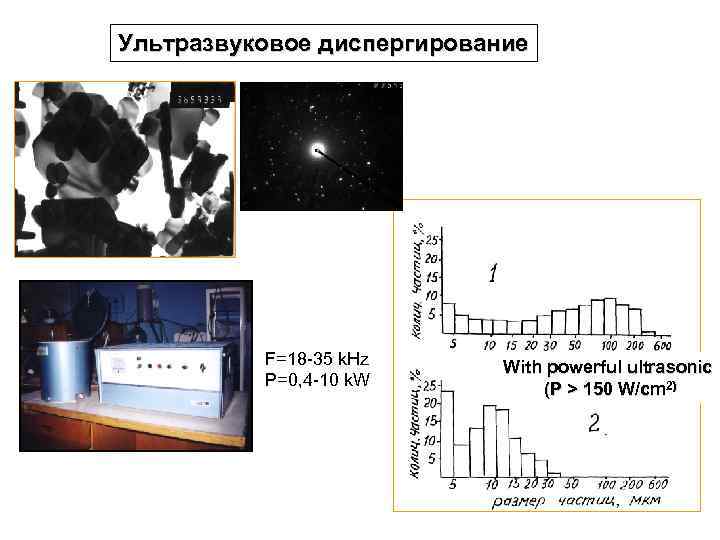
Ультразвуковое диспергирование F=18 -35 k. Hz P=0, 4 -10 k. W With powerful ultrasonic (P > 150 W/cm 2)
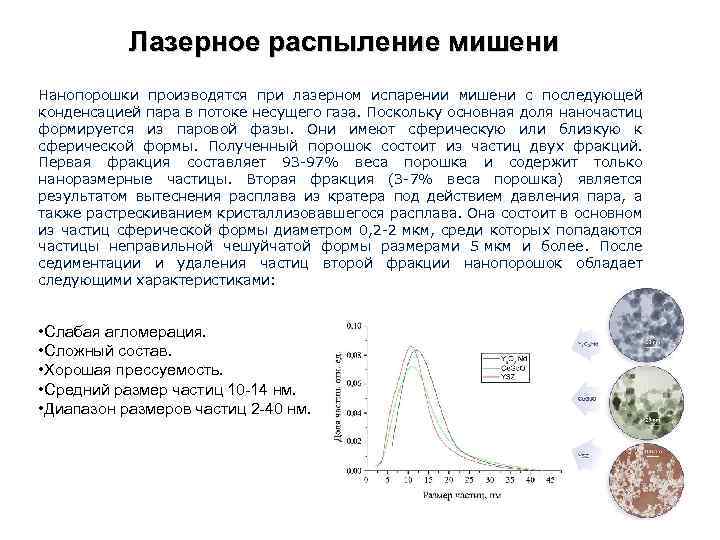
Лазерное распыление мишени Нанопорошки производятся при лазерном испарении мишени с последующей конденсацией пара в потоке несущего газа. Поскольку основная доля наночастиц формируется из паровой фазы. Они имеют сферическую или близкую к сферической формы. Полученный порошок состоит из частиц двух фракций. Первая фракция составляет 93 -97% веса порошка и содержит только наноразмерные частицы. Вторая фракция (3 -7% веса порошка) является результатом вытеснения расплава из кратера под действием давления пара, а также растрескиванием кристаллизовавшегося расплава. Она состоит в основном из частиц сферической формы диаметром 0, 2 -2 мкм, среди которых попадаются частицы неправильной чешуйчатой формы размерами 5 мкм и более. После седиментации и удаления частиц второй фракции нанопорошок обладает следующими характеристиками: • Слабая агломерация. • Сложный состав. • Хорошая прессуемость. • Средний размер частиц 10 -14 нм. • Диапазон размеров частиц 2 -40 нм.

Способ получения НП методом электрического взрыва проволок (ЭВП). В свое время появился, а в дальнейшем утвердился способ получения наноматериалов путем электрического взрыва проволок (проводников). В этом случае в реакторе между электродами помещают проволоки металла, из которого намечается получение нанопорошка, диаметром 0, 1. . . 1, 0 мм. На электроды подают импульс тока большой силы (104. . . 106 А/мм 2). При этом происходит мгновенный разогрев и испарение проволок. Пары металла разлетаются, охлаждаются и конденсируются. Процесс идет в атмосфере гелия или аргона. Наночастицы оседают в реакторе. Таким способом получают металлические (Тi, Со, W, Fе, Мо) и оксидные (Ti. O 2, Аl 2 O 3, Zr. O 2) нанопорошки с крупностью частиц до 100 нм. Дисперсность порошка, структура частиц и другие свойства определяются параметрами разрядного контура, материалом и геометрическими размерами проволоки (фольги) и характеристиками газовой среды, в которой производится взрыв.

Молекулярное разложение В этой технике, наноразмерные порошки образованы при разложении (или фрагментации на атомном уровне) более крупной молекулы при удаление нежелательных летучих составляющих. Первоначально большая молекула синтезируется таким образом, что она содержит нужные компоненты, а также некоторые летучие компоненты. Этот материал-предшественник последовательно контактирует с жидкостью, в которой предшественник нерастворим. Однако жидкость должна быть такой, чтобы она вступает в реакцию с предшественником с образованием желаемого нерастворимый продукт в виде наноразмерных объектов, а также образуют растворимые вещества, содержащие летучие компоненты. Удаление из летучих компонентов из молекулы-предшественника приводит к фрагментации на атомном уровне, тем самым формируя наноразмерные порошки. For the synthesis of nanosize yttria-stabilized zirconia by the present method, the precursor can be a suitable alkali or an alkaline earth zirconate. For the synthesis of Y-Na 2 Zr. O 3, Na 2 CO 3 and commercial YSZ powder were mixed in the requisite proportion, wet ballmilled, and then dried. Doped sodium zirconate was then boiled and washed in deionized water since the reaction between Na 2 Zr. O 3 and water is thermodynamically favored. In this way, Na 2 O can be easily leached out. Y-Na 2 Zr. O 3+2 H 2 O=2 Na. OH+Y 2 O 3 -Zr. O 2,
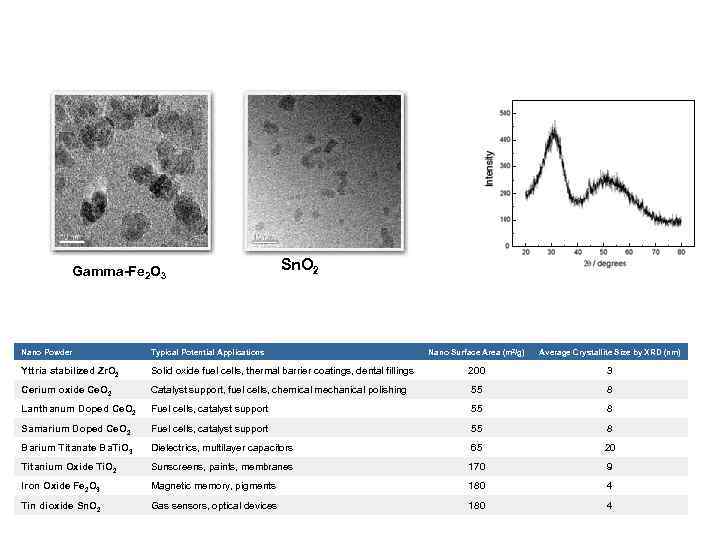
Gamma-Fe 2 O 3 Nano Powder Typical Potential Applications Yttria stabilized Zr. O 2 Sn. O 2 Nano Surface Area (m 2/g) Average Crystallite Size by XRD (nm) Solid oxide fuel cells, thermal barrier coatings, dental fillings 200 3 Cerium oxide Ce. O 2 Catalyst support, fuel cells, chemical mechanical polishing 55 8 Lanthanum Doped Ce. O 2 Fuel cells, catalyst support 55 8 Samarium Doped Ce. O 2 Fuel cells, catalyst support 55 8 Barium Titanate Ba. Ti. O 3 Dielectrics, multilayer capacitors 65 20 Titanium Oxide Ti. O 2 Sunscreens, paints, membranes 170 9 Iron Oxide Fe 2 O 3 Magnetic memory, pigments 180 4 Tin dioxide Sn. O 2 Gas sensors, optical devices 180 4

Газофазный синтез ( конденсация паров )
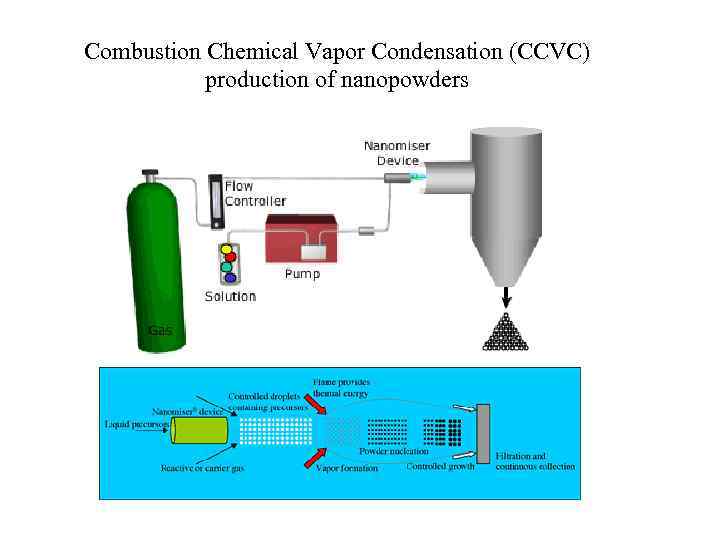
Combustion Chemical Vapor Condensation (CCVC) production of nanopowders
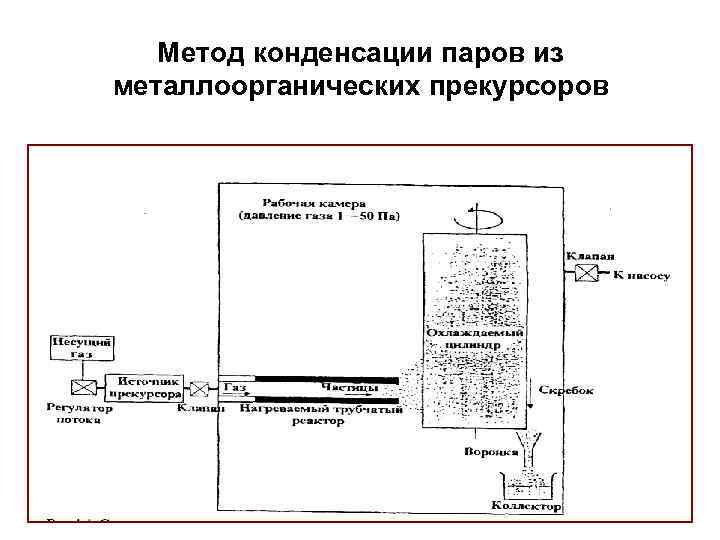
Метод конденсации паров из металлоорганических прекурсоров

Плазмохимический синтез 1 – пирометр, 2 - окно для пирометра, 3 – индуктор, 4 - кварцевая камера, 5 - сопловой блок, 6 - рабочий поток, 7 - рабочая камера, 8 – образец, 9 – державка, 10 – подвеска, 11 - механизм ввода-вывода, 12 – диффузор, 13 - трубки водяного охлаждения, 14 - ядро потока, 15 - зона разряда, 16 – газоформирователь

PLASMA производство нанопорошков Описание системы Наша система для производства нанопорошков является гибкой и дает производству и лабораториям надежный метод синтеза широкого диапазона нанопорошков. Система использует внедренную технологию контроля для мониторинга условий производства и обеспечивает безопасную работу. 60 k. V Induction Plasma System для производства нанопорошков


Example of incorrect powder use ПХС порошки с идеальным химическим составом, Но Не спекаются

Термическое разложение Метод Pechini In standard GNP, an aqueous solution containing glycine and the appropriate amounts of metal nitrates is prepared and heated until the excess water has boiled away and the remaining material ignites— the ash and smoke resulting from this reaction being the desired ceramic phase.

Золь-гель технология В золь-гель технологии прекурсор – это вещество, которое при определенных условиях может образовывать полимолекулы, полисольватированные группы, мицеллы, из которых будут формировать зародыши наночастиц золя. В качестве прекурсоров могут использоваться практически любые, как правило, гидролизующиеся соединения – алкоксиды кремния Si(OR)4 и ряда других металлов (Me – Al, Ti, Sn, Zr и др. ), соли металлов (например, хлориды титана, оксохлориды ванадия). Изначально, в момент смешивания исходных компонентов друг с другом, они, как правило, представляют собой истинные растворы. В результате гидролитической поликонденсации молекул прекурсора образуется наночастицы (твердая фаза), размер которых обычно находится в диапазоне 1 -100 нм
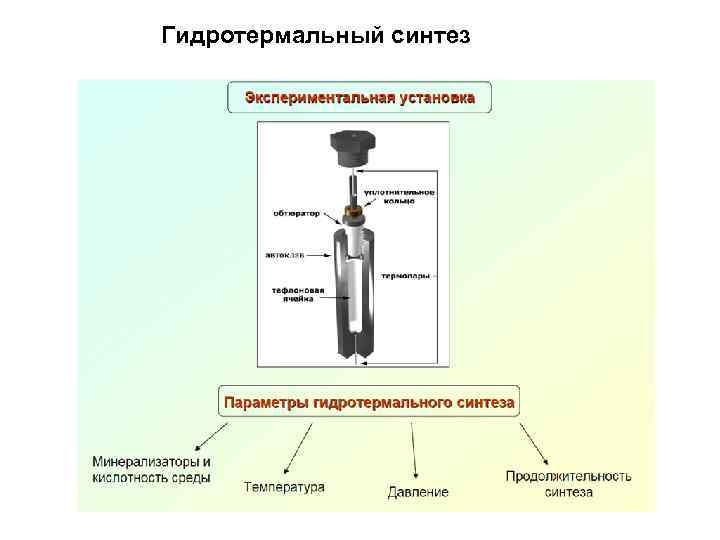
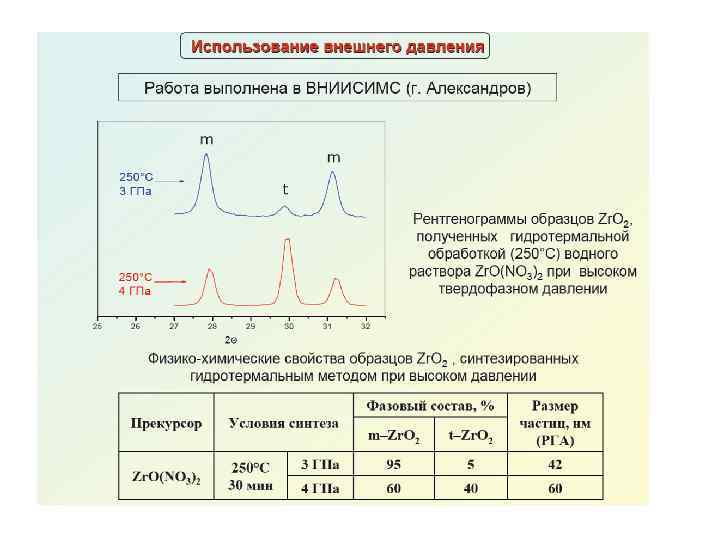
Гидротермальный синтез
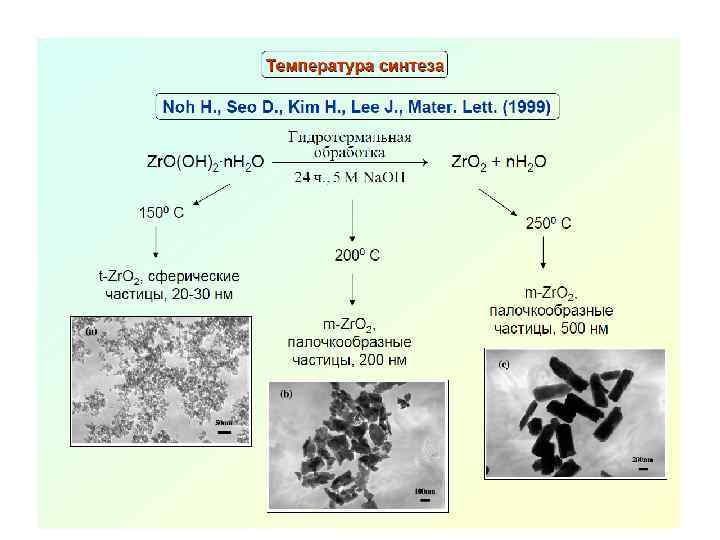
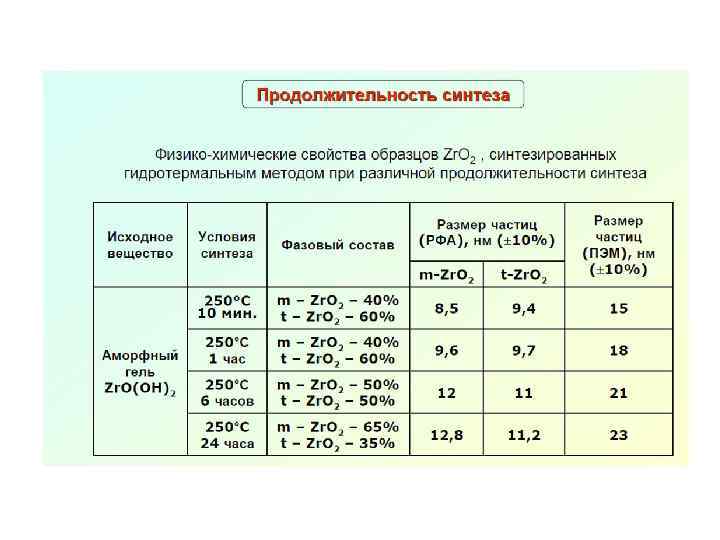
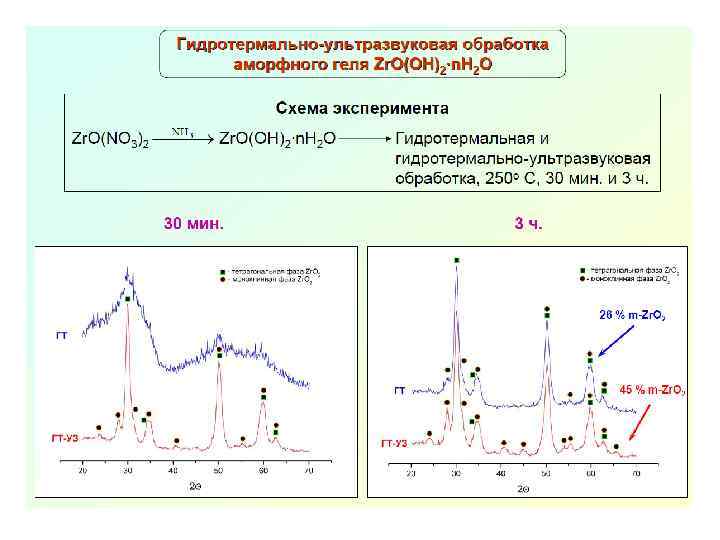

Механохимический синтез
Детонационный синтез и метод взрыва Нановзрывное производство мультиметаллических оксидов и металлокерамических композитных нанопорошков Nano-explosion synthesis of multi-metal oxides and metal/ceramic composite nanopowders Scientific Advisor Dr. Yoshio Sakka

Oleg VASYLKIV Идеальная агрегация двухкомпонентных нано/композитов Отличная морфология на наноуровне Строго унифицированное определение составов
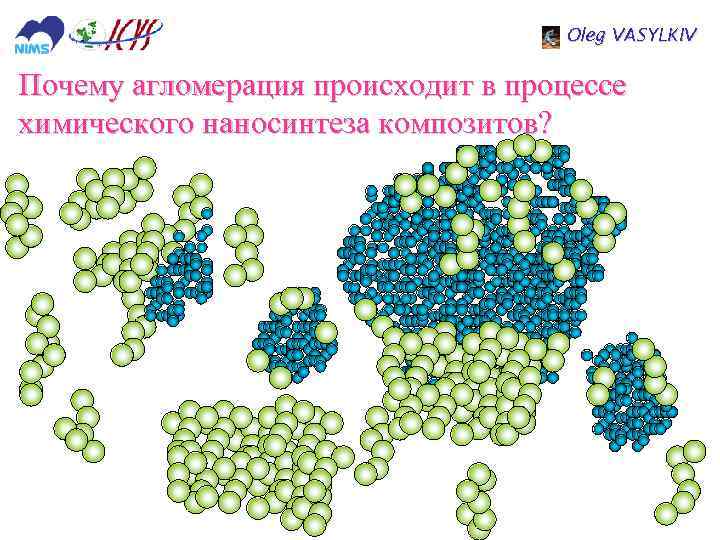
Oleg VASYLKIV Почему агломерация происходит в процессе химического наносинтеза композитов?
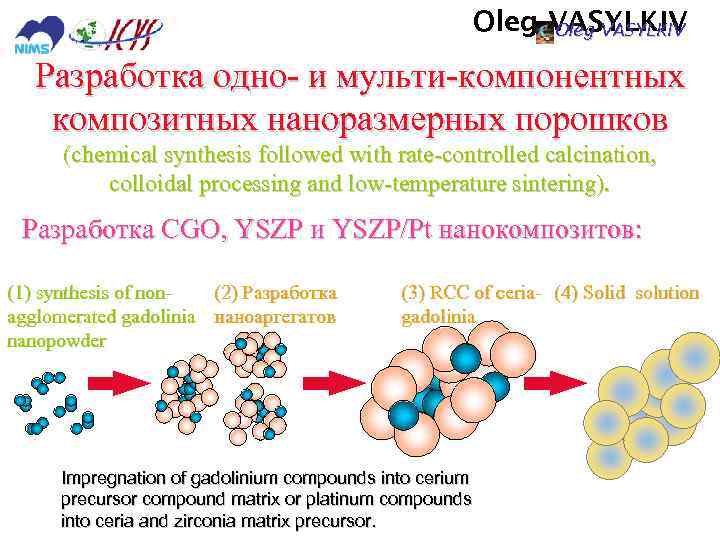
Oleg VASYLKIV Разработка одно- и мульти-компонентных композитных наноразмерных порошков (chemical synthesis followed with rate-controlled calcination, colloidal processing and low-temperature sintering). Разработка CGO, YSZP и YSZP/Pt нанокомпозитов: (1) synthesis of non(2) Разработка agglomerated gadolinia наноаргегатов nanopowder (3) RCC of ceria- (4) Solid solution gadolinia Impregnation of gadolinium compounds into cerium precursor compound matrix or platinum compounds into ceria and zirconia matrix precursor.
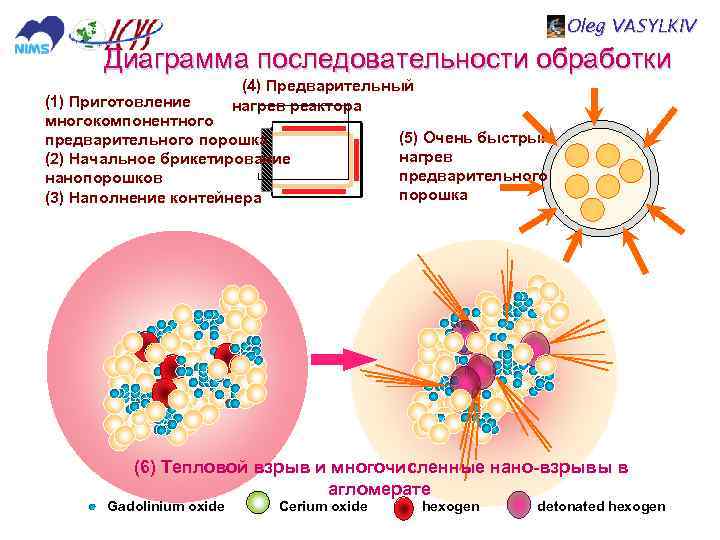
Oleg VASYLKIV Диаграмма последовательности обработки (4) Предварительный нагрев реактора (1) Приготовление многокомпонентного предварительного порошка (2) Начальное брикетирование нанопорошков (3) Наполнение контейнера (5) Очень быстрый нагрев предварительного порошка (6) Тепловой взрыв и многочисленные нано-взрывы в агломерате Gadolinium oxide Cerium oxide hexogen detonated hexogen
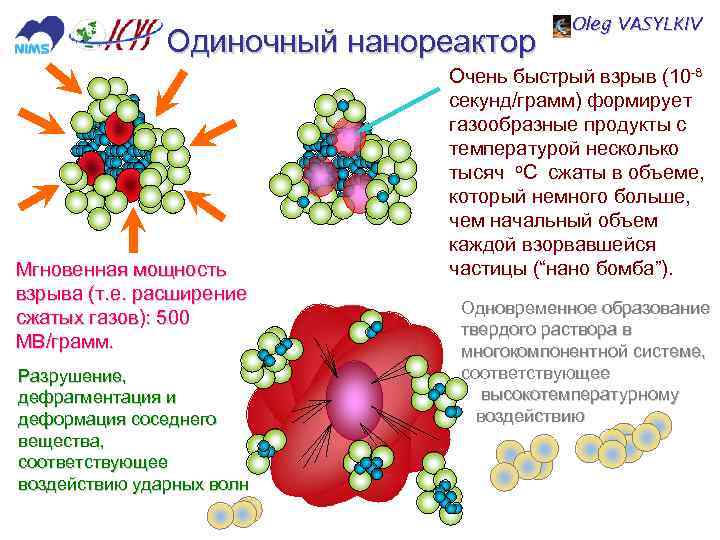
Одиночный нанореактор Мгновенная мощность взрыва (т. е. расширение сжатых газов): 500 MВ/грамм. Разрушение, дефрагментация и деформация соседнего вещества, соответствующее воздействию ударных волн Oleg VASYLKIV Очень быстрый взрыв (10 -8 секунд/грамм) формирует газообразные продукты с температурой несколько тысяч о. C сжаты в объеме, который немного больше, чем начальный объем каждой взорвавшейся частицы (“нано бомба”). Одновременное образование твердого раствора в многокомпонентной системе, соответствующее высокотемпературному воздействию

CGO наноагрегаты Oleg VASYLKIV Описанная технология открывает возможности синтеза широкого диапазона многокомпонентной керамики и металлокерамических композитных нанопорошков с унифицированной морфологией и точной стехиометрией

Метод совместного осаждения способ получения наночастиц из смеси водных растворов солей, содержащих необходимые катионы ( металлы ) путем введения реагентов, приводящих к образованию нерастворимого осадка –аморфного гидроксида. Осадок промывается, фильтруется и прокаливаеся. В результате гидроксид теряет воду и ОН- группы и превращается в оксид.

Основные характеристики нанопорошков. 1. 2. 3. 4. 5. 6. Размер частиц и их распределение Удельная поверхность Степень и жесткость агломерации Химический состав Распределение легирующих элементов Фазовый состав Проблемы 1. 2. 3. 4. 5. Уменьшение степени агломерации Монодисперсность Получение заданного размера частиц Стабильность фазового состава Химическая чистота
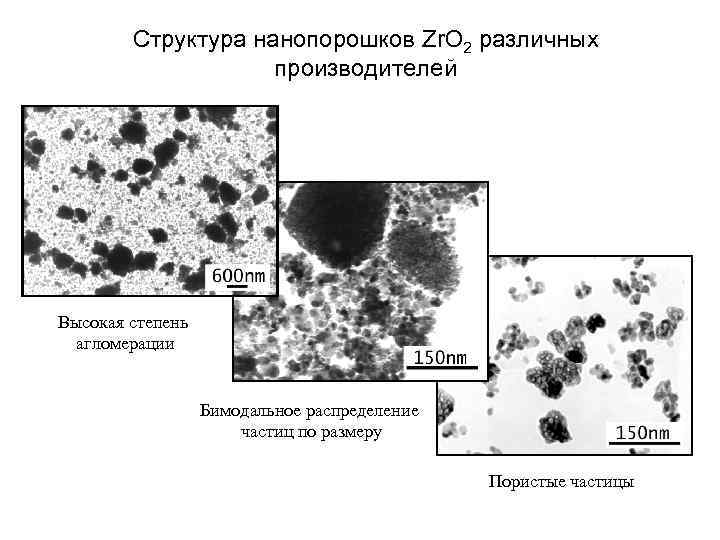
Структура нанопорошков Zr. O 2 различных производителей Высокая степень агломерации Бимодальное распределение частиц по размеру Пористые частицы

Физические воздействия в химической технологии Технология реализована для Zr. O 2, Ti. O 2, La 0. 7 Sr 0. 3 Mn. O 3 9 -th Cimtec –World Ceramics Congress, 1998, Florence
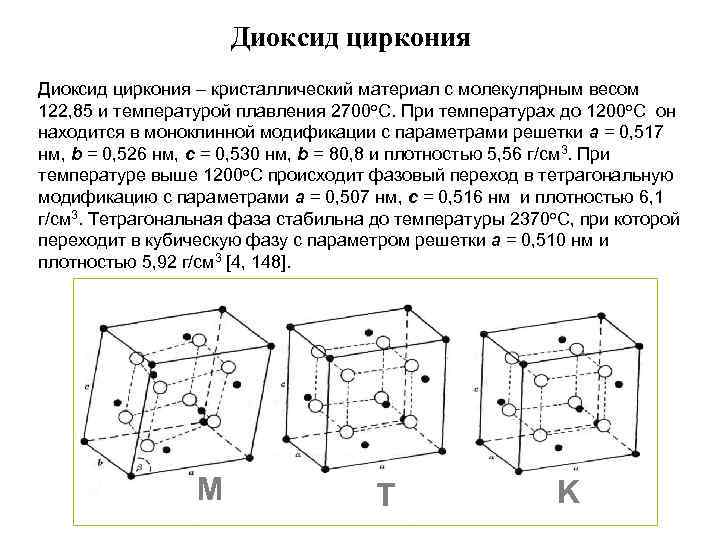
Диоксид циркония – кристаллический материал с молекулярным весом 122, 85 и температурой плавления 2700 о. С. При температурах до 1200 о. С он находится в моноклинной модификации с параметрами решетки a = 0, 517 нм, b = 0, 526 нм, c = 0, 530 нм, b = 80, 8 и плотностью 5, 56 г/см 3. При температуре выше 1200 o. С происходит фазовый переход в тетрагональную модификацию с параметрами a = 0, 507 нм, c = 0, 516 нм и плотностью 6, 1 г/см 3. Тетрагональная фаза стабильна до температуры 2370 о. С, при которой переходит в кубическую фазу с параметром решетки a = 0, 510 нм и плотностью 5, 92 г/см 3 [4, 148]. M T K
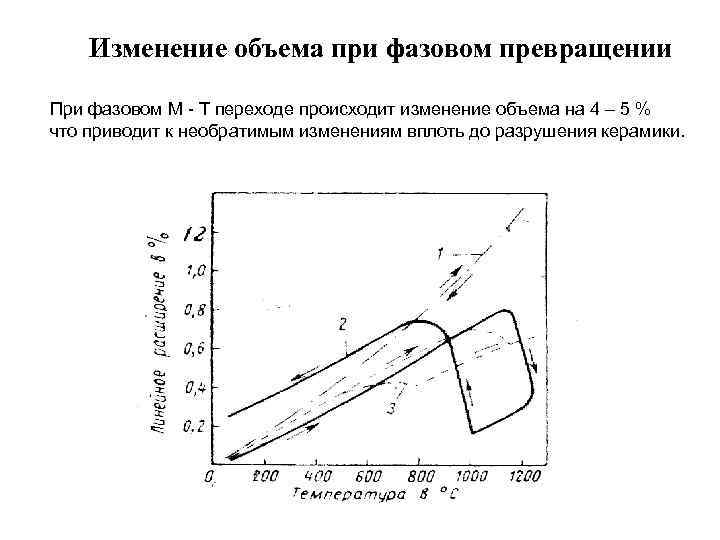
Изменение объема при фазовом превращении При фазовом М - Т переходе происходит изменение объема на 4 – 5 % что приводит к необратимым изменениям вплоть до разрушения керамики.
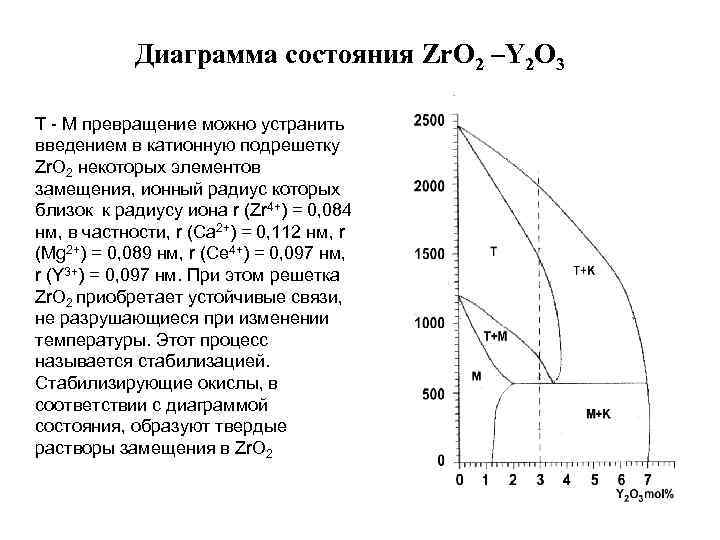
Диаграмма состояния Zr. O 2 –Y 2 O 3 T - M превращение можно устранить введением в катионную подрешетку Zr. O 2 некоторых элементов замещения, ионный радиус которых близок к радиусу иона r (Zr 4+) = 0, 084 нм, в частности, r (Ca 2+) = 0, 112 нм, r (Mg 2+) = 0, 089 нм, r (Ce 4+) = 0, 097 нм, r (Y 3+) = 0, 097 нм. При этом решетка Zr. O 2 приобретает устойчивые связи, не разрушающиеся при изменении температуры. Этот процесс называется стабилизацией. Стабилизирующие окислы, в соответствии с диаграммой состояния, образуют твердые растворы замещения в Zr. O 2
![Получение наночастиц диоксида циркония t t [Zr 4(OH)16(H 2 O)8]n Zr. O(OH)2 Zr. O Получение наночастиц диоксида циркония t t [Zr 4(OH)16(H 2 O)8]n Zr. O(OH)2 Zr. O](https://present5.com/presentation/50301259_437031769/image-42.jpg)
Получение наночастиц диоксида циркония t t [Zr 4(OH)16(H 2 O)8]n Zr. O(OH)2 Zr. O 2 o - СВЧ излучение с частотой 2, 45 ГГц, мощностью 600 Вт и 5 к. Вт; - Ультразвук частотой 18 – 22 к. Гц, мощностью 600 Вт и 10 к. Вт; - Импульсное магнитное поле напряженностью104 – 106 А/м; - Температурные воздействия в интервале 120 - 1000 о. С.

Структура порошков диоксида циркония (Zr. O 2 – 3 мол%Y 2 O 3) 700 о. С Предварительная сушка 120 о. С СВЧ
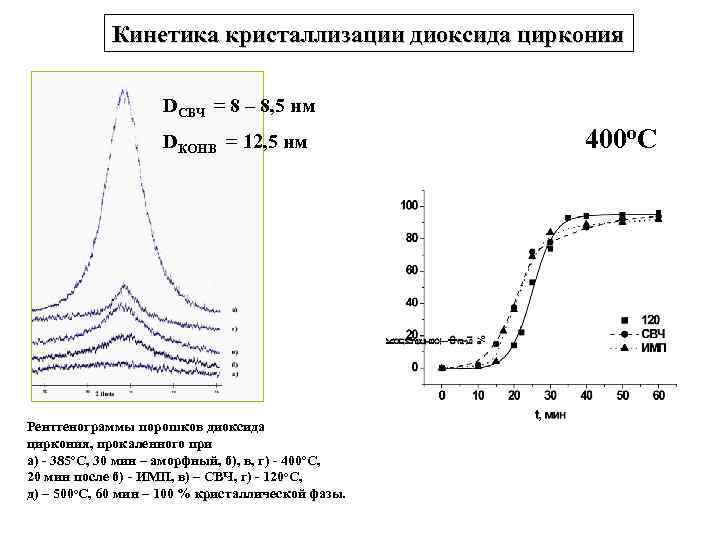
Кинетика кристаллизации диоксида циркония DСВЧ = 8 – 8, 5 нм DКОНВ = 12, 5 нм Рентгенограммы порошков диоксида циркония, прокаленного при а) - 385 о. С, 30 мин – аморфный, б), в, г) - 400 о. С, 20 мин после б) - ИМП, в) – СВЧ, г) - 120 о. С, д) – 500 о. С, 60 мин – 100 % кристаллической фазы. 400 о. С

Электроная микроскопия нанопорошков 120 о. С в ИМП
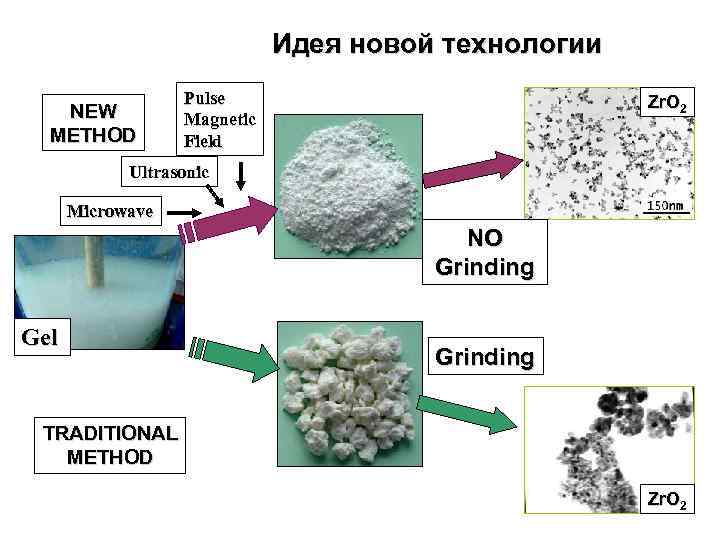
Идея новой технологии NEW METHOD Pulse Magnetic Field Zr. O 2 Ultrasonic Microwave NO Grinding Gel Grinding TRADITIONAL METHOD Zr. O 2
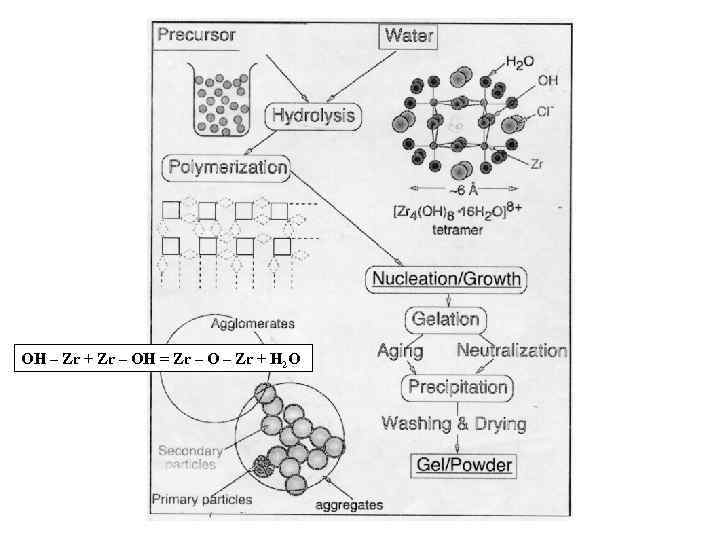
ОН – Zr + Zr – OH = Zr – O – Zr + H 2 O
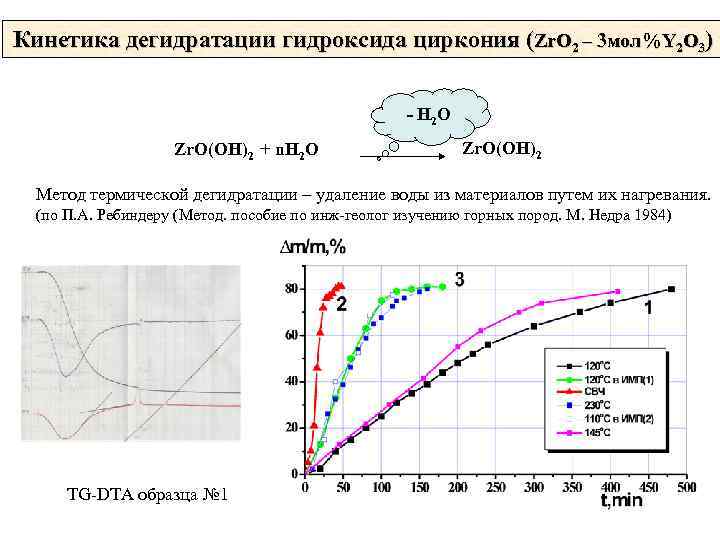
Кинетика дегидратации гидроксида циркония (Zr. O 2 – 3 мол%Y 2 O 3) - H 2 O Zr. O(OH)2 + n. H 2 O Zr. O(OH)2 Метод термической дегидратации – удаление воды из материалов путем их нагревания. (по П. А. Ребиндеру (Метод. пособие по инж-геолог изучению горных пород. М. Недра 1984) TG-DTA образца № 1
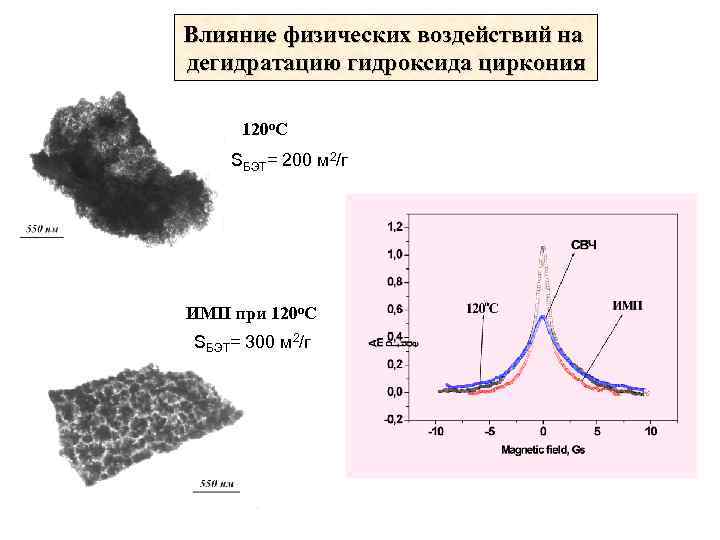
Влияние физических воздействий на дегидратацию гидроксида циркония 120 о. С SБЭТ= 200 м 2/г ИМП при 120 о. С SБЭТ= 300 м 2/г
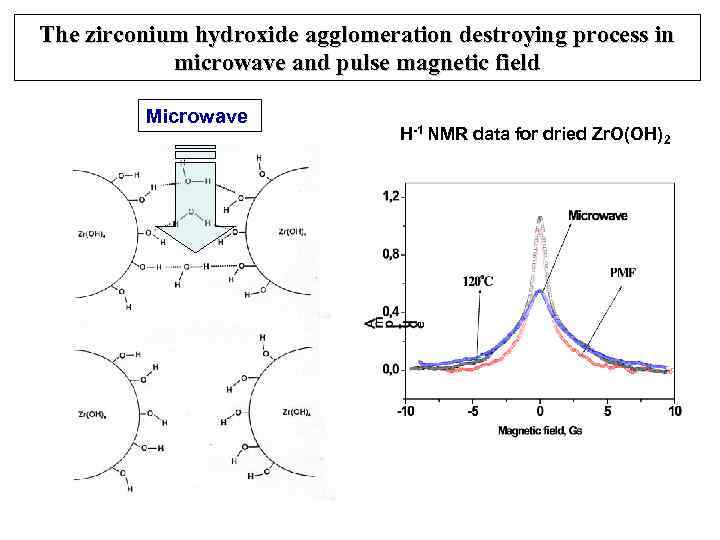
The zirconium hydroxide agglomeration destroying process in microwave and pulse magnetic field Microwave H-1 NMR data for dried Zr. O(OH)2
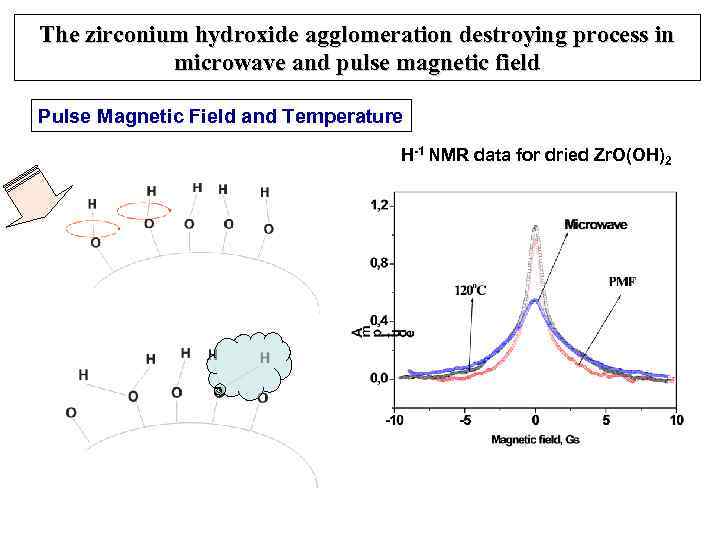
The zirconium hydroxide agglomeration destroying process in microwave and pulse magnetic field Pulse Magnetic Field and Temperature H-1 NMR data for dried Zr. O(OH)2
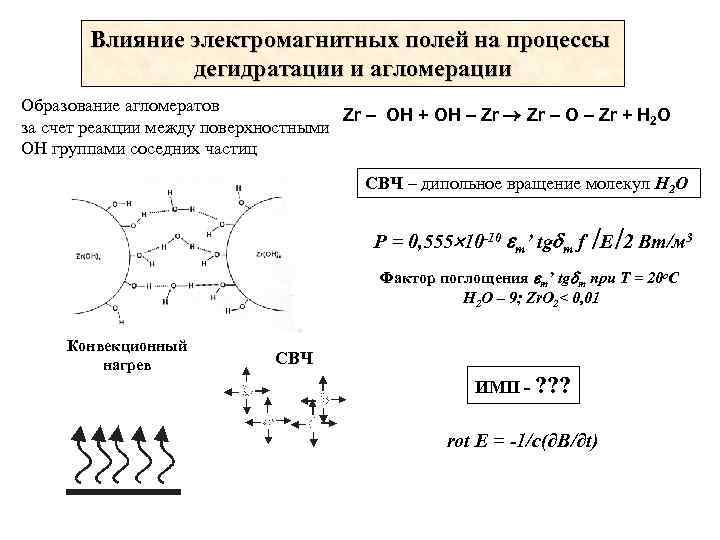
Влияние электромагнитных полей на процессы дегидратации и агломерации Образование агломератов Zr – ОН + OH – Zr – O – Zr + H 2 O за счет реакции между поверхностными ОН группами соседних частиц СВЧ – дипольное вращение молекул H 2 O Р = 0, 555 10 -10 m’ tg m f E 2 Вт/м 3 Фактор поглощения m’ tg m при Т = 20 о. С H 2 O – 9; Zr. O 2< 0, 01 Конвекционный нагрев СВЧ ИМП - ? ? ? rot E = -1/c(∂B/∂t)
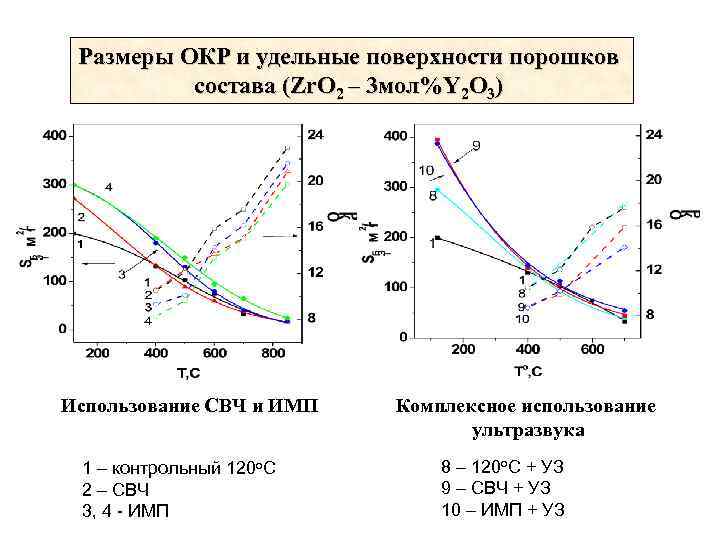
Размеры ОКР и удельные поверхности порошков состава (Zr. O 2 – 3 мол%Y 2 O 3) Использование СВЧ и ИМП 1 – контрольный 120 о. С 2 – СВЧ 3, 4 - ИМП Комплексное использование ультразвука 8 – 120 о. С + УЗ 9 – СВЧ + УЗ 10 – ИМП + УЗ
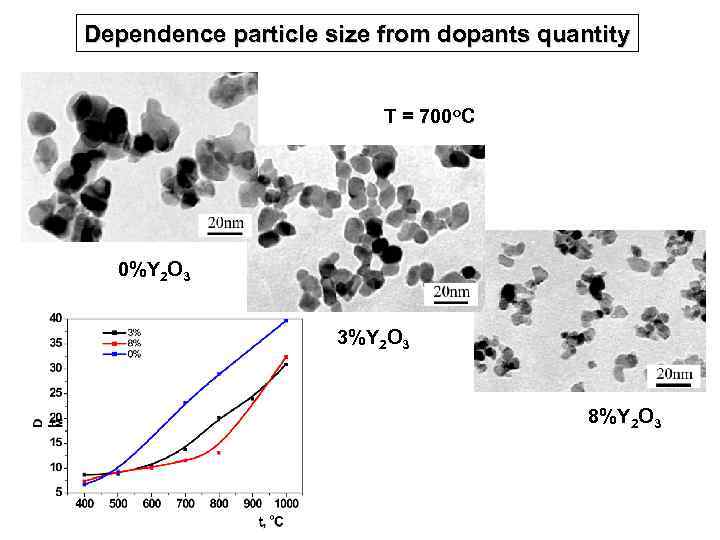
Dependence particle size from dopants quantity Т = 700 о. С 0%Y 2 O 3 3%Y 2 O 3 8%Y 2 O 3
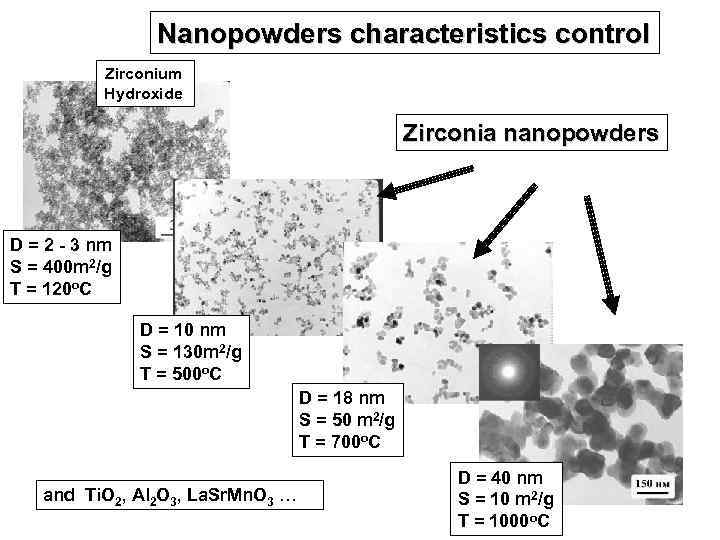
Nanopowders characteristics control Zirconium Hydroxide Zirconia nanopowders D = 2 - 3 nm S = 400 m 2/g T = 120 o. C D = 10 nm S = 130 m 2/g T = 500 o. C D = 18 nm S = 50 m 2/g T = 700 o. C and Ti. O 2, Al 2 O 3, La. Sr. Mn. O 3 … D = 40 nm S = 10 m 2/g T = 1000 o. C
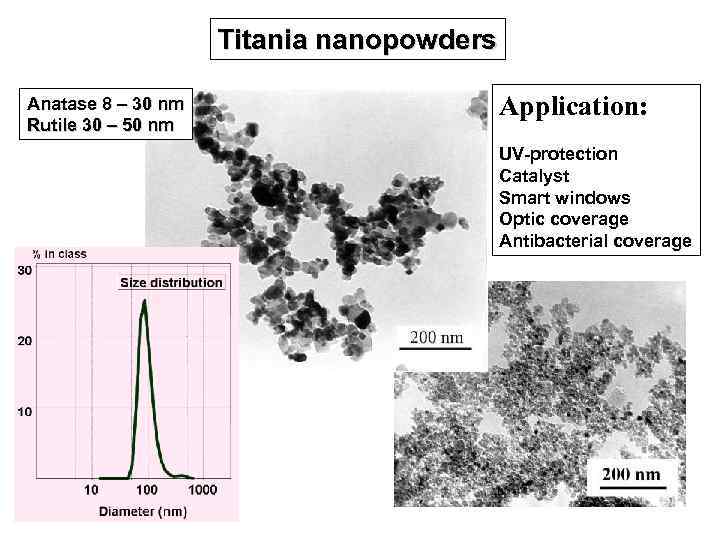
Titania nanopowders Anatase 8 – 30 nm Rutile 30 – 50 nm Application: UV-protection Catalyst Smart windows Optic coverage Antibacterial coverage
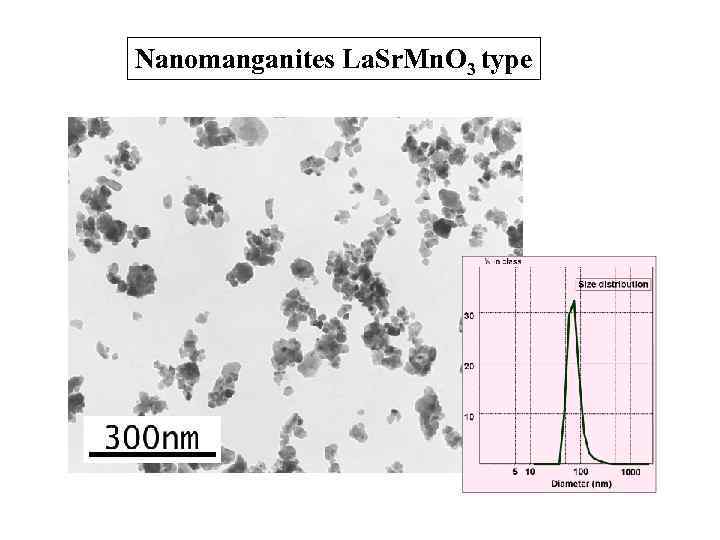
Nanomanganites La. Sr. Mn. O 3 type

Composites and ceramics pigments Ni + Zr. O 2 La. Sr. Mn. O 3 + Zr. O 2 Mg. O + Al 2 O 3 + Co. O and other
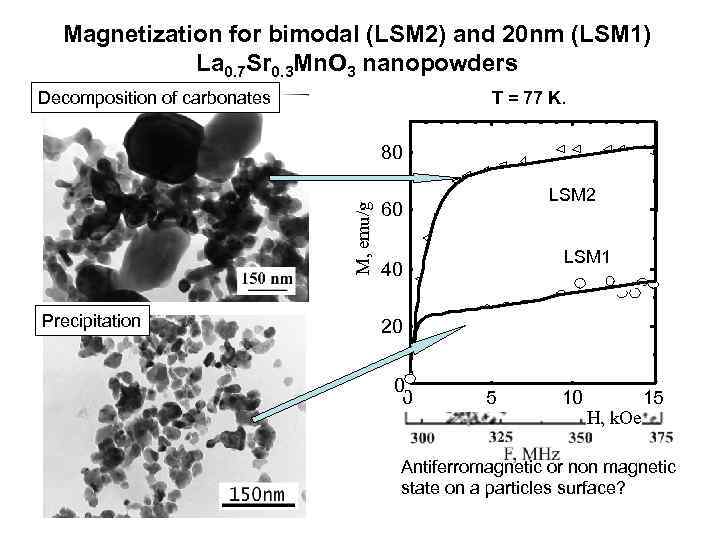
Magnetization for bimodal (LSM 2) and 20 nm (LSM 1) La 0. 7 Sr 0. 3 Mn. O 3 nanopowders Decomposition of carbonates T = 77 K. Precipitation LSM 2 60 LSM 1 40 M, emu/g 80 20 0 0 5 10 H, k. Oe 15 Antiferromagnetic or non magnetic state on a particles surface?
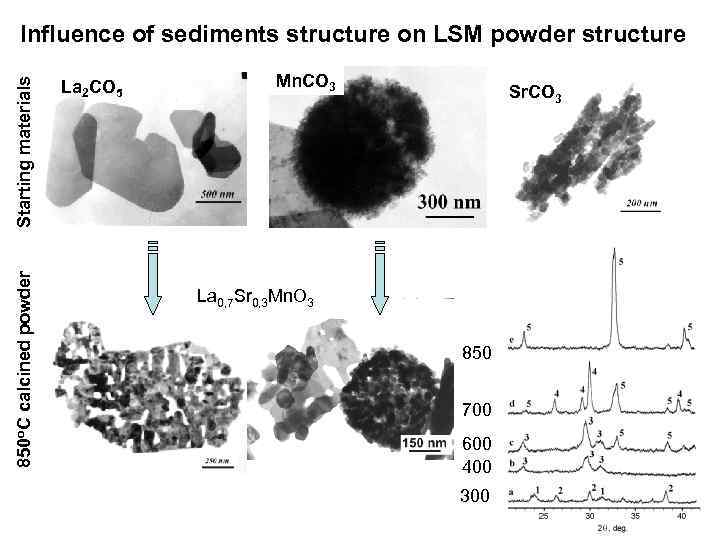
850 o. C calcined powder Starting materials Influence of sediments structure on LSM powder structure La 2 CO 5 Mn. CO 3 Sr. CO 3 La 0, 7 Sr 0, 3 Mn. O 3 850 700 600 400 300
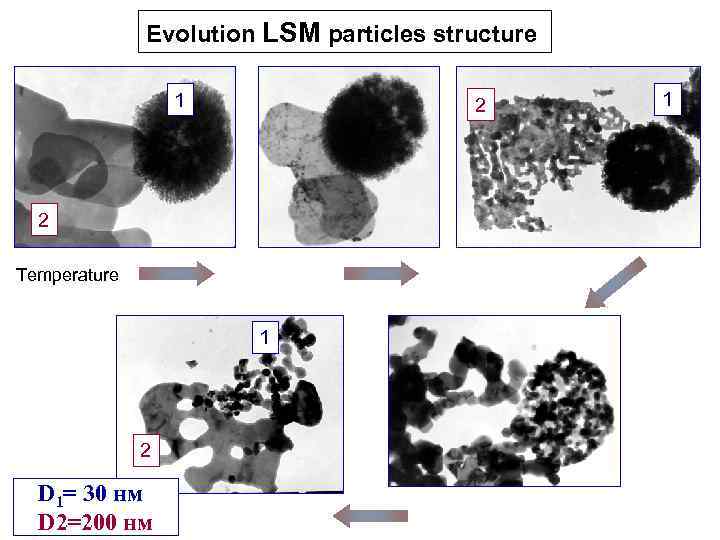
Evolution LSM particles structure 1 2 2 Temperature 1 2 D 1= 30 нм D 2=200 нм 1
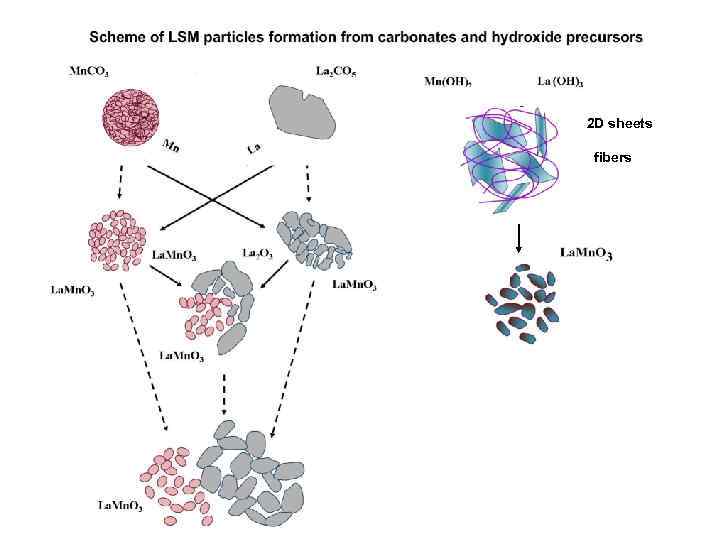
2 D sheets fibers

The influence of structure of sediments on LSM powder structure La(OH)3 La 0, 7 Sr 0, 3 Mn. O 3 Mn(OH)2 Calcinations at 600 o. C
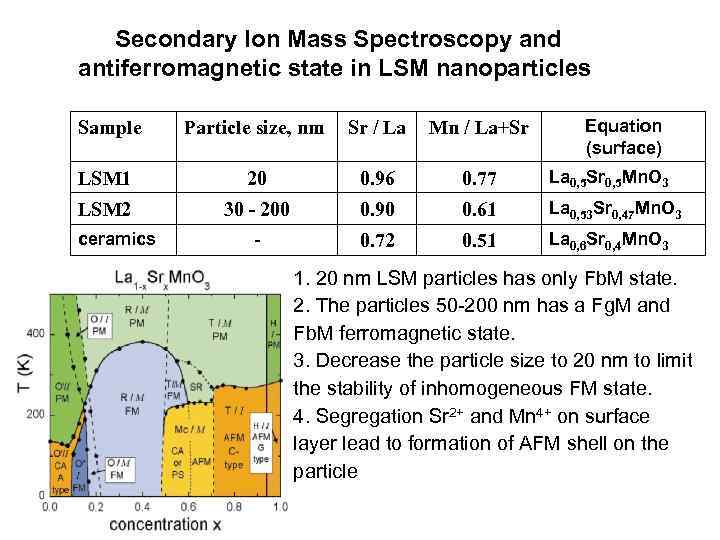
Secondary Ion Mass Spectroscopy and antiferromagnetic state in LSM nanoparticles Equation (surface) Sample Particle size, nm Sr / La Mn / La+Sr LSM 1 20 0. 96 0. 77 La 0, 5 Sr 0, 5 Mn. O 3 LSM 2 30 - 200 0. 90 0. 61 La 0, 53 Sr 0, 47 Mn. O 3 - 0. 72 0. 51 La 0, 6 Sr 0, 4 Mn. O 3 ceramics 1. 20 nm LSM particles has only Fb. M state. 2. The particles 50 -200 nm has a Fg. M and Fb. M ferromagnetic state. 3. Decrease the particle size to 20 nm to limit the stability of inhomogeneous FM state. 4. Segregation Sr 2+ and Mn 4+ on surface layer lead to formation of AFM shell on the particle
порошки.ppt