Южный Федеральный Университет Физический факультет Кафедра нанотехнологии





![Структура иона [Re 6 S 8 Cl 6]4 - Структура иона [Re 6 S 8 Cl 6]4 -](https://present5.com/presentation/3/15557033_87084937.pdf-img/15557033_87084937.pdf-9.jpg)













Кластеры и кластерные материалы.ppt
- Количество слайдов: 51
 Южный Федеральный Университет Физический факультет Кафедра нанотехнологии КЛАСТЕРЫ И КЛАСТЕРНЫЕ МАТЕРИАЛЫ Проф. В. М. Таланов
Южный Федеральный Университет Физический факультет Кафедра нанотехнологии КЛАСТЕРЫ И КЛАСТЕРНЫЕ МАТЕРИАЛЫ Проф. В. М. Таланов
 Al 60 Mn 11 Ni 4 Ga 137 Mn 123 План лекции 1. Что такое кластеры? 2. Классификация кластеров 3. Кластеры металлов 4. Оболочечная модель электронной структуры кластеров 5. Модель желе 6. Химическая связь в кластерных комплексах переходных элементов и их свойства 7. Размерные физические эффекты 8. Молекулярные гигантские кластеры металлов 9. Кластерные материалы 10. Методы получения кластеров
Al 60 Mn 11 Ni 4 Ga 137 Mn 123 План лекции 1. Что такое кластеры? 2. Классификация кластеров 3. Кластеры металлов 4. Оболочечная модель электронной структуры кластеров 5. Модель желе 6. Химическая связь в кластерных комплексах переходных элементов и их свойства 7. Размерные физические эффекты 8. Молекулярные гигантские кластеры металлов 9. Кластерные материалы 10. Методы получения кластеров
 1. Что такое кластеры? Термин “кластер” начал широко использоваться в научной литературе в 70 -е годы, хотя первое полиядерное соединение Ta 6 Cl 14 H 2 O с гомоатомными связями Ta–Ta было получено еще в 1907 году. Основной смысл, вкладываемый в этот термин состоит в замкнутости , структурной выделенности определенной группировки атомов, связанных между собой гомоатомными вязями. с Способность большого числа атомов образовывать между собой гомоатомные ковалентные связи – отличительная особенность атомов углерода. В химии давно известны и другие вещества, содержащие гомоатомные связи: в молекуле озона O 3 таких связей две, в P 4 – шесть, в ромбической сере S 8 –— восемь связей. В 10 -20 -х годах прошлого века были получены многочисленные бороводороды , в структурах которых присутствовали цепи и каркасы из атомов бора. Но особое значение имеют кластеры из металлических атомов. В 30 -х годах гомоатомные связи металл-металл были открыты в многозарядных катионах Sn 9 4– и Bi 9 5+ , входящих в состав т называемых фаз Цинтля.
1. Что такое кластеры? Термин “кластер” начал широко использоваться в научной литературе в 70 -е годы, хотя первое полиядерное соединение Ta 6 Cl 14 H 2 O с гомоатомными связями Ta–Ta было получено еще в 1907 году. Основной смысл, вкладываемый в этот термин состоит в замкнутости , структурной выделенности определенной группировки атомов, связанных между собой гомоатомными вязями. с Способность большого числа атомов образовывать между собой гомоатомные ковалентные связи – отличительная особенность атомов углерода. В химии давно известны и другие вещества, содержащие гомоатомные связи: в молекуле озона O 3 таких связей две, в P 4 – шесть, в ромбической сере S 8 –— восемь связей. В 10 -20 -х годах прошлого века были получены многочисленные бороводороды , в структурах которых присутствовали цепи и каркасы из атомов бора. Но особое значение имеют кластеры из металлических атомов. В 30 -х годах гомоатомные связи металл-металл были открыты в многозарядных катионах Sn 9 4– и Bi 9 5+ , входящих в состав т называемых фаз Цинтля.
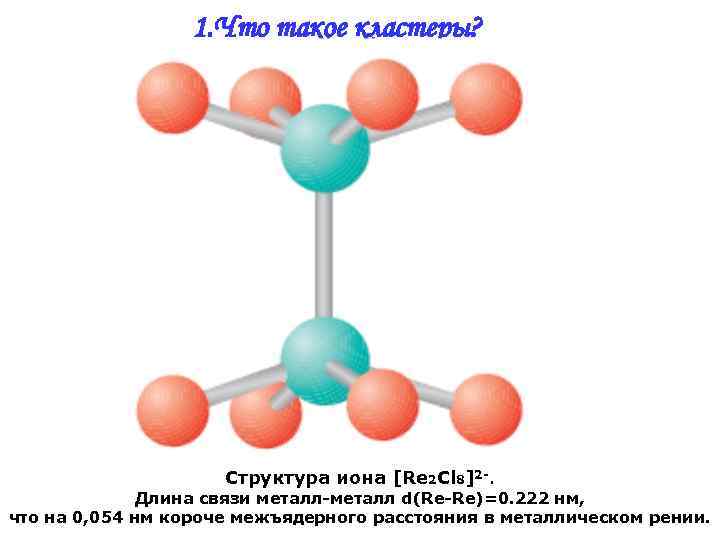
 1. Что такое кластеры? Структура иона [Re 2 Cl 8]2 -. Длина связи металл-металл d(Re-Re)=0. 222 нм, что на 0, 054 нм короче межъядерного расстояния в металлическом рении.
1. Что такое кластеры? Структура иона [Re 2 Cl 8]2 -. Длина связи металл-металл d(Re-Re)=0. 222 нм, что на 0, 054 нм короче межъядерного расстояния в металлическом рении.
 1. Что такое кластеры? Кластеры, как замкнутые структурные образования из атомов одного ( гомоядерные ) или нескольких ( гетероядерные ) элементо относятся к 0 D – наноструктурам. Кластеры состоят из различного числа атомов – от единиц до десятков и сотен тысяч, поэтому занимают промежуточную область между отдельными атомами и микроскопическими образованиями и проявляют свойства, отличные от тех и других. Их физические характеристики существенно зависят от вида и числа входящих в них атомов. С уменьшением размеров кластеры теряют металлические свойства, т. е. характер химической связи в кластере зависит от его размера. Кластеры Au , состоящие менее чем из 100 атомов металлическими свойствами не обладают. Металлические свойства начинают проявляться, начиная со 150 -500 атомов. В кластерах Na металлические свойства проявляются для числа атомов свыше 10 -300 атомов. У кластеров Fe , состоящих из 13 атомов, проявляются неметаллические свойства, а из 35 атомов – металлические. Кластеры могут существовать как самостоятельно, так и входить в состав сложных структур, образуя 0 D – и 1 D – наноматериалы. В кластерном состоянии могу находиться любые металлы и сплавы, карбиды, нитриды, оксиды, бориды, сульфиды и другие соединения, в том числе керамические и композиционные.
1. Что такое кластеры? Кластеры, как замкнутые структурные образования из атомов одного ( гомоядерные ) или нескольких ( гетероядерные ) элементо относятся к 0 D – наноструктурам. Кластеры состоят из различного числа атомов – от единиц до десятков и сотен тысяч, поэтому занимают промежуточную область между отдельными атомами и микроскопическими образованиями и проявляют свойства, отличные от тех и других. Их физические характеристики существенно зависят от вида и числа входящих в них атомов. С уменьшением размеров кластеры теряют металлические свойства, т. е. характер химической связи в кластере зависит от его размера. Кластеры Au , состоящие менее чем из 100 атомов металлическими свойствами не обладают. Металлические свойства начинают проявляться, начиная со 150 -500 атомов. В кластерах Na металлические свойства проявляются для числа атомов свыше 10 -300 атомов. У кластеров Fe , состоящих из 13 атомов, проявляются неметаллические свойства, а из 35 атомов – металлические. Кластеры могут существовать как самостоятельно, так и входить в состав сложных структур, образуя 0 D – и 1 D – наноматериалы. В кластерном состоянии могу находиться любые металлы и сплавы, карбиды, нитриды, оксиды, бориды, сульфиды и другие соединения, в том числе керамические и композиционные.
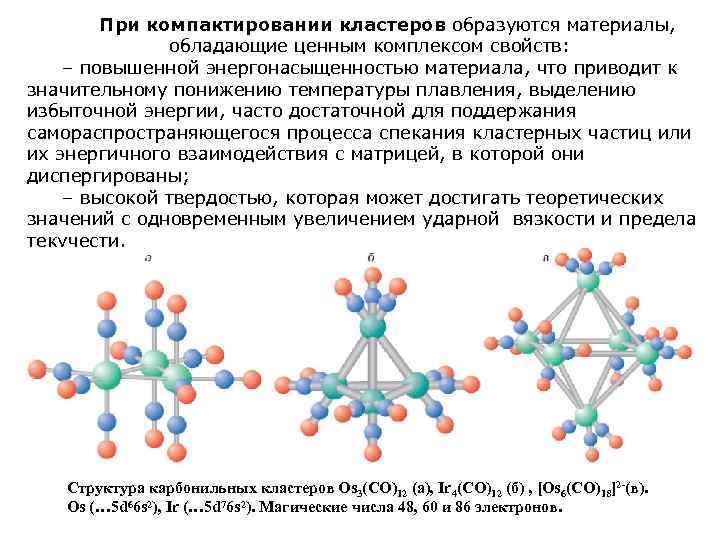
 При компактировании кластеров образуются материалы, обладающие ценным комплексом свойств: – повышенной энергонасыщенностью материала, что приводит к значительному понижению температуры плавления, выделению избыточной энергии, часто достаточной для поддержания самораспространяющегося процесса спекания кластерных частиц или их энергичного взаимодействия с матрицей, в которой они диспергированы; – высокой твердостью, которая может достигать теоретических значений с одновременным увеличением ударной вязкости и предела текучести. Структура карбонильных кластеров Os 3(CO)12 (а), Ir 4(CO)12 (б) , [Os 6(CO)18]2 -(в). Os (… 5 d 66 s 2), Ir (… 5 d 76 s 2). Магические числа 48, 60 и 86 электронов.
При компактировании кластеров образуются материалы, обладающие ценным комплексом свойств: – повышенной энергонасыщенностью материала, что приводит к значительному понижению температуры плавления, выделению избыточной энергии, часто достаточной для поддержания самораспространяющегося процесса спекания кластерных частиц или их энергичного взаимодействия с матрицей, в которой они диспергированы; – высокой твердостью, которая может достигать теоретических значений с одновременным увеличением ударной вязкости и предела текучести. Структура карбонильных кластеров Os 3(CO)12 (а), Ir 4(CO)12 (б) , [Os 6(CO)18]2 -(в). Os (… 5 d 66 s 2), Ir (… 5 d 76 s 2). Магические числа 48, 60 и 86 электронов.
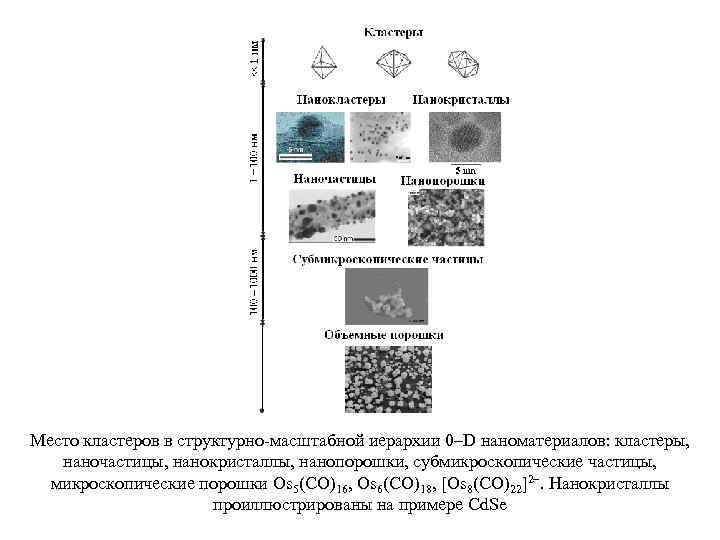
 Место кластеров в структурно-масштабной иерархии 0–D наноматериалов: кластеры, наночастицы, нанокристаллы, нанопорошки, субмикроскопические частицы, микроскопические порошки Os 5(CO)16, Os 6(CO)18, [Os 8(CO)22]2–. Нанокристаллы проиллюстрированы на примере Cd. Se
Место кластеров в структурно-масштабной иерархии 0–D наноматериалов: кластеры, наночастицы, нанокристаллы, нанопорошки, субмикроскопические частицы, микроскопические порошки Os 5(CO)16, Os 6(CO)18, [Os 8(CO)22]2–. Нанокристаллы проиллюстрированы на примере Cd. Se
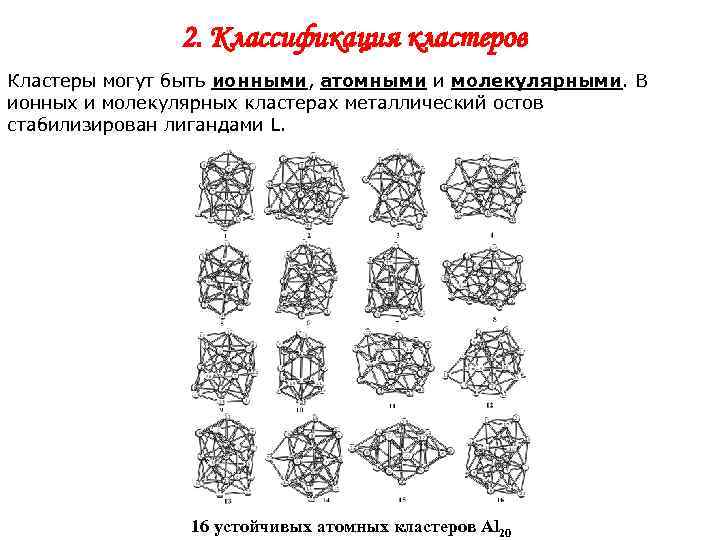
 2. Классификация кластеров Кластеры могут быть ионными, атомными и молекулярными. В ионных и молекулярных кластерах металлический остов стабилизирован лигандами L. 16 устойчивых атомных кластеров Al 20
2. Классификация кластеров Кластеры могут быть ионными, атомными и молекулярными. В ионных и молекулярных кластерах металлический остов стабилизирован лигандами L. 16 устойчивых атомных кластеров Al 20
![>Структура иона [Re 6 S 8 Cl 6]4 - >Структура иона [Re 6 S 8 Cl 6]4 -](https://present5.com/presentation/3/15557033_87084937.pdf-img/15557033_87084937.pdf-9.jpg) Структура иона [Re 6 S 8 Cl 6]4 -
Структура иона [Re 6 S 8 Cl 6]4 -
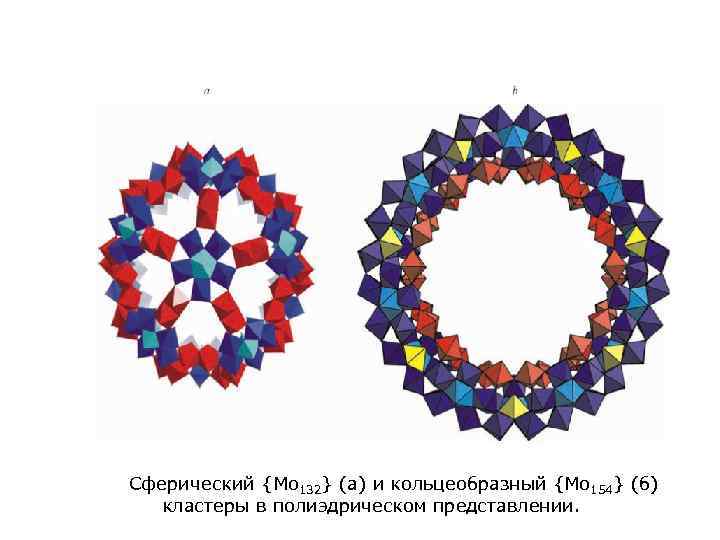
 Сферический {Mo 132} (a) и кольцеобразный {Mo 154} (б) кластеры в полиэдрическом представлении.
Сферический {Mo 132} (a) и кольцеобразный {Mo 154} (б) кластеры в полиэдрическом представлении.
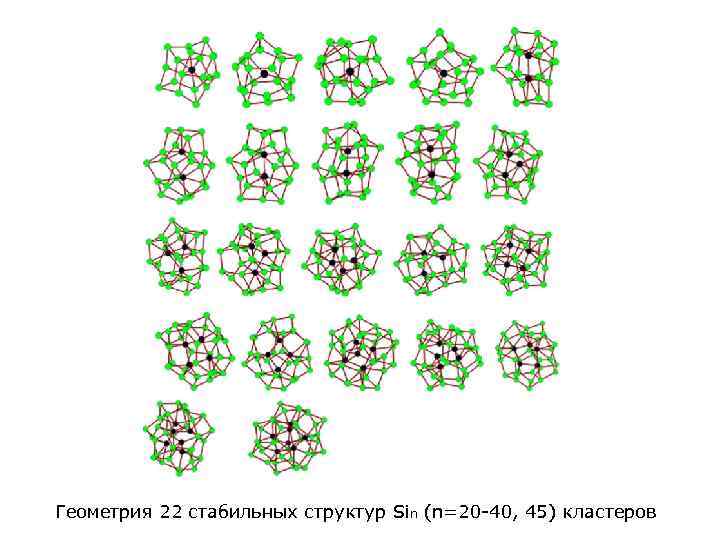
 Геометрия 22 стабильных структур Sin (n=20 -40, 45) кластеров
Геометрия 22 стабильных структур Sin (n=20 -40, 45) кластеров
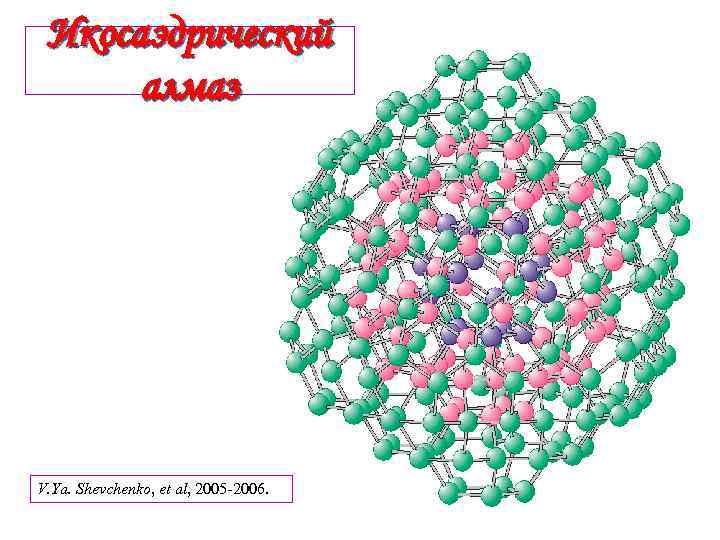
 Икосаэдрический алмаз V. Ya. Shevchenko, et al, 2005 -2006.
Икосаэдрический алмаз V. Ya. Shevchenko, et al, 2005 -2006.
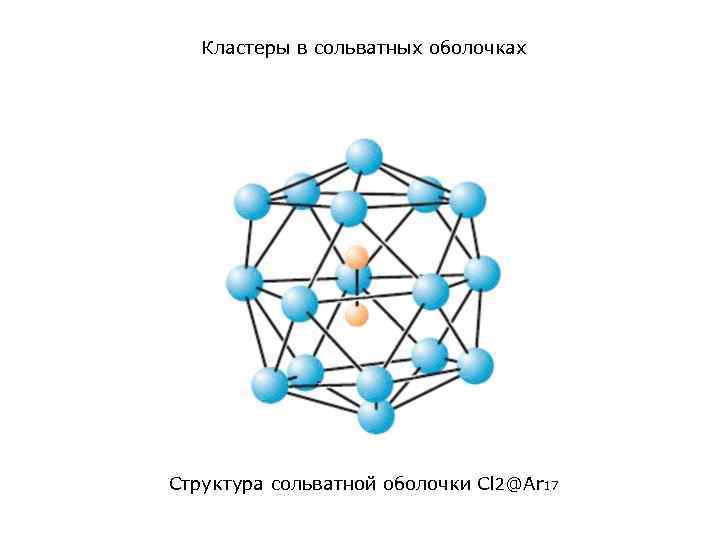
 Кластеры в сольватных оболочках Структура сольватной оболочки Сl 2@Ar 17
Кластеры в сольватных оболочках Структура сольватной оболочки Сl 2@Ar 17
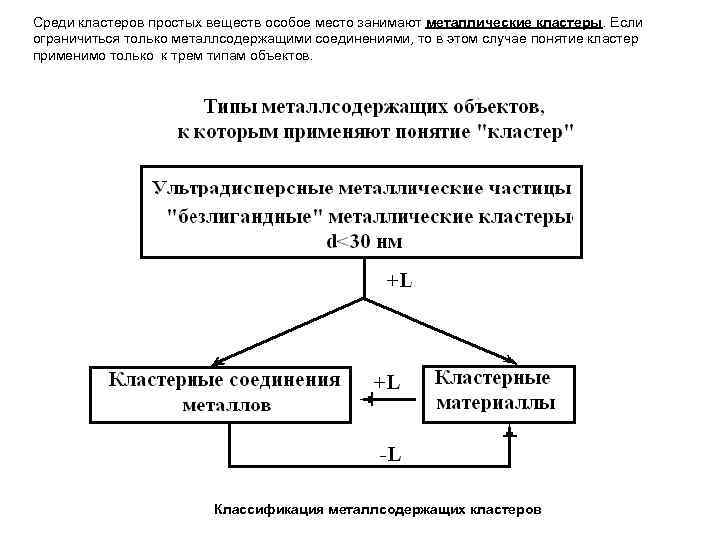
 Среди кластеров простых веществ особое место занимают металлические кластеры. Если ограничиться только металлсодержащими соединениями, то в этом случае понятие кластер применимо только к трем типам объектов. Классификация металлсодержащих кластеров
Среди кластеров простых веществ особое место занимают металлические кластеры. Если ограничиться только металлсодержащими соединениями, то в этом случае понятие кластер применимо только к трем типам объектов. Классификация металлсодержащих кластеров
 Частицы с диаметром менее 30 нм называют ультрадисперсными. Металлические кластеры по своей природе являются неравновесными образованиями и характеризуются высокой плотностью электронных состояний и обладают большим запасом внутренней энергии. Это означает, что кластеры – неустойчивые образования, стремящиеся к самопроизвольной агрегации и активному взаимодействию со средой, в которой они находятся. Поэтому проблема их стабилизации – это центральная проблема химии и физики кластеров. Для стабилизации кластеров их окружают лигандами, в качестве которых могут быть молекулы CO, NH 3, органические cоединения, полимеры. Условно выделяют две группы соединений: молекулярные кластерные соединения или полимерные соединения, содержащие кластеры и кластерные материалы. Кластерные соединения – соединения металлов, молекулы которых содержат окруженный лигандами остов из атомов металлов, находящихся на расстояниях, допускающих прямое взаимодействие металл-металл. Кластерные материалы – вещества, в составе которых имеются группировки из атомов металлов, находящихся на расстояниях, допускающих взаимодействие металл-металл. Кластерные материалы содержат металлоцепи, металлоциклы, металлополиэдры. К кластерным материалам относятся также вещества, содержащие в матрицах органических полимеров или цеолитов металлические атомы.
Частицы с диаметром менее 30 нм называют ультрадисперсными. Металлические кластеры по своей природе являются неравновесными образованиями и характеризуются высокой плотностью электронных состояний и обладают большим запасом внутренней энергии. Это означает, что кластеры – неустойчивые образования, стремящиеся к самопроизвольной агрегации и активному взаимодействию со средой, в которой они находятся. Поэтому проблема их стабилизации – это центральная проблема химии и физики кластеров. Для стабилизации кластеров их окружают лигандами, в качестве которых могут быть молекулы CO, NH 3, органические cоединения, полимеры. Условно выделяют две группы соединений: молекулярные кластерные соединения или полимерные соединения, содержащие кластеры и кластерные материалы. Кластерные соединения – соединения металлов, молекулы которых содержат окруженный лигандами остов из атомов металлов, находящихся на расстояниях, допускающих прямое взаимодействие металл-металл. Кластерные материалы – вещества, в составе которых имеются группировки из атомов металлов, находящихся на расстояниях, допускающих взаимодействие металл-металл. Кластерные материалы содержат металлоцепи, металлоциклы, металлополиэдры. К кластерным материалам относятся также вещества, содержащие в матрицах органических полимеров или цеолитов металлические атомы.
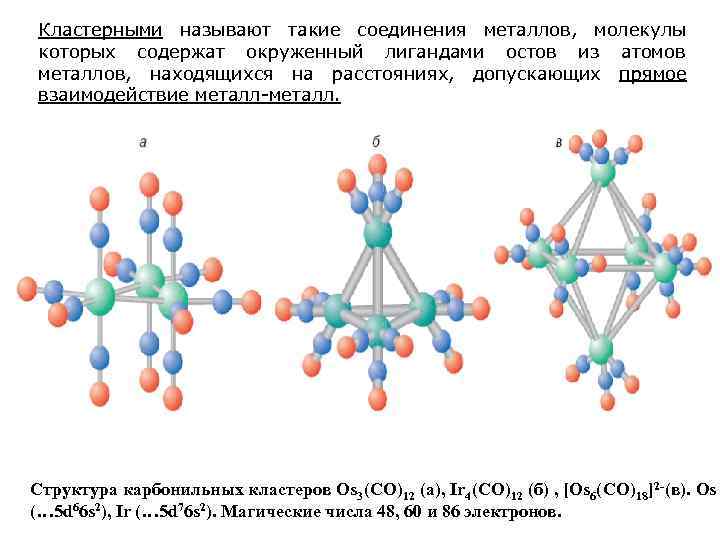
 Кластерными называют такие соединения металлов, молекулы которых содержат окруженный лигандами остов из атомов металлов, находящихся на расстояниях, допускающих прямое взаимодействие металл-металл. Структура карбонильных кластеров Os 3(CO)12 (а), Ir 4(CO)12 (б) , [Os 6(CO)18]2 -(в). Os (… 5 d 66 s 2), Ir (… 5 d 76 s 2). Магические числа 48, 60 и 86 электронов.
Кластерными называют такие соединения металлов, молекулы которых содержат окруженный лигандами остов из атомов металлов, находящихся на расстояниях, допускающих прямое взаимодействие металл-металл. Структура карбонильных кластеров Os 3(CO)12 (а), Ir 4(CO)12 (б) , [Os 6(CO)18]2 -(в). Os (… 5 d 66 s 2), Ir (… 5 d 76 s 2). Магические числа 48, 60 и 86 электронов.
 Связь между ультрадисперсными металлическими частицами и кластерными соединениями металлов
Связь между ультрадисперсными металлическими частицами и кластерными соединениями металлов
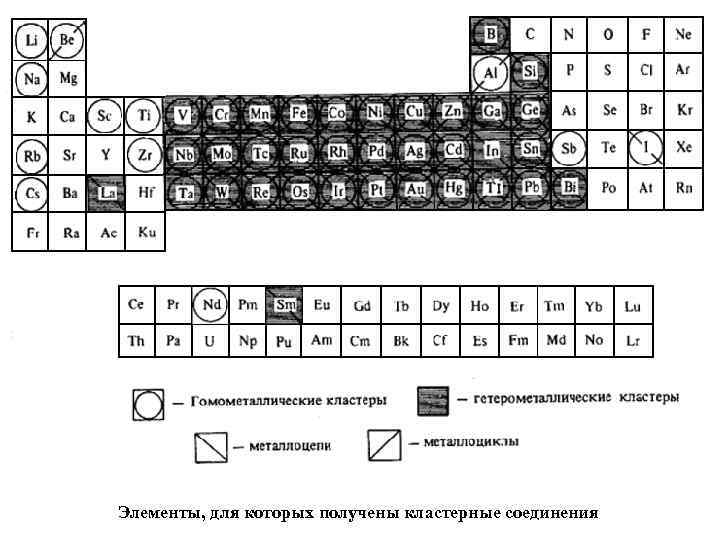
 Элементы, для которых получены кластерные соединения
Элементы, для которых получены кластерные соединения
 3. Кластеры металлов Каково типичное время формирования кластеров? Пусть металлический сферический кластер находится в инертной среде. Типичная температура T v и давление Р v испарения для металлов порядка 1000– 1500 К и 1– 10 мбар соответственно. Рассмотрим рост нанокластера радиусом R в 1 нм, в котором находится 100– 200 атомов. Кинетическая теория газов дает для атомного потока Фv (то есть, числа металлических атомов в секунду, попадающих на поверхность кластера) Фv = рv. Аeff/(2πmvk. BTv)1/2, где А eff = 4 π R 2 , и m v – масса атомов. Это дает Ф v ~ 10 7 c соответствуя времени = Фv– 1 ~ 102 нc. Таким образом, кластер из 103 атомов выращен за миллисекунды. С помощью масс-спектроскопии можно выделить кластеры с числом атомов или молекул, обеспечивающим им наибольшую стабильность. Число атомов (или молекул) у такого стабильного кластера носит название магического числа. Согласно определению кластера наибольшие значения магических чисел и характеризуют кластеры с максимальным числом атомов или молекул.
3. Кластеры металлов Каково типичное время формирования кластеров? Пусть металлический сферический кластер находится в инертной среде. Типичная температура T v и давление Р v испарения для металлов порядка 1000– 1500 К и 1– 10 мбар соответственно. Рассмотрим рост нанокластера радиусом R в 1 нм, в котором находится 100– 200 атомов. Кинетическая теория газов дает для атомного потока Фv (то есть, числа металлических атомов в секунду, попадающих на поверхность кластера) Фv = рv. Аeff/(2πmvk. BTv)1/2, где А eff = 4 π R 2 , и m v – масса атомов. Это дает Ф v ~ 10 7 c соответствуя времени = Фv– 1 ~ 102 нc. Таким образом, кластер из 103 атомов выращен за миллисекунды. С помощью масс-спектроскопии можно выделить кластеры с числом атомов или молекул, обеспечивающим им наибольшую стабильность. Число атомов (или молекул) у такого стабильного кластера носит название магического числа. Согласно определению кластера наибольшие значения магических чисел и характеризуют кластеры с максимальным числом атомов или молекул.
 3. Кластеры металлов Установлено, что кластеры гелия Hen имеют магические числа n = 7, 10, 14, 30 для обоих изотопов и n =23 для изотопа 4 Не. Магические числа для кластеров неона Ne n n =13, 21, 55, 75, для кластеров аргона Ar n =14, 16, 19, 21, 23, 27, для кластеров криптона Kr n =14, 16, 19, 22, 27, 29, 75, 87, для кластеров ксенона Xe n =13, 16, 19, 25, 55, 71, 87, 147. Отметим, что икосаэдр – аналог кристаллической системы с плотной упаковкой, имеющей структуру гранецентрированной кубической решетки. Такую структуру обычно имеют кристаллы инертного газа. Поэтому для кластеров инертного газа структура икосаэдра наиболее приемлема. Икосаэдр можно представить как систему с оболочечной структурой, причем магические числа отвечают заполнению соответствующей оболочки и даются формулой n = (10 N 3 – 15 N 2 + 11 N – 3)/3, где N – номер оболочки. Из этой формулы находим последовательность магических чисел n = 1, 13, 55, 147, 309, 567
3. Кластеры металлов Установлено, что кластеры гелия Hen имеют магические числа n = 7, 10, 14, 30 для обоих изотопов и n =23 для изотопа 4 Не. Магические числа для кластеров неона Ne n n =13, 21, 55, 75, для кластеров аргона Ar n =14, 16, 19, 21, 23, 27, для кластеров криптона Kr n =14, 16, 19, 22, 27, 29, 75, 87, для кластеров ксенона Xe n =13, 16, 19, 25, 55, 71, 87, 147. Отметим, что икосаэдр – аналог кристаллической системы с плотной упаковкой, имеющей структуру гранецентрированной кубической решетки. Такую структуру обычно имеют кристаллы инертного газа. Поэтому для кластеров инертного газа структура икосаэдра наиболее приемлема. Икосаэдр можно представить как систему с оболочечной структурой, причем магические числа отвечают заполнению соответствующей оболочки и даются формулой n = (10 N 3 – 15 N 2 + 11 N – 3)/3, где N – номер оболочки. Из этой формулы находим последовательность магических чисел n = 1, 13, 55, 147, 309, 567
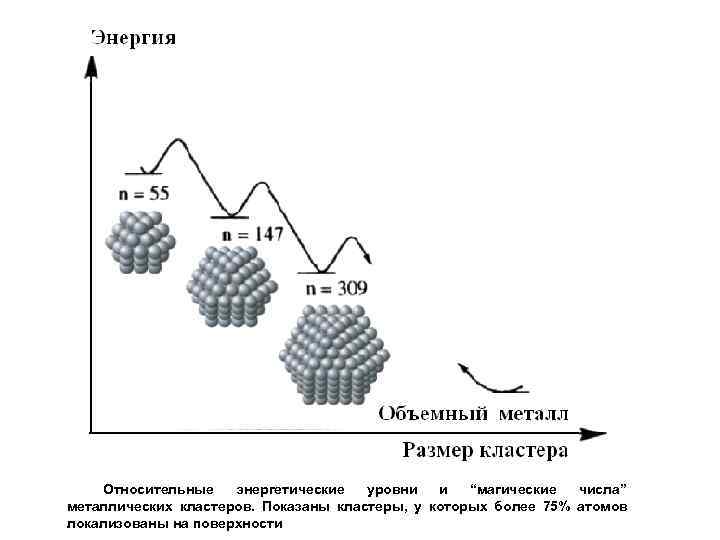
 Относительные энергетические уровни и “магические числа” металлических кластеров. Показаны кластеры, у которых более 75% атомов локализованы на поверхности
Относительные энергетические уровни и “магические числа” металлических кластеров. Показаны кластеры, у которых более 75% атомов локализованы на поверхности
 3. Кластеры металлов Кластеры щелочных металлов имеют простое электронное строение; в каждом атоме на внешнем энергетическом уровне имеется один s–электрон. Такие s 1 –кластеры образуются в атомных или молекулярных пучках в высоком вакууме, они не имеют лигандов и представляют собой удобный объект для изучения электронных свойств наноразмерных (1– 2 нм) структур. Как и для молекул, основными параметрами, которые поддаются измерению и интерпретации, являются энергия ионизации, энергия сродства к электрону, энергия диссоциации и оптическое поглощение кластеров. Исследовав эти величины, можно строить кластерные модели, характеризующие их свойства. Кластеры, наночастицы металлов агрегируют в определенной последовательности, образуя ансамбли с периодичностью состава, числа атомов в частице, формы и способа организации. Так, атомы натрия образуют устойчивые одновалентные частицы Na 3 , Na 9 , Na 19 и галогеноподобные кластеры Na 7 N обладающие повышенной химической активностью. Наименьшую активность проявляют частицы с закрытыми электронными оболочками катионы Na 2 , Na 8 , Na 18 , Na 20. Магические числа, установленные для кластеров Nan, составляют n = 2, 8, 20, 40, 58, 92, что хорошо соответствует набору магических чисел для модели жестких сфер.
3. Кластеры металлов Кластеры щелочных металлов имеют простое электронное строение; в каждом атоме на внешнем энергетическом уровне имеется один s–электрон. Такие s 1 –кластеры образуются в атомных или молекулярных пучках в высоком вакууме, они не имеют лигандов и представляют собой удобный объект для изучения электронных свойств наноразмерных (1– 2 нм) структур. Как и для молекул, основными параметрами, которые поддаются измерению и интерпретации, являются энергия ионизации, энергия сродства к электрону, энергия диссоциации и оптическое поглощение кластеров. Исследовав эти величины, можно строить кластерные модели, характеризующие их свойства. Кластеры, наночастицы металлов агрегируют в определенной последовательности, образуя ансамбли с периодичностью состава, числа атомов в частице, формы и способа организации. Так, атомы натрия образуют устойчивые одновалентные частицы Na 3 , Na 9 , Na 19 и галогеноподобные кластеры Na 7 N обладающие повышенной химической активностью. Наименьшую активность проявляют частицы с закрытыми электронными оболочками катионы Na 2 , Na 8 , Na 18 , Na 20. Магические числа, установленные для кластеров Nan, составляют n = 2, 8, 20, 40, 58, 92, что хорошо соответствует набору магических чисел для модели жестких сфер.
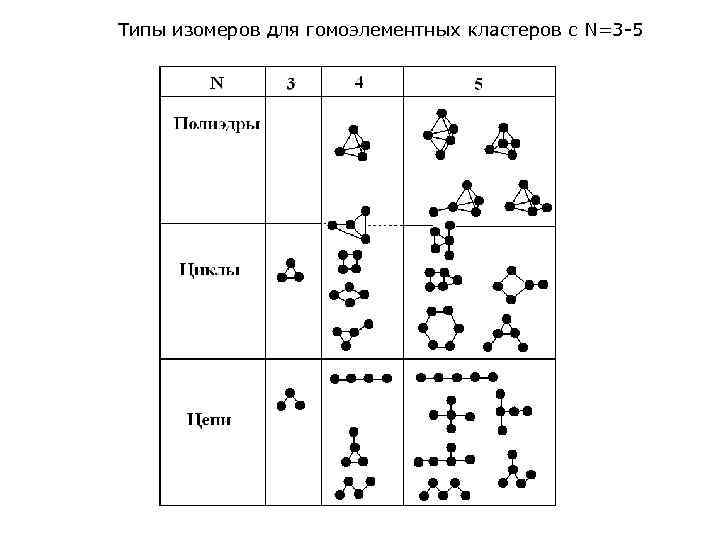
 Типы изомеров для гомоэлементных кластеров с N=3 -5
Типы изомеров для гомоэлементных кластеров с N=3 -5
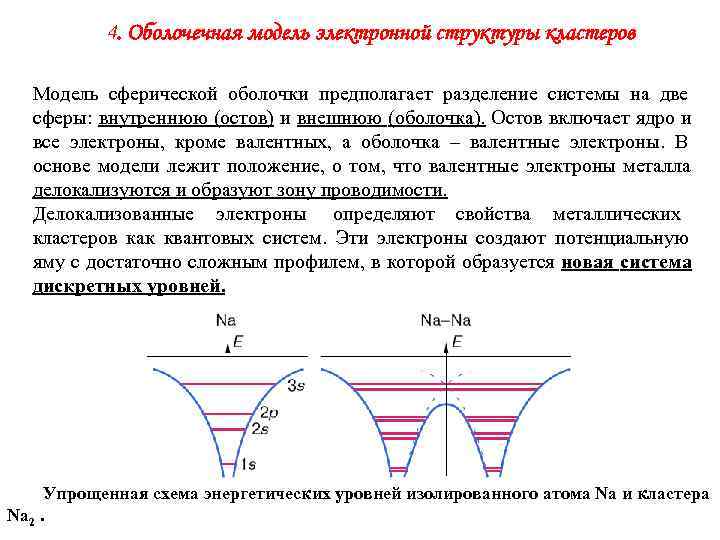
 4. Оболочечная модель электронной структуры кластеров Модель сферической оболочки предполагает разделение системы на две сферы: внутреннюю (остов) и внешнюю (оболочка). Остов включает ядро и все электроны, кроме валентных, а оболочка – валентные электроны. В основе модели лежит положение, о том, что валентные электроны металла делокализуются и образуют зону проводимости. Делокализованные электроны определяют свойства металлических кластеров как квантовых систем. Эти электроны создают потенциальную яму с достаточно сложным профилем, в которой образуется новая система дискретных уровней. Упрощенная схема энергетических уровней изолированного атома Na и кластера Na 2.
4. Оболочечная модель электронной структуры кластеров Модель сферической оболочки предполагает разделение системы на две сферы: внутреннюю (остов) и внешнюю (оболочка). Остов включает ядро и все электроны, кроме валентных, а оболочка – валентные электроны. В основе модели лежит положение, о том, что валентные электроны металла делокализуются и образуют зону проводимости. Делокализованные электроны определяют свойства металлических кластеров как квантовых систем. Эти электроны создают потенциальную яму с достаточно сложным профилем, в которой образуется новая система дискретных уровней. Упрощенная схема энергетических уровней изолированного атома Na и кластера Na 2.
 4. Оболочечная модель электронной структуры кластеров Наглядное описание структуры кластера и возможность прогноза магических чисел – сильные стороны модели сферической оболочки кластера. Однако при малом числе атомов, образующих кластер, реальная симметрия отличается от сферической. Кроме того, результаты строгих квантово-химических расчетов для очень маленьких кластеров (с числом атомов N = 3– 8) показали, что электронная структура действительно зависит от геометрии ионного остова. Однако для больших N многоцентровая задача с точным учетом взаиморасположения ионов становится трудноразрешимой и для ее решения необходимо использовать приближенные методы теории многих тел, которые бы адекватно описывали основные свойства кластеров. Эти ограничения снимаются в усовершенствованных моделях кластеров, одной из которых является модель желе.
4. Оболочечная модель электронной структуры кластеров Наглядное описание структуры кластера и возможность прогноза магических чисел – сильные стороны модели сферической оболочки кластера. Однако при малом числе атомов, образующих кластер, реальная симметрия отличается от сферической. Кроме того, результаты строгих квантово-химических расчетов для очень маленьких кластеров (с числом атомов N = 3– 8) показали, что электронная структура действительно зависит от геометрии ионного остова. Однако для больших N многоцентровая задача с точным учетом взаиморасположения ионов становится трудноразрешимой и для ее решения необходимо использовать приближенные методы теории многих тел, которые бы адекватно описывали основные свойства кластеров. Эти ограничения снимаются в усовершенствованных моделях кластеров, одной из которых является модель желе.
 5. Модель желе В большинстве современных теоретических подходов используется модель желе, суть которой состоит в следующих положениях. 1. Кластер, содержащий N атомов, рассматривается как две квазинезависимые подсистемы: систему валентных электронов и систему положительных ионов остова. 2. Обобществленные валентные электроны движутся в среднем поле, создаваемом всеми ионами кластера. 3. В первом приближении можно не учитывать сложную ионную структуру кора, заменив положительные ионы остова усредненным фоном нескомпенсированного заряда, считая его распределение п(r) однородным и сферически-симметричным. 4. В рамках обычной электростатики нетрудно сосчитать потенциал, создаваемый равномерно заряженным шаром радиуса R в зависимости от расстояния до центра шара r: V(r) = Ne 2[3 – (r/R)2/2 R], r R, V(r) = Ne 2/r, r > R, где Ne – полный заряд шара (в случае одновалентных щелочных металлов число свободных электронов равно числу атомов в кластере N), радиус кластера R рассматривается как параметр теории и меняется в зависимости от числа содержащихся в нем атомов N по закону R = rs. N 1/3, где rs – среднее расстояние между атомами в объемном металле. Плотность распределения положительного заряда n(r) и создаваемый им потенциал V(r) для металлического кластера в рамках обычной модели желе.
5. Модель желе В большинстве современных теоретических подходов используется модель желе, суть которой состоит в следующих положениях. 1. Кластер, содержащий N атомов, рассматривается как две квазинезависимые подсистемы: систему валентных электронов и систему положительных ионов остова. 2. Обобществленные валентные электроны движутся в среднем поле, создаваемом всеми ионами кластера. 3. В первом приближении можно не учитывать сложную ионную структуру кора, заменив положительные ионы остова усредненным фоном нескомпенсированного заряда, считая его распределение п(r) однородным и сферически-симметричным. 4. В рамках обычной электростатики нетрудно сосчитать потенциал, создаваемый равномерно заряженным шаром радиуса R в зависимости от расстояния до центра шара r: V(r) = Ne 2[3 – (r/R)2/2 R], r R, V(r) = Ne 2/r, r > R, где Ne – полный заряд шара (в случае одновалентных щелочных металлов число свободных электронов равно числу атомов в кластере N), радиус кластера R рассматривается как параметр теории и меняется в зависимости от числа содержащихся в нем атомов N по закону R = rs. N 1/3, где rs – среднее расстояние между атомами в объемном металле. Плотность распределения положительного заряда n(r) и создаваемый им потенциал V(r) для металлического кластера в рамках обычной модели желе.
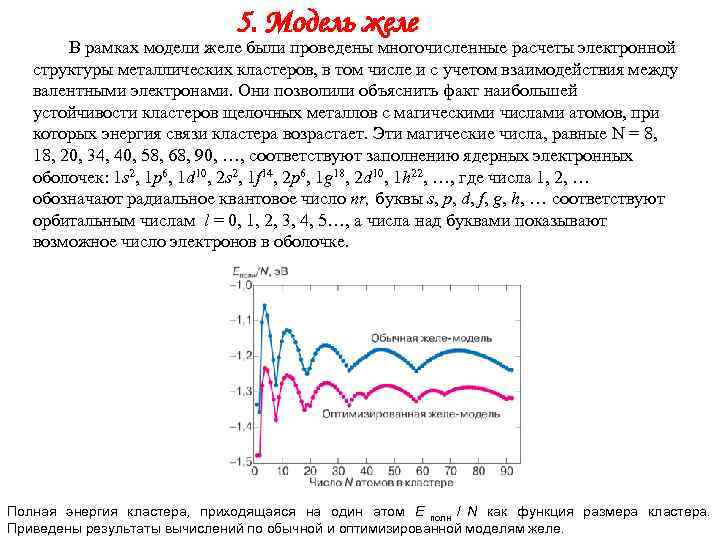
 5. Модель желе В рамках модели желе были проведены многочисленные расчеты электронной структуры металлических кластеров, в том числе и с учетом взаимодействия между валентными электронами. Они позволили объяснить факт наибольшей устойчивости кластеров щелочных металлов с магическими числами атомов, при которых энергия связи кластера возрастает. Эти магические числа, равные N = 8, 18, 20, 34, 40, 58, 68, 90, …, соответствуют заполнению ядерных электронных оболочек: 1 s 2, 1 p 6, 1 d 10, 2 s 2, 1 f 14, 2 p 6, 1 g 18, 2 d 10, 1 h 22, …, где числа 1, 2, … обозначают радиальное квантовое число nr, буквы s, p, d, f, g, h, … соответствуют орбитальным числам l = 0, 1, 2, 3, 4, 5…, а числа над буквами показывают возможное число электронов в оболочке. Полная энергия кластера, приходящаяся на один атом E полн / N как функция размера кластера. Приведены результаты вычислений по обычной и оптимизированной моделям желе.
5. Модель желе В рамках модели желе были проведены многочисленные расчеты электронной структуры металлических кластеров, в том числе и с учетом взаимодействия между валентными электронами. Они позволили объяснить факт наибольшей устойчивости кластеров щелочных металлов с магическими числами атомов, при которых энергия связи кластера возрастает. Эти магические числа, равные N = 8, 18, 20, 34, 40, 58, 68, 90, …, соответствуют заполнению ядерных электронных оболочек: 1 s 2, 1 p 6, 1 d 10, 2 s 2, 1 f 14, 2 p 6, 1 g 18, 2 d 10, 1 h 22, …, где числа 1, 2, … обозначают радиальное квантовое число nr, буквы s, p, d, f, g, h, … соответствуют орбитальным числам l = 0, 1, 2, 3, 4, 5…, а числа над буквами показывают возможное число электронов в оболочке. Полная энергия кластера, приходящаяся на один атом E полн / N как функция размера кластера. Приведены результаты вычислений по обычной и оптимизированной моделям желе.
 6. Химическая связь в кластерных комплексах переходных элементов и их свойства Схематическая диаграмма валентных молекулярных орбиталей типичного кластера M n L m переходного металла; ВАО–М и ВО–L – валентные атомные орбитали металла М и лиганда L соответственно. Электроны связей М–М делокализованы по связывающим валентным молекулярным орбиталям , число и характер которых предопределены числом атомов М n -группе, ее геометрией, числом и типом координированных лигандов , симметрией кластера M n L m. Эти связывающие МО (М–М) являются самыми верхними по энергии занятыми молекулярными орбиталями в единой электронной структуре кластера M n L m. Соответственные разрыхляющие МО (М–М*) в большинстве случаев вакантны и являются самыми нижними по энергии свободными МО. Вклад орбиталей лигандов в МО М–М невелик, и связи М–М в n –центровой группировке М n существенно обособлены от связей M–L в единой электронной структуре кластера Mn. Lm.
6. Химическая связь в кластерных комплексах переходных элементов и их свойства Схематическая диаграмма валентных молекулярных орбиталей типичного кластера M n L m переходного металла; ВАО–М и ВО–L – валентные атомные орбитали металла М и лиганда L соответственно. Электроны связей М–М делокализованы по связывающим валентным молекулярным орбиталям , число и характер которых предопределены числом атомов М n -группе, ее геометрией, числом и типом координированных лигандов , симметрией кластера M n L m. Эти связывающие МО (М–М) являются самыми верхними по энергии занятыми молекулярными орбиталями в единой электронной структуре кластера M n L m. Соответственные разрыхляющие МО (М–М*) в большинстве случаев вакантны и являются самыми нижними по энергии свободными МО. Вклад орбиталей лигандов в МО М–М невелик, и связи М–М в n –центровой группировке М n существенно обособлены от связей M–L в единой электронной структуре кластера Mn. Lm.
 6. Химическая связь в кластерных комплексах переходных элементов и их свойства Кластерные комплексы переходных элементов способны поглощать свет в видимой и ультрафиолетовой частях спектра благодаря электронным переходам с занятых МО, соответствующих связям М-М, на свободные (обычно – разрыхляющие) МО. Переход кластера в электронно-возбужденное состояние (ЭВС) обусловливает процессы люминисценции (электронные переходы из ЭВС), фоторедокс-процессы без значительного изменения структуры кластера, т. е. его фотоионизация (электронный перенос с участием ЭВС), фотостимулированные процессы значительного изменения структуры кластера (включая изомеризацию, разрыв связей М–М, отщепление лигандов и др. ). Гомолитический разрыв связей М–М при фотовозбуждении – свойство карбонильных кластеров переходных элементов. Чаще всего такие процессы протекают одновременно на одном кластере. Время жизни ЭВС достаточно большое (например, 200 мкс для Mo 6 Cl 142–). При фотовозбуждении можно целенаправленно изменять структуру кластера и регулировать механизм реакций, в которые он вступает. Реакции кластерных комплексов можно разделить на две группы: 1) реакции кластеров в основных состояниях; 2) реакции кластеров в электронно-возбужденных состояниях. К первой группе реакций относятся реакции замещения лигандов , реакции замещения атомов металла при сохранении нуклеарности кластера, конформационные превращения с изменением лигандной короны и одновременным сохранением М n – группы, реакции реорганизации Мn – группы,
6. Химическая связь в кластерных комплексах переходных элементов и их свойства Кластерные комплексы переходных элементов способны поглощать свет в видимой и ультрафиолетовой частях спектра благодаря электронным переходам с занятых МО, соответствующих связям М-М, на свободные (обычно – разрыхляющие) МО. Переход кластера в электронно-возбужденное состояние (ЭВС) обусловливает процессы люминисценции (электронные переходы из ЭВС), фоторедокс-процессы без значительного изменения структуры кластера, т. е. его фотоионизация (электронный перенос с участием ЭВС), фотостимулированные процессы значительного изменения структуры кластера (включая изомеризацию, разрыв связей М–М, отщепление лигандов и др. ). Гомолитический разрыв связей М–М при фотовозбуждении – свойство карбонильных кластеров переходных элементов. Чаще всего такие процессы протекают одновременно на одном кластере. Время жизни ЭВС достаточно большое (например, 200 мкс для Mo 6 Cl 142–). При фотовозбуждении можно целенаправленно изменять структуру кластера и регулировать механизм реакций, в которые он вступает. Реакции кластерных комплексов можно разделить на две группы: 1) реакции кластеров в основных состояниях; 2) реакции кластеров в электронно-возбужденных состояниях. К первой группе реакций относятся реакции замещения лигандов , реакции замещения атомов металла при сохранении нуклеарности кластера, конформационные превращения с изменением лигандной короны и одновременным сохранением М n – группы, реакции реорганизации Мn – группы,
 Взаимодействие кластеров с малыми молекулами Кластеры обладают способностью активировать координирующиеся на них молекулы. Активация молекул есть модификация электронно –ядерной структуры молекул, повышающая их реакционную способность. Суммарная энергия связей в активированной молекуле существенно меньше, чем в той же молекуле в свободном основном состоянии. Межъядерные расстояния в активированной молекуле увеличены. Так, одна из самых эффективных активаций наблюдается при координации молекулы СО “плашмя” на треугольной Nb 3 –группе в составе трехъядерного кластера Nb 3 (π– C 5 H 5 ) 3 ( CO ) 7 , где молекула СО координирована таким образом, что ат находится над центром треугольной Nb 3 –группы, а область связи С–О – над серединой одного из ребер Nb–Nb. Экспериментальные данные показывают, что здесь происходит сильнейшая активация молекулы СО, поскольку частота валентных колебаний С–О уменьшается (по сравнению со стандартным значением 2170 см – 1 ) до аномально малого значения 1330 см – 1 , силовая постоянная связи С–О падает почти втрое – от 19 до 7 мдин/А. Структура центрального фрагмента кластера Nb 3(π–C 5 H 5)3(CO)7 с 3 – СО–группой.
Взаимодействие кластеров с малыми молекулами Кластеры обладают способностью активировать координирующиеся на них молекулы. Активация молекул есть модификация электронно –ядерной структуры молекул, повышающая их реакционную способность. Суммарная энергия связей в активированной молекуле существенно меньше, чем в той же молекуле в свободном основном состоянии. Межъядерные расстояния в активированной молекуле увеличены. Так, одна из самых эффективных активаций наблюдается при координации молекулы СО “плашмя” на треугольной Nb 3 –группе в составе трехъядерного кластера Nb 3 (π– C 5 H 5 ) 3 ( CO ) 7 , где молекула СО координирована таким образом, что ат находится над центром треугольной Nb 3 –группы, а область связи С–О – над серединой одного из ребер Nb–Nb. Экспериментальные данные показывают, что здесь происходит сильнейшая активация молекулы СО, поскольку частота валентных колебаний С–О уменьшается (по сравнению со стандартным значением 2170 см – 1 ) до аномально малого значения 1330 см – 1 , силовая постоянная связи С–О падает почти втрое – от 19 до 7 мдин/А. Структура центрального фрагмента кластера Nb 3(π–C 5 H 5)3(CO)7 с 3 – СО–группой.
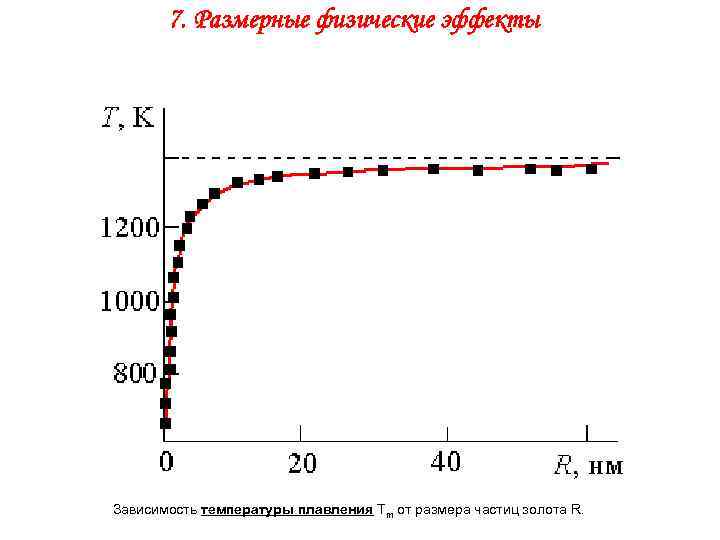
 7. Размерные физические эффекты Зависимость температуры плавления Тm от размера частиц золота R.
7. Размерные физические эффекты Зависимость температуры плавления Тm от размера частиц золота R.
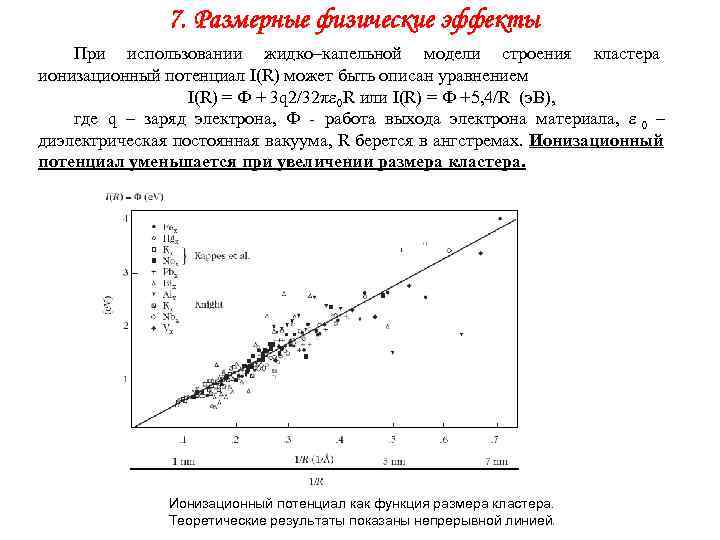
 7. Размерные физические эффекты При использовании жидко–капельной модели строения кластера ионизационный потенциал I(R) может быть описан уравнением I(R) = Ф + 3 q 2/32π 0 R или I(R) = Ф +5, 4/R (э. В), где q – заряд электрона, Ф - работа выхода электрона материала, 0 – диэлектрическая постоянная вакуума, R берется в ангстремах. Ионизационный потенциал уменьшается при увеличении размера кластера. Ионизационный потенциал как функция размера кластера. Теоретические результаты показаны непрерывной линией.
7. Размерные физические эффекты При использовании жидко–капельной модели строения кластера ионизационный потенциал I(R) может быть описан уравнением I(R) = Ф + 3 q 2/32π 0 R или I(R) = Ф +5, 4/R (э. В), где q – заряд электрона, Ф - работа выхода электрона материала, 0 – диэлектрическая постоянная вакуума, R берется в ангстремах. Ионизационный потенциал уменьшается при увеличении размера кластера. Ионизационный потенциал как функция размера кластера. Теоретические результаты показаны непрерывной линией.
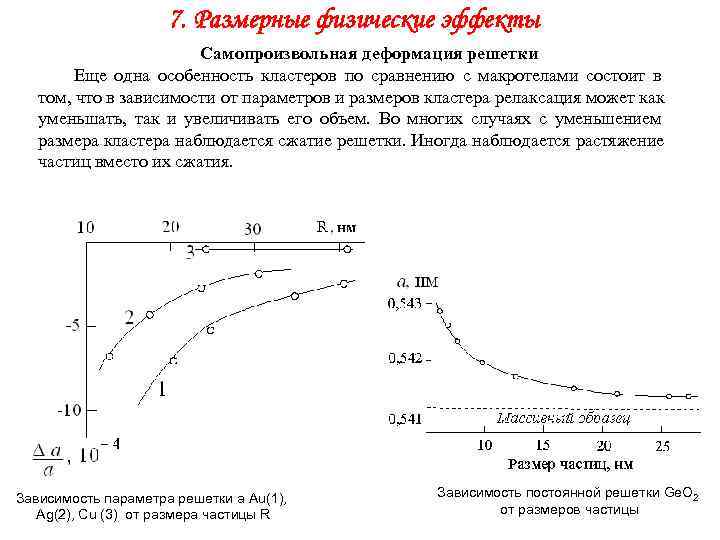
 7. Размерные физические эффекты Самопроизвольная деформация решетки Еще одна особенность кластеров по сравнению с макротелами состоит в том, что в зависимости от параметров и размеров кластера релаксация может как уменьшать, так и увеличивать его объем. Во многих случаях с уменьшением размера кластера наблюдается сжатие решетки. Иногда наблюдается растяжение частиц вместо их сжатия. Зависимость параметра решетки a Au(1), Зависимость постоянной решетки Ge. O 2 Ag(2), Cu (3) от размера частицы R от размеров частицы
7. Размерные физические эффекты Самопроизвольная деформация решетки Еще одна особенность кластеров по сравнению с макротелами состоит в том, что в зависимости от параметров и размеров кластера релаксация может как уменьшать, так и увеличивать его объем. Во многих случаях с уменьшением размера кластера наблюдается сжатие решетки. Иногда наблюдается растяжение частиц вместо их сжатия. Зависимость параметра решетки a Au(1), Зависимость постоянной решетки Ge. O 2 Ag(2), Cu (3) от размера частицы R от размеров частицы
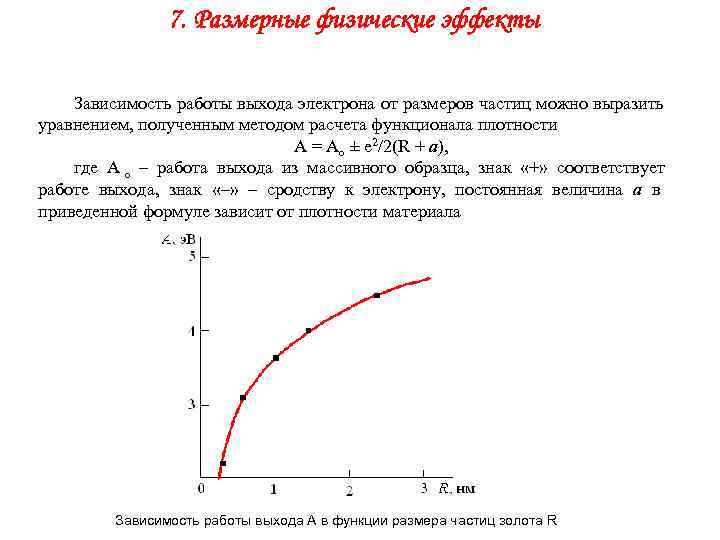
 7. Размерные физические эффекты Зависимость работы выхода электрона от размеров частиц можно выразить уравнением, полученным методом расчета функционала плотности A = Ao ± e 2/2(R + a), где A o – работа выхода из массивного образца, знак «+» соответствует работе выхода, знак «–» – сродству к электрону, постоянная величина а в приведенной формуле зависит от плотности материала Зависимость работы выхода А в функции размера частиц золота R
7. Размерные физические эффекты Зависимость работы выхода электрона от размеров частиц можно выразить уравнением, полученным методом расчета функционала плотности A = Ao ± e 2/2(R + a), где A o – работа выхода из массивного образца, знак «+» соответствует работе выхода, знак «–» – сродству к электрону, постоянная величина а в приведенной формуле зависит от плотности материала Зависимость работы выхода А в функции размера частиц золота R
 7. Размерные физические эффекты Кулоновский взрыв При изучении кластеров обнаружено новое явление – многократная ионизация малых частиц, которая приводит к их мгновенному распаду на однократно заряженные осколки. Это явление называют кулоновским взрывом. Установлено критическое число атомов в кластере n с , начиная с которого обнаруживается стабильность двукратно заряженных кластеров: Pb (nс = 30), Na. I (nс = 20), Ag (nс = 52). Были также обнаружены двукратно заряженные кластеры с размерами ниже критического: Pb n 2+ ( n = 7), Pb n 2+ ( n = 9), Pb n 2+ ( n = 11), Pb n 2+ ( n = 13), Ag n 2+ ( n 19), Pb 3+ ( n > 45), Pb n 4+ ( n > 60 – 70), Ni n 2+ n (n = 3), Aun 2+ (n = 3), Wn 2+ (n = 3). При взрыве кластеров образующиеся осколки ионов, содержат «магические» числа электронов (2, 8, 18 и т. д. ).
7. Размерные физические эффекты Кулоновский взрыв При изучении кластеров обнаружено новое явление – многократная ионизация малых частиц, которая приводит к их мгновенному распаду на однократно заряженные осколки. Это явление называют кулоновским взрывом. Установлено критическое число атомов в кластере n с , начиная с которого обнаруживается стабильность двукратно заряженных кластеров: Pb (nс = 30), Na. I (nс = 20), Ag (nс = 52). Были также обнаружены двукратно заряженные кластеры с размерами ниже критического: Pb n 2+ ( n = 7), Pb n 2+ ( n = 9), Pb n 2+ ( n = 11), Pb n 2+ ( n = 13), Ag n 2+ ( n 19), Pb 3+ ( n > 45), Pb n 4+ ( n > 60 – 70), Ni n 2+ n (n = 3), Aun 2+ (n = 3), Wn 2+ (n = 3). При взрыве кластеров образующиеся осколки ионов, содержат «магические» числа электронов (2, 8, 18 и т. д. ).
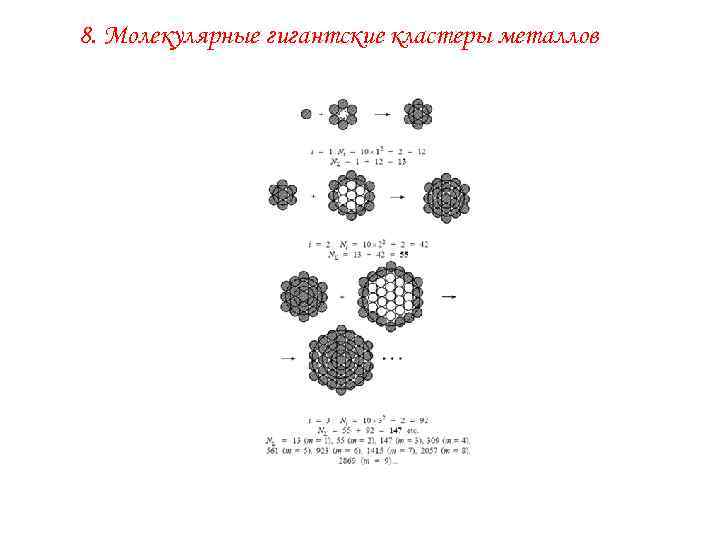
 8. Молекулярные гигантские кластеры металлов
8. Молекулярные гигантские кластеры металлов
 8. Молекулярные гигантские кластеры металлов Кластер 561 стабилизирован 60 молекулами бидентантно координированных лигандов фенантролина, а 180 анионов выполняют функцию внешнесферических лигандов, располагаясь на периферии гигантского кластера-катиона [Pd 251 phen 60]180+ (phen – фенантролин). Идеализированная структура гигантского кластера Рd 251 phen 60(OAc)180. 1 атомы палладия металлического остова, связанные с бидентантно координированными лигандами (phen); 2 атомы палладия, доступные для координации молекул растворителя или субстрата, не связанные с лигандами; 3 ван-дер-ваальсовы контуры координированных лигандов phen.
8. Молекулярные гигантские кластеры металлов Кластер 561 стабилизирован 60 молекулами бидентантно координированных лигандов фенантролина, а 180 анионов выполняют функцию внешнесферических лигандов, располагаясь на периферии гигантского кластера-катиона [Pd 251 phen 60]180+ (phen – фенантролин). Идеализированная структура гигантского кластера Рd 251 phen 60(OAc)180. 1 атомы палладия металлического остова, связанные с бидентантно координированными лигандами (phen); 2 атомы палладия, доступные для координации молекул растворителя или субстрата, не связанные с лигандами; 3 ван-дер-ваальсовы контуры координированных лигандов phen.
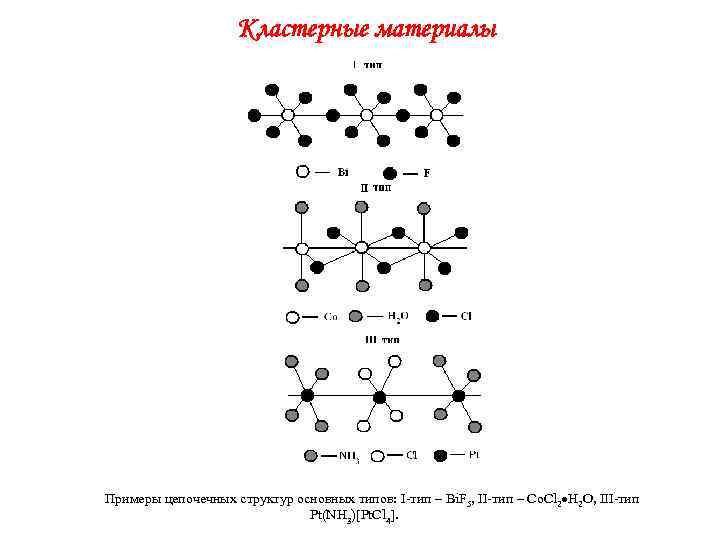
 Кластерные материалы Примеры цепочечных структур основных типов: I-тип – Bi. F 5, II-тип – Co. Cl 2 H 2 O, III-тип Pt(NH 3)[Pt. Cl 4].
Кластерные материалы Примеры цепочечных структур основных типов: I-тип – Bi. F 5, II-тип – Co. Cl 2 H 2 O, III-тип Pt(NH 3)[Pt. Cl 4].
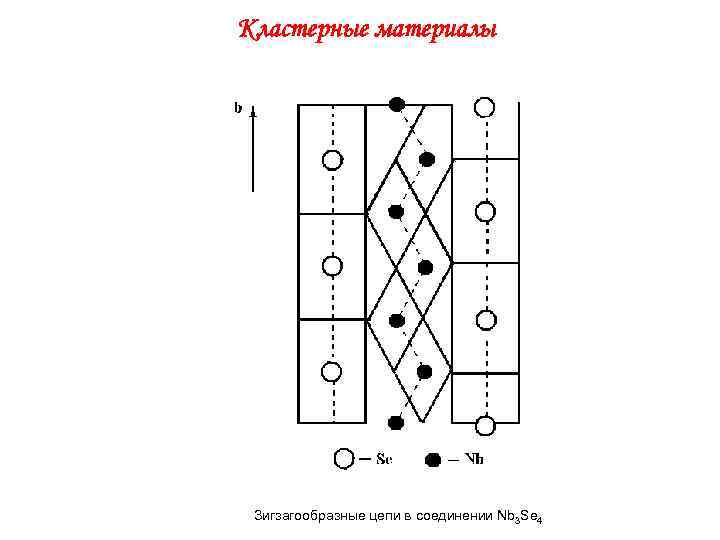
 Кластерные материалы Зигзагообразные цепи в соединении Nb 3 Se 4
Кластерные материалы Зигзагообразные цепи в соединении Nb 3 Se 4
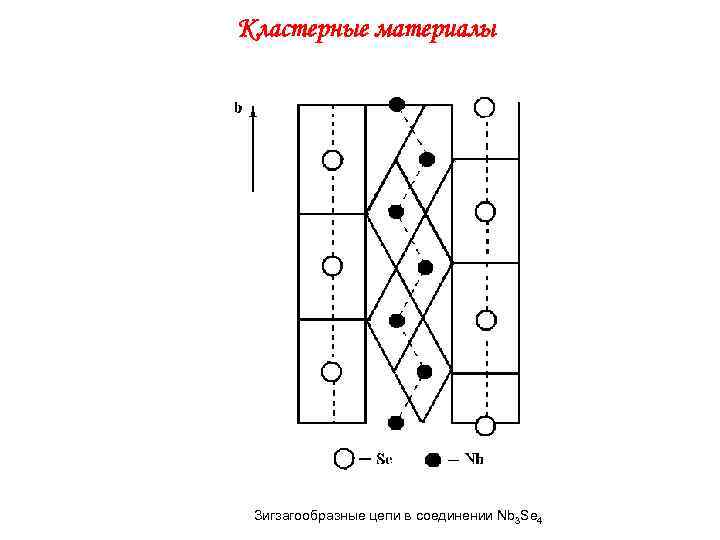
 Кластерные материалы Зигзагообразные цепи в соединении Nb 3 Se 4
Кластерные материалы Зигзагообразные цепи в соединении Nb 3 Se 4
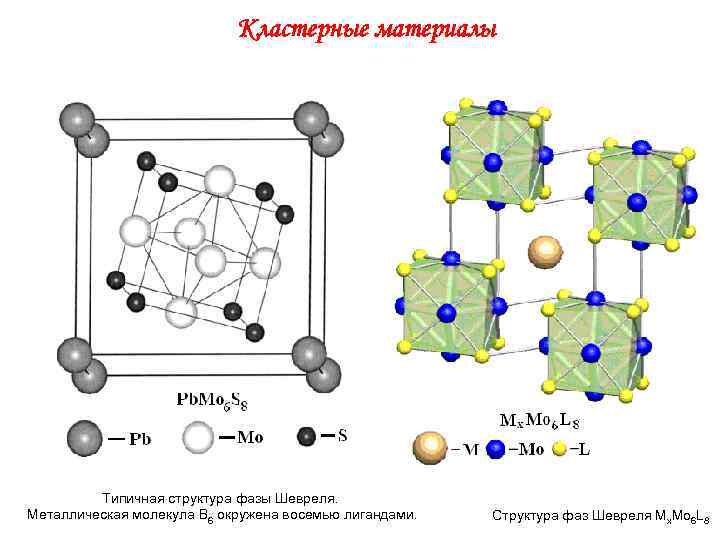
 Кластерные материалы Типичная структура фазы Шевреля. Металлическая молекула В 6 окружена восемью лигандами. Структура фаз Шевреля Mx. Mo 6 L 8
Кластерные материалы Типичная структура фазы Шевреля. Металлическая молекула В 6 окружена восемью лигандами. Структура фаз Шевреля Mx. Mo 6 L 8
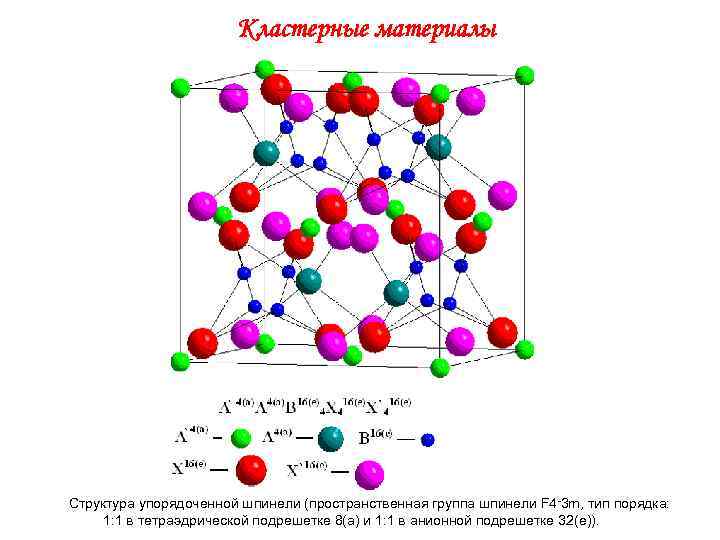
 Кластерные материалы Структура упорядоченной шпинели (пространственная группа шпинели F 4 -3 m, тип порядка: 1: 1 в тетраэдрической подрешетке 8(а) и 1: 1 в анионной подрешетке 32(e)).
Кластерные материалы Структура упорядоченной шпинели (пространственная группа шпинели F 4 -3 m, тип порядка: 1: 1 в тетраэдрической подрешетке 8(а) и 1: 1 в анионной подрешетке 32(e)).
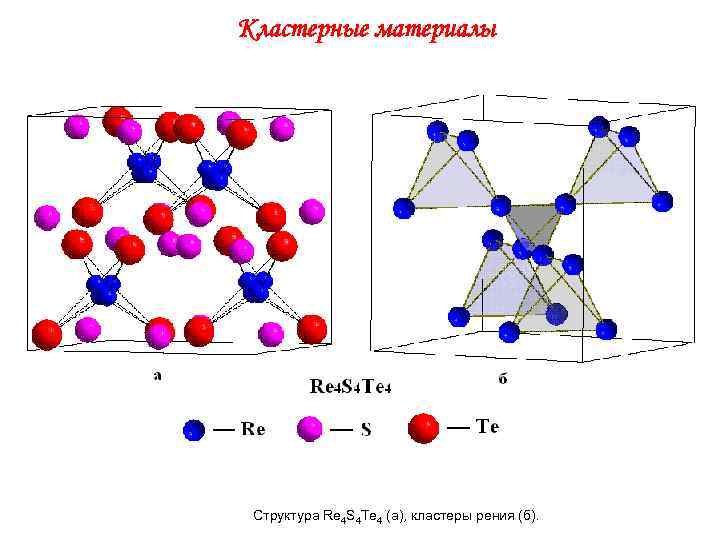
 Кластерные материалы Структура Re 4 S 4 Te 4 (а), кластеры рения (б).
Кластерные материалы Структура Re 4 S 4 Te 4 (а), кластеры рения (б).
 10. Методы получения кластеров Кластеры металлов, оксидов, углерода, инертных газов, малых молекул получают путем конденсации в атомных пучках или парах. Формирование кластера может происходить за время, превышающее 10– 13 с; этот процесс зависит в основном от кинетической энергии кластера, это очень маленький промежуток времени для опытного изучения процесса формирования кластера (время одной компьютерной операции 10– 9 с). Физические методы получения кластеров включают: – конденсацию атомов в атмосфере инертных газов, – дуговой разряд, – ионное распыление, – лазерная абляция, – пиролиз.
10. Методы получения кластеров Кластеры металлов, оксидов, углерода, инертных газов, малых молекул получают путем конденсации в атомных пучках или парах. Формирование кластера может происходить за время, превышающее 10– 13 с; этот процесс зависит в основном от кинетической энергии кластера, это очень маленький промежуток времени для опытного изучения процесса формирования кластера (время одной компьютерной операции 10– 9 с). Физические методы получения кластеров включают: – конденсацию атомов в атмосфере инертных газов, – дуговой разряд, – ионное распыление, – лазерная абляция, – пиролиз.
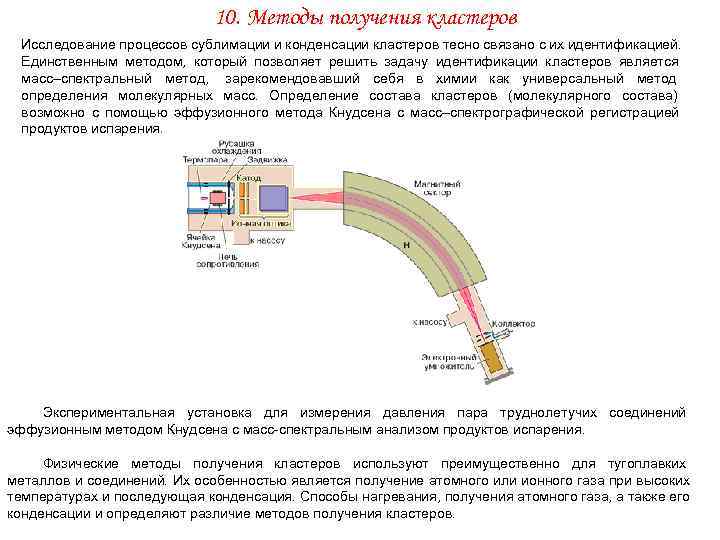
 10. Методы получения кластеров Исследование процессов сублимации и конденсации кластеров тесно связано с их идентификацией. Единственным методом, который позволяет решить задачу идентификации кластеров является масс–спектральный метод, зарекомендовавший себя в химии как универсальный метод определения молекулярных масс. Определение состава кластеров (молекулярного состава) возможно с помощью эффузионного метода Кнудсена с масс–спектрографической регистрацией продуктов испарения. Экспериментальная установка для измерения давления пара труднолетучих соединений эффузионным методом Кнудсена с масс-спектральным анализом продуктов испарения. Физические методы получения кластеров используют преимущественно для тугоплавких металлов и соединений. Их особенностью является получение атомного или ионного газа при высоких температурах и последующая конденсация. Способы нагревания, получения атомного газа, а также его конденсации и определяют различие методов получения кластеров.
10. Методы получения кластеров Исследование процессов сублимации и конденсации кластеров тесно связано с их идентификацией. Единственным методом, который позволяет решить задачу идентификации кластеров является масс–спектральный метод, зарекомендовавший себя в химии как универсальный метод определения молекулярных масс. Определение состава кластеров (молекулярного состава) возможно с помощью эффузионного метода Кнудсена с масс–спектрографической регистрацией продуктов испарения. Экспериментальная установка для измерения давления пара труднолетучих соединений эффузионным методом Кнудсена с масс-спектральным анализом продуктов испарения. Физические методы получения кластеров используют преимущественно для тугоплавких металлов и соединений. Их особенностью является получение атомного или ионного газа при высоких температурах и последующая конденсация. Способы нагревания, получения атомного газа, а также его конденсации и определяют различие методов получения кластеров.
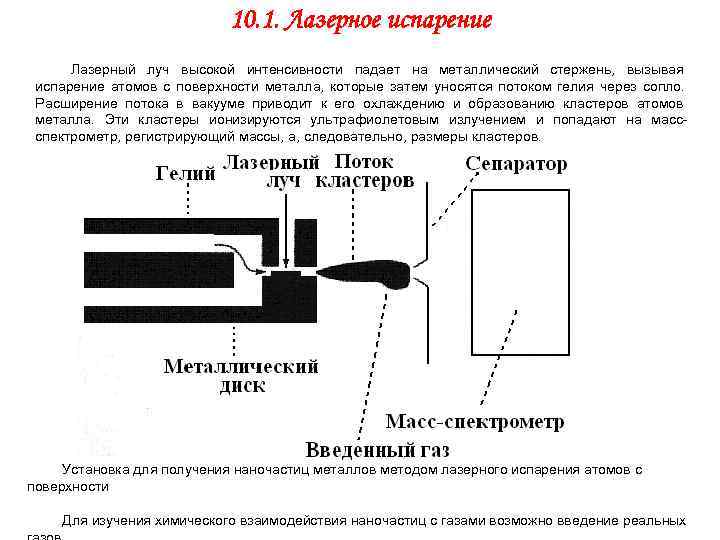
 10. 1. Лазерное испарение Лазерный луч высокой интенсивности падает на металлический стержень, вызывая испарение атомов с поверхности металла, которые затем уносятся потоком гелия через сопло. Расширение потока в вакууме приводит к его охлаждению и образованию кластеров атомов металла. Эти кластеры ионизируются ультрафиолетовым излучением и попадают на масс- спектрометр, регистрирующий массы, а, следовательно, размеры кластеров. Установка для получения наночастиц металлов методом лазерного испарения атомов с поверхности Для изучения химического взаимодействия наночастиц с газами возможно введение реальных
10. 1. Лазерное испарение Лазерный луч высокой интенсивности падает на металлический стержень, вызывая испарение атомов с поверхности металла, которые затем уносятся потоком гелия через сопло. Расширение потока в вакууме приводит к его охлаждению и образованию кластеров атомов металла. Эти кластеры ионизируются ультрафиолетовым излучением и попадают на масс- спектрометр, регистрирующий массы, а, следовательно, размеры кластеров. Установка для получения наночастиц металлов методом лазерного испарения атомов с поверхности Для изучения химического взаимодействия наночастиц с газами возможно введение реальных
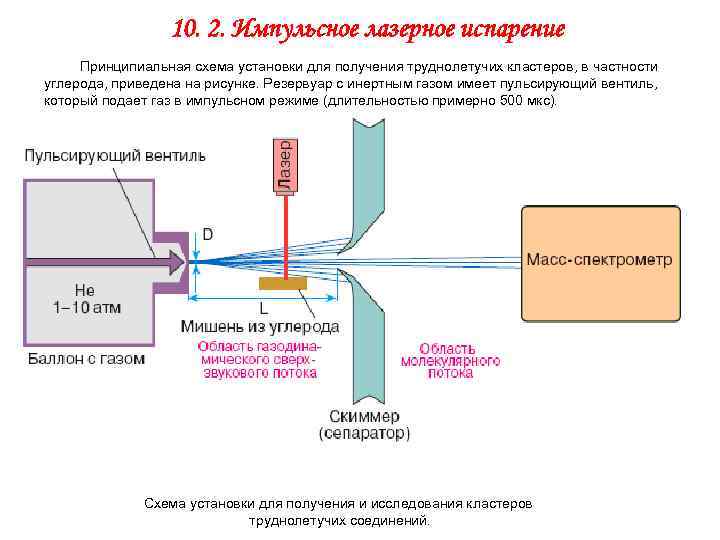
 10. 2. Импульсное лазерное испарение Принципиальная схема установки для получения труднолетучих кластеров, в частности углерода, приведена на рисунке. Резервуар с инертным газом имеет пульсирующий вентиль, который подает газ в импульсном режиме (длительностью примерно 500 мкс). Схема установки для получения и исследования кластеров труднолетучих соединений.
10. 2. Импульсное лазерное испарение Принципиальная схема установки для получения труднолетучих кластеров, в частности углерода, приведена на рисунке. Резервуар с инертным газом имеет пульсирующий вентиль, который подает газ в импульсном режиме (длительностью примерно 500 мкс). Схема установки для получения и исследования кластеров труднолетучих соединений.
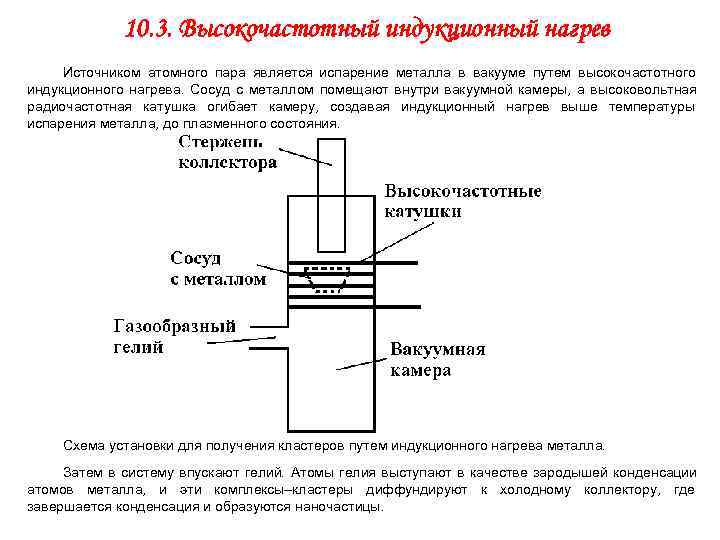
 10. 3. Высокочастотный индукционный нагрев Источником атомного пара является испарение металла в вакууме путем высокочастотного индукционного нагрева. Сосуд с металлом помещают внутри вакуумной камеры, а высоковольтная радиочастотная катушка огибает камеру, создавая индукционный нагрев выше температуры испарения металла, до плазменного состояния. Схема установки для получения кластеров путем индукционного нагрева металла. Затем в систему впускают гелий. Атомы гелия выступают в качестве зародышей конденсации атомов металла, и эти комплексы–кластеры диффундируют к холодному коллектору, где завершается конденсация и образуются наночастицы.
10. 3. Высокочастотный индукционный нагрев Источником атомного пара является испарение металла в вакууме путем высокочастотного индукционного нагрева. Сосуд с металлом помещают внутри вакуумной камеры, а высоковольтная радиочастотная катушка огибает камеру, создавая индукционный нагрев выше температуры испарения металла, до плазменного состояния. Схема установки для получения кластеров путем индукционного нагрева металла. Затем в систему впускают гелий. Атомы гелия выступают в качестве зародышей конденсации атомов металла, и эти комплексы–кластеры диффундируют к холодному коллектору, где завершается конденсация и образуются наночастицы.
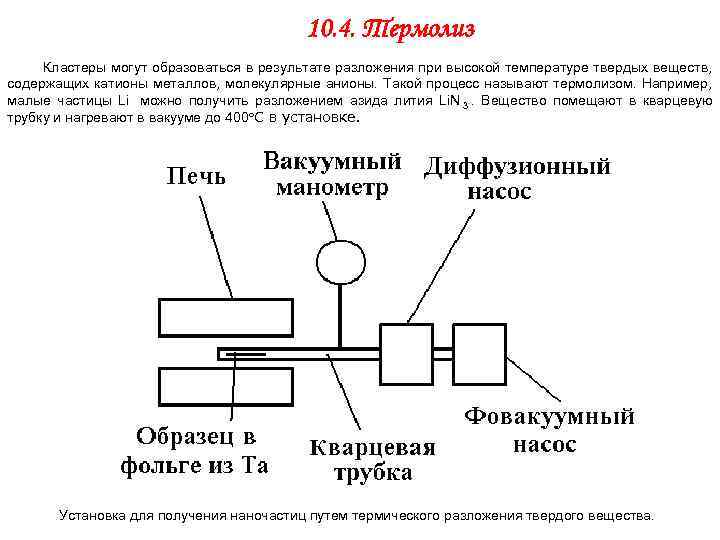
 10. 4. Термолиз Кластеры могут образоваться в результате разложения при высокой температуре твердых веществ, содержащих катионы металлов, молекулярные анионы. Такой процесс называют термолизом. Например, малые частицы Li можно получить разложением азида лития Li. N 3. Вещество помещают в кварцевую трубку и нагревают в вакууме до 400 С в установке. Установка для получения наночастиц путем термического разложения твердого вещества.
10. 4. Термолиз Кластеры могут образоваться в результате разложения при высокой температуре твердых веществ, содержащих катионы металлов, молекулярные анионы. Такой процесс называют термолизом. Например, малые частицы Li можно получить разложением азида лития Li. N 3. Вещество помещают в кварцевую трубку и нагревают в вакууме до 400 С в установке. Установка для получения наночастиц путем термического разложения твердого вещества.
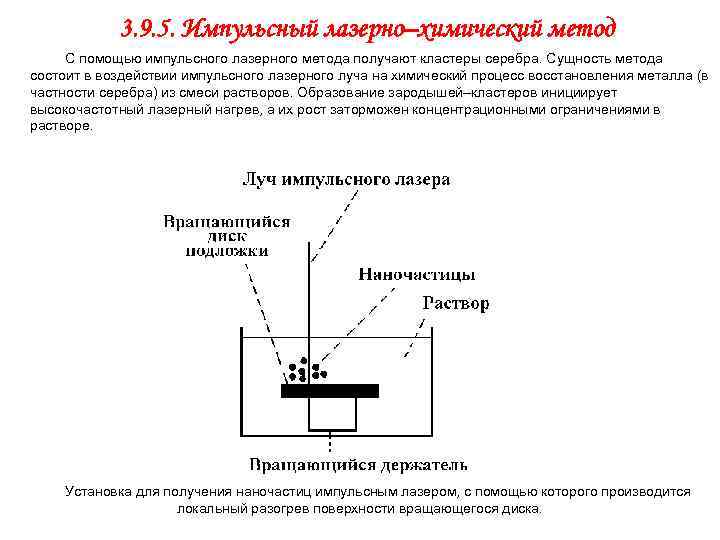
 3. 9. 5. Импульсный лазерно–химический метод С помощью импульсного лазерного метода получают кластеры серебра. Сущность метода состоит в воздействии импульсного лазерного луча на химический процесс восстановления металла (в частности серебра) из смеси растворов. Образование зародышей–кластеров инициирует высокочастотный лазерный нагрев, а их рост заторможен концентрационными ограничениями в растворе. Установка для получения наночастиц импульсным лазером, с помощью которого производится локальный разогрев поверхности вращающегося диска.
3. 9. 5. Импульсный лазерно–химический метод С помощью импульсного лазерного метода получают кластеры серебра. Сущность метода состоит в воздействии импульсного лазерного луча на химический процесс восстановления металла (в частности серебра) из смеси растворов. Образование зародышей–кластеров инициирует высокочастотный лазерный нагрев, а их рост заторможен концентрационными ограничениями в растворе. Установка для получения наночастиц импульсным лазером, с помощью которого производится локальный разогрев поверхности вращающегося диска.
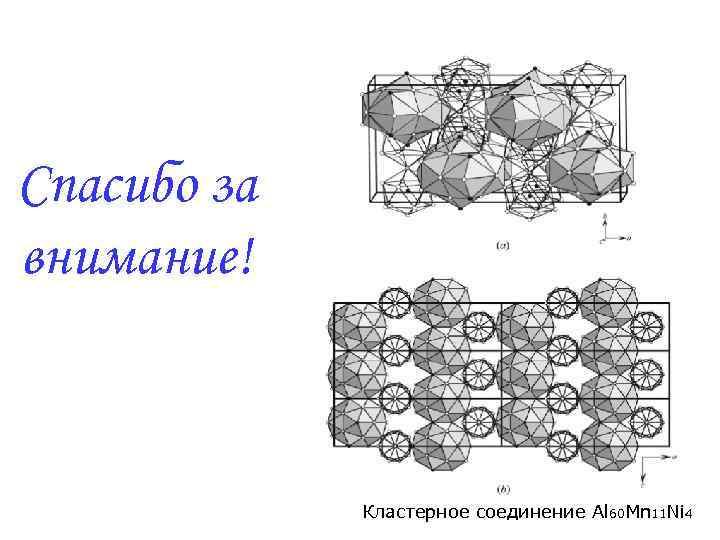
 Спасибо за внимание! Кластерное соединение Al 60 Mn 11 Ni 4
Спасибо за внимание! Кластерное соединение Al 60 Mn 11 Ni 4

