LECTURE_BIOLOGY_12.ppt
- Количество слайдов: 60
 ЯВЛЕНИЕ СМАЧИВАНИЯ. КАПИЛЛЯРНЫЕ ЯВЛЕНИЯ.
ЯВЛЕНИЕ СМАЧИВАНИЯ. КАПИЛЛЯРНЫЕ ЯВЛЕНИЯ.
 ЯВЛЕНИЕ СМАЧИВАНИЯ
ЯВЛЕНИЕ СМАЧИВАНИЯ
 Эксперимент 1 http: //web. mit. edu/nnf/education/
Эксперимент 1 http: //web. mit. edu/nnf/education/
 Эксперимент 2 http: //web. mit. edu/nnf/education/
Эксперимент 2 http: //web. mit. edu/nnf/education/
 Эксперимент 3 http: //web. mit. edu/nnf/education/
Эксперимент 3 http: //web. mit. edu/nnf/education/
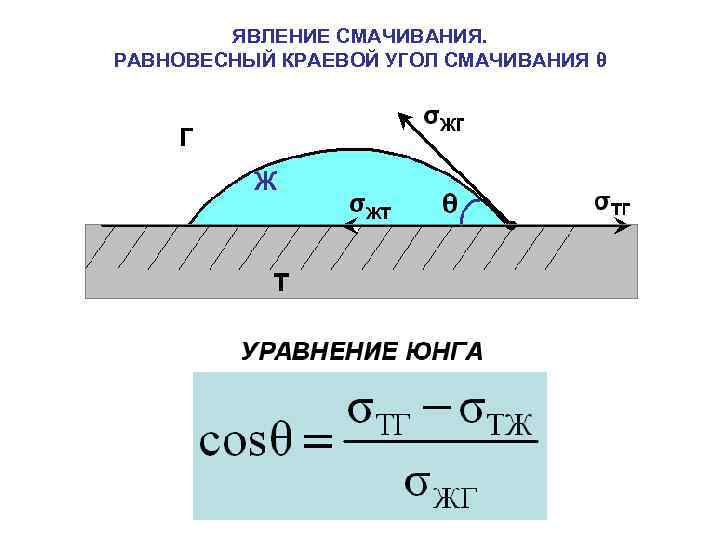 ЯВЛЕНИЕ СМАЧИВАНИЯ. РАВНОВЕСНЫЙ КРАЕВОЙ УГОЛ СМАЧИВАНИЯ θ
ЯВЛЕНИЕ СМАЧИВАНИЯ. РАВНОВЕСНЫЙ КРАЕВОЙ УГОЛ СМАЧИВАНИЯ θ
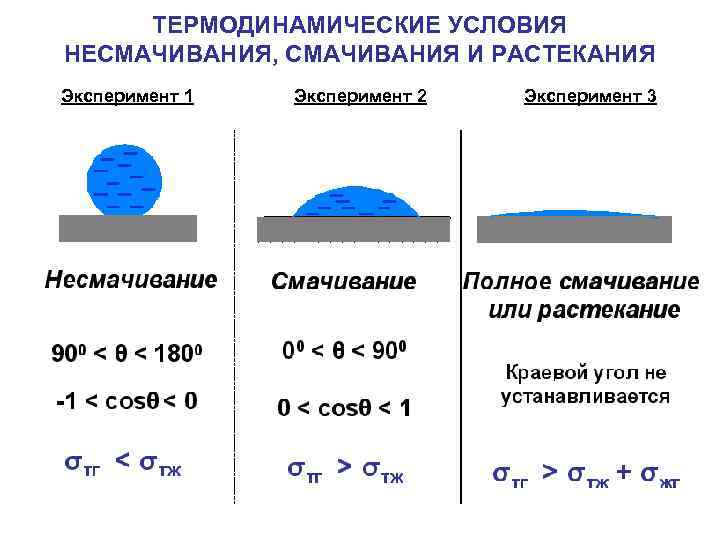 ТЕРМОДИНАМИЧЕСКИЕ УСЛОВИЯ НЕСМАЧИВАНИЯ, СМАЧИВАНИЯ И РАСТЕКАНИЯ Эксперимент 1 Эксперимент 2 Эксперимент 3
ТЕРМОДИНАМИЧЕСКИЕ УСЛОВИЯ НЕСМАЧИВАНИЯ, СМАЧИВАНИЯ И РАСТЕКАНИЯ Эксперимент 1 Эксперимент 2 Эксперимент 3
 СВЯЗЬ КРАЕВОГО УГЛА С РАБОТОЙ АДГЕЗИИ И КОГЕЗИИ Формула Дюпре
СВЯЗЬ КРАЕВОГО УГЛА С РАБОТОЙ АДГЕЗИИ И КОГЕЗИИ Формула Дюпре
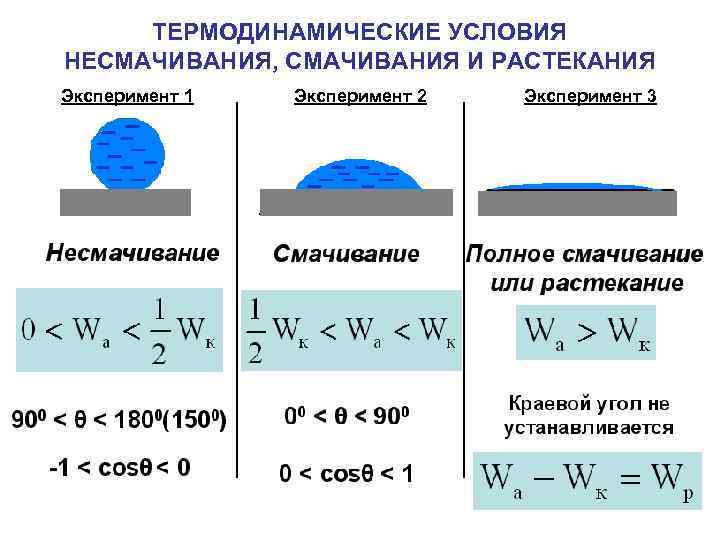 ТЕРМОДИНАМИЧЕСКИЕ УСЛОВИЯ НЕСМАЧИВАНИЯ, СМАЧИВАНИЯ И РАСТЕКАНИЯ Эксперимент 1 Эксперимент 2 Эксперимент 3
ТЕРМОДИНАМИЧЕСКИЕ УСЛОВИЯ НЕСМАЧИВАНИЯ, СМАЧИВАНИЯ И РАСТЕКАНИЯ Эксперимент 1 Эксперимент 2 Эксперимент 3
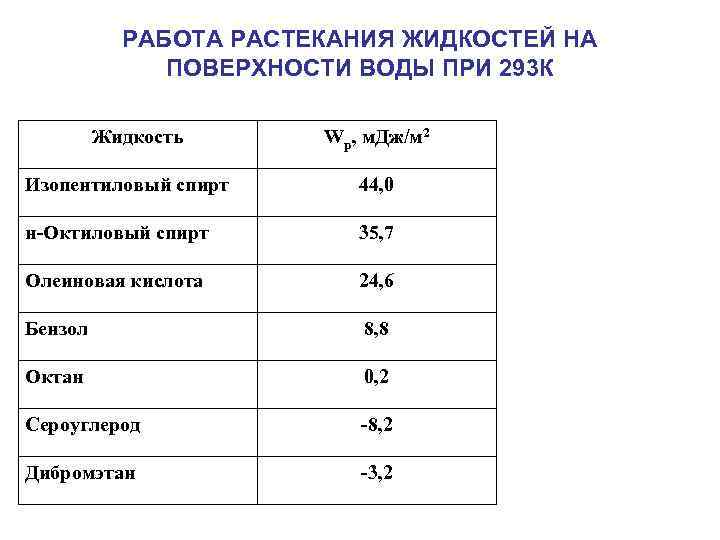 РАБОТА РАСТЕКАНИЯ ЖИДКОСТЕЙ НА ПОВЕРХНОСТИ ВОДЫ ПРИ 293 К Жидкость Wр, м. Дж/м 2 Изопентиловый спирт 44, 0 н-Октиловый спирт 35, 7 Олеиновая кислота 24, 6 Бензол 8, 8 Октан 0, 2 Сероуглерод -8, 2 Дибромэтан -3, 2
РАБОТА РАСТЕКАНИЯ ЖИДКОСТЕЙ НА ПОВЕРХНОСТИ ВОДЫ ПРИ 293 К Жидкость Wр, м. Дж/м 2 Изопентиловый спирт 44, 0 н-Октиловый спирт 35, 7 Олеиновая кислота 24, 6 Бензол 8, 8 Октан 0, 2 Сероуглерод -8, 2 Дибромэтан -3, 2
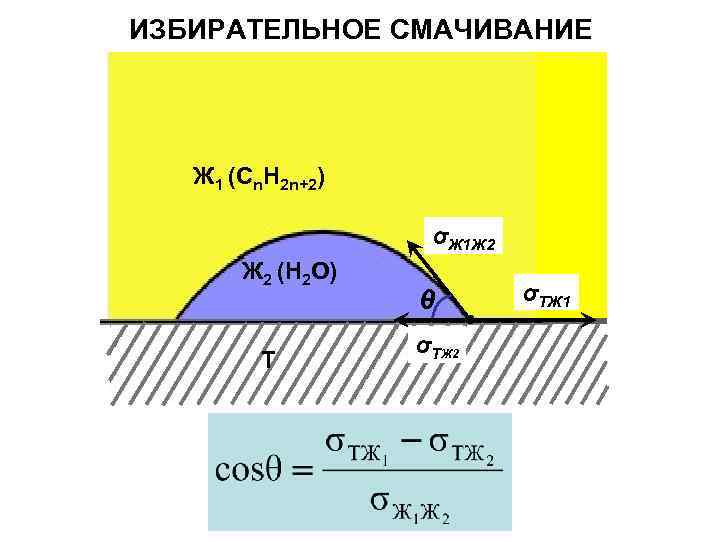 ИЗБИРАТЕЛЬНОЕ СМАЧИВАНИЕ Ж 1 (Cn. H 2 n+2) σЖ 1 Ж 2 (H 2 O) Т θ σТЖ 2 σТЖ 1
ИЗБИРАТЕЛЬНОЕ СМАЧИВАНИЕ Ж 1 (Cn. H 2 n+2) σЖ 1 Ж 2 (H 2 O) Т θ σТЖ 2 σТЖ 1
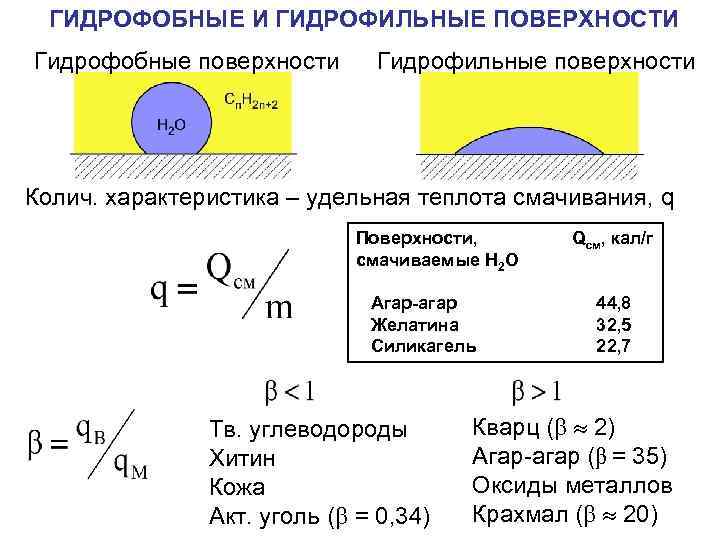 ГИДРОФОБНЫЕ И ГИДРОФИЛЬНЫЕ ПОВЕРХНОСТИ Гидрофобные поверхности Гидрофильные поверхности Колич. характеристика – удельная теплота смачивания, q Поверхности, смачиваемые H 2 O Агар-агар Желатина Силикагель Тв. углеводороды Хитин Кожа Акт. уголь ( = 0, 34) Qсм, кал/г 44, 8 32, 5 22, 7 Кварц ( 2) Агар-агар (β = 35) Оксиды металлов Крахмал ( 20)
ГИДРОФОБНЫЕ И ГИДРОФИЛЬНЫЕ ПОВЕРХНОСТИ Гидрофобные поверхности Гидрофильные поверхности Колич. характеристика – удельная теплота смачивания, q Поверхности, смачиваемые H 2 O Агар-агар Желатина Силикагель Тв. углеводороды Хитин Кожа Акт. уголь ( = 0, 34) Qсм, кал/г 44, 8 32, 5 22, 7 Кварц ( 2) Агар-агар (β = 35) Оксиды металлов Крахмал ( 20)
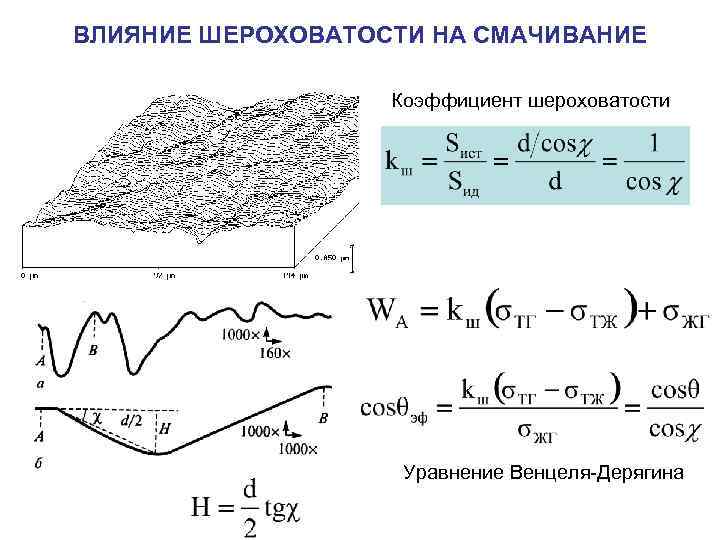 ВЛИЯНИЕ ШЕРОХОВАТОСТИ НА СМАЧИВАНИЕ Коэффициент шероховатости Уравнение Венцеля-Дерягина
ВЛИЯНИЕ ШЕРОХОВАТОСТИ НА СМАЧИВАНИЕ Коэффициент шероховатости Уравнение Венцеля-Дерягина
 ЭФФЕКТ ЛОТОСА
ЭФФЕКТ ЛОТОСА
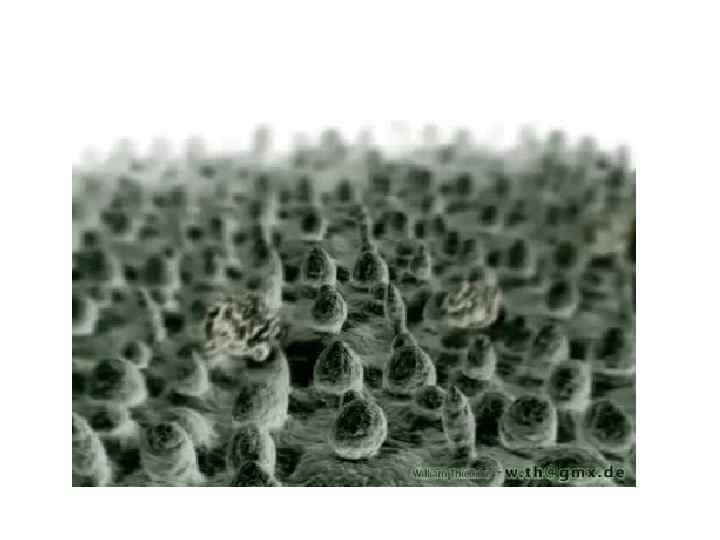
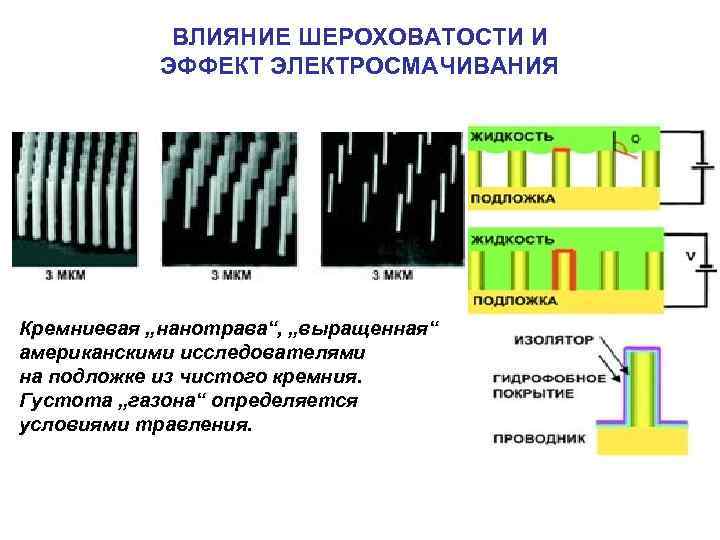 ВЛИЯНИЕ ШЕРОХОВАТОСТИ И ЭФФЕКТ ЭЛЕКТРОСМАЧИВАНИЯ Кремниевая „нанотрава“, „выращенная“ американскими исследователями на подложке из чистого кремния. Густота „газона“ определяется условиями травления.
ВЛИЯНИЕ ШЕРОХОВАТОСТИ И ЭФФЕКТ ЭЛЕКТРОСМАЧИВАНИЯ Кремниевая „нанотрава“, „выращенная“ американскими исследователями на подложке из чистого кремния. Густота „газона“ определяется условиями травления.
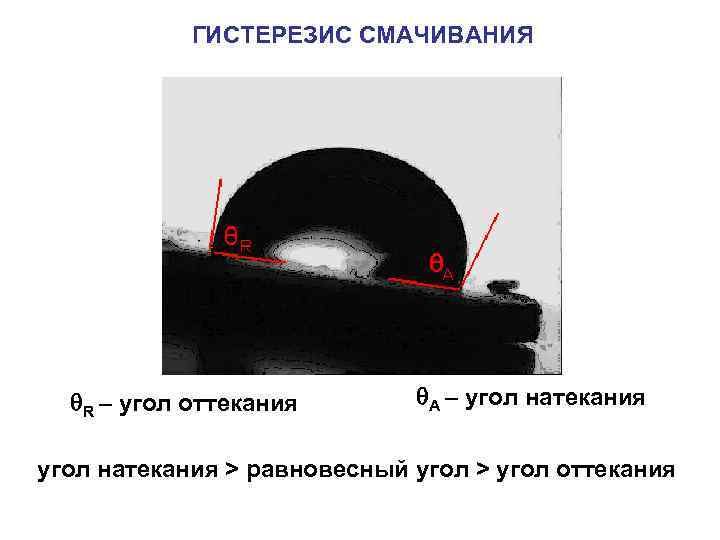 ГИСТЕРЕЗИС СМАЧИВАНИЯ R – угол оттекания А – угол натекания > равновесный угол > угол оттекания
ГИСТЕРЕЗИС СМАЧИВАНИЯ R – угол оттекания А – угол натекания > равновесный угол > угол оттекания
 Капиллярные явления
Капиллярные явления
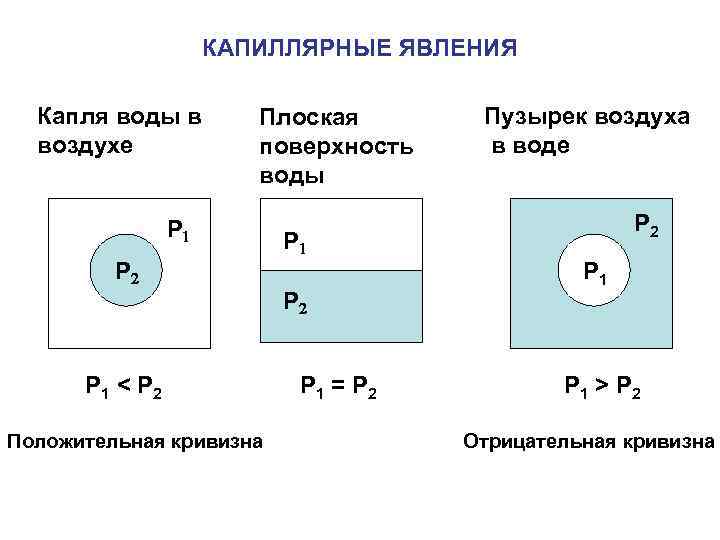 КАПИЛЛЯРНЫЕ ЯВЛЕНИЯ Капля воды в воздухе Плоская поверхность воды P 1 P 2 P 1 < P 2 Положительная кривизна P 1 P 2 P 1 = P 2 Пузырек воздуха в воде P 2 P 1 > P 2 Отрицательная кривизна
КАПИЛЛЯРНЫЕ ЯВЛЕНИЯ Капля воды в воздухе Плоская поверхность воды P 1 P 2 P 1 < P 2 Положительная кривизна P 1 P 2 P 1 = P 2 Пузырек воздуха в воде P 2 P 1 > P 2 Отрицательная кривизна
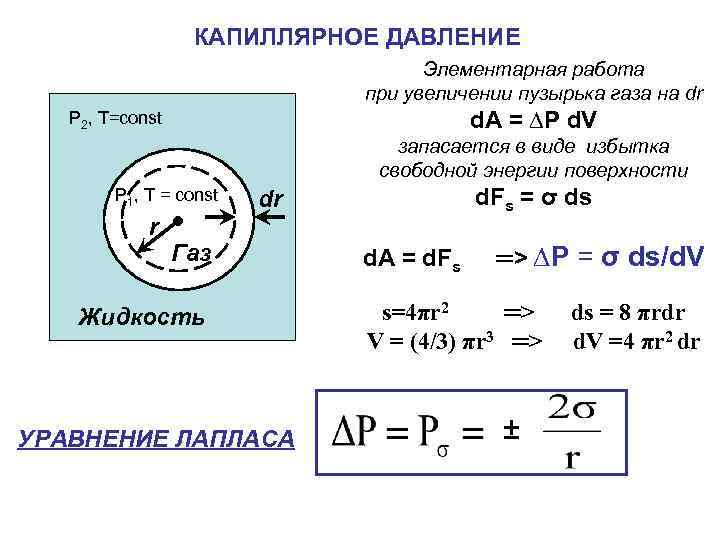 КАПИЛЛЯРНОЕ ДАВЛЕНИЕ Элементарная работа при увеличении пузырька газа на dr d. A = ∆P d. V P 2, T=const запасается в виде избытка свободной энергии поверхности Р 1, T = const r d. Fs = σ ds dr Газ Жидкость УРАВНЕНИЕ ЛАПЛАСА d. A = d. Fs ═> ∆P = σ ds/d. V s=4πr 2 ═> V = (4/3) πr 3 ═> ± ds = 8 πrdr d. V =4 πr 2 dr
КАПИЛЛЯРНОЕ ДАВЛЕНИЕ Элементарная работа при увеличении пузырька газа на dr d. A = ∆P d. V P 2, T=const запасается в виде избытка свободной энергии поверхности Р 1, T = const r d. Fs = σ ds dr Газ Жидкость УРАВНЕНИЕ ЛАПЛАСА d. A = d. Fs ═> ∆P = σ ds/d. V s=4πr 2 ═> V = (4/3) πr 3 ═> ± ds = 8 πrdr d. V =4 πr 2 dr
 УРАВНЕНИЕ ЛАПЛАСА В общем виде r 1 и r 2 – главные радиусы кривизны
УРАВНЕНИЕ ЛАПЛАСА В общем виде r 1 и r 2 – главные радиусы кривизны
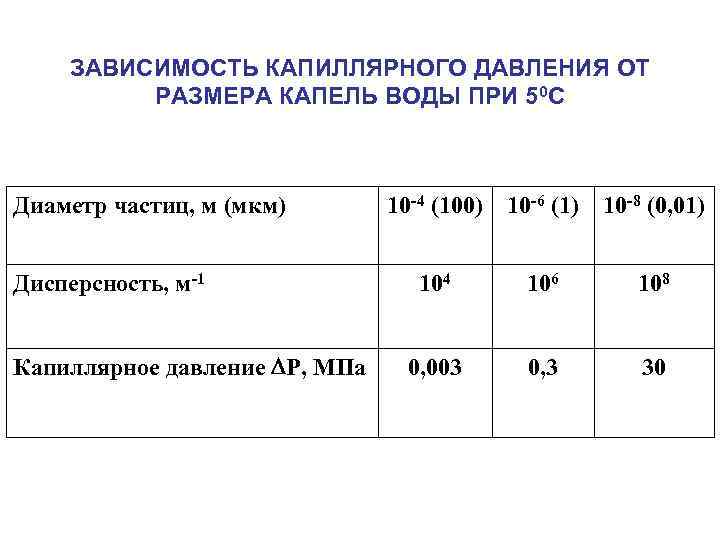 ЗАВИСИМОСТЬ КАПИЛЛЯРНОГО ДАВЛЕНИЯ ОТ РАЗМЕРА КАПЕЛЬ ВОДЫ ПРИ 50 С Диаметр частиц, м (мкм) Дисперсность, м-1 Капиллярное давление P, МПа 10 -4 (100) 10 -6 (1) 10 -8 (0, 01) 104 106 108 0, 003 0, 3 30
ЗАВИСИМОСТЬ КАПИЛЛЯРНОГО ДАВЛЕНИЯ ОТ РАЗМЕРА КАПЕЛЬ ВОДЫ ПРИ 50 С Диаметр частиц, м (мкм) Дисперсность, м-1 Капиллярное давление P, МПа 10 -4 (100) 10 -6 (1) 10 -8 (0, 01) 104 106 108 0, 003 0, 3 30
 ПОДНЯТИЕ ОКРАШЕННОЙ ВОДЫ В СТЕКЛЯННОМ КАПИЛЛЯРЕ
ПОДНЯТИЕ ОКРАШЕННОЙ ВОДЫ В СТЕКЛЯННОМ КАПИЛЛЯРЕ
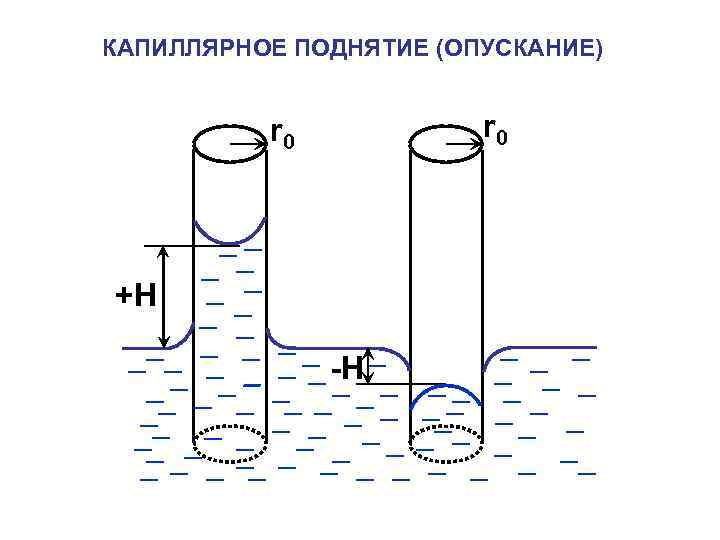 КАПИЛЛЯРНОЕ ПОДНЯТИЕ (ОПУСКАНИЕ) r 0 +H -H
КАПИЛЛЯРНОЕ ПОДНЯТИЕ (ОПУСКАНИЕ) r 0 +H -H
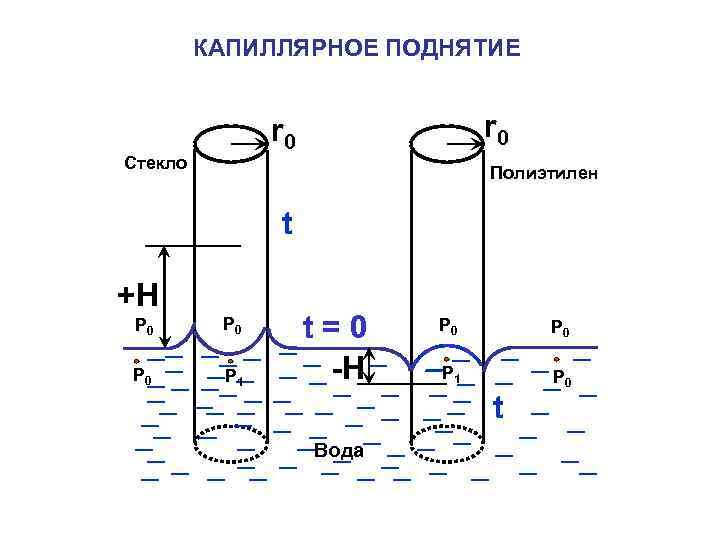 КАПИЛЛЯРНОЕ ПОДНЯТИЕ r 0 Стекло Полиэтилен t +H P 0 P 0 P 1 t=0 -H P 0 P 1 P 0 t Вода
КАПИЛЛЯРНОЕ ПОДНЯТИЕ r 0 Стекло Полиэтилен t +H P 0 P 0 P 1 t=0 -H P 0 P 1 P 0 t Вода
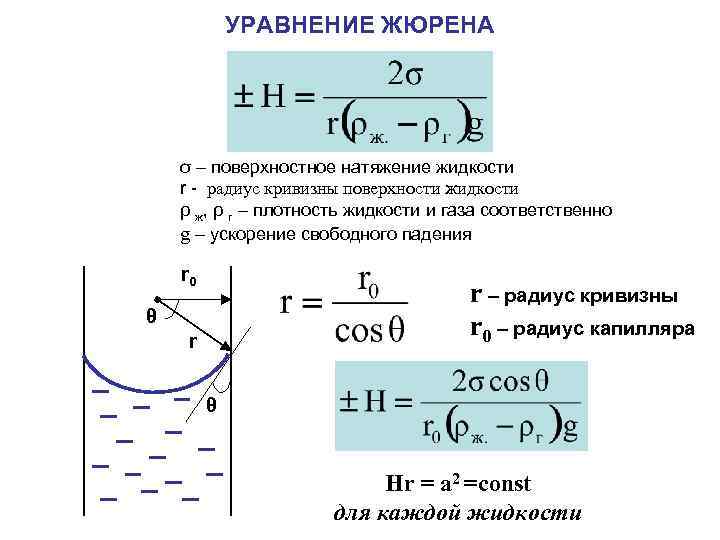 УРАВНЕНИЕ ЖЮРЕНА σ – поверхностное натяжение жидкости r - радиус кривизны поверхности жидкости ρ ж, ρ г – плотность жидкости и газа соответственно g – ускорение свободного падения r 0 r – радиус кривизны r 0 – радиус капилляра θ r θ Hr = a 2 =const для каждой жидкости
УРАВНЕНИЕ ЖЮРЕНА σ – поверхностное натяжение жидкости r - радиус кривизны поверхности жидкости ρ ж, ρ г – плотность жидкости и газа соответственно g – ускорение свободного падения r 0 r – радиус кривизны r 0 – радиус капилляра θ r θ Hr = a 2 =const для каждой жидкости
 ВЫСОТА ПОДНЯТИЯ ВОДЫ В СТЕКЛЯННОМ КАПИЛЛЯРЕ ПРИ УСЛОВИИ ПОЛНОГО СМАЧИВАНИЯ r 0 1 см 1 мкм 1 нм Н 1, 5 мм 1, 5 см 15 км
ВЫСОТА ПОДНЯТИЯ ВОДЫ В СТЕКЛЯННОМ КАПИЛЛЯРЕ ПРИ УСЛОВИИ ПОЛНОГО СМАЧИВАНИЯ r 0 1 см 1 мкм 1 нм Н 1, 5 мм 1, 5 см 15 км

 КАПИЛЛЯРНАЯ СТЯГИВАЮЩАЯ СИЛА
КАПИЛЛЯРНАЯ СТЯГИВАЮЩАЯ СИЛА
 ЗАКОН ТОМПСОНА (КЕЛЬВИНА) – зависимость давления насыщенного пара от радиуса кривизны P 0 - давление насыщенного пара над плоской поверхностью жидкости σ - поверхностное натяжение жидкости Vm- молярный объем жидкости r - радиус кривизны R - универсальная газовая постоянная T - температура
ЗАКОН ТОМПСОНА (КЕЛЬВИНА) – зависимость давления насыщенного пара от радиуса кривизны P 0 - давление насыщенного пара над плоской поверхностью жидкости σ - поверхностное натяжение жидкости Vm- молярный объем жидкости r - радиус кривизны R - универсальная газовая постоянная T - температура
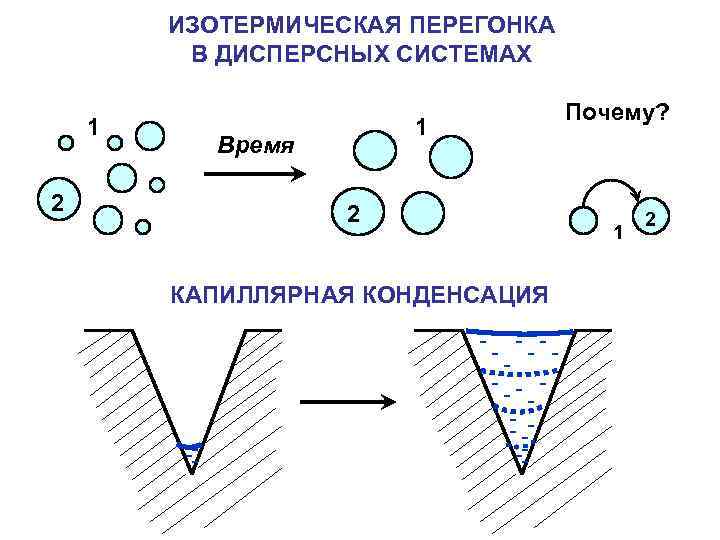 ИЗОТЕРМИЧЕСКАЯ ПЕРЕГОНКА В ДИСПЕРСНЫХ СИСТЕМАХ 1 2 1 Время 2 КАПИЛЛЯРНАЯ КОНДЕНСАЦИЯ Почему? 1 2
ИЗОТЕРМИЧЕСКАЯ ПЕРЕГОНКА В ДИСПЕРСНЫХ СИСТЕМАХ 1 2 1 Время 2 КАПИЛЛЯРНАЯ КОНДЕНСАЦИЯ Почему? 1 2
 АДСОРБЦИЯ ИЗ РАСТВОРОВ НА МЕЖФАЗНЫХ ПОВЕРХНОСТЯХ РАЗДЕЛА ФАЗ РАЗЛИЧНОЙ ПРИРОДЫ
АДСОРБЦИЯ ИЗ РАСТВОРОВ НА МЕЖФАЗНЫХ ПОВЕРХНОСТЯХ РАЗДЕЛА ФАЗ РАЗЛИЧНОЙ ПРИРОДЫ
 Адсорбция – самопроизвольное концентрирование вещества на поверхности раздела фаз Удельная адсорбция (Г) – избыточное количество вещества на единицу площади поверхности раздела фаз [моль/м 2] n – общее число молей растворенного вещества n’, n” – число молей растворенного вещества в каждой фазе s - площадь поверхности раздела фаз
Адсорбция – самопроизвольное концентрирование вещества на поверхности раздела фаз Удельная адсорбция (Г) – избыточное количество вещества на единицу площади поверхности раздела фаз [моль/м 2] n – общее число молей растворенного вещества n’, n” – число молей растворенного вещества в каждой фазе s - площадь поверхности раздела фаз
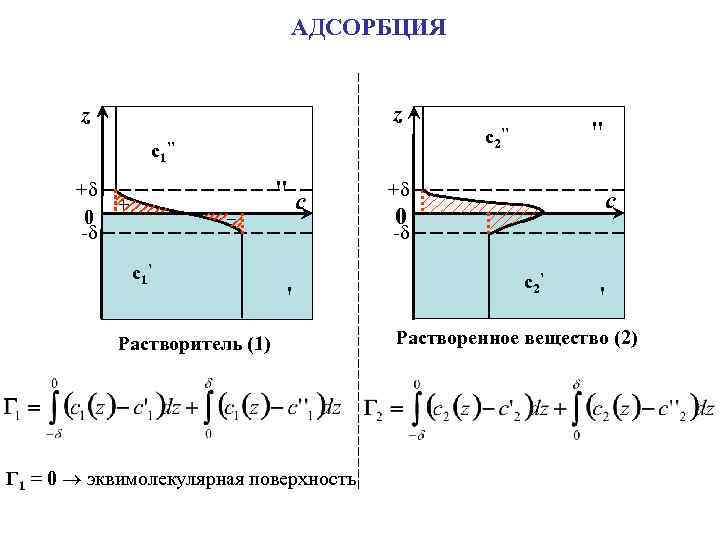 АДСОРБЦИЯ z z c 1 + + 0 - ’’ _ " c 2’’ + c 0 - c 1 ’ ' Растворитель (1) Г 1 = 0 эквимолекулярная поверхность c 2 ’ ' Растворенное вещество (2)
АДСОРБЦИЯ z z c 1 + + 0 - ’’ _ " c 2’’ + c 0 - c 1 ’ ' Растворитель (1) Г 1 = 0 эквимолекулярная поверхность c 2 ’ ' Растворенное вещество (2)
 ТЕРМОДИНАМИКА АДСОРБЦИИ Определение адсорбции Г 2 и поверхностной концентрации с2 S Гексиловый спирт – вода: = 0, 7 нм с2(S) = 5, 8. 10 -2 моль/л 6· 10 -6 моль/м 2
ТЕРМОДИНАМИКА АДСОРБЦИИ Определение адсорбции Г 2 и поверхностной концентрации с2 S Гексиловый спирт – вода: = 0, 7 нм с2(S) = 5, 8. 10 -2 моль/л 6· 10 -6 моль/м 2
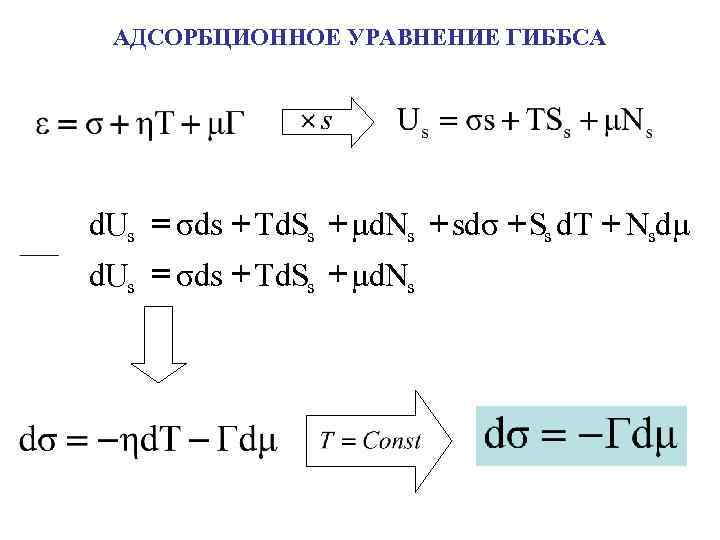 АДСОРБЦИОННОЕ УРАВНЕНИЕ ГИББСА d. Us = σds + Td. Ss + μd. Ns + sdσ + Ss d. T + Nsdμ d. Us = σds + Td. Ss + μd. Ns
АДСОРБЦИОННОЕ УРАВНЕНИЕ ГИББСА d. Us = σds + Td. Ss + μd. Ns + sdσ + Ss d. T + Nsdμ d. Us = σds + Td. Ss + μd. Ns
 АДСОРБЦИОННОЕ УРАВНЕНИЕ ГИББСА при α = 1
АДСОРБЦИОННОЕ УРАВНЕНИЕ ГИББСА при α = 1
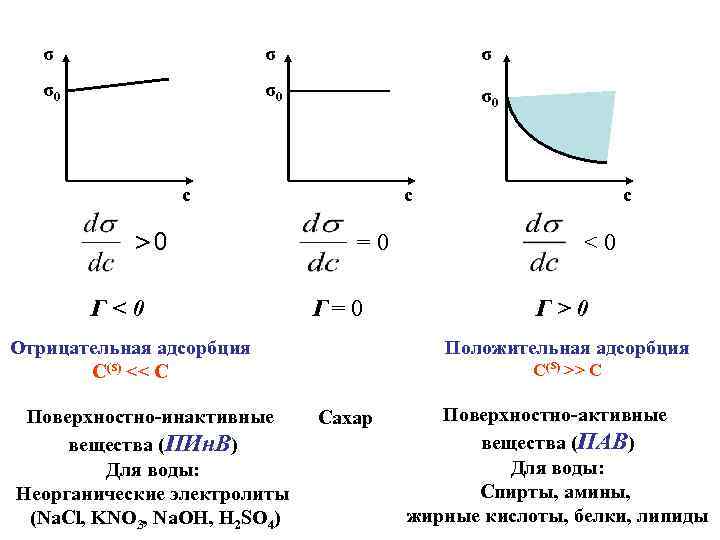 σ σ σ σ0 σ0 σ0 c >0 Г<0 c =0 Г= 0 Отрицательная адсорбция С(s) << C Поверхностно-инактивные вещества (ПИн. В) Для воды: Неорганические электролиты (Na. Cl, KNO 3, Na. OH, H 2 SO 4) c <0 Г>0 Положительная адсорбция С(s) >> C Сахар Поверхностно-активные вещества (ПАВ) Для воды: Спирты, амины, жирные кислоты, белки, липиды
σ σ σ σ0 σ0 σ0 c >0 Г<0 c =0 Г= 0 Отрицательная адсорбция С(s) << C Поверхностно-инактивные вещества (ПИн. В) Для воды: Неорганические электролиты (Na. Cl, KNO 3, Na. OH, H 2 SO 4) c <0 Г>0 Положительная адсорбция С(s) >> C Сахар Поверхностно-активные вещества (ПАВ) Для воды: Спирты, амины, жирные кислоты, белки, липиды

 СХЕМА СТРОЕНИЯ МОЛЕКУЛЫ ПАВ Компьютерная модель молекулы тридециловой кислоты C 12 H 25 COO Полярная (гидрофильная) группа -OH, -COOMe, -NH 2 Углеводородная (гидрофобная) часть С n H m-
СХЕМА СТРОЕНИЯ МОЛЕКУЛЫ ПАВ Компьютерная модель молекулы тридециловой кислоты C 12 H 25 COO Полярная (гидрофильная) группа -OH, -COOMe, -NH 2 Углеводородная (гидрофобная) часть С n H m-
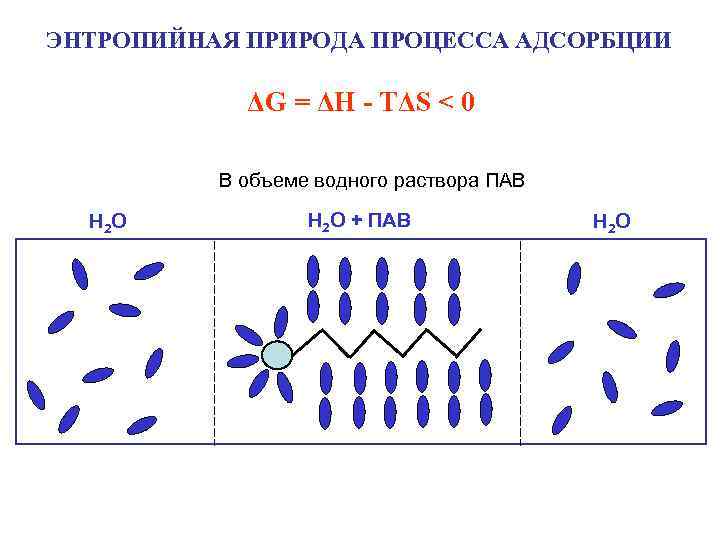 ЭНТРОПИЙНАЯ ПРИРОДА ПРОЦЕССА АДСОРБЦИИ ΔG = ΔH - TΔS < 0 В объеме водного раствора ПАВ H 2 O H 2 O + ПАВ H 2 O
ЭНТРОПИЙНАЯ ПРИРОДА ПРОЦЕССА АДСОРБЦИИ ΔG = ΔH - TΔS < 0 В объеме водного раствора ПАВ H 2 O H 2 O + ПАВ H 2 O
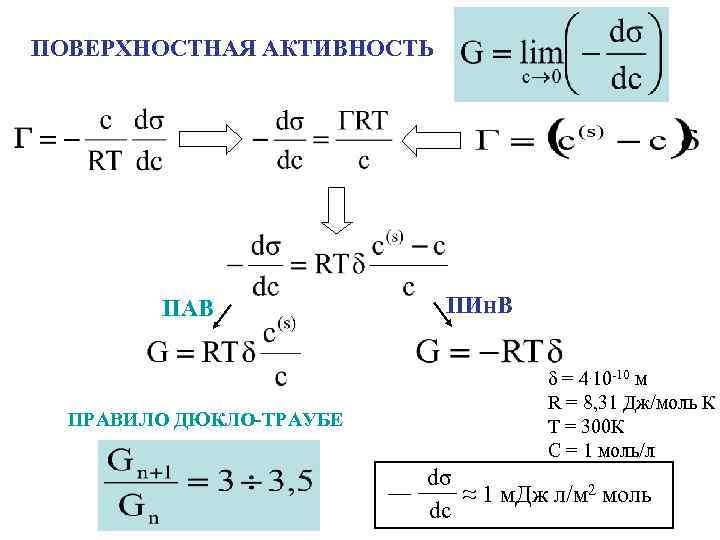 ПОВЕРХНОСТНАЯ АКТИВНОСТЬ ПАВ ПРАВИЛО ДЮКЛО-ТРАУБЕ ПИн. В δ = 4. 10 -10 м R = 8, 31 Дж/моль К Т = 300 К С = 1 моль/л dσ ≈ 1 м. Дж л/м 2 моль dc
ПОВЕРХНОСТНАЯ АКТИВНОСТЬ ПАВ ПРАВИЛО ДЮКЛО-ТРАУБЕ ПИн. В δ = 4. 10 -10 м R = 8, 31 Дж/моль К Т = 300 К С = 1 моль/л dσ ≈ 1 м. Дж л/м 2 моль dc
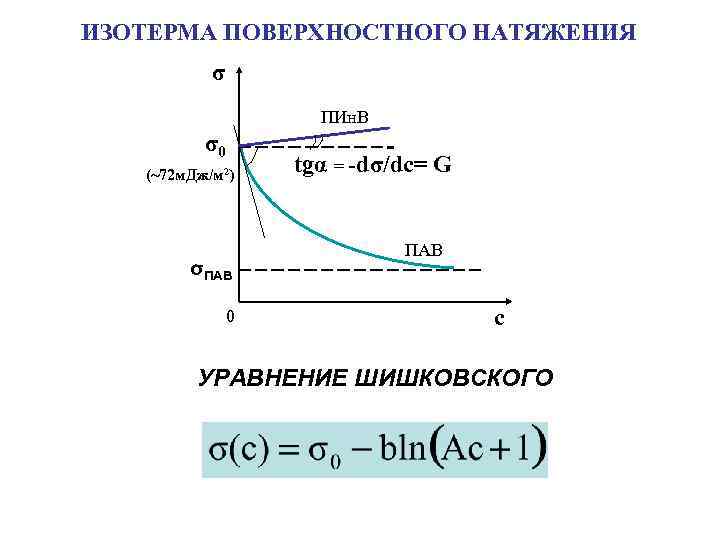 ИЗОТЕРМА ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ σ ПИн. В σ0 (~72 м. Дж/м 2) σПАВ 0 tgα = -dσ/dc= G ПАВ c УРАВНЕНИЕ ШИШКОВСКОГО
ИЗОТЕРМА ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ σ ПИн. В σ0 (~72 м. Дж/м 2) σПАВ 0 tgα = -dσ/dc= G ПАВ c УРАВНЕНИЕ ШИШКОВСКОГО
 АНАЛИЗ УРАВНЕНИЯ ШИШКОВСКОГО При условии c < 1/A (Область Генри) σ σ0 n n+1 n+2 с
АНАЛИЗ УРАВНЕНИЯ ШИШКОВСКОГО При условии c < 1/A (Область Генри) σ σ0 n n+1 n+2 с
 АНАЛИЗ УРАВНЕНИЯ ШИШКОВСКОГО При условии c > 1/A На границе с воздухом σmin~ 20 м. Дж/м 2 , т. е. Г=Гmax
АНАЛИЗ УРАВНЕНИЯ ШИШКОВСКОГО При условии c > 1/A На границе с воздухом σmin~ 20 м. Дж/м 2 , т. е. Г=Гmax
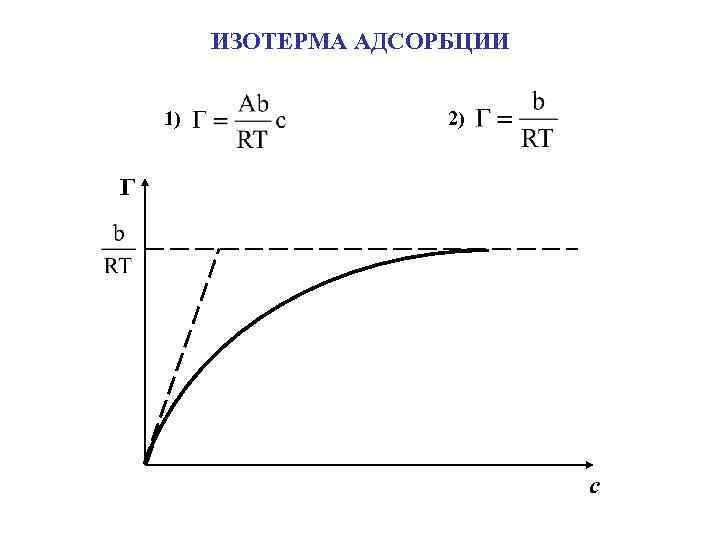 ИЗОТЕРМА АДСОРБЦИИ 1) 2) Г с
ИЗОТЕРМА АДСОРБЦИИ 1) 2) Г с
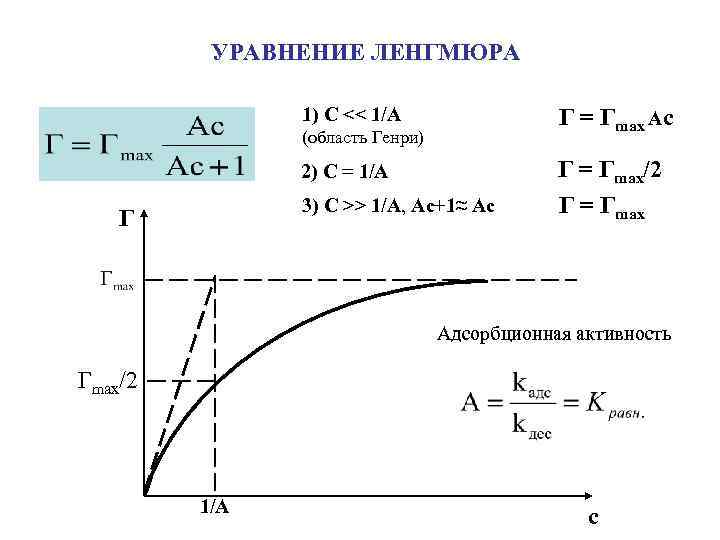 УРАВНЕНИЕ ЛЕНГМЮРА 1) C << 1/A Г = Гmax Ac (область Генри) 2) C = 1/A 3) C >> 1/A, Ac+1≈ Ac Г Г = Гmax/2 Г = Гmax Адсорбционная активность Гmax/2 1/A с
УРАВНЕНИЕ ЛЕНГМЮРА 1) C << 1/A Г = Гmax Ac (область Генри) 2) C = 1/A 3) C >> 1/A, Ac+1≈ Ac Г Г = Гmax/2 Г = Гmax Адсорбционная активность Гmax/2 1/A с
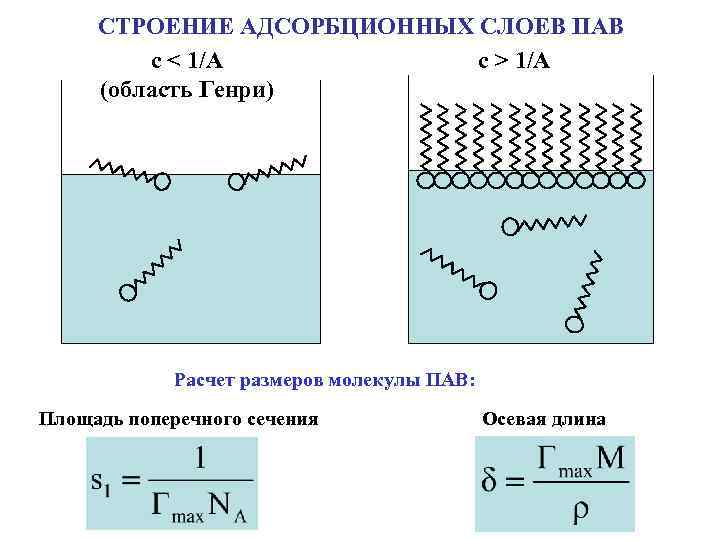 СТРОЕНИЕ АДСОРБЦИОННЫХ СЛОЕВ ПАВ с > 1/A с < 1/A (область Генри) Расчет размеров молекулы ПАВ: Площадь поперечного сечения Осевая длина
СТРОЕНИЕ АДСОРБЦИОННЫХ СЛОЕВ ПАВ с > 1/A с < 1/A (область Генри) Расчет размеров молекулы ПАВ: Площадь поперечного сечения Осевая длина
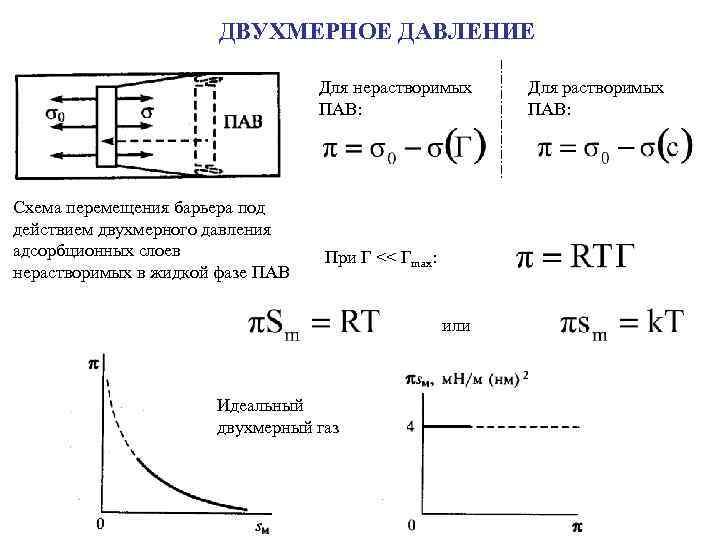 ДВУХМЕРНОЕ ДАВЛЕНИЕ Для нерастворимых ПАВ: Схема перемещения барьера под действием двухмерного давления адсорбционных слоев нерастворимых в жидкой фазе ПАВ При Г << Гmax: или Идеальный двухмерный газ Для растворимых ПАВ:
ДВУХМЕРНОЕ ДАВЛЕНИЕ Для нерастворимых ПАВ: Схема перемещения барьера под действием двухмерного давления адсорбционных слоев нерастворимых в жидкой фазе ПАВ При Г << Гmax: или Идеальный двухмерный газ Для растворимых ПАВ:
 ВАННА ЛЕНГМЮРА Учет площади молекул дает: Схема прибора Ленгмюра для измерения адсорбционных слоев нерастворимых ПАВ
ВАННА ЛЕНГМЮРА Учет площади молекул дает: Схема прибора Ленгмюра для измерения адсорбционных слоев нерастворимых ПАВ
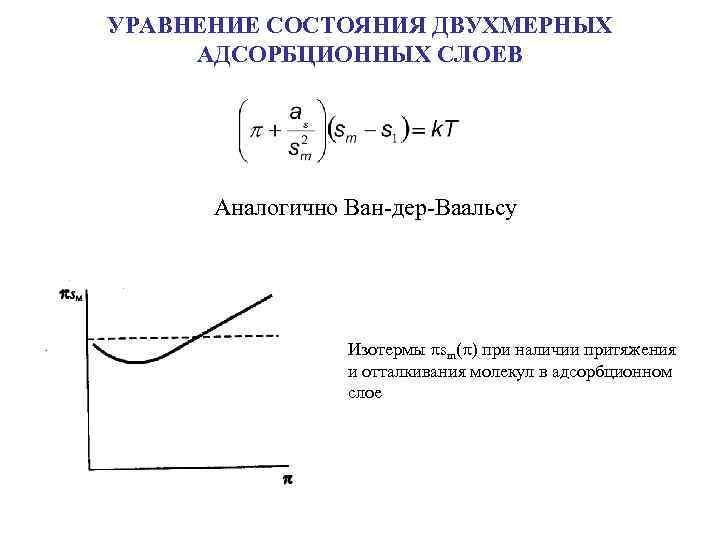 УРАВНЕНИЕ СОСТОЯНИЯ ДВУХМЕРНЫХ АДСОРБЦИОННЫХ СЛОЕВ Аналогично Ван-дер-Ваальсу Изотермы sm( ) при наличии притяжения и отталкивания молекул в адсорбционном слое
УРАВНЕНИЕ СОСТОЯНИЯ ДВУХМЕРНЫХ АДСОРБЦИОННЫХ СЛОЕВ Аналогично Ван-дер-Ваальсу Изотермы sm( ) при наличии притяжения и отталкивания молекул в адсорбционном слое
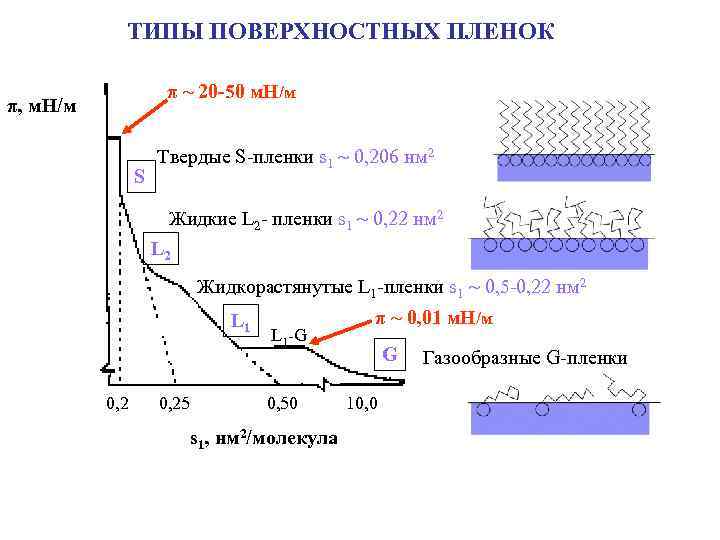 ТИПЫ ПОВЕРХНОСТНЫХ ПЛЕНОК π ~ 20 -50 м. Н/м π, м. Н/м S Твердые S-пленки s 1 0, 206 нм 2 Жидкие L 2 - пленки s 1 0, 22 нм 2 L 2 Жидкорастянутые L 1 -пленки s 1 0, 5 -0, 22 нм 2 L 1 0, 25 L 1 -G 0, 50 s 1, нм 2/молекула π ~ 0, 01 м. Н/м G 10, 0 Газообразные G-пленки
ТИПЫ ПОВЕРХНОСТНЫХ ПЛЕНОК π ~ 20 -50 м. Н/м π, м. Н/м S Твердые S-пленки s 1 0, 206 нм 2 Жидкие L 2 - пленки s 1 0, 22 нм 2 L 2 Жидкорастянутые L 1 -пленки s 1 0, 5 -0, 22 нм 2 L 1 0, 25 L 1 -G 0, 50 s 1, нм 2/молекула π ~ 0, 01 м. Н/м G 10, 0 Газообразные G-пленки
![СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА: Ethanaminium, 2 -[[[(2, 2 -dipentadecyl-1, 3 -dioxolan-4 yl)methoxy]hydroxyphosphinyl]oxy]-N, N, N-trimethyl-, inner СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА: Ethanaminium, 2 -[[[(2, 2 -dipentadecyl-1, 3 -dioxolan-4 yl)methoxy]hydroxyphosphinyl]oxy]-N, N, N-trimethyl-, inner](https://present5.com/presentation/81098163_62754721/image-54.jpg) СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА: Ethanaminium, 2 -[[[(2, 2 -dipentadecyl-1, 3 -dioxolan-4 yl)methoxy]hydroxyphosphinyl]oxy]-N, N, N-trimethyl-, inner salt
СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА: Ethanaminium, 2 -[[[(2, 2 -dipentadecyl-1, 3 -dioxolan-4 yl)methoxy]hydroxyphosphinyl]oxy]-N, N, N-trimethyl-, inner salt
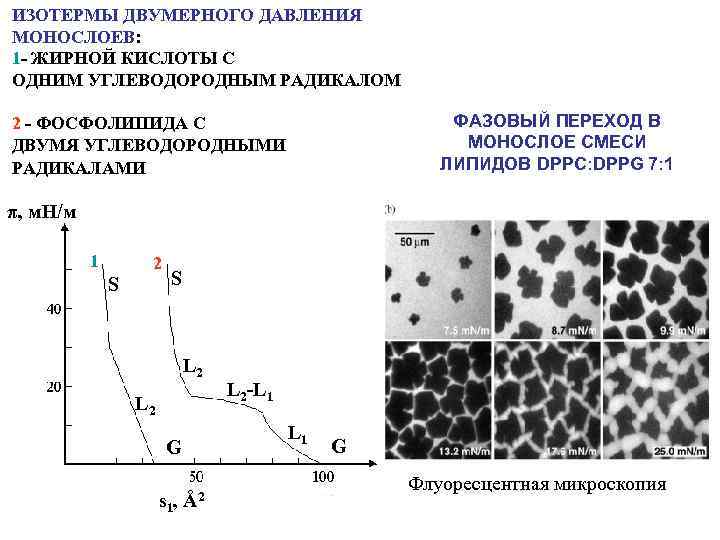 ИЗОТЕРМЫ ДВУМЕРНОГО ДАВЛЕНИЯ МОНОСЛОЕВ: 1 - ЖИРНОЙ КИСЛОТЫ С ОДНИМ УГЛЕВОДОРОДНЫМ РАДИКАЛОМ ФАЗОВЫЙ ПЕРЕХОД В МОНОСЛОЕ СМЕСИ ЛИПИДОВ DPPC: DPPG 7: 1 2 - ФОСФОЛИПИДА С ДВУМЯ УГЛЕВОДОРОДНЫМИ РАДИКАЛАМИ π, м. Н/м 1 2 S S L 2 L 1 G s 1 , L 2 -L 1 Å2 G Флуоресцентная микроскопия
ИЗОТЕРМЫ ДВУМЕРНОГО ДАВЛЕНИЯ МОНОСЛОЕВ: 1 - ЖИРНОЙ КИСЛОТЫ С ОДНИМ УГЛЕВОДОРОДНЫМ РАДИКАЛОМ ФАЗОВЫЙ ПЕРЕХОД В МОНОСЛОЕ СМЕСИ ЛИПИДОВ DPPC: DPPG 7: 1 2 - ФОСФОЛИПИДА С ДВУМЯ УГЛЕВОДОРОДНЫМИ РАДИКАЛАМИ π, м. Н/м 1 2 S S L 2 L 1 G s 1 , L 2 -L 1 Å2 G Флуоресцентная микроскопия
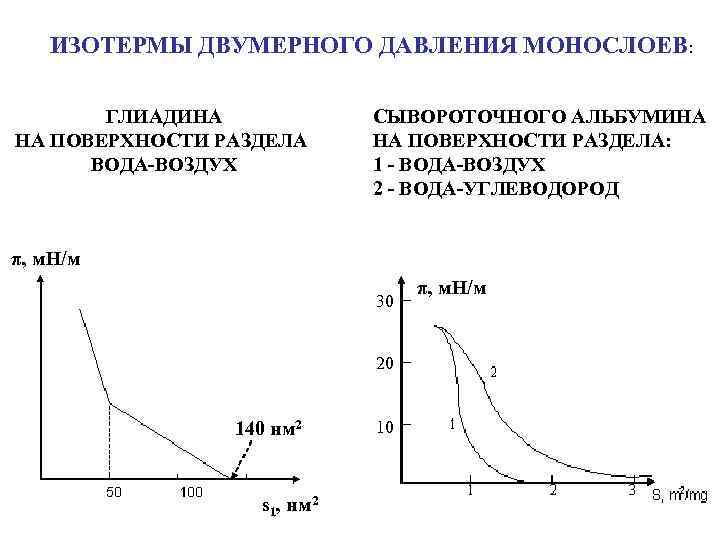 ИЗОТЕРМЫ ДВУМЕРНОГО ДАВЛЕНИЯ МОНОСЛОЕВ: ГЛИАДИНА НА ПОВЕРХНОСТИ РАЗДЕЛА ВОДА-ВОЗДУХ СЫВОРОТОЧНОГО АЛЬБУМИНА НА ПОВЕРХНОСТИ РАЗДЕЛА: 1 - ВОДА-ВОЗДУХ 2 - ВОДА-УГЛЕВОДОРОД π, м. Н/м 30 20 140 нм 2 s 1, нм 2 10 π, м. Н/м
ИЗОТЕРМЫ ДВУМЕРНОГО ДАВЛЕНИЯ МОНОСЛОЕВ: ГЛИАДИНА НА ПОВЕРХНОСТИ РАЗДЕЛА ВОДА-ВОЗДУХ СЫВОРОТОЧНОГО АЛЬБУМИНА НА ПОВЕРХНОСТИ РАЗДЕЛА: 1 - ВОДА-ВОЗДУХ 2 - ВОДА-УГЛЕВОДОРОД π, м. Н/м 30 20 140 нм 2 s 1, нм 2 10 π, м. Н/м
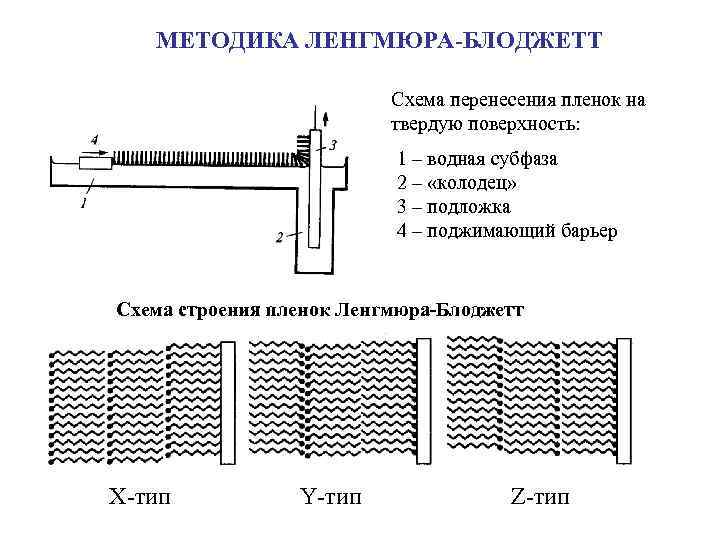 МЕТОДИКА ЛЕНГМЮРА-БЛОДЖЕТТ Схема перенесения пленок на твердую поверхность: 1 – водная субфаза 2 – «колодец» 3 – подложка 4 – поджимающий барьер Схема строения пленок Ленгмюра-Блоджетт X-тип Y-тип Z-тип
МЕТОДИКА ЛЕНГМЮРА-БЛОДЖЕТТ Схема перенесения пленок на твердую поверхность: 1 – водная субфаза 2 – «колодец» 3 – подложка 4 – поджимающий барьер Схема строения пленок Ленгмюра-Блоджетт X-тип Y-тип Z-тип
 АДСОРБЦИЯ НА ГРАНИЦЕ ДВУХ КОНДЕНСИРОВАННЫХ ФАЗ Правило уравнивания полярностей Ребиндера: Для границы 2 -х конденсированных фаз поверхностно-активным является вещество, имеющее промежуточную полярность по сравнению с конденсированными фазами. Его молекулы размещаются на границе 2 -х конденсированных фаз таким образом, чтобы снизить разность полярностей, существующую между контактирующими фазами. ОСОБЕННОСТИ АДСОРБЦИИ НА ГРАНИЦЕ ДВУХ НЕСМЕШИВАЮЩИХСЯ ЖИДКОСТЕЙ 1. Область Генри: Масло 2. На границе с неполярной жидкостью σmin~ 1 м. Дж/м 2, но может быть и 0, 01 - 0, 1 м. Дж/м 2 3. Выход из воды – энтропийная природа адсорбции; выход из масла – энтальпийная. Вода 4. Правило Дюкло-Траубе работает при выходе из воды, не работает при выходе из масла
АДСОРБЦИЯ НА ГРАНИЦЕ ДВУХ КОНДЕНСИРОВАННЫХ ФАЗ Правило уравнивания полярностей Ребиндера: Для границы 2 -х конденсированных фаз поверхностно-активным является вещество, имеющее промежуточную полярность по сравнению с конденсированными фазами. Его молекулы размещаются на границе 2 -х конденсированных фаз таким образом, чтобы снизить разность полярностей, существующую между контактирующими фазами. ОСОБЕННОСТИ АДСОРБЦИИ НА ГРАНИЦЕ ДВУХ НЕСМЕШИВАЮЩИХСЯ ЖИДКОСТЕЙ 1. Область Генри: Масло 2. На границе с неполярной жидкостью σmin~ 1 м. Дж/м 2, но может быть и 0, 01 - 0, 1 м. Дж/м 2 3. Выход из воды – энтропийная природа адсорбции; выход из масла – энтальпийная. Вода 4. Правило Дюкло-Траубе работает при выходе из воды, не работает при выходе из масла
![АДСОРБЦИЯ ИЗ РАСТВОРОВ НА ТВЕРДОЙ ПОВЕРХНОСТИ [моль/г] С 0 – исходная концентрация ПАВ; С АДСОРБЦИЯ ИЗ РАСТВОРОВ НА ТВЕРДОЙ ПОВЕРХНОСТИ [моль/г] С 0 – исходная концентрация ПАВ; С](https://present5.com/presentation/81098163_62754721/image-59.jpg) АДСОРБЦИЯ ИЗ РАСТВОРОВ НА ТВЕРДОЙ ПОВЕРХНОСТИ [моль/г] С 0 – исходная концентрация ПАВ; С равн – равновесная концентрация ПАВ (концентрация ПАВ после установления адсорбционного равновесия); V – объем раствора; m - масса адсорбента
АДСОРБЦИЯ ИЗ РАСТВОРОВ НА ТВЕРДОЙ ПОВЕРХНОСТИ [моль/г] С 0 – исходная концентрация ПАВ; С равн – равновесная концентрация ПАВ (концентрация ПАВ после установления адсорбционного равновесия); V – объем раствора; m - масса адсорбента
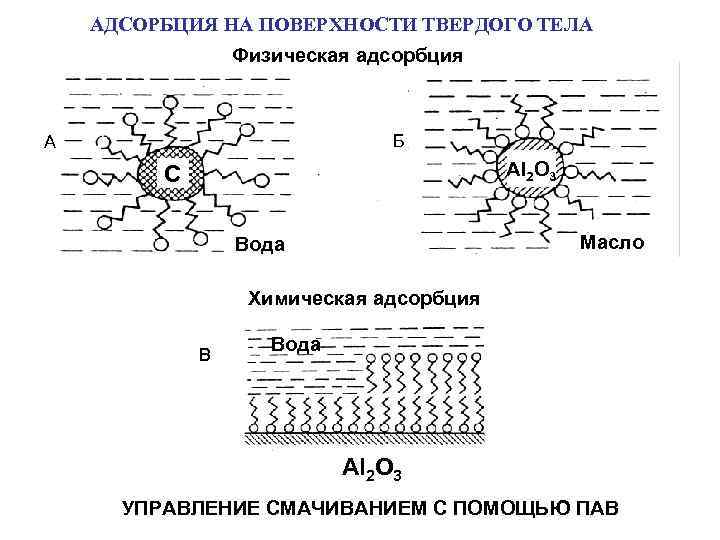 АДСОРБЦИЯ НА ПОВЕРХНОСТИ ТВЕРДОГО ТЕЛА Физическая адсорбция Б А Al 2 O 3 C Масло Вода Химическая адсорбция В Вода Al 2 O 3 УПРАВЛЕНИЕ СМАЧИВАНИЕМ С ПОМОЩЬЮ ПАВ
АДСОРБЦИЯ НА ПОВЕРХНОСТИ ТВЕРДОГО ТЕЛА Физическая адсорбция Б А Al 2 O 3 C Масло Вода Химическая адсорбция В Вода Al 2 O 3 УПРАВЛЕНИЕ СМАЧИВАНИЕМ С ПОМОЩЬЮ ПАВ


