 ЯДЕРНЫЙ ТОПЛИВНЫЙ ЦИКЛ
ЯДЕРНЫЙ ТОПЛИВНЫЙ ЦИКЛ
 n n n Молекулой называется малейшая частица вещества, обладающая его основными химическими свойствами. Молекула состоит из одинаковых или разных атомов, соединенных межатомными связями. Молекулы простых веществ (К, Не, О 2, Н 2, Мо, . . . ) состоят из одного или нескольких атомов одного химического элемента. Молекулы сложных веществ (UO 2, Н 3 ВО 3, В 4 С, . . . ) состоят из атомов нескольких химических элементов.
n n n Молекулой называется малейшая частица вещества, обладающая его основными химическими свойствами. Молекула состоит из одинаковых или разных атомов, соединенных межатомными связями. Молекулы простых веществ (К, Не, О 2, Н 2, Мо, . . . ) состоят из одного или нескольких атомов одного химического элемента. Молекулы сложных веществ (UO 2, Н 3 ВО 3, В 4 С, . . . ) состоят из атомов нескольких химических элементов.
 n 1 а. е. м. - это 1/12 часть массы изотопа атома углерода-12. В единицах системы СГС (которая чаще всего используется в нейтронно фи зических расчетах) 1 а. е. м. эквивалентна 1. 660567. 10 24 г. Относитель ная масса молекулы или атома, выраженная в а. е. м. , называется молеку лярной(или атомной соответственно) массой и обозначается символом А.
n 1 а. е. м. - это 1/12 часть массы изотопа атома углерода-12. В единицах системы СГС (которая чаще всего используется в нейтронно фи зических расчетах) 1 а. е. м. эквивалентна 1. 660567. 10 24 г. Относитель ная масса молекулы или атома, выраженная в а. е. м. , называется молеку лярной(или атомной соответственно) массой и обозначается символом А.
 n молекулярная концентрация любого вещества легко рассчитывается по известным величинам плотности и молекулярной массы А вещества по формуле: n (1)
n молекулярная концентрация любого вещества легко рассчитывается по известным величинам плотности и молекулярной массы А вещества по формуле: n (1)
 Для сложных веществ (2)
Для сложных веществ (2)
 Пример Кристаллическая борная кислота H 3 BO 3 плотностью = 1. 28 г/см 3 будет иметь относительную молекулярную массу: n А = 3 Ан+1 Ав+3 Ао = 3· 1 + 1· 1 0. 81 + 3· 16 = =61. 81 а. е. м. , n а, следовательно, её молекулярная концентрация будет равна: n
Пример Кристаллическая борная кислота H 3 BO 3 плотностью = 1. 28 г/см 3 будет иметь относительную молекулярную массу: n А = 3 Ан+1 Ав+3 Ао = 3· 1 + 1· 1 0. 81 + 3· 16 = =61. 81 а. е. м. , n а, следовательно, её молекулярная концентрация будет равна: n
 n n n атомные концентрации компонентов сложных веществ находятся по общей формуле: (3) где ni число атомов i го компонента в каждой молекуле вещества, а N молекулярная концентрация вещества.
n n n атомные концентрации компонентов сложных веществ находятся по общей формуле: (3) где ni число атомов i го компонента в каждой молекуле вещества, а N молекулярная концентрация вещества.
 В упомянутом выше примере борной кислоты: n атомная концентрация водорода Nн= 3 N = 3· 1, 2471· 1022 = 3. 7413 · 1022 см 3, т. к. в каждой молекуле борной кислоты содержится по три атома водорода; n атомная концентрация бора Nв = N =1, 247· 1022 см 3, т. к. в молекуле борной кислоты содержится только один атом бора; n атомная концентрация кислорода No= 3 N = 3· 1, 2471· 1022 = 3. 7413· 1022 см 3, т. к. в каждой молекуле борной кислоты по три атома кислорода.
В упомянутом выше примере борной кислоты: n атомная концентрация водорода Nн= 3 N = 3· 1, 2471· 1022 = 3. 7413 · 1022 см 3, т. к. в каждой молекуле борной кислоты содержится по три атома водорода; n атомная концентрация бора Nв = N =1, 247· 1022 см 3, т. к. в молекуле борной кислоты содержится только один атом бора; n атомная концентрация кислорода No= 3 N = 3· 1, 2471· 1022 = 3. 7413· 1022 см 3, т. к. в каждой молекуле борной кислоты по три атома кислорода.
 атомные концентрации в простых многоатомных веществах, очевидно, можно рассматривать как частность случая и находить по общей формуле (3). n Пример. Молекула йода (J 2) содержит по два атома химического элемента йода, поэтому атомная концентрация йода в кристаллическом йоде плотностью = 4. 9 г/см 3 будет равна n n
атомные концентрации в простых многоатомных веществах, очевидно, можно рассматривать как частность случая и находить по общей формуле (3). n Пример. Молекула йода (J 2) содержит по два атома химического элемента йода, поэтому атомная концентрация йода в кристаллическом йоде плотностью = 4. 9 г/см 3 будет равна n n
 Строение и характеристики атомов n n n Атомы состоят из ядра и электронной оболочки. Атомы различных химических элементов отличаются прежде всего по их массе, и атомная масса в какой то мере определяет периодичность повто рения химических свойств различных атомов. Однако массовое число A не является однозначной характеристикой всех свойств атомов любых веществ. Действительной характеристикой, определяющей физико химическую индивидуальность атома вещества, является его атомный номер (z) в от крытой Д. И. Менделеевым Периодической Системе элементов. Называя атомный номер элемента z, мы фактически называем сам этот элемент, об атомах которого идёт речь. Например, если z = 6, нам ясно, что речь идет об углероде (С), а если z = 92, это равносильно тому, что элемент назван ураном (U), и т. д. Поэтому атомный номер элемента z характеристика, равноценная при нятому химическому символу атомов вещества. Массовое число A и атомный номер z элемента - пара характе ристик , полностью определяющих физико химическую индивидуальность ато мов любого вещества.
Строение и характеристики атомов n n n Атомы состоят из ядра и электронной оболочки. Атомы различных химических элементов отличаются прежде всего по их массе, и атомная масса в какой то мере определяет периодичность повто рения химических свойств различных атомов. Однако массовое число A не является однозначной характеристикой всех свойств атомов любых веществ. Действительной характеристикой, определяющей физико химическую индивидуальность атома вещества, является его атомный номер (z) в от крытой Д. И. Менделеевым Периодической Системе элементов. Называя атомный номер элемента z, мы фактически называем сам этот элемент, об атомах которого идёт речь. Например, если z = 6, нам ясно, что речь идет об углероде (С), а если z = 92, это равносильно тому, что элемент назван ураном (U), и т. д. Поэтому атомный номер элемента z характеристика, равноценная при нятому химическому символу атомов вещества. Массовое число A и атомный номер z элемента - пара характе ристик , полностью определяющих физико химическую индивидуальность ато мов любого вещества.
 n Размеры атомов, найденные в экспериментах, выполненных по различным методикам, имеют порядок 10 8 см, а размеры ядер атомов величины порядка 10 13 см. Эти цифры свидетельствуют о том, что ядро занимает ничтожную часть объёма атома. Если под объёмом ядра понимать сферу, в пределах которой эффек тивно действуют ядерные силы, радиус этой сферы можно оценить по полу эмпирической формуле: (4) n где А, а. е. м. атомная масса элемента. n n
n Размеры атомов, найденные в экспериментах, выполненных по различным методикам, имеют порядок 10 8 см, а размеры ядер атомов величины порядка 10 13 см. Эти цифры свидетельствуют о том, что ядро занимает ничтожную часть объёма атома. Если под объёмом ядра понимать сферу, в пределах которой эффек тивно действуют ядерные силы, радиус этой сферы можно оценить по полу эмпирической формуле: (4) n где А, а. е. м. атомная масса элемента. n n
 Строение ядер и свойства ядерных сил n n n Ядром называется центральная часть атома, в которой сосредоточена почти вся масса атома и его положительный электрический заряд. Все атомные ядра состоят из протонов и нейтронов, которые считаются двумя зарядовыми состояниями одной частицы – нуклона. Ядро любого атома имеет сложную структуру и состоит из частиц, называемых нуклонами. Известно два типа нуклонов протоны и нейтроны. Протоны нуклоны массой 1 а. е. м. с положительным зарядом, равным единице, то есть величине элементарного заряда (электрона). Нейтроны электронейтральные нуклоны массой 1 а. е. м. *) Строго говоря, массы покоя протонов и нейтронов несколько отличаются: mр= 1. 6726 · 10 24 г mn= 1. 67439· 10 24 г.
Строение ядер и свойства ядерных сил n n n Ядром называется центральная часть атома, в которой сосредоточена почти вся масса атома и его положительный электрический заряд. Все атомные ядра состоят из протонов и нейтронов, которые считаются двумя зарядовыми состояниями одной частицы – нуклона. Ядро любого атома имеет сложную структуру и состоит из частиц, называемых нуклонами. Известно два типа нуклонов протоны и нейтроны. Протоны нуклоны массой 1 а. е. м. с положительным зарядом, равным единице, то есть величине элементарного заряда (электрона). Нейтроны электронейтральные нуклоны массой 1 а. е. м. *) Строго говоря, массы покоя протонов и нейтронов несколько отличаются: mр= 1. 6726 · 10 24 г mn= 1. 67439· 10 24 г.
 n Так как масса ядра практически равна A, заряд ядра z, а массы протона и нейтрона практически равны, при таких представлениях следует принять как должное, что ядро устойчивого электронейтрального атома состоит из z протонов и (A z) нейтронов. Следовательно, атомный номер элемента есть не что иное как протонный заряд ядра атома, выраженный в единицах элементарного заряда электрона. Другими словами, z - это число протонов в ядре атома.
n Так как масса ядра практически равна A, заряд ядра z, а массы протона и нейтрона практически равны, при таких представлениях следует принять как должное, что ядро устойчивого электронейтрального атома состоит из z протонов и (A z) нейтронов. Следовательно, атомный номер элемента есть не что иное как протонный заряд ядра атома, выраженный в единицах элементарного заряда электрона. Другими словами, z - это число протонов в ядре атома.
 n n Протон в свободном состоянии (то есть вне атомных ядер) стабилен. Нейтрон в свободном состоянии длительно существовать не может, он претерпевает распад на протон, электрон и антинейтрино с периодом полураспада T 1/2 = 11. 2 мин. по схеме: Антинейтрино электронейтральная частица материи с нулевой массой покоя.
n n Протон в свободном состоянии (то есть вне атомных ядер) стабилен. Нейтрон в свободном состоянии длительно существовать не может, он претерпевает распад на протон, электрон и антинейтрино с периодом полураспада T 1/2 = 11. 2 мин. по схеме: Антинейтрино электронейтральная частица материи с нулевой массой покоя.
 n n Нуклидами называются атомы с определенным порядковым номером, массовым числом и ядром в основном или метастабильном состоянии. Среди множества нуклидов (а их в настоящее время известно более 2000 естественных и искусственных) есть такие, у которых одна из двух упомянутых характеристик одинакова, а другая – различна по величине. Нуклиды с одинаковым z (числом протонов) называют изотопами. Поскольку атомный номер определяет в соответствии с Периодическим Законом Д. И. Менделеева индивидуальность только химических свойств атома элемента, об изотопах всегда говорят со ссылкой на символ соответствующего им химического элемента в Периодической Системе. Например, 233 U, 234 U, 235 U, 236 U, 238 U, 239 U все это изотопы урана, который в Периодической Системе элементов Д. И. Менделеева имеет порядковый номер z = 92.
n n Нуклидами называются атомы с определенным порядковым номером, массовым числом и ядром в основном или метастабильном состоянии. Среди множества нуклидов (а их в настоящее время известно более 2000 естественных и искусственных) есть такие, у которых одна из двух упомянутых характеристик одинакова, а другая – различна по величине. Нуклиды с одинаковым z (числом протонов) называют изотопами. Поскольку атомный номер определяет в соответствии с Периодическим Законом Д. И. Менделеева индивидуальность только химических свойств атома элемента, об изотопах всегда говорят со ссылкой на символ соответствующего им химического элемента в Периодической Системе. Например, 233 U, 234 U, 235 U, 236 U, 238 U, 239 U все это изотопы урана, который в Периодической Системе элементов Д. И. Менделеева имеет порядковый номер z = 92.
 n n n n Нуклиды равной массы (A), но с различными зарядами z называют изобарами. Изобары, в отличие от изотопов, нуклиды различных химических элементов. Примеры: и изобары нуклидов бора и углерода; и изобары нуклидов лития и бериллия; также являются изобарами йода, ксенона и цезия соответственно. Изотонами называются атомы химических элементов, имеющие одинаковое число нейтронов. Пример: Изомерами называются атомы с одинаковыми A и Z, но с разными энергетическими состояниями.
n n n n Нуклиды равной массы (A), но с различными зарядами z называют изобарами. Изобары, в отличие от изотопов, нуклиды различных химических элементов. Примеры: и изобары нуклидов бора и углерода; и изобары нуклидов лития и бериллия; также являются изобарами йода, ксенона и цезия соответственно. Изотонами называются атомы химических элементов, имеющие одинаковое число нейтронов. Пример: Изомерами называются атомы с одинаковыми A и Z, но с разными энергетическими состояниями.
 Задача n Какое количество энергии выделяется при полном окислении одного моля углерода, если теплота образования CO 2 составляет H=94, 05 ккал/моль?
Задача n Какое количество энергии выделяется при полном окислении одного моля углерода, если теплота образования CO 2 составляет H=94, 05 ккал/моль?
 Решение n Процесс окисления углерода можно представить следующей схемой: C + O 2 = CO 2 + Q. Из термохимии количество теплоты, выделяемое в химической реакции, есть разность между теплотами образования конечного и исходных продуктов. Так как теплоты образования углерода и кислорода равны нулю, то в рассматриваемой реакции образуется энергия в количестве 94, 05 ккал/моль. Зная, что в одном моле вещества содержится =6, 023 1023 (число Авогадро) частиц, имеем, что в одном элементарном акте окисления углерода выделится энергия в количестве:
Решение n Процесс окисления углерода можно представить следующей схемой: C + O 2 = CO 2 + Q. Из термохимии количество теплоты, выделяемое в химической реакции, есть разность между теплотами образования конечного и исходных продуктов. Так как теплоты образования углерода и кислорода равны нулю, то в рассматриваемой реакции образуется энергия в количестве 94, 05 ккал/моль. Зная, что в одном моле вещества содержится =6, 023 1023 (число Авогадро) частиц, имеем, что в одном элементарном акте окисления углерода выделится энергия в количестве:
 n Какая энергия выделится при полном делении 1 г
n Какая энергия выделится при полном делении 1 г
 n В 1 г содержится следующее количество ядер : n Зная, что в одном акте деления выделяется энергия в количестве Qf≈200 Мэ. В, получим, что при делении 1 г 235 U выделяется энергия:
n В 1 г содержится следующее количество ядер : n Зная, что в одном акте деления выделяется энергия в количестве Qf≈200 Мэ. В, получим, что при делении 1 г 235 U выделяется энергия:
 n Оценить радиус ядра
n Оценить радиус ядра
 n Радиус ядра можно оценить по эмпирическому соотношению вида: n Тогда для ядра 16 О имеем:
n Радиус ядра можно оценить по эмпирическому соотношению вида: n Тогда для ядра 16 О имеем:
 n Найти концентрацию молекул UO 2 и концентрации входящих в нее атомов, полагая, что уран имеет природный изотопный состав.
n Найти концентрацию молекул UO 2 и концентрации входящих в нее атомов, полагая, что уран имеет природный изотопный состав.
 n определим концентрацию молекул UO 2: n Тогда концентрация атомов кислорода будет равна n n а концентрация атомов урана составит n По условию задачи уран имеет природный изотопный состав: содержание 238 U— P 8 = 0, 99284; 235 U— P 5 = 0, 0071; 234 U — P 4= 6 10– 5. Следовательно концентрации изотопов урана составит для: n n
n определим концентрацию молекул UO 2: n Тогда концентрация атомов кислорода будет равна n n а концентрация атомов урана составит n По условию задачи уран имеет природный изотопный состав: содержание 238 U— P 8 = 0, 99284; 235 U— P 5 = 0, 0071; 234 U — P 4= 6 10– 5. Следовательно концентрации изотопов урана составит для: n n
 n Определить концентрацию ядер водорода и кислорода в воде.
n Определить концентрацию ядер водорода и кислорода в воде.
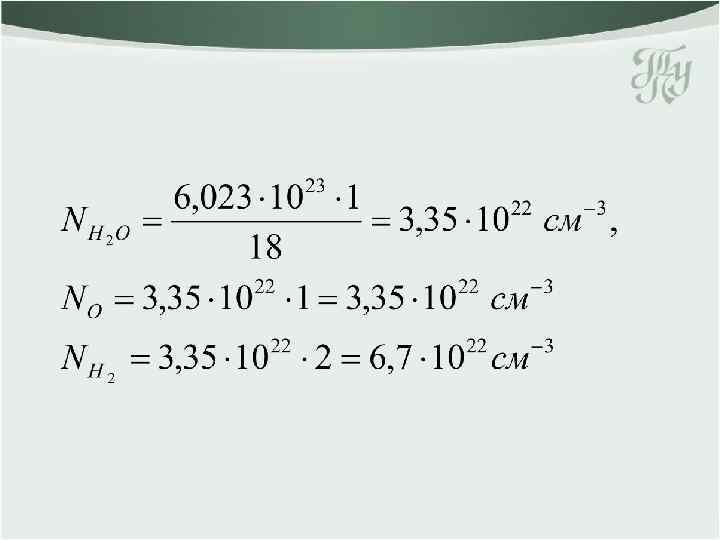
 n Вычислить концентрацию атомов U 235 U 238 в обогащенном уране (20%).
n Вычислить концентрацию атомов U 235 U 238 в обогащенном уране (20%).
 Т. к. обогащение 20% то необходимо N 235=4, 79· 1022· 0, 2=9, 58· 1021 см 3 N 238=4, 73· 1022· 0, 8=3, 78· 1022 см 3
Т. к. обогащение 20% то необходимо N 235=4, 79· 1022· 0, 2=9, 58· 1021 см 3 N 238=4, 73· 1022· 0, 8=3, 78· 1022 см 3
 Домашняя работа Найти концентрацию молекул и атомов в следующих элементах и соединениях
Домашняя работа Найти концентрацию молекул и атомов в следующих элементах и соединениях


