01 Введение в ЯФ. Свойства ядер.ppt
- Количество слайдов: 29
 Ядерная физика Основные разделы курса: • Характеристики атомного ядра • Энергия связи и устойчивость ядер • Модели атомного ядра • Спин и момент ядер • Ядерные силы • Структура ядра • Ядерные реакции • Радиоактивность
Ядерная физика Основные разделы курса: • Характеристики атомного ядра • Энергия связи и устойчивость ядер • Модели атомного ядра • Спин и момент ядер • Ядерные силы • Структура ядра • Ядерные реакции • Радиоактивность
 Список литературы Рекомендуемая литература: • Типлер П. А. , Ллуэллин Р. А. Современная физика. Т 2. М. : Мир, 2007 • Бейзер А. Основные представления современной физики. М. : Атомиздат, 1973 • Сивухин Д. В. Т 5. Атомная и ядерная физика. М. : Физматлит, 2002 Дополнительная литература: • Абрамов А. И. История ядерной физики. УРСС, 2006. • Ахиезер А. И. Биография элементарных частиц. Киев, 1979. • Хэлперн П. Коллайдер. М. : ЭКСМО, 2010.
Список литературы Рекомендуемая литература: • Типлер П. А. , Ллуэллин Р. А. Современная физика. Т 2. М. : Мир, 2007 • Бейзер А. Основные представления современной физики. М. : Атомиздат, 1973 • Сивухин Д. В. Т 5. Атомная и ядерная физика. М. : Физматлит, 2002 Дополнительная литература: • Абрамов А. И. История ядерной физики. УРСС, 2006. • Ахиезер А. И. Биография элементарных частиц. Киев, 1979. • Хэлперн П. Коллайдер. М. : ЭКСМО, 2010.
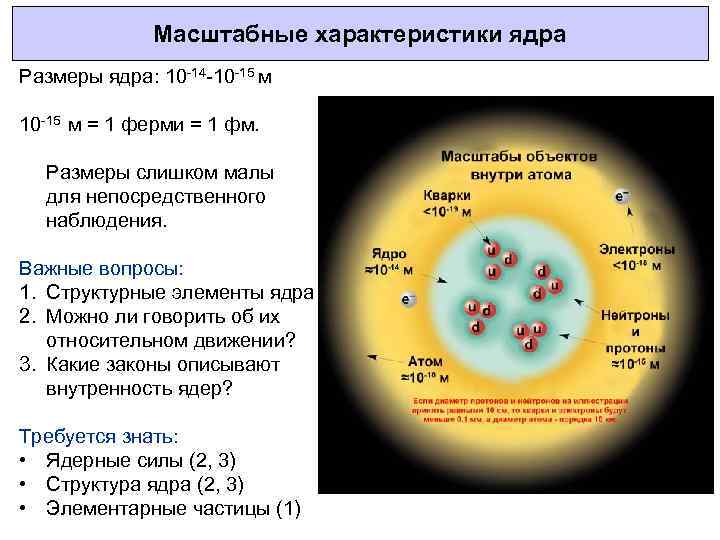 Масштабные характеристики ядра Размеры ядра: 10 -14 -10 -15 м = 1 ферми = 1 фм. Размеры слишком малы для непосредственного наблюдения. Важные вопросы: 1. Структурные элементы ядра 2. Можно ли говорить об их относительном движении? 3. Какие законы описывают внутренность ядер? Требуется знать: • Ядерные силы (2, 3) • Структура ядра (2, 3) • Элементарные частицы (1) 3
Масштабные характеристики ядра Размеры ядра: 10 -14 -10 -15 м = 1 ферми = 1 фм. Размеры слишком малы для непосредственного наблюдения. Важные вопросы: 1. Структурные элементы ядра 2. Можно ли говорить об их относительном движении? 3. Какие законы описывают внутренность ядер? Требуется знать: • Ядерные силы (2, 3) • Структура ядра (2, 3) • Элементарные частицы (1) 3
 Предпосылки ядерной физики – открытие радиоактивности 1895 г. – открытие рентгентовских лучей 1896 г. – Антуан Анри Беккерель при изучении флуоресценции уранила калия открыл радиоактивность. Нобелевская премия по физике в 1903 г. вместе с Марией и Пьером Кюри. 1903 г. – Нобелевская премия по физике за открытие радиоактивности (Беккерель, Мария и Пьер Кюри). 4
Предпосылки ядерной физики – открытие радиоактивности 1895 г. – открытие рентгентовских лучей 1896 г. – Антуан Анри Беккерель при изучении флуоресценции уранила калия открыл радиоактивность. Нобелевская премия по физике в 1903 г. вместе с Марией и Пьером Кюри. 1903 г. – Нобелевская премия по физике за открытие радиоактивности (Беккерель, Мария и Пьер Кюри). 4
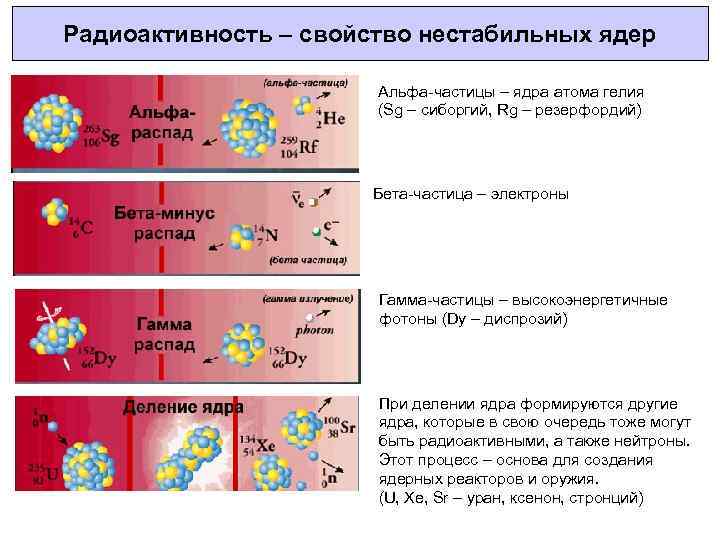 Радиоактивность – свойство нестабильных ядер Альфа-частицы – ядра атома гелия (Sg – сиборгий, Rg – резерфордий) Бета-частица – электроны Гамма-частицы – высокоэнергетичные фотоны (Dy – диспрозий) При делении ядра формируются другие ядра, которые в свою очередь тоже могут быть радиоактивными, а также нейтроны. Этот процесс – основа для создания ядерных реакторов и оружия. (U, Xe, Sr – уран, ксенон, стронций)
Радиоактивность – свойство нестабильных ядер Альфа-частицы – ядра атома гелия (Sg – сиборгий, Rg – резерфордий) Бета-частица – электроны Гамма-частицы – высокоэнергетичные фотоны (Dy – диспрозий) При делении ядра формируются другие ядра, которые в свою очередь тоже могут быть радиоактивными, а также нейтроны. Этот процесс – основа для создания ядерных реакторов и оружия. (U, Xe, Sr – уран, ксенон, стронций)
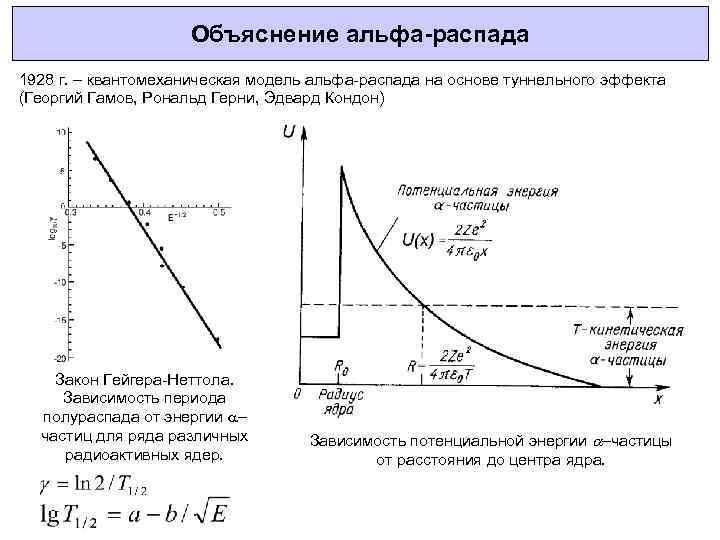 Объяснение альфа-распада 1928 г. – квантомеханическая модель альфа-распада на основе туннельного эффекта (Георгий Гамов, Рональд Герни, Эдвард Кондон) Закон Гейгера-Неттола. Зависимость периода полураспада от энергии – частиц для ряда различных радиоактивных ядер. Зависимость потенциальной энергии –частицы от расстояния до центра ядра.
Объяснение альфа-распада 1928 г. – квантомеханическая модель альфа-распада на основе туннельного эффекта (Георгий Гамов, Рональд Герни, Эдвард Кондон) Закон Гейгера-Неттола. Зависимость периода полураспада от энергии – частиц для ряда различных радиоактивных ядер. Зависимость потенциальной энергии –частицы от расстояния до центра ядра.
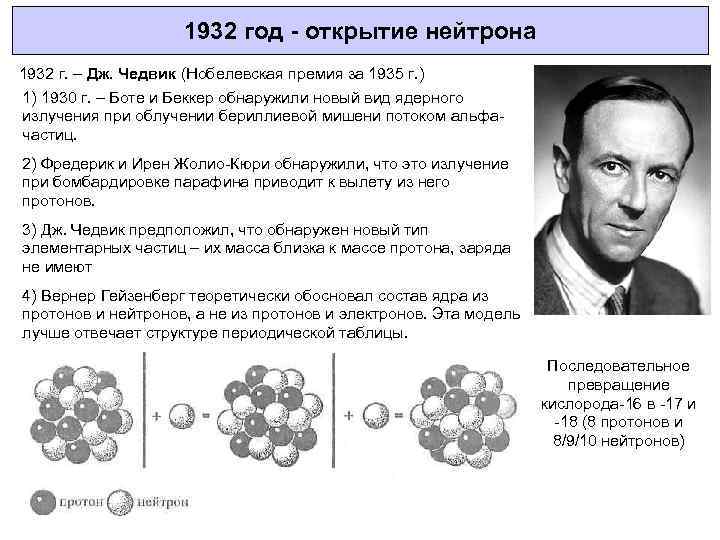 1932 год - открытие нейтрона 1932 г. – Дж. Чедвик (Нобелевская премия за 1935 г. ) 1) 1930 г. – Боте и Беккер обнаружили новый вид ядерного излучения при облучении бериллиевой мишени потоком альфачастиц. 2) Фредерик и Ирен Жолио-Кюри обнаружили, что это излучение при бомбардировке парафина приводит к вылету из него протонов. 3) Дж. Чедвик предположил, что обнаружен новый тип элементарных частиц – их масса близка к массе протона, заряда не имеют 4) Вернер Гейзенберг теоретически обосновал состав ядра из протонов и нейтронов, а не из протонов и электронов. Эта модель лучше отвечает структуре периодической таблицы. Последовательное превращение кислорода-16 в -17 и -18 (8 протонов и 8/9/10 нейтронов)
1932 год - открытие нейтрона 1932 г. – Дж. Чедвик (Нобелевская премия за 1935 г. ) 1) 1930 г. – Боте и Беккер обнаружили новый вид ядерного излучения при облучении бериллиевой мишени потоком альфачастиц. 2) Фредерик и Ирен Жолио-Кюри обнаружили, что это излучение при бомбардировке парафина приводит к вылету из него протонов. 3) Дж. Чедвик предположил, что обнаружен новый тип элементарных частиц – их масса близка к массе протона, заряда не имеют 4) Вернер Гейзенберг теоретически обосновал состав ядра из протонов и нейтронов, а не из протонов и электронов. Эта модель лучше отвечает структуре периодической таблицы. Последовательное превращение кислорода-16 в -17 и -18 (8 протонов и 8/9/10 нейтронов)
 1932 год - открытие позитрона 1932 г. – Карл Андерсон (Нобелевская премия за 1936 г. ) При изучении космических лучей обнаружил необычные следы в камере Вильсона при изучении. Объяснил их как следы частицы с массой электрона, но положительным зарядом. Подтвердил теоретические предсказания о существовании позитрона Поля Дирака. Трек позитрона в камере Вильсона в магнитном поле. Тонкая изогнутая прерывистая линия, идущая снизу вверх – трек позитрона. Темная полоса, пересекающая трек – слой вещества, в нем позитрон теряет часть энергии и при выходе двигается с меньшей скоростью (трек искривлён сильнее).
1932 год - открытие позитрона 1932 г. – Карл Андерсон (Нобелевская премия за 1936 г. ) При изучении космических лучей обнаружил необычные следы в камере Вильсона при изучении. Объяснил их как следы частицы с массой электрона, но положительным зарядом. Подтвердил теоретические предсказания о существовании позитрона Поля Дирака. Трек позитрона в камере Вильсона в магнитном поле. Тонкая изогнутая прерывистая линия, идущая снизу вверх – трек позитрона. Темная полоса, пересекающая трек – слой вещества, в нем позитрон теряет часть энергии и при выходе двигается с меньшей скоростью (трек искривлён сильнее).
 1932 год – первая ядерная реакция с использованием ускорителя 1932 г. – Джон Кокрофт и Эрнст Уолтон Умножитель преобразует переменное напряжение в высокое постоянное напряжение с использованием конденсаторов и диодов. Разрушили ядро Li посредством бомбардировки ускоренными протонами и исследовали продукты реакции (гелий). Умножитель напряжения Кокрофта-Уолтона Нобелевская премия 1951 г. – «За работы по трансмутации атомных ядер с помощью искусственно ускоренных частиц»
1932 год – первая ядерная реакция с использованием ускорителя 1932 г. – Джон Кокрофт и Эрнст Уолтон Умножитель преобразует переменное напряжение в высокое постоянное напряжение с использованием конденсаторов и диодов. Разрушили ядро Li посредством бомбардировки ускоренными протонами и исследовали продукты реакции (гелий). Умножитель напряжения Кокрофта-Уолтона Нобелевская премия 1951 г. – «За работы по трансмутации атомных ядер с помощью искусственно ускоренных частиц»
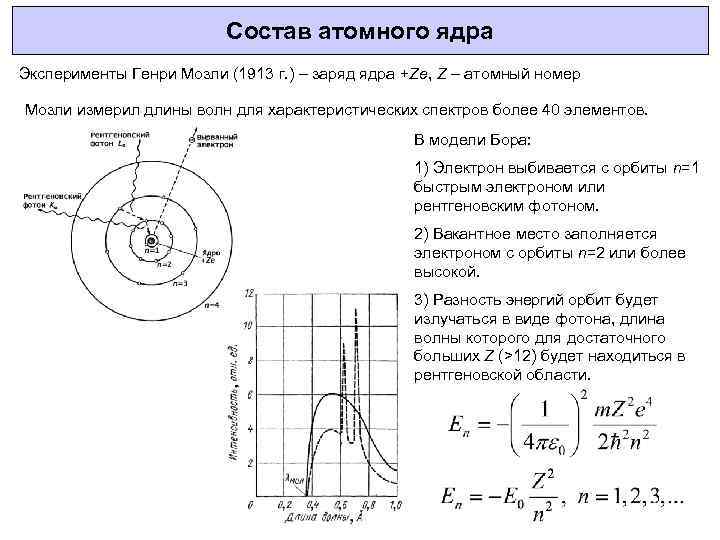 Состав атомного ядра Эксперименты Генри Мозли (1913 г. ) – заряд ядра +Ze, Z – атомный номер Мозли измерил длины волн для характеристических спектров более 40 элементов. В модели Бора: 1) Электрон выбивается с орбиты n=1 быстрым электроном или рентгеновским фотоном. 2) Вакантное место заполняется электроном с орбиты n=2 или более высокой. 3) Разность энергий орбит будет излучаться в виде фотона, длина волны которого для достаточного больших Z (>12) будет находиться в рентгеновской области.
Состав атомного ядра Эксперименты Генри Мозли (1913 г. ) – заряд ядра +Ze, Z – атомный номер Мозли измерил длины волн для характеристических спектров более 40 элементов. В модели Бора: 1) Электрон выбивается с орбиты n=1 быстрым электроном или рентгеновским фотоном. 2) Вакантное место заполняется электроном с орбиты n=2 или более высокой. 3) Разность энергий орбит будет излучаться в виде фотона, длина волны которого для достаточного больших Z (>12) будет находиться в рентгеновской области.
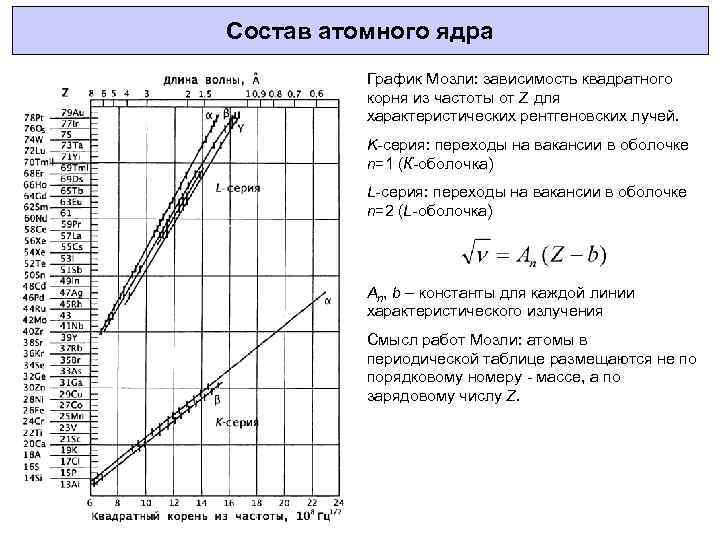 Состав атомного ядра График Мозли: зависимость квадратного корня из частоты от Z для характеристических рентгеновских лучей. K-серия: переходы на вакансии в оболочке n=1 (К-оболочка) L-серия: переходы на вакансии в оболочке n=2 (L-оболочка) An, b – константы для каждой линии характеристического излучения Смысл работ Мозли: атомы в периодической таблице размещаются не по порядковому номеру - массе, а по зарядовому числу Z.
Состав атомного ядра График Мозли: зависимость квадратного корня из частоты от Z для характеристических рентгеновских лучей. K-серия: переходы на вакансии в оболочке n=1 (К-оболочка) L-серия: переходы на вакансии в оболочке n=2 (L-оболочка) An, b – константы для каждой линии характеристического излучения Смысл работ Мозли: атомы в периодической таблице размещаются не по порядковому номеру - массе, а по зарядовому числу Z.
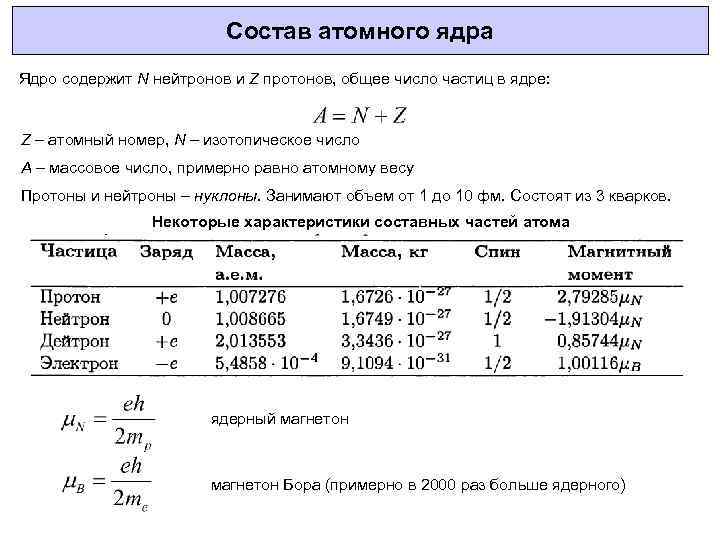 Состав атомного ядра Ядро содержит N нейтронов и Z протонов, общее число частиц в ядре: Z – атомный номер, N – изотопическое число A – массовое число, примерно равно атомному весу Протоны и нейтроны – нуклоны. Занимают объем от 1 до 10 фм. Состоят из 3 кварков. Некоторые характеристики составных частей атома ядерный магнетон Бора (примерно в 2000 раз больше ядерного)
Состав атомного ядра Ядро содержит N нейтронов и Z протонов, общее число частиц в ядре: Z – атомный номер, N – изотопическое число A – массовое число, примерно равно атомному весу Протоны и нейтроны – нуклоны. Занимают объем от 1 до 10 фм. Состоят из 3 кварков. Некоторые характеристики составных частей атома ядерный магнетон Бора (примерно в 2000 раз больше ядерного)
 Состав атомного ядра Химическое обозначение: Изотопы: одинаковое Z Изотоны: одинаковое N Изобары: одинаковое A
Состав атомного ядра Химическое обозначение: Изотопы: одинаковое Z Изотоны: одинаковое N Изобары: одинаковое A
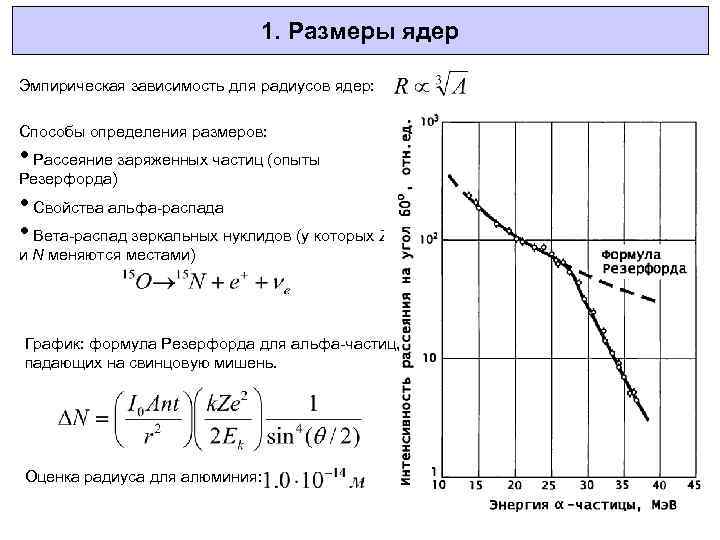 1. Размеры ядер Эмпирическая зависимость для радиусов ядер: Способы определения размеров: • Рассеяние заряженных частиц (опыты Резерфорда) • Свойства альфа-распада • Вета-распад зеркальных нуклидов (у которых Z и N меняются местами) График: формула Резерфорда для альфа-частиц, падающих на свинцовую мишень. Оценка радиуса для алюминия:
1. Размеры ядер Эмпирическая зависимость для радиусов ядер: Способы определения размеров: • Рассеяние заряженных частиц (опыты Резерфорда) • Свойства альфа-распада • Вета-распад зеркальных нуклидов (у которых Z и N меняются местами) График: формула Резерфорда для альфа-частиц, падающих на свинцовую мишень. Оценка радиуса для алюминия:
 1. Размеры ядер Уточнение выражения для радиуса ядер: Радиусы ядер 4 He и 238 U:
1. Размеры ядер Уточнение выражения для радиуса ядер: Радиусы ядер 4 He и 238 U:
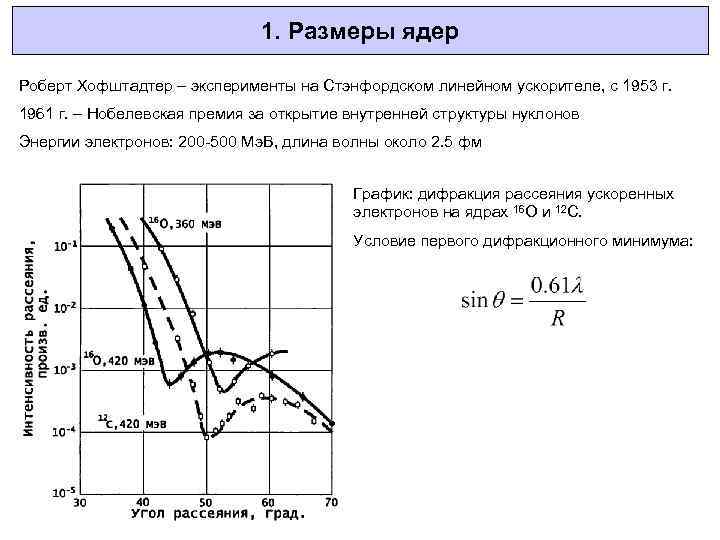 1. Размеры ядер Роберт Хофштадтер – эксперименты на Стэнфордском линейном ускорителе, с 1953 г. 1961 г. – Нобелевская премия за открытие внутренней структуры нуклонов Энергии электронов: 200 -500 Мэ. В, длина волны около 2. 5 фм График: дифракция рассеяния ускоренных электронов на ядрах 16 O и 12 C. Условие первого дифракционного минимума:
1. Размеры ядер Роберт Хофштадтер – эксперименты на Стэнфордском линейном ускорителе, с 1953 г. 1961 г. – Нобелевская премия за открытие внутренней структуры нуклонов Энергии электронов: 200 -500 Мэ. В, длина волны около 2. 5 фм График: дифракция рассеяния ускоренных электронов на ядрах 16 O и 12 C. Условие первого дифракционного минимума:
 1. Размеры ядер - пример Вычислить радиус ядра 16 O, используя данные, полученные при рассеянии на них электронов с энергией 420 Мэ. В. Формула для вычисления радиуса по дифракционной картине: Местоположение первого минимума: Дебройлевская длина волны электрона: Импульс электрона с энергией 420 Мэ. В: Длина волны электрона: Оценка радиуса ядра:
1. Размеры ядер - пример Вычислить радиус ядра 16 O, используя данные, полученные при рассеянии на них электронов с энергией 420 Мэ. В. Формула для вычисления радиуса по дифракционной картине: Местоположение первого минимума: Дебройлевская длина волны электрона: Импульс электрона с энергией 420 Мэ. В: Длина волны электрона: Оценка радиуса ядра:
 2. Плотность ядер Разные методы измерения размеров ядер дают похожие, но не одинаковые результаты. Может измеряться или радиус ядерного взаимодействия (рассеяние нейтронов), или распределение заряда в ядре (рассеяние электронов). - все ядра имеют примерно одинаковую плотность Капельная модель ядра: аналогия с жидкостью – ядра рассматриваются как шарообразные капли несжимаемой ядерной жидкости. Капельная модель: • • Позволяет вычислять массы ядер Объясняет ряд свойств ядер, в т. ч. деление тяжелых ядер Плотность ядра: 1017 кг/м 3 (V=1 мм 3 – m=200000 т) Плотность атома: 103 кг/м 3
2. Плотность ядер Разные методы измерения размеров ядер дают похожие, но не одинаковые результаты. Может измеряться или радиус ядерного взаимодействия (рассеяние нейтронов), или распределение заряда в ядре (рассеяние электронов). - все ядра имеют примерно одинаковую плотность Капельная модель ядра: аналогия с жидкостью – ядра рассматриваются как шарообразные капли несжимаемой ядерной жидкости. Капельная модель: • • Позволяет вычислять массы ядер Объясняет ряд свойств ядер, в т. ч. деление тяжелых ядер Плотность ядра: 1017 кг/м 3 (V=1 мм 3 – m=200000 т) Плотность атома: 103 кг/м 3
 2. Плотность ядер – пример Радиус нейтронной звезды. При возникновении сверхновой оболочка звезды взрывается и остается ядро, содержащее только нейтроны – нейтронная звезда. Ее плотность примерно равна плотности ядер. Вычислить радиус звезды с массой, равной массе Солнца 1. 99· 10 30 кг. Масса нейтронной звезды с ядерной плотностью 1017 кг/м 3 :
2. Плотность ядер – пример Радиус нейтронной звезды. При возникновении сверхновой оболочка звезды взрывается и остается ядро, содержащее только нейтроны – нейтронная звезда. Ее плотность примерно равна плотности ядер. Вычислить радиус звезды с массой, равной массе Солнца 1. 99· 10 30 кг. Масса нейтронной звезды с ядерной плотностью 1017 кг/м 3 :
 2. Плотность ядер – нейтронная звезда Схема образования миллисекундного пульсара: 1) Имеется тесная пара звезд, состоящая из сверхгиганта и солнцеподобной звезды 2) Массивная звезда быстро эволюционирует, взрывается как сверхновая и образует пульсар 3) Спустя миллиарды лет вторая звезда становится красным гигантом, и ее вещество начинает перетекать на нейтронную звезду 4) Скорость вращения нейтронной звезды увеличивается, ее излучение разогревает и развеивает в пространстве внешние слои звезды-гиганта
2. Плотность ядер – нейтронная звезда Схема образования миллисекундного пульсара: 1) Имеется тесная пара звезд, состоящая из сверхгиганта и солнцеподобной звезды 2) Массивная звезда быстро эволюционирует, взрывается как сверхновая и образует пульсар 3) Спустя миллиарды лет вторая звезда становится красным гигантом, и ее вещество начинает перетекать на нейтронную звезду 4) Скорость вращения нейтронной звезды увеличивается, ее излучение разогревает и развеивает в пространстве внешние слои звезды-гиганта
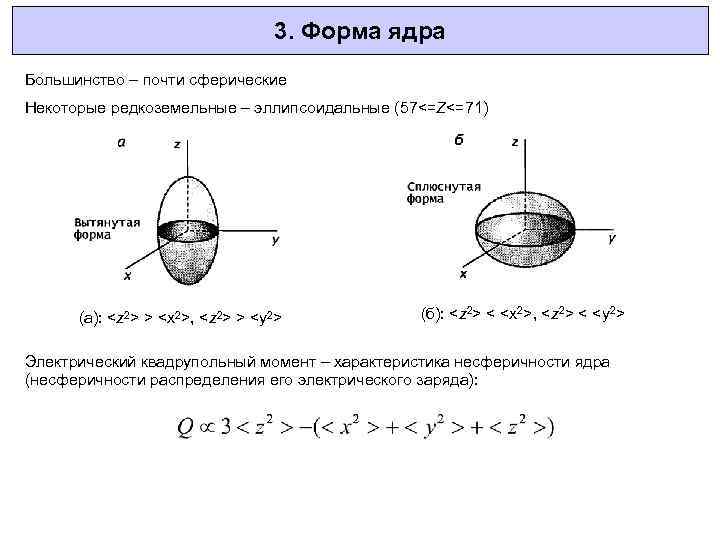 3. Форма ядра Большинство – почти сферические Некоторые редкоземельные – эллипсоидальные (57<=Z<=71) (a):
3. Форма ядра Большинство – почти сферические Некоторые редкоземельные – эллипсоидальные (57<=Z<=71) (a):
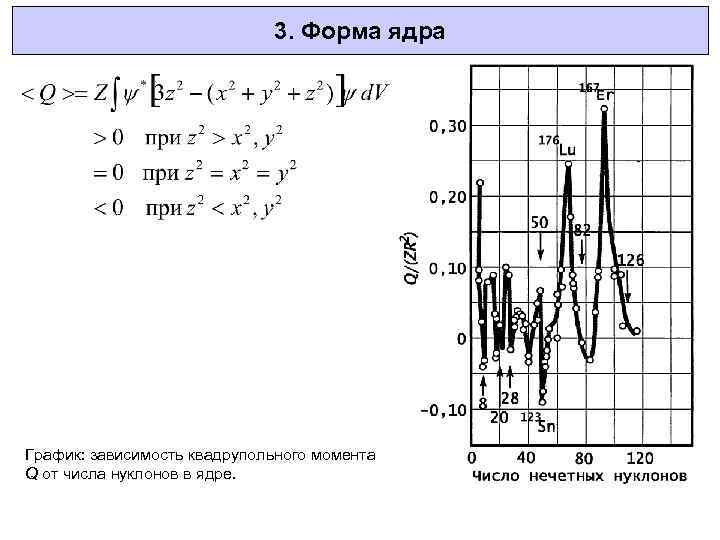 3. Форма ядра График: зависимость квадрупольного момента Q от числа нуклонов в ядре.
3. Форма ядра График: зависимость квадрупольного момента Q от числа нуклонов в ядре.
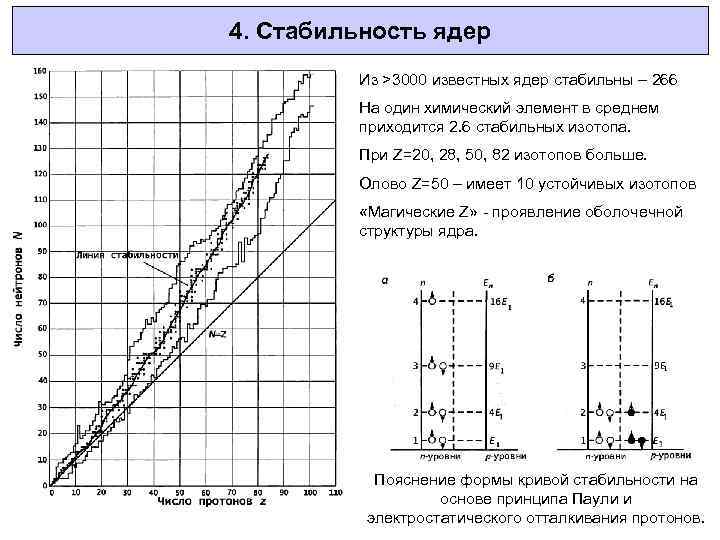 4. Стабильность ядер Из >3000 известных ядер стабильны – 266 На один химический элемент в среднем приходится 2. 6 стабильных изотопа. При Z=20, 28, 50, 82 изотопов больше. Олово Z=50 – имеет 10 устойчивых изотопов «Магические Z» - проявление оболочечной структуры ядра. Пояснение формы кривой стабильности на основе принципа Паули и электростатического отталкивания протонов.
4. Стабильность ядер Из >3000 известных ядер стабильны – 266 На один химический элемент в среднем приходится 2. 6 стабильных изотопа. При Z=20, 28, 50, 82 изотопов больше. Олово Z=50 – имеет 10 устойчивых изотопов «Магические Z» - проявление оболочечной структуры ядра. Пояснение формы кривой стабильности на основе принципа Паули и электростатического отталкивания протонов.
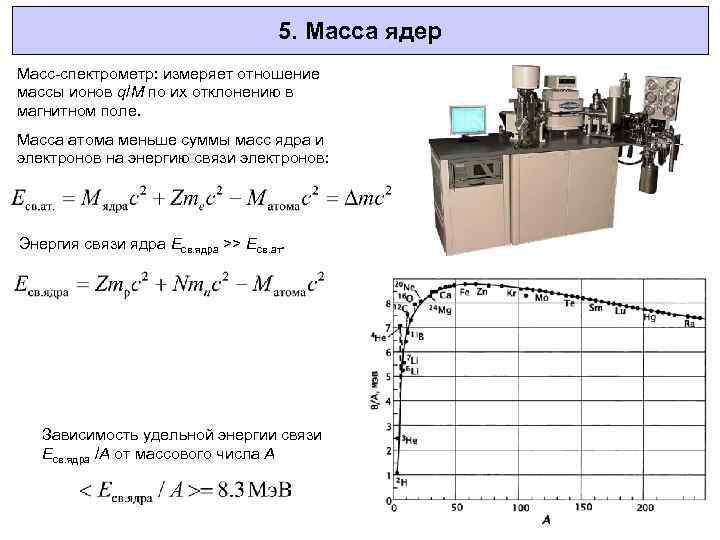 5. Масса ядер Масс-спектрометр: измеряет отношение массы ионов q/M по их отклонению в магнитном поле. Масса атома меньше суммы масс ядра и электронов на энергию связи электронов: Энергия связи ядра Eсв. ядра >> Есв. ат. Зависимость удельной энергии связи Eсв. ядра /A от массового числа A
5. Масса ядер Масс-спектрометр: измеряет отношение массы ионов q/M по их отклонению в магнитном поле. Масса атома меньше суммы масс ядра и электронов на энергию связи электронов: Энергия связи ядра Eсв. ядра >> Есв. ат. Зависимость удельной энергии связи Eсв. ядра /A от массового числа A
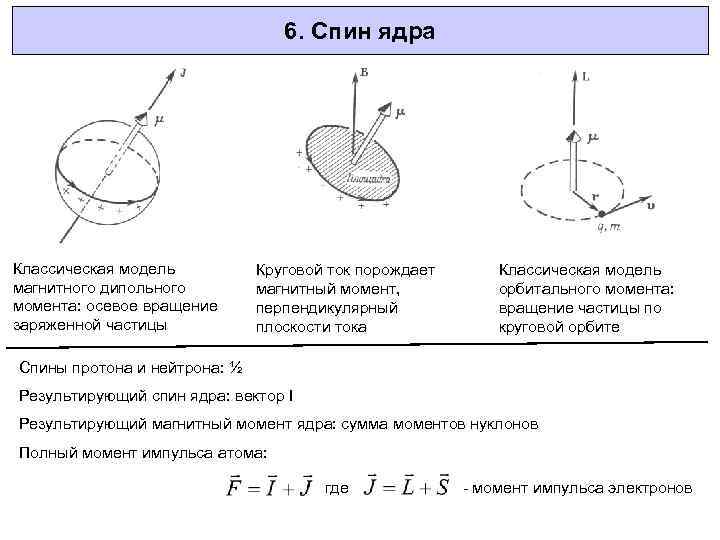 6. Спин ядра Классическая модель магнитного дипольного момента: осевое вращение заряженной частицы Круговой ток порождает магнитный момент, перпендикулярный плоскости тока Классическая модель орбитального момента: вращение частицы по круговой орбите Спины протона и нейтрона: ½ Результирующий спин ядра: вектор I Результирующий магнитный момент ядра: сумма моментов нуклонов Полный момент импульса атома: где - момент импульса электронов
6. Спин ядра Классическая модель магнитного дипольного момента: осевое вращение заряженной частицы Круговой ток порождает магнитный момент, перпендикулярный плоскости тока Классическая модель орбитального момента: вращение частицы по круговой орбите Спины протона и нейтрона: ½ Результирующий спин ядра: вектор I Результирующий магнитный момент ядра: сумма моментов нуклонов Полный момент импульса атома: где - момент импульса электронов
 6. Спин ядра Полный момент импульса ядра может принимать следующие значения: F = (I+J), (I+J-1), …, |I-J| Правило отбора: Число возможных значений F: Результат – каждая спектральная линия атома расщепляется на NF компонент – сверхтонкая структура спектральных линий. Величина расщепления (примерно в 2000 раз меньше тонкого расщепления): g. N – фактор (множитель) Ланде, обычно от 1 до 5 m. I – магнитное квантовое число (Iz), max(|m. I |)=I – ядерный магнетон Be – магнитное поле в области ядра, создаваемое электронами – магнитный момент ядра
6. Спин ядра Полный момент импульса ядра может принимать следующие значения: F = (I+J), (I+J-1), …, |I-J| Правило отбора: Число возможных значений F: Результат – каждая спектральная линия атома расщепляется на NF компонент – сверхтонкая структура спектральных линий. Величина расщепления (примерно в 2000 раз меньше тонкого расщепления): g. N – фактор (множитель) Ланде, обычно от 1 до 5 m. I – магнитное квантовое число (Iz), max(|m. I |)=I – ядерный магнетон Be – магнитное поле в области ядра, создаваемое электронами – магнитный момент ядра
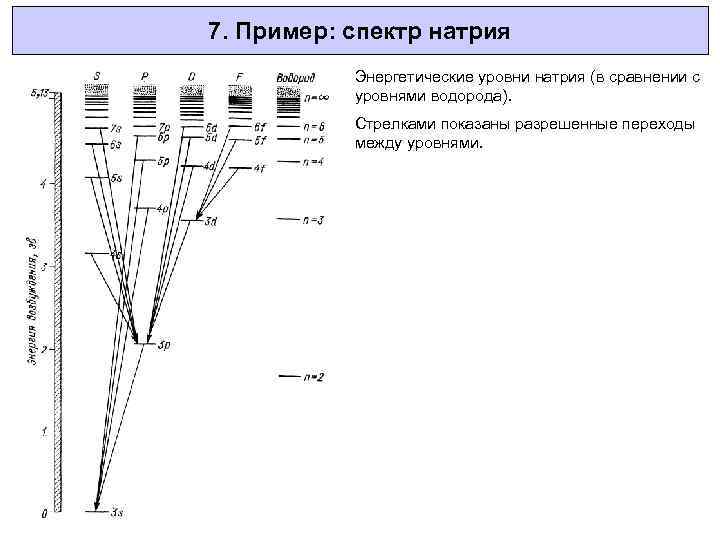 7. Пример: спектр натрия Энергетические уровни натрия (в сравнении с уровнями водорода). Стрелками показаны разрешенные переходы между уровнями.
7. Пример: спектр натрия Энергетические уровни натрия (в сравнении с уровнями водорода). Стрелками показаны разрешенные переходы между уровнями.
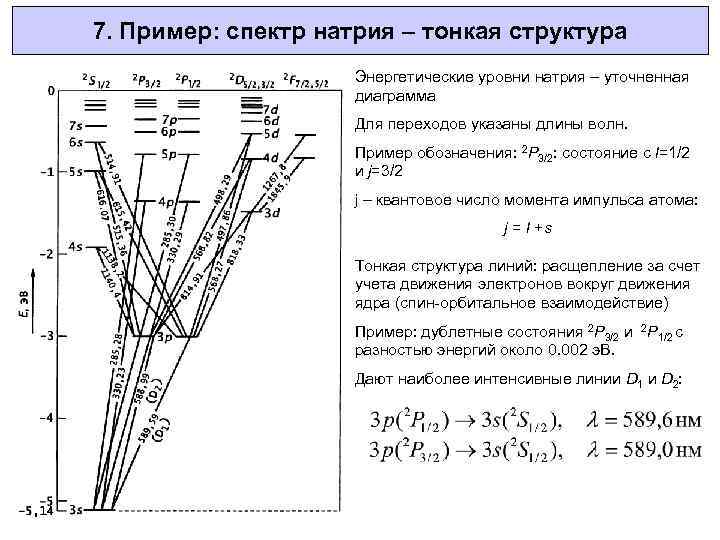 7. Пример: спектр натрия – тонкая структура Энергетические уровни натрия – уточненная диаграмма Для переходов указаны длины волн. Пример обозначения: 2 P 3/2: состояние с l=1/2 и j=3/2 j – квантовое число момента импульса атома: j = l +s Тонкая структура линий: расщепление за счет учета движения электронов вокруг движения ядра (спин-орбитальное взаимодействие) Пример: дублетные состояния 2 P 3/2 и 2 P 1/2 c разностью энергий около 0. 002 э. В. Дают наиболее интенсивные линии D 1 и D 2:
7. Пример: спектр натрия – тонкая структура Энергетические уровни натрия – уточненная диаграмма Для переходов указаны длины волн. Пример обозначения: 2 P 3/2: состояние с l=1/2 и j=3/2 j – квантовое число момента импульса атома: j = l +s Тонкая структура линий: расщепление за счет учета движения электронов вокруг движения ядра (спин-орбитальное взаимодействие) Пример: дублетные состояния 2 P 3/2 и 2 P 1/2 c разностью энергий около 0. 002 э. В. Дают наиболее интенсивные линии D 1 и D 2:
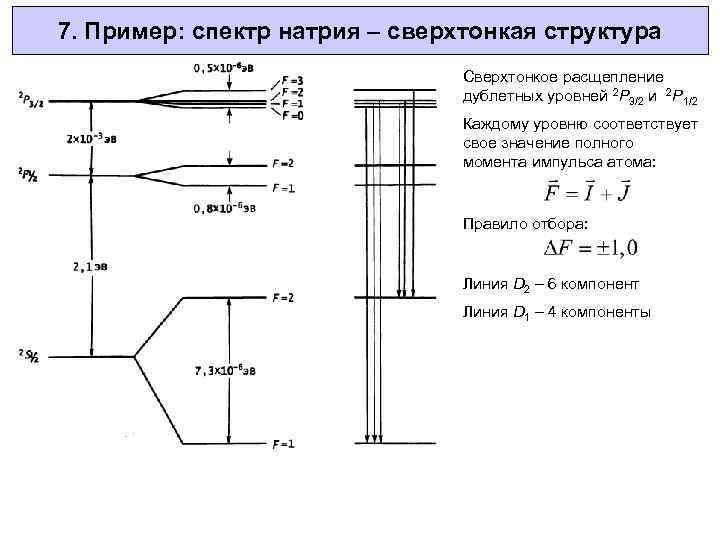 7. Пример: спектр натрия – сверхтонкая структура Сверхтонкое расщепление дублетных уровней 2 P 3/2 и 2 P 1/2 Каждому уровню соответствует свое значение полного момента импульса атома: Правило отбора: Линия D 2 – 6 компонент Линия D 1 – 4 компоненты
7. Пример: спектр натрия – сверхтонкая структура Сверхтонкое расщепление дублетных уровней 2 P 3/2 и 2 P 1/2 Каждому уровню соответствует свое значение полного момента импульса атома: Правило отбора: Линия D 2 – 6 компонент Линия D 1 – 4 компоненты


