 Я НИ НЕ И Е НЫ Д О ОР СЛ А 3 КИ ОТИ Я 2 АЗЕ К Ц Л С ЕД О
Я НИ НЕ И Е НЫ Д О ОР СЛ А 3 КИ ОТИ Я 2 АЗЕ К Ц Л С ЕД О
 ПОЛУЧЕНИЕ NO Действие восстановителей на нитриты в кислой среде: Na. NO 2 + Fe. Cl 2 + 2 HCl → Fe. Cl 3 + NO + Na. Cl + H 2 O
ПОЛУЧЕНИЕ NO Действие восстановителей на нитриты в кислой среде: Na. NO 2 + Fe. Cl 2 + 2 HCl → Fe. Cl 3 + NO + Na. Cl + H 2 O
 ХИМИЧЕСКИЕ СВОЙСТВА NO o Окислительные свойства: 10 NO + P 4 → P 4 O 10 + 5 N 2 (при нагревании) o Восстановительные свойства: 2 NO + K 2 Cr 2 O 7 +4 H 2 SO 4 → 2 HNO 3 + Cr 2(SO 4)3 + K 2 SO 4 + 3 H 2 O o Комплексообразование: [Fe(H 2 O)6]SO 4 + NO ↔ [Fe(H 2 O)5 NO]SO 4 + H 2 O
ХИМИЧЕСКИЕ СВОЙСТВА NO o Окислительные свойства: 10 NO + P 4 → P 4 O 10 + 5 N 2 (при нагревании) o Восстановительные свойства: 2 NO + K 2 Cr 2 O 7 +4 H 2 SO 4 → 2 HNO 3 + Cr 2(SO 4)3 + K 2 SO 4 + 3 H 2 O o Комплексообразование: [Fe(H 2 O)6]SO 4 + NO ↔ [Fe(H 2 O)5 NO]SO 4 + H 2 O
 ПОЛУЧЕНИЕ NO 2 o Термическое разложение нитратов тяжелых металлов: 2 Pb(NO 3)2 → 2 Pb. O + 4 NO 2 + O 2 (при нагревании) o Действие сильных кислот на нитриты: 2 Na. NO 2 + H 2 SO 4 → Na 2 SO 4 + NO 2 + H 2 O 2 NO + O 2 → 2 NO 2
ПОЛУЧЕНИЕ NO 2 o Термическое разложение нитратов тяжелых металлов: 2 Pb(NO 3)2 → 2 Pb. O + 4 NO 2 + O 2 (при нагревании) o Действие сильных кислот на нитриты: 2 Na. NO 2 + H 2 SO 4 → Na 2 SO 4 + NO 2 + H 2 O 2 NO + O 2 → 2 NO 2
 ХИМИЧЕСКИЕ СВОЙСТВА NO 2 o Разлагается при нагревании: 2 NO 2 → 2 NO + O 2 (t > 500 °C) o Проявляет окислительные свойства: 2 NO 2 + 2 S → 2 SO 2 + N 2 (при нагревании) o Проявляет восстановительные свойства: 2 NO 2 + F 2 + 2 H 2 O → 2 HNO 3 + 2 HF
ХИМИЧЕСКИЕ СВОЙСТВА NO 2 o Разлагается при нагревании: 2 NO 2 → 2 NO + O 2 (t > 500 °C) o Проявляет окислительные свойства: 2 NO 2 + 2 S → 2 SO 2 + N 2 (при нагревании) o Проявляет восстановительные свойства: 2 NO 2 + F 2 + 2 H 2 O → 2 HNO 3 + 2 HF
 ПОЛУЧЕНИЕ АЗОТИСТОЙ КИСЛОТЫ 1) Действие сильных кислот на нитриты: 2 Na. NO 2 + H 2 SO 4 → Na 2 SO 4 + 2 HNO 2 2) Из оксидов: NO + NO 2 +H 2 O ↔ 2 HNO 2
ПОЛУЧЕНИЕ АЗОТИСТОЙ КИСЛОТЫ 1) Действие сильных кислот на нитриты: 2 Na. NO 2 + H 2 SO 4 → Na 2 SO 4 + 2 HNO 2 2) Из оксидов: NO + NO 2 +H 2 O ↔ 2 HNO 2
 ПОЛУЧЕНИЕ НИТРИТОВ 1) Действие N 2 O 3 на гидроксиды: NO + NO 2 +2 Na. OH → 2 Na. NO 2 + H 2 O 2) Восстановление нитратов: Na. NO 3 + Pb → Pb. O + Na. NO 2 (сплавление)
ПОЛУЧЕНИЕ НИТРИТОВ 1) Действие N 2 O 3 на гидроксиды: NO + NO 2 +2 Na. OH → 2 Na. NO 2 + H 2 O 2) Восстановление нитратов: Na. NO 3 + Pb → Pb. O + Na. NO 2 (сплавление)
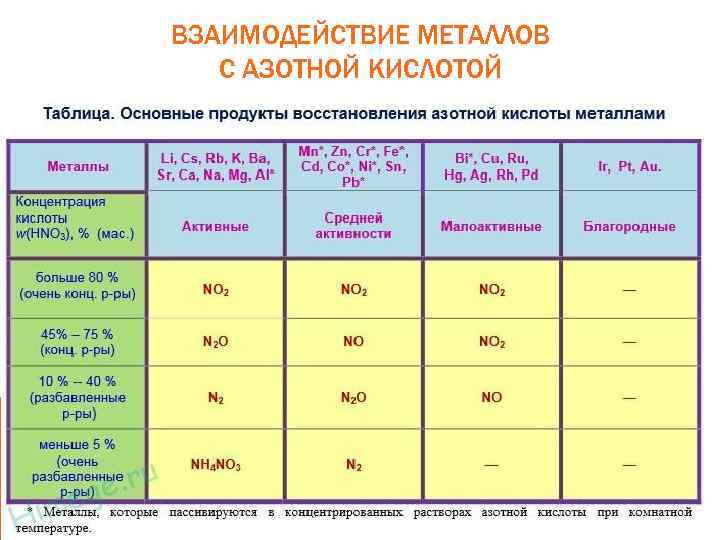 ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С АЗОТНОЙ КИСЛОТОЙ
ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С АЗОТНОЙ КИСЛОТОЙ
 ПОЛУЧЕНИЕ НИТРАТОВ Действие азотной кислоты на металлы, оксиды, гидроксиды, карбонаты: 3 Ag + 4 HNO 3 (разб. ) → 3 Ag. NO 3 + NO + 2 H 2 O Ni. O + 2 HNO 3 → Ni(NO 3)2 + H 2 O KOH + HNO 3 → KNO 3 + H 2 O Na 2 CO 3 + 2 HNO 3 → 2 Na. NO 3 + CO 2 + H 2 O
ПОЛУЧЕНИЕ НИТРАТОВ Действие азотной кислоты на металлы, оксиды, гидроксиды, карбонаты: 3 Ag + 4 HNO 3 (разб. ) → 3 Ag. NO 3 + NO + 2 H 2 O Ni. O + 2 HNO 3 → Ni(NO 3)2 + H 2 O KOH + HNO 3 → KNO 3 + H 2 O Na 2 CO 3 + 2 HNO 3 → 2 Na. NO 3 + CO 2 + H 2 O
 А! К ТИ К А ЕП Т РЬ Е РА П
А! К ТИ К А ЕП Т РЬ Е РА П