Химические забавы 1.pptx
- Количество слайдов: 20

ХЗ: химические забавы Лекция 1 Атом мирный и не очень

История: первые представления Атом: от греческого ἄτομος – неделимый. Мельчайшая частица вещества, материи, отвечающая за его свойства L E U K I P P O S

История: пудинговая модель Атом: «…атомы элементов состоят из нескольких отрицательно заряженных корпускул, заключённых в сферу, имеющую однородно распределённый положительный электрический заряд…» Дж. Томсон, 1904 г.
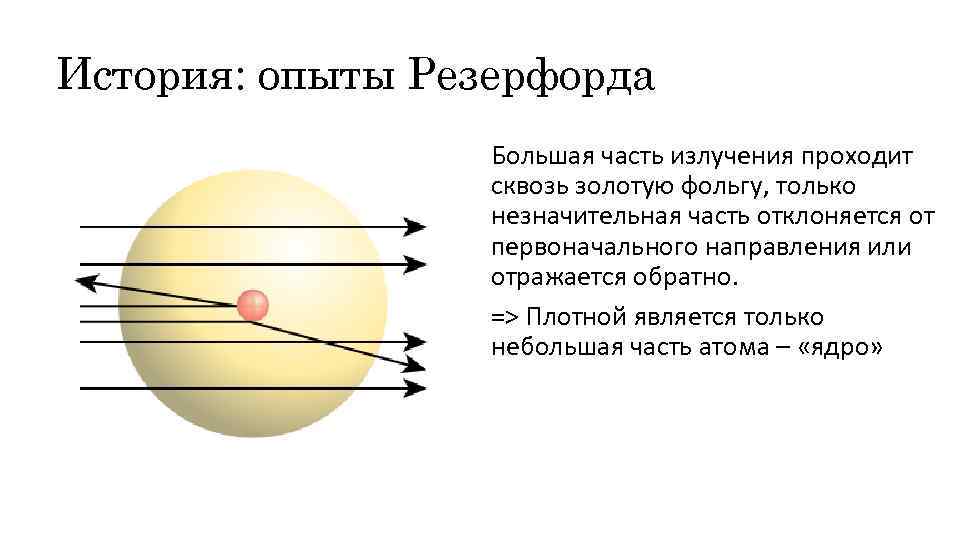
История: опыты Резерфорда Большая часть излучения проходит сквозь золотую фольгу, только незначительная часть отклоняется от первоначального направления или отражается обратно. => Плотной является только небольшая часть атома – «ядро»

История: планетарная модель Атом: Состоит из ядра и электронной оболочки, причем электроны движутся по своим отдельным орбитам Э. Резерфорд, 1911 г.

История: планетарная модель Атом: Состоит из ядра и электронной оболочки, причем электроны движутся по своим отдельным орбитам Э. Резерфорд, 1911 г. НО: а не упадут ли электроны на ядро? . .

История: модель Бора-Резерфорда НЕ УПАДУТ Н. Бор, 1913 г. 1. Атом и атомные системы могут длительно пребывать только в особенных стационарных или квантовых состояниях, каждому из которых отвечает определенная энергия 2. Излучение света происходит только при переходе электрона из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией. Энергия излученного фотона равна разности энергий стационарных состояний.

Строение атома Ядро: p+ – протоны, заряд «+» , mp 1 а. е. м. (1/12 m. C) n 0 – нейтроны, заряда нет, mn = mp 1 а. е. м. Электронная оболочка: e- - электроны, заряд «–» , me 0, 0005 mp Строение электронной оболочки? . . В атомной массе элемента масса электронов, как правило, не учитывается! Заряд атома равен нулю => количество протонов равно количеству электронов.

Периодический закон

Промежуточные выводы 1. Атом состоит из ядра (протонов, нейтронов) и электронов, причем mp = mn >> me 2. Символ атома определяет количество протонов в ядре 3. Химию атома определяют • Внешний электронный слой (сколько там электронов) • Размер атома (насколько хорошо они там держатся)
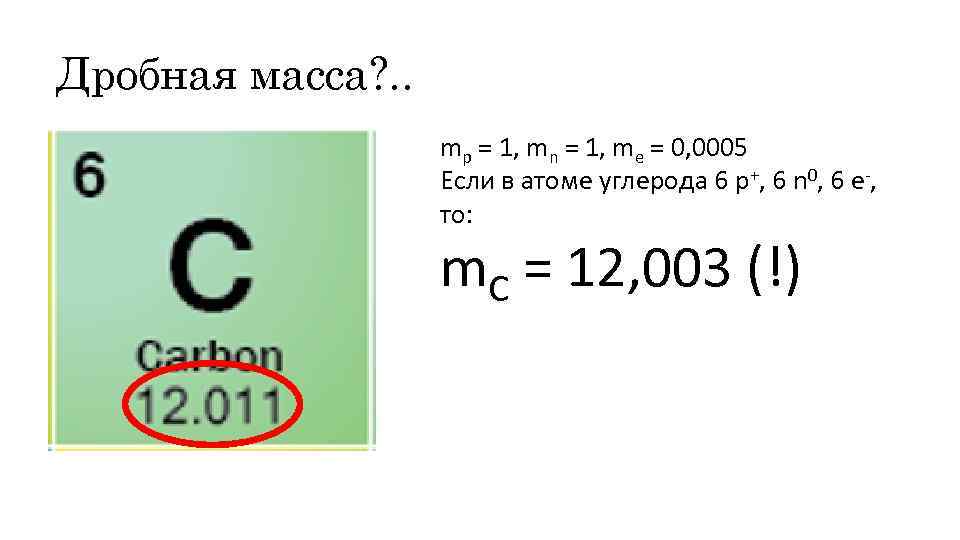
Дробная масса? . . mp = 1, mn = 1, me = 0, 0005 Если в атоме углерода 6 p+, 6 n 0, 6 e-, то: m. C = 12, 003 (!)

Средняя масса! Изотопы – атомы с одинаковым количеством протонов и разным количеством нейтронов. Для углерода эти изотопы: 12 С – 98, 93% 13 С – 1, 07% 14 С - 0, 000001% В таблице Менделеева указана средняя масса по всем природным изотопам

Радиоактивный распад Не все изотопы одинаково полезны стабильны. Ядра некоторых элементы способны самопроизвольно распадаться на более легкие ядра с выбросом (излучением) чего-нибудь. Чего именно?
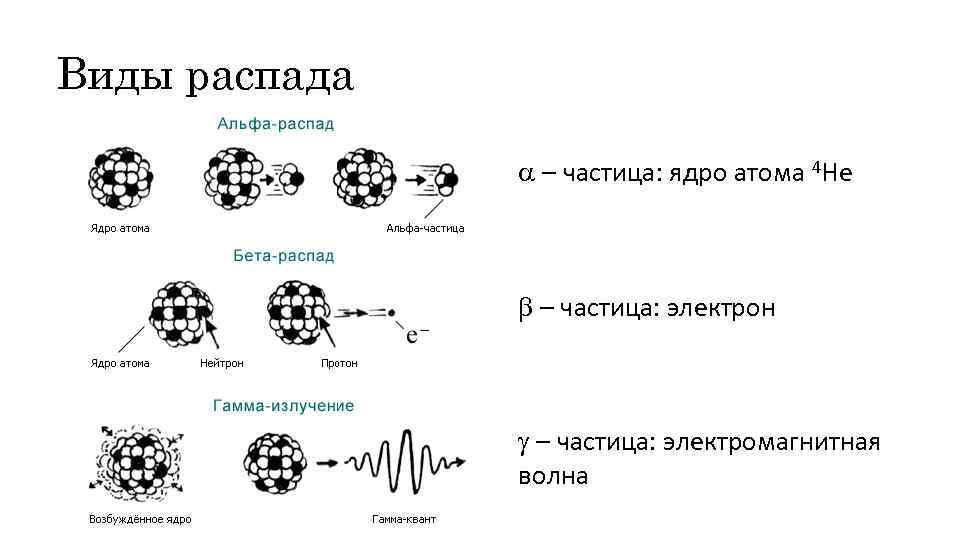
Виды распада a – частица: ядро атома 4 He b – частица: электрон g – частица: электромагнитная волна
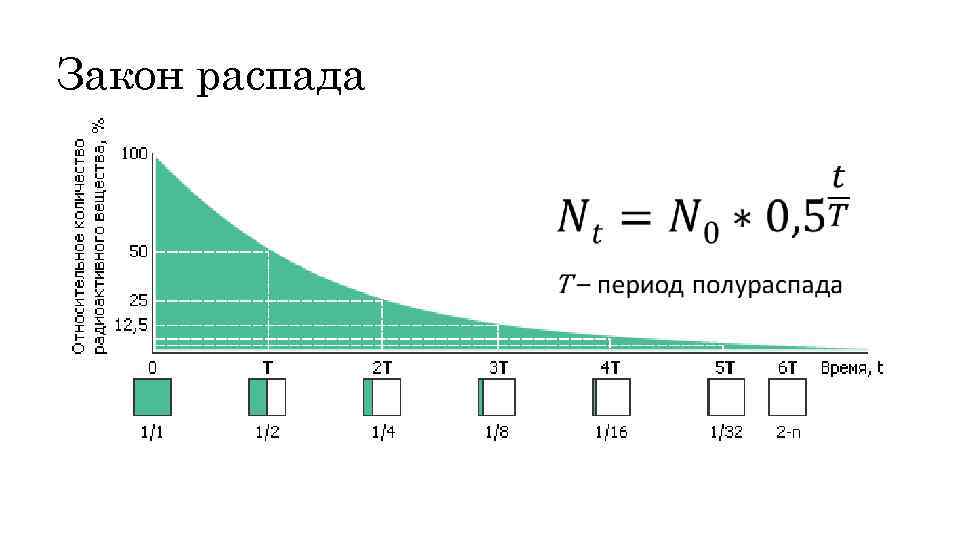
Закон распада

Радиоуглеродный анализ 1. В верхних слоях атмосферы происходит ядерная реакция: 2. Полученный 14 С распределяется по всей атмосфере в виде CO 2 3. Растения поглощают CO 2 (фотосинтез), животные кушают растения => 14 С оказывается в живых организмах Концентрация 14 С во всех живых организмах и атмосфере постоянна! 4. После смерти живого организма поступление 14 С прекращается

Радиоуглеродный анализ 5. Теперь, когда 14 С не поступает в организм, его концентрация постоянно падает из-за радиоактивного распада: T = 5730± 30 лет 6. Если вытащить углерод из образца и измерить интенсивность излучения, можно оценить концентрацию 14 С в образце, а следовательно, и рассчитать его возраст. Точность метода: 30 -300 лет в зависимости от образца!
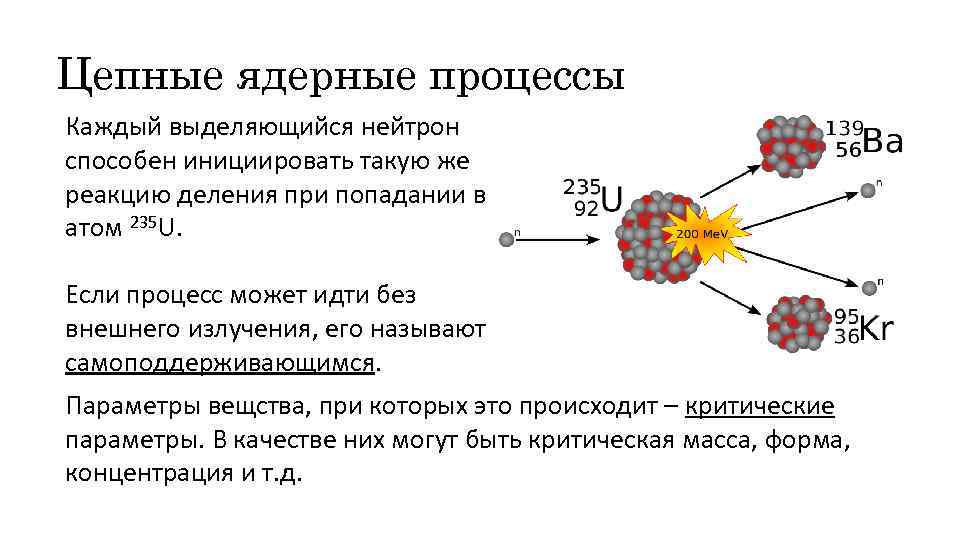
Цепные ядерные процессы Каждый выделяющийся нейтрон способен инициировать такую же реакцию деления при попадании в атом 235 U. Если процесс может идти без внешнего излучения, его называют самоподдерживающимся. Параметры вещства, при которых это происходит – критические параметры. В качестве них могут быть критическая масса, форма, концентрация и т. д.
Использование цепных процессов Самоподдерживающаяся реакция Управляемая Неуправляемая

Домашнее задание № 1 Содержание основных изотопов урана в земной коре в настоящее время таково: 238 U – 99, 27%, T = 4, 47*109 лет 1/2 235 U – 0, 73%, T = 7, 04*108 лет 1/2 Предполагая, что при образовании Земли этих изотопов было одинаковое количество, оцените её возраст. Подсказка: поймите, что такое логарифм, и рассчитайте его с помощью wolframalpha. com или любого другого калькулятора.
Химические забавы 1.pptx