 Хронопотенциометрия простых процессов Определение и основные принципы метода Выполнила: студентка 5 курса ХТФ гр. ХЭ-31 м Фетисова И. С.
Хронопотенциометрия простых процессов Определение и основные принципы метода Выполнила: студентка 5 курса ХТФ гр. ХЭ-31 м Фетисова И. С.
 Хронопотенциометрия - электрохимический метод исследования и анализа, основанный на изучении изменения электродного потенциала Е во времени при контролируемом значении тока электролиза Хронопотенциометрия позволяет решать следующие задачи электрохимичской кинетики: 1. Определение коэффициентов диффузии. 2. Определение электродной поляризации и механизма электродных реакций. 3. Определение констант скоростей химических реакций, связанных с электродными процессами. 4. Определение концентрации разряжающихся ионов.
Хронопотенциометрия - электрохимический метод исследования и анализа, основанный на изучении изменения электродного потенциала Е во времени при контролируемом значении тока электролиза Хронопотенциометрия позволяет решать следующие задачи электрохимичской кинетики: 1. Определение коэффициентов диффузии. 2. Определение электродной поляризации и механизма электродных реакций. 3. Определение констант скоростей химических реакций, связанных с электродными процессами. 4. Определение концентрации разряжающихся ионов.
 Чтобы описать поведение системы O/R при I= const, необходимо решить систему уравнений второго закона. Фика При t=0 при t≤ 0 Сумма потоков веществ от поверхности и поверхности электрода должна быть равна нулю При I= const это условие можно записать в виде уравнения, которое означает независимость потоков диффузии от времени
Чтобы описать поведение системы O/R при I= const, необходимо решить систему уравнений второго закона. Фика При t=0 при t≤ 0 Сумма потоков веществ от поверхности и поверхности электрода должна быть равна нулю При I= const это условие можно записать в виде уравнения, которое означает независимость потоков диффузии от времени
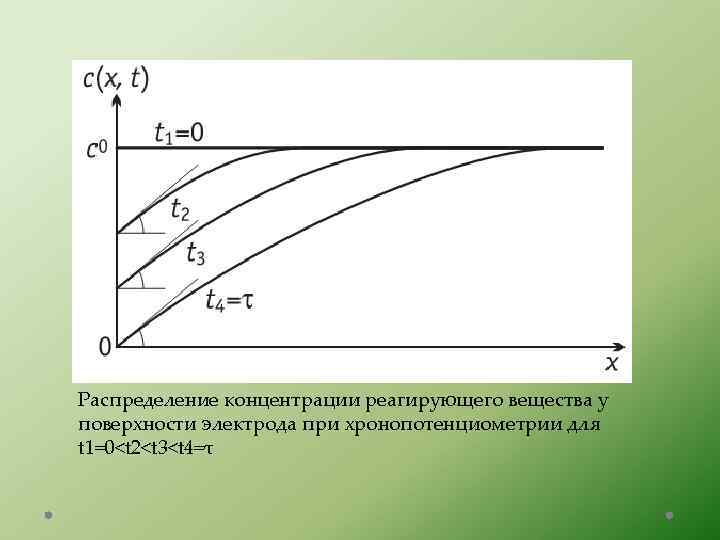 Распределение концентрации реагирующего вещества у поверхности электрода при хронопотенциометрии для t 1=0
Распределение концентрации реагирующего вещества у поверхности электрода при хронопотенциометрии для t 1=0
 Зависимости концентрацийот времени и расстояния для хронопотенциометрии на постоянном токе (Г. Санд, З. Караогланов) имеют вид: (4) (5) (6) (7) Поскольку при t=τ, то из уравнения (6) можно получить уравнение Санда для объемной концентрации: Используя уравнение (8), вместо (6) можно записать И найти соотношение концентраций окисленной и восстановленной форм: (8) (9) (10)
Зависимости концентрацийот времени и расстояния для хронопотенциометрии на постоянном токе (Г. Санд, З. Караогланов) имеют вид: (4) (5) (6) (7) Поскольку при t=τ, то из уравнения (6) можно получить уравнение Санда для объемной концентрации: Используя уравнение (8), вместо (6) можно записать И найти соотношение концентраций окисленной и восстановленной форм: (8) (9) (10)
 Из (10) и уравнения Нернста можно вывести зависимость между потенциалом и временем: (11) уравнением Караогланова Из уравнения видно, что потенциал электрода равен потенциалу полуволны при Отсюда следует, что Е=Е 1/2 при t=τ/4. При t=0 потенциал электрода стремится к бесконечности. Однако потенциал реального электрода при разомкнутой цепи достигает лишь значений, соответствующих началу анодного растворения металла
Из (10) и уравнения Нернста можно вывести зависимость между потенциалом и временем: (11) уравнением Караогланова Из уравнения видно, что потенциал электрода равен потенциалу полуволны при Отсюда следует, что Е=Е 1/2 при t=τ/4. При t=0 потенциал электрода стремится к бесконечности. Однако потенциал реального электрода при разомкнутой цепи достигает лишь значений, соответствующих началу анодного растворения металла
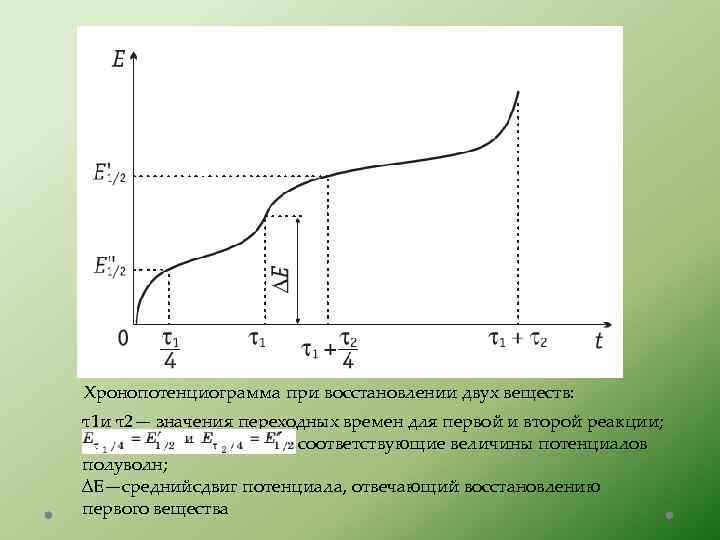 Хронопотенциограмма при восстановлении двух веществ: τ1 и τ2— значения переходных времен для первой и второй реакции; соответствующие величины потенциалов полуволн; ∆E—среднийсдвиг потенциала, отвечающий восстановлению первого вещества
Хронопотенциограмма при восстановлении двух веществ: τ1 и τ2— значения переходных времен для первой и второй реакции; соответствующие величины потенциалов полуволн; ∆E—среднийсдвиг потенциала, отвечающий восстановлению первого вещества
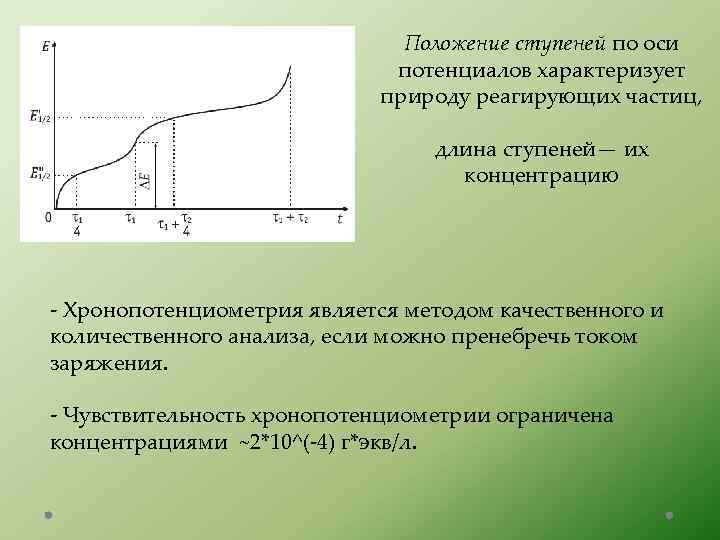 Положение ступеней по оси потенциалов характеризует природу реагирующих частиц, длина ступеней— их концентрацию - Хронопотенциометрия является методом качественного и количественного анализа, если можно пренебречь током заряжения. - Чувствительность хронопотенциометрии ограничена концентрациями ~2*10^(-4) г*экв/л.
Положение ступеней по оси потенциалов характеризует природу реагирующих частиц, длина ступеней— их концентрацию - Хронопотенциометрия является методом качественного и количественного анализа, если можно пренебречь током заряжения. - Чувствительность хронопотенциометрии ограничена концентрациями ~2*10^(-4) г*экв/л.
 Инверсионная амальгамная хронопотенциометрия включает в себя предварительное накопление определяемого вещества в виде амальгамы выдержкой висячей ртутной капли при заданном потенциале в изучаемом растворе и последующее измерение кривых потенциал —время при пропускании постоянного анодного тока. Импульсная хронопотенциометрия (импульсный гальваностатический метод) применяется в электрохимической кинетике для исследования быстрых электродных процессов и процессов заряжения межфазных границ. При этом изменения потенциала регистрируют в микросекундных промежутках времени после включения токов большой плотности. Чтобы разделить вклады процессов заряжения и электродной реакции, применяют двухимпульсный гальваностатический метод с большей плотностью тока в первом импульсе.
Инверсионная амальгамная хронопотенциометрия включает в себя предварительное накопление определяемого вещества в виде амальгамы выдержкой висячей ртутной капли при заданном потенциале в изучаемом растворе и последующее измерение кривых потенциал —время при пропускании постоянного анодного тока. Импульсная хронопотенциометрия (импульсный гальваностатический метод) применяется в электрохимической кинетике для исследования быстрых электродных процессов и процессов заряжения межфазных границ. При этом изменения потенциала регистрируют в микросекундных промежутках времени после включения токов большой плотности. Чтобы разделить вклады процессов заряжения и электродной реакции, применяют двухимпульсный гальваностатический метод с большей плотностью тока в первом импульсе.
 Спасибо за внимание.
Спасибо за внимание.