ХЛЛ 2010.ppt
- Количество слайдов: 43

Хронический лимфолейкоз. Биологические особенности и современные подходы к его терапии Докладчик: Пономаренко О. Б. , 638 гр

Распространенность ХЛЛ В странах Европы и Северной Америки на долю ХЛЛ приходится 30% среди всех лейкозов. Ежегодная заболеваемость ХЛЛ в этих странах составляет 3 – 3, 5 на 100 000 населения Среди лиц старше 65 лет – до 20 на 100 000 Около 70% пациентов заболевают между 50 и 70 годами Мужчины болеют чаще женщин (2: 1) ХЛЛ является самой частой формой лейкоза у кровных родственников как по горизонтальной, так и по вертикальной линии.

Согласно современным критериям, установленным Международным рабочим совещанием в 1989 г. , для постановки диагноза ХЛЛ необходимо наличие трех признаков: l абсолютного количества лимфоцитов крови, превышающего 5, 0*109/л l обнаружение более 30% лимфоцитов в костномозговом пунктате l иммунологического подтверждения наличия В – клеточного клона лейкемических лимфоцитов
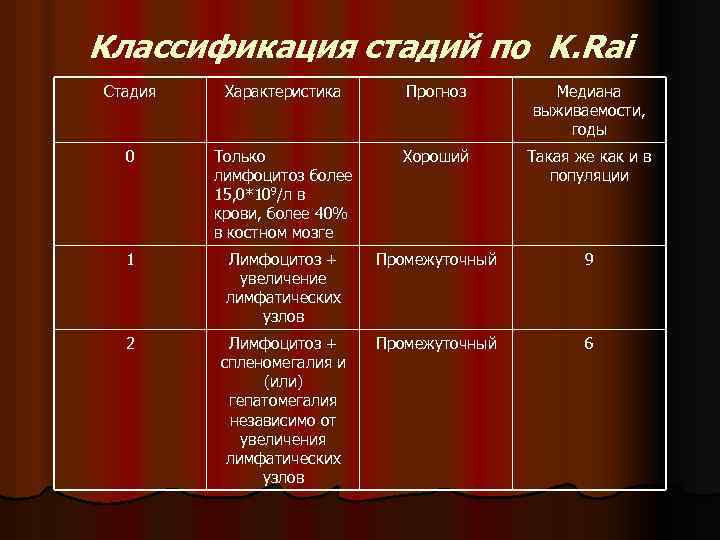
Классификация стадий по K. Rai Стадия Характеристика Прогноз Медиана выживаемости, годы 0 Только лимфоцитоз более 15, 0*109/л в крови, более 40% в костном мозге Хороший Такая же как и в популяции 1 Лимфоцитоз + увеличение лимфатических узлов Промежуточный 9 2 Лимфоцитоз + спленомегалия и (или) гепатомегалия независимо от увеличения лимфатических узлов Промежуточный 6
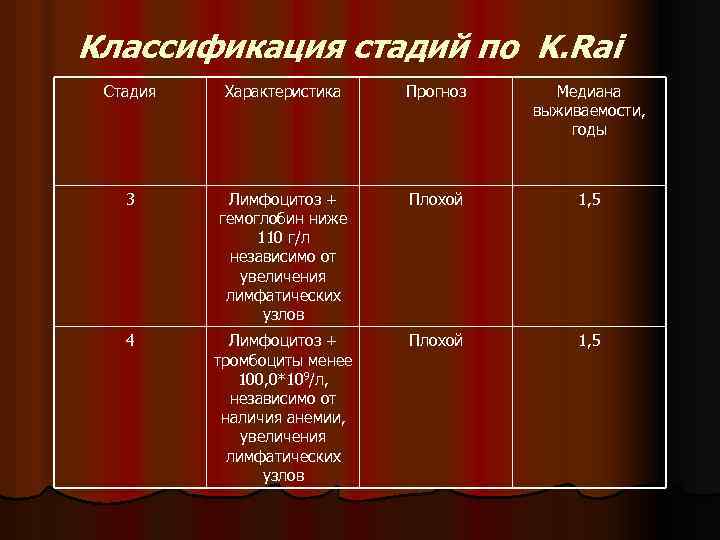
Классификация стадий по K. Rai Стадия Характеристика Прогноз Медиана выживаемости, годы 3 Лимфоцитоз + гемоглобин ниже 110 г/л независимо от увеличения лимфатических узлов Плохой 1, 5 4 Лимфоцитоз + тромбоциты менее 100, 0*109/л, независимо от наличия анемии, увеличения лимфатических узлов Плохой 1, 5

Классификация стадий по J. Binet Стадия Характеристика Медиана выживаемости, годы А Гемоглобин – более 100 г/л, тромбоциты – более 100*109/л, увеличение лимфатических узлов в 1 - 2 областях Такая же, как и в популяции В Гемоглобин – более 100 г/л, тромбоциты – более 100*109/л, увеличение лимфатических узлов в 3 и более областях 7 С Гемоглобин – менее 100 г/л, тромбоциты – менее 100*109/л, при любом количестве зон с увеличенными лимфатическими узлами и независимо от увеличения органов 2

l Морфологическим субстратом ХЛЛ является клон CD 5+ В – лимфоцитов, иммунофенотипом CD 5+, CD 19+, CD 20+, CD 23+, слабой экспрессией CD 22+ и поверхностных иммуноглобулинов, FMC 7 - , аналогичный нормальным CD 5+ В – лимфоцитам мантийной зоны вторичного фолликула лимфоузла, участвующим в независимой от Т – лимфоцитов иммунном ответе.

Виды ХЛЛ l Морфологический субстрат – «наивные» лимфоциты. Имеет более агрессивное течение и нуждается в более интенсивной терапии. l Морфологический субстрат – «клетки памяти»
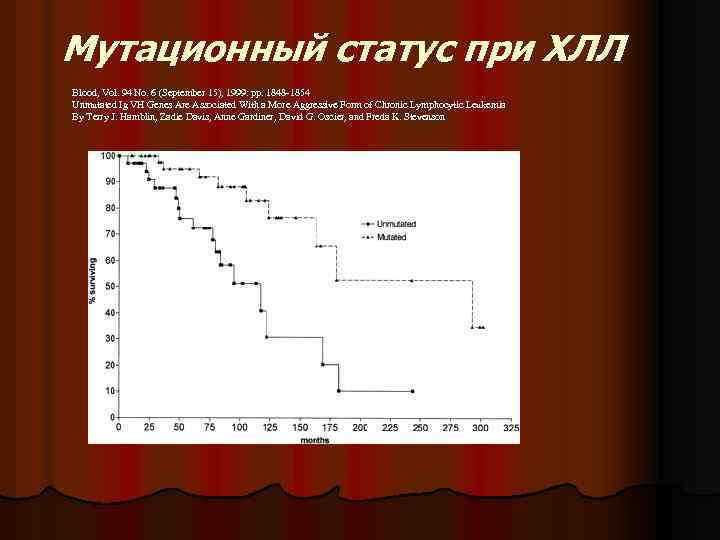
Мутационный статус при ХЛЛ Blood, Vol. 94 No. 6 (September 15), 1999: pp. 1848 -1854 Unmutated Ig VH Genes Are Associated With a More Aggressive Form of Chronic Lymphocytic Leukemia By Terry J. Hamblin, Zadie Davis, Anne Gardiner, David G. Oscier, and Freda K. Stevenson

Наиболее часто втречающиеся и прогностически значимые хромосомные абберации при ХЛЛ l l l l l Делеция длинного плеча хромосомы 13 (13 q-) определяется у 55% больных Делеция длинного плеча хромосомы 11 (11 q-) у 18% Трисомия 12 хромосомы – у 16% Делеция короткого плеча хромосомы 17 (17 p-) – у 7 % больных Делеция длинного плеча хромосомы 6 (6 q-) – у 6% Транслокации с участием хромосомы 14 (14 q 32) – в 4% случаев Удлинение длинного плеча хромосомы 14 (14 q+) Трисомия хромосомы 8 – в 5% случаев Трисомия хромосомы 3 – у 3% больных
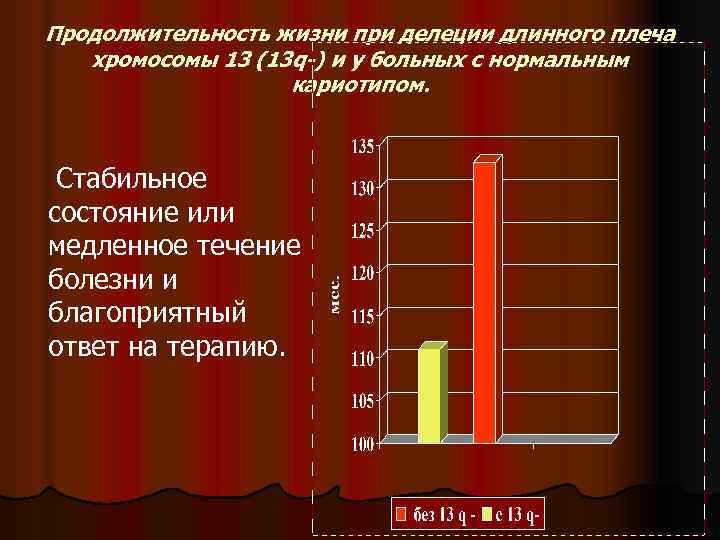
Продолжительность жизни при делеции длинного плеча хромосомы 13 (13 q-) и у больных с нормальным кариотипом. Стабильное состояние или медленное течение болезни и благоприятный ответ на терапию.
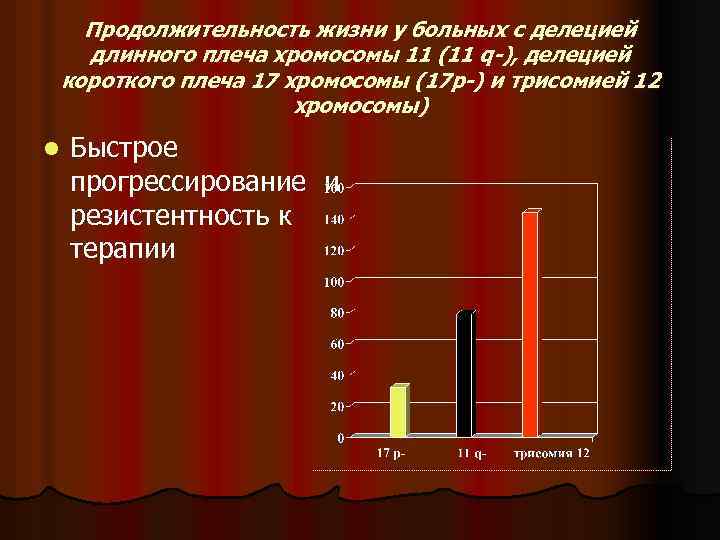
Продолжительность жизни у больных с делецией длинного плеча хромосомы 11 (11 q-), делецией короткого плеча 17 хромосомы (17 p-) и трисомией 12 хромосомы) l Быстрое прогрессирование и резистентность к терапии

Сопоставление хромосомных аббераций с мутационным статусом Ig. VH гена 13 q- статистически значимо чаще встречалась у больных с мутациями гена Ig. VH 11 q- и 17 р- с высокой степенью достоверности чаще при отсутствии таких мутаций
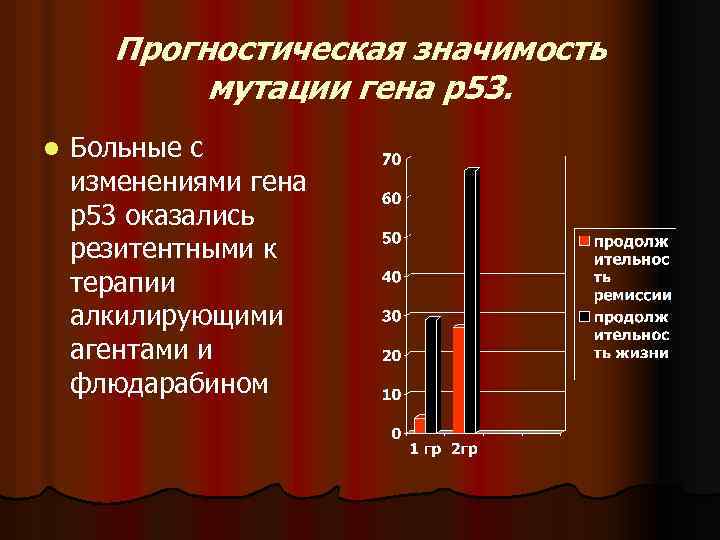
Прогностическая значимость мутации гена р53. l Больные с изменениями гена р53 оказались резитентными к терапии алкилирующими агентами и флюдарабином

Экспрессия поверхностных антигенов при ХЛЛ СD 5+ CD 19+ CD 20+ CD 23+ Слабая экспрессия CD 22
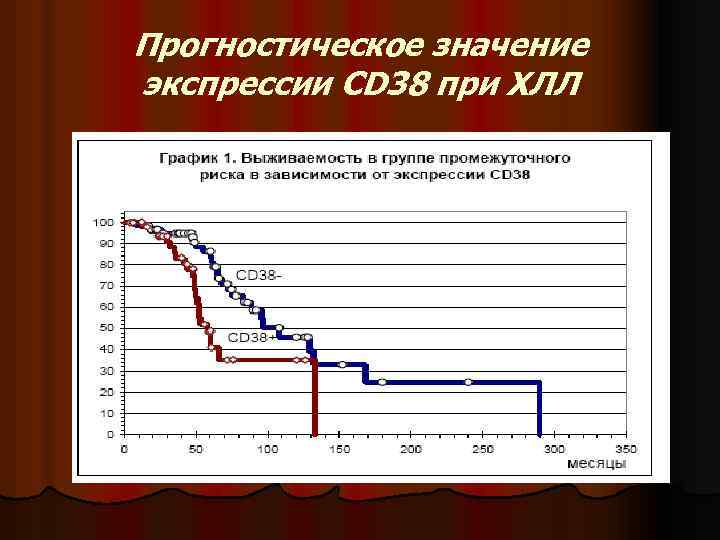
Прогностическое значение экспрессии CD 38 при ХЛЛ
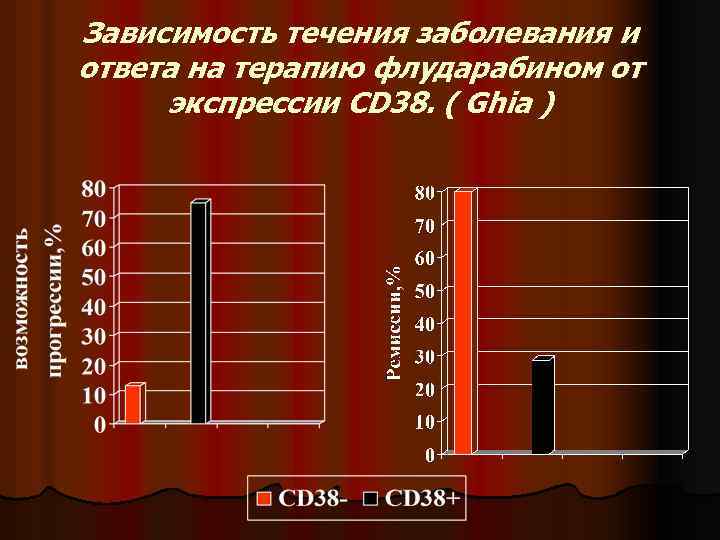
Зависимость течения заболевания и ответа на терапию флударабином от экспрессии CD 38. ( Ghia )
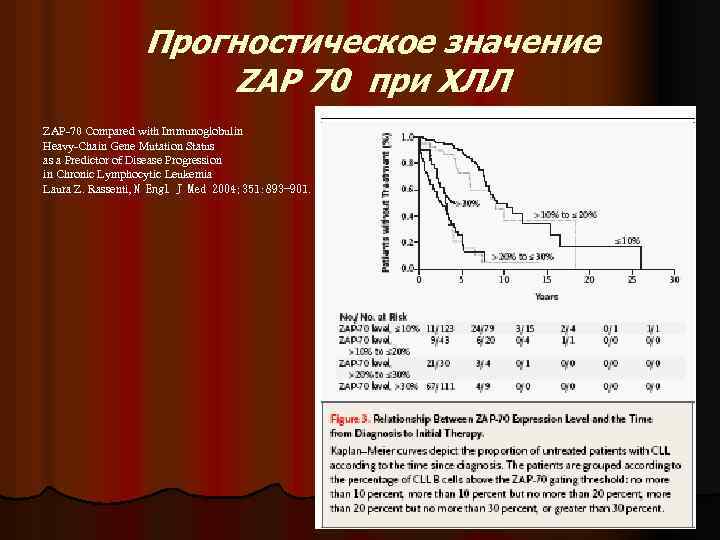
Прогностическое значение ZAP 70 при ХЛЛ ZAP-70 Compared with Immunoglobulin Heavy-Chain Gene Mutation Status as a Predictor of Disease Progression in Chronic Lymphocytic Leukemia Laura Z. Rassenti, N Engl J Med 2004; 351: 893 -901.

l l При уровне ЛДГ, повышенном в 1, 25 раза – медиана продолжительности жизни составляет 4, 4 года; при нормальном уровне – 12, 6 лет При концентрации бета– 2 -микроглобулина более 3 мг/л – 4, 6 лет; При уровне растворимой СD 23, превышающим норму в 10 раз, выживаемость составила 6, 4 года, при меньшем содержании – около 10 лет С уровнем тимидин киназы в начальной стадии болезни среднее время без признаков прогрессирования составило 49 месяцев, с более высоким уровнем фермента – 8 месяцев.

Продолжительность жизни при медленном и быстром удвоении количества лимфоцитов. (Monserrat) l Медиана выживаемости для пациентов с медленным удвоением количества лимфоцитов – более 118 месяцев, тогда как для пациентов с быстрым – 61 месяц

Диагностические критерии l l Лимфоцитоз более 5*109/л Продолжительность лимфоцитоза более 2 месяцев Лимфоцитов в костном мозге более 30% Находки проточной цитомфлюориметрии (CD 5+, CD 19+, CD 23+, CD 20+) Критерии высокого риска Экспрессия CD 38 в более 30% лимфоцитов Экспрессия ZAP 70 в более 30% лимфоцитов Наличие лимфоцитов без признаков мутации VH гена. Изменения кариотипа удлинение длинного плеча хромосомы 14 (14 q+) транслокация с участием хромосомы 14 (14 q 32) делеция длинного плеча хромосомы 11 (11 q-) делеция короткого плеча хромосомы 17 (17 p-) трисомия 12 хромосомы Стадии 3 или 4 ( Rai system) или стадия С ( Binet system) Повышенный уровень бета – 2 – микроглобулина (В 2 М) Повышение уровня тимидин киназы Удвоение абсолютного числа лимфоцитов в периферической крови менее чем за 12 месяцев

Начало лечения ХЛЛ В настоящее время тактика «наблюдай и жди» сохраняется только в отношении больных с минимальными проявлениями заболевания и лишь до тех пор, пока не появятся любые признаки прогрессирования (не только нарастание лейкоцитоза, лимфоцитоза, увеличение размеров лимфатических узлов и селезенки, но и такие, как аутоиммунный гемолиз и учащение бактериальных инфекций). l Таким образом, больной не нуждается в лечении лишь до тех пор, пока стабильно сохраняется стадии 0 – I по Rai или A по Binet l

Показания к началу цитостатической терапии 1. Как минимум один из симптомов интоксикации: - снижение веса > 10% массы тела за 6 месяцев (если пациент не предпринимал мер к похуданию) - выраженная слабость (>2 по шкале ECOG – не может работать или следовать привычному (активному) образу жизни) - повышение температуры > 37, 5 без признаков инфекции в течение 2 недель ночная потливость без признаков инфекции 2. Нарастающая анемия и/или тромбоцитопения, обусловленная инфиальтрацией костного мозга 3. Аутоиммунная анемия и/или тромбоцитопения, резистентные к преднизолону 4. Большие размеры селезенки (>6 см ниже реберной дуги), явный рост селезенки 5. Массивная и нарастающая лимфаденопатия (размер одного из конгломератов превышает 10 см) 6. Прирост лимфоцитоза более, чем на 50% за 2 месяца; ожидаемое время удвоения лимфоцитов менее 6 месяцев 7. Увеличенная подверженность бактериальным инфекциям 8. Массивная лимфоцитарная инфильтрация костного мозга (более 80% лимфоцитов в миелограмме) 9. Наличие комплексных хромосомных аббераций 10. Продвинутая стадия болезни (стадия С по J. Binet, III-IV по K. Rai)

Лечение ХЛЛ В 1949 году Person и соавт сообщили об уменьшении лимфоидной пролиферации при ХЛЛ под влиянием стероидных гормонов l Затем в 1955 году появилось первое сообщение об использовании хлорамбуцила при лимфопролиферативных заболеваниях и была отмечена его высокая эффективность при ХЛЛ l В 70 – 80 годы на базе алкилирующих препаратов (чаще всего циклофосфана и лейкерана) были созданы комбинированные лечебные схемы. l

Комбинированные лечебные схемы l l l COP: циклофосфан, винкристин, преднизолон CHOP: циклофосфан, винкристин, адриамицин, преднизолон CAP: циклофосфан, адриомицин, преднизолон POACH: циклофосфан, винкристин, адриамицин, цитозин-арабинозид, преднизолон М – 2: циклофосфан, кармустин, винкристин, мелфалан, преднизолон LVPP: хлорамбуцил, натулан, преднизолон, винбластин
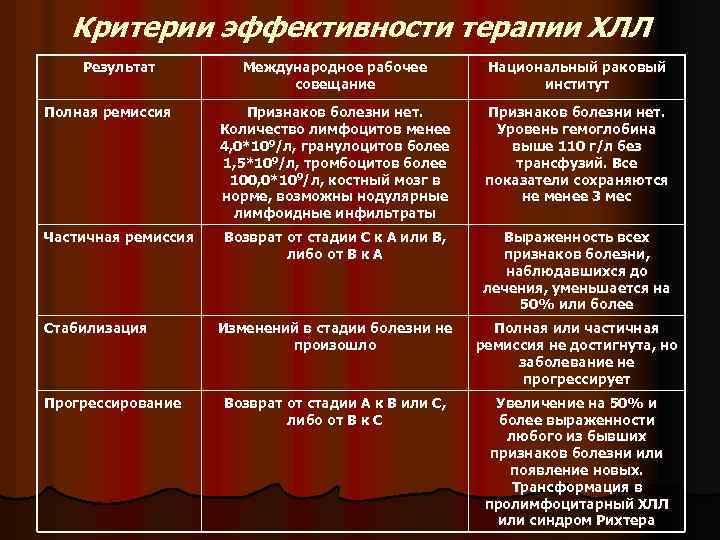
Критерии эффективности терапии ХЛЛ Результат Полная ремиссия Частичная ремиссия Стабилизация Прогрессирование Международное рабочее совещание Национальный раковый институт Признаков болезни нет. Количество лимфоцитов менее 4, 0*109/л, гранулоцитов более 1, 5*109/л, тромбоцитов более 100, 0*109/л, костный мозг в норме, возможны нодулярные лимфоидные инфильтраты Признаков болезни нет. Уровень гемоглобина выше 110 г/л без трансфузий. Все показатели сохраняются не менее 3 мес Возврат от стадии С к А или В, либо от В к А Выраженность всех признаков болезни, наблюдавшихся до лечения, уменьшается на 50% или более Изменений в стадии болезни не произошло Полная или частичная ремиссия не достигнута, но заболевание не прогрессирует Возврат от стадии А к В или С, либо от В к С Увеличение на 50% и более выраженности любого из бывших признаков болезни или появление новых. Трансформация в пролимфоцитарный ХЛЛ или синдром Рихтера

Лечение ХЛЛ l. В конце 80 – х годов был синтезирован препарат – фтор – аденин - арабинозид – монофосфат, получивший название флюдара
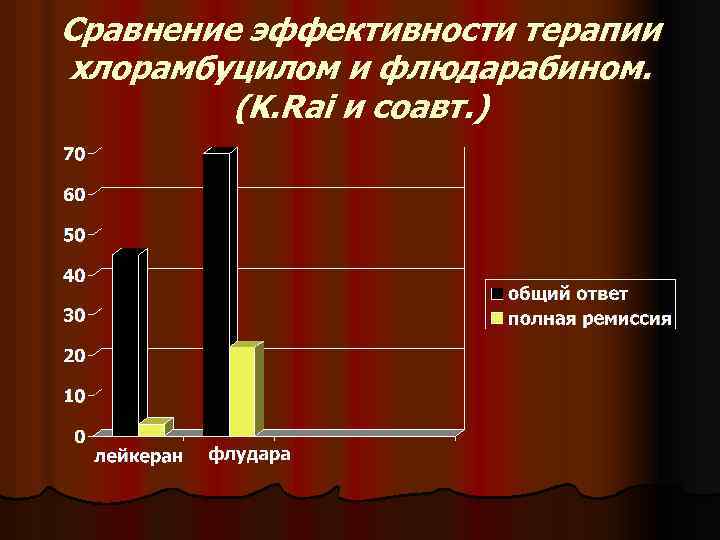
Сравнение эффективности терапии хлорамбуцилом и флюдарабином. (K. Rai и соавт. )

l По данным Ракового центра M. D. Anderson (США), у первичных больных, получавших Флюдарабин, медиана выживаемости не достигнута за 66 месяцев наблюдения, что превосходит ранее имевшиеся результаты.
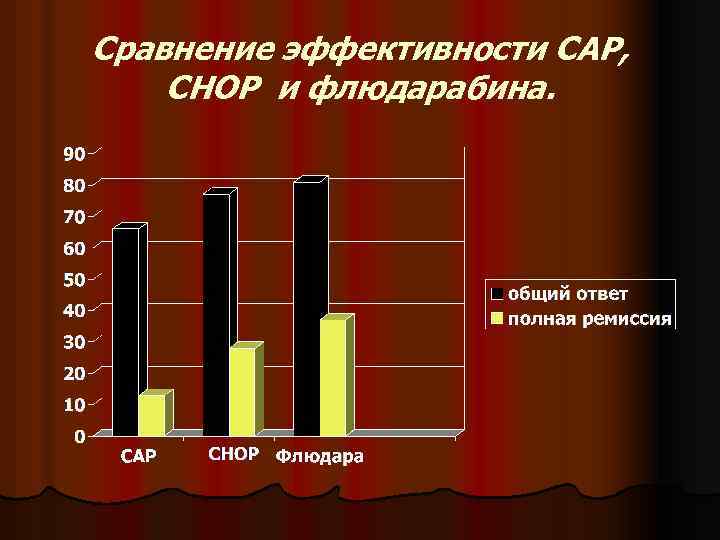
Сравнение эффективности CAP, CHOP и флюдарабина.
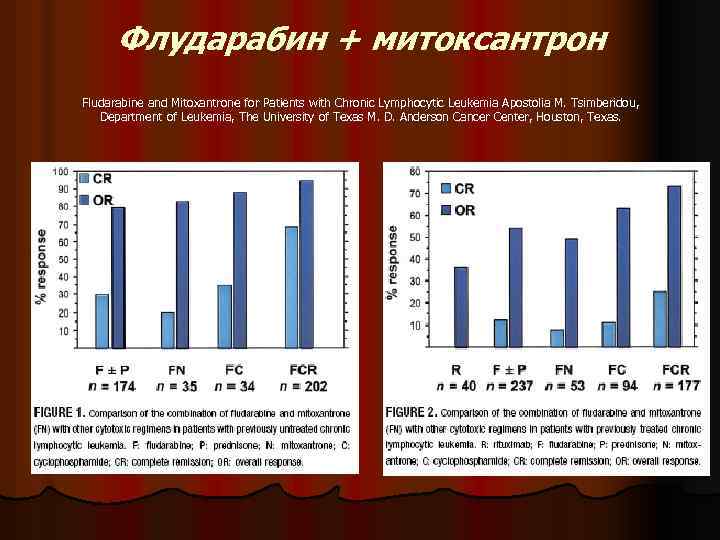
Флударабин + митоксантрон Fludarabine and Mitoxantrone for Patients with Chronic Lymphocytic Leukemia Apostolia M. Tsimberidou, Department of Leukemia, The University of Texas M. D. Anderson Cancer Center, Houston, Texas.

Применение G-CSF в лечении ХЛЛ l Добавление к комбинации флюдарабина с циклофосфаном G-CSF, позволившего за счет укорочения периода миелосупрессии исключить вынужденное удлинение интервалов между курсами, дало возможность получить 100% ремиссий – 47% полных и 53% частичных.

Побочные эффекты флюдарабина l l l Тошнота и рвота наблюдается в очень редких случаях Алопеция – не более, чем у 2% больных (только у тех, которые получале ранее многочисленные курсы ХТ) Нейротоксичность, у 16% (всегда обратима) Миелосупрессия III – IV степени у 20 – 43% больных Инфекционные осложнения 15 – 20% Аутоиммунная анемия (у больных, в анамнезе которых отмечались эпизоды аутоиммунной гемолитической анемии)

ТГСК при ХЛЛ Аллогенная трансплантация считается показанной больным до 55 лет с вышеуказанными неблагоприятными прогностическими признаками l больным до 65 лет при наличии признаков плохого прогноза показана аутологичная трансплантация l больным до 75 лет – трансплантация с немиелоаблативными режимами кондиционирования l

ТГСК при ХЛЛ l При аллогенных трансплантациях смертность составила 50% l возможность рецидива в течение 3 лет – 15% l при аутологичных – смертность составила 15% l возможность рецидива – 45%.

Лечение ХЛЛ l. В конце 80 -х – начале 90 -х годов появились первые сообщения об использовании моноклональных антител в лечении ХЛЛ. l Клиническое применение нашли два препарата: Rituximab (Mabthera) и Campath-1 H.
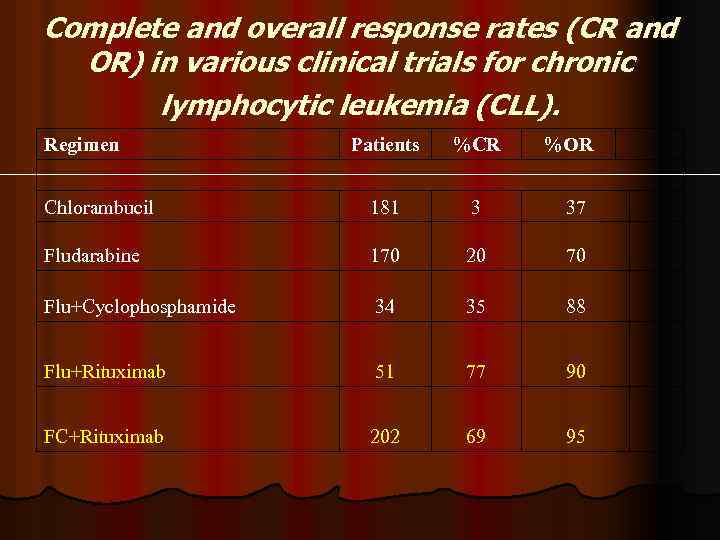
Complete and overall response rates (CR and OR) in various clinical trials for chronic lymphocytic leukemia (CLL). Regimen Patients %CR %OR Chlorambucil 181 3 37 Fludarabine 170 20 70 Flu+Cyclophosphamide 34 35 88 Flu+Rituximab 51 77 90 FC+Rituximab 202 69 95
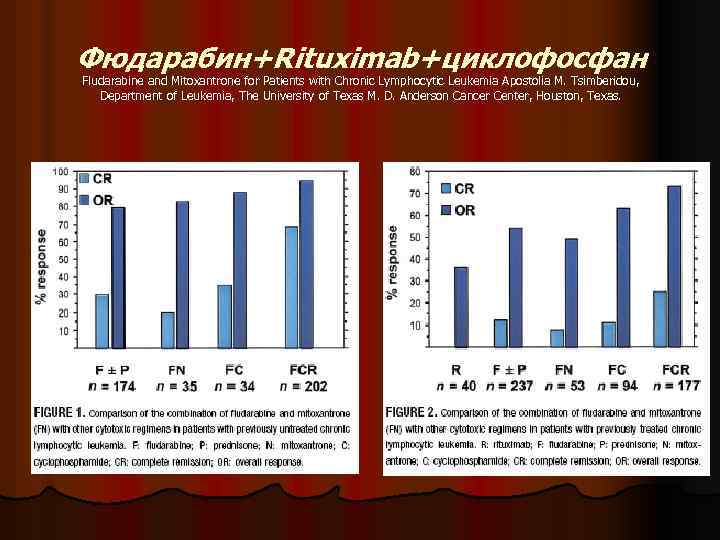
Фюдарабин+Rituximab+циклофосфан Fludarabine and Mitoxantrone for Patients with Chronic Lymphocytic Leukemia Apostolia M. Tsimberidou, Department of Leukemia, The University of Texas M. D. Anderson Cancer Center, Houston, Texas.

l. У ранее леченных больных, в том числе и резистентных к алкилирующим агентам и флюдарабину: l Общий эффект достигнут в 70% случаев l Полные ремиссии достигнуты в 14% случаев
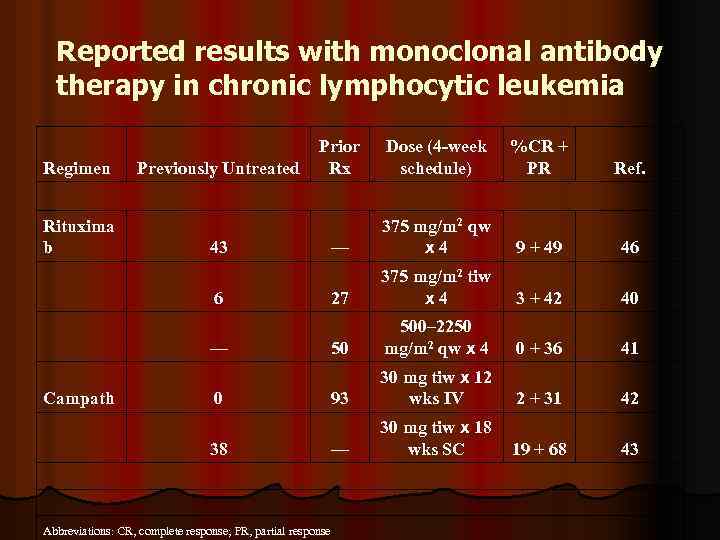
Reported results with monoclonal antibody therapy in chronic lymphocytic leukemia Regimen Rituxima b Previously Untreated Prior Rx Dose (4 -week schedule) %CR + PR Ref. — 375 mg/m 2 qw x 4 9 + 49 46 27 375 mg/m 2 tiw x 4 3 + 42 40 50 500– 2250 mg/m 2 qw x 4 0 + 36 41 93 30 mg tiw x 12 wks IV 2 + 31 42 — 30 mg tiw x 18 wks SC 19 + 68 43 43 6 — Campath 0 38 Abbreviations: CR, complete response; PR, partial response
Побочные эффекты моноклональных антител l l l Высокая температура Озноб Одышка Падение АД Резкое снижение иммунитета Развитие тяжелых инфекций
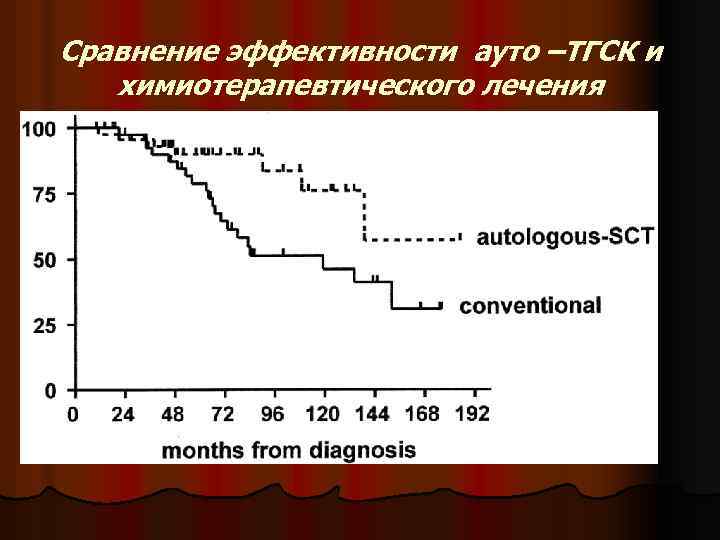
Сравнение эффективности ауто –ТГСК и химиотерапевтического лечения

Выводы Ауто-ТГСК l Ауто-ТГСК может увеличивать выживаемость пациентов с плохим прогнозом l Плохие результаты в случае выполнения ауто-ТГСК в поздние сроки у химиорезистентных пациентов l Не гарантирует излечение Алло-ТГСК l Может приводить к продолжительной безрецидивной выживаемости и излечению l Эффективна у пациентов с рецидивами после ауто-ТГСК l Высокая смертность на трансплантации
ХЛЛ 2010.ppt