 ХРОМАТОГРАФИЯ 1903 г. – М. С. Цвет 1917 г. – М. С. Цвет выдвинут на нобелевскую премию (умер в 1919 г. ) 1937 г. – П. Каррер, химик – органик. Нобелевская премия. Исследовал коротиноиды, флавины, витамины А и B 2 хроматографическим методом. 1938 г. – Л. Цехмейстер, Л. Чолноки венгерские химики выпустили первую книгу по хроматографии, где однозначно придается приоритет М. С. Цвета – как создателя хроматографии. 1936 г. – Дубинин М. М. , разделение газов методом адсорбционной хроматографии. 1938 г. – Измайлов Н. А. , Шрайбер М. С. – создание тонкослойной хроматографии. Начало 1940 -х годов – США (Манхэттенский проект создания атомной бомбы) – метод ионообменной хроматографии по разделению редкоземельных элементов, продуктов деления урана. 1952 г. – А. Мартин, Р. Синджем. Нобелевская премия. Разработка метода распределительной хроматографии (разделение смеси аминокислот). 1953 г. – А. Мартин, Э. Г. Джеймс. Разработка метода газожидкостной хроматографии. 1
ХРОМАТОГРАФИЯ 1903 г. – М. С. Цвет 1917 г. – М. С. Цвет выдвинут на нобелевскую премию (умер в 1919 г. ) 1937 г. – П. Каррер, химик – органик. Нобелевская премия. Исследовал коротиноиды, флавины, витамины А и B 2 хроматографическим методом. 1938 г. – Л. Цехмейстер, Л. Чолноки венгерские химики выпустили первую книгу по хроматографии, где однозначно придается приоритет М. С. Цвета – как создателя хроматографии. 1936 г. – Дубинин М. М. , разделение газов методом адсорбционной хроматографии. 1938 г. – Измайлов Н. А. , Шрайбер М. С. – создание тонкослойной хроматографии. Начало 1940 -х годов – США (Манхэттенский проект создания атомной бомбы) – метод ионообменной хроматографии по разделению редкоземельных элементов, продуктов деления урана. 1952 г. – А. Мартин, Р. Синджем. Нобелевская премия. Разработка метода распределительной хроматографии (разделение смеси аминокислот). 1953 г. – А. Мартин, Э. Г. Джеймс. Разработка метода газожидкостной хроматографии. 1
 1956 -1957 года – М. Голей – Метод капиллярной хроматографии. 1959 г – Дж. Порат, Р. Флори – гель-проникающая хроматография. 1955 г – «Perkin – Elmer» США первый газовый хроматограф. Конец 1960 -х годов – Ш. Хорват. Йельский университет США – Разработал первый высокоэффективный жидкостный хроматограф (ВЭЖХ). В РАЗВИТИЕ СУЩЕСТВЕННЫЙ ВКЛАД ХРОМАТОГРАФИИ ВНЕСЛИ ТАКЖЕ СОВЕТСКИЕ (РОССИЙСКИЕ) УЧЕНЫЕ: А. А. Жуховитский, Н. М. Туркельтауб, Б. Г. Беленький, Г. Б. Темникова, В. А. Даванков, Л. Н. Москвин, А. И. Горшков, М. Ф. Гумеров, О. В. Родинков, Б. В. Иоффе, А. Г. Витенберг и др. 2
1956 -1957 года – М. Голей – Метод капиллярной хроматографии. 1959 г – Дж. Порат, Р. Флори – гель-проникающая хроматография. 1955 г – «Perkin – Elmer» США первый газовый хроматограф. Конец 1960 -х годов – Ш. Хорват. Йельский университет США – Разработал первый высокоэффективный жидкостный хроматограф (ВЭЖХ). В РАЗВИТИЕ СУЩЕСТВЕННЫЙ ВКЛАД ХРОМАТОГРАФИИ ВНЕСЛИ ТАКЖЕ СОВЕТСКИЕ (РОССИЙСКИЕ) УЧЕНЫЕ: А. А. Жуховитский, Н. М. Туркельтауб, Б. Г. Беленький, Г. Б. Темникова, В. А. Даванков, Л. Н. Москвин, А. И. Горшков, М. Ф. Гумеров, О. В. Родинков, Б. В. Иоффе, А. Г. Витенберг и др. 2
 ХРОМАТОГРАФИЯ a T=const а – доля адсорбированного вещества. С – концентрация вещества в исходной пробе C Изотерма адсорбции (Лэнгмюр) – скорость адсорбции; - скорость десорбции; - константа скорости адсорбции; - константа скорости десорбции; – степень наполняемости поглощаемым веществом адсорбента. 3
ХРОМАТОГРАФИЯ a T=const а – доля адсорбированного вещества. С – концентрация вещества в исходной пробе C Изотерма адсорбции (Лэнгмюр) – скорость адсорбции; - скорость десорбции; - константа скорости адсорбции; - константа скорости десорбции; – степень наполняемости поглощаемым веществом адсорбента. 3
 АДСОРБЕНТЫ 1. Полярные – силикагель, , алюмосиликаты и др. Неполярные – активированный уголь и др. 2. Органические – крахмал, целлюлоза, лактоза и др. Неорганические – , , , и др. ХРОМАТОГРАФИЧЕСКИЕ КОЛОНКИ l – до 20 м. d – от нескольких мм до 15 см. РАСПРЕДЕЛИТЕЛЬНАЯ – концентрация вещества неподвижной фазы; ХРОМАТОГРАФИЯ Xk 2 Xkn Xk 1 Коэффициент распределения: – концентрация вещества подвижной фазы. Xp Коэффициент разделения: - смещение зоны с компонентом; -смещение зоны с растворителем (подвижной фазы). 4
АДСОРБЕНТЫ 1. Полярные – силикагель, , алюмосиликаты и др. Неполярные – активированный уголь и др. 2. Органические – крахмал, целлюлоза, лактоза и др. Неорганические – , , , и др. ХРОМАТОГРАФИЧЕСКИЕ КОЛОНКИ l – до 20 м. d – от нескольких мм до 15 см. РАСПРЕДЕЛИТЕЛЬНАЯ – концентрация вещества неподвижной фазы; ХРОМАТОГРАФИЯ Xk 2 Xkn Xk 1 Коэффициент распределения: – концентрация вещества подвижной фазы. Xp Коэффициент разделения: - смещение зоны с компонентом; -смещение зоны с растворителем (подвижной фазы). 4
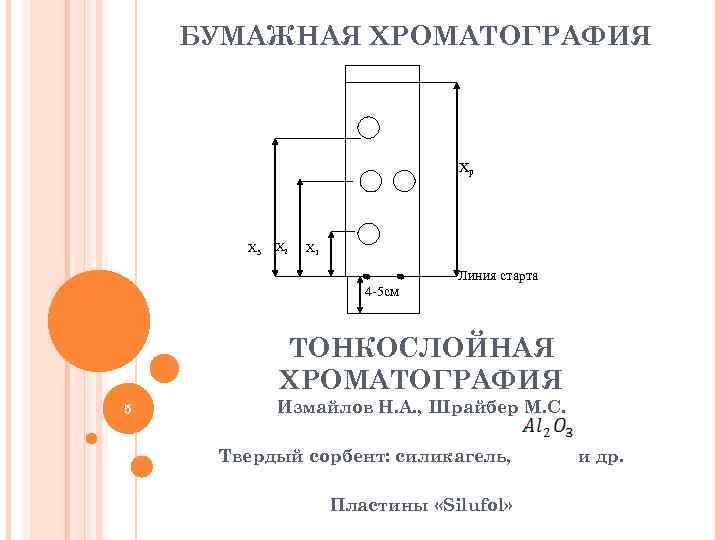 БУМАЖНАЯ ХРОМАТОГРАФИЯ Xp X 3 X 2 X 1 Линия старта 4 -5 см ТОНКОСЛОЙНАЯ ХРОМАТОГРАФИЯ 5 Измайлов Н. А. , Шрайбер М. С. Твердый сорбент: силикагель, Пластины «Silufol» и др.
БУМАЖНАЯ ХРОМАТОГРАФИЯ Xp X 3 X 2 X 1 Линия старта 4 -5 см ТОНКОСЛОЙНАЯ ХРОМАТОГРАФИЯ 5 Измайлов Н. А. , Шрайбер М. С. Твердый сорбент: силикагель, Пластины «Silufol» и др.
 АНАЛИЗ ХРОМАТОГРАММ Качественный анализ: по сопоставлению Rf со стандартом. Количественный анализ: -по площади пятен на хроматографических пластинах; -колориметрически; -по площади пиков на хроматограммах и др. a h ИОНООБМЕННАЯ ХРОМАТОГРАФИЯ 1. Катионный обмен: 2. Анионный обмен: 6
АНАЛИЗ ХРОМАТОГРАММ Качественный анализ: по сопоставлению Rf со стандартом. Количественный анализ: -по площади пятен на хроматографических пластинах; -колориметрически; -по площади пиков на хроматограммах и др. a h ИОНООБМЕННАЯ ХРОМАТОГРАФИЯ 1. Катионный обмен: 2. Анионный обмен: 6
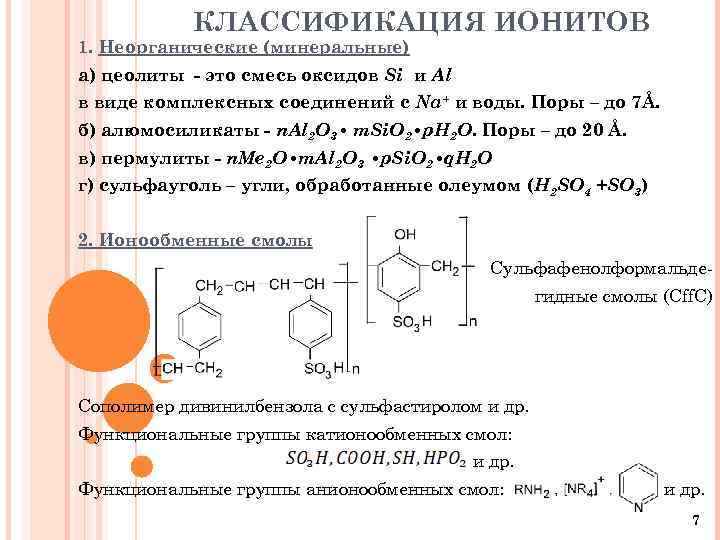 КЛАССИФИКАЦИЯ ИОНИТОВ 1. Неорганические (минеральные) а) цеолиты - это смесь оксидов Si и Al в виде комплексных соединений с Na+ и воды. Поры – до 7Å. б) алюмосиликаты - n. Al 2 O 3 • m. Si. O 2 • p. H 2 O. Поры – до 20 Å. в) пермулиты - n. Me 2 O • m. Al 2 O 3 • p. Si. O 2 • q. H 2 O г) сульфауголь – угли, обработанные олеумом (H 2 SO 4 +SO 3) 2. Ионообменные смолы Сульфафенолформальдегидные смолы (Cff. C) Сополимер дивинилбензола с сульфастиролом и др. Функциональные группы катионообменных смол: и др. Функциональные группы анионообменных смол: и др. 7
КЛАССИФИКАЦИЯ ИОНИТОВ 1. Неорганические (минеральные) а) цеолиты - это смесь оксидов Si и Al в виде комплексных соединений с Na+ и воды. Поры – до 7Å. б) алюмосиликаты - n. Al 2 O 3 • m. Si. O 2 • p. H 2 O. Поры – до 20 Å. в) пермулиты - n. Me 2 O • m. Al 2 O 3 • p. Si. O 2 • q. H 2 O г) сульфауголь – угли, обработанные олеумом (H 2 SO 4 +SO 3) 2. Ионообменные смолы Сульфафенолформальдегидные смолы (Cff. C) Сополимер дивинилбензола с сульфастиролом и др. Функциональные группы катионообменных смол: и др. Функциональные группы анионообменных смол: и др. 7
 ОБМЕННАЯ ЕМКОСТЬ ИОНИТОВ Весовая обменная емкость (ВОЕ): мг-экв/г Объемная обменная емкость (ООЕ): мг-экв/см 3 Полная обменная емкость – ПОЕ (СОЕ) Рабочая обменная емкость – РОЕ (ДОЕ) Влияние различных факторов на обменную емкость ионитов 1. Влияние р. Н - среды (по Na+): Ионит СФФС ВОЕ мг-экв/г р. Н 3 10 2 5, 2 2. Влияние природы катиона Ионит, сульфауголь ВОЕ мг-экв/г Катион Na+ Ca 2+ 3, 2 1 8
ОБМЕННАЯ ЕМКОСТЬ ИОНИТОВ Весовая обменная емкость (ВОЕ): мг-экв/г Объемная обменная емкость (ООЕ): мг-экв/см 3 Полная обменная емкость – ПОЕ (СОЕ) Рабочая обменная емкость – РОЕ (ДОЕ) Влияние различных факторов на обменную емкость ионитов 1. Влияние р. Н - среды (по Na+): Ионит СФФС ВОЕ мг-экв/г р. Н 3 10 2 5, 2 2. Влияние природы катиона Ионит, сульфауголь ВОЕ мг-экв/г Катион Na+ Ca 2+ 3, 2 1 8
 УСТРОЙСТВО И РАБОТА ИОНООБМЕННОГО ХРОМАТОГРАФА С ДАТЧИКОМ ПО ЭЛЕКТРОПРОВОДНОСТИ 9
УСТРОЙСТВО И РАБОТА ИОНООБМЕННОГО ХРОМАТОГРАФА С ДАТЧИКОМ ПО ЭЛЕКТРОПРОВОДНОСТИ 9
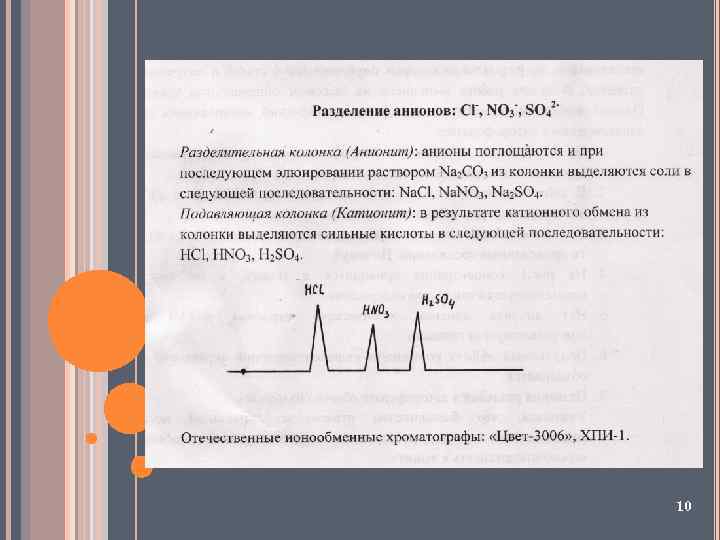 10
10
 ГАЗОВАЯ ГАЗОЖИДКОСТНАЯ ХРОМАТОГРАФИЯ 11
ГАЗОВАЯ ГАЗОЖИДКОСТНАЯ ХРОМАТОГРАФИЯ 11
 ГЕЛЬ – ПРОНИКАЮЩАЯ ХРОМАТОГРАФИЯ 12
ГЕЛЬ – ПРОНИКАЮЩАЯ ХРОМАТОГРАФИЯ 12
 УСТРОЙСТВО И РАБОТА ГЕЛЬ ПРОНИКАЮЩЕГО ХРОМАТОГРАФА 13
УСТРОЙСТВО И РАБОТА ГЕЛЬ ПРОНИКАЮЩЕГО ХРОМАТОГРАФА 13
 МЕТОД ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА (ЯМР) 1946 г. – Ф. Блох, Э. Персил (США) Некоторые ядра, обладающие магнитным моментом (µ): 1 Н, 10 F, 31 Р, 13 С, 15 N и др. Ядро 1 Н имеет 2 квантовых магнитных числа: 14
МЕТОД ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА (ЯМР) 1946 г. – Ф. Блох, Э. Персил (США) Некоторые ядра, обладающие магнитным моментом (µ): 1 Н, 10 F, 31 Р, 13 С, 15 N и др. Ядро 1 Н имеет 2 квантовых магнитных числа: 14
 При переходе из одного энергетического состояния в другое происходит изменение внутренней энергии ядра: 1 2 4 3 5 7 6 8 ∆E – эрг; h - const Планка; 6, 6∙ 10 -27 эрг∙с; Н 0=14100 Гс; γ – гидромагнитное отношение, Гс-1∙с-1; µ - эрг∙Гс-1; J – силовое квантовое число (для 1 Н=1/2); µк=1, 41∙ 10 -23 эрг∙Гс-1. 15
При переходе из одного энергетического состояния в другое происходит изменение внутренней энергии ядра: 1 2 4 3 5 7 6 8 ∆E – эрг; h - const Планка; 6, 6∙ 10 -27 эрг∙с; Н 0=14100 Гс; γ – гидромагнитное отношение, Гс-1∙с-1; µ - эрг∙Гс-1; J – силовое квантовое число (для 1 Н=1/2); µк=1, 41∙ 10 -23 эрг∙Гс-1. 15
 ПРИРОДА ВОЗНИКНОВЕНИЯ ЯВЛЕНИЯ ЯМР 16
ПРИРОДА ВОЗНИКНОВЕНИЯ ЯВЛЕНИЯ ЯМР 16
 Вещества, обладающие экранированием ядер: наибольшим электронным Si(CH 3)4 – тетраметилсилон (ТМС) (CH 3)3 Si-O- Si(CH 3)3 – гексаметилдисилоксон (ГМДС) Смещение сигналов относительно стандарта называется химическим сдвигом НТМС – НС В относительных единицах: 17
Вещества, обладающие экранированием ядер: наибольшим электронным Si(CH 3)4 – тетраметилсилон (ТМС) (CH 3)3 Si-O- Si(CH 3)3 – гексаметилдисилоксон (ГМДС) Смещение сигналов относительно стандарта называется химическим сдвигом НТМС – НС В относительных единицах: 17
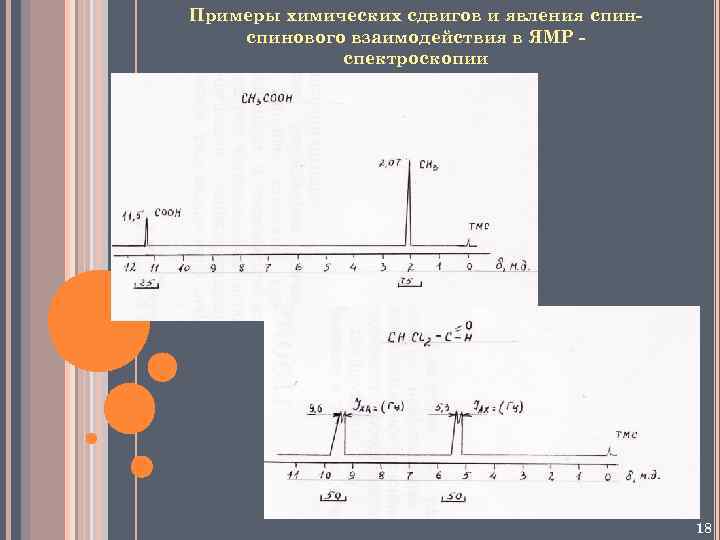 Примеры химических сдвигов и явления спинового взаимодействия в ЯМР спектроскопии 18
Примеры химических сдвигов и явления спинового взаимодействия в ЯМР спектроскопии 18
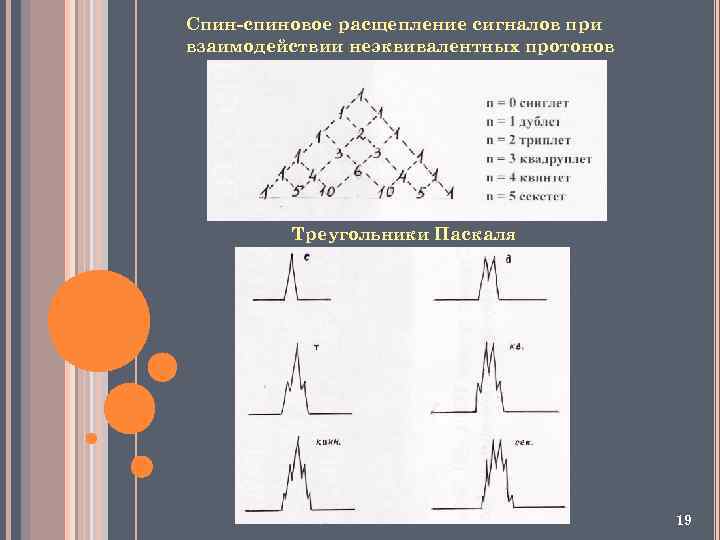 Спин-спиновое расщепление сигналов при взаимодействии неэквивалентных протонов Треугольники Паскаля 19
Спин-спиновое расщепление сигналов при взаимодействии неэквивалентных протонов Треугольники Паскаля 19
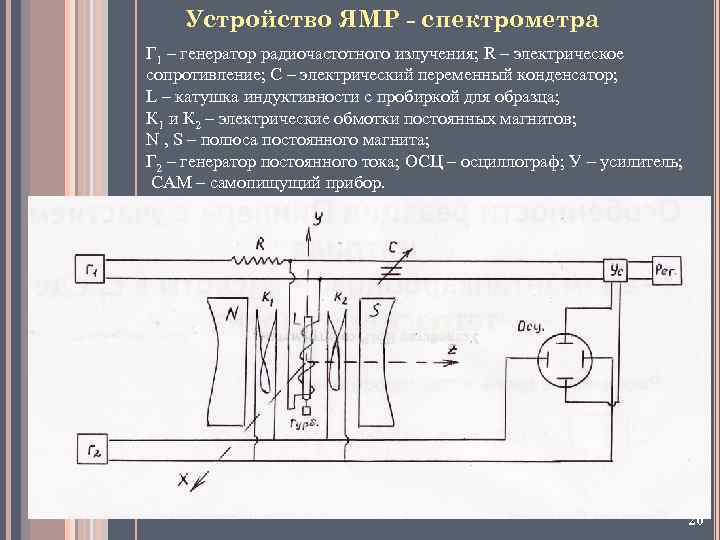 Устройство ЯМР - спектрометра Г 1 – генератор радиочастотного излучения; R – электрическое сопротивление; C – электрический переменный конденсатор; L – катушка индуктивности с пробиркой для образца; К 1 и К 2 – электрические обмотки постоянных магнитов; N , S – полюса постоянного магнита; Г 2 – генератор постоянного тока; ОСЦ – осциллограф; У – усилитель; САМ – самопищущий прибор. 20
Устройство ЯМР - спектрометра Г 1 – генератор радиочастотного излучения; R – электрическое сопротивление; C – электрический переменный конденсатор; L – катушка индуктивности с пробиркой для образца; К 1 и К 2 – электрические обмотки постоянных магнитов; N , S – полюса постоянного магнита; Г 2 – генератор постоянного тока; ОСЦ – осциллограф; У – усилитель; САМ – самопищущий прибор. 20
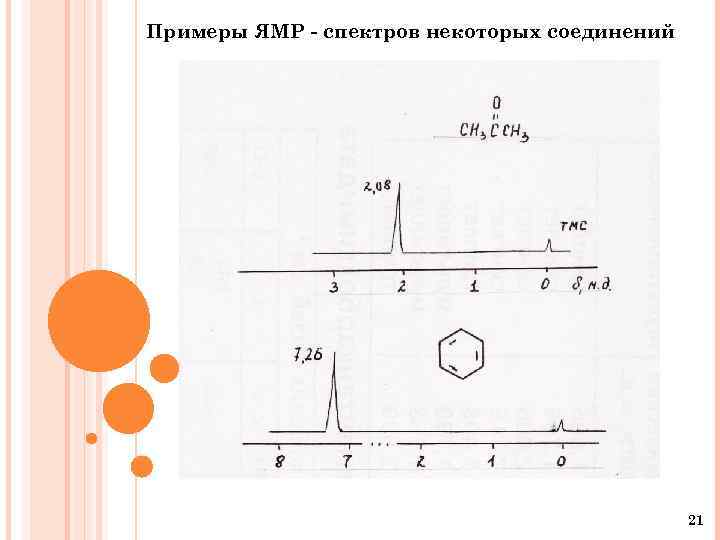 Примеры ЯМР - спектров некоторых соединений 21
Примеры ЯМР - спектров некоторых соединений 21
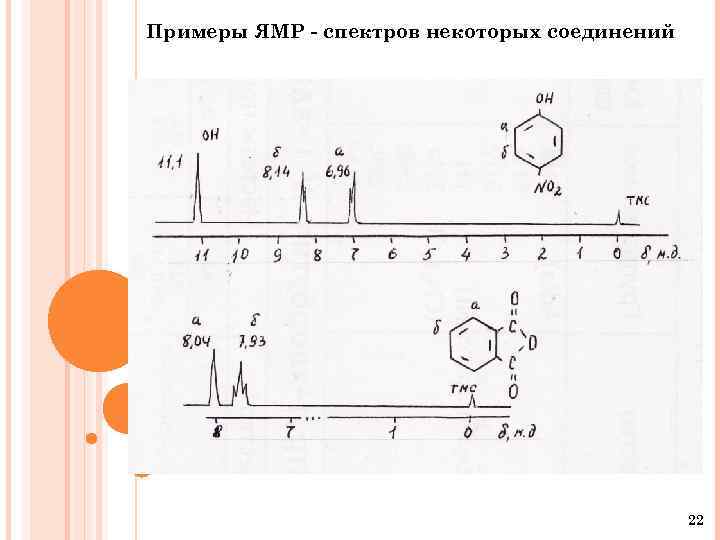 Примеры ЯМР - спектров некоторых соединений 22
Примеры ЯМР - спектров некоторых соединений 22
 АНАЛИЗА Термостойкость – это химическая устойчивость веществ при повышенных температурах. Методы расчета термодеструкции: кинетических параметров - средняя скорость термодеструкции ϕ 23
АНАЛИЗА Термостойкость – это химическая устойчивость веществ при повышенных температурах. Методы расчета термодеструкции: кинетических параметров - средняя скорость термодеструкции ϕ 23
 УРАВНЕНИЕ АРРЕНИУСА k – константа скорости реакции lnk 0 – предэкспонента Е – энергия активации к. Дж/моль R – газовая постоянная, 8, 314 Дж/моль∙K lnk φ 1/T 24
УРАВНЕНИЕ АРРЕНИУСА k – константа скорости реакции lnk 0 – предэкспонента Е – энергия активации к. Дж/моль R – газовая постоянная, 8, 314 Дж/моль∙K lnk φ 1/T 24
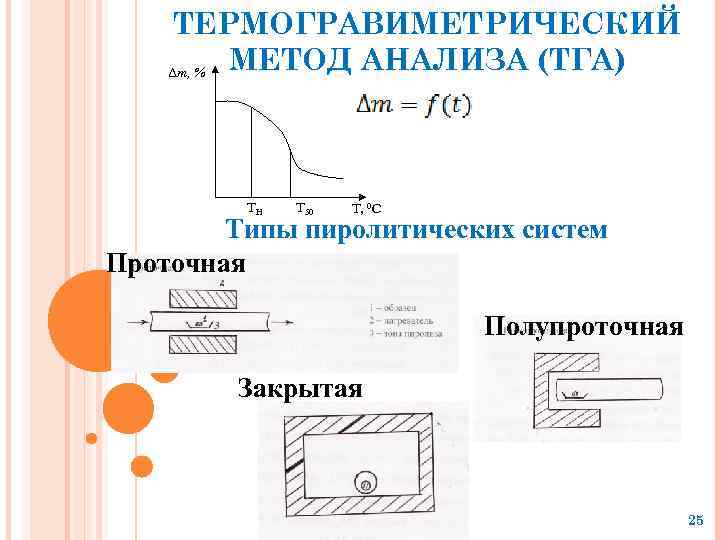 ТЕРМОГРАВИМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА (ТГА) ∆m, % TH T 50 T, 0 C Типы пиролитических систем Проточная Полупроточная Закрытая 25
ТЕРМОГРАВИМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА (ТГА) ∆m, % TH T 50 T, 0 C Типы пиролитических систем Проточная Полупроточная Закрытая 25
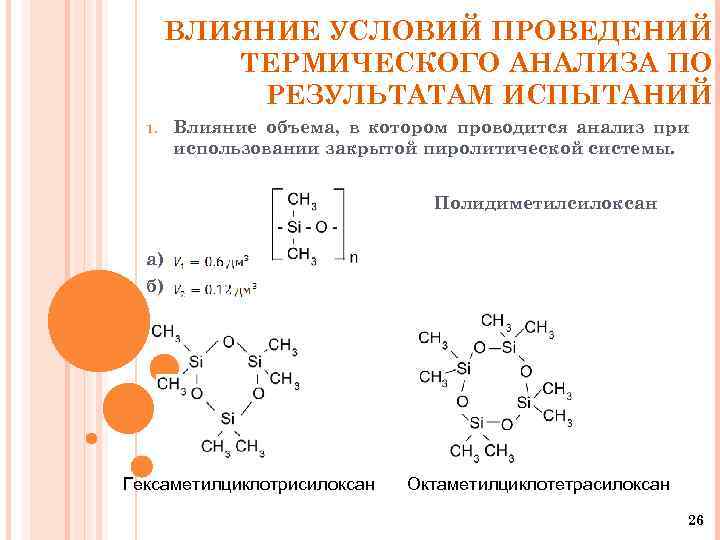 ВЛИЯНИЕ УСЛОВИЙ ПРОВЕДЕНИЙ ТЕРМИЧЕСКОГО АНАЛИЗА ПО РЕЗУЛЬТАТАМ ИСПЫТАНИЙ 1. Влияние объема, в котором проводится анализ при использовании закрытой пиролитической системы. Полидиметилсилоксан а) б) Гексаметилциклотрисилоксан Октаметилциклотетрасилоксан 26
ВЛИЯНИЕ УСЛОВИЙ ПРОВЕДЕНИЙ ТЕРМИЧЕСКОГО АНАЛИЗА ПО РЕЗУЛЬТАТАМ ИСПЫТАНИЙ 1. Влияние объема, в котором проводится анализ при использовании закрытой пиролитической системы. Полидиметилсилоксан а) б) Гексаметилциклотрисилоксан Октаметилциклотетрасилоксан 26
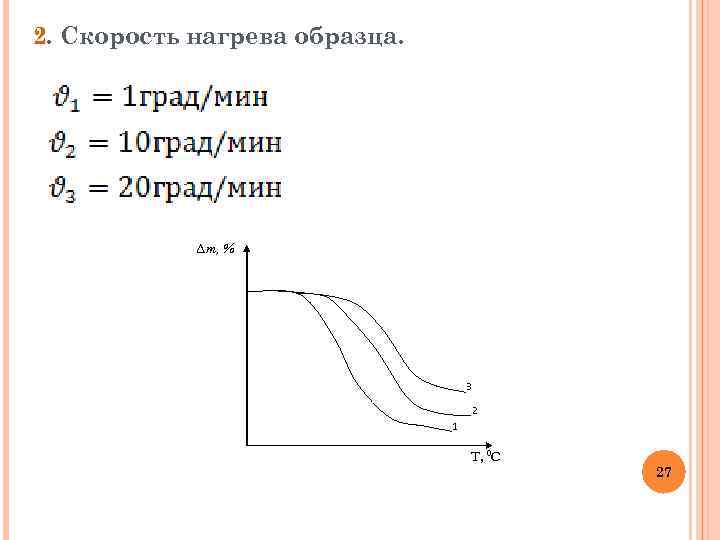 2. Скорость нагрева образца. ∆m, % 3 2 1 T, 0 C 27
2. Скорость нагрева образца. ∆m, % 3 2 1 T, 0 C 27
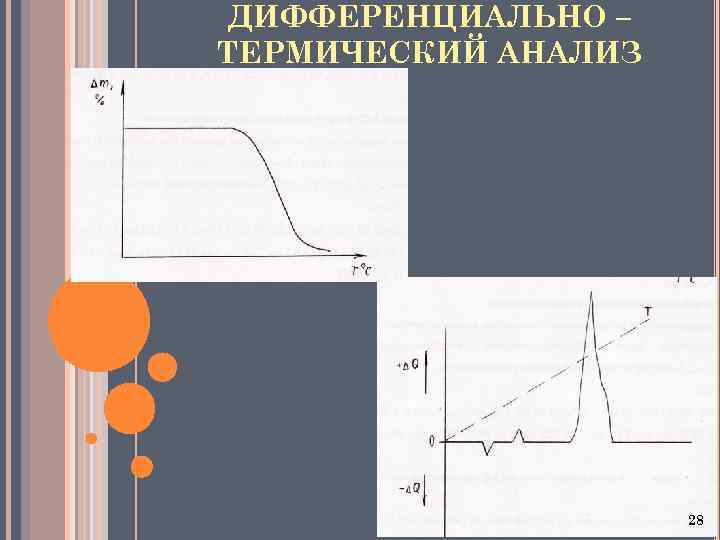 ДИФФЕРЕНЦИАЛЬНО – ТЕРМИЧЕСКИЙ АНАЛИЗ 28
ДИФФЕРЕНЦИАЛЬНО – ТЕРМИЧЕСКИЙ АНАЛИЗ 28
 РАДИОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА Наряду с α- и β-распадом, часто присутствует γ-излучение (более мощное) с энергией от 0, 005 до 8 Мэ. В (λ=0, 016÷ 0, 23Å) Примеры γ - спектров: Радиоактивное Fe (1, 10; 1, 29 Мэ. В) радиоактивного Со (1, 17; 1, 33 Мэ. В), поэтому эти элементы разделять ионообменной хроматографии). трудно отличить (например от методом Или Sb (0, 564 Мэ. В) и As (0, 555 Мэ. В) разделяют методом экстракции. 29
РАДИОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА Наряду с α- и β-распадом, часто присутствует γ-излучение (более мощное) с энергией от 0, 005 до 8 Мэ. В (λ=0, 016÷ 0, 23Å) Примеры γ - спектров: Радиоактивное Fe (1, 10; 1, 29 Мэ. В) радиоактивного Со (1, 17; 1, 33 Мэ. В), поэтому эти элементы разделять ионообменной хроматографии). трудно отличить (например от методом Или Sb (0, 564 Мэ. В) и As (0, 555 Мэ. В) разделяют методом экстракции. 29
 РАЗБАВЛЕНИЯ I 0– активность в исходном состоянии; I 1– активность после добавления изотопа; m – масса пробы. Блок – схема прибора, основанного на способности отражать β - лучи 1 -образец; 2 -радиоактивный препарат; 3 -защитная оболочка; 4 фильтр; 5 -счетчик β – частиц. 30
РАЗБАВЛЕНИЯ I 0– активность в исходном состоянии; I 1– активность после добавления изотопа; m – масса пробы. Блок – схема прибора, основанного на способности отражать β - лучи 1 -образец; 2 -радиоактивный препарат; 3 -защитная оболочка; 4 фильтр; 5 -счетчик β – частиц. 30


