Хроматографический метод исследования






































































слайды хроматграфия копия.ppt
- Количество слайдов: 96
 Хроматографический метод исследования План 1. Теоретические основы метода. 2. Классификация хроматографических методов анализа. 3. Хроматограммы. Оборудование и Приборы для проведения хроматографии. 4. Характеристика основных видов хроматографии.
Хроматографический метод исследования План 1. Теоретические основы метода. 2. Классификация хроматографических методов анализа. 3. Хроматограммы. Оборудование и Приборы для проведения хроматографии. 4. Характеристика основных видов хроматографии.
 ВОПРОС 1. Теоретические основы метода.
ВОПРОС 1. Теоретические основы метода.
 Одна из важных задач современной химии – надежный и точный анализ органических веществ, часто близких по строению и свойствам. Без этого невозможно проведение химических, биохимических и медицинских исследований, на этом в значительной степени базируются экологические методы анализа окружающей среды, криминалистическая экспертиза, а также химическая, нефтяная, газовая, пищевая, медицинская отрасли промышленности и многие другие отрасли народного хозяйства.
Одна из важных задач современной химии – надежный и точный анализ органических веществ, часто близких по строению и свойствам. Без этого невозможно проведение химических, биохимических и медицинских исследований, на этом в значительной степени базируются экологические методы анализа окружающей среды, криминалистическая экспертиза, а также химическая, нефтяная, газовая, пищевая, медицинская отрасли промышленности и многие другие отрасли народного хозяйства.
 Основу хроматографического (от греч. "хромос" - цвет) метода заложил русский химик М. С. Цвет (1903) ". . . при фильтрации смешанного раствора через столб адсорбента пигменты. . . расслаиваются в виде отдельных, различно окрашенных зон. Подобно световым лучам в спектре, различные компоненты сложного пигмента закономерно распределяются друг за другом в столбе адсорбента и становятся доступными качественному и количественному определению. Такой расцвеченный препарат я назвал хроматограммой, а соответствующий метод анализа - хроматографическим методом" М. С. Цвет
Основу хроматографического (от греч. "хромос" - цвет) метода заложил русский химик М. С. Цвет (1903) ". . . при фильтрации смешанного раствора через столб адсорбента пигменты. . . расслаиваются в виде отдельных, различно окрашенных зон. Подобно световым лучам в спектре, различные компоненты сложного пигмента закономерно распределяются друг за другом в столбе адсорбента и становятся доступными качественному и количественному определению. Такой расцвеченный препарат я назвал хроматограммой, а соответствующий метод анализа - хроматографическим методом" М. С. Цвет
 Хроматография – физико химический метод, который используется для разделения и последующей идентификации веществ аналитические цели препаративные цели Служит для идентификации и количественного определения органических и неорганических веществ
Хроматография – физико химический метод, который используется для разделения и последующей идентификации веществ аналитические цели препаративные цели Служит для идентификации и количественного определения органических и неорганических веществ
 Из истории хроматографии День рождения хроматографии – 21 марта 1903 г. Доклад М. С. Цвета «О новой категории адсорбционных явлений и о применении их к биохимическому анализу» Свой метод М. С. Цвет назвал – «хроматография» (запись цвета) Ричард Кун (институт фундаментальной медицины г. Гейдельберг) (1938 г. Нобелевская премия по химии за предложенную Цветом адсорбционную хроматографию каратиноидов и витаминов): Альфред Винтерштайн (1915 г. Нобелевская премия по химии за исследования хлорофиллов) Арчер Портер Мартин, Ричард Лоуренс Миллингтон Синдж (1938 г. первый противоточный экстрактор с использованием воды и хлороформа для разделения олигопептидов; 1940 г. Использование жидкость жидкостной хроматографии для разделения аминокислот; 19 ноября 1941 г. Статья «Новая форма использования двух жидких фаз для хроматографии» в «Biochemical journal» ; 1952 г. Нобелевская премия за открытие распределительной хроматографии Арчер Портер Мартин, Энтони Траффорд Джеймс (50 е годы первый газовый хроматограф) Измаилов, Шрайбер (1938 г. Первые работы по тонкослойной хроматографии) Шталь (1956 г. Использование тонкослойной хроматографии как аналитического метода)
Из истории хроматографии День рождения хроматографии – 21 марта 1903 г. Доклад М. С. Цвета «О новой категории адсорбционных явлений и о применении их к биохимическому анализу» Свой метод М. С. Цвет назвал – «хроматография» (запись цвета) Ричард Кун (институт фундаментальной медицины г. Гейдельберг) (1938 г. Нобелевская премия по химии за предложенную Цветом адсорбционную хроматографию каратиноидов и витаминов): Альфред Винтерштайн (1915 г. Нобелевская премия по химии за исследования хлорофиллов) Арчер Портер Мартин, Ричард Лоуренс Миллингтон Синдж (1938 г. первый противоточный экстрактор с использованием воды и хлороформа для разделения олигопептидов; 1940 г. Использование жидкость жидкостной хроматографии для разделения аминокислот; 19 ноября 1941 г. Статья «Новая форма использования двух жидких фаз для хроматографии» в «Biochemical journal» ; 1952 г. Нобелевская премия за открытие распределительной хроматографии Арчер Портер Мартин, Энтони Траффорд Джеймс (50 е годы первый газовый хроматограф) Измаилов, Шрайбер (1938 г. Первые работы по тонкослойной хроматографии) Шталь (1956 г. Использование тонкослойной хроматографии как аналитического метода)
 Михаил Семёнович Цвет (1872— 1919)
Михаил Семёнович Цвет (1872— 1919)
 Разделение Цвет проводил в колонке, показанной на рис. 1. Смесь веществ А, Б и В – природных пигментов, первоначально находящихся в зоне е, – разделяется приливании соответствующего растворителя Д (элюент) на отдельные зоны. Рис. 1. Хроматографическое разделение пигментов хлорофилла М. C. Цветом: а – адсорбент; б – колонка; в – приемник; г – делительная воронка; д – вата. Смесь веществ А, Б и В, сначала находящихся в зоне е, разделяется при элюировании растворителем Д (элюент) на отдельные зоны, движущиеся с разными скоростями к выходу из колонки
Разделение Цвет проводил в колонке, показанной на рис. 1. Смесь веществ А, Б и В – природных пигментов, первоначально находящихся в зоне е, – разделяется приливании соответствующего растворителя Д (элюент) на отдельные зоны. Рис. 1. Хроматографическое разделение пигментов хлорофилла М. C. Цветом: а – адсорбент; б – колонка; в – приемник; г – делительная воронка; д – вата. Смесь веществ А, Б и В, сначала находящихся в зоне е, разделяется при элюировании растворителем Д (элюент) на отдельные зоны, движущиеся с разными скоростями к выходу из колонки
 Хроматография - метод разделения, анализа и физико- химического исследования веществ, основанный на распределении компонентов между двумя несмешивающимися фазами - подвижной и неподвижной. *Неподвижная (стационарная) фаза (НФ) - представляет собой сорбент с сильно развитой поверхностью раздела. В качестве подвижной фазы используется твердое вещество или пленка жидкости, нанесенная на твердое вещество. *Подвижная фаза (ПФ) - поток газа (пара) или жидкости, перемещающийся (протекающий) через неподвижную фазу (иногда под давлением). В качестве подвижной фазы используется газ или жидкость.
Хроматография - метод разделения, анализа и физико- химического исследования веществ, основанный на распределении компонентов между двумя несмешивающимися фазами - подвижной и неподвижной. *Неподвижная (стационарная) фаза (НФ) - представляет собой сорбент с сильно развитой поверхностью раздела. В качестве подвижной фазы используется твердое вещество или пленка жидкости, нанесенная на твердое вещество. *Подвижная фаза (ПФ) - поток газа (пара) или жидкости, перемещающийся (протекающий) через неподвижную фазу (иногда под давлением). В качестве подвижной фазы используется газ или жидкость.
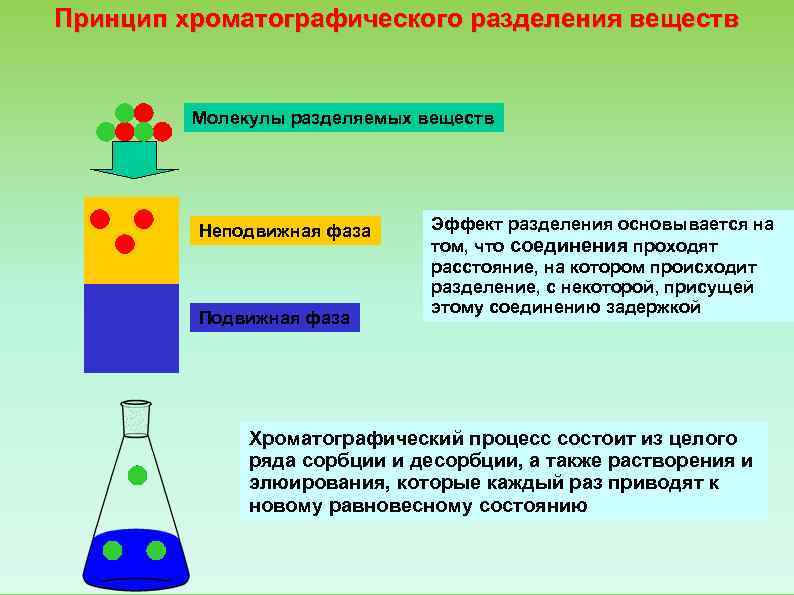
 Принцип хроматографического разделения веществ Молекулы разделяемых веществ Неподвижная фаза Эффект разделения основывается на том, что соединения проходят расстояние, на котором происходит разделение, с некоторой, присущей этому соединению задержкой Подвижная фаза Хроматографический процесс состоит из целого ряда сорбции и десорбции, а также растворения и элюирования, которые каждый раз приводят к новому равновесному состоянию
Принцип хроматографического разделения веществ Молекулы разделяемых веществ Неподвижная фаза Эффект разделения основывается на том, что соединения проходят расстояние, на котором происходит разделение, с некоторой, присущей этому соединению задержкой Подвижная фаза Хроматографический процесс состоит из целого ряда сорбции и десорбции, а также растворения и элюирования, которые каждый раз приводят к новому равновесному состоянию
 Образец смеси веществ вводят в слой неподвижной фазы, а затем различные соединения, входящие в состав смеси, вместе с подвижной фазой (элюент) двигаются вдоль слоя, подгоняемые этой фазой. Подвижная фаза, все время продвигается, нарушая равновесие. Скорость перемещения зависит от величины взаимодействия (сродство) компонентов в неподвижной и подвижной фазах: чем лучше то или иное вещество сорбируется или растворяется в неподвижной фазе, тем меньше скорость его движения, и, наоборот, чем меньше сорбируется соединение тем скорость перемещения больше.
Образец смеси веществ вводят в слой неподвижной фазы, а затем различные соединения, входящие в состав смеси, вместе с подвижной фазой (элюент) двигаются вдоль слоя, подгоняемые этой фазой. Подвижная фаза, все время продвигается, нарушая равновесие. Скорость перемещения зависит от величины взаимодействия (сродство) компонентов в неподвижной и подвижной фазах: чем лучше то или иное вещество сорбируется или растворяется в неподвижной фазе, тем меньше скорость его движения, и, наоборот, чем меньше сорбируется соединение тем скорость перемещения больше.
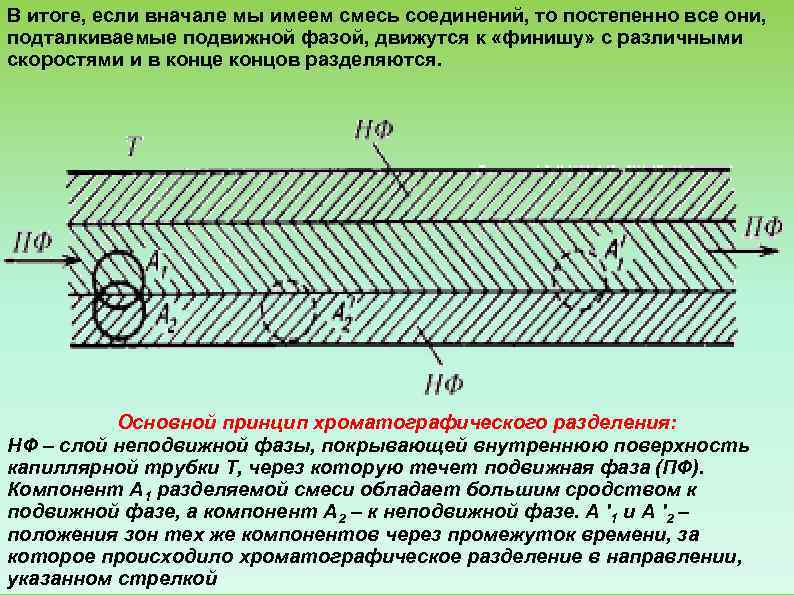
 В итоге, если вначале мы имеем смесь соединений, то постепенно все они, подталкиваемые подвижной фазой, движутся к «финишу» с различными скоростями и в конце концов разделяются. Основной принцип хроматографического разделения: НФ – слой неподвижной фазы, покрывающей внутреннюю поверхность капиллярной трубки Т, через которую течет подвижная фаза (ПФ). Компонент А 1 разделяемой смеси обладает большим сродством к подвижной фазе, а компонент А 2 – к неподвижной фазе. А '1 и А '2 – положения зон тех же компонентов через промежуток времени, за которое происходило хроматографическое разделение в направлении, указанном стрелкой
В итоге, если вначале мы имеем смесь соединений, то постепенно все они, подталкиваемые подвижной фазой, движутся к «финишу» с различными скоростями и в конце концов разделяются. Основной принцип хроматографического разделения: НФ – слой неподвижной фазы, покрывающей внутреннюю поверхность капиллярной трубки Т, через которую течет подвижная фаза (ПФ). Компонент А 1 разделяемой смеси обладает большим сродством к подвижной фазе, а компонент А 2 – к неподвижной фазе. А '1 и А '2 – положения зон тех же компонентов через промежуток времени, за которое происходило хроматографическое разделение в направлении, указанном стрелкой
 После разделения необходимо идентифицировать все компоненты и оценить их количественно. Такова общая схема хроматографии. Следует отметить, что этот метод позволяет в течение нескольких минут определить содержание десятков и сотен различных соединений в смеси, причем даже в ничтожных, «следовых» количествах.
После разделения необходимо идентифицировать все компоненты и оценить их количественно. Такова общая схема хроматографии. Следует отметить, что этот метод позволяет в течение нескольких минут определить содержание десятков и сотен различных соединений в смеси, причем даже в ничтожных, «следовых» количествах.
 По расположению фаз хроматографические системы подразделяют на две группы: 1. плоскостные 2. колоночные. Колоночные, в свою очередь, разделяются на : а) насадочные заполненные зернистым твердым материалом (мелкие шарики); б) капиллярные внутренние стенки которых покрыты пленкой неподвижной жидкости или слоем твердого адсорбента (поглотителем). Взаимодействие между разделяемым веществом и фазами хроматографической системы может осуществляться или на поверхности фазы, или в объеме. В первом случае хроматография называется адсорбционной, во втором – распределительной.
По расположению фаз хроматографические системы подразделяют на две группы: 1. плоскостные 2. колоночные. Колоночные, в свою очередь, разделяются на : а) насадочные заполненные зернистым твердым материалом (мелкие шарики); б) капиллярные внутренние стенки которых покрыты пленкой неподвижной жидкости или слоем твердого адсорбента (поглотителем). Взаимодействие между разделяемым веществом и фазами хроматографической системы может осуществляться или на поверхности фазы, или в объеме. В первом случае хроматография называется адсорбционной, во втором – распределительной.
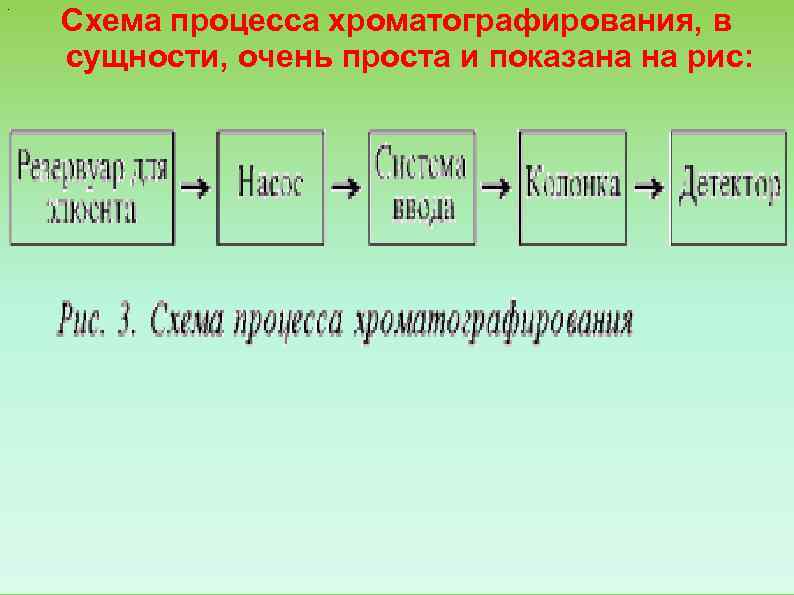
 . Схема процесса хроматографирования, в сущности, очень проста и показана на рис:
. Схема процесса хроматографирования, в сущности, очень проста и показана на рис:
 Наличие как минимум двух фаз и их относительное движение, то есть динамика процесса, неотъемлемые признаки хроматографии. В хроматографии используются методы разделения, в которых происходит изменение фазовых равновесий: дистилляция, кристаллизация, экстракция и адсорбция. Молекулы веществ, которые образуют смесь, переходят через границу раздела фаз, стремясь к такому распределению, при котором в каждой фаз устанавливается постоянная равновесная концентрация. Практически любую смесь, даже веществ с очень близкими свойствами, можно разделить при соответствующем выборе хроматографического метода.
Наличие как минимум двух фаз и их относительное движение, то есть динамика процесса, неотъемлемые признаки хроматографии. В хроматографии используются методы разделения, в которых происходит изменение фазовых равновесий: дистилляция, кристаллизация, экстракция и адсорбция. Молекулы веществ, которые образуют смесь, переходят через границу раздела фаз, стремясь к такому распределению, при котором в каждой фаз устанавливается постоянная равновесная концентрация. Практически любую смесь, даже веществ с очень близкими свойствами, можно разделить при соответствующем выборе хроматографического метода.
 В основе хроматографии лежит явление сорбции. Сорбция – это процесс поглощения газов, паров или растворённых веществ жидкими или твёрдыми растворителями. Виды сорбции: 1. Абсорбция – поглощение всем объёмом жидкого поглотителя; 2. Адсорбция – поглощение поверхностью поглотителя (на границе раздела фаз) 3. Капиллярная конденсация – образование жидкой фазы в порах и капиллярах твёрдого поглатителя.
В основе хроматографии лежит явление сорбции. Сорбция – это процесс поглощения газов, паров или растворённых веществ жидкими или твёрдыми растворителями. Виды сорбции: 1. Абсорбция – поглощение всем объёмом жидкого поглотителя; 2. Адсорбция – поглощение поверхностью поглотителя (на границе раздела фаз) 3. Капиллярная конденсация – образование жидкой фазы в порах и капиллярах твёрдого поглатителя.
 Вдоль хроматографической системы движутся только те молекулы, которые находятся в подвижной фазе. Вещество, поглощающее при сорбции, называют сорбентом . Вещество, поглощающееся при сорбции, называют сорбатом. Сорбция может протекать как в статических так и в динамических условиях. Статический вариант используют, если она протекает быстро и количественно.
Вдоль хроматографической системы движутся только те молекулы, которые находятся в подвижной фазе. Вещество, поглощающее при сорбции, называют сорбентом . Вещество, поглощающееся при сорбции, называют сорбатом. Сорбция может протекать как в статических так и в динамических условиях. Статический вариант используют, если она протекает быстро и количественно.
 Требования к неподвижной фазе: 1. Физически сорбировать вещество, находящееся в подвижной фазе. 2. Химически сорбировать вещество, находящееся в подвижной фазе. 3. Растворять разделяемые вещества. 4. Иметь пористую структуру и поэтому удерживать одни вещества и не удерживать другие, в зависимости от их размера и формы.
Требования к неподвижной фазе: 1. Физически сорбировать вещество, находящееся в подвижной фазе. 2. Химически сорбировать вещество, находящееся в подвижной фазе. 3. Растворять разделяемые вещества. 4. Иметь пористую структуру и поэтому удерживать одни вещества и не удерживать другие, в зависимости от их размера и формы.
 Основные достоинства хроматографического анализа: 1. экспрессность; 2. высокая эффективность; 3. возможность автоматизации и получение объективной информации; 4. сочетание с другими физико химическими методами; 5. широкий интервал концентраций соединений; 6. возможность изучения физико химических свойств соединений; 7. осуществление проведения качественного и количественного анализа; 8. применение для контроля и автоматического регулирования технологических процессов.
Основные достоинства хроматографического анализа: 1. экспрессность; 2. высокая эффективность; 3. возможность автоматизации и получение объективной информации; 4. сочетание с другими физико химическими методами; 5. широкий интервал концентраций соединений; 6. возможность изучения физико химических свойств соединений; 7. осуществление проведения качественного и количественного анализа; 8. применение для контроля и автоматического регулирования технологических процессов.
 ВОПРОС 2. КЛАССИФИКАЦИЯ ХРОМАТОГРАФИЧЕСКИХ МЕТОДОВ АНАЛИЗА
ВОПРОС 2. КЛАССИФИКАЦИЯ ХРОМАТОГРАФИЧЕСКИХ МЕТОДОВ АНАЛИЗА
 I. По агрегатному состоянию фаз 1. По агрегатному состоянию подвижной фазы: а) Газовая; б) Жидкостная. 2. По агрегатному состоянию подвижной фазы: а) Твёрдая; б) Жидкая. Таким образом, возможны следующие сочетания: 1. ГЖХ (газожидкостная хроматография – распределительная); 2. ГТХ (газо твердофазная – газо адсорбционная); 3. ЖЖХ (жидкостная – распеределительная); 4. ЖТХ (жидко твёрдофазная)
I. По агрегатному состоянию фаз 1. По агрегатному состоянию подвижной фазы: а) Газовая; б) Жидкостная. 2. По агрегатному состоянию подвижной фазы: а) Твёрдая; б) Жидкая. Таким образом, возможны следующие сочетания: 1. ГЖХ (газожидкостная хроматография – распределительная); 2. ГТХ (газо твердофазная – газо адсорбционная); 3. ЖЖХ (жидкостная – распеределительная); 4. ЖТХ (жидко твёрдофазная)
 II. По механизму распределения веществ: 1. Адсорбционная х я. (когда неподвижной фазой является твёрдое вещество способное адсорбировать определяемое вещество) 2. Распределительная х я. (если неподвижной фазой является жидкость и анализируемое вещество способно в ней растворяться, то оно распределяется между подвижной и неподвижной фазой); 3. Ионно обменная х я. (в основе лежит процесс ионного обмена); 4. Реакционная х я. (идёт химическая реакция между компонентами смеси и неподвижной фазой). 5. Молекулярно ситовая или гельпроникающая х я. (разделение происходит по размерам молекул)
II. По механизму распределения веществ: 1. Адсорбционная х я. (когда неподвижной фазой является твёрдое вещество способное адсорбировать определяемое вещество) 2. Распределительная х я. (если неподвижной фазой является жидкость и анализируемое вещество способно в ней растворяться, то оно распределяется между подвижной и неподвижной фазой); 3. Ионно обменная х я. (в основе лежит процесс ионного обмена); 4. Реакционная х я. (идёт химическая реакция между компонентами смеси и неподвижной фазой). 5. Молекулярно ситовая или гельпроникающая х я. (разделение происходит по размерам молекул)
 III. По способу размещения неподвижной фазы: 1. Колоночная (при этом неподвижная фаза помещается в трубку из стекла или металла, т. е. в колонку): набивные колонки, капиллярные колонки; 2. Плоскостная (неподвижная фаза наносится тонким слоем на стеклянную пластинку): тонкослойная (ТСХ), бумажная (неподвижной фазой удерживается на специально обработанной хроматографической бумаге, которая служит носителем).
III. По способу размещения неподвижной фазы: 1. Колоночная (при этом неподвижная фаза помещается в трубку из стекла или металла, т. е. в колонку): набивные колонки, капиллярные колонки; 2. Плоскостная (неподвижная фаза наносится тонким слоем на стеклянную пластинку): тонкослойная (ТСХ), бумажная (неподвижной фазой удерживается на специально обработанной хроматографической бумаге, которая служит носителем).
 IV. По способу проведения анализа: 1. Фронтальная (анализируемую смесь непрерывно вводят в хроматографическую колонку); 2. Вытеснительная (после введения пробы и предварительного разделения слабоактивным элюентом состав элюента меняется. Новый элюент вытесняет компоненты, которые выходят из колонки в порядке их взаимодействия с неподвижной фазой); 3. Элюентная (пробу вводят в поток подвижной фазы. Состав подвижной фазы постоянен. В процессе движения по колонке компоненты смеси разделяются на зоны, которые поочередно выходят из колонки).
IV. По способу проведения анализа: 1. Фронтальная (анализируемую смесь непрерывно вводят в хроматографическую колонку); 2. Вытеснительная (после введения пробы и предварительного разделения слабоактивным элюентом состав элюента меняется. Новый элюент вытесняет компоненты, которые выходят из колонки в порядке их взаимодействия с неподвижной фазой); 3. Элюентная (пробу вводят в поток подвижной фазы. Состав подвижной фазы постоянен. В процессе движения по колонке компоненты смеси разделяются на зоны, которые поочередно выходят из колонки).
 Современные хроматографические методы: капиллярная газовая хроматография (КГХ), • высокоэффективная жидкостная хроматография (ВЭЖХ), • высокоэффективная тонкослойная хроматография (ВЭТСХ), • высокоэффективная ионная хроматография (ВЭИХ), • сверхкритическая флюидная хроматография (ВЭИХ), • капиллярный электрофорез (КЭ)
Современные хроматографические методы: капиллярная газовая хроматография (КГХ), • высокоэффективная жидкостная хроматография (ВЭЖХ), • высокоэффективная тонкослойная хроматография (ВЭТСХ), • высокоэффективная ионная хроматография (ВЭИХ), • сверхкритическая флюидная хроматография (ВЭИХ), • капиллярный электрофорез (КЭ)
 Вопрос 3. Хроматограмма. Оборудование и приборы для проведения хроматографии
Вопрос 3. Хроматограмма. Оборудование и приборы для проведения хроматографии
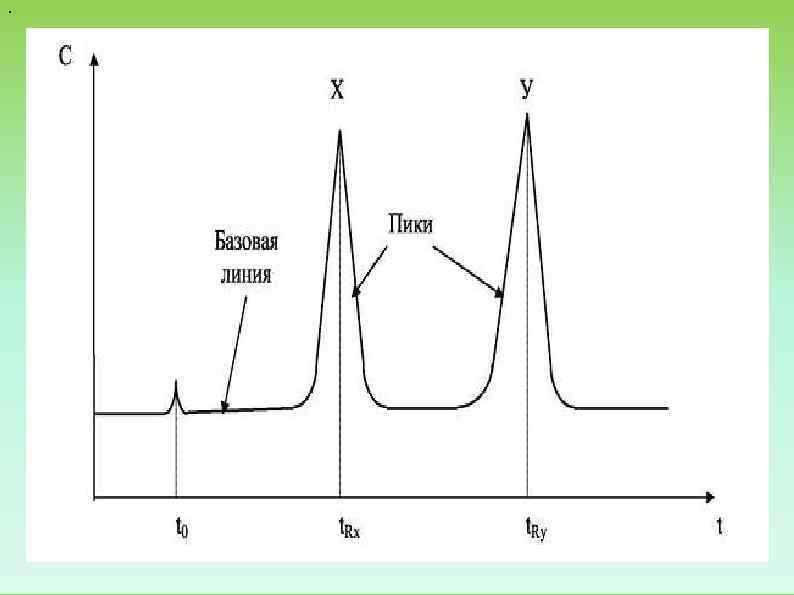
 Хроматограмма кривая, изображающая зависимость концентрации соединений, вы ходящих из колонки с потоком подвижной фазы, от времени с момента начала разделения Хроматографический пик – концентрация пробы в подвижной фазе на выходе из колонки как функция времени. Пик качественная и количественная характеристика Время удерживания – время, которое проходит с момента введения пробы до регистрации самописцем максимума сигнала. Время удерживание одного компонента при одинаковых условиях хроматографирования – постоянная величина. Условия хроматографии, влияющие на время удерживания: 1. тип колонки; 2. состав подвижной фазы; 3. скорость потока подвижной фазы; 4. температура Две возможности проведения достоверного качественного анализа: 1. И пробу и стандарт хроматографируют в разных хроматографических условиях 2. Выбор соответствующих детекторов
Хроматограмма кривая, изображающая зависимость концентрации соединений, вы ходящих из колонки с потоком подвижной фазы, от времени с момента начала разделения Хроматографический пик – концентрация пробы в подвижной фазе на выходе из колонки как функция времени. Пик качественная и количественная характеристика Время удерживания – время, которое проходит с момента введения пробы до регистрации самописцем максимума сигнала. Время удерживание одного компонента при одинаковых условиях хроматографирования – постоянная величина. Условия хроматографии, влияющие на время удерживания: 1. тип колонки; 2. состав подвижной фазы; 3. скорость потока подвижной фазы; 4. температура Две возможности проведения достоверного качественного анализа: 1. И пробу и стандарт хроматографируют в разных хроматографических условиях 2. Выбор соответствующих детекторов
 .
.
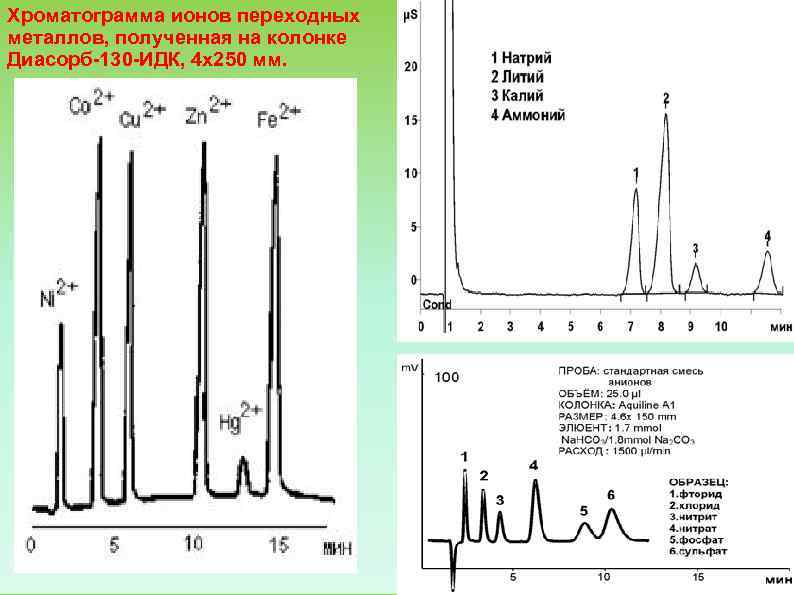
 Хроматограмма ионов переходных металлов, полученная на колонке Диасорб 130 ИДК, 4 x 250 мм.
Хроматограмма ионов переходных металлов, полученная на колонке Диасорб 130 ИДК, 4 x 250 мм.
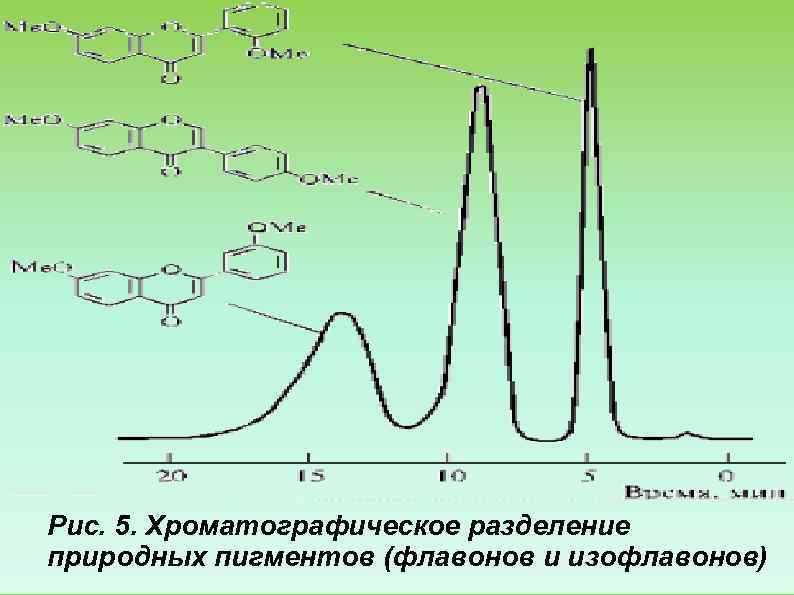
 Рис. 5. Хроматографическое разделение природных пигментов (флавонов и изофлавонов)
Рис. 5. Хроматографическое разделение природных пигментов (флавонов и изофлавонов)
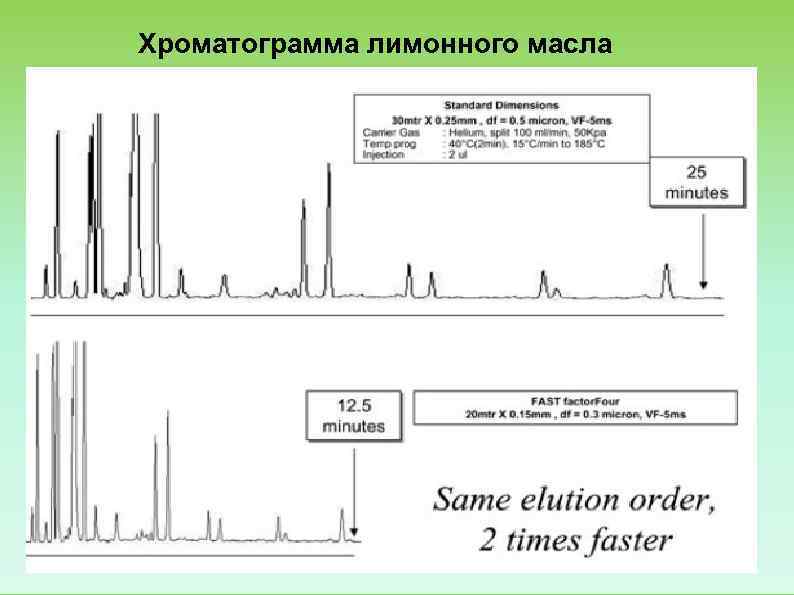
 Хроматограмма лимонного масла
Хроматограмма лимонного масла
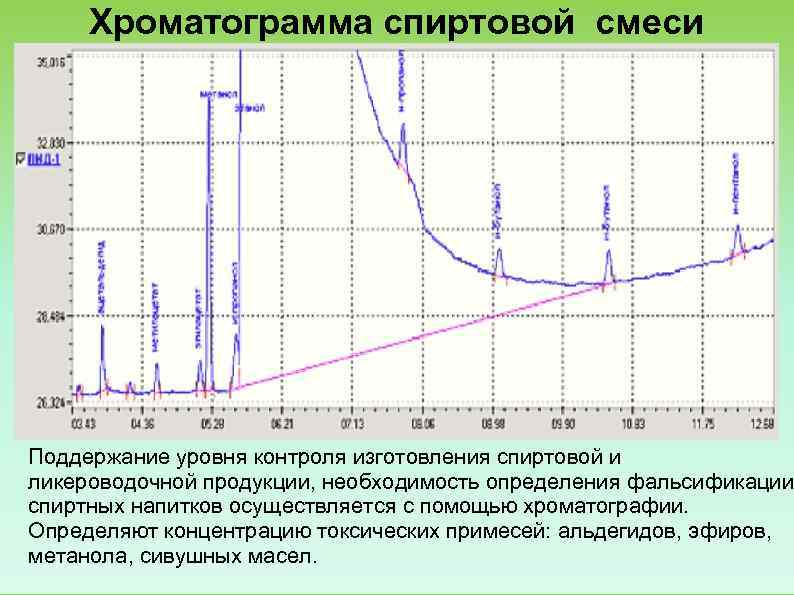
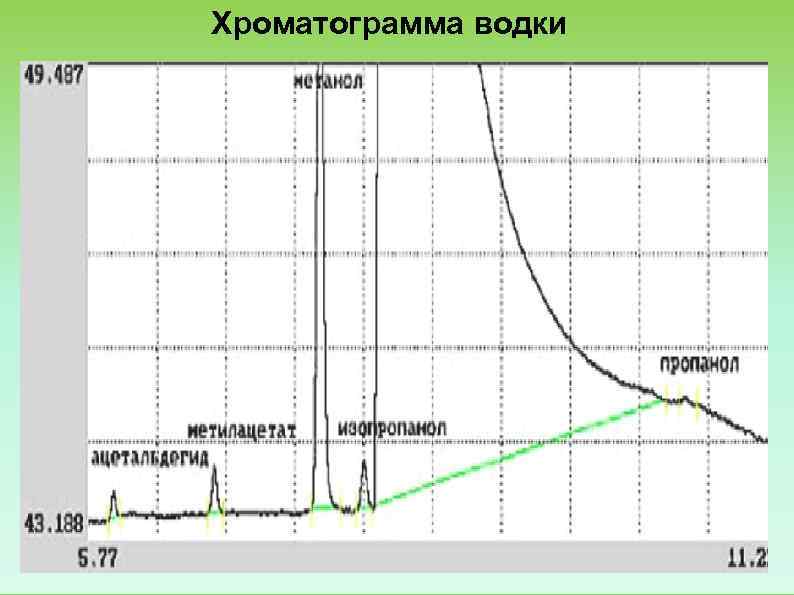
 Хроматограмма спиртовой смеси Поддержание уровня контроля изготовления спиртовой и ликероводочной продукции, необходимость определения фальсификации спиртных напитков осуществляется с помощью хроматографии. Определяют концентрацию токсических примесей: альдегидов, эфиров, метанола, сивушных масел.
Хроматограмма спиртовой смеси Поддержание уровня контроля изготовления спиртовой и ликероводочной продукции, необходимость определения фальсификации спиртных напитков осуществляется с помощью хроматографии. Определяют концентрацию токсических примесей: альдегидов, эфиров, метанола, сивушных масел.
 Хроматограмма водки
Хроматограмма водки
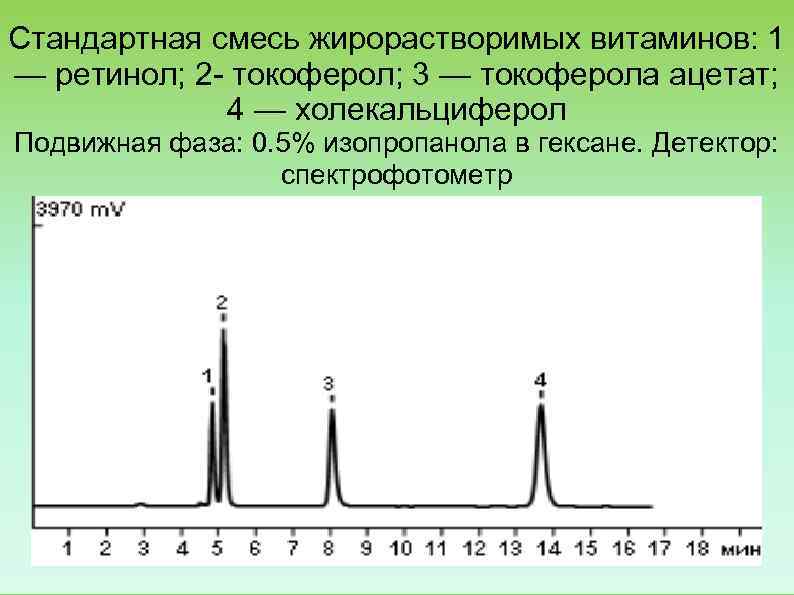
 Стандартная смесь жирорастворимых витаминов: 1 — ретинол; 2 токоферол; 3 — токоферола ацетат; 4 — холекальциферол Подвижная фаза: 0. 5% изопропанола в гексане. Детектор: спектрофотометр
Стандартная смесь жирорастворимых витаминов: 1 — ретинол; 2 токоферол; 3 — токоферола ацетат; 4 — холекальциферол Подвижная фаза: 0. 5% изопропанола в гексане. Детектор: спектрофотометр
 Экран ноутбука с получаемой Примеры хроматограмм и на приборе «РУБИН» масс спектров. хроматограммой.
Экран ноутбука с получаемой Примеры хроматограмм и на приборе «РУБИН» масс спектров. хроматограммой.
 Правильная запись данных ГЖХ 1. Номер (шифр) эксперимента или номер образца 2. Количество введенной пробы 3. Используемая колонка (неподвижная фаза и процент ее нанесения, материал носителя, длина (см) 4. Расход газа носителя 5. Рабочая температура 6. Усиление, используемое для каждого пика 7. Скорость диаграммы Пример: Опыт К 9 1 мкл 10% смазки апиезон APL на хромасорбе W, 200 см N 2, 60 мл/мин 1500 С Все пики при 50 • 102 Диаграмма 60 см/ч
Правильная запись данных ГЖХ 1. Номер (шифр) эксперимента или номер образца 2. Количество введенной пробы 3. Используемая колонка (неподвижная фаза и процент ее нанесения, материал носителя, длина (см) 4. Расход газа носителя 5. Рабочая температура 6. Усиление, используемое для каждого пика 7. Скорость диаграммы Пример: Опыт К 9 1 мкл 10% смазки апиезон APL на хромасорбе W, 200 см N 2, 60 мл/мин 1500 С Все пики при 50 • 102 Диаграмма 60 см/ч
 Прибордля проведения хроматографии называют хроматограф. В его состав входят: 1. система для ввода исследуемой смеси веществ (пробы); 2. хроматографическая колонка; 3. детектирующее устройство (детектор); 4. системы регистрации и термостатирования; 5. отборные приспособления и приёмники для разделённых компонентов (для препаративных и. производственных хроматографов). В соответствии с состоянием используемой подвижной фазы различают газовые и жидкостные хроматографы
Прибордля проведения хроматографии называют хроматограф. В его состав входят: 1. система для ввода исследуемой смеси веществ (пробы); 2. хроматографическая колонка; 3. детектирующее устройство (детектор); 4. системы регистрации и термостатирования; 5. отборные приспособления и приёмники для разделённых компонентов (для препаративных и. производственных хроматографов). В соответствии с состоянием используемой подвижной фазы различают газовые и жидкостные хроматографы
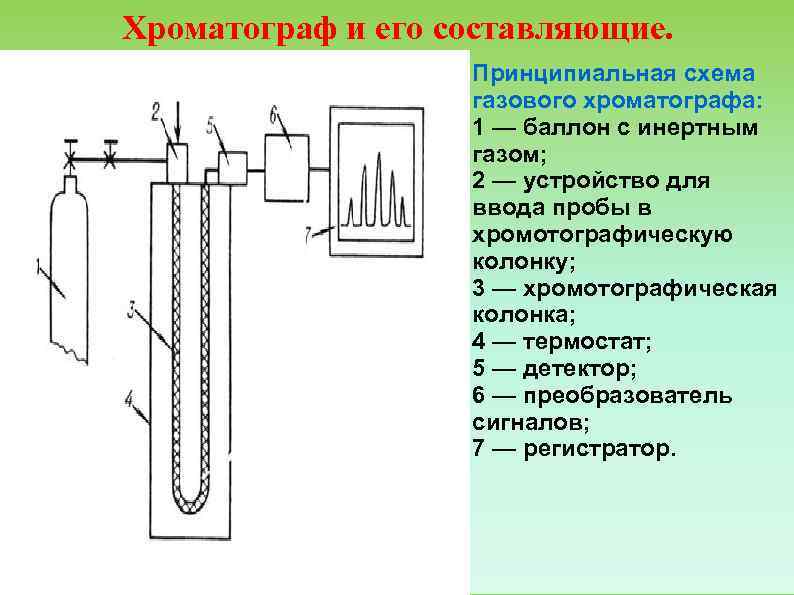
 Хроматограф и его составляющие. Принципиальная схема газового хроматографа: 1 — баллон с инертным газом; 2 — устройство для ввода пробы в хромотографическую колонку; 3 — хромотографическая колонка; 4 — термостат; 5 — детектор; 6 — преобразователь сигналов; 7 — регистратор.
Хроматограф и его составляющие. Принципиальная схема газового хроматографа: 1 — баллон с инертным газом; 2 — устройство для ввода пробы в хромотографическую колонку; 3 — хромотографическая колонка; 4 — термостат; 5 — детектор; 6 — преобразователь сигналов; 7 — регистратор.
 Схема работы газового хроматографа: *Из баллона непрерывно с постоянной или переменной скоростью в хроматографическую колонку (диаметр 2 5 мм и длина 1 10 м) подается газ носитель. *Проба (несколько микролитров) вводятся газовым шприцем или микродозатором. *В хроматографической колонке исходная смесь разделяется на ряд бинарных смесей, состоящих из газа носителя и одного из анализируемых компонентов. *В зависимости от сорбируемости компонентов бинарные смеси в определённом порядке поступают в детектор. *В результате происходящих в детекторе процессов фиксируется изменение концентрации выходящих компонентов. Эти процессы, преобразованные в электрический сигнал, записываются в виде выходной кривой хроматограммы.
Схема работы газового хроматографа: *Из баллона непрерывно с постоянной или переменной скоростью в хроматографическую колонку (диаметр 2 5 мм и длина 1 10 м) подается газ носитель. *Проба (несколько микролитров) вводятся газовым шприцем или микродозатором. *В хроматографической колонке исходная смесь разделяется на ряд бинарных смесей, состоящих из газа носителя и одного из анализируемых компонентов. *В зависимости от сорбируемости компонентов бинарные смеси в определённом порядке поступают в детектор. *В результате происходящих в детекторе процессов фиксируется изменение концентрации выходящих компонентов. Эти процессы, преобразованные в электрический сигнал, записываются в виде выходной кривой хроматограммы.
 Хроматографы жидкостные изократические предназначены для количественного анализа методом ВЭЖХ различных органических соединений в пищевой продукции и сырье, безалкогольных и алкогольных напитках, кормах, воде, биологических жидкостях и т. д. Для контроля продукции и технологических процессов в фармацевтической, химической, нефтехимической, нефтеперерабатывающей и других отраслях промышленности.
Хроматографы жидкостные изократические предназначены для количественного анализа методом ВЭЖХ различных органических соединений в пищевой продукции и сырье, безалкогольных и алкогольных напитках, кормах, воде, биологических жидкостях и т. д. Для контроля продукции и технологических процессов в фармацевтической, химической, нефтехимической, нефтеперерабатывающей и других отраслях промышленности.
 Промышленный газовый хроматограф "Хроматэк Кристалл 7000"
Промышленный газовый хроматограф "Хроматэк Кристалл 7000"
 Хроматограф жидкостный изократический «Стайер»
Хроматограф жидкостный изократический «Стайер»
 Жидкостный хроматограф Jasco
Жидкостный хроматограф Jasco
 Хроматограф Газовый хроматограф Жидкостный промышленный CLARUS 500. хроматограф ионный Стайер А. ф. BISCHOFF CHROMATOGRAPHY
Хроматограф Газовый хроматограф Жидкостный промышленный CLARUS 500. хроматограф ионный Стайер А. ф. BISCHOFF CHROMATOGRAPHY
 Газовые хроматографы серии ЭХО предназначены для проведения оперативных качественных и количественных анализов широкого класса органических веществ в газообразных или жидких пробах в лабораторных и полевых условиях. Жидкостный хроматограф фирмы "Bruker" Пример отбора проб при поиске взрывчатых веществ.
Газовые хроматографы серии ЭХО предназначены для проведения оперативных качественных и количественных анализов широкого класса органических веществ в газообразных или жидких пробах в лабораторных и полевых условиях. Жидкостный хроматограф фирмы "Bruker" Пример отбора проб при поиске взрывчатых веществ.
 Жидкостный хроматограф «ЛЮМАХРОМ» позволяет реализовать метод высокоэффективной жидкостной хроматографии, который заключается в разделении веществ вследствие различного распределения между подвижной и неподвижной фазами с последующей регистрацией фотометрическим и/или флуориметрическим детекторами.
Жидкостный хроматограф «ЛЮМАХРОМ» позволяет реализовать метод высокоэффективной жидкостной хроматографии, который заключается в разделении веществ вследствие различного распределения между подвижной и неподвижной фазами с последующей регистрацией фотометрическим и/или флуориметрическим детекторами.
 ДЕТЕКТОРЫ ХРОМАТОГРАФИЧЕСКИЕ (лат. detector тот, кто раскрывает, обнаруживает), устройства для количественного и качественного определения веществ разделяемой смеси в потоке подвижной фазы на выходе из хроматографической колонки. Детекторы хроматографические можно рассматривать также как преобразовательный элемент, в котором изменение состава проходящей через него смеси преобразуется в изменение выходного сигнала. Различают детекторы хроматографические : 1. дифференциального типа регистрируют мгновенное значение одной из характеристик (концентрации или потока) 2. интегрального типа суммируют количество вещества за определенный промежуток времени.
ДЕТЕКТОРЫ ХРОМАТОГРАФИЧЕСКИЕ (лат. detector тот, кто раскрывает, обнаруживает), устройства для количественного и качественного определения веществ разделяемой смеси в потоке подвижной фазы на выходе из хроматографической колонки. Детекторы хроматографические можно рассматривать также как преобразовательный элемент, в котором изменение состава проходящей через него смеси преобразуется в изменение выходного сигнала. Различают детекторы хроматографические : 1. дифференциального типа регистрируют мгновенное значение одной из характеристик (концентрации или потока) 2. интегрального типа суммируют количество вещества за определенный промежуток времени.
 Существует уже более 20 типов детекторов. Классификация детекторов: • оптические, • электрохимические • детекторы для измерения радиоактивных веществ. К оптическим детекторам относятся: ультрафиолетовый (УФД), инфракрасный (ИКД), рефрактометрический (РМД) и флуорометрический (ФМД), а также все детекторы, в которых в той или иной мере используется лазерное излучение, такие как детектор светового рассеяния (СРД), фотоакустический (ФАД), фотокалориметрический (ФКД), фотоионизационный (ФИД) и поляризационный (ПОД) детекторы. К электрическим детекторам обычно относят: детектор по диэлектрической постоянной (ДПД), акустический (АД), емкостный (ЕМД), детектор тока потока (ТПД) и некоторые другие.
Существует уже более 20 типов детекторов. Классификация детекторов: • оптические, • электрохимические • детекторы для измерения радиоактивных веществ. К оптическим детекторам относятся: ультрафиолетовый (УФД), инфракрасный (ИКД), рефрактометрический (РМД) и флуорометрический (ФМД), а также все детекторы, в которых в той или иной мере используется лазерное излучение, такие как детектор светового рассеяния (СРД), фотоакустический (ФАД), фотокалориметрический (ФКД), фотоионизационный (ФИД) и поляризационный (ПОД) детекторы. К электрическим детекторам обычно относят: детектор по диэлектрической постоянной (ДПД), акустический (АД), емкостный (ЕМД), детектор тока потока (ТПД) и некоторые другие.
 DORS 50 ультрафиолетовый детектор. Спектрофотометрический детектор Jasco UV 975 Диапазон длин волн 190 600 нм Кондуктометрический детектор Waters 430.
DORS 50 ультрафиолетовый детектор. Спектрофотометрический детектор Jasco UV 975 Диапазон длин волн 190 600 нм Кондуктометрический детектор Waters 430.
 Устройство ввода пробы Предназначено для подачи пробы анализируемой смеси в хроматографическую колонку. В том случае, если хроматограф предназначен для анализа жидких проб, устройство ввода проб совмещается с испарителем. Проба вводится в испаритель при помощи микрошприца путём прокалывания эластичной прокладки. Испаритель обычно нагрет до температуры, превышающей температуру самой колонки на 50 °C. Объём вводимой пробы — несколько микролитров.
Устройство ввода пробы Предназначено для подачи пробы анализируемой смеси в хроматографическую колонку. В том случае, если хроматограф предназначен для анализа жидких проб, устройство ввода проб совмещается с испарителем. Проба вводится в испаритель при помощи микрошприца путём прокалывания эластичной прокладки. Испаритель обычно нагрет до температуры, превышающей температуру самой колонки на 50 °C. Объём вводимой пробы — несколько микролитров.
 УСТРОЙСТВО ВВОДА ПРОБЫ. Устройство ввода пробы предназначено для ручного ввода автоматическое (вид сверху) пробы в колонку.
УСТРОЙСТВО ВВОДА ПРОБЫ. Устройство ввода пробы предназначено для ручного ввода автоматическое (вид сверху) пробы в колонку.
 Хроматографическая колонка главная часть хроматографической системы Колонка может быть наполнена сорбентом, или представляет собой полую трубку с нанесенным на внутреннюю поверхность сорбентом, в объеме которого осуществляется хроматографи ческое разделение смеси веществ.
Хроматографическая колонка главная часть хроматографической системы Колонка может быть наполнена сорбентом, или представляет собой полую трубку с нанесенным на внутреннюю поверхность сорбентом, в объеме которого осуществляется хроматографи ческое разделение смеси веществ.
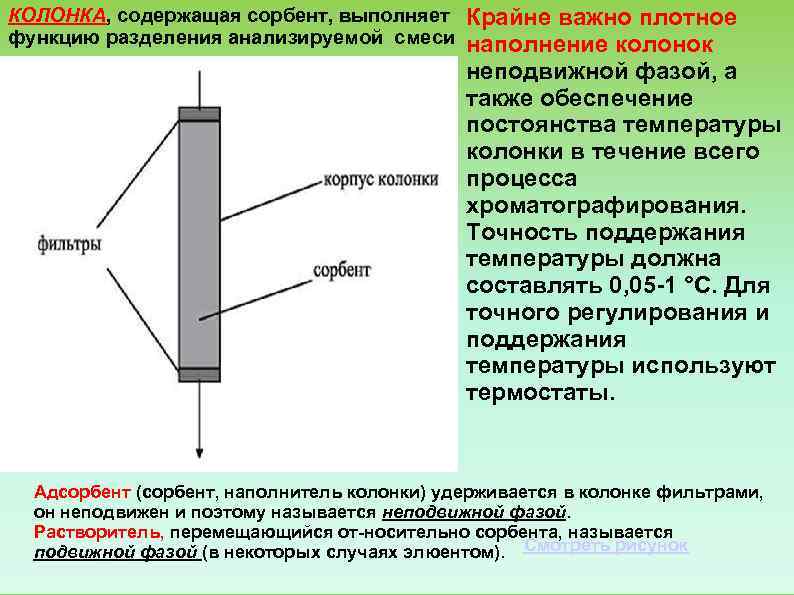
 КОЛОНКА, содержащая сорбент, выполняет Крайне важно плотное функцию разделения анализируемой смеси наполнение колонок на составные компоненты. неподвижной фазой, а также обеспечение постоянства температуры колонки в течение всего процесса хроматографирования. Точность поддержания температуры должна составлять 0, 05 1 °C. Для точного регулирования и поддержания температуры используют термостаты. Адсорбент (сорбент, наполнитель колонки) удерживается в колонке фильтрами, он неподвижен и поэтому называется неподвижной фазой. Растворитель, перемещающийся от носительно сорбента, называется подвижной фазой (в некоторых случаях элюентом). Смотреть рисунок
КОЛОНКА, содержащая сорбент, выполняет Крайне важно плотное функцию разделения анализируемой смеси наполнение колонок на составные компоненты. неподвижной фазой, а также обеспечение постоянства температуры колонки в течение всего процесса хроматографирования. Точность поддержания температуры должна составлять 0, 05 1 °C. Для точного регулирования и поддержания температуры используют термостаты. Адсорбент (сорбент, наполнитель колонки) удерживается в колонке фильтрами, он неподвижен и поэтому называется неподвижной фазой. Растворитель, перемещающийся от носительно сорбента, называется подвижной фазой (в некоторых случаях элюентом). Смотреть рисунок
 Типичный прибор для колоночной хроматографии
Типичный прибор для колоночной хроматографии
 Стеклянные колонки и наборы для флэш хроматографии низкого давления.
Стеклянные колонки и наборы для флэш хроматографии низкого давления.
 Стеклянные колонки Eco. Plus, наборы для Колонки Хроматографические. Проведение шкалирования ID 5 50 анализа. mm, до 80 mm
Стеклянные колонки Eco. Plus, наборы для Колонки Хроматографические. Проведение шкалирования ID 5 50 анализа. mm, до 80 mm
 Существует множество типов колонок: для хроматографии низкого и высокого давления; для аналитической, препаративной или промышленной хроматографии; для радиальной или аксиальной хроматографии. Также колонки подразделяют на неразборные (упакованные в заводских условиях) и разборные с подвижными и не подвижными адапторами. Каждый тип колонки имеет свои конструкционные особенности. Конструкционно КЖХ состоит из обязательных частей: трубки и адапторов, и не обязательных частей: рубашки термостата, гидравлической системы для упаковки колонки и т. д.
Существует множество типов колонок: для хроматографии низкого и высокого давления; для аналитической, препаративной или промышленной хроматографии; для радиальной или аксиальной хроматографии. Также колонки подразделяют на неразборные (упакованные в заводских условиях) и разборные с подвижными и не подвижными адапторами. Каждый тип колонки имеет свои конструкционные особенности. Конструкционно КЖХ состоит из обязательных частей: трубки и адапторов, и не обязательных частей: рубашки термостата, гидравлической системы для упаковки колонки и т. д.
 Хроматографическая колонка с адсорбентом Колонка должна быть равномерно заполнена максимально однородным слоем сорбента.
Хроматографическая колонка с адсорбентом Колонка должна быть равномерно заполнена максимально однородным слоем сорбента.
 Хроматографические колонки имеют геометрию удлиненного цилиндра с жесткими стенками, изготовленного из металлических, стеклянных или полимерных трубок.
Хроматографические колонки имеют геометрию удлиненного цилиндра с жесткими стенками, изготовленного из металлических, стеклянных или полимерных трубок.
 Хроматографические колонки Под колонкой подразумевается сосуд, длина которого значительно больше диаметра. Для газовой хроматографии обычно используют U образные или спиральные колонки. Внутренний диаметр колонок — 2 15 мм, а длина — 1 20 м. Материалом для изготовления колонок служит стекло, нержавеющая сталь, медь, иногда фторопласт. В последнее время наибольшее распространение получили капиллярные колонки изготовленные из плавленного кварца, с нанесенной внутри неподвижной фазой. Длина подобных колонок может достигать сотен и даже тысяч метров, хотя чаще используются колонки длиной 30 50 м. Крайне важно плотное наполнение колонок неподвижной фазой, а также обеспечение постоянства температуры колонки в течение всего процесса хроматографирования. Точность поддержания температуры должна составлять 0, 05 1 °C. Для точного регулирования и поддержания температуры используют термостаты.
Хроматографические колонки Под колонкой подразумевается сосуд, длина которого значительно больше диаметра. Для газовой хроматографии обычно используют U образные или спиральные колонки. Внутренний диаметр колонок — 2 15 мм, а длина — 1 20 м. Материалом для изготовления колонок служит стекло, нержавеющая сталь, медь, иногда фторопласт. В последнее время наибольшее распространение получили капиллярные колонки изготовленные из плавленного кварца, с нанесенной внутри неподвижной фазой. Длина подобных колонок может достигать сотен и даже тысяч метров, хотя чаще используются колонки длиной 30 50 м. Крайне важно плотное наполнение колонок неподвижной фазой, а также обеспечение постоянства температуры колонки в течение всего процесса хроматографирования. Точность поддержания температуры должна составлять 0, 05 1 °C. Для точного регулирования и поддержания температуры используют термостаты.
 Вопрос 3. Характеристика основных видов хроматографии
Вопрос 3. Характеристика основных видов хроматографии
 К основным видам хроматографии относят адсорбционную, ионообменную, жидкостную, бумажную, тонкослойную, гель фильтрационную и афинную хроматографию.
К основным видам хроматографии относят адсорбционную, ионообменную, жидкостную, бумажную, тонкослойную, гель фильтрационную и афинную хроматографию.
 Адсорбционная хроматография. В этом случае разделение веществ осуществляется за счет выборочной (селективной) адсорбции веществ на неподвижной фазе. Селективная адсорбция обусловлена сродством того или иного соединения к твердому адсорбенту (н. ф. ), что определяется полярными взаимодействиями их молекул. К адсорбционной хроматографии относят: 1. ионообменную, 2. жидкостную, 3. бумажную, 4. тонкослойную 5. газо-адсорбционную хроматографию.
Адсорбционная хроматография. В этом случае разделение веществ осуществляется за счет выборочной (селективной) адсорбции веществ на неподвижной фазе. Селективная адсорбция обусловлена сродством того или иного соединения к твердому адсорбенту (н. ф. ), что определяется полярными взаимодействиями их молекул. К адсорбционной хроматографии относят: 1. ионообменную, 2. жидкостную, 3. бумажную, 4. тонкослойную 5. газо-адсорбционную хроматографию.
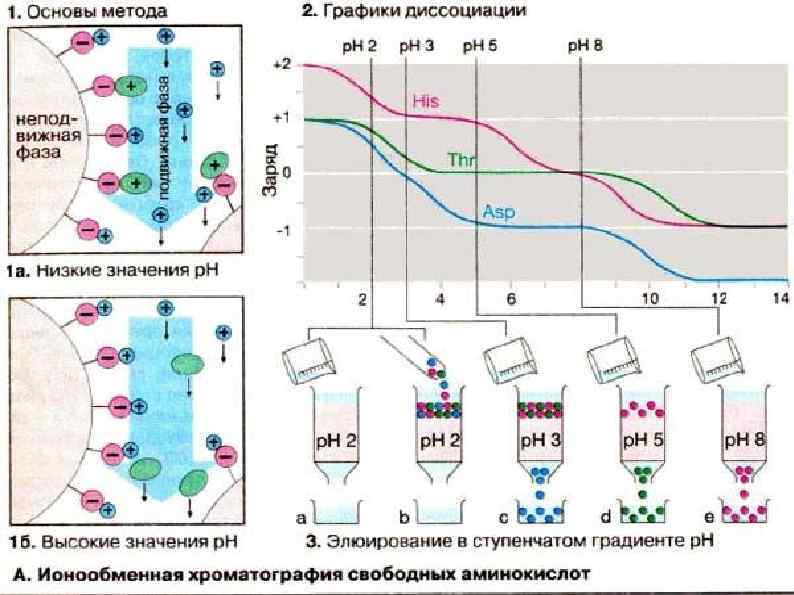
 Ионообменная хроматография. В качестве неподвижной фазы используют ионообменные смолы (рис. 4) как в колонках, так и в виде тонкого слоя на пластинке или бумаге. Разделение обычно проводят в водных средах, поэтому этот метод используется главным образом в неорганической химии, хотя применяются и смешанные растворители. Движущей силой разделения в этом случае является различное сродство разделяемых ионов раствора к ионообменным центрам противоположной полярности в неподвижной фазе.
Ионообменная хроматография. В качестве неподвижной фазы используют ионообменные смолы (рис. 4) как в колонках, так и в виде тонкого слоя на пластинке или бумаге. Разделение обычно проводят в водных средах, поэтому этот метод используется главным образом в неорганической химии, хотя применяются и смешанные растворители. Движущей силой разделения в этом случае является различное сродство разделяемых ионов раствора к ионообменным центрам противоположной полярности в неподвижной фазе.
 Рис. 4. Изображение структуры частицы ионообменной смолы: · – заряженные функциональные группы, ковалентно связанные с нитями решетки; ° – свободно перемещающиеся противоположно заряженные протовоионы, электростатически связанные с частицей смолы, способные претерпевать обмен с другими ионами
Рис. 4. Изображение структуры частицы ионообменной смолы: · – заряженные функциональные группы, ковалентно связанные с нитями решетки; ° – свободно перемещающиеся противоположно заряженные протовоионы, электростатически связанные с частицей смолы, способные претерпевать обмен с другими ионами

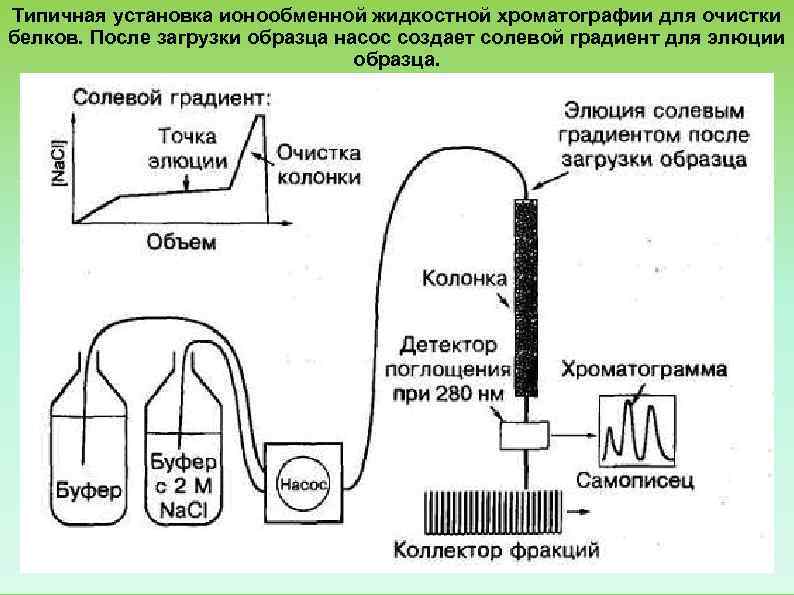
 Типичная установка ионообменной жидкостной хроматографии для очистки белков. После загрузки образца насос создает солевой градиент для элюции образца.
Типичная установка ионообменной жидкостной хроматографии для очистки белков. После загрузки образца насос создает солевой градиент для элюции образца.
 Жидкостная хроматография. В этом случае неподвижной фазой служит жидкость. Наиболее распространенным случаем является адсорбционный вариант жидкостной колоночной хроматографии.
Жидкостная хроматография. В этом случае неподвижной фазой служит жидкость. Наиболее распространенным случаем является адсорбционный вариант жидкостной колоночной хроматографии.
 Жидкостная хроматография (ЖХ) 1)По агрегатному состоянию фаз хроматографической системы: а)жидкостно адсорбционную, б)жидкостно жидкостную, в)противоточную ЖХ. 2) По способу перемещения сорбата: а)вытеснительная, б)фронтальная, в)элюентная, г)градиентная. 3) По конфигурации разделяющей системы: а)планарную (бумажную, тонкослойную), б)колоночную, микроколоночную, многоколоночную, в)циркуляционную, г)многомерную, д)перколяционную, е)мультихроматографию.
Жидкостная хроматография (ЖХ) 1)По агрегатному состоянию фаз хроматографической системы: а)жидкостно адсорбционную, б)жидкостно жидкостную, в)противоточную ЖХ. 2) По способу перемещения сорбата: а)вытеснительная, б)фронтальная, в)элюентная, г)градиентная. 3) По конфигурации разделяющей системы: а)планарную (бумажную, тонкослойную), б)колоночную, микроколоночную, многоколоночную, в)циркуляционную, г)многомерную, д)перколяционную, е)мультихроматографию.
 4) По относительной полярности подвижной и неподвижной фаз: нормально и обращенно фазовую ЖХ. 5) По механизму разделения: адсорбционную, распределительную, эксклюзионную, афинную, лигандообменную, ионообменную ЖХ. 6) По цели и задачам можно выделить аналитическую, препаративную и обращенную ситовую ЖХ. 7) По химическому превращению сорбата выделяют реакционную и осадочную ЖХ. 8) По способу детектирования различают ЖХ сочетающую разделение компонентов смеси с прямым детектированием веществ оптическими детекторами, работающими в: УФ, видимой, ИК области, рефрактометрическими, эмиссионными, флуориметрическими, хемилюминесцентными, электрохимическими и другими детекторами.
4) По относительной полярности подвижной и неподвижной фаз: нормально и обращенно фазовую ЖХ. 5) По механизму разделения: адсорбционную, распределительную, эксклюзионную, афинную, лигандообменную, ионообменную ЖХ. 6) По цели и задачам можно выделить аналитическую, препаративную и обращенную ситовую ЖХ. 7) По химическому превращению сорбата выделяют реакционную и осадочную ЖХ. 8) По способу детектирования различают ЖХ сочетающую разделение компонентов смеси с прямым детектированием веществ оптическими детекторами, работающими в: УФ, видимой, ИК области, рефрактометрическими, эмиссионными, флуориметрическими, хемилюминесцентными, электрохимическими и другими детекторами.
 Бумажная хроматография. В качестве неподвижной фазы используют полосы или листы бумаги. Разделение происходит по адсорбционному механизму, причем иногда его проводят в двух перпендикулярных направлениях. Рис. 6. Схема разделения методом бумажной хроматографии: А, Б и В – положения компонентов смеси по окончании хроматографического разделения. Подвижная фаза впитывается в бумагу (неподвижная фаза) под действием капиллярных сил и переносит индивидуальные компоненты смеси с различными скоростями, зависящими от отношений растворимости этих компонентов в обеих фазах. Отношение а/б = Rf (фактор запаздывания) характеризует данное разделяемое вещество
Бумажная хроматография. В качестве неподвижной фазы используют полосы или листы бумаги. Разделение происходит по адсорбционному механизму, причем иногда его проводят в двух перпендикулярных направлениях. Рис. 6. Схема разделения методом бумажной хроматографии: А, Б и В – положения компонентов смеси по окончании хроматографического разделения. Подвижная фаза впитывается в бумагу (неподвижная фаза) под действием капиллярных сил и переносит индивидуальные компоненты смеси с различными скоростями, зависящими от отношений растворимости этих компонентов в обеих фазах. Отношение а/б = Rf (фактор запаздывания) характеризует данное разделяемое вещество
 прибор для бумажной хроматографии.
прибор для бумажной хроматографии.
 , БХ вид ХРОМАТОГРАФИИ, в котором применяется абсорбирующая бумага. Анализируемая смесь растворяется, затем капля раствора помещается на лист бумаги возле его края. Лист держится вертикально, а его край опускается в РАСТВОРИТЕЛЬ. Так как растворитель поднимается вверх по бумаге благодаря ее капиллярным свойствам, компоненты раствора также передвигаются с фронтом растворителя, но с различными скоростями, в зависимости от их состава. Когда бумага высыхает, компоненты проявляются на ней в виде ряда пятен, которые необходимо обработать соответственным реактивом для того, чтобы они окрасились и проявились. Расстояние на которое продвигается вещество за данный отрезок времени, является параметром его идентификации.
, БХ вид ХРОМАТОГРАФИИ, в котором применяется абсорбирующая бумага. Анализируемая смесь растворяется, затем капля раствора помещается на лист бумаги возле его края. Лист держится вертикально, а его край опускается в РАСТВОРИТЕЛЬ. Так как растворитель поднимается вверх по бумаге благодаря ее капиллярным свойствам, компоненты раствора также передвигаются с фронтом растворителя, но с различными скоростями, в зависимости от их состава. Когда бумага высыхает, компоненты проявляются на ней в виде ряда пятен, которые необходимо обработать соответственным реактивом для того, чтобы они окрасились и проявились. Расстояние на которое продвигается вещество за данный отрезок времени, является параметром его идентификации.
 Расстояние, пройденное на бумаге каждым компонентом в течение времени, отведенного под эксперимент, служит показателем скорости переноса каждого из компонентов и может быть использовано для определения этих компонентов
Расстояние, пройденное на бумаге каждым компонентом в течение времени, отведенного под эксперимент, служит показателем скорости переноса каждого из компонентов и может быть использовано для определения этих компонентов
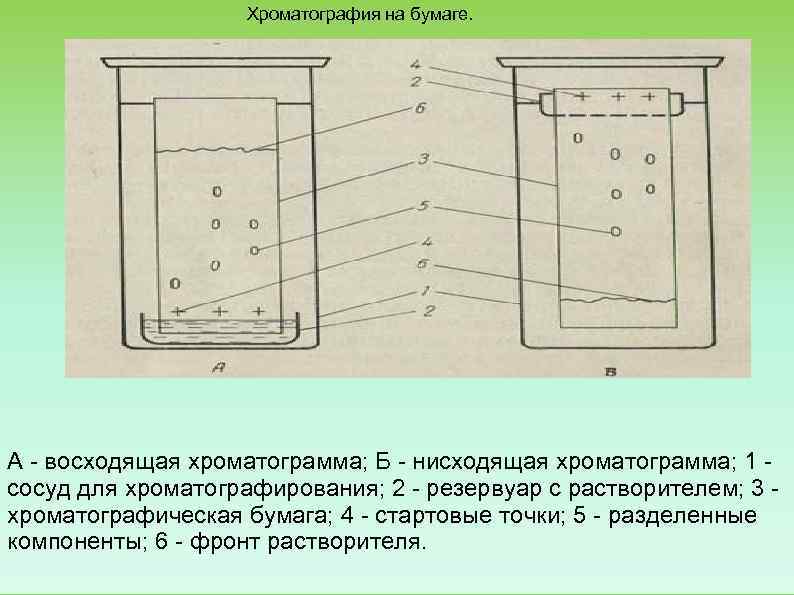
 Хроматография на бумаге. А восходящая хроматограмма; Б нисходящая хроматограмма; 1 сосуд для хроматографирования; 2 резервуар с растворителем; 3 хроматографическая бумага; 4 стартовые точки; 5 разделенные компоненты; 6 фронт растворителя.
Хроматография на бумаге. А восходящая хроматограмма; Б нисходящая хроматограмма; 1 сосуд для хроматографирования; 2 резервуар с растворителем; 3 хроматографическая бумага; 4 стартовые точки; 5 разделенные компоненты; 6 фронт растворителя.
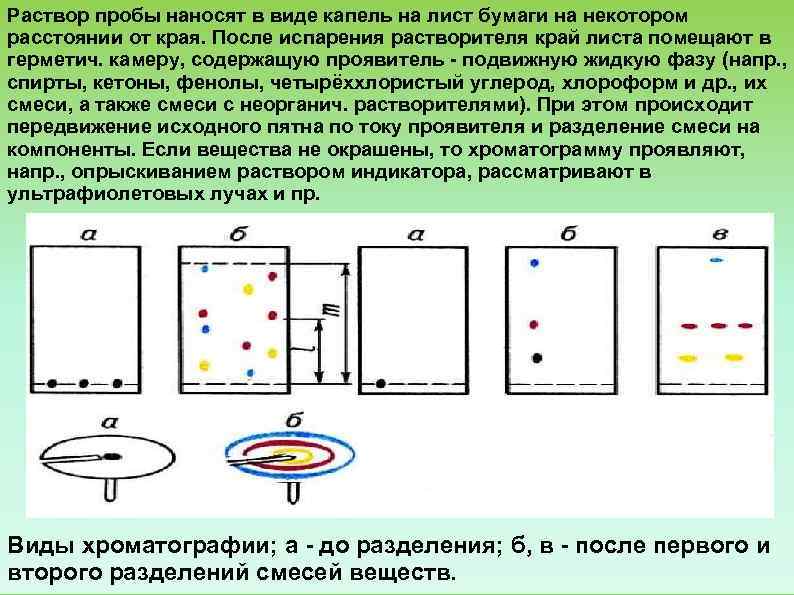
 Раствор пробы наносят в виде капель на лист бумаги на некотором расстоянии от края. После испарения растворителя край листа помещают в герметич. камеру, содержащую проявитель подвижную жидкую фазу (напр. , спирты, кетоны, фенолы, четырёххлористый углерод, хлороформ и др. , их смеси, а также смеси с неорганич. растворителями). При этом происходит передвижение исходного пятна по току проявителя и разделение смеси на компоненты. Если вещества не окрашены, то хроматограмму проявляют, напр. , опрыскиванием раствором индикатора, рассматривают в ультрафиолетовых лучах и пр. Виды хроматографии; а до разделения; б, в после первого и второго разделений смесей веществ.
Раствор пробы наносят в виде капель на лист бумаги на некотором расстоянии от края. После испарения растворителя край листа помещают в герметич. камеру, содержащую проявитель подвижную жидкую фазу (напр. , спирты, кетоны, фенолы, четырёххлористый углерод, хлороформ и др. , их смеси, а также смеси с неорганич. растворителями). При этом происходит передвижение исходного пятна по току проявителя и разделение смеси на компоненты. Если вещества не окрашены, то хроматограмму проявляют, напр. , опрыскиванием раствором индикатора, рассматривают в ультрафиолетовых лучах и пр. Виды хроматографии; а до разделения; б, в после первого и второго разделений смесей веществ.
 Тонкослойная хроматография (ТСХ) – это любая система, в которой неподвижной фазой является тонкий слой в виде пасты, нанесенной на стеклянную пластинку, фольгу или пластик. Рис. 7. Камера для тонкослойной хроматографии:
Тонкослойная хроматография (ТСХ) – это любая система, в которой неподвижной фазой является тонкий слой в виде пасты, нанесенной на стеклянную пластинку, фольгу или пластик. Рис. 7. Камера для тонкослойной хроматографии:
 ТОНКОСЛОЙНАЯ ХРОМАТОГРАФИЯ Основана на различии в скорости перемещения компонентов смеси в плоском тонком слое (0, 1 0, 5 мм) сорбента при их движении в потоке подвижной (жидкой) фазы элюента. ТСХ является планарной разновидностью жидкостной хроматографии, в которой подвижная фаза (ПФ) движется в пористой среде слоя адсорбента.
ТОНКОСЛОЙНАЯ ХРОМАТОГРАФИЯ Основана на различии в скорости перемещения компонентов смеси в плоском тонком слое (0, 1 0, 5 мм) сорбента при их движении в потоке подвижной (жидкой) фазы элюента. ТСХ является планарной разновидностью жидкостной хроматографии, в которой подвижная фаза (ПФ) движется в пористой среде слоя адсорбента.
 Сорбентами могут быть: 1. силикагель (гидратированная кремниевая кислота полярный сорбент), 2. Аl 2 О 3 (основный сорбент), 3. целлюлоза, крахмал, полиамид, иониты и др. для закрепления слоя применяют крахмал, гипс или др. Элюентами служат смеси органических растворителей, водные растворы кислот, солей.
Сорбентами могут быть: 1. силикагель (гидратированная кремниевая кислота полярный сорбент), 2. Аl 2 О 3 (основный сорбент), 3. целлюлоза, крахмал, полиамид, иониты и др. для закрепления слоя применяют крахмал, гипс или др. Элюентами служат смеси органических растворителей, водные растворы кислот, солей.
 По технике работы различают ТСХ: 1. фронтальную подвижной фазой служит анализируемая смесь, 2. элюционную — на слой сорбента наносят капли (объемом 1 5 мкл) анализируемого раствора и погружают край пластинки в элюент, который находится на дне герметично закрываемой стеклянной камеры. 3. круговую анализируемый раствор и растворитель последовательно подаются в центр пластинки), 4. антикруговую анализируемый раствор наносится по окружности и элюент перемещается от периферии к центру пластинки).
По технике работы различают ТСХ: 1. фронтальную подвижной фазой служит анализируемая смесь, 2. элюционную — на слой сорбента наносят капли (объемом 1 5 мкл) анализируемого раствора и погружают край пластинки в элюент, который находится на дне герметично закрываемой стеклянной камеры. 3. круговую анализируемый раствор и растворитель последовательно подаются в центр пластинки), 4. антикруговую анализируемый раствор наносится по окружности и элюент перемещается от периферии к центру пластинки).
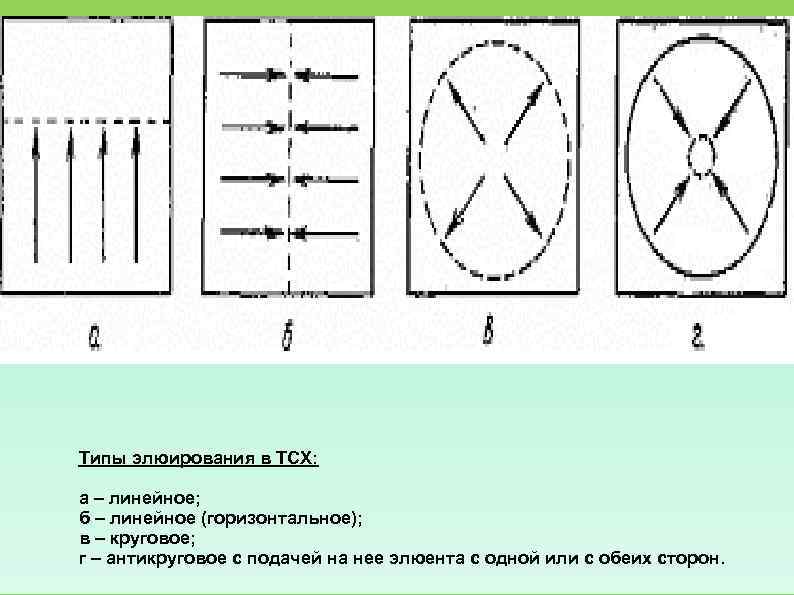
 Типы элюирования в ТСХ: а – линейное; б – линейное (горизонтальное); в – круговое; г – антикруговое с подачей на нее элюента с одной или с обеих сторон.
Типы элюирования в ТСХ: а – линейное; б – линейное (горизонтальное); в – круговое; г – антикруговое с подачей на нее элюента с одной или с обеих сторон.
 Оборудование для нанесения образцов Торрированные стеклянные капилляры Шприцевой дозатор "MULTISTEP-50" в комплекте с микрошприцем V=1 мкл Принципиальная схема автосемплера, где: 1 флаконы (виалы) с пробами, 2 игла для отбора проб, 3 гамильтоновский шприц, 4 распределительный 6 ти клапанный кран. Столик для нанесения образцов на пластины (с подогревом) Камера для окрашивания пластин
Оборудование для нанесения образцов Торрированные стеклянные капилляры Шприцевой дозатор "MULTISTEP-50" в комплекте с микрошприцем V=1 мкл Принципиальная схема автосемплера, где: 1 флаконы (виалы) с пробами, 2 игла для отбора проб, 3 гамильтоновский шприц, 4 распределительный 6 ти клапанный кран. Столик для нанесения образцов на пластины (с подогревом) Камера для окрашивания пластин
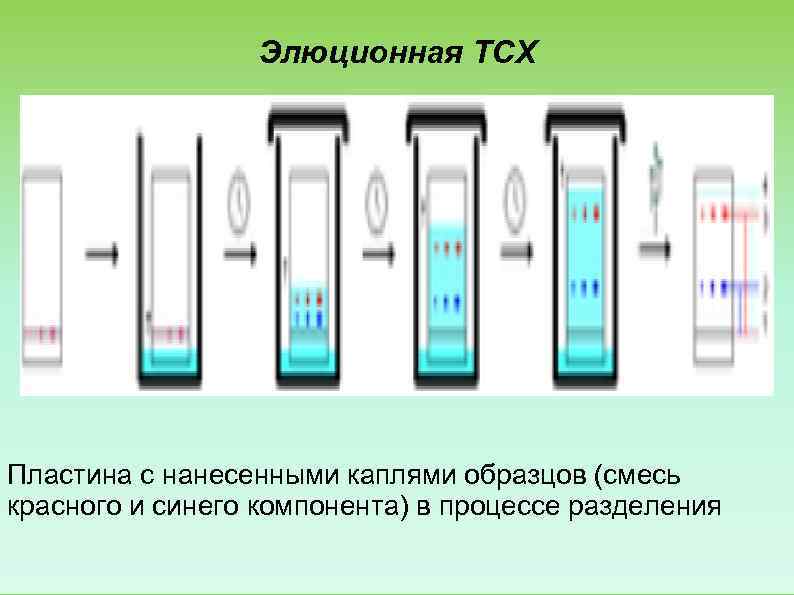
 Элюционная ТСХ Пластина с нанесенными каплями образцов (смесь красного и синего компонента) в процессе разделения
Элюционная ТСХ Пластина с нанесенными каплями образцов (смесь красного и синего компонента) в процессе разделения
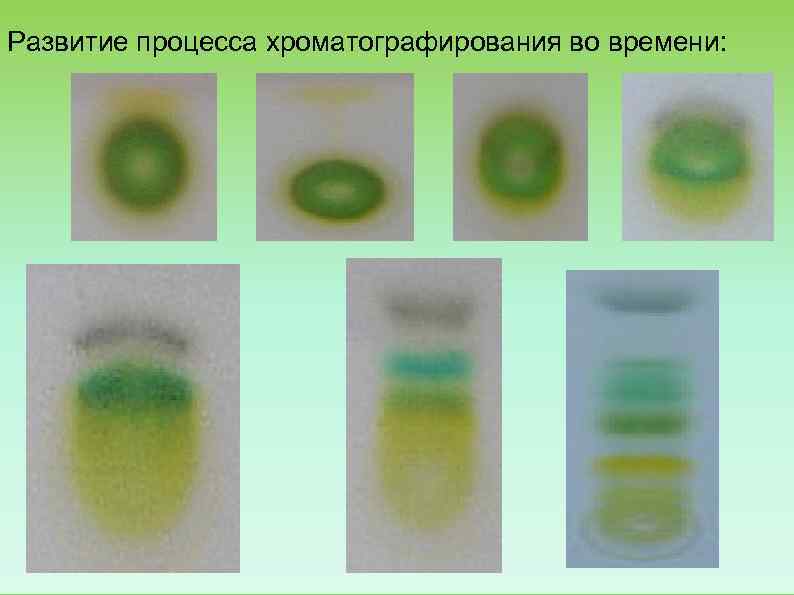
 Развитие процесса хроматографирования во времени:
Развитие процесса хроматографирования во времени:
 Камеры для ТСХ Набор для ТСХ
Камеры для ТСХ Набор для ТСХ
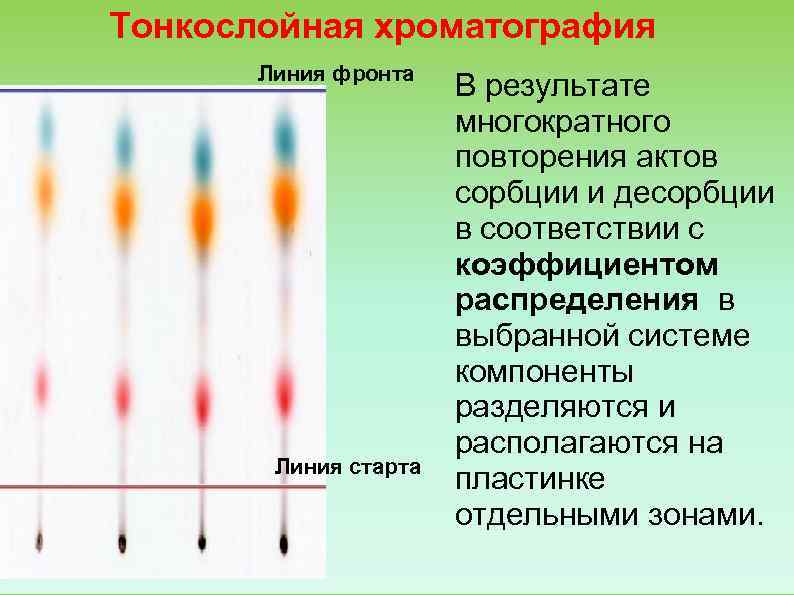
 Тонкослойная хроматография Линия фронта В результате многократного повторения актов сорбции и десорбции в соответствии с коэффициентом распределения в выбранной системе компоненты разделяются и располагаются на Линия старта пластинке отдельными зонами.
Тонкослойная хроматография Линия фронта В результате многократного повторения актов сорбции и десорбции в соответствии с коэффициентом распределения в выбранной системе компоненты разделяются и располагаются на Линия старта пластинке отдельными зонами.
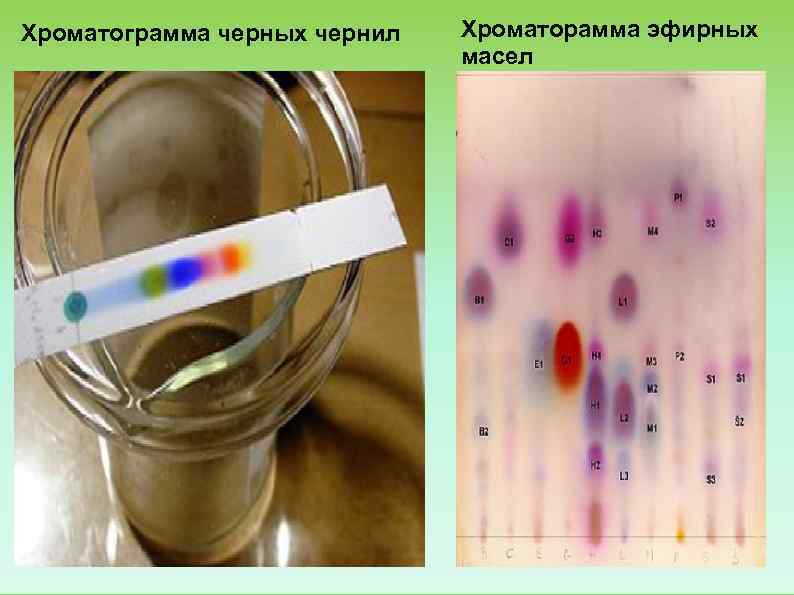
 Хроматограмма черных чернил Хроматорамма эфирных масел
Хроматограмма черных чернил Хроматорамма эфирных масел
 Хроматограмма, полученная при разделении смеси трех компонентов Положение хроматографи ческих зон характеризует Rf отношение пути li, пройденного центром зоны i го компонента от линии старта, к пути l, пройден ному элюентом: Rf = li/l;
Хроматограмма, полученная при разделении смеси трех компонентов Положение хроматографи ческих зон характеризует Rf отношение пути li, пройденного центром зоны i го компонента от линии старта, к пути l, пройден ному элюентом: Rf = li/l;
 Величина Rf зависит от коэффициента распределения (адсорбции) и от соотношения объемов подвижной и неподвижной фаз. В стандартных условиях величина Rf постоянна для данного вещества и используется для идентификации последнего.
Величина Rf зависит от коэффициента распределения (адсорбции) и от соотношения объемов подвижной и неподвижной фаз. В стандартных условиях величина Rf постоянна для данного вещества и используется для идентификации последнего.
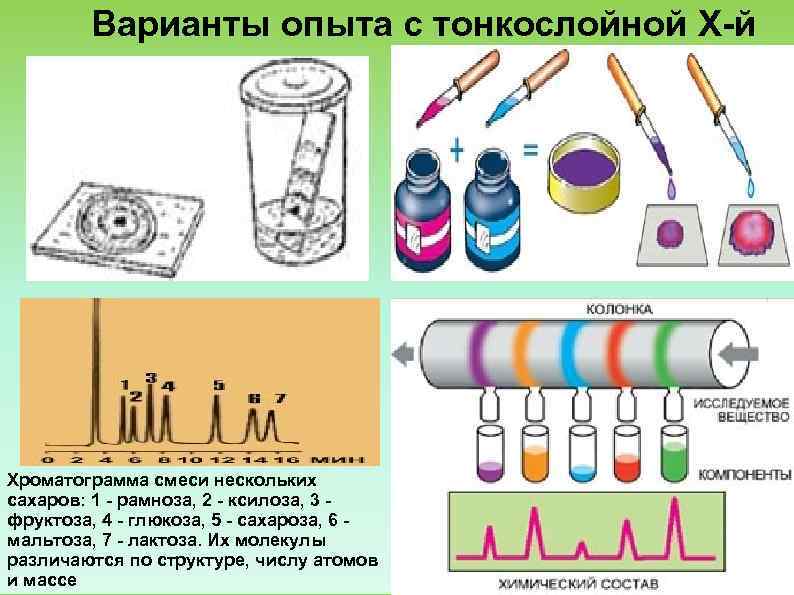
 Варианты опыта с тонкослойной Х й Хроматограмма смеси нескольких сахаров: 1 рамноза, 2 ксилоза, 3 фруктоза, 4 глюкоза, 5 сахароза, 6 мальтоза, 7 лактоза. Их молекулы различаются по структуре, числу атомов и массе
Варианты опыта с тонкослойной Х й Хроматограмма смеси нескольких сахаров: 1 рамноза, 2 ксилоза, 3 фруктоза, 4 глюкоза, 5 сахароза, 6 мальтоза, 7 лактоза. Их молекулы различаются по структуре, числу атомов и массе
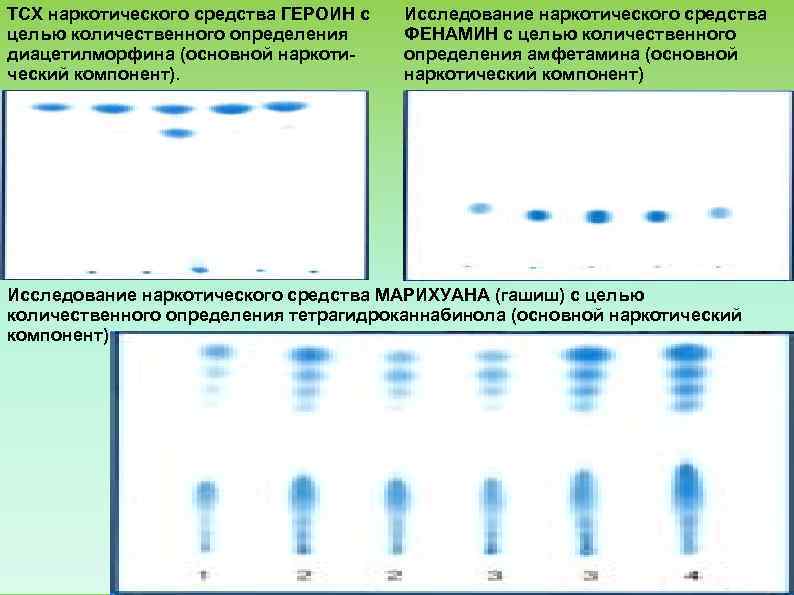
 ТСХ наркотического средства ГЕРОИН с Исследование наркотического средства целью количественного определения ФЕНАМИН с целью количественного диацетилморфина (основной наркоти определения амфетамина (основной ческий компонент). наркотический компонент) Исследование наркотического средства МАРИХУАНА (гашиш) с целью количественного определения тетрагидроканнабинола (основной наркотический компонент).
ТСХ наркотического средства ГЕРОИН с Исследование наркотического средства целью количественного определения ФЕНАМИН с целью количественного диацетилморфина (основной наркоти определения амфетамина (основной ческий компонент). наркотический компонент) Исследование наркотического средства МАРИХУАНА (гашиш) с целью количественного определения тетрагидроканнабинола (основной наркотический компонент).
 Достоинства ТСХ: 1. простота, 2. экономичность, 3. доступность оборудования, 4. экспрессность (продолжительность разделения 10 100 мин), 5. высокие производительность и эффективность разделения, 6. наглядность результатов разделения, 7. простота обнаружения хроматографичских зон. Применение. ТСХ: 1. для разделения и анализа органических, и неорганических веществ: катионов и анионов, полимеров, пестицидов, аминокислот, липидов, алкалоидов и т. д. 2. анализ микрообъекты, 3. оценкат чистоты препаратов, лек. Средств. 4. контроль технологических процессов, 5. анализ состава сточных вод.
Достоинства ТСХ: 1. простота, 2. экономичность, 3. доступность оборудования, 4. экспрессность (продолжительность разделения 10 100 мин), 5. высокие производительность и эффективность разделения, 6. наглядность результатов разделения, 7. простота обнаружения хроматографичских зон. Применение. ТСХ: 1. для разделения и анализа органических, и неорганических веществ: катионов и анионов, полимеров, пестицидов, аминокислот, липидов, алкалоидов и т. д. 2. анализ микрообъекты, 3. оценкат чистоты препаратов, лек. Средств. 4. контроль технологических процессов, 5. анализ состава сточных вод.
 Гель-фильтрационная, или молекулярно-ситовая, хроматография. Принцип разделения в таких системах несколько иной, чем в предыдущих случаях. Неподвижной фазой являются материалы, обычно гели, со строго контролируемой пористостью, в результате чего одни компоненты смеси в соответствии с размером и формой молекул могут проникать между частицами геля, а другие не могут. Наиболее часто этот вид хроматографии используется для разделения высокомолекулярных соединений. Один из вариантов применения этого метода – определение молекулярных масс разделяемых веществ, часто необходимых для химических исследований.
Гель-фильтрационная, или молекулярно-ситовая, хроматография. Принцип разделения в таких системах несколько иной, чем в предыдущих случаях. Неподвижной фазой являются материалы, обычно гели, со строго контролируемой пористостью, в результате чего одни компоненты смеси в соответствии с размером и формой молекул могут проникать между частицами геля, а другие не могут. Наиболее часто этот вид хроматографии используется для разделения высокомолекулярных соединений. Один из вариантов применения этого метода – определение молекулярных масс разделяемых веществ, часто необходимых для химических исследований.
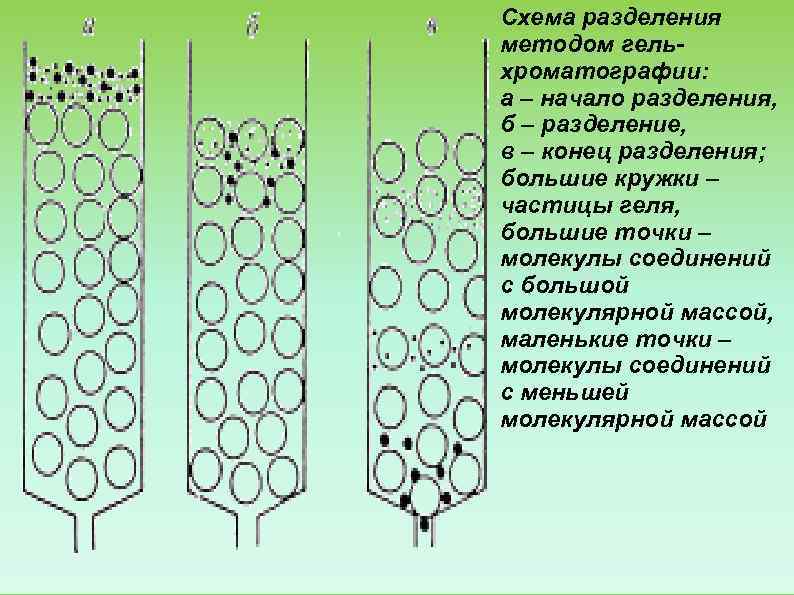
 Схема разделения методом гель- хроматографии: а – начало разделения, б – разделение, в – конец разделения; большие кружки – частицы геля, большие точки – молекулы соединений с большой молекулярной массой, маленькие точки – молекулы соединений с меньшей молекулярной массой
Схема разделения методом гель- хроматографии: а – начало разделения, б – разделение, в – конец разделения; большие кружки – частицы геля, большие точки – молекулы соединений с большой молекулярной массой, маленькие точки – молекулы соединений с меньшей молекулярной массой
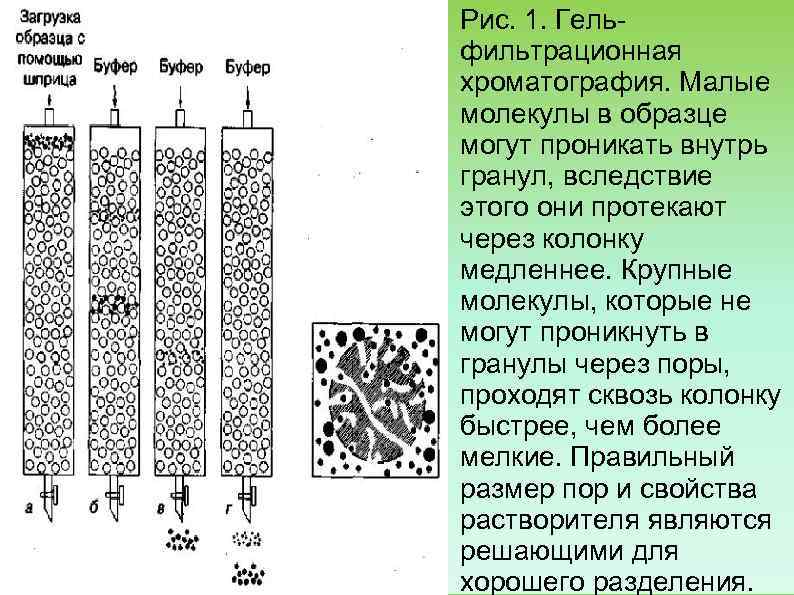
 Рис. 1. Гель фильтрационная хроматография. Малые молекулы в образце могут проникать внутрь гранул, вследствие этого они протекают через колонку медленнее. Крупные молекулы, которые не могут проникнуть в гранулы через поры, проходят сквозь колонку быстрее, чем более мелкие. Правильный размер пор и свойства растворителя являются решающими для хорошего разделения.
Рис. 1. Гель фильтрационная хроматография. Малые молекулы в образце могут проникать внутрь гранул, вследствие этого они протекают через колонку медленнее. Крупные молекулы, которые не могут проникнуть в гранулы через поры, проходят сквозь колонку быстрее, чем более мелкие. Правильный размер пор и свойства растворителя являются решающими для хорошего разделения.

