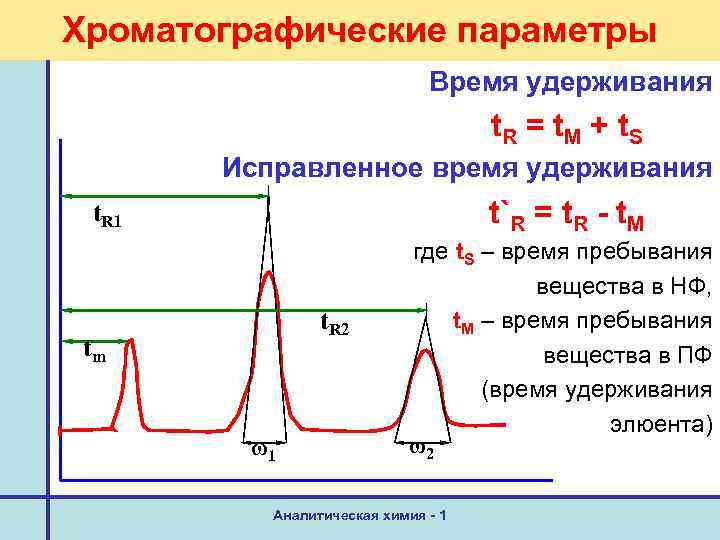
 Хроматографические параметры Время удерживания t. R = t. M + t. S Исправленное время удерживания t`R = t. R - t. M t. R 1 t. R 2 tm ω1 где t. S – время пребывания вещества в НФ, t. M – время пребывания вещества в ПФ (время удерживания элюента) ω2 Аналитическая химия - 1
Хроматографические параметры Время удерживания t. R = t. M + t. S Исправленное время удерживания t`R = t. R - t. M t. R 1 t. R 2 tm ω1 где t. S – время пребывания вещества в НФ, t. M – время пребывания вещества в ПФ (время удерживания элюента) ω2 Аналитическая химия - 1
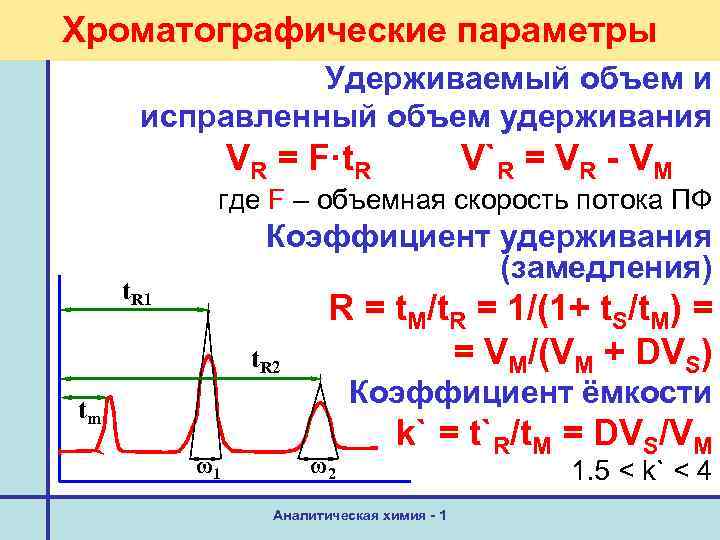 Хроматографические параметры Удерживаемый объем и исправленный объем удерживания VR = F·t. R V`R = VR - VМ где F – объемная скорость потока ПФ Коэффициент удерживания (замедления) t. R 1 t. R 2 R = t. M/t. R = 1/(1+ t. S/t. M) = = VM/(VM + DVS) Коэффициент ёмкости tm ω1 ω2 k` = t`R/t. M = DVS/VM Аналитическая химия - 1 1. 5 < k` < 4
Хроматографические параметры Удерживаемый объем и исправленный объем удерживания VR = F·t. R V`R = VR - VМ где F – объемная скорость потока ПФ Коэффициент удерживания (замедления) t. R 1 t. R 2 R = t. M/t. R = 1/(1+ t. S/t. M) = = VM/(VM + DVS) Коэффициент ёмкости tm ω1 ω2 k` = t`R/t. M = DVS/VM Аналитическая химия - 1 1. 5 < k` < 4
 ЭФФЕКТИВНОСТЬ Теоретическая тарелка H АM Аналитическая химия - 1 AS
ЭФФЕКТИВНОСТЬ Теоретическая тарелка H АM Аналитическая химия - 1 AS
 Эффективность и селективность Число теоретических тарелок N = 16(t. R/ω)2 ВЭТТ Н = L/N где L – длина колонки Разрешение RS ≥ 1. 5 RS = 2(t. R 1 - t. R 2)/(ω1 + ω2) t. R 1 Фактор разделения, или коэффициент селективности t. R 2 tm = k'2/k'1 = t`R 2/t`R 1 разделение невозможно при = 1 ω1 ω2 Аналитическая химия - 1
Эффективность и селективность Число теоретических тарелок N = 16(t. R/ω)2 ВЭТТ Н = L/N где L – длина колонки Разрешение RS ≥ 1. 5 RS = 2(t. R 1 - t. R 2)/(ω1 + ω2) t. R 1 Фактор разделения, или коэффициент селективности t. R 2 tm = k'2/k'1 = t`R 2/t`R 1 разделение невозможно при = 1 ω1 ω2 Аналитическая химия - 1
![Эффективность и селективность RS = 0. 25√N[(α – 1)/α][k'/(1 + k')] Для разделения необходимо Эффективность и селективность RS = 0. 25√N[(α – 1)/α][k'/(1 + k')] Для разделения необходимо](https://present5.com/presentation/-29902326_167436329/image-5.jpg) Эффективность и селективность RS = 0. 25√N[(α – 1)/α][k'/(1 + k')] Для разделения необходимо N = 16 RS 2[(1 + k')/k']2[α/(α – 1)]2 1 2 Аналитическая химия - 1 3
Эффективность и селективность RS = 0. 25√N[(α – 1)/α][k'/(1 + k')] Для разделения необходимо N = 16 RS 2[(1 + k')/k']2[α/(α – 1)]2 1 2 Аналитическая химия - 1 3
 Качественный анализ Времена удерживания Корреляционные зависимости параметров удерживания Индекс удерживания Ковача (ИУК) In = 100 n t`Rn < t`Rx < t`R(n+1) (lgt`Rx – lgt`Rn) Ix = 100 n + 100 ———— (lgt`R(n+1) – lgt`Rn) Аналитическая химия - 1
Качественный анализ Времена удерживания Корреляционные зависимости параметров удерживания Индекс удерживания Ковача (ИУК) In = 100 n t`Rn < t`Rx < t`R(n+1) (lgt`Rx – lgt`Rn) Ix = 100 n + 100 ———— (lgt`R(n+1) – lgt`Rn) Аналитическая химия - 1
 Количественный анализ По площади или высоте хроматографического пика S S = f (C) h Методы количественного анализа Метод нормировки Метод абсолютной калибровки Метод внутреннего стандарта Аналитическая химия - 1
Количественный анализ По площади или высоте хроматографического пика S S = f (C) h Методы количественного анализа Метод нормировки Метод абсолютной калибровки Метод внутреннего стандарта Аналитическая химия - 1
 Теории хроматографии Изотерма сорбции – зависимость концентрации вещества в НФ от его концентрации в ПФ при t 0 = const CS Коэффициент распределения – угол наклона CM изотермы: 1 2 3 Аналитическая химия - 1 D = d. CS/d. CM
Теории хроматографии Изотерма сорбции – зависимость концентрации вещества в НФ от его концентрации в ПФ при t 0 = const CS Коэффициент распределения – угол наклона CM изотермы: 1 2 3 Аналитическая химия - 1 D = d. CS/d. CM
 Теории хроматографии ТЕОРИЯ ТЕОРЕТИЧЕСКИХ ТАРЕЛОК - колонка состоит из определенного числа ТТ - равновесие на каждой ТТ считается достигнутым до того, как ПФ переместиться на следующую ТТ (т. е. мгновенно) - на каждой ТТ число частиц сорбируемых веществ < числа сорбируемых частиц элюента - все процессы в колонке независимы друг от друга Аналитическая химия - 1
Теории хроматографии ТЕОРИЯ ТЕОРЕТИЧЕСКИХ ТАРЕЛОК - колонка состоит из определенного числа ТТ - равновесие на каждой ТТ считается достигнутым до того, как ПФ переместиться на следующую ТТ (т. е. мгновенно) - на каждой ТТ число частиц сорбируемых веществ < числа сорбируемых частиц элюента - все процессы в колонке независимы друг от друга Аналитическая химия - 1
 Теории хроматографии КИНЕТИЧЕСКАЯ ТЕОРИЯ H = A + B/v + Cv где А –вихревая диффузия, B/v – молекулярная диффузия, Cv – отклонение от сорбционного равновесия (сопротивление массопереносу), v – скорость потока Аналитическая химия - 1
Теории хроматографии КИНЕТИЧЕСКАЯ ТЕОРИЯ H = A + B/v + Cv где А –вихревая диффузия, B/v – молекулярная диффузия, Cv – отклонение от сорбционного равновесия (сопротивление массопереносу), v – скорость потока Аналитическая химия - 1
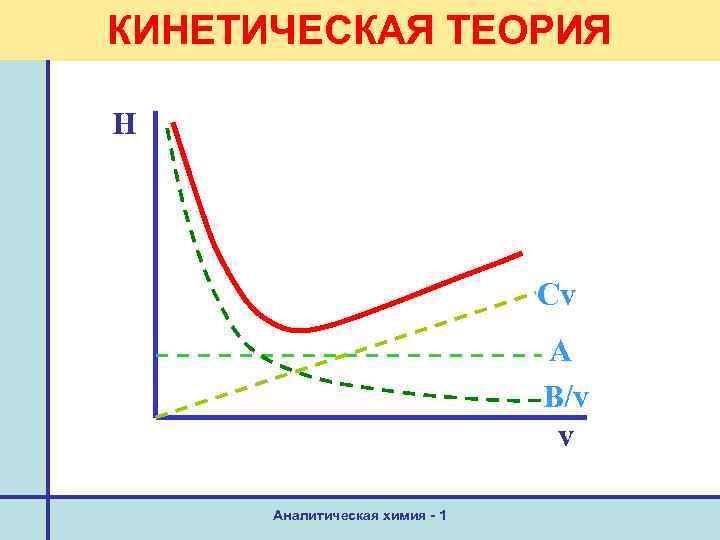 КИНЕТИЧЕСКАЯ ТЕОРИЯ H Cv A B/v v Аналитическая химия - 1
КИНЕТИЧЕСКАЯ ТЕОРИЯ H Cv A B/v v Аналитическая химия - 1