BAC_chromo.ppt
- Количество слайдов: 127
 ХРОМАТОГРАФИЧЕСКИЕ МЕТОДЫ РАЗДЕЛЕНИЯ ВЕЩЕСТВ
ХРОМАТОГРАФИЧЕСКИЕ МЕТОДЫ РАЗДЕЛЕНИЯ ВЕЩЕСТВ
 Как все начиналось Впервые термин «хроматография» использовал Михаил Семенович Цвет в своем сообщение о разделении растительных пигментов на конференции в 1903 г.
Как все начиналось Впервые термин «хроматография» использовал Михаил Семенович Цвет в своем сообщение о разделении растительных пигментов на конференции в 1903 г.
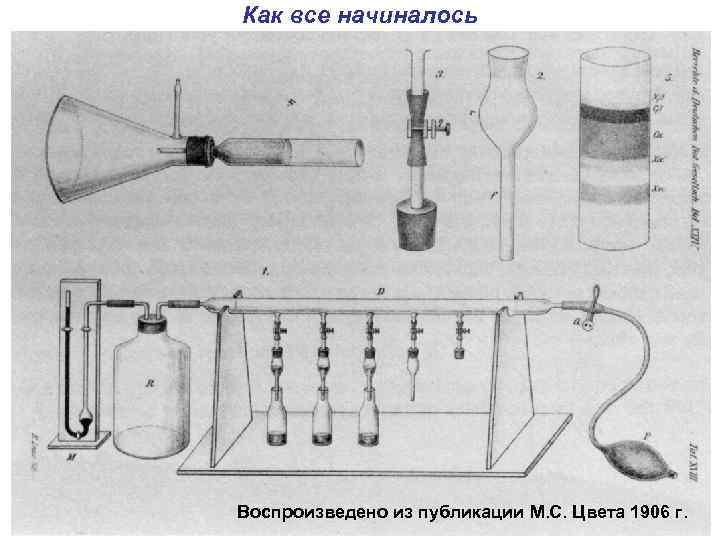 Как все начиналось Воспроизведено из публикации М. С. Цвета 1906 г.
Как все начиналось Воспроизведено из публикации М. С. Цвета 1906 г.
 Разделение методом адсорбционной хроматографии по М. С. Цвету а – адсорбент (сорбент, обменник, смола) б – хроматографическая колонка в – элюат г – делительная воронка (резервуар для растворителя) д – элюент е – хлопковая вата (поддерживающий пористый материал) Смесь веществ А, Б и В, предварительно адсорбированная в зоне Г, разделяется при элюировании растворителем Д (элюентом) на независимые зоны, движущиеся по направлению к выходу из колонки
Разделение методом адсорбционной хроматографии по М. С. Цвету а – адсорбент (сорбент, обменник, смола) б – хроматографическая колонка в – элюат г – делительная воронка (резервуар для растворителя) д – элюент е – хлопковая вата (поддерживающий пористый материал) Смесь веществ А, Б и В, предварительно адсорбированная в зоне Г, разделяется при элюировании растворителем Д (элюентом) на независимые зоны, движущиеся по направлению к выходу из колонки
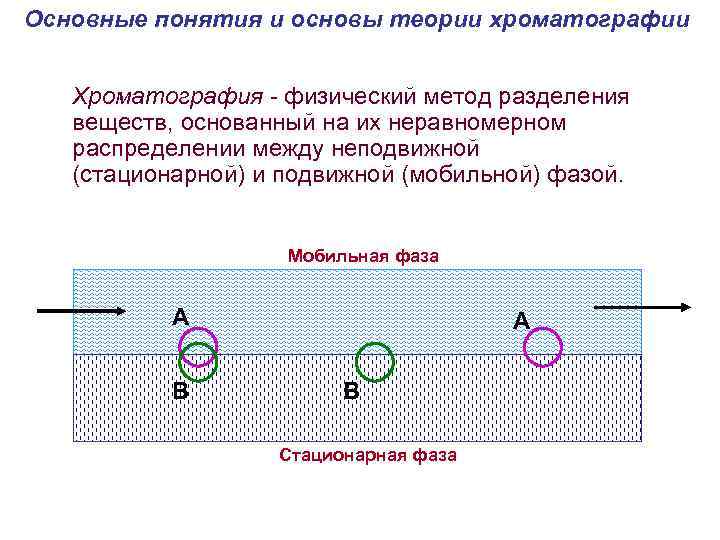 Основные понятия и основы теории хроматографии Хроматография - физический метод разделения веществ, основанный на их неравномерном распределении между неподвижной (стационарной) и подвижной (мобильной) фазой. Мобильная фаза A B Стационарная фаза
Основные понятия и основы теории хроматографии Хроматография - физический метод разделения веществ, основанный на их неравномерном распределении между неподвижной (стационарной) и подвижной (мобильной) фазой. Мобильная фаза A B Стационарная фаза
 Основные понятия и основы теории хроматографии Сечение хроматографической колонки 1. Неподвижная фаза занимает определенный объем колонки и определенную площадь любого сечения колонки 2. Диффузия молекул от подвижной к неподвижной фазе и обратно протекает свободно и (благодаря малым размерам гранул) на небольших расстояниях 3. Для каждого вещества имеет место определенное соотношение между степенями его сродства к подвижной и неподвижной фазе системы. Количественной характеристикой равновесного распределения вещества между фазами является константа распределения K=Сs/Сm, где Сs и Сm– концентрация вещества в стационарной и мобильной фазе соответственно.
Основные понятия и основы теории хроматографии Сечение хроматографической колонки 1. Неподвижная фаза занимает определенный объем колонки и определенную площадь любого сечения колонки 2. Диффузия молекул от подвижной к неподвижной фазе и обратно протекает свободно и (благодаря малым размерам гранул) на небольших расстояниях 3. Для каждого вещества имеет место определенное соотношение между степенями его сродства к подвижной и неподвижной фазе системы. Количественной характеристикой равновесного распределения вещества между фазами является константа распределения K=Сs/Сm, где Сs и Сm– концентрация вещества в стационарной и мобильной фазе соответственно.
 Сказка о прекрасной принцессе
Сказка о прекрасной принцессе
 Осы и пчелы http: //antoine. frostburg. edu/chem/senese/101/matter/chromatography. shtml
Осы и пчелы http: //antoine. frostburg. edu/chem/senese/101/matter/chromatography. shtml
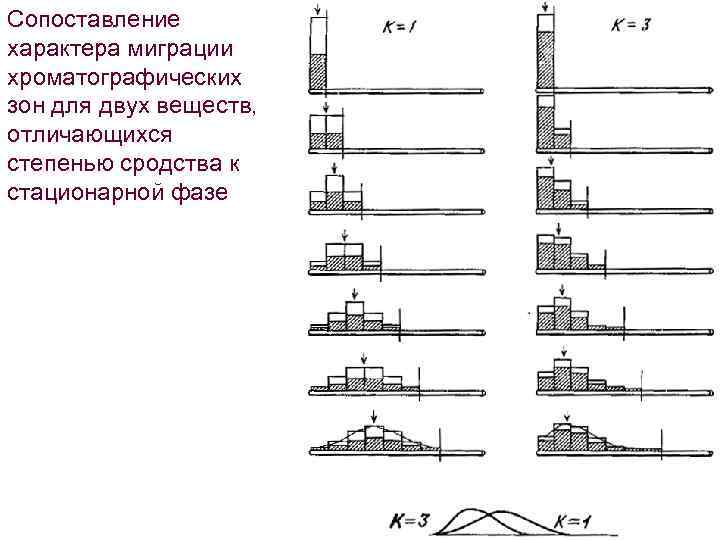 Сопоставление характера миграции хроматографических зон для двух веществ, отличающихся степенью сродства к стационарной фазе
Сопоставление характера миграции хроматографических зон для двух веществ, отличающихся степенью сродства к стационарной фазе
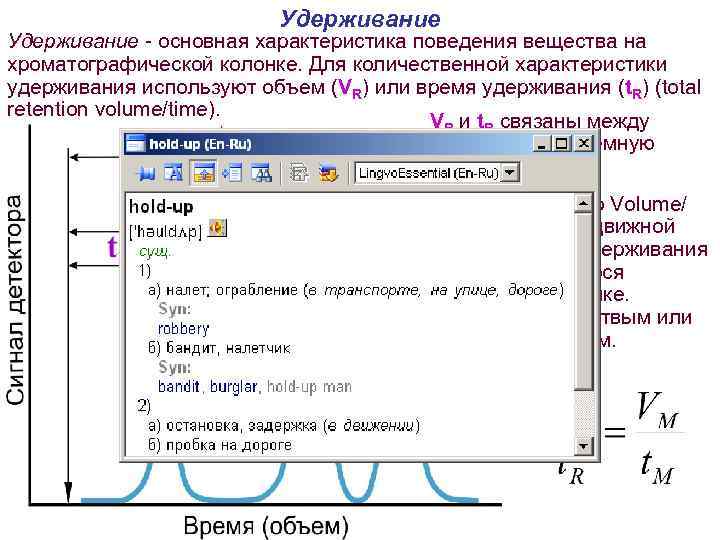 Удерживание - основная характеристика поведения вещества на хроматографической колонке. Для количественной характеристики удерживания используют объем (VR) или время удерживания (t. R) (total retention volume/time). VR и t. R связаны между собой через объемную скорость (F). VM и t. M - Hold-Up Volume/ Time – объем подвижной фазы и время удерживания не сорбирующегося вещества в колонке. VM называют мертвым или нулевым объемом.
Удерживание - основная характеристика поведения вещества на хроматографической колонке. Для количественной характеристики удерживания используют объем (VR) или время удерживания (t. R) (total retention volume/time). VR и t. R связаны между собой через объемную скорость (F). VM и t. M - Hold-Up Volume/ Time – объем подвижной фазы и время удерживания не сорбирующегося вещества в колонке. VM называют мертвым или нулевым объемом.
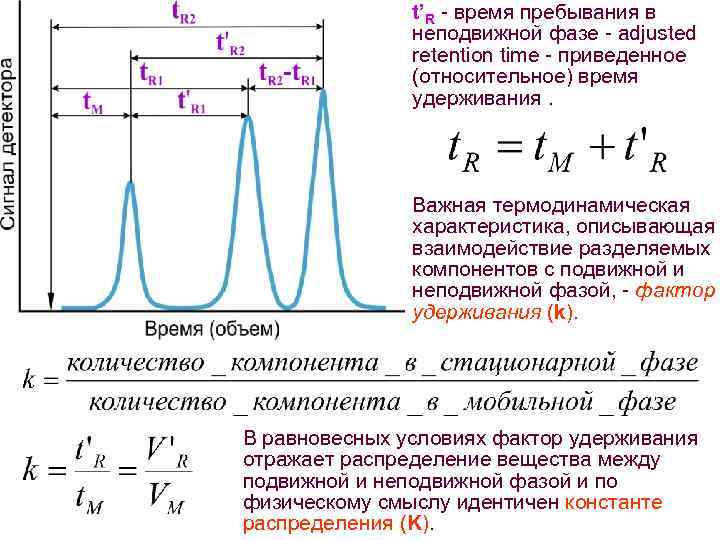 t’R - время пребывания в неподвижной фазе - adjusted retention time - приведенное (относительное) время удерживания. Важная термодинамическая характеристика, описывающая взаимодействие разделяемых компонентов с подвижной и неподвижной фазой, - фактор удерживания (k). В равновесных условиях фактор удерживания отражает распределение вещества между подвижной и неподвижной фазой и по физическому смыслу идентичен константе распределения (K).
t’R - время пребывания в неподвижной фазе - adjusted retention time - приведенное (относительное) время удерживания. Важная термодинамическая характеристика, описывающая взаимодействие разделяемых компонентов с подвижной и неподвижной фазой, - фактор удерживания (k). В равновесных условиях фактор удерживания отражает распределение вещества между подвижной и неподвижной фазой и по физическому смыслу идентичен константе распределения (K).
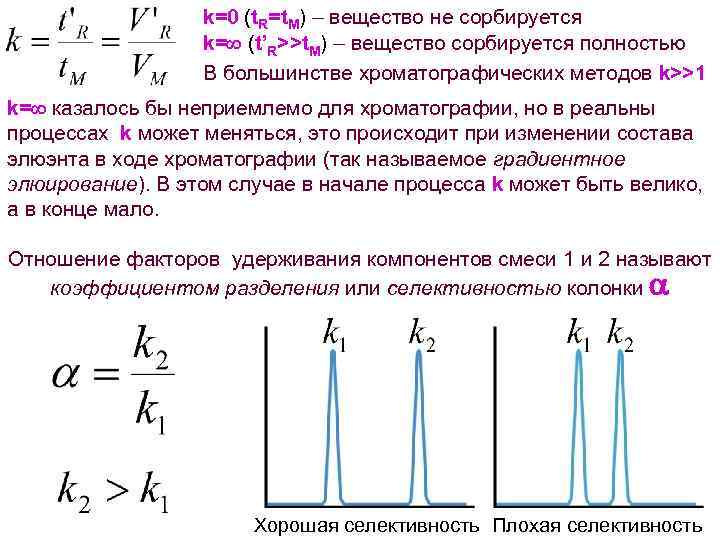 k=0 (t. R=t. M) – вещество не сорбируется k= (t’R>>t. M) – вещество сорбируется полностью В большинстве хроматографических методов k>>1 k= казалось бы неприемлемо для хроматографии, но в реальны процессах k может меняться, это происходит при изменении состава элюэнта в ходе хроматографии (так называемое градиентное элюирование). В этом случае в начале процесса k может быть велико, а в конце мало. Отношение факторов удерживания компонентов смеси 1 и 2 называют коэффициентом разделения или селективностью колонки a Хорошая селективность Плохая селективность
k=0 (t. R=t. M) – вещество не сорбируется k= (t’R>>t. M) – вещество сорбируется полностью В большинстве хроматографических методов k>>1 k= казалось бы неприемлемо для хроматографии, но в реальны процессах k может меняться, это происходит при изменении состава элюэнта в ходе хроматографии (так называемое градиентное элюирование). В этом случае в начале процесса k может быть велико, а в конце мало. Отношение факторов удерживания компонентов смеси 1 и 2 называют коэффициентом разделения или селективностью колонки a Хорошая селективность Плохая селективность
 Разрешение или разрешение пиков – характеристика эффективности хроматографического разделения. Разрешение определяется двумя процессами: расхождением зон за счет неравномерного распределения разделяемых веществ между фазами и, так называемым, размыванием зон. Расхождение пиков зависит от селективности колонки и ее длины: Т. к. скорость перемещения фронта подвижной фазы где L – длина колонки. ,
Разрешение или разрешение пиков – характеристика эффективности хроматографического разделения. Разрешение определяется двумя процессами: расхождением зон за счет неравномерного распределения разделяемых веществ между фазами и, так называемым, размыванием зон. Расхождение пиков зависит от селективности колонки и ее длины: Т. к. скорость перемещения фронта подвижной фазы где L – длина колонки. ,
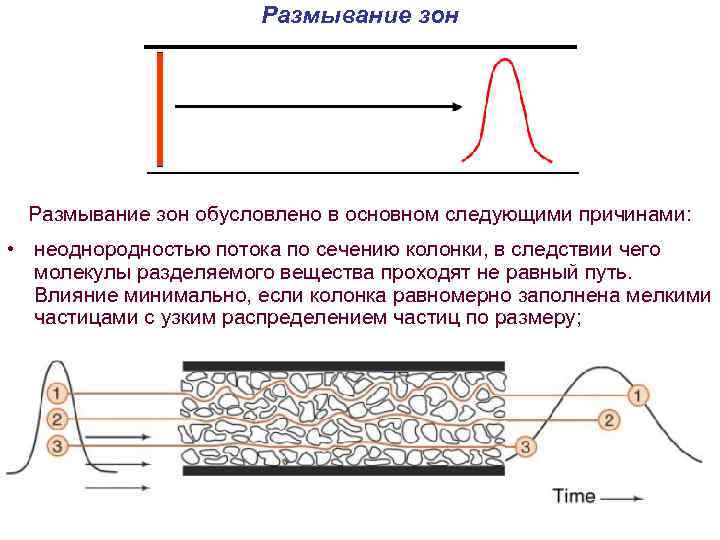 Размывание зон обусловлено в основном следующими причинами: • неоднородностью потока по сечению колонки, в следствии чего молекулы разделяемого вещества проходят не равный путь. Влияние минимально, если колонка равномерно заполнена мелкими частицами с узким распределением частиц по размеру;
Размывание зон обусловлено в основном следующими причинами: • неоднородностью потока по сечению колонки, в следствии чего молекулы разделяемого вещества проходят не равный путь. Влияние минимально, если колонка равномерно заполнена мелкими частицами с узким распределением частиц по размеру;
 Влияние неравномерности потока минимально, если колонка равномерно заполнена мелкими частицами с узким распределением частиц по размеру Сферический Нерегулярный 3, 5 мкм 10 мкм
Влияние неравномерности потока минимально, если колонка равномерно заполнена мелкими частицами с узким распределением частиц по размеру Сферический Нерегулярный 3, 5 мкм 10 мкм
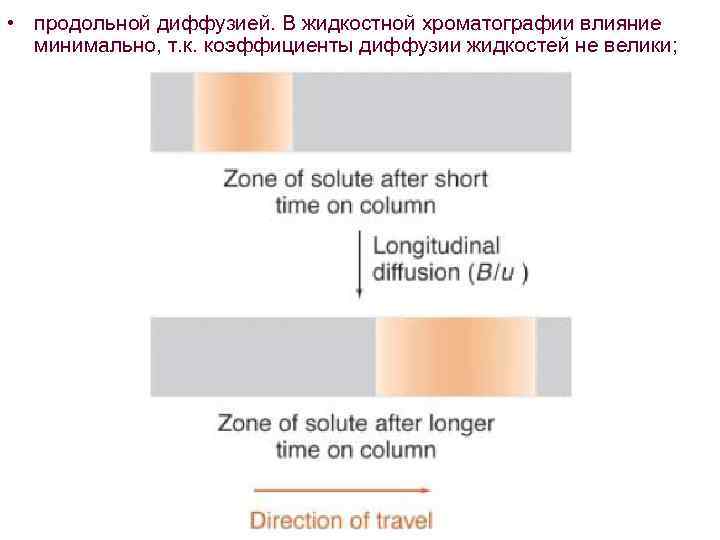 • продольной диффузией. В жидкостной хроматографии влияние минимально, т. к. коэффициенты диффузии жидкостей не велики;
• продольной диффузией. В жидкостной хроматографии влияние минимально, т. к. коэффициенты диффузии жидкостей не велики;
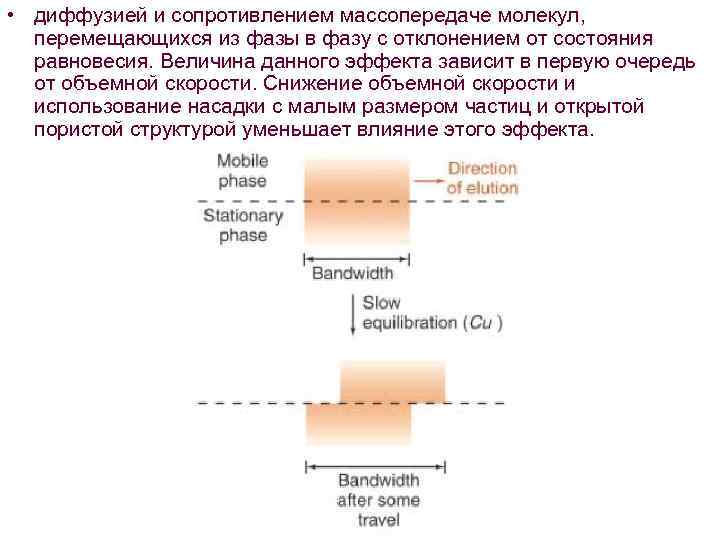 • диффузией и сопротивлением массопередаче молекул, перемещающихся из фазы в фазу с отклонением от состояния равновесия. Величина данного эффекта зависит в первую очередь от объемной скорости. Снижение объемной скорости и использование насадки с малым размером частиц и открытой пористой структурой уменьшает влияние этого эффекта.
• диффузией и сопротивлением массопередаче молекул, перемещающихся из фазы в фазу с отклонением от состояния равновесия. Величина данного эффекта зависит в первую очередь от объемной скорости. Снижение объемной скорости и использование насадки с малым размером частиц и открытой пористой структурой уменьшает влияние этого эффекта.
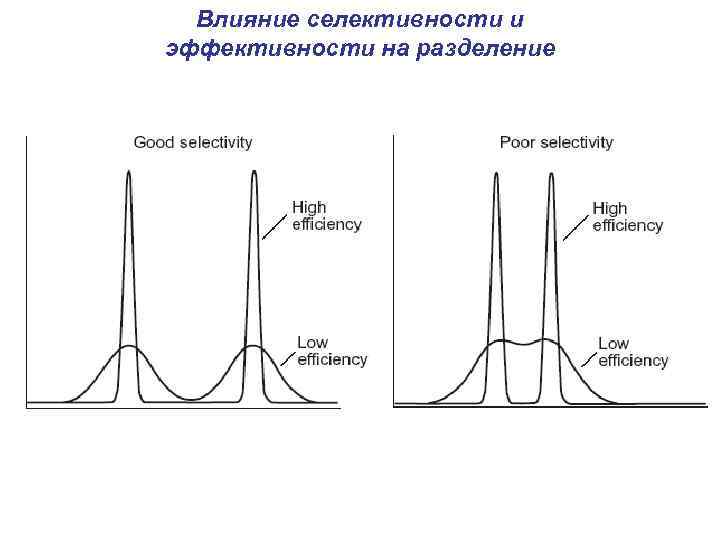 Влияние селективности и эффективности на разделение
Влияние селективности и эффективности на разделение
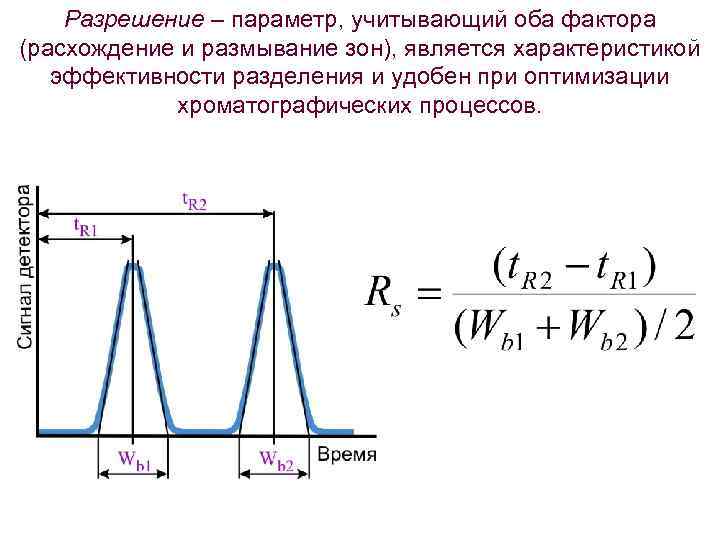 Разрешение – параметр, учитывающий оба фактора (расхождение и размывание зон), является характеристикой эффективности разделения и удобен при оптимизации хроматографических процессов.
Разрешение – параметр, учитывающий оба фактора (расхождение и размывание зон), является характеристикой эффективности разделения и удобен при оптимизации хроматографических процессов.
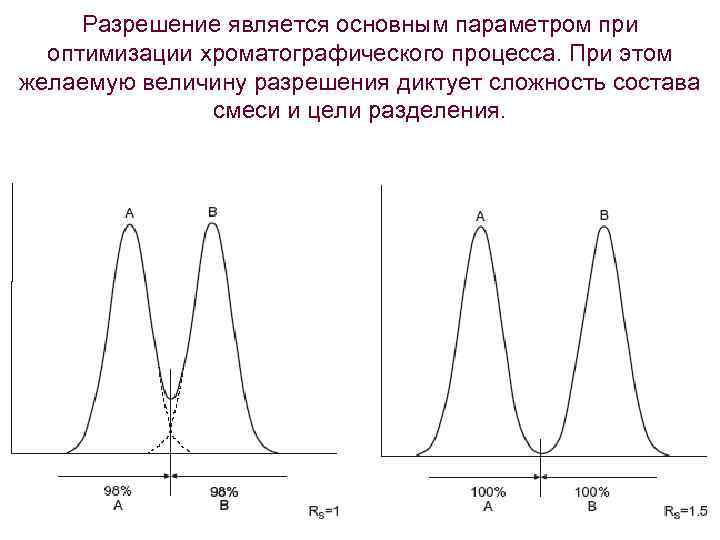 Разрешение является основным параметром при оптимизации хроматографического процесса. При этом желаемую величину разрешения диктует сложность состава смеси и цели разделения.
Разрешение является основным параметром при оптимизации хроматографического процесса. При этом желаемую величину разрешения диктует сложность состава смеси и цели разделения.
 Понятие о теоретической тарелке Математическая модель хроматографической колонки, представляет собой колонку с тарелками на каждой из которых достигается равновесие между подвижной и неподвижной фазой. Не следует упускать из виду и реальный смысл этого понятия. Высота эквивалентная теоретической тарелке (ВЭТТ) параметр хроматографического процесса, учитывающий ряд физических факторов, размывающих зону, а его размерность совпадает с размерностью длины. Для характеристики хроматографического процесса обычно используют два параметра ВЭТТ - H (сейчас для ВЭЖХ H<20 мкм) и число ТТ - N, эти значения связаны через длину колонки L=NH.
Понятие о теоретической тарелке Математическая модель хроматографической колонки, представляет собой колонку с тарелками на каждой из которых достигается равновесие между подвижной и неподвижной фазой. Не следует упускать из виду и реальный смысл этого понятия. Высота эквивалентная теоретической тарелке (ВЭТТ) параметр хроматографического процесса, учитывающий ряд физических факторов, размывающих зону, а его размерность совпадает с размерностью длины. Для характеристики хроматографического процесса обычно используют два параметра ВЭТТ - H (сейчас для ВЭЖХ H<20 мкм) и число ТТ - N, эти значения связаны через длину колонки L=NH.
 Понятие о теоретической тарелке Число тарелок может быть рассчитано исходя из времени удерживания и размывания хроматографической зоны, характеристикой которого является ширина пика. Это коэффициент пропорциональности между этими двумя величинами. Часто оперируют понятием эффективная теоретическая тарелка (Neff, Heff), «эффективная» означает, что количество тарелок рассчитано из приведенного времени (объема) удерживания t’R, а не из t. R, поскольку в реальных условиях t. R снятое с хроматограммы не соответствует t. R используемому в теории.
Понятие о теоретической тарелке Число тарелок может быть рассчитано исходя из времени удерживания и размывания хроматографической зоны, характеристикой которого является ширина пика. Это коэффициент пропорциональности между этими двумя величинами. Часто оперируют понятием эффективная теоретическая тарелка (Neff, Heff), «эффективная» означает, что количество тарелок рассчитано из приведенного времени (объема) удерживания t’R, а не из t. R, поскольку в реальных условиях t. R снятое с хроматограммы не соответствует t. R используемому в теории.
 Классификация хроматографических методов 1. По характеру фаз, между которыми осуществляется процесс разделение Жидкостная хроматография – мобильная фаза жидкость Жидко(мобильная фаза) - твердофазная (стационарная фаза) хроматография Жидко-жидкостная (жидко-[жидко-твердофазная]) хроматография Газовая хроматография – мобильная фаза газ Газо-твердофазная хроматография Газо-жидкостная (газо-[жидко-твердофазная]) хроматография Cверхкритическая флюидная хроматография – мобильная фаза сверхкритический флюид
Классификация хроматографических методов 1. По характеру фаз, между которыми осуществляется процесс разделение Жидкостная хроматография – мобильная фаза жидкость Жидко(мобильная фаза) - твердофазная (стационарная фаза) хроматография Жидко-жидкостная (жидко-[жидко-твердофазная]) хроматография Газовая хроматография – мобильная фаза газ Газо-твердофазная хроматография Газо-жидкостная (газо-[жидко-твердофазная]) хроматография Cверхкритическая флюидная хроматография – мобильная фаза сверхкритический флюид
 Сверхкритическое состояние вещества Сверхкритическому флюиду соответствует зона на фазовой диаграмме при температуре и давлении выше критического. Для CO 2 Tc=31°C Pc=73 atm Флюид нельзя перевести в жидкое состояние путем повышения давления и в газообразное путем повышения температуры. Выше критической точки вещество приближается по плотности и растворяющей способности к жидкости, а по вязкости к газу, а его коэффициент диффузии имеет промежуточное значение между соответствующими значениями газа и жидкости.
Сверхкритическое состояние вещества Сверхкритическому флюиду соответствует зона на фазовой диаграмме при температуре и давлении выше критического. Для CO 2 Tc=31°C Pc=73 atm Флюид нельзя перевести в жидкое состояние путем повышения давления и в газообразное путем повышения температуры. Выше критической точки вещество приближается по плотности и растворяющей способности к жидкости, а по вязкости к газу, а его коэффициент диффузии имеет промежуточное значение между соответствующими значениями газа и жидкости.
 Классификация хроматографических методов 2. В соответствии с формой стационарной фазы Колоночная хроматография С использованием упакованных колонок С использованием капиллярных колонок (называемых также открытыми трубчатыми) Планарная хроматография Бумажная Тонкослойная (тонкий слой сорбента на подложке)
Классификация хроматографических методов 2. В соответствии с формой стационарной фазы Колоночная хроматография С использованием упакованных колонок С использованием капиллярных колонок (называемых также открытыми трубчатыми) Планарная хроматография Бумажная Тонкослойная (тонкий слой сорбента на подложке)
 Классификация хроматографических методов 3. В соответствии с типом элюции Изократическая Градиентная 4. В соответствии с целью разделения Аналитическая качественная количественная Препаративная 5. В соответствии с давлением мобильной фазы Низкого давления (<5 атм), Среднего (умеренного) давления (до 50 атм) Высокого давления (до 400 атм).
Классификация хроматографических методов 3. В соответствии с типом элюции Изократическая Градиентная 4. В соответствии с целью разделения Аналитическая качественная количественная Препаративная 5. В соответствии с давлением мобильной фазы Низкого давления (<5 атм), Среднего (умеренного) давления (до 50 атм) Высокого давления (до 400 атм).
 Классификация хроматографических методов 6. В соответствии с механизмом удерживания Адсорбционная хроматография Распределительная хроматография Нормально-фазовая хроматография Обращено-фазовая хроматография Ионообменная хроматография Гель-проникающая хроматография (гель-фильтрация, size exclusion chromatography) Аффинная хроматография 7. В соответствии с материалом матрицы сорбентов и обменников
Классификация хроматографических методов 6. В соответствии с механизмом удерживания Адсорбционная хроматография Распределительная хроматография Нормально-фазовая хроматография Обращено-фазовая хроматография Ионообменная хроматография Гель-проникающая хроматография (гель-фильтрация, size exclusion chromatography) Аффинная хроматография 7. В соответствии с материалом матрицы сорбентов и обменников
 Материалы матриц сорбентов и обменников Основные требования к материалам матриц: - химическая инертность в условиях хроматографии - большая удельная площадь поверхности - наличие функциональных групп, позволяющих осуществить модификацию
Материалы матриц сорбентов и обменников Основные требования к материалам матриц: - химическая инертность в условиях хроматографии - большая удельная площадь поверхности - наличие функциональных групп, позволяющих осуществить модификацию
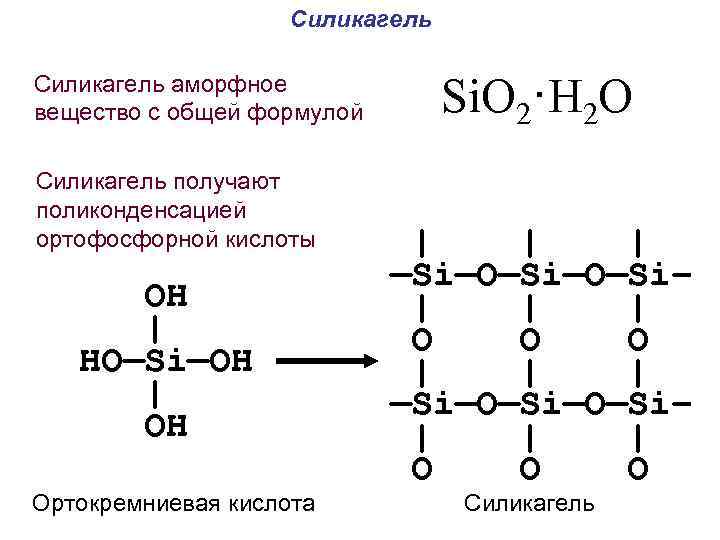 Силикагель аморфное вещество с общей формулой Силикагель получают поликонденсацией ортофосфорной кислоты OH | HO—Si—OH | OH Ортокремниевая кислота Si. O 2·H 2 O | | | —Si—O—Si—O—Si– | | | O O O Силикагель
Силикагель аморфное вещество с общей формулой Силикагель получают поликонденсацией ортофосфорной кислоты OH | HO—Si—OH | OH Ортокремниевая кислота Si. O 2·H 2 O | | | —Si—O—Si—O—Si– | | | O O O Силикагель
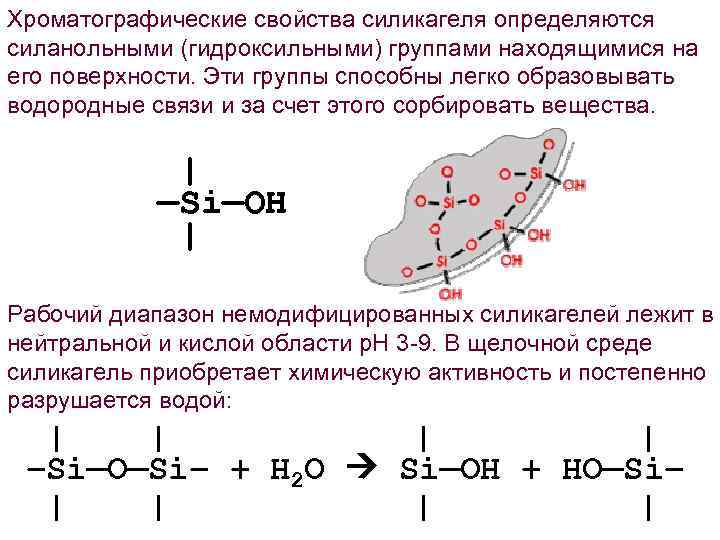 Хроматографические свойства силикагеля определяются силанольными (гидроксильными) группами находящимися на его поверхности. Эти группы способны легко образовывать водородные связи и за счет этого сорбировать вещества. | —Si—OH | Рабочий диапазон немодифицированных силикагелей лежит в нейтральной и кислой области р. Н 3 -9. В щелочной среде силикагель приобретает химическую активность и постепенно разрушается водой: | | –Si—O—Si– + H 2 O Si—OH + HO—Si– | |
Хроматографические свойства силикагеля определяются силанольными (гидроксильными) группами находящимися на его поверхности. Эти группы способны легко образовывать водородные связи и за счет этого сорбировать вещества. | —Si—OH | Рабочий диапазон немодифицированных силикагелей лежит в нейтральной и кислой области р. Н 3 -9. В щелочной среде силикагель приобретает химическую активность и постепенно разрушается водой: | | –Si—O—Si– + H 2 O Si—OH + HO—Si– | |
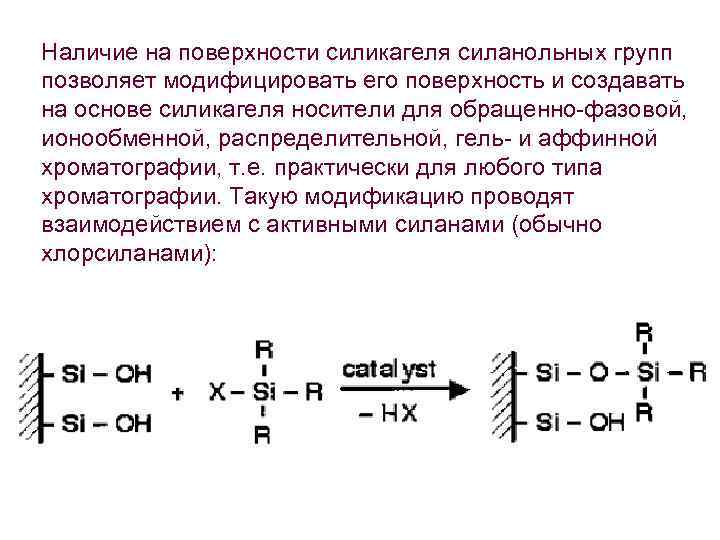 Наличие на поверхности силикагеля силанольных групп позволяет модифицировать его поверхность и создавать на основе силикагеля носители для обращенно-фазовой, ионообменной, распределительной, гель- и аффинной хроматографии, т. е. практически для любого типа хроматографии. Такую модификацию проводят взаимодействием с активными силанами (обычно хлорсиланами):
Наличие на поверхности силикагеля силанольных групп позволяет модифицировать его поверхность и создавать на основе силикагеля носители для обращенно-фазовой, ионообменной, распределительной, гель- и аффинной хроматографии, т. е. практически для любого типа хроматографии. Такую модификацию проводят взаимодействием с активными силанами (обычно хлорсиланами):
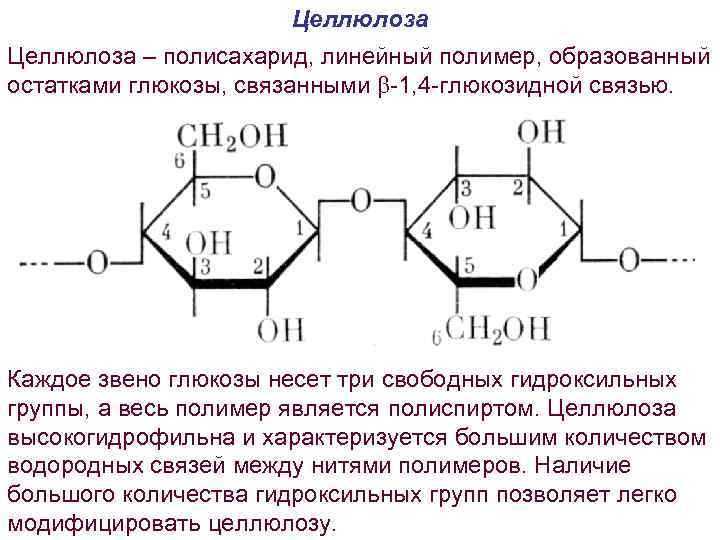 Целлюлоза – полисахарид, линейный полимер, образованный остатками глюкозы, связанными b-1, 4 -глюкозидной связью. Каждое звено глюкозы несет три свободных гидроксильных группы, а весь полимер является полиспиртом. Целлюлоза высокогидрофильна и характеризуется большим количеством водородных связей между нитями полимеров. Наличие большого количества гидроксильных групп позволяет легко модифицировать целлюлозу.
Целлюлоза – полисахарид, линейный полимер, образованный остатками глюкозы, связанными b-1, 4 -глюкозидной связью. Каждое звено глюкозы несет три свободных гидроксильных группы, а весь полимер является полиспиртом. Целлюлоза высокогидрофильна и характеризуется большим количеством водородных связей между нитями полимеров. Наличие большого количества гидроксильных групп позволяет легко модифицировать целлюлозу.
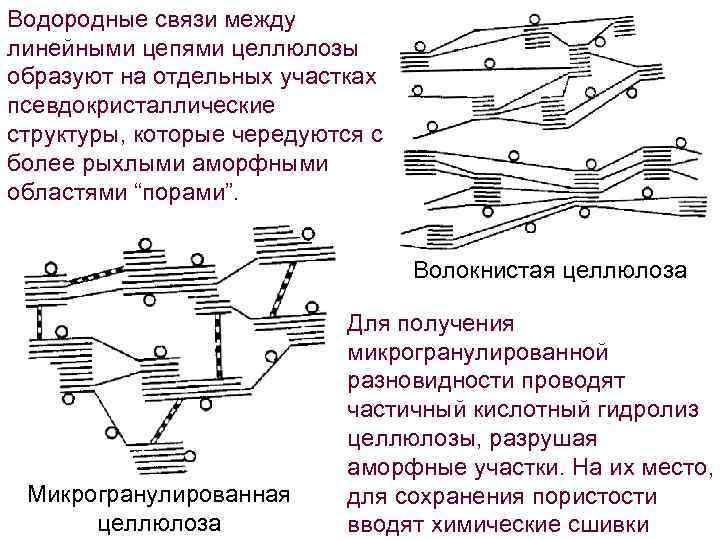 Водородные связи между линейными цепями целлюлозы образуют на отдельных участках псевдокристаллические структуры, которые чередуются с более рыхлыми аморфными областями “порами”. Волокнистая целлюлоза Микрогранулированная целлюлоза Для получения микрогранулированной разновидности проводят частичный кислотный гидролиз целлюлозы, разрушая аморфные участки. На их место, для сохранения пористости вводят химические сшивки
Водородные связи между линейными цепями целлюлозы образуют на отдельных участках псевдокристаллические структуры, которые чередуются с более рыхлыми аморфными областями “порами”. Волокнистая целлюлоза Микрогранулированная целлюлоза Для получения микрогранулированной разновидности проводят частичный кислотный гидролиз целлюлозы, разрушая аморфные участки. На их место, для сохранения пористости вводят химические сшивки
 Целлюлоза достаточно химически инертна и не вступает во взаимодействие, например, с белками и НК. Целлюлоза не устойчива к воздействию сильных кислот, щелочей и окислителей. Она выдерживает контакт с минеральными кислотами с концентрацией 0. 5 н не более 2 ч. Рабочий интервал р. Н для обменников на основе целлюлозы составляет 3 -10. Целлюлоза охотно атакуется микроорганизмами даже на холоду. Целлюлоза главным образом используется для создания ионообменников и для нормально фазовой распределительной хроматографии
Целлюлоза достаточно химически инертна и не вступает во взаимодействие, например, с белками и НК. Целлюлоза не устойчива к воздействию сильных кислот, щелочей и окислителей. Она выдерживает контакт с минеральными кислотами с концентрацией 0. 5 н не более 2 ч. Рабочий интервал р. Н для обменников на основе целлюлозы составляет 3 -10. Целлюлоза охотно атакуется микроорганизмами даже на холоду. Целлюлоза главным образом используется для создания ионообменников и для нормально фазовой распределительной хроматографии
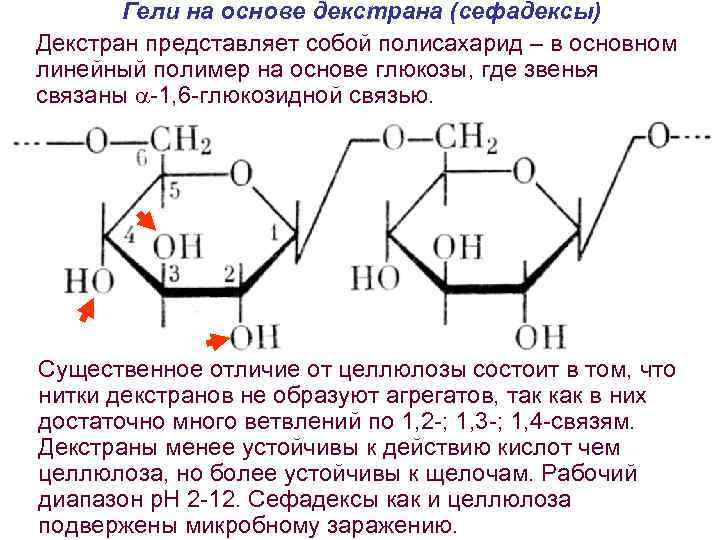 Гели на основе декстрана (сефадексы) Декстран представляет собой полисахарид – в основном линейный полимер на основе глюкозы, где звенья связаны a-1, 6 -глюкозидной связью. Декстран как и целлюлоза - полиатомный спирт с высокой степенью гидрофильности, химически инертный и представляющий возможности для модификации. Существенное отличие от целлюлозы состоит в том, что нитки декстранов не образуют агрегатов, так как в них достаточно много ветвлений по 1, 2 -; 1, 3 -; 1, 4 -связям. Декстраны менее устойчивы к действию кислот чем целлюлоза, но более устойчивы к щелочам. Рабочий диапазон р. Н 2 -12. Сефадексы как и целлюлоза подвержены микробному заражению.
Гели на основе декстрана (сефадексы) Декстран представляет собой полисахарид – в основном линейный полимер на основе глюкозы, где звенья связаны a-1, 6 -глюкозидной связью. Декстран как и целлюлоза - полиатомный спирт с высокой степенью гидрофильности, химически инертный и представляющий возможности для модификации. Существенное отличие от целлюлозы состоит в том, что нитки декстранов не образуют агрегатов, так как в них достаточно много ветвлений по 1, 2 -; 1, 3 -; 1, 4 -связям. Декстраны менее устойчивы к действию кислот чем целлюлоза, но более устойчивы к щелочам. Рабочий диапазон р. Н 2 -12. Сефадексы как и целлюлоза подвержены микробному заражению.
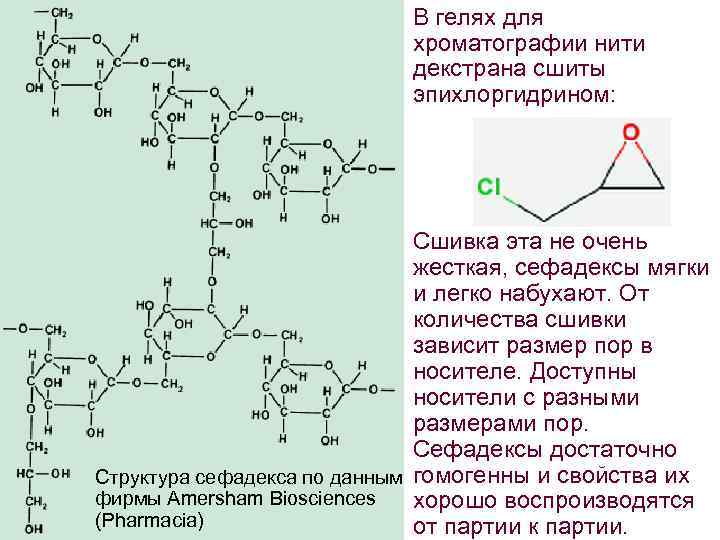 В гелях для хроматографии нити декстрана сшиты эпихлоргидрином: Сшивка эта не очень жесткая, сефадексы мягки и легко набухают. От количества сшивки зависит размер пор в носителе. Доступны носители с разными размерами пор. Сефадексы достаточно Структура сефадекса по данным гомогенны и свойства их фирмы Amersham Biosciences хорошо воспроизводятся (Pharmacia) от партии к партии.
В гелях для хроматографии нити декстрана сшиты эпихлоргидрином: Сшивка эта не очень жесткая, сефадексы мягки и легко набухают. От количества сшивки зависит размер пор в носителе. Доступны носители с разными размерами пор. Сефадексы достаточно Структура сефадекса по данным гомогенны и свойства их фирмы Amersham Biosciences хорошо воспроизводятся (Pharmacia) от партии к партии.
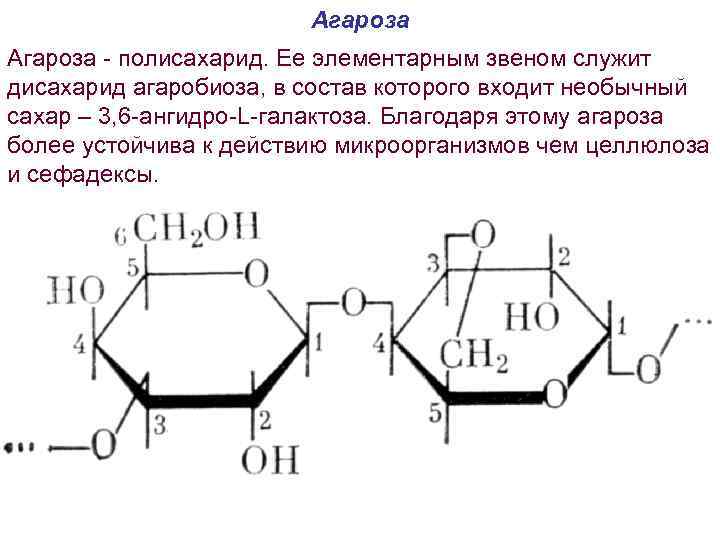 Агароза - полисахарид. Ее элементарным звеном служит дисахарид агаробиоза, в состав которого входит необычный сахар – 3, 6 -ангидро-L-галактоза. Благодаря этому агароза более устойчива к действию микроорганизмов чем целлюлоза и сефадексы.
Агароза - полисахарид. Ее элементарным звеном служит дисахарид агаробиоза, в состав которого входит необычный сахар – 3, 6 -ангидро-L-галактоза. Благодаря этому агароза более устойчива к действию микроорганизмов чем целлюлоза и сефадексы.
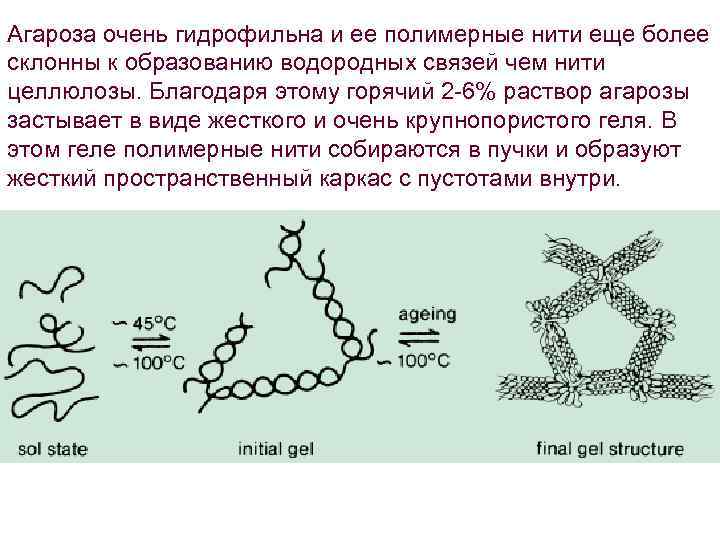 Агароза очень гидрофильна и ее полимерные нити еще более склонны к образованию водородных связей чем нити целлюлозы. Благодаря этому горячий 2 -6% раствор агарозы застывает в виде жесткого и очень крупнопористого геля. В этом геле полимерные нити собираются в пучки и образуют жесткий пространственный каркас с пустотами внутри.
Агароза очень гидрофильна и ее полимерные нити еще более склонны к образованию водородных связей чем нити целлюлозы. Благодаря этому горячий 2 -6% раствор агарозы застывает в виде жесткого и очень крупнопористого геля. В этом геле полимерные нити собираются в пучки и образуют жесткий пространственный каркас с пустотами внутри.
 Модификация агарозы может происходить по гидроксильным группам, однако плотность их расположения ниже чем у сефадексов. Кроме того группы внутри пучков также недоступны для модификации. В условиях хроматографии агароза химически неактивна, но уязвима для действия кислот, щелочей и окислителей. Рабочий диапазон обычной агарозы р. Н 4 -9. Для повышения химической и термической стойкости агарозных матриц фирма Pharmacia (Amersham Biosciences, GE Healthcare) разработала вариант хроматографического носителя в котором нити полимера дополнительно сшиты обработкой 2, 3 -дибромпропанолом. Эти матрицы можно использовать в диапазоне р. Н 3 -14. Агароза для хроматографии выпускается под различными торговыми марками, например, Sepharose (Amersham) и Bio Gel A (Bio-Rad). Используется как носитель для ионообменников, для гель-проникающей и аффинной хроматографии.
Модификация агарозы может происходить по гидроксильным группам, однако плотность их расположения ниже чем у сефадексов. Кроме того группы внутри пучков также недоступны для модификации. В условиях хроматографии агароза химически неактивна, но уязвима для действия кислот, щелочей и окислителей. Рабочий диапазон обычной агарозы р. Н 4 -9. Для повышения химической и термической стойкости агарозных матриц фирма Pharmacia (Amersham Biosciences, GE Healthcare) разработала вариант хроматографического носителя в котором нити полимера дополнительно сшиты обработкой 2, 3 -дибромпропанолом. Эти матрицы можно использовать в диапазоне р. Н 3 -14. Агароза для хроматографии выпускается под различными торговыми марками, например, Sepharose (Amersham) и Bio Gel A (Bio-Rad). Используется как носитель для ионообменников, для гель-проникающей и аффинной хроматографии.
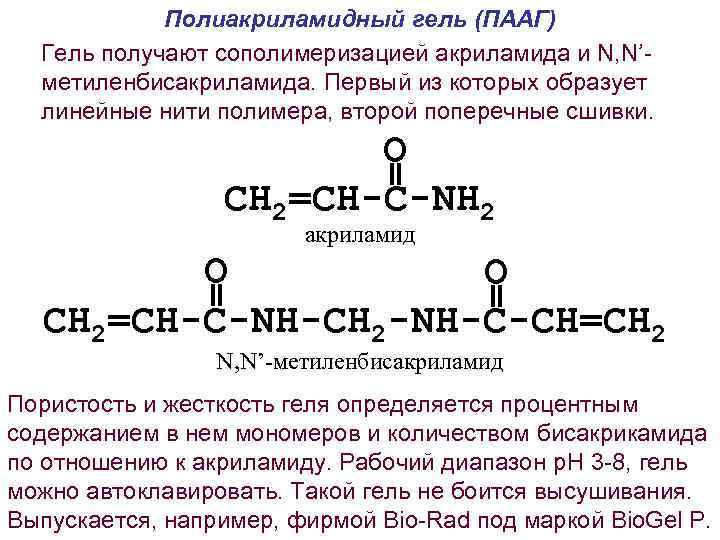 Полиакриламидный гель (ПААГ) Гель получают сополимеризацией акриламида и N, N’метиленбисакриламида. Первый из которых образует линейные нити полимера, второй поперечные сшивки. = O СН 2=СН-С-NH 2 акриламид = = O O СН 2=СН-С-NH-CH 2 -NH-C-CH=CH 2 N, N’-метиленбисакриламид Пористость и жесткость геля определяется процентным содержанием в нем мономеров и количеством бисакрикамида по отношению к акриламиду. Рабочий диапазон р. Н 3 -8, гель можно автоклавировать. Такой гель не боится высушивания. Выпускается, например, фирмой Bio-Rad под маркой Bio. Gel P.
Полиакриламидный гель (ПААГ) Гель получают сополимеризацией акриламида и N, N’метиленбисакриламида. Первый из которых образует линейные нити полимера, второй поперечные сшивки. = O СН 2=СН-С-NH 2 акриламид = = O O СН 2=СН-С-NH-CH 2 -NH-C-CH=CH 2 N, N’-метиленбисакриламид Пористость и жесткость геля определяется процентным содержанием в нем мономеров и количеством бисакрикамида по отношению к акриламиду. Рабочий диапазон р. Н 3 -8, гель можно автоклавировать. Такой гель не боится высушивания. Выпускается, например, фирмой Bio-Rad под маркой Bio. Gel P.
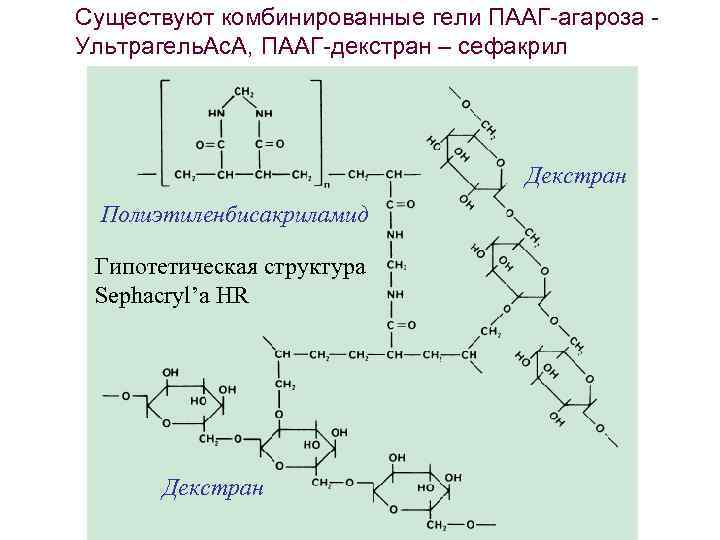 Существуют комбинированные гели ПААГ-агароза Ультрагель. Ас. А, ПААГ-декстран – сефакрил Декстран Полиэтиленбисакриламид Гипотетическая структура Sephacryl’а HR Декстран
Существуют комбинированные гели ПААГ-агароза Ультрагель. Ас. А, ПААГ-декстран – сефакрил Декстран Полиэтиленбисакриламид Гипотетическая структура Sephacryl’а HR Декстран
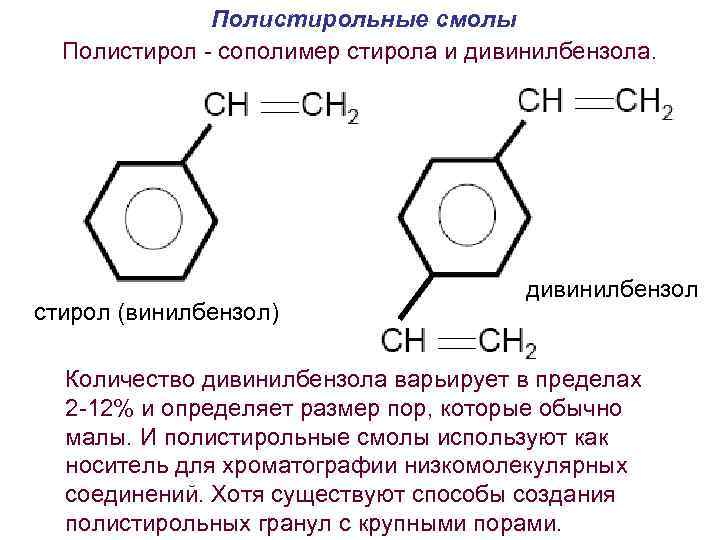 Полистирольные смолы Полистирол - сополимер стирола и дивинилбензола. стирол (винилбензол) дивинилбензол Количество дивинилбензола варьирует в пределах 2 -12% и определяет размер пор, которые обычно малы. И полистирольные смолы используют как носитель для хроматографии низкомолекулярных соединений. Хотя существуют способы создания полистирольных гранул с крупными порами.
Полистирольные смолы Полистирол - сополимер стирола и дивинилбензола. стирол (винилбензол) дивинилбензол Количество дивинилбензола варьирует в пределах 2 -12% и определяет размер пор, которые обычно малы. И полистирольные смолы используют как носитель для хроматографии низкомолекулярных соединений. Хотя существуют способы создания полистирольных гранул с крупными порами.
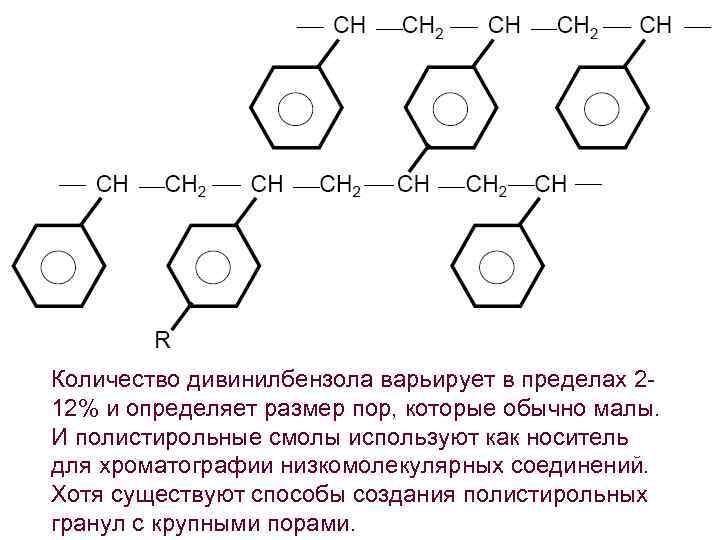 Количество дивинилбензола варьирует в пределах 212% и определяет размер пор, которые обычно малы. И полистирольные смолы используют как носитель для хроматографии низкомолекулярных соединений. Хотя существуют способы создания полистирольных гранул с крупными порами.
Количество дивинилбензола варьирует в пределах 212% и определяет размер пор, которые обычно малы. И полистирольные смолы используют как носитель для хроматографии низкомолекулярных соединений. Хотя существуют способы создания полистирольных гранул с крупными порами.
 Не модифицированные полистирольные смолы гидрофобны. модификация осуществляется по остатка бензола в параположение. Введение гидрофильных и особенно ионогенных остатков придает смоле гидрофильность, хотя склонность к гидрофобным взаимодействиям сохраняется. Полистирольные смолы используют наиболее часто в качестве ионообменников. Благодаря высокому содержанию остатков бензола в эти матрицы можно ввести и большое количество ионогенных групп. Наиболее популярные ионообменники на основе полистирола выпускаются под торговыми марками Dowex и Amberlit. Полистирольные смолы очень устойчивы химически.
Не модифицированные полистирольные смолы гидрофобны. модификация осуществляется по остатка бензола в параположение. Введение гидрофильных и особенно ионогенных остатков придает смоле гидрофильность, хотя склонность к гидрофобным взаимодействиям сохраняется. Полистирольные смолы используют наиболее часто в качестве ионообменников. Благодаря высокому содержанию остатков бензола в эти матрицы можно ввести и большое количество ионогенных групп. Наиболее популярные ионообменники на основе полистирола выпускаются под торговыми марками Dowex и Amberlit. Полистирольные смолы очень устойчивы химически.
 Окись алюминия Al 2 O 3 Окись алюминия для хроматографических целей получают в результате термического дегидрирования гидроокиси алюминия, осажденной в виде золя из раствора алюмината натрия. Ее подвергают старению, в процессе которого образуются прочные конгломераты с большой удельной поверхностью. Используют для абсорбционной хроматографии. Пористое стекло Путем специальной обработки щелочно-боросиликатного стекла последующей экстракции растворенного материала удается получить стеклянные шарики с хорошо контролируемым размером пор. Эти шарики могут быть использованы в качестве матриц для гель-проникающей хроматографии.
Окись алюминия Al 2 O 3 Окись алюминия для хроматографических целей получают в результате термического дегидрирования гидроокиси алюминия, осажденной в виде золя из раствора алюмината натрия. Ее подвергают старению, в процессе которого образуются прочные конгломераты с большой удельной поверхностью. Используют для абсорбционной хроматографии. Пористое стекло Путем специальной обработки щелочно-боросиликатного стекла последующей экстракции растворенного материала удается получить стеклянные шарики с хорошо контролируемым размером пор. Эти шарики могут быть использованы в качестве матриц для гель-проникающей хроматографии.
 Гидроксиапатит Фосфат кальция Ca. HPO 4· 2 H 2 O (брушит) растворим, но может давать суспензию мелких кристаллов отличающихся высокой сорбционной емкостью. Его получают, сливая растворы Ca. Cl 2 и Na. H 2 PO 4. При p. H>7 брушит постепенно превращается в гидроксипатит, который можно представить брутто формулой Ca 5(PO 4)3 OH. Гидроксиапатит можно приготовить в лабораторных условиях. Гидроксиапатит используется в качестве сорбента главным образом для белков и нуклеиновых кислот. Природа адсорбционного взаимодействия до конца не ясна. Основную роль, по-видимому, играют ионы Ca 2+, находящиеся на поверхности.
Гидроксиапатит Фосфат кальция Ca. HPO 4· 2 H 2 O (брушит) растворим, но может давать суспензию мелких кристаллов отличающихся высокой сорбционной емкостью. Его получают, сливая растворы Ca. Cl 2 и Na. H 2 PO 4. При p. H>7 брушит постепенно превращается в гидроксипатит, который можно представить брутто формулой Ca 5(PO 4)3 OH. Гидроксиапатит можно приготовить в лабораторных условиях. Гидроксиапатит используется в качестве сорбента главным образом для белков и нуклеиновых кислот. Природа адсорбционного взаимодействия до конца не ясна. Основную роль, по-видимому, играют ионы Ca 2+, находящиеся на поверхности.
 МЕТОДЫ ХРОМАТОГРАФИИ
МЕТОДЫ ХРОМАТОГРАФИИ
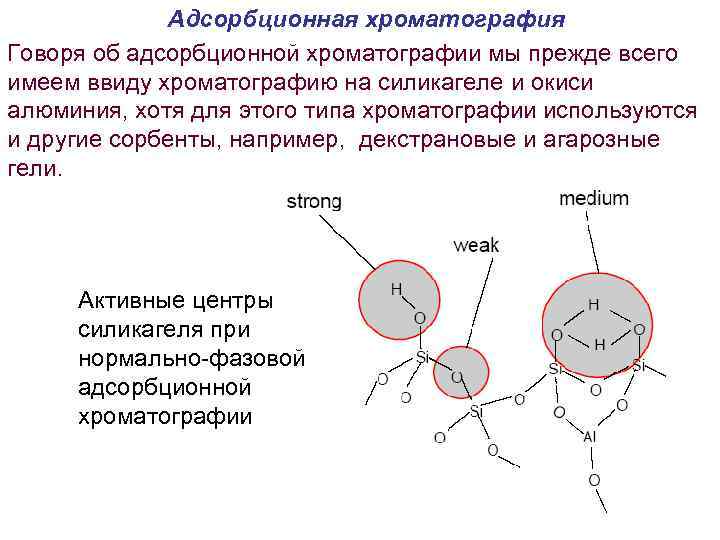 Адсорбционная хроматография Говоря об адсорбционной хроматографии мы прежде всего имеем ввиду хроматографию на силикагеле и окиси алюминия, хотя для этого типа хроматографии используются и другие сорбенты, например, декстрановые и агарозные гели. Активные центры силикагеля при нормально-фазовой адсорбционной хроматографии
Адсорбционная хроматография Говоря об адсорбционной хроматографии мы прежде всего имеем ввиду хроматографию на силикагеле и окиси алюминия, хотя для этого типа хроматографии используются и другие сорбенты, например, декстрановые и агарозные гели. Активные центры силикагеля при нормально-фазовой адсорбционной хроматографии
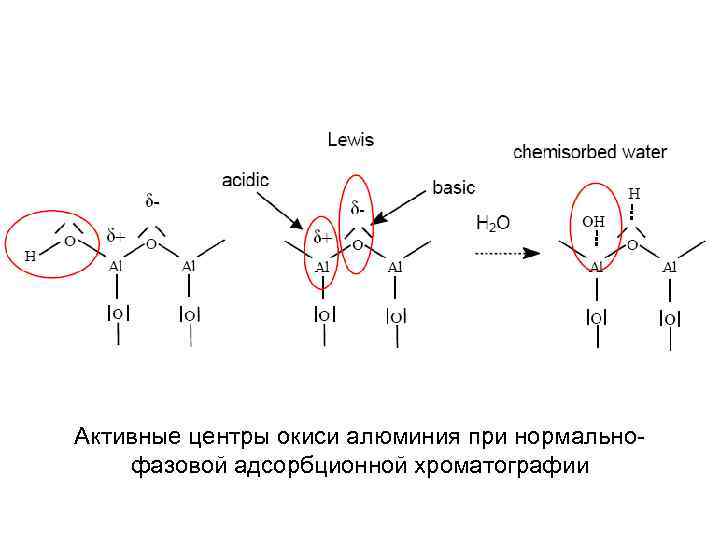 Активные центры окиси алюминия при нормальнофазовой адсорбционной хроматографии
Активные центры окиси алюминия при нормальнофазовой адсорбционной хроматографии
 Главным механизмом удерживания при адсорбционной хроматографии служит адсорбция, а роль константы распределения играет константа адсорбции.
Главным механизмом удерживания при адсорбционной хроматографии служит адсорбция, а роль константы распределения играет константа адсорбции.
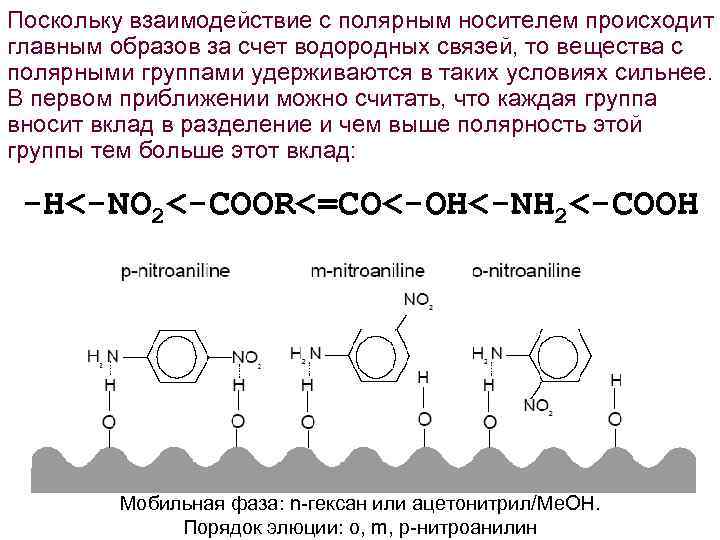 Поскольку взаимодействие с полярным носителем происходит главным образов за счет водородных связей, то вещества с полярными группами удерживаются в таких условиях сильнее. В первом приближении можно считать, что каждая группа вносит вклад в разделение и чем выше полярность этой группы тем больше этот вклад: -H<-NO 2<-COOR<=CO<-OH<-NH 2<-COOH Мобильная фаза: n-гексан или ацетонитрил/Me. OH. Порядок элюции: o, m, p-нитроанилин
Поскольку взаимодействие с полярным носителем происходит главным образов за счет водородных связей, то вещества с полярными группами удерживаются в таких условиях сильнее. В первом приближении можно считать, что каждая группа вносит вклад в разделение и чем выше полярность этой группы тем больше этот вклад: -H<-NO 2<-COOR<=CO<-OH<-NH 2<-COOH Мобильная фаза: n-гексан или ацетонитрил/Me. OH. Порядок элюции: o, m, p-нитроанилин
 Выбор элюента в нормально-фазовой адсорбционной хроматографии обычно влияет на разделение более значительно, чем выбор неподвижной фазы. И здесь существует основное правило, чем сильнее элюент адсорбируется на неподвижной фазе тем больше его элюирующая способность. Молекулы элюента и растворенных в нем соединений конкурируют за центры связывания на поверхности сорбента. В адсорбционной хроматографии сорбент (силикагель) используется в качестве полярной неподвижной фазы в сочетании с неполярными элюентами, например, алифатическими углеводородами, в которые добавляют полярные органические растворители, например, спирты, диоксан, тетрогидрофуран, следует отметить, что набор растворителей достаточно широк. Сильно сказывается на элюирующей способности растворителей и содержание в них воды.
Выбор элюента в нормально-фазовой адсорбционной хроматографии обычно влияет на разделение более значительно, чем выбор неподвижной фазы. И здесь существует основное правило, чем сильнее элюент адсорбируется на неподвижной фазе тем больше его элюирующая способность. Молекулы элюента и растворенных в нем соединений конкурируют за центры связывания на поверхности сорбента. В адсорбционной хроматографии сорбент (силикагель) используется в качестве полярной неподвижной фазы в сочетании с неполярными элюентами, например, алифатическими углеводородами, в которые добавляют полярные органические растворители, например, спирты, диоксан, тетрогидрофуран, следует отметить, что набор растворителей достаточно широк. Сильно сказывается на элюирующей способности растворителей и содержание в них воды.
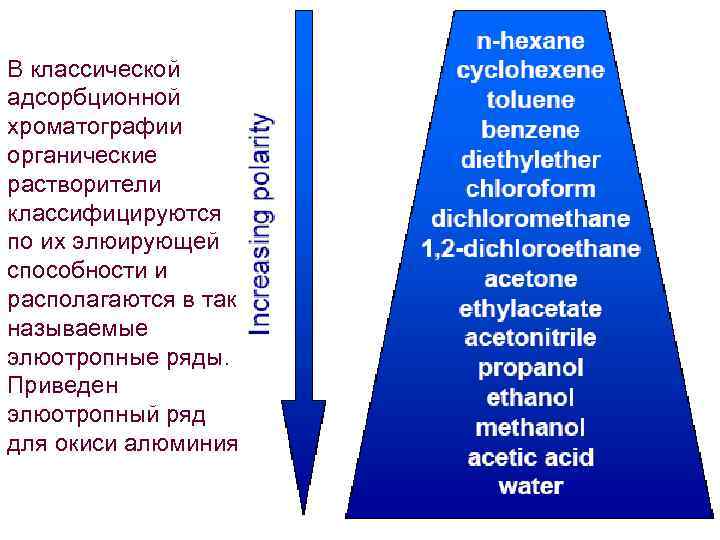 В классической адсорбционной хроматографии органические растворители классифицируются по их элюирующей способности и располагаются в так называемые элюотропные ряды. Приведен элюотропный ряд для окиси алюминия.
В классической адсорбционной хроматографии органические растворители классифицируются по их элюирующей способности и располагаются в так называемые элюотропные ряды. Приведен элюотропный ряд для окиси алюминия.
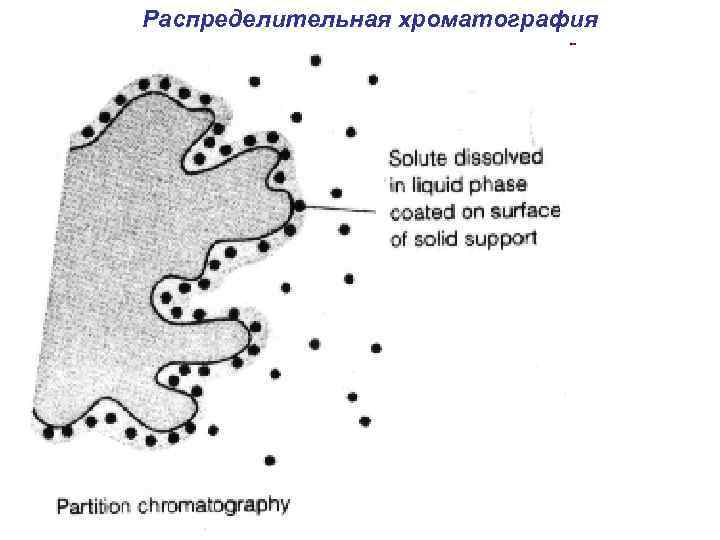 Распределительная хроматография
Распределительная хроматография
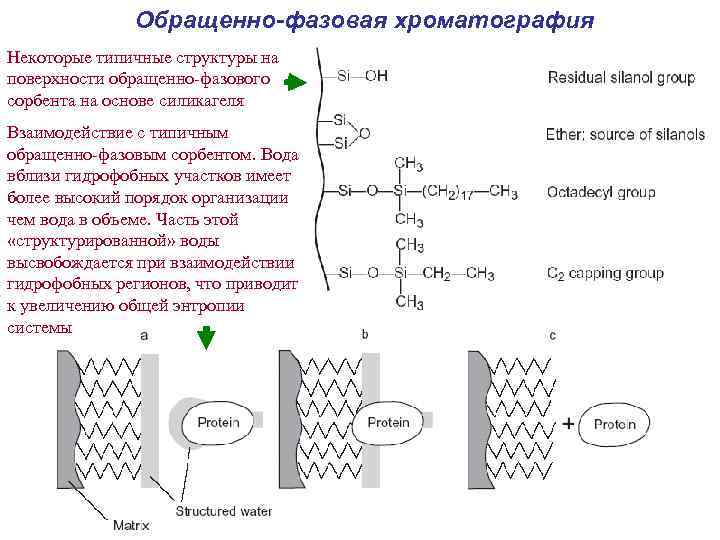 Обращенно-фазовая хроматография Некоторые типичные структуры на поверхности обращенно-фазового сорбента на основе силикагеля Взаимодействие с типичным обращенно-фазовым сорбентом. Вода вблизи гидрофобных участков имеет более высокий порядок организации чем вода в объеме. Часть этой «структурированной» воды высвобождается при взаимодействии гидрофобных регионов, что приводит к увеличению общей энтропии системы
Обращенно-фазовая хроматография Некоторые типичные структуры на поверхности обращенно-фазового сорбента на основе силикагеля Взаимодействие с типичным обращенно-фазовым сорбентом. Вода вблизи гидрофобных участков имеет более высокий порядок организации чем вода в объеме. Часть этой «структурированной» воды высвобождается при взаимодействии гидрофобных регионов, что приводит к увеличению общей энтропии системы
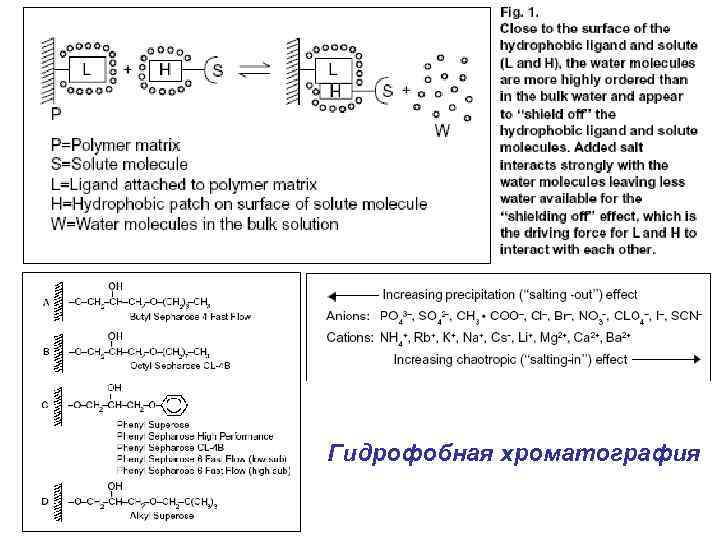 Гидрофобная хроматография
Гидрофобная хроматография
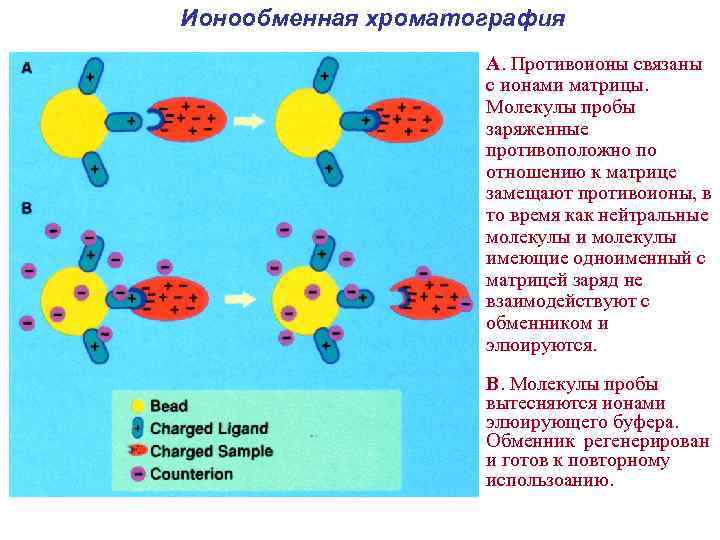 Ионообменная хроматография А. Противоионы связаны с ионами матрицы. Молекулы пробы заряженные противоположно по отношению к матрице замещают противоионы, в то время как нейтральные молекулы имеющие одноименный с матрицей заряд не взаимодействуют с обменником и элюируются. B. Молекулы пробы вытесняются ионами элюирующего буфера. Обменник регенерирован и готов к повторному использоанию.
Ионообменная хроматография А. Противоионы связаны с ионами матрицы. Молекулы пробы заряженные противоположно по отношению к матрице замещают противоионы, в то время как нейтральные молекулы имеющие одноименный с матрицей заряд не взаимодействуют с обменником и элюируются. B. Молекулы пробы вытесняются ионами элюирующего буфера. Обменник регенерирован и готов к повторному использоанию.
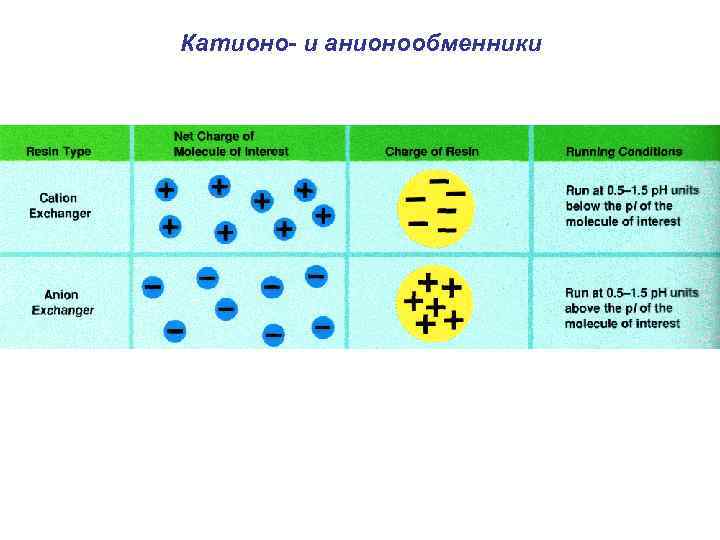 Катионо- и анионообменники
Катионо- и анионообменники
 АНИОНИТЫ КАТИОНИТЫ
АНИОНИТЫ КАТИОНИТЫ
 слабые сильные Кривые титрования катионо- и анионообменников
слабые сильные Кривые титрования катионо- и анионообменников
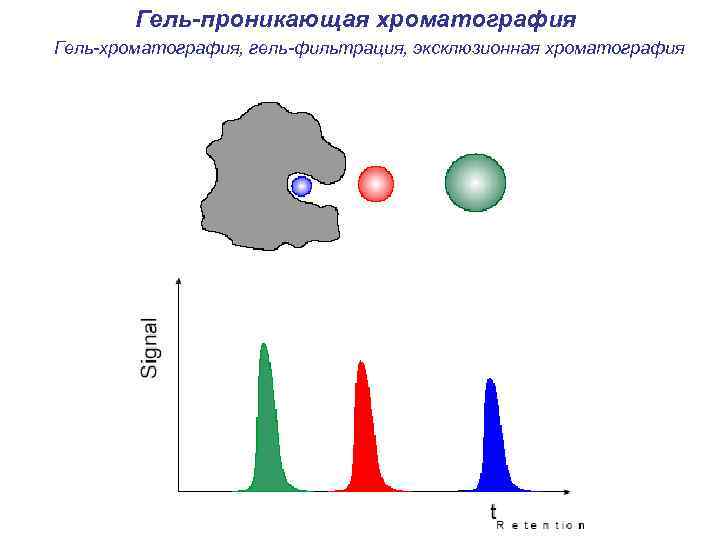 Гель-проникающая хроматография Гель-хроматография, гель-фильтрация, эксклюзионная хроматография
Гель-проникающая хроматография Гель-хроматография, гель-фильтрация, эксклюзионная хроматография
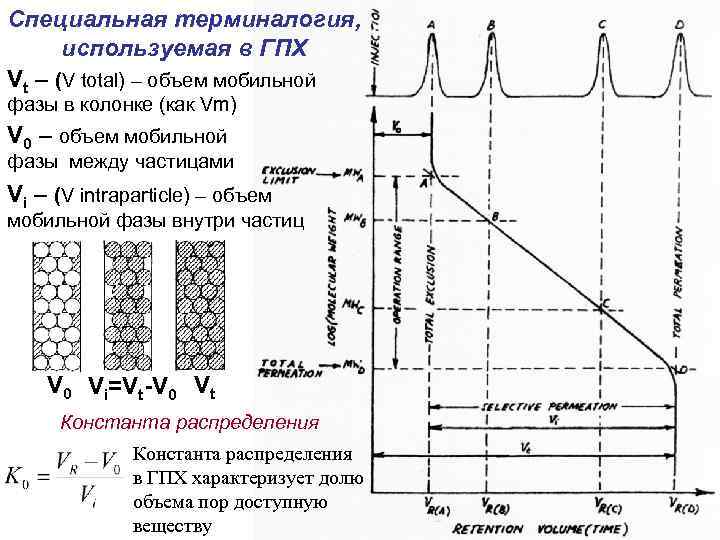 Специальная терминалогия, используемая в ГПХ Vt – (V total) – объем мобильной фазы в колонке (как Vm) V 0 – объем мобильной фазы между частицами Vi – (V intraparticle) – объем мобильной фазы внутри частиц V 0 Vi=Vt-V 0 Vt Константа распределения в ГПХ характеризует долю объема пор доступную веществу
Специальная терминалогия, используемая в ГПХ Vt – (V total) – объем мобильной фазы в колонке (как Vm) V 0 – объем мобильной фазы между частицами Vi – (V intraparticle) – объем мобильной фазы внутри частиц V 0 Vi=Vt-V 0 Vt Константа распределения в ГПХ характеризует долю объема пор доступную веществу
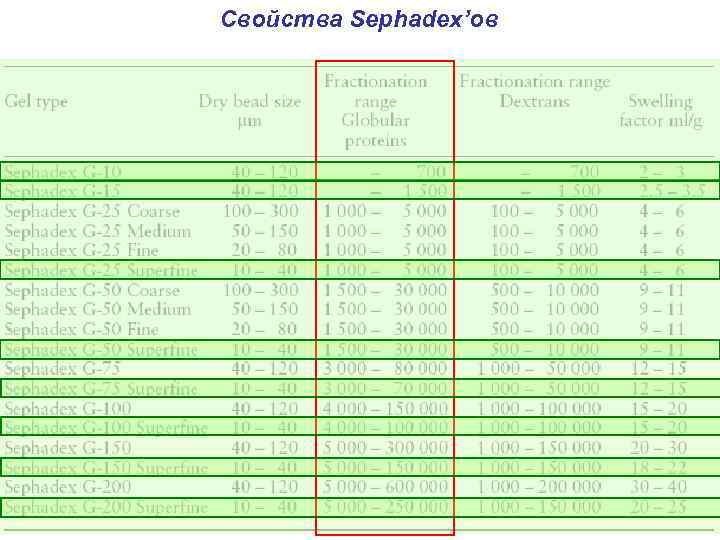 Свойства Sephadex’ов
Свойства Sephadex’ов
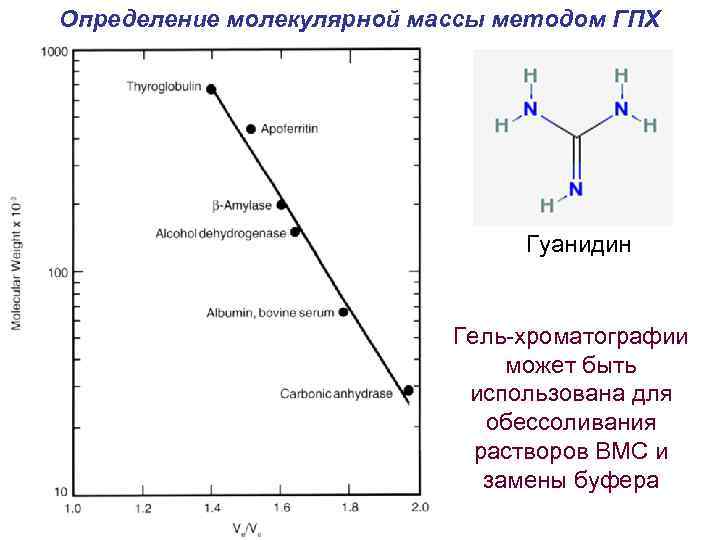 Определение молекулярной массы методом ГПХ Гуанидин Гель-хроматографии может быть использована для обессоливания растворов ВМС и замены буфера
Определение молекулярной массы методом ГПХ Гуанидин Гель-хроматографии может быть использована для обессоливания растворов ВМС и замены буфера
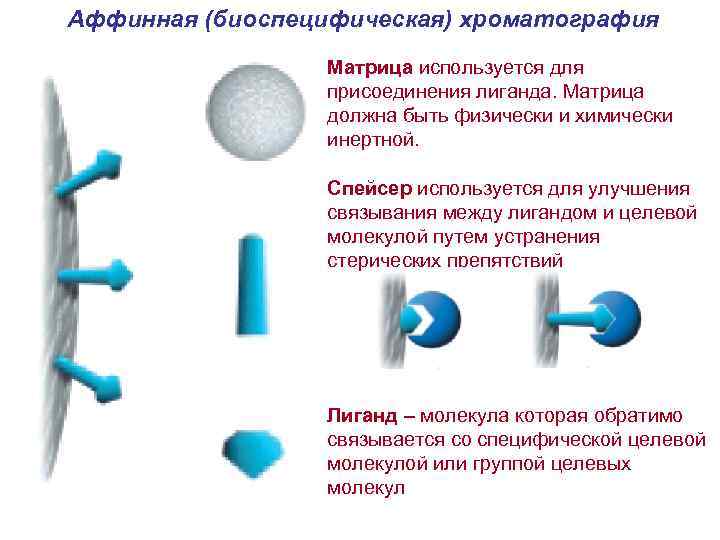 Аффинная (биоспецифическая) хроматография Матрица используется для присоединения лиганда. Матрица должна быть физически и химически инертной. Спейсер используется для улучшения связывания между лигандом и целевой молекулой путем устранения стерических препятствий Лиганд – молекула которая обратимо связывается со специфической целевой молекулой или группой целевых молекул
Аффинная (биоспецифическая) хроматография Матрица используется для присоединения лиганда. Матрица должна быть физически и химически инертной. Спейсер используется для улучшения связывания между лигандом и целевой молекулой путем устранения стерических препятствий Лиганд – молекула которая обратимо связывается со специфической целевой молекулой или группой целевых молекул
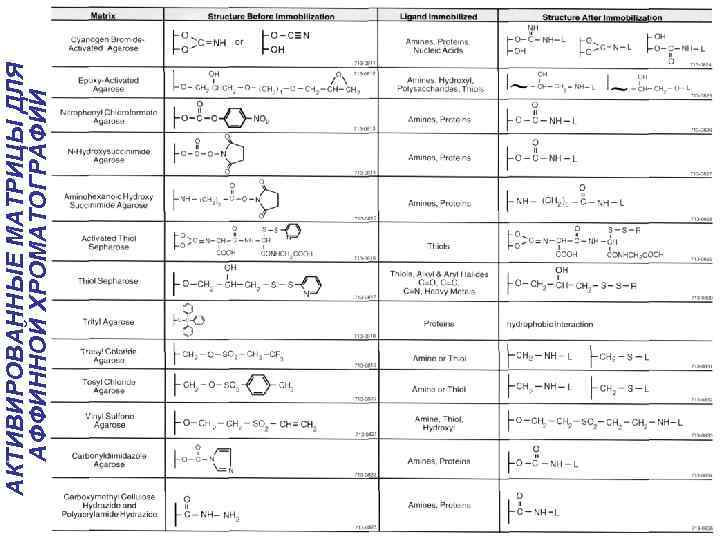 АКТИВИРОВАННЫЕ МАТРИЦЫ ДЛЯ АФФИННОЙ ХРОМАТОГРАФИИ
АКТИВИРОВАННЫЕ МАТРИЦЫ ДЛЯ АФФИННОЙ ХРОМАТОГРАФИИ
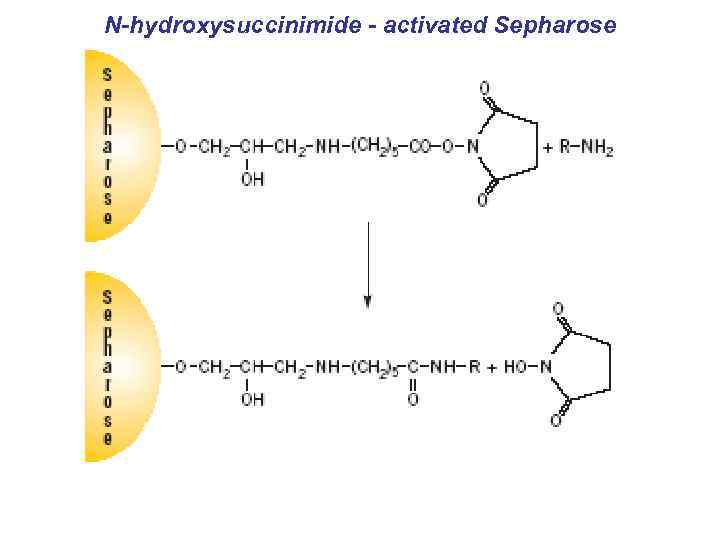 N-hydroxysuccinimide - activated Sepharose
N-hydroxysuccinimide - activated Sepharose
 Лиганды для аффинной хроматографии ØЛИГАНДЫ С ИНДИВИДУАЛЬНОЙ СПЕЦИФИЧНОСТЬЮ ØЛИГАНДЫ С ГРУППОВОЙ СПЕЦИФИЧНОСТЬЮ
Лиганды для аффинной хроматографии ØЛИГАНДЫ С ИНДИВИДУАЛЬНОЙ СПЕЦИФИЧНОСТЬЮ ØЛИГАНДЫ С ГРУППОВОЙ СПЕЦИФИЧНОСТЬЮ
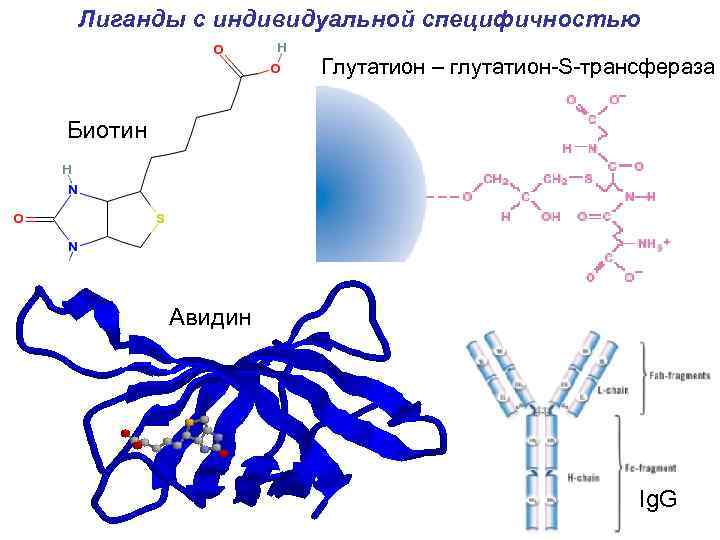 Лиганды с индивидуальной специфичностью Глутатион – глутатион-S-трансфераза Биотин Авидин Ig. G
Лиганды с индивидуальной специфичностью Глутатион – глутатион-S-трансфераза Биотин Авидин Ig. G
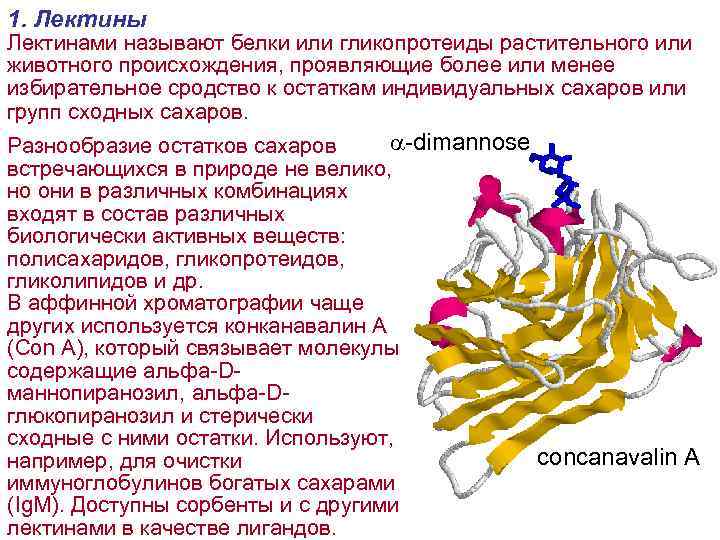 1. Лектины Лектинами называют белки или гликопротеиды растительного или животного происхождения, проявляющие более или менее избирательное сродство к остаткам индивидуальных сахаров или групп сходных сахаров. a-dimannose Разнообразие остатков сахаров встречающихся в природе не велико, но они в различных комбинациях входят в состав различных биологически активных веществ: полисахаридов, гликопротеидов, гликолипидов и др. В аффинной хроматографии чаще других используется конканавалин А (Con A), который связывает молекулы содержащие альфа-Dманнопиранозил, альфа-Dглюкопиранозил и стерически сходные с ними остатки. Используют, concanavalin A например, для очистки иммуноглобулинов богатых сахарами (Ig. M). Доступны сорбенты и с другими лектинами в качестве лигандов.
1. Лектины Лектинами называют белки или гликопротеиды растительного или животного происхождения, проявляющие более или менее избирательное сродство к остаткам индивидуальных сахаров или групп сходных сахаров. a-dimannose Разнообразие остатков сахаров встречающихся в природе не велико, но они в различных комбинациях входят в состав различных биологически активных веществ: полисахаридов, гликопротеидов, гликолипидов и др. В аффинной хроматографии чаще других используется конканавалин А (Con A), который связывает молекулы содержащие альфа-Dманнопиранозил, альфа-Dглюкопиранозил и стерически сходные с ними остатки. Используют, concanavalin A например, для очистки иммуноглобулинов богатых сахарами (Ig. M). Доступны сорбенты и с другими лектинами в качестве лигандов.
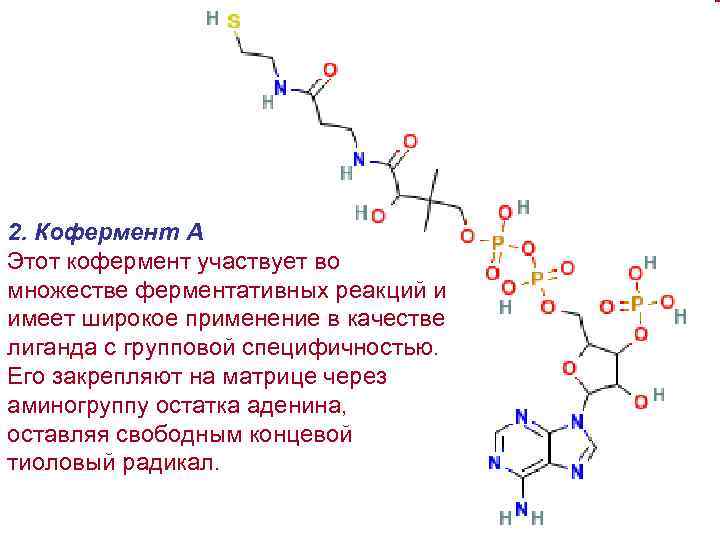 2. Кофермент А Этот кофермент участвует во множестве ферментативных реакций и имеет широкое применение в качестве лиганда с групповой специфичностью. Его закрепляют на матрице через аминогруппу остатка аденина, оставляя свободным концевой тиоловый радикал.
2. Кофермент А Этот кофермент участвует во множестве ферментативных реакций и имеет широкое применение в качестве лиганда с групповой специфичностью. Его закрепляют на матрице через аминогруппу остатка аденина, оставляя свободным концевой тиоловый радикал.
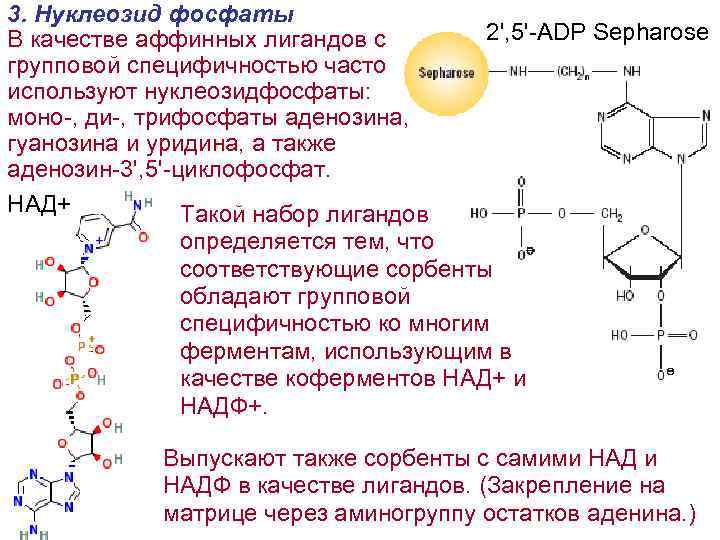 3. Нуклеозид фосфаты В качестве аффинных лигандов с групповой специфичностью часто используют нуклеозидфосфаты: моно-, ди-, трифосфаты аденозина, гуанозина и уридина, а также аденозин-3', 5'-циклофосфат. НАД+ Такой набор лигандов 2', 5'-ADP Sepharose определяется тем, что соответствующие сорбенты обладают групповой специфичностью ко многим ферментам, использующим в качестве коферментов НАД+ и НАДФ+. Выпускают также сорбенты с самими НАДФ в качестве лигандов. (Закрепление на матрице через аминогруппу остатков аденина. )
3. Нуклеозид фосфаты В качестве аффинных лигандов с групповой специфичностью часто используют нуклеозидфосфаты: моно-, ди-, трифосфаты аденозина, гуанозина и уридина, а также аденозин-3', 5'-циклофосфат. НАД+ Такой набор лигандов 2', 5'-ADP Sepharose определяется тем, что соответствующие сорбенты обладают групповой специфичностью ко многим ферментам, использующим в качестве коферментов НАД+ и НАДФ+. Выпускают также сорбенты с самими НАДФ в качестве лигандов. (Закрепление на матрице через аминогруппу остатков аденина. )
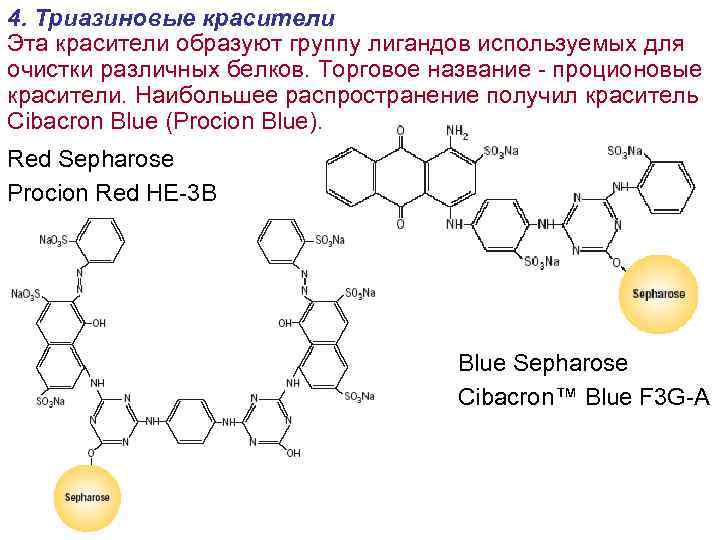 4. Триазиновые красители Эта красители образуют группу лигандов используемых для очистки различных белков. Торговое название - проционовые красители. Наибольшее распространение получил краситель Cibacron Blue (Procion Blue). Red Sepharose Procion Red HE-3 B Blue Sepharose Cibacron™ Blue F 3 G-A
4. Триазиновые красители Эта красители образуют группу лигандов используемых для очистки различных белков. Торговое название - проционовые красители. Наибольшее распространение получил краситель Cibacron Blue (Procion Blue). Red Sepharose Procion Red HE-3 B Blue Sepharose Cibacron™ Blue F 3 G-A
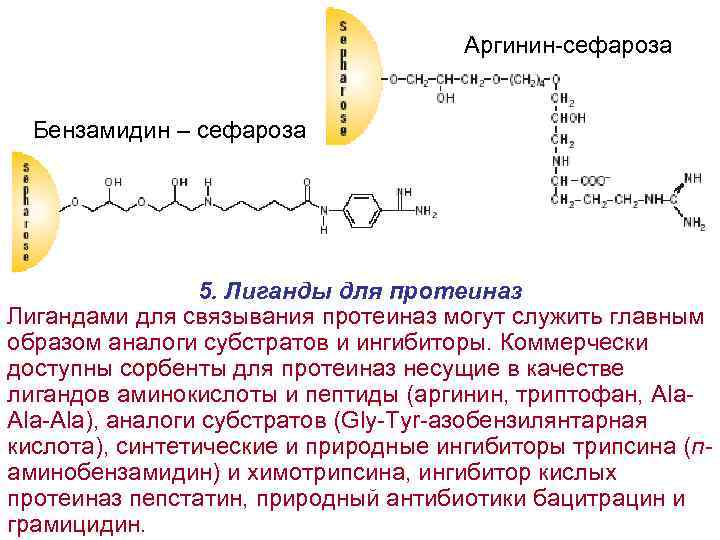 Аргинин-сефароза Бензамидин – сефароза 5. Лиганды для протеиназ Лигандами для связывания протеиназ могут служить главным образом аналоги субстратов и ингибиторы. Коммерчески доступны сорбенты для протеиназ несущие в качестве лигандов аминокислоты и пептиды (аргинин, триптофан, Аla. Ala-Ala), аналоги субстратов (Gly-Tyr-азобензилянтарная кислота), синтетические и природные ингибиторы трипсина (паминобензамидин) и химотрипсина, ингибитор кислых протеиназ пепстатин, природный антибиотики бацитрацин и грамицидин.
Аргинин-сефароза Бензамидин – сефароза 5. Лиганды для протеиназ Лигандами для связывания протеиназ могут служить главным образом аналоги субстратов и ингибиторы. Коммерчески доступны сорбенты для протеиназ несущие в качестве лигандов аминокислоты и пептиды (аргинин, триптофан, Аla. Ala-Ala), аналоги субстратов (Gly-Tyr-азобензилянтарная кислота), синтетические и природные ингибиторы трипсина (паминобензамидин) и химотрипсина, ингибитор кислых протеиназ пепстатин, природный антибиотики бацитрацин и грамицидин.
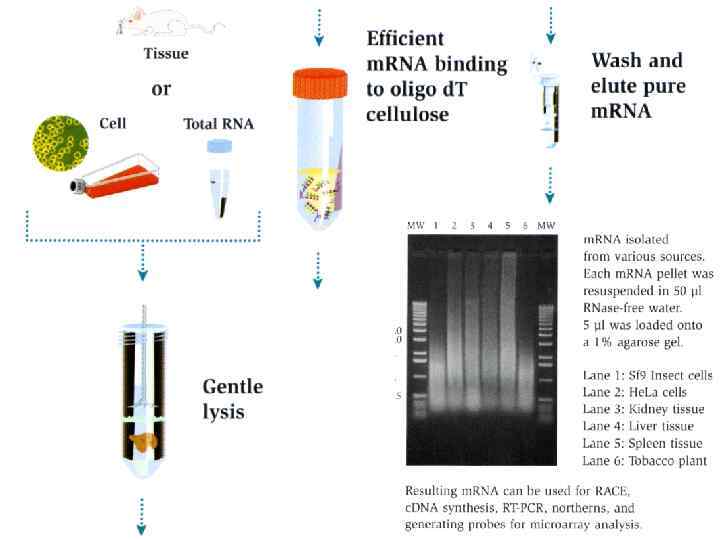
 6. Олиго(d. T) и полиуридировая кислота Большинство молекул эукариотических м. РНК содержат на своем 3'-конце более или менее протяженную полиадениновую последовательность (средняя длина - около 100 адениловых остатков). Это обстоятельство дало возможность создать аффинный сорбент с групповой специфичностью к любой молекуле м. РНК, содержащей такую последовательность. На матрице агарозы закрепляют комплементарный гомополимер олиго(U) или олиго(d. T) длиной около 100 остатков. Коммерческий сорбент выпускавшийся фирмой Pharmacia называется Poly(U)Sepharose сейчас GE Helthcare (до этого Amersham) продает Oligo(d. T)-Cellulose.
6. Олиго(d. T) и полиуридировая кислота Большинство молекул эукариотических м. РНК содержат на своем 3'-конце более или менее протяженную полиадениновую последовательность (средняя длина - около 100 адениловых остатков). Это обстоятельство дало возможность создать аффинный сорбент с групповой специфичностью к любой молекуле м. РНК, содержащей такую последовательность. На матрице агарозы закрепляют комплементарный гомополимер олиго(U) или олиго(d. T) длиной около 100 остатков. Коммерческий сорбент выпускавшийся фирмой Pharmacia называется Poly(U)Sepharose сейчас GE Helthcare (до этого Amersham) продает Oligo(d. T)-Cellulose.
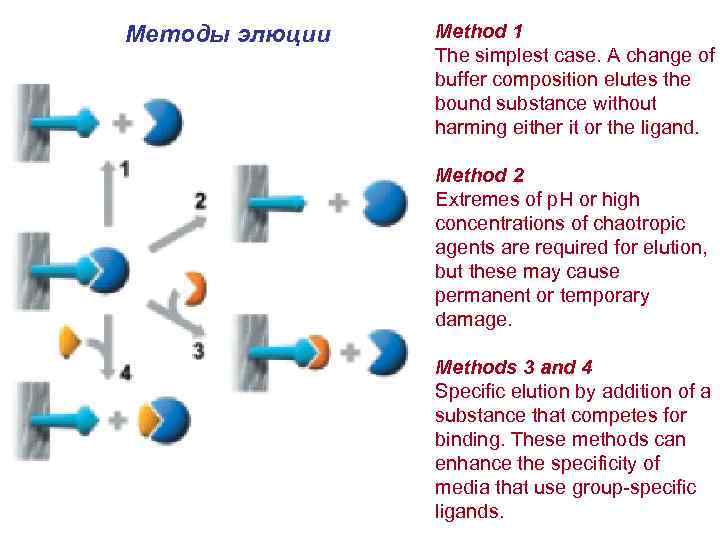 Методы элюции Method 1 The simplest case. A change of buffer composition elutes the bound substance without harming either it or the ligand. Method 2 Extremes of p. H or high concentrations of chaotropic agents are required for elution, but these may cause permanent or temporary damage. Methods 3 and 4 Specific elution by addition of a substance that competes for binding. These methods can enhance the specificity of media that use group-specific ligands.
Методы элюции Method 1 The simplest case. A change of buffer composition elutes the bound substance without harming either it or the ligand. Method 2 Extremes of p. H or high concentrations of chaotropic agents are required for elution, but these may cause permanent or temporary damage. Methods 3 and 4 Specific elution by addition of a substance that competes for binding. These methods can enhance the specificity of media that use group-specific ligands.
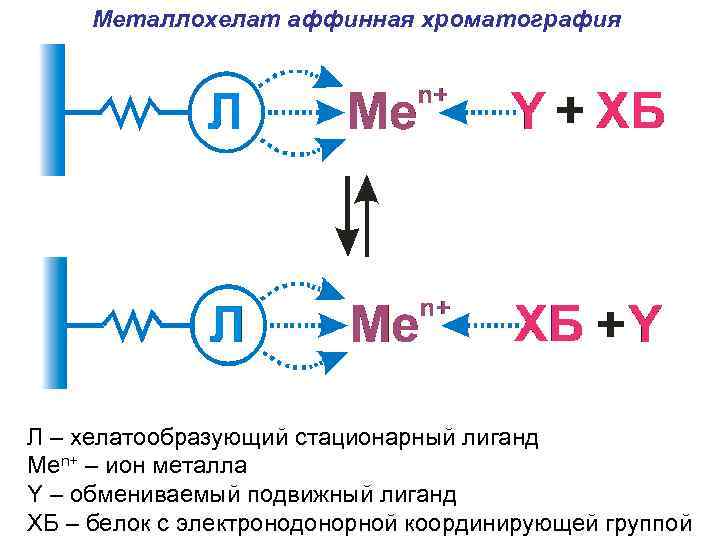 Металлохелат аффинная хроматография Л – хелатообразующий стационарный лиганд Меn+ – ион металла Y – обмениваемый подвижный лиганд XБ – белок с электронодонорной координирующей группой
Металлохелат аффинная хроматография Л – хелатообразующий стационарный лиганд Меn+ – ион металла Y – обмениваемый подвижный лиганд XБ – белок с электронодонорной координирующей группой
 Металлохелат аффинная хроматография Один из распространенных стационарных лигандов – иминодиуксусная кислота (ИДК, IDA) Chelating Sepharose (IDA) В качестве металла могут выступать Cu 2+, Ni 2+, Fe 3+, Co 2+, Zn 2+ Основной вклад в связывание белка вносят остатки Вклад в связывание вносят также остатки His. Cys и Cys-Cys, а также амино и карбоксильные группы.
Металлохелат аффинная хроматография Один из распространенных стационарных лигандов – иминодиуксусная кислота (ИДК, IDA) Chelating Sepharose (IDA) В качестве металла могут выступать Cu 2+, Ni 2+, Fe 3+, Co 2+, Zn 2+ Основной вклад в связывание белка вносят остатки Вклад в связывание вносят также остатки His. Cys и Cys-Cys, а также амино и карбоксильные группы.
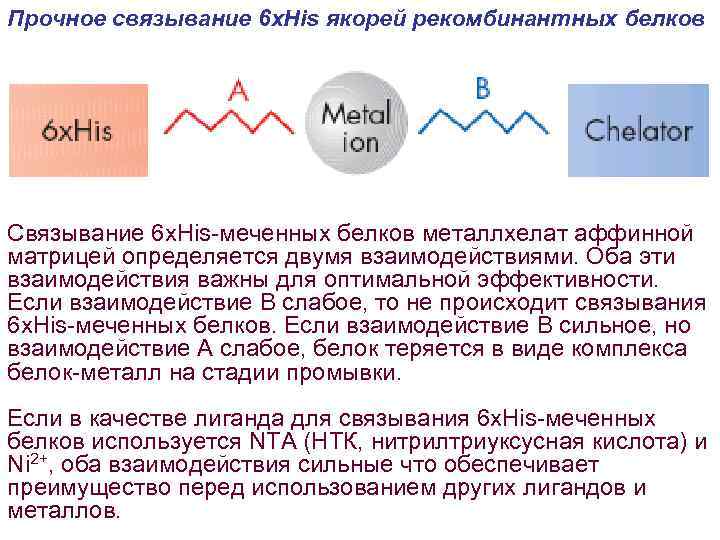 Прочное связывание 6 х. His якорей рекомбинантных белков Связывание 6 x. His-меченных белков металлхелат аффинной матрицей определяется двумя взаимодействиями. Оба эти взаимодействия важны для оптимальной эффективности. Если взаимодействие B слабое, то не происходит связывания 6 x. His-меченных белков. Если взаимодействие B сильное, но взаимодействие A слабое, белок теряется в виде комплекса белок-металл на стадии промывки. Если в качестве лиганда для связывания 6 x. His-меченных белков используется NTA (НТК, нитрилтриуксусная кислота) и Ni 2+, оба взаимодействия сильные что обеспечивает преимущество перед использованием других лигандов и металлов.
Прочное связывание 6 х. His якорей рекомбинантных белков Связывание 6 x. His-меченных белков металлхелат аффинной матрицей определяется двумя взаимодействиями. Оба эти взаимодействия важны для оптимальной эффективности. Если взаимодействие B слабое, то не происходит связывания 6 x. His-меченных белков. Если взаимодействие B сильное, но взаимодействие A слабое, белок теряется в виде комплекса белок-металл на стадии промывки. Если в качестве лиганда для связывания 6 x. His-меченных белков используется NTA (НТК, нитрилтриуксусная кислота) и Ni 2+, оба взаимодействия сильные что обеспечивает преимущество перед использованием других лигандов и металлов.
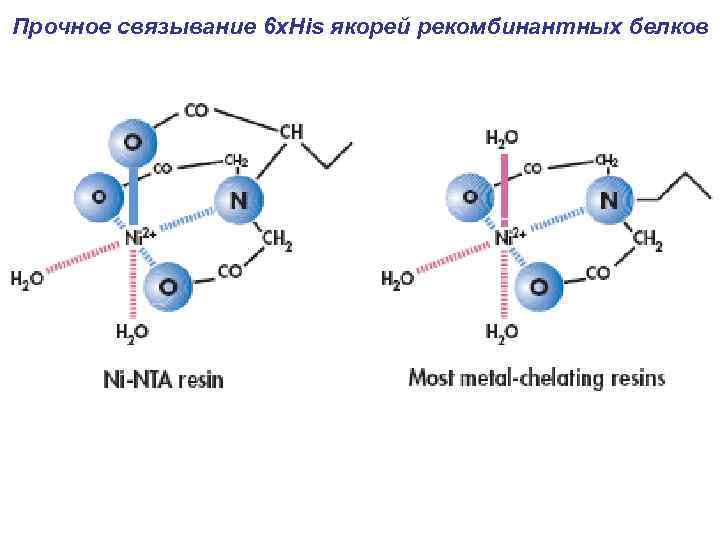 Прочное связывание 6 х. His якорей рекомбинантных белков
Прочное связывание 6 х. His якорей рекомбинантных белков
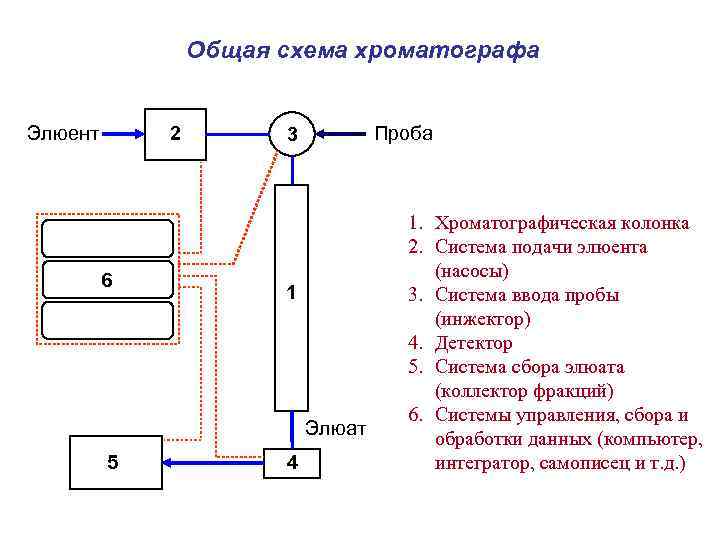 Общая схема хроматографа Элюент 2 6 Проба 3 1 Элюат 5 4 1. Хроматографическая колонка 2. Система подачи элюента (насосы) 3. Система ввода пробы (инжектор) 4. Детектор 5. Система сбора элюата (коллектор фракций) 6. Системы управления, сбора и обработки данных (компьютер, интегратор, самописец и т. д. )
Общая схема хроматографа Элюент 2 6 Проба 3 1 Элюат 5 4 1. Хроматографическая колонка 2. Система подачи элюента (насосы) 3. Система ввода пробы (инжектор) 4. Детектор 5. Система сбора элюата (коллектор фракций) 6. Системы управления, сбора и обработки данных (компьютер, интегратор, самописец и т. д. )
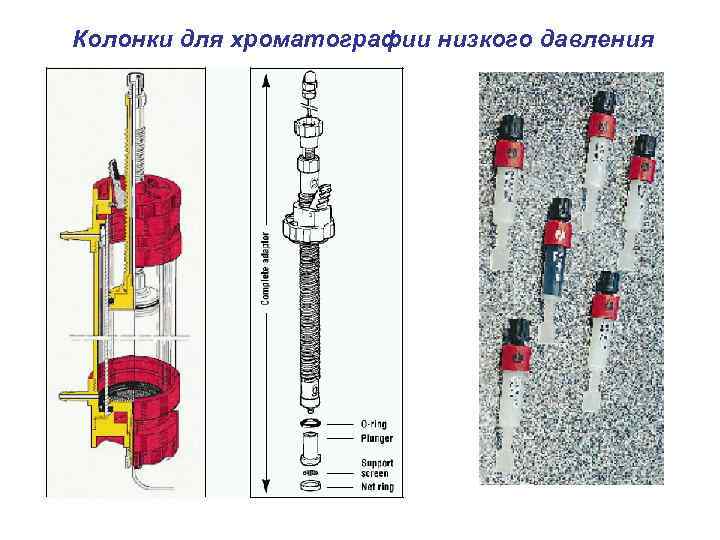 Колонки для хроматографии низкого давления
Колонки для хроматографии низкого давления
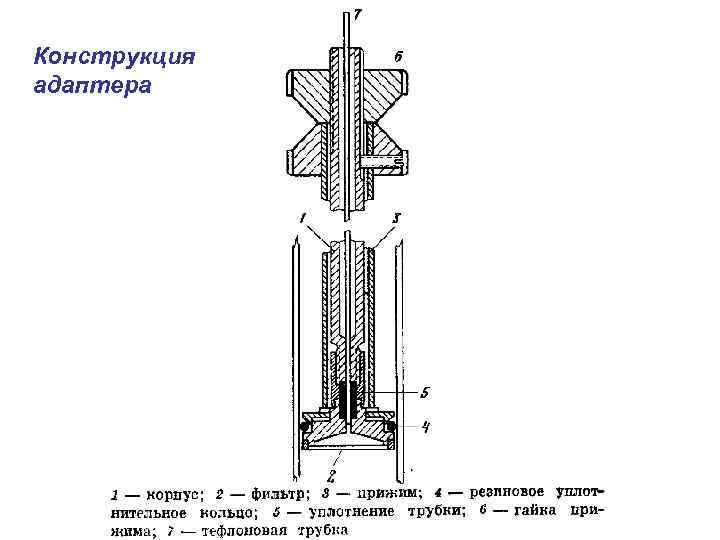 Конструкция адаптера
Конструкция адаптера
 Колонки для ВЭЖХ
Колонки для ВЭЖХ
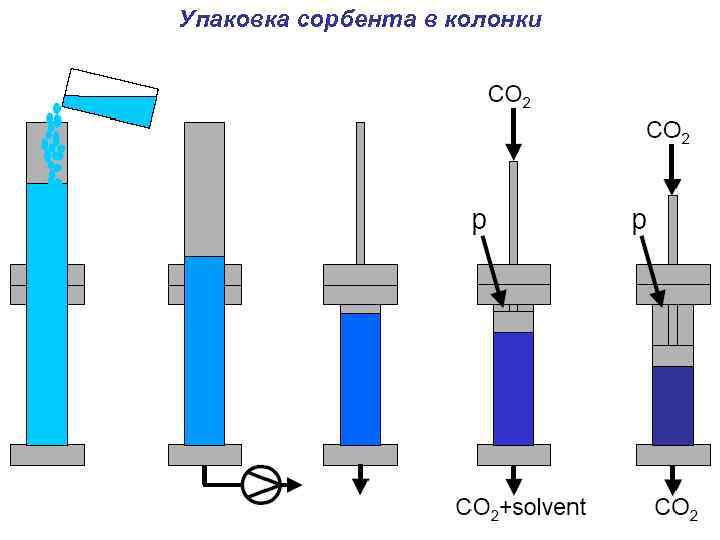 Упаковка сорбента в колонки
Упаковка сорбента в колонки
 Ion exclusion chromatography columns for fructose syrup (2 x 60 m 3)
Ion exclusion chromatography columns for fructose syrup (2 x 60 m 3)

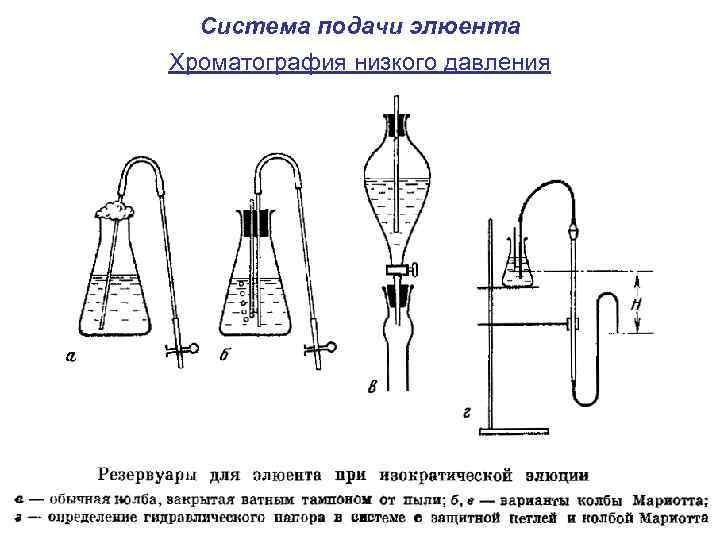 Система подачи элюента Хроматография низкого давления
Система подачи элюента Хроматография низкого давления
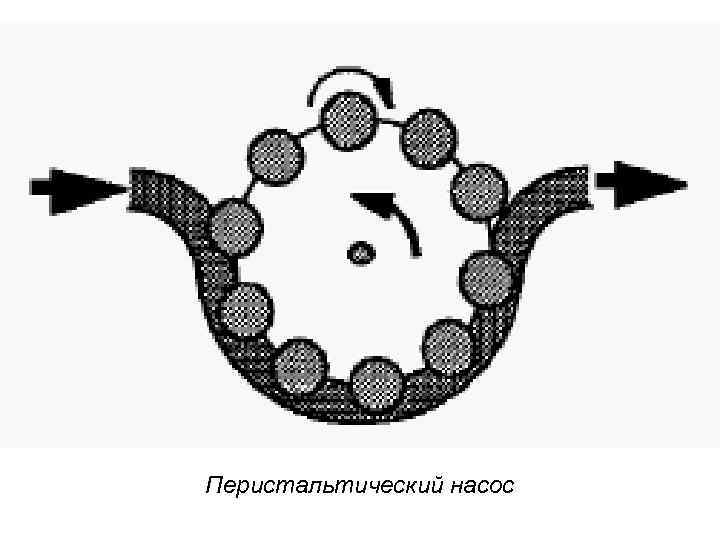 Перистальтический насос
Перистальтический насос
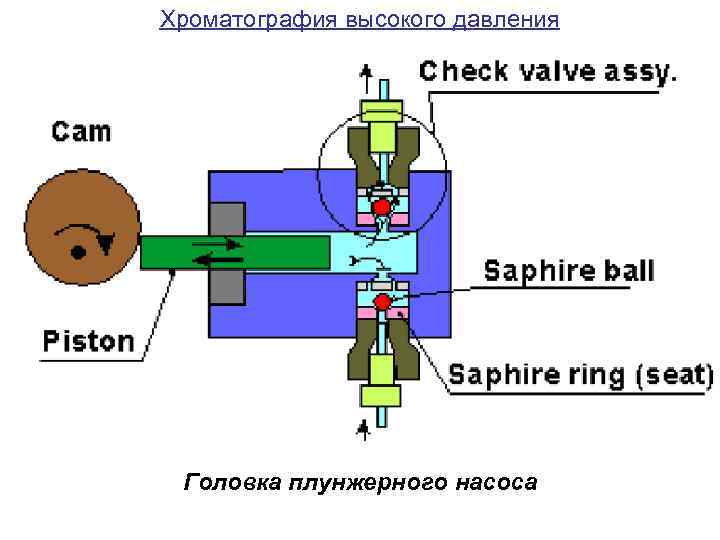 Хроматография высокого давления Головка плунжерного насоса
Хроматография высокого давления Головка плунжерного насоса
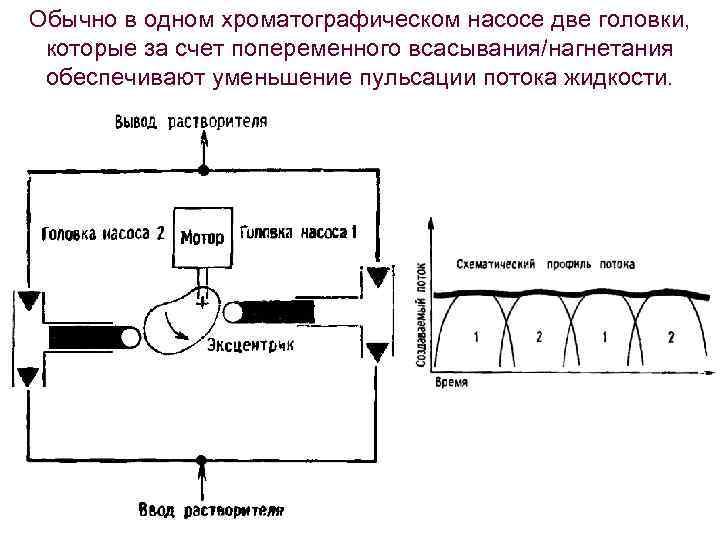 Обычно в одном хроматографическом насосе две головки, которые за счет попеременного всасывания/нагнетания обеспечивают уменьшение пульсации потока жидкости.
Обычно в одном хроматографическом насосе две головки, которые за счет попеременного всасывания/нагнетания обеспечивают уменьшение пульсации потока жидкости.
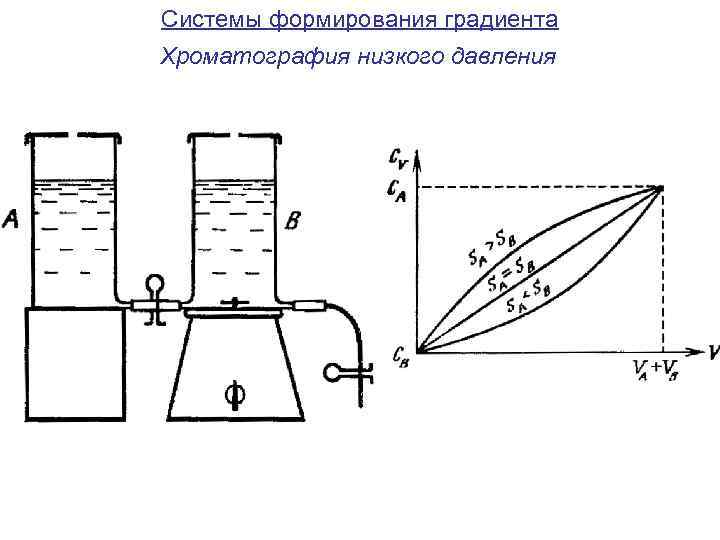 Системы формирования градиента Хроматография низкого давления
Системы формирования градиента Хроматография низкого давления

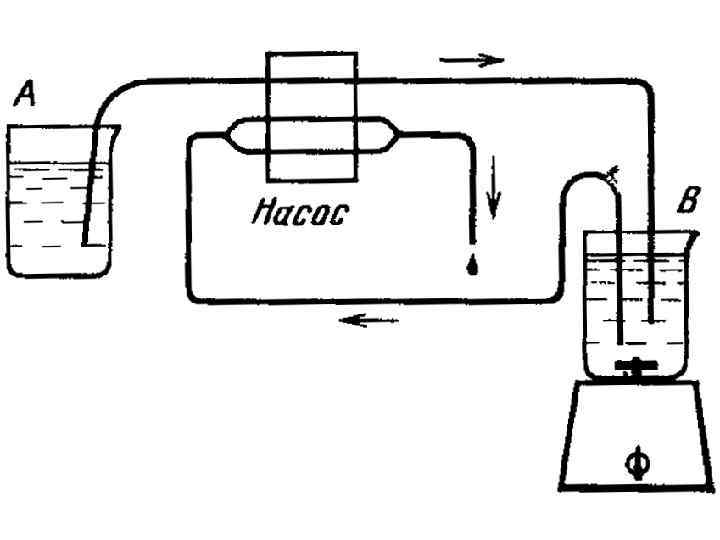
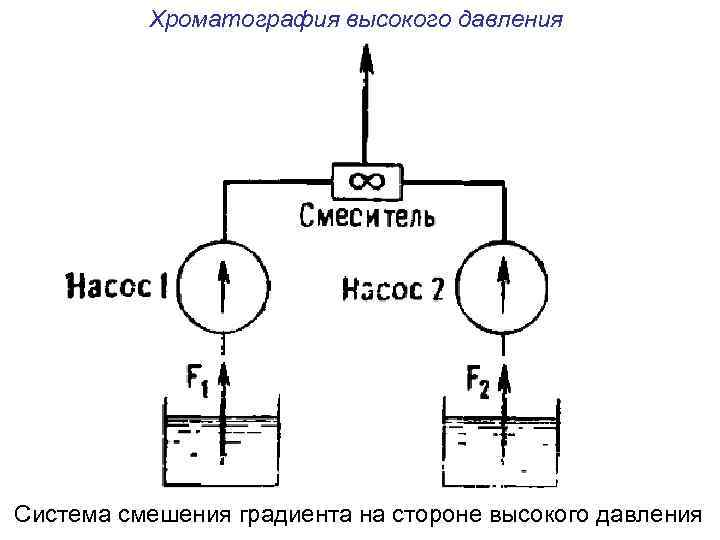 Хроматография высокого давления Система смешения градиента на стороне высокого давления
Хроматография высокого давления Система смешения градиента на стороне высокого давления
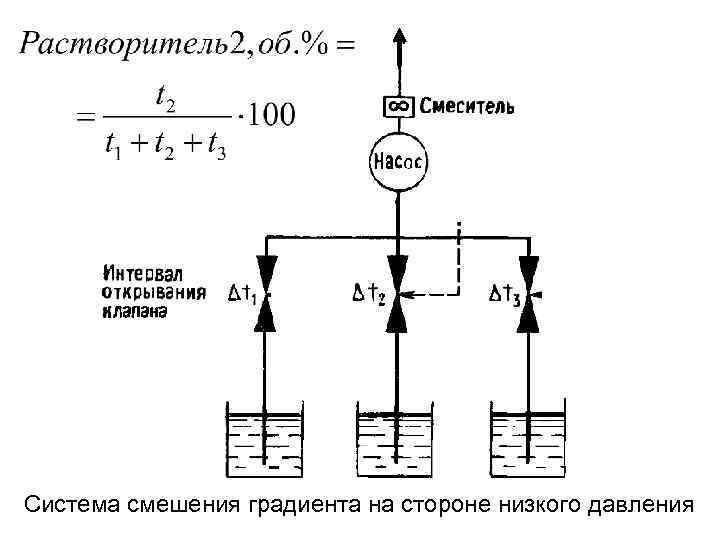 Система смешения градиента на стороне низкого давления
Система смешения градиента на стороне низкого давления
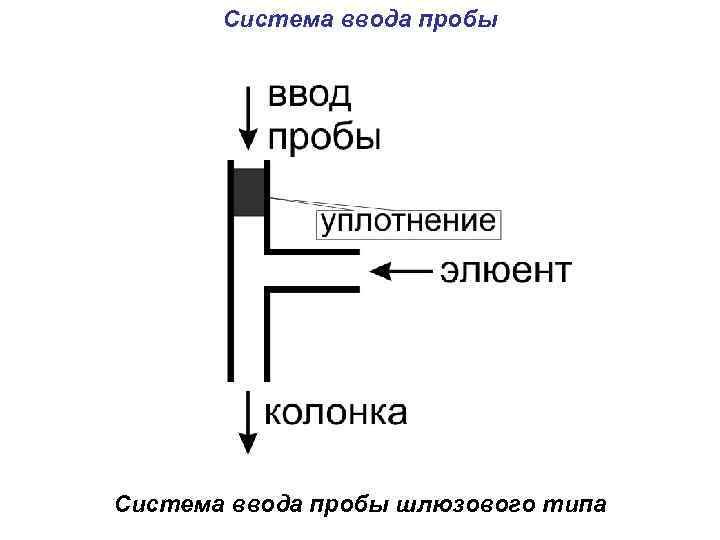 Система ввода пробы шлюзового типа
Система ввода пробы шлюзового типа
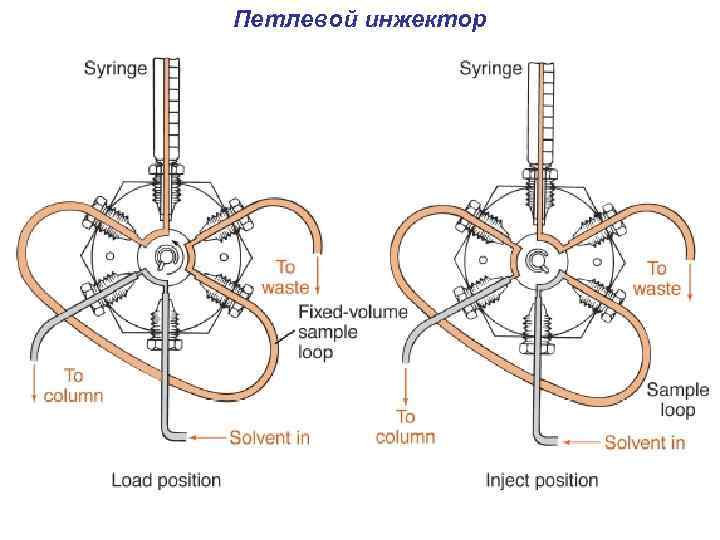 Петлевой инжектор
Петлевой инжектор
 Детекторы Назначение детектора - вести непрерывную регистрацию какого-либо физического параметра в токе элюата для количественной оценки ширины и амплитуды хроматографических зон. Абсорбционные детекторы работают как правило в УФи видимой областях спектра и являются практически проточными фотометрами. Закон Ламберта-Бэра A – абсорбция (поглощение или оптическая плотность ) раствора, ОЕ e – коэффициент экстинкции (поглощения), ОЕ M-1 cм-1 l – длина оптического пути, см
Детекторы Назначение детектора - вести непрерывную регистрацию какого-либо физического параметра в токе элюата для количественной оценки ширины и амплитуды хроматографических зон. Абсорбционные детекторы работают как правило в УФи видимой областях спектра и являются практически проточными фотометрами. Закон Ламберта-Бэра A – абсорбция (поглощение или оптическая плотность ) раствора, ОЕ e – коэффициент экстинкции (поглощения), ОЕ M-1 cм-1 l – длина оптического пути, см
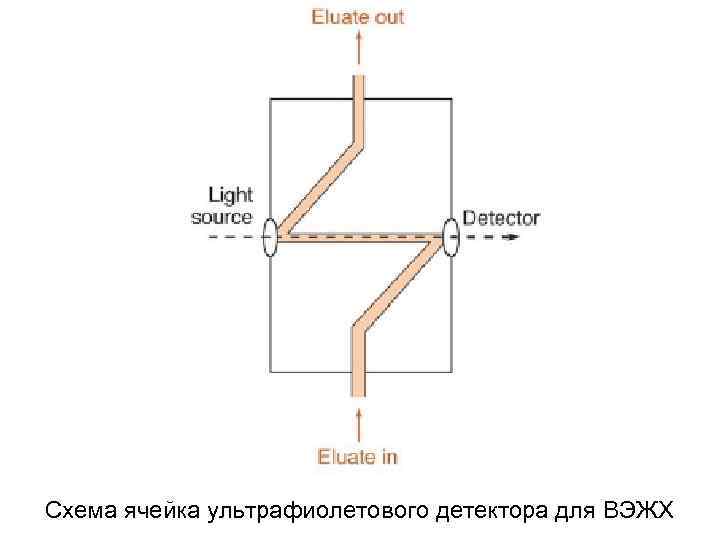 Схема ячейка ультрафиолетового детектора для ВЭЖХ
Схема ячейка ультрафиолетового детектора для ВЭЖХ
 Типы абсорбционных детекторв Детекторы с фиксированной длиной волны В этих детекторах используются как правило лампы с линейчатым спектром, т. е. излучающие несколько фиксированных длин волн, и вырезающий или отсекающий фильтр Детекторы с переменной длиной волны В этих детекторах используются источники с непрерывным спектром излучения и узкополосный фильтр К этому типу относятся детекторы способные быстро изменять длину волны и диодно-матричные детекторы
Типы абсорбционных детекторв Детекторы с фиксированной длиной волны В этих детекторах используются как правило лампы с линейчатым спектром, т. е. излучающие несколько фиксированных длин волн, и вырезающий или отсекающий фильтр Детекторы с переменной длиной волны В этих детекторах используются источники с непрерывным спектром излучения и узкополосный фильтр К этому типу относятся детекторы способные быстро изменять длину волны и диодно-матричные детекторы
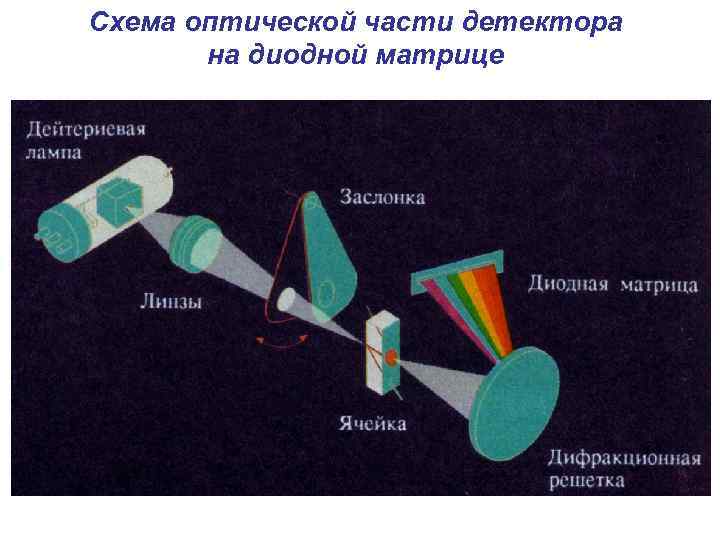 Схема оптической части детектора на диодной матрице
Схема оптической части детектора на диодной матрице
 Задачи решаемые с помощью детектора на диодной матрице Ø выбор наилучшей длины волны детектирования Ø проверка чистоты пика Ø подтверждение идентичности пиков
Задачи решаемые с помощью детектора на диодной матрице Ø выбор наилучшей длины волны детектирования Ø проверка чистоты пика Ø подтверждение идентичности пиков
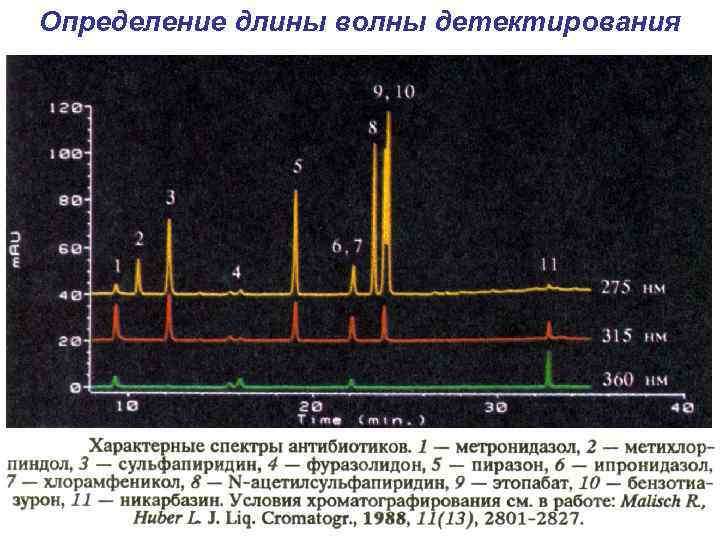 Определение длины волны детектирования
Определение длины волны детектирования
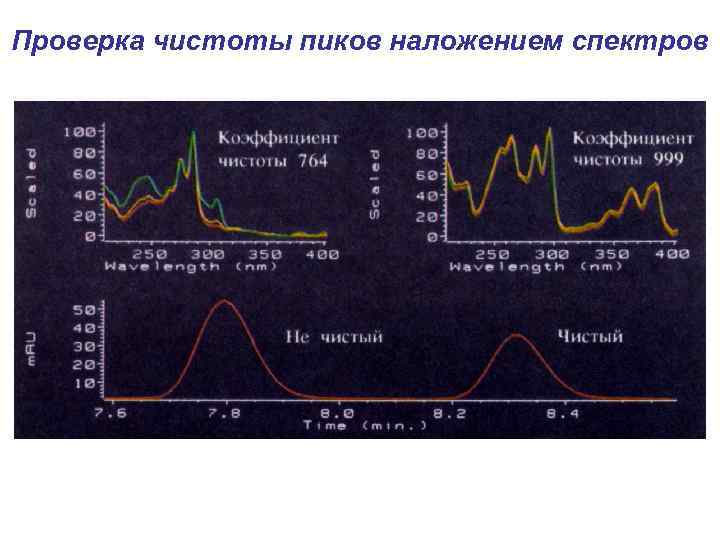 Проверка чистоты пиков наложением спектров
Проверка чистоты пиков наложением спектров
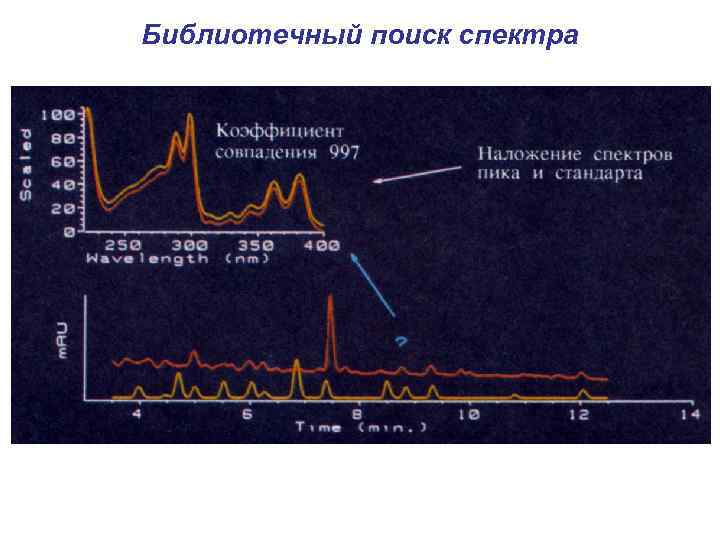 Библиотечный поиск спектра
Библиотечный поиск спектра
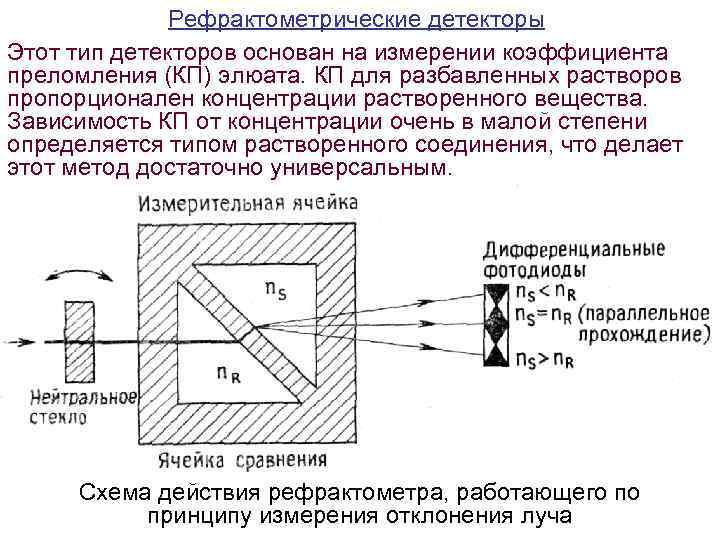 Рефрактометрические детекторы Этот тип детекторов основан на измерении коэффициента преломления (КП) элюата. КП для разбавленных растворов пропорционален концентрации растворенного вещества. Зависимость КП от концентрации очень в малой степени определяется типом растворенного соединения, что делает этот метод достаточно универсальным. Схема действия рефрактометра, работающего по принципу измерения отклонения луча
Рефрактометрические детекторы Этот тип детекторов основан на измерении коэффициента преломления (КП) элюата. КП для разбавленных растворов пропорционален концентрации растворенного вещества. Зависимость КП от концентрации очень в малой степени определяется типом растворенного соединения, что делает этот метод достаточно универсальным. Схема действия рефрактометра, работающего по принципу измерения отклонения луча
 Флуорометрические детекторы Флуориметрические детекторы, как следует из названия, основаны на измерении флуоресценнции растворенных соединений. Электрохимичекие детекторы Существует достаточно много различных типов электрохимических детекторов: вольтамперометричекие, кулонометрические. Они сравнительно мало распространены. Например, кондуктометрические детекторы, основаны на измерении проводимости раствора. Проводимость - величина обратная электрическому сопротивлению, - зависит непосредственно от числа заряженных частиц в растворе: G= (A/l), где -удельная проводимость (зависит только от концентрации), A/l - параметры ячейки (площадь электродов на расстояние между ними). Детекторы основанные на регистрации радиоактивности
Флуорометрические детекторы Флуориметрические детекторы, как следует из названия, основаны на измерении флуоресценнции растворенных соединений. Электрохимичекие детекторы Существует достаточно много различных типов электрохимических детекторов: вольтамперометричекие, кулонометрические. Они сравнительно мало распространены. Например, кондуктометрические детекторы, основаны на измерении проводимости раствора. Проводимость - величина обратная электрическому сопротивлению, - зависит непосредственно от числа заряженных частиц в растворе: G= (A/l), где -удельная проводимость (зависит только от концентрации), A/l - параметры ячейки (площадь электродов на расстояние между ними). Детекторы основанные на регистрации радиоактивности
 Системы сбора элюата - коллекторы фракций
Системы сбора элюата - коллекторы фракций

 Системы сбора и обработки данных. Системы управления хроматографом.
Системы сбора и обработки данных. Системы управления хроматографом.
 ТОНКОСЛОЙНАЯ ХРОМАТОГРАФИЯ Принципы разделения и типы сорбентов для ТСХ (TLC) те же, что и для других вариантов хроматографического разделения. ТСХ отличается формой стационарной фазы и аппаратурным оформлением, кроме того для характеристики разделения в ТСХ применяются некоторые специфические параметры не используемые в колоночной хроматографии. Пластинки для ТСХ представляют собой слой сорбента нанесенный на подложку из стекла, металлической фольги или полимерного материала, в сорбент обычно используется не в чистом виде. а с добавкой связующего как правило гипса до 15 %, позволяющего формировать более прочный слой. Сорбенты для ТСХ различаются размером частиц 5 мкм – ВТСХ (HPTLС) до 50 мкм при обычной ТСХ.
ТОНКОСЛОЙНАЯ ХРОМАТОГРАФИЯ Принципы разделения и типы сорбентов для ТСХ (TLC) те же, что и для других вариантов хроматографического разделения. ТСХ отличается формой стационарной фазы и аппаратурным оформлением, кроме того для характеристики разделения в ТСХ применяются некоторые специфические параметры не используемые в колоночной хроматографии. Пластинки для ТСХ представляют собой слой сорбента нанесенный на подложку из стекла, металлической фольги или полимерного материала, в сорбент обычно используется не в чистом виде. а с добавкой связующего как правило гипса до 15 %, позволяющего формировать более прочный слой. Сорбенты для ТСХ различаются размером частиц 5 мкм – ВТСХ (HPTLС) до 50 мкм при обычной ТСХ.
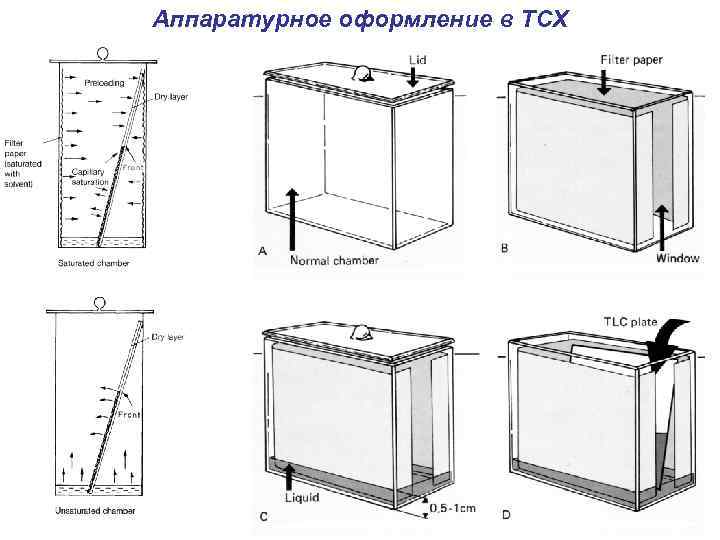 Аппаратурное оформление в TCХ
Аппаратурное оформление в TCХ
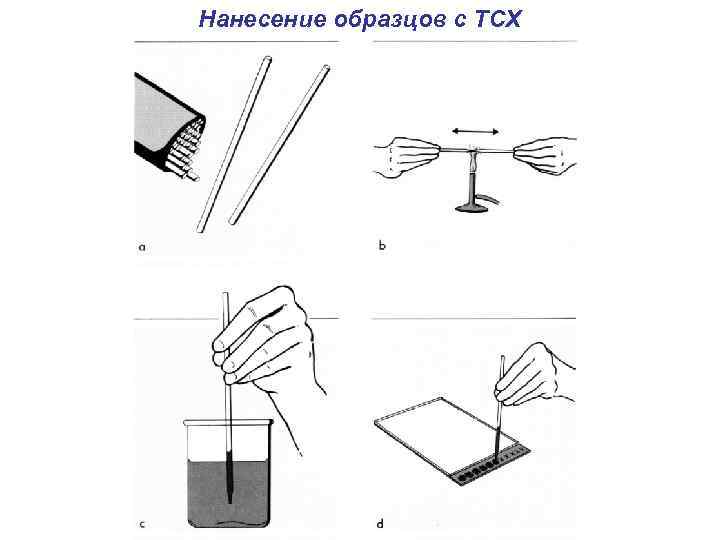 Нанесение образцов с ТСХ
Нанесение образцов с ТСХ
 Обнаружение зон в ТСХ После проведения хроматографии пластинку высушивают, а затем проводят детектирование хроматографических зон. Обнаружение зон не представляет сложности в случае если соединения окрашены, поглощают ультрафиолет или флуоресцируют. Для детектирование в ультрафиолете используют специальные лампы с длиной волны 254 или 366 нм помещенные в темной комнате или боксе. Освещая пластинки с включенным в них флуоресцентным индикатором, который испускает зеленую флуоресценцию при 254 нм, мы видим темно-фиолетовые пятна вещества, ослабляющего флуоресценцию индикатора, на светлом флуоресцирующем фоне.
Обнаружение зон в ТСХ После проведения хроматографии пластинку высушивают, а затем проводят детектирование хроматографических зон. Обнаружение зон не представляет сложности в случае если соединения окрашены, поглощают ультрафиолет или флуоресцируют. Для детектирование в ультрафиолете используют специальные лампы с длиной волны 254 или 366 нм помещенные в темной комнате или боксе. Освещая пластинки с включенным в них флуоресцентным индикатором, который испускает зеленую флуоресценцию при 254 нм, мы видим темно-фиолетовые пятна вещества, ослабляющего флуоресценцию индикатора, на светлом флуоресцирующем фоне.
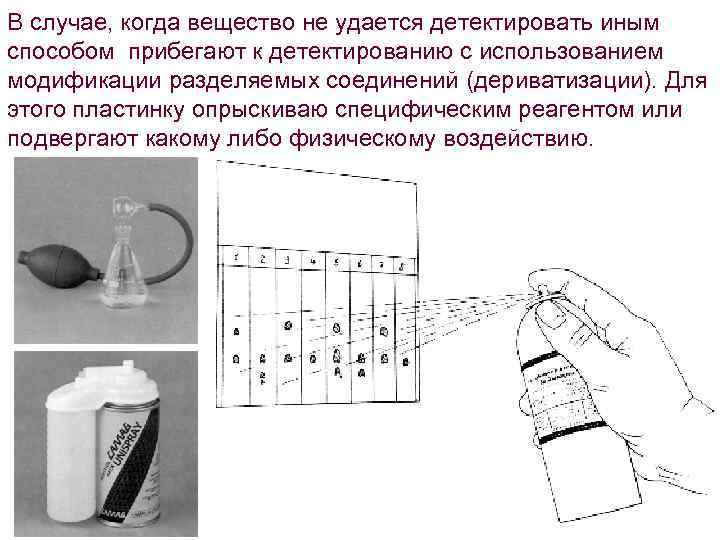 В случае, когда вещество не удается детектировать иным способом прибегают к детектированию с использованием модификации разделяемых соединений (дериватизации). Для этого пластинку опрыскиваю специфическим реагентом или подвергают какому либо физическому воздействию.
В случае, когда вещество не удается детектировать иным способом прибегают к детектированию с использованием модификации разделяемых соединений (дериватизации). Для этого пластинку опрыскиваю специфическим реагентом или подвергают какому либо физическому воздействию.
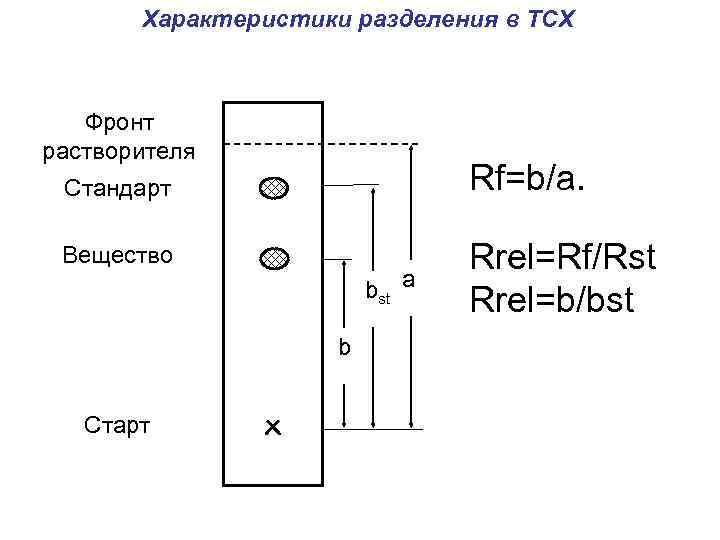 Характеристики разделения в ТСХ Фронт растворителя Rf=b/a. Стандарт Вещество bst a b Старт Rrel=Rf/Rst Rrel=b/bst
Характеристики разделения в ТСХ Фронт растворителя Rf=b/a. Стандарт Вещество bst a b Старт Rrel=Rf/Rst Rrel=b/bst
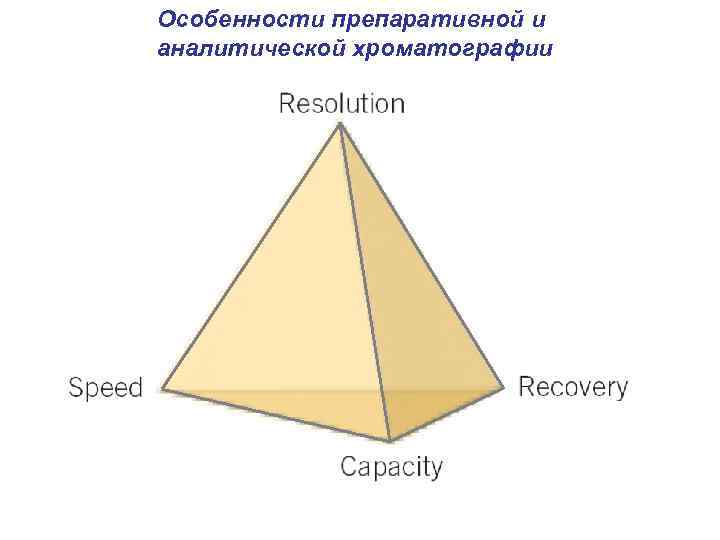
 Особенности препаративной и аналитической хроматографии Analytical chromatography: - determine chemical composition of a sample - separate and quantify - columns max. 10 mm i. d. , flow rate 0, 1 -30 ml/min Preparative chromatography: - purify and collect one or more components of a sample (µg to g) - columns 7 -50 mm i. d. , flow rate 20 -1200 ml/min Production scale chromatography: - commercial production of one component (kg to tons) - columns up to 1500 mm i. d. , flow rate >1000 ml/min
Особенности препаративной и аналитической хроматографии Analytical chromatography: - determine chemical composition of a sample - separate and quantify - columns max. 10 mm i. d. , flow rate 0, 1 -30 ml/min Preparative chromatography: - purify and collect one or more components of a sample (µg to g) - columns 7 -50 mm i. d. , flow rate 20 -1200 ml/min Production scale chromatography: - commercial production of one component (kg to tons) - columns up to 1500 mm i. d. , flow rate >1000 ml/min
 Особенности препаративной и аналитической хроматографии Количество разделяемого вещества. Все аналитические методов характерна тенденция к уменьшению количества анализируемых веществ, снижения предела обнаружения и увеличения чувствительности метода. Это позволяет работать с минимальными количествами веществ. В препаративных методах ситуация обратная - необходимо работать с большими вещества количествами, однако в случае БАВ и с развитием современных аналитических методов препаративные количества зачастую очень незначительны. Однако общая тенденция такова: для аналитической хроматографии используются колонки меньшего размера и следовательно системы подачи элюента обеспечивающие меньшие расходы, но системы детектирования для аналитической хроматографии должны быть более чувствительными.
Особенности препаративной и аналитической хроматографии Количество разделяемого вещества. Все аналитические методов характерна тенденция к уменьшению количества анализируемых веществ, снижения предела обнаружения и увеличения чувствительности метода. Это позволяет работать с минимальными количествами веществ. В препаративных методах ситуация обратная - необходимо работать с большими вещества количествами, однако в случае БАВ и с развитием современных аналитических методов препаративные количества зачастую очень незначительны. Однако общая тенденция такова: для аналитической хроматографии используются колонки меньшего размера и следовательно системы подачи элюента обеспечивающие меньшие расходы, но системы детектирования для аналитической хроматографии должны быть более чувствительными.
 Особенности препаративной и аналитической хроматографии Эффективность разделения. Аналитичекое разделение должно быть высокоэффективным для всех веществ разделяемой смеси. Все хроматографические зоны должны иметь разрешение близкое к 1, но превышение этого значение не желательно, поскольку это будет влиять на разрешение соседних веществ. Это накладывает ограничения и на максимальную загрузку колонки. В препаративной хроматографии нас как правило интересует одно из веществ разделяемой смеси, поэтому разрешение соответствующей ему хроматографической зоны должно быть больше или равным 1, причем часто удобно иметь разрешение больше единицы. Это позволяет существенно увеличивать нагрузку на колонку, что важно при препаративной хроматографии. Кроме того более низкие требования к эффективности разделения позволяют использовать для перпаративной хроматографии менее продвинутые, а следовательно более дешевые сорбенты.
Особенности препаративной и аналитической хроматографии Эффективность разделения. Аналитичекое разделение должно быть высокоэффективным для всех веществ разделяемой смеси. Все хроматографические зоны должны иметь разрешение близкое к 1, но превышение этого значение не желательно, поскольку это будет влиять на разрешение соседних веществ. Это накладывает ограничения и на максимальную загрузку колонки. В препаративной хроматографии нас как правило интересует одно из веществ разделяемой смеси, поэтому разрешение соответствующей ему хроматографической зоны должно быть больше или равным 1, причем часто удобно иметь разрешение больше единицы. Это позволяет существенно увеличивать нагрузку на колонку, что важно при препаративной хроматографии. Кроме того более низкие требования к эффективности разделения позволяют использовать для перпаративной хроматографии менее продвинутые, а следовательно более дешевые сорбенты.
 Особенности препаративной и аналитической хроматографии Время, затрачиваемое на разделение. Всегда хорошо если разделение занимает меньше времени, но в аналитической хроматографии, особенно при серийном анализе этот параметр, становится одним из важнейших. Для препаративной хроматографии важно не собственно время разделения, а соотношение время разделение/количество полученного продукта.
Особенности препаративной и аналитической хроматографии Время, затрачиваемое на разделение. Всегда хорошо если разделение занимает меньше времени, но в аналитической хроматографии, особенно при серийном анализе этот параметр, становится одним из важнейших. Для препаративной хроматографии важно не собственно время разделения, а соотношение время разделение/количество полученного продукта.
 Особенности препаративной и аналитической хроматографии
Особенности препаративной и аналитической хроматографии
 ПОДГОТОВКА ПРОБ ДЛЯ ХРОМАТОГРАФИИ
ПОДГОТОВКА ПРОБ ДЛЯ ХРОМАТОГРАФИИ
 Твердофазная экстракция - процесс экстракции с участием твердой и жидкой фазы. При этом целевой компонент и балластные примеси находятся в жидкой фазе. • • • Для твердофазной экстракции коммерчески доступны различные сорбенты: с обращенной фазой: октадецил, октил, этил, циклогексил, фенил с нормальной фазой: силикагель модифицированный циано-, амино- и диольными группами ионообменные с амино, четвертичными амино-, карбоксигруппами, ароматическими сульфоновыми кислотами обращеннофазовые и ионообменные носители с широкими порами окись алюминия, немодифицированные силикагель, флорисил (Mg. Si. O 3)
Твердофазная экстракция - процесс экстракции с участием твердой и жидкой фазы. При этом целевой компонент и балластные примеси находятся в жидкой фазе. • • • Для твердофазной экстракции коммерчески доступны различные сорбенты: с обращенной фазой: октадецил, октил, этил, циклогексил, фенил с нормальной фазой: силикагель модифицированный циано-, амино- и диольными группами ионообменные с амино, четвертичными амино-, карбоксигруппами, ароматическими сульфоновыми кислотами обращеннофазовые и ионообменные носители с широкими порами окись алюминия, немодифицированные силикагель, флорисил (Mg. Si. O 3)
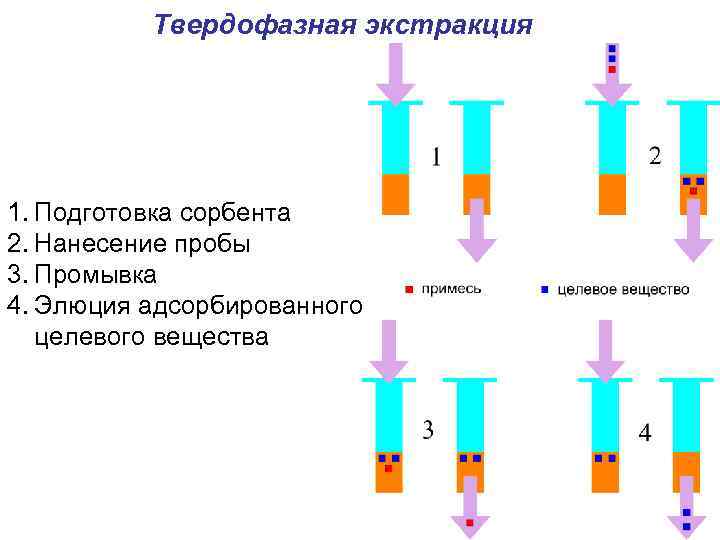 Твердофазная экстракция 1. Подготовка сорбента 2. Нанесение пробы 3. Промывка 4. Элюция адсорбированного целевого вещества
Твердофазная экстракция 1. Подготовка сорбента 2. Нанесение пробы 3. Промывка 4. Элюция адсорбированного целевого вещества
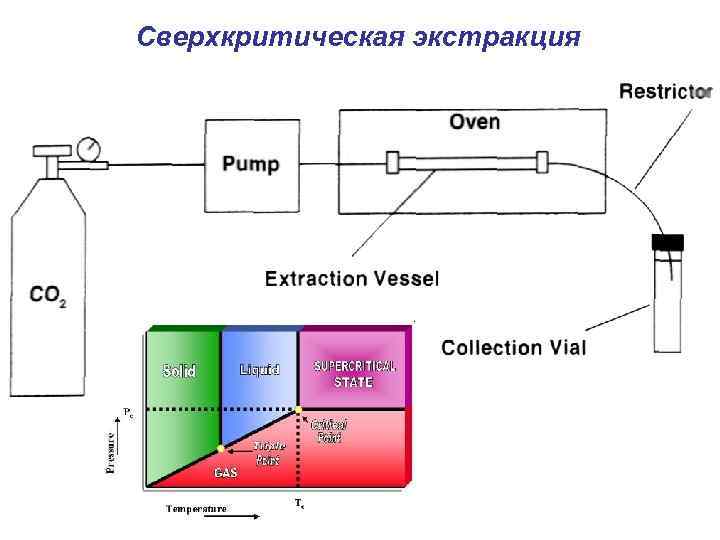 Сверхкритическая экстракция
Сверхкритическая экстракция


